文档内容
H
2025-2026 学年高一下学期素养测评(一)
化学试题
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案字母涂黑,
如需改动,用橡皮擦干净后,再选涂其他答案字母。回答非选择题时,将答案写在
答题卡上,写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
考试时间为75分钟,满分100分
可能用到的相对原子质量:H-1 C-12 N-14 0-16 Na-23 S-32 C1-35.5Ca-40Fe-56
Cu-64
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只
有一项是符合题目要求的。
1.河南博物院珍藏下列文物的主要成分属于传统无机非金属材料的是
A.杜岭方鼎
B.贾湖骨笛
C.彩陶双连壶 D.武则天金简
2.硅是无机非金属材料的主角。下列物质含有硅单质的是
A.光导纤维 B.太阳能电池板 C.水玻璃 D.水晶
3.下列物质不属于酸性氧化物的是
A.SiO2 B.SO2 C.SO3 D.NO
4.下列试剂的实验室保存方法错误的是
A.浓硝酸保存在棕色试剂瓶中 B.NaOH溶液保存在带玻璃塞的细口瓶中
C.KMnO,固体保存在棕色广口瓶中 D.少量的Na保存在装有煤油的试剂瓶中
5.在下列给定条件下的溶液中,一定能大量共存的离子组是
A.无色溶液中:Ca2+ 、H+ 、Cl− 、HSO−
3
B.能使pH试纸呈蓝色的溶液中:Na+ 、N H+ 、I− 、NO−
4 3
C.Na S溶液中:K+ 、Na+ 、H+ 、NO−
2 3
D.澄清透明的无色溶液中:K+ 、SO2− 、OH− 、Na+
4
第1页(共6页)
学科网(北京)股份有限公司6.下列说法正确的是
A.用含铝的原料可以制作透光性好、折射率高的光学玻璃
B.硅酸盐中Si和O构成了硅氧平面三角形结构
C.使用石膏可以有效调节水泥的硬化速率,再磨成细粉就是普通水泥
D.硅元素在自然界大多以硅离子的形态存在
7.对比是学习化学的重要方法。下列关于CO2与SiO2的比较中正确的是
A.CO2和SiO2均能与H2O反应生成相应的含氧酸
B.CO2和SiO2均能与NaOH溶液发生反应
C.CO2和SiO2常温下都是气体
D.CO2和SiO2均可以与焦碳发生置换反应
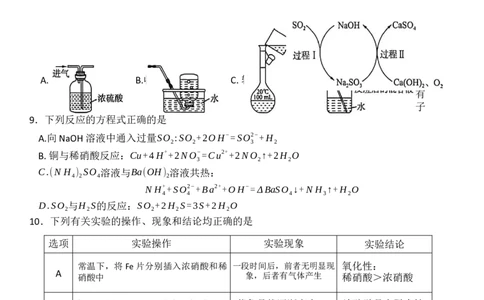
8.下列实验操作规范且能达到实验目的的是
A.干燥SO 气体 B.收集NJO 气体 C.转移洗涤液 D.检验过量浓硫酸与铜反
2 2
应后的产物中是否含有
铜离子
9.下列反应的方程式正确的是
A.向NaOH溶液中通入过量SO :SO +2OH−=SO2−+H
2 2 3 2
B.铜与稀硝酸反应:Cu+4H++2NO−=Cu2++2NO ↑+2H O
3 2 2
C.(N H ) SO 溶液与Ba(OH) 溶液共热:
4 2 4 2
N H++SO2−+Ba2++OH−=ΔBaSO ↓+N H ↑+H O
4 4 4 3 2
D.SO 与H S的反应:SO +2H S=3S+2H O
2 2 2 2 2
10.下列有关实验的操作、现象和结论均正确的是
选项 实验操作 实验现象 实验结论
常温下,将Fe片分别插入浓硝酸和稀 一段时间后,前者无明显现 氧化性:
A 硝酸中 象,后者有气体产生 稀硝酸>浓硝酸
B 向 CuSO4·5H2O晶体中滴加浓硫酸 蓝色晶体逐渐变白 浓硫酸具有脱水性
取少量溶液于试管中,加入稀
NaOH 溶液并加热,将湿润的红色 该溶液中一定含有
试纸变蓝
C NH+
石蕊试纸放在试管口
取少量溶液于试管中,滴加盐酸酸化 该溶液中一定含有
出现白色沉淀
D
的BaCl2溶液 SO2-
11.下列有关氮及其化合物的叙述正确的是
①CO、NO、NO2都是大气污染物,都能在空气中稳定存在
②N2中两个氮原子间以共价三键(N=)结合,性质稳定
第1页(共6页)
学科网(北京)股份有限公司③工业生产金属镁时,为防止Mg被氧化,可以用N 作保护气
2
④敞口放置的浓硝酸和浓硫酸,浓度均会降低,原因相同
⑤NNO 是酸性氧化物
2
⑥通过豆科植物的根瘤菌将氮气转化为氨,是自然固氮的途径之一
⑦足量铁粉与稀硝酸反应后所得溶液呈浅绿色,说明稀硝酸不能氧化Fe2+
A.②③⑥ B.②⑥ C.⑥⑦ D.③⑤⑥
12.烟道气中的SO2气体是一种污染性气体,可采用“双碱法”脱硫除去,脱硫过程如图
所示。下列说法错误的是
A.“过程I”中S的化合价不发生变化
B.“过程II”中CaSO,既是氧化产物,又是还原产物
C.“双碱法”脱硫过程中,NaOH可以循环利用
D.总反应中每消耗 4.48LO ((标准状况),则理论
2
上能脱除12.8gSO2
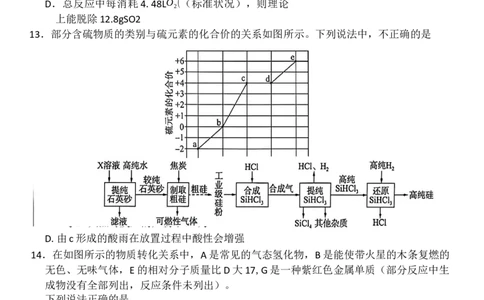
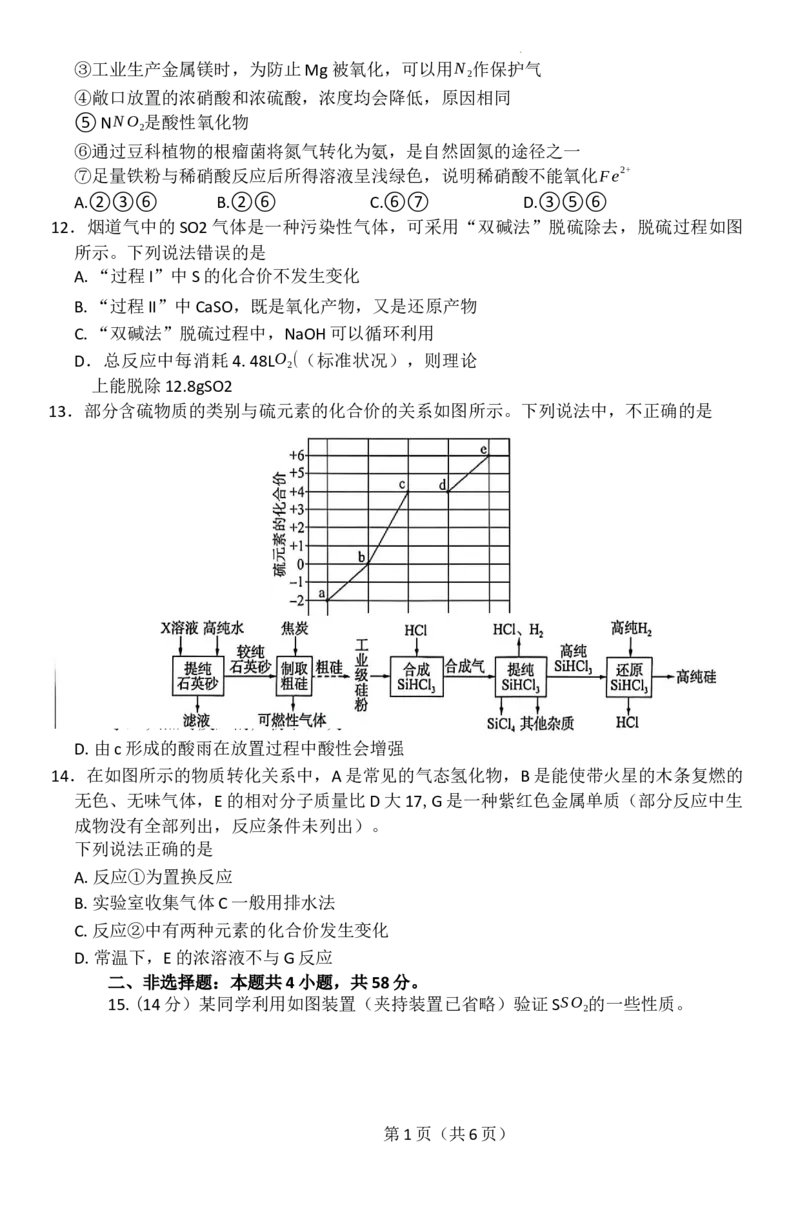
13.部分含硫物质的类别与硫元素的化合价的关系如图所示。下列说法中,不正确的是
A.食品中添加适量c可起到漂白、防腐和抗氧化等作用
B.e的稀溶液与a反应可能生成b和c
C.b与Fe共热时反应的产物中Fe为+2价
D.由c形成的酸雨在放置过程中酸性会增强
14.在如图所示的物质转化关系中,A是常见的气态氢化物,B是能使带火星的木条复燃的
无色、无味气体,E的相对分子质量比D大17,G是一种紫红色金属单质(部分反应中生
成物没有全部列出,反应条件未列出)。
下列说法正确的是
A.反应①为置换反应
B.实验室收集气体C一般用排水法
C.反应②中有两种元素的化合价发生变化
D.常温下,E的浓溶液不与G反应
二、非选择题:本题共4小题,共58分。
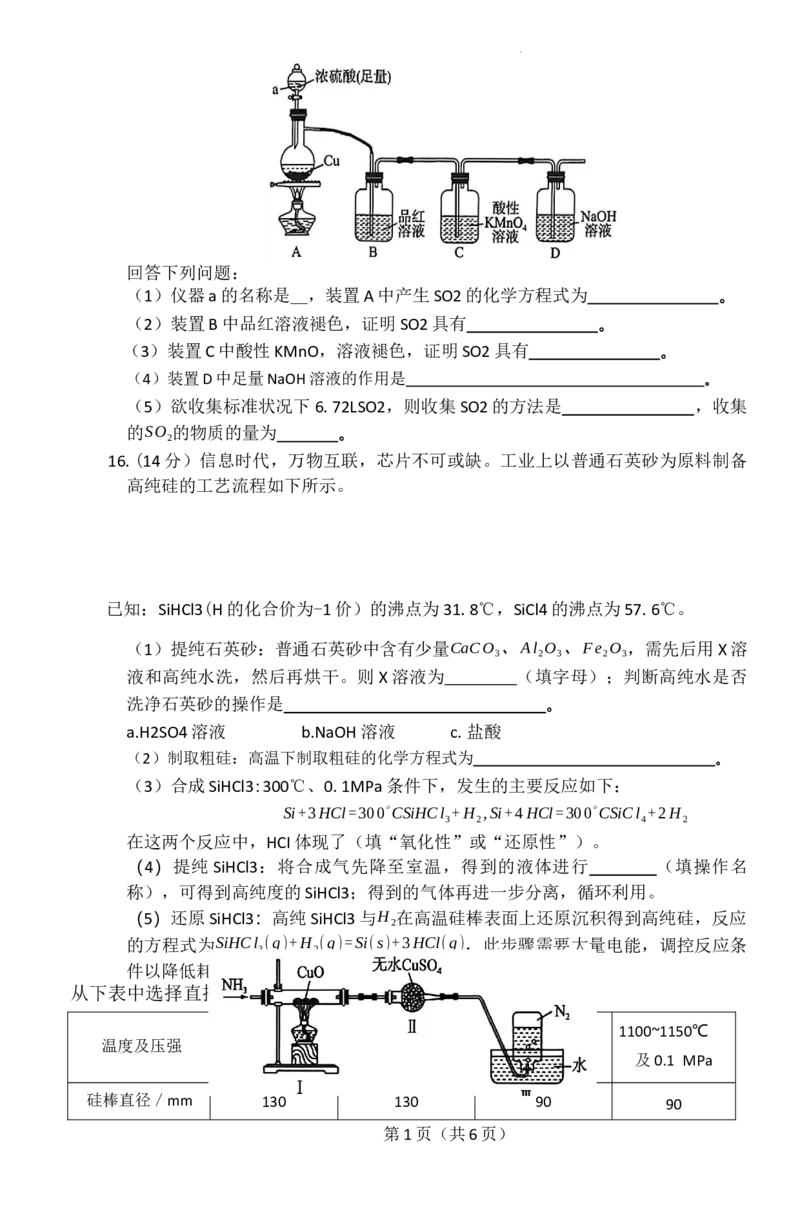
15.(14分)某同学利用如图装置(夹持装置已省略)验证SSO 的一些性质。
2
第1页(共6页)
学科网(北京)股份有限公司回答下列问题:
(1)仪器a的名称是_,装置A中产生SO2的化学方程式为 。
(2)装置B中品红溶液褪色,证明SO2具有 。
(3)装置C中酸性KMnO,溶液褪色,证明SO2具有 。
(4)装置D中足量NaOH溶液的作用是 。
(5)欲收集标准状况下6.72LSO2,则收集SO2的方法是 ,收集
的SO 的物质的量为 。
2
16.(14分)信息时代,万物互联,芯片不可或缺。工业上以普通石英砂为原料制备
高纯硅的工艺流程如下所示。
已知:SiHCl3(H的化合价为-1价)的沸点为31.8℃,SiCl4的沸点为57.6℃。
(1)提纯石英砂:普通石英砂中含有少量CaCO 、Al O 、Fe O ,需先后用X溶
3 2 3 2 3
液和高纯水洗,然后再烘干。则 X溶液为 (填字母);判断高纯水是否
洗净石英砂的操作是 。
a.H2SO4溶液 b.NaOH溶液 c.盐酸
(2)制取粗硅:高温下制取粗硅的化学方程式为 。
(3)合成SiHCl3:300℃、0.1MPa条件下,发生的主要反应如下:
Si+3HCl=300∘CSiHCl +H ,Si+4HCl=300∘CSiCl +2H
3 2 4 2
在这两个反应中,HCI体现了(填“氧化性”或“还原性”)。
(4)提纯 SiHCl3:将合成气先降至室温,得到的液体进行 (填操作名
称),可得到高纯度的SiHCl3;得到的气体再进一步分离,循环利用。
(5)还原SiHCl3:高纯SiHCl3与H 在高温硅棒表面上还原沉积得到高纯硅,反应
2
的方程式为SiHCl (g)+H (g)=Si(s)+3HCl(g),此步骤需要大量电能,调控反应条
3 2
件以降低耗电量有重大意义。
从下表中选择直接耗电量最低的反应条件: (填字母)。
1050~1100℃ 1050~1100℃ 1050~1100℃ 1100~1150℃
温度及压强
及0.1 MPa 及0.6 MPa 及0.1 MPa 及0.1 MPa
硅棒直径/mm 130 130 90 90
第1页(共6页)
学科网(北京)股份有限公司直接耗电量/
140 73 208.5 182.2
kWh⋅(kgSi) −1
第1页(共6页)
学科网(北京)股份有限公司a.1050~1100℃、0.6 MPa、90mm b.1100~1150℃、0.6 MPa、90mm
c.1100~1150℃、0.1 MPa、130mm d.1100~1150℃、0.6MPa、130mm
(6)尾气处理:提纯 SiHCl3步骤中分离出来的 SiCl,可转化为 SiHCl3后再利用,
2.5MPa
实现闭环生产,方法为2SiCl (g)+H (g)+Si(s)+HCl(g)= 3SiHCl (g)。该方案
4 2 540∘C 3
的优点为 (写一条即可)。
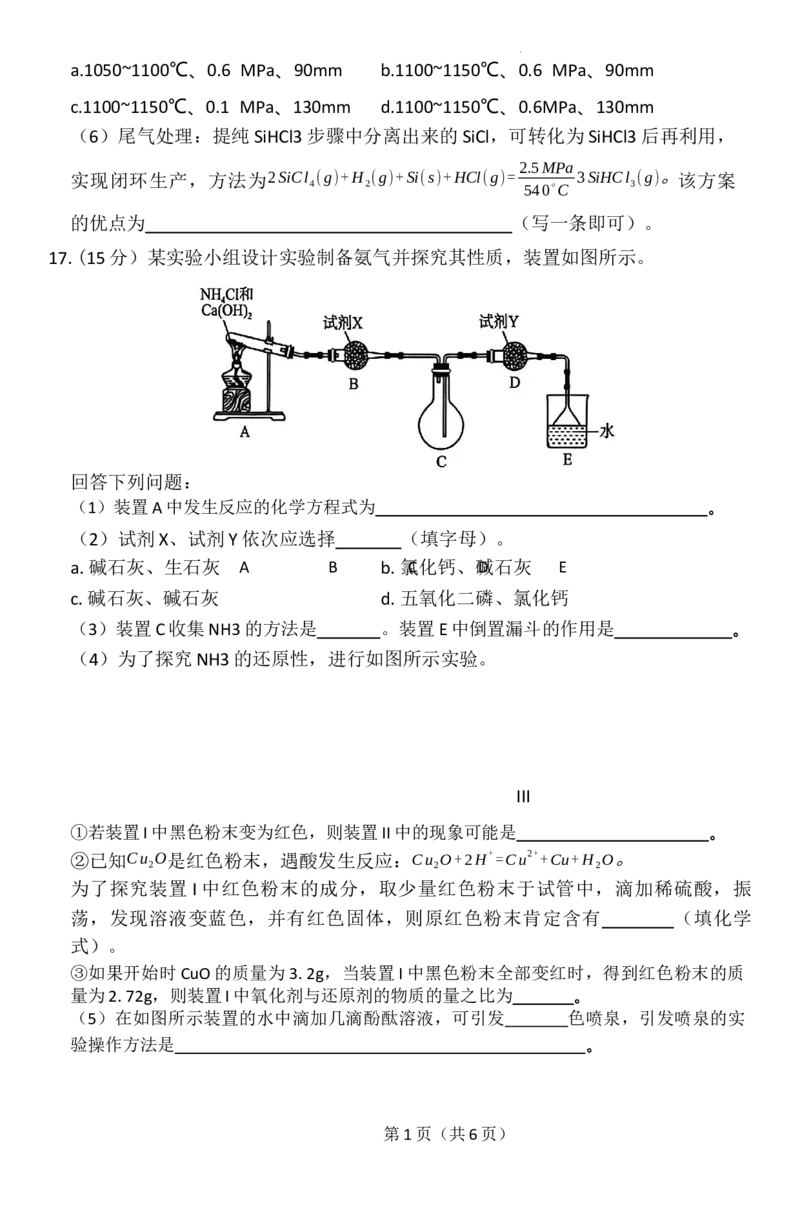
17.(15分)某实验小组设计实验制备氨气并探究其性质,装置如图所示。
回答下列问题:
(1)装置A中发生反应的化学方程式为 。
(2)试剂X、试剂Y依次应选择 (填字母)。
a.碱石灰、生石灰 A B b . 氯C 化 钙 、 碱D 石 灰 E
c.碱石灰、碱石灰 d.五氧化二磷、氯化钙
(3)装置C收集NH3的方法是 。装置E中倒置漏斗的作用是 。
(4)为了探究NH3的还原性,进行如图所示实验。
III
①若装置I中黑色粉末变为红色,则装置II中的现象可能是 。
②已知Cu O是红色粉末,遇酸发生反应:Cu O+2H+=Cu2++Cu+H O。
2 2 2
为了探究装置 I 中红色粉末的成分,取少量红色粉末于试管中,滴加稀硫酸,振
荡,发现溶液变蓝色,并有红色固体,则原红色粉末肯定含有 (填化学
式)。
③如果开始时CuO的质量为3.2g,当装置I中黑色粉末全部变红时,得到红色粉末的质
量为2.72g,则装置I中氧化剂与还原剂的物质的量之比为 。
(5)在如图所示装置的水中滴加几滴酚酞溶液,可引发 色喷泉,引发喷泉的实
验操作方法是 。
第1页(共6页)
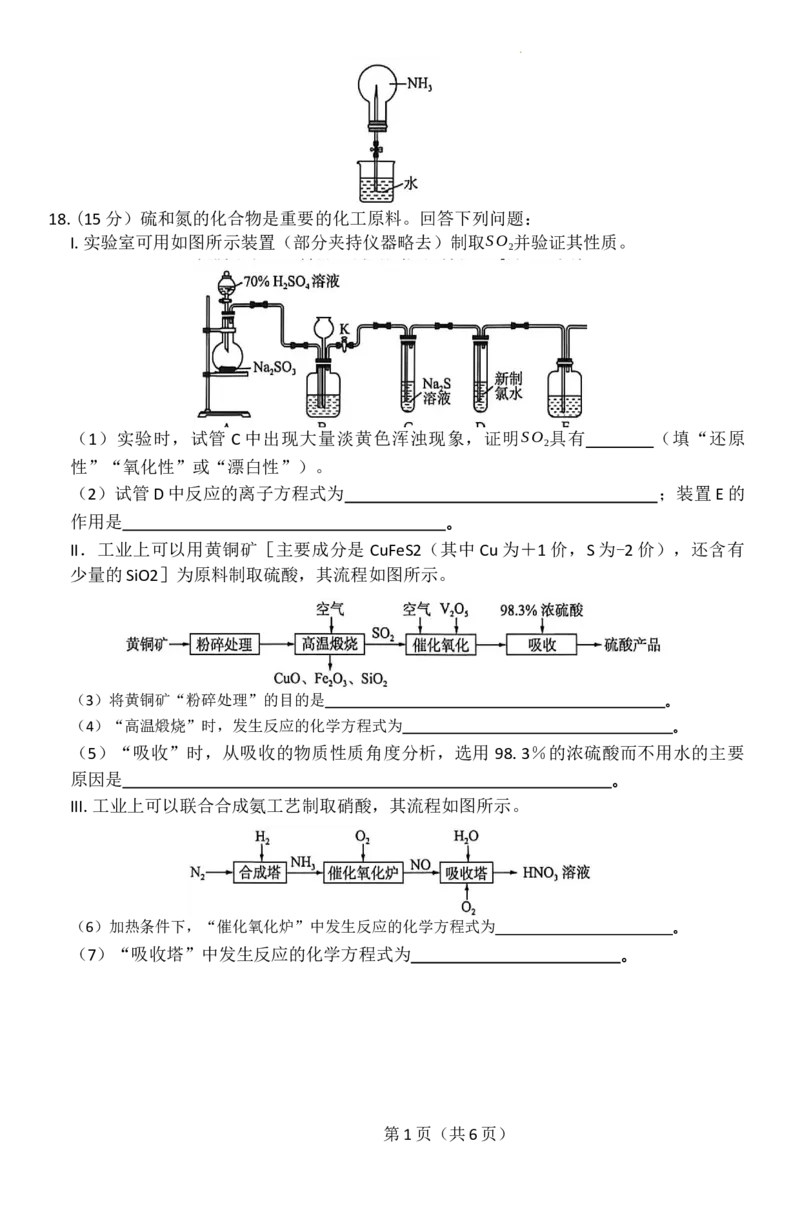
学科网(北京)股份有限公司18.(15分)硫和氮的化合物是重要的化工原料。回答下列问题:
I.实验室可用如图所示装置(部分夹持仪器略去)制取SO 并验证其性质。
2
(1)实验时,试管 C 中出现大量淡黄色浑浊现象,证明SO 具有 (填“还原
2
性”“氧化性”或“漂白性”)。
(2)试管D中反应的离子方程式为 ;装置E的
作用是 。
II.工业上可以用黄铜矿[主要成分是 CuFeS2(其中 Cu为+1价,S为-2价),还含有
少量的SiO2]为原料制取硫酸,其流程如图所示。
(3)将黄铜矿“粉碎处理”的目的是 。
(4)“高温煅烧”时,发生反应的化学方程式为 。
(5)“吸收”时,从吸收的物质性质角度分析,选用 98.3%的浓硫酸而不用水的主要
原因是 。
III.工业上可以联合合成氨工艺制取硝酸,其流程如图所示。
(6)加热条件下,“催化氧化炉”中发生反应的化学方程式为 。
(7)“吸收塔”中发生反应的化学方程式为 。
第1页(共6页)
学科网(北京)股份有限公司