文档内容
专题 06 化学反应与能量
1.下列电池工作时,O 在正极放电的是( )
2
A.锌锰电池 B.氢燃料电池 C.铅蓄电池 D.镍镉电池
2.下列对能量转化的认知中,不正确的是( )
A.电解水生成H 和O 时,电能主要转化为化学能
2 2
B.风力发电时,风能主要转化为电能
C.煤燃烧时,化学能主要转化为热能
D.白炽灯工作时,电能全部转化为光能
3.有关原电池的下列说法中正确的是( )
A.在外电路中电子由正极流向负极 B.在原电池中,只有金属锌作为负极
C.原电池工作时,阳离子向正极方向移动 D.原电池工作时,阳离子向负极方向移动
4.从宏观来看化学变化的本质是有新物质生成。从微观角度来看,下列变化不能说明发生了化学变化
的是( )
A.变化时有电子的得失或共用电子对的形成
B.变化过程中有化学键的断裂和形成
C.变化时释放出能量
D.变化前后原子的种类和数目没有改变,分子种类增加了
5.化学与能源开发、环境保护、资源利用等密切相关。下列说法正确的是( )
A.天然气、石油、流水、风力、氢气为一次能源
B.无论是风力发电还是火力发电,都是将化学能转化为电能
C.PM2.5含有的铅、镉、铬、钒、砷等对人体有害的元素均是金属元素
D.发展低碳经济、循环经济,推广可利用太阳能、风能的城市照明系统
6.可逆反应A (g)+3B(g) 2C(g)+2D(g)在4种不同情况下反应速率分别如下,其中反应速率v
最大的是( )
A.v(A)=0.15mol/(L·min) B.v (B)=0.6 mol/(L·min)
C.v (C)=0.3 mol/(L·min) D.v (D)=0.1 mol/(L·min)
7.在2A(g)+B(g) 3C(g)+4D(g)反应中,表示该反应速率最快的是( )
A.v(A)=0.5 mol·L-1·s-1 B.v(B)=0.3 mol·L-1·s-1
C.v(C)=0.8 mol·L-1·s-1 D.v(D)=1 mol·L-1·s-18.在容积为2 L的密闭容器中充入2 mol SO 和一定量O ,发生反应2SO +O 2SO ,当反应
2 2 2 2 3
进行到4 min时,测得n(SO )=0.4 mol。若反应进行2 min末时,容器中SO 的物质的量是( )
2 2
A.等于1.6 mol B.等于1.2 mol C.大于1.6 mol D.小于1.2 mol
9.汽车尾气里含有有毒的NO和CO,NO和CO能缓慢地反应生成N 和CO 。对此反应的下列叙述不
2 2
正确的是( )
A.使用催化剂能加快反应速率 B.升高温度能加快反应速率
C.改变压强对反应速率无影响 D.此反应能减轻尾气对环境的污染
10.化学反应的发生必然伴随有能量的转化,其最根本的原因是( )
A. 化学反应中一定有新物质生成
B. 化学反应中旧的化学键的断裂需要吸收能量,新的化学键的生成需要放出能量
C. 化学反应通常需要加热等条件才能发生
D. 能量变化是化学反应的基本特征之一
11.对化学反应速率与化学反应限度的叙述,不正确的是( )
A.当化学反应达到最大限度时反应速率为0
B.同一化学反应,若反应条件不同,限度可能不同
C.化学反应达到限度时,正逆反应速率相等
D.化学反应的限度与时间的长短无关
12.下列关于能源和作为能源使用的物质的叙述中错误的是( )
A.化石能源物质内部蕴含着大量的能量
B.绿色植物进行光合作用时,将太阳能转化为化学能“贮存”起来
C.物质的化学能可以在一定条件下转化为热能、电能,为人类所利用
D.吸热反应没有利用价值
13.一定条件下,向2 L密闭容器中加入2 mol N 和10 mol H ,发生反应N +3H 2NH 2 min时
2 2 2 2 3,
测得剩余N 1 mol,下列化学反应速率不正确的是( )
2
A.v(N )=0.25 mol·L-1·min-1 B.v(H )=0.75 mol·L-1·min-1
2 2
C.v(NH )=1 mol·L-1·min-1 D.v(NH )=0.5 mol·L-1·min-1
3 3
14.已知反应X+Y===M+N为吸热反应,下列说法正确的是( )
A.X的能量一定低于M的,Y的能量一定低于N的
B.该反应一定要加热,反应才能进行
C.破坏反应物中的化学键所吸收的能量小于形成生成物中的化学键所放出的能量
D.X和Y的总能量低于M和N的总能量
15.反应2SO +O 2SO 达到平衡后,再向反应容器中充入含氧的同位素O的氧气,经过一段时
2 2 3
间后,O原子存在于( )
A.O B.SO C.O 和SO D.O、SO 和SO
2 2 2 2 2 2 3
16.已知断裂1 mol共价键所需要吸收的能量分别为H—H:436 kJ,I—I:151 kJ,H—I:299 kJ,下列对H(g)+I(g) 2HI(g)的反应类型判断错误的是( )
2 2
A.放出能量的反应 B.吸收能量的反应 C.氧化还原反应 D.可逆反应
17.观察右图:对合成氨反应中,下列叙述错误的是( )
A.开始反应时,正反应速率最大,逆反应速率为零
B.随着反应的进行,正反应速率逐渐减小,逆反应速率逐渐增大
C.反应到达t 时,正反应速率与逆反应速率相等,反应停止
1
D.反应在t 之后,正反应速率与逆反应速率相等,反应达到化学平衡状态
1
18.电池是人类生产和生活中的重要能量来源,各式各样电池的发明是化学对人
类的一项重大贡献。下列有关电池的叙述正确的是( )
A.锌锰干电池工作一段时间后碳棒变细
B.氢氧燃料电池可将热能直接转变为电能
C.氢氧燃料电池工作时氢气在负极被氧化
D.太阳能电池的主要材料是高纯度的二氧化硅
19.废电池处理不当不仅造成浪费,还会对环境造成严重污染,对人体健康也存在极大的危害。有同
学想将其变废为宝,他的以下想法你认为不正确的是( )
A.把锌皮取下洗净用于实验室制取氢气
B.碳棒取出洗净用作电极
C.把铜帽取下洗净回收利用
D.电池内部填有NH Cl等化学物质,将废电池中的黑色糊状物作化肥施用
4
20.CO和H 在一定条件下可以合成乙醇:2CO(g)+4H(g) CHCHOH(g)+HO(g),下列叙述
2 2 3 2 2
中能说明上述反应在一定条件下已达到最大限度的是( )
A.CO全部转化为乙醇
B.正反应和逆反应的化学反应速率均为零
C.CO和H 以1∶2的物质的量之比反应生成乙醇
2
D.反应体系中乙醇的物质的量浓度不再变化
21.在一定温度下,向密闭容器中充入一定量的 NO 和SO ,发生反应:NO +SO NO+
2 2 2 2
SO (g),当化学反应达到平衡时,下列叙述正确的是( )
3
A.SO 和SO 的物质的量一定相等
2 3
B.NO 和SO 的物质的量一定相等
2 3
C.反应混合物的总物质的量一定等于反应开始时NO 和SO 的总物质的量
2 2
D.SO 、NO 、NO、SO 的物质的量一定相等
2 2 3
22.课堂学习中,同学们利用铝条、锌片、铜片、导线、电流计、橙汁、烧杯等用品探究原电池的组
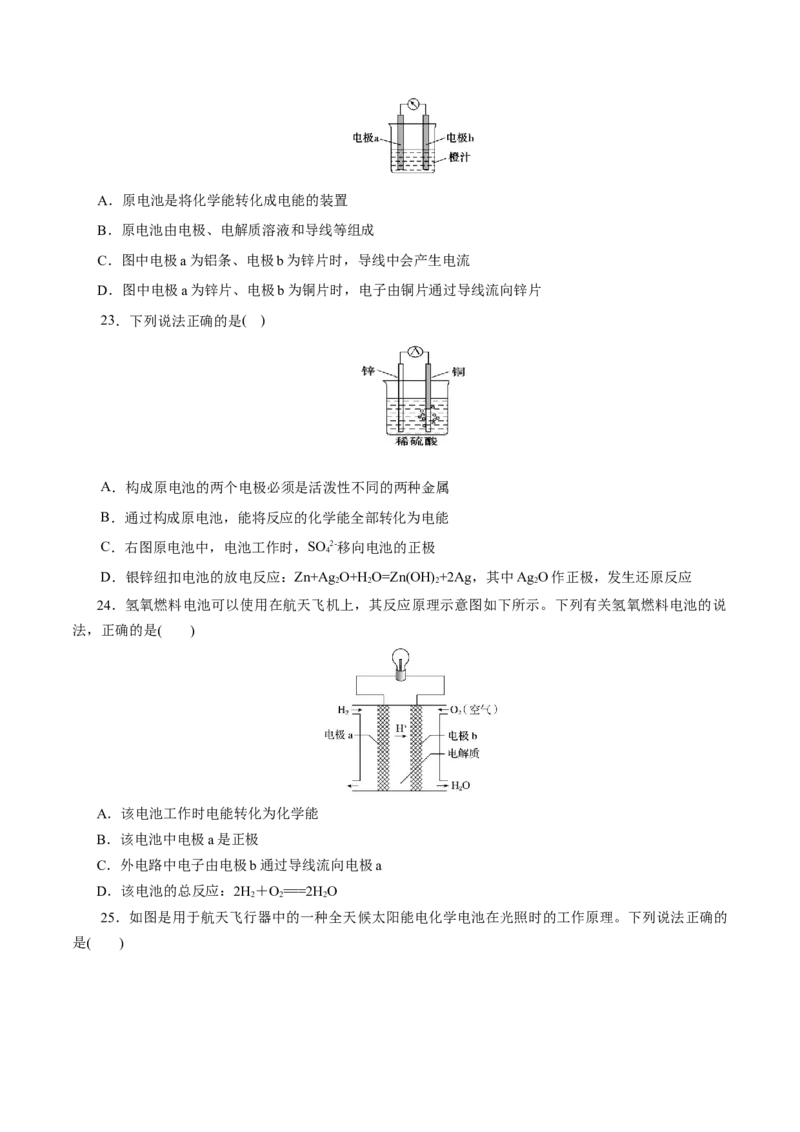
成。下列结论错误的是( )A.原电池是将化学能转化成电能的装置
B.原电池由电极、电解质溶液和导线等组成
C.图中电极a为铝条、电极b为锌片时,导线中会产生电流
D.图中电极a为锌片、电极b为铜片时,电子由铜片通过导线流向锌片
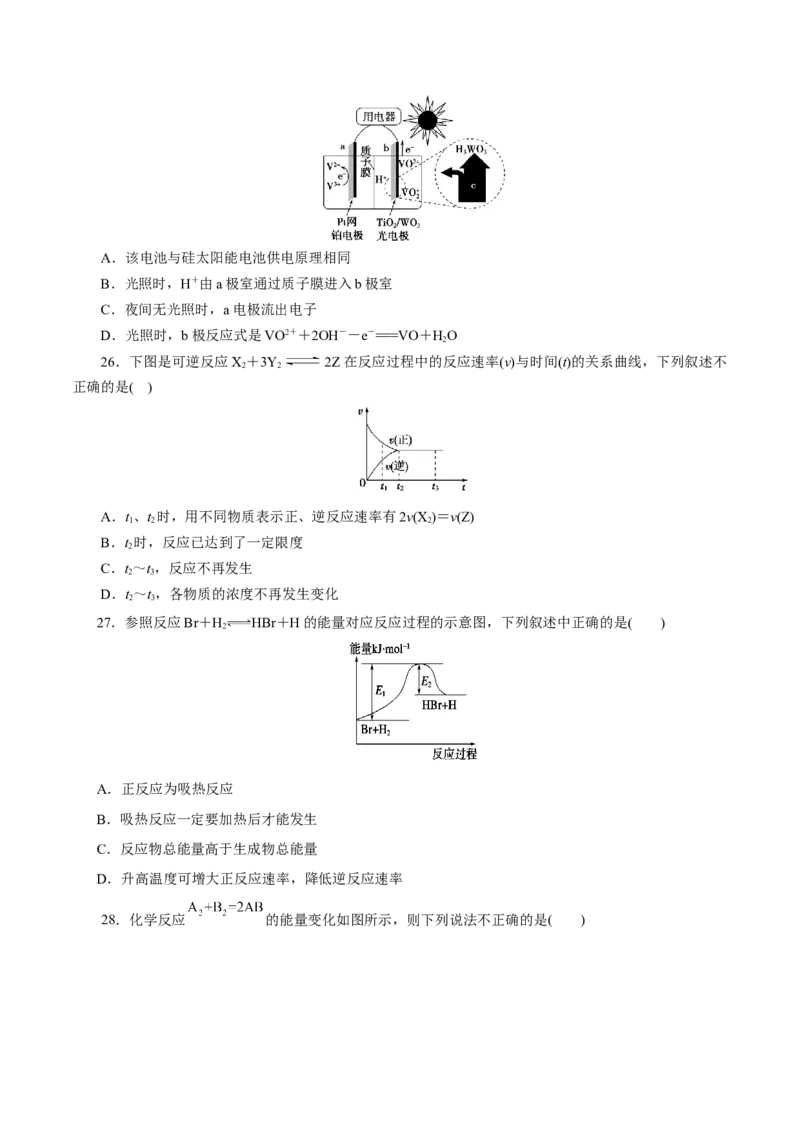
23.下列说法正确的是( )
A.构成原电池的两个电极必须是活泼性不同的两种金属
B.通过构成原电池,能将反应的化学能全部转化为电能
C.右图原电池中,电池工作时,SO 2-移向电池的正极
4
D.银锌纽扣电池的放电反应:Zn+Ag O+HO=Zn(OH) +2Ag,其中Ag O作正极,发生还原反应
2 2 2 2
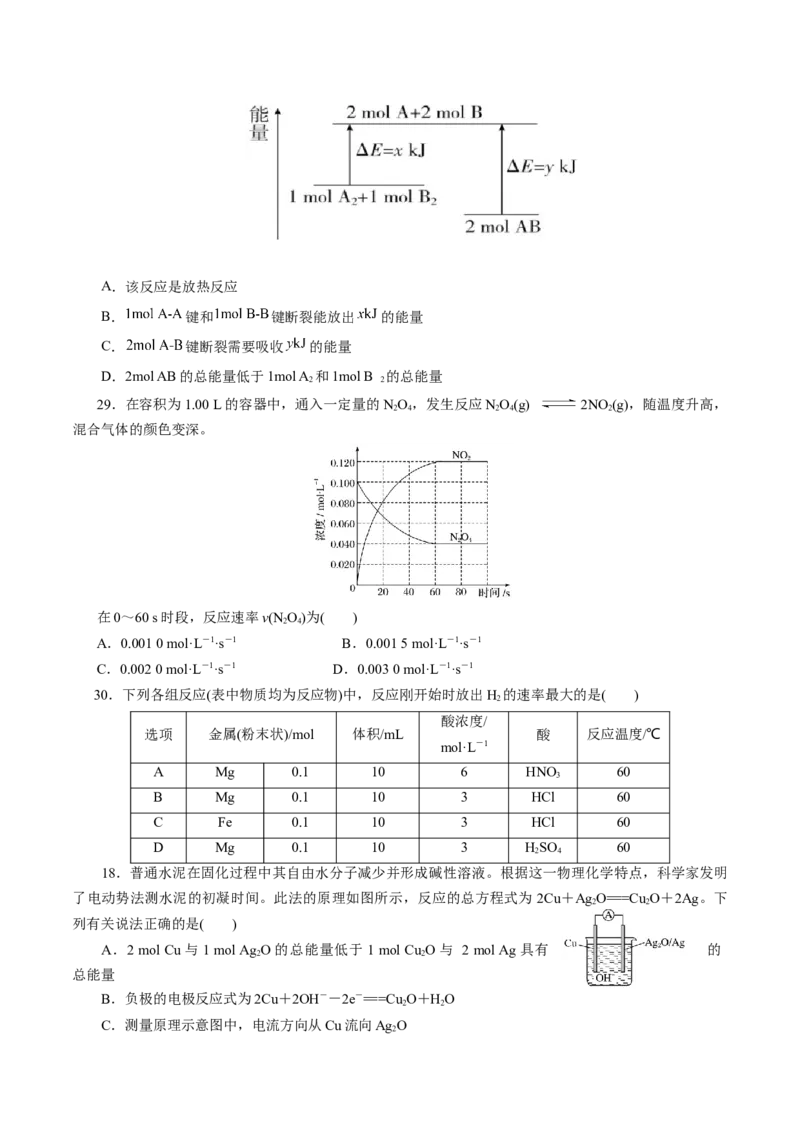
24.氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如下所示。下列有关氢氧燃料电池的说
法,正确的是( )
A.该电池工作时电能转化为化学能
B.该电池中电极a是正极
C.外电路中电子由电极b通过导线流向电极a
D.该电池的总反应:2H+O===2H O
2 2 2
25.如图是用于航天飞行器中的一种全天候太阳能电化学电池在光照时的工作原理。下列说法正确的
是( )A.该电池与硅太阳能电池供电原理相同
B.光照时,H+由a极室通过质子膜进入b极室
C.夜间无光照时,a电极流出电子
D.光照时,b极反应式是VO2++2OH--e-===VO+HO
2
26.下图是可逆反应X +3Y 2Z在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述不
2 2
正确的是( )
A.t、t 时,用不同物质表示正、逆反应速率有2v(X )=v(Z)
1 2 2
B.t 时,反应已达到了一定限度
2
C.t~t,反应不再发生
2 3
D.t~t,各物质的浓度不再发生变化
2 3
27.参照反应Br+H HBr+H的能量对应反应过程的示意图,下列叙述中正确的是( )
2
A.正反应为吸热反应
B.吸热反应一定要加热后才能发生
C.反应物总能量高于生成物总能量
D.升高温度可增大正反应速率,降低逆反应速率
28.化学反应 的能量变化如图所示,则下列说法不正确的是( )A.该反应是放热反应
B. 键和 键断裂能放出 的能量
C. 键断裂需要吸收 的能量
D.2mol AB的总能量低于1mol A 和1mol B 的总能量
2 2
29.在容积为1.00 L的容器中,通入一定量的NO ,发生反应NO(g) 2NO (g),随温度升高,
2 4 2 4 2
混合气体的颜色变深。
在0~60 s时段,反应速率v(N O)为( )
2 4
A.0.001 0 mol·L-1·s-1 B.0.001 5 mol·L-1·s-1
C.0.002 0 mol·L-1·s-1 D.0.003 0 mol·L-1·s-1
30.下列各组反应(表中物质均为反应物)中,反应刚开始时放出H 的速率最大的是( )
2
酸浓度/
选项 金属(粉末状)/mol 体积/mL 酸 反应温度/℃
mol·L-1
A Mg 0.1 10 6 HNO 60
3
B Mg 0.1 10 3 HCl 60
C Fe 0.1 10 3 HCl 60
D Mg 0.1 10 3 HSO 60
2 4
18.普通水泥在固化过程中其自由水分子减少并形成碱性溶液。根据这一物理化学特点,科学家发明
了电动势法测水泥的初凝时间。此法的原理如图所示,反应的总方程式为 2Cu+Ag O===Cu O+2Ag。下
2 2
列有关说法正确的是( )
A.2 mol Cu与1 mol Ag O的总能量低于1 mol Cu O与 2 mol Ag具有 的
2 2
总能量
B.负极的电极反应式为2Cu+2OH--2e-===Cu O+HO
2 2
C.测量原理示意图中,电流方向从Cu流向Ag O
2D.电池工作时,OH-向正极移动
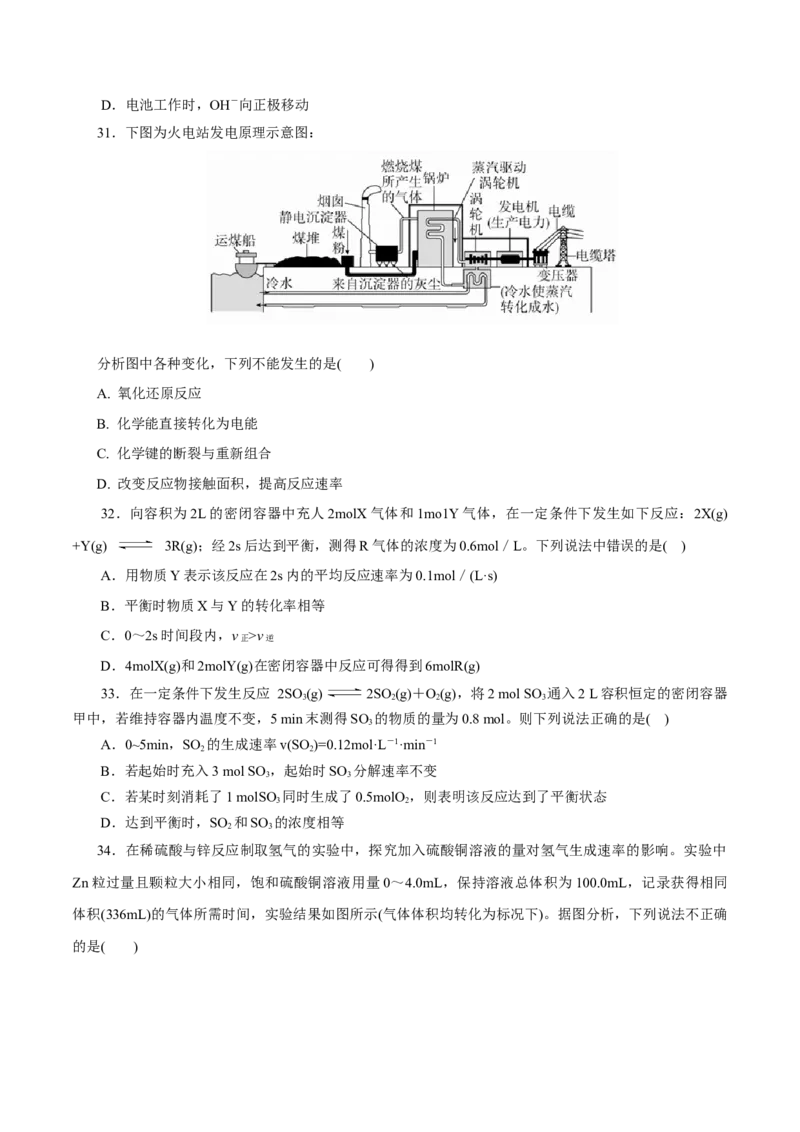
31.下图为火电站发电原理示意图:
分析图中各种变化,下列不能发生的是( )
A. 氧化还原反应
B. 化学能直接转化为电能
C. 化学键的断裂与重新组合
D. 改变反应物接触面积,提高反应速率
32.向容积为2L的密闭容器中充人2molX气体和1mo1Y气体,在一定条件下发生如下反应:2X(g)
+Y(g) 3R(g);经2s后达到平衡,测得R气体的浓度为0.6mol/L。下列说法中错误的是( )
A.用物质Y表示该反应在2s内的平均反应速率为0.1mol/(L·s)
B.平衡时物质X与Y的转化率相等
C.0~2s时间段内,v >v
正 逆
D.4molX(g)和2molY(g)在密闭容器中反应可得得到6molR(g)
33.在一定条件下发生反应 2SO (g) 2SO (g)+O(g),将2 mol SO 通入2 L容积恒定的密闭容器
3 2 2 3
甲中,若维持容器内温度不变,5 min末测得SO 的物质的量为0.8 mol。则下列说法正确的是( )
3
A.0~5min,SO 的生成速率v(SO )=0.12mol·L-1·min-1
2 2
B.若起始时充入3 mol SO ,起始时SO 分解速率不变
3 3
C.若某时刻消耗了1 molSO 同时生成了0.5molO,则表明该反应达到了平衡状态
3 2
D.达到平衡时,SO 和SO 的浓度相等
2 3
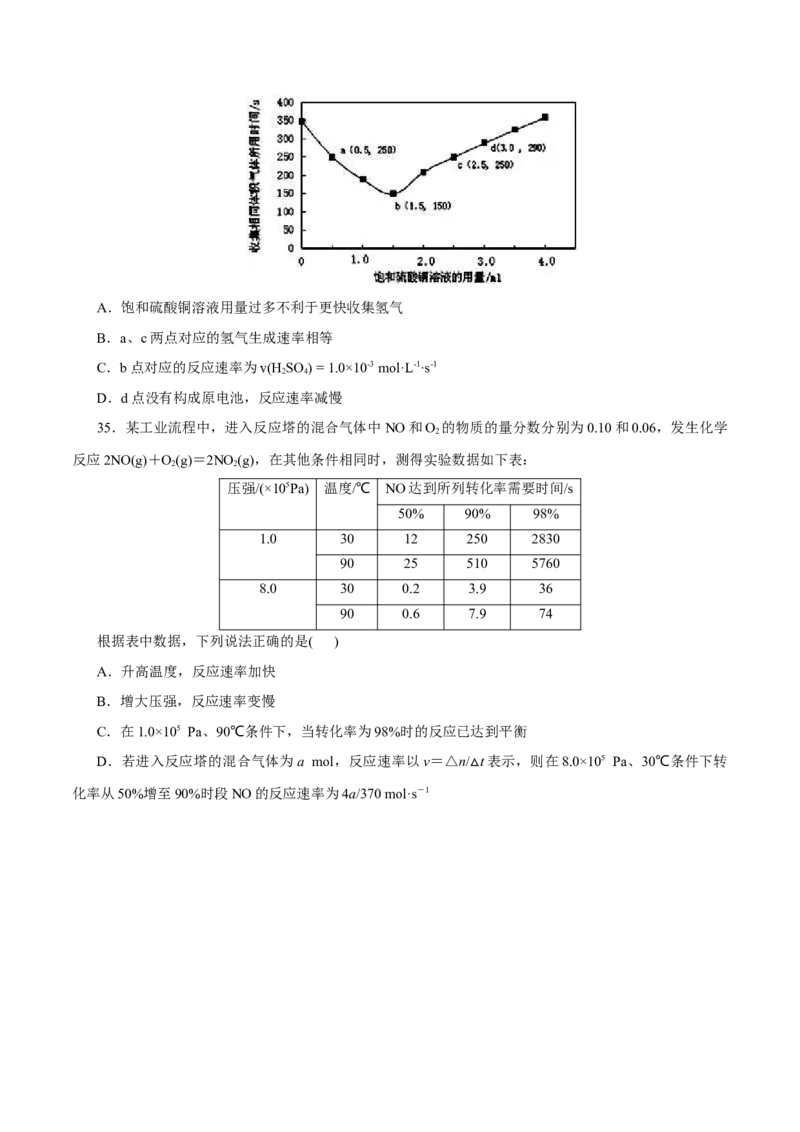
34.在稀硫酸与锌反应制取氢气的实验中,探究加入硫酸铜溶液的量对氢气生成速率的影响。实验中
Zn粒过量且颗粒大小相同,饱和硫酸铜溶液用量0~4.0mL,保持溶液总体积为100.0mL,记录获得相同
体积(336mL)的气体所需时间,实验结果如图所示(气体体积均转化为标况下)。据图分析,下列说法不正确
的是( )A.饱和硫酸铜溶液用量过多不利于更快收集氢气
B.a、c两点对应的氢气生成速率相等
C.b点对应的反应速率为v(H SO ) = 1.0×10-3 mol·L-1·s-1
2 4
D.d点没有构成原电池,反应速率减慢
35.某工业流程中,进入反应塔的混合气体中NO和O 的物质的量分数分别为0.10和0.06,发生化学
2
反应2NO(g)+O(g)=2NO (g),在其他条件相同时,测得实验数据如下表:
2 2
压强/(×105Pa) 温度/℃ NO达到所列转化率需要时间/s
50% 90% 98%
1.0 30 12 250 2830
90 25 510 5760
8.0 30 0.2 3.9 36
90 0.6 7.9 74
根据表中数据,下列说法正确的是( )
A.升高温度,反应速率加快
B.增大压强,反应速率变慢
C.在1.0×105 Pa、90℃条件下,当转化率为98%时的反应已达到平衡
D.若进入反应塔的混合气体为a mol,反应速率以v=△n/ t表示,则在8.0×105 Pa、30℃条件下转
化率从50%增至90%时段NO的反应速率为4a/370 mol·s-1 △