文档内容
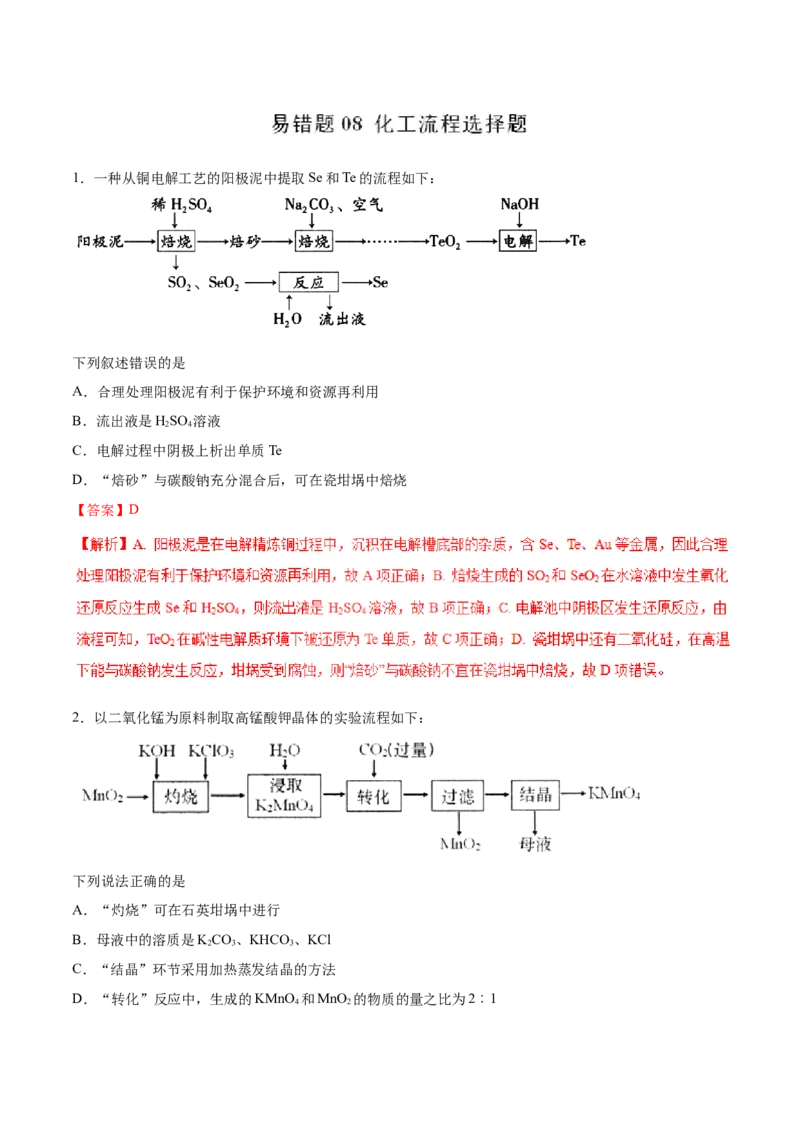
1.一种从铜电解工艺的阳极泥中提取Se和Te的流程如下:
下列叙述错误的是
A.合理处理阳极泥有利于保护环境和资源再利用
B.流出液是HSO 溶液
2 4
C.电解过程中阴极上析出单质Te
D.“焙砂”与碳酸钠充分混合后,可在瓷坩埚中焙烧
【答案】D
2.以二氧化锰为原料制取高锰酸钾晶体的实验流程如下:
下列说法正确的是
A.“灼烧”可在石英坩埚中进行
B.母液中的溶质是KCO、KHCO 、KCl
2 3 3
C.“结晶”环节采用加热蒸发结晶的方法
D.“转化”反应中,生成的KMnO 和MnO 的物质的量之比为2︰1
4 2【答案】D
【解析】A.“灼烧”时,可在铁坩埚中进行,KOH与玻璃中的二氧化硅反应,选项A错误;B.结晶后的母液
中有KMnO 、KMnO 和KCO 等溶质,若二氧化碳过量还可能存在碳酸氢钾,选项B错误;C. “结晶”环节
2 4 4 2 3
采用加蒸发浓缩、蒸发结晶的方法,选项C错误;D.由3KMnO +2CO ═2KMnO+MnO↓+2K CO,氧化产物
2 4 2 4 2 2 3
为KMnO ,还原产物为MnO ,氧化产物与还原产物的物质的量之比为2:1,选项D正确。
4 2
3.某学习小组以废催化剂(主要成分SiO、ZnO、ZnS和CuS)为原料,制备锌和铜的硫酸盐晶体。设计的实验
2
方案如下:
下列说法正确的是
A.步骤①中能溶于稀硫酸的是ZnO、ZnS和CuS
B.步骤①、③中发生的反应均为氧化还原反应
C.步骤③涉及的离子反应可能为CuS+HO+2H+ Cu2++S+2HO
2 2 2
D.步骤②和④,采用蒸发结晶,过滤后均可获取粗晶体
【答案】C
4.从海水晒盐的母液中提取金属镁的一种工艺流程如下:
下列说法不正确的是
A.步骤① 沉镁可加入石灰乳,说明Mg(OH) 的溶解度更小
2
B.步骤③ 脱水时,在空气中加热MgCl ·6H O得到MgCl
2 2 2
C.步骤④ 电解熔融MgCl 时,阴极有金属Mg析出
2D.设计步骤① 、② 、③ 的主要目的是富集镁元素
【答案】B
5.废铁屑制Fe O 的一种流程如下图:
2 3
下列说法不正确的是
A.热的纯碱溶液可去除废铁屑表面的油污
[来源:学科网]
B.操作a是萃取
C.冰水既可洗去杂质又可减少固休的溶解
D.Fe O 可用作红色颜料
2 3
【答案】B
【解析】A.热的纯碱溶液可去除废铁屑表面的油污,故A项正确;B.操作a是过滤,故B项错误;C.冰水既可洗
去杂质又降低温度,减少固休的溶解,故C项正确;D.Fe O 俗名铁红,可用作红色颜料,故D项正确。
2 3
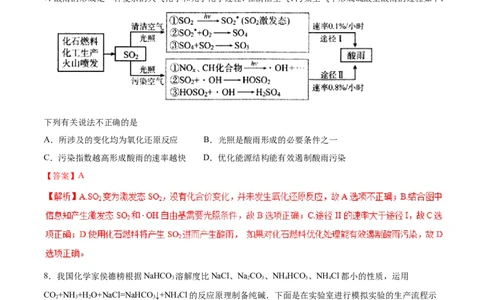
6.一种以“火法粗炼”、“电解精炼”相结合的炼制精铜工艺流程如下,已知“还原”反应中,冰铜中的
Cu S先转化为Cu O,然后Cu O再与Cu S反应生成粗铜。下列叙述正确的是
2 2 2 2
A.该炼铜工艺对环境友好,不会产生大气污染物
B.“烙烧”过程中, CuFeS 既是氧化剂又是还原剂
2
C.在Cu S”还原”为Cu的总反应中,Cu O作催化剂
2 2
D.“电解”时,金、银等贵金属被置换出来形成阳极泥
【答案】B
【解析】A、根据流程,冰铜得到粗铜过程中发生的反应是2Cu S+3O 2Cu O+2SO 、2Cu O+Cu S
2 2 2 2 2 26Cu+SO ↑,SO 能引起酸雨,属于大气污染物,该工艺对环境不友好,故A说法错误;B、焙烧中发生
2 2
2CuFeS+O Cu S+2FeS+SO ,CuFeS 中S的价态为-2价,Fe的基态为+2价,Cu的价态为+2价,
2 2 2 2 2
在反应中部分S的价态升高,Cu的价态降低,因此CuFeS 在该反应中既是氧化剂又是还原剂,故B说法正
2
确;C、根据催化剂的定义,以及A选项分析,Cu O不是催化剂,故C说法错误;D、粗铜中金、银以单质的形
2
式存在,没有发生反应,金、银最终以单质的形式在阳极沉积出来,故D说法错误。
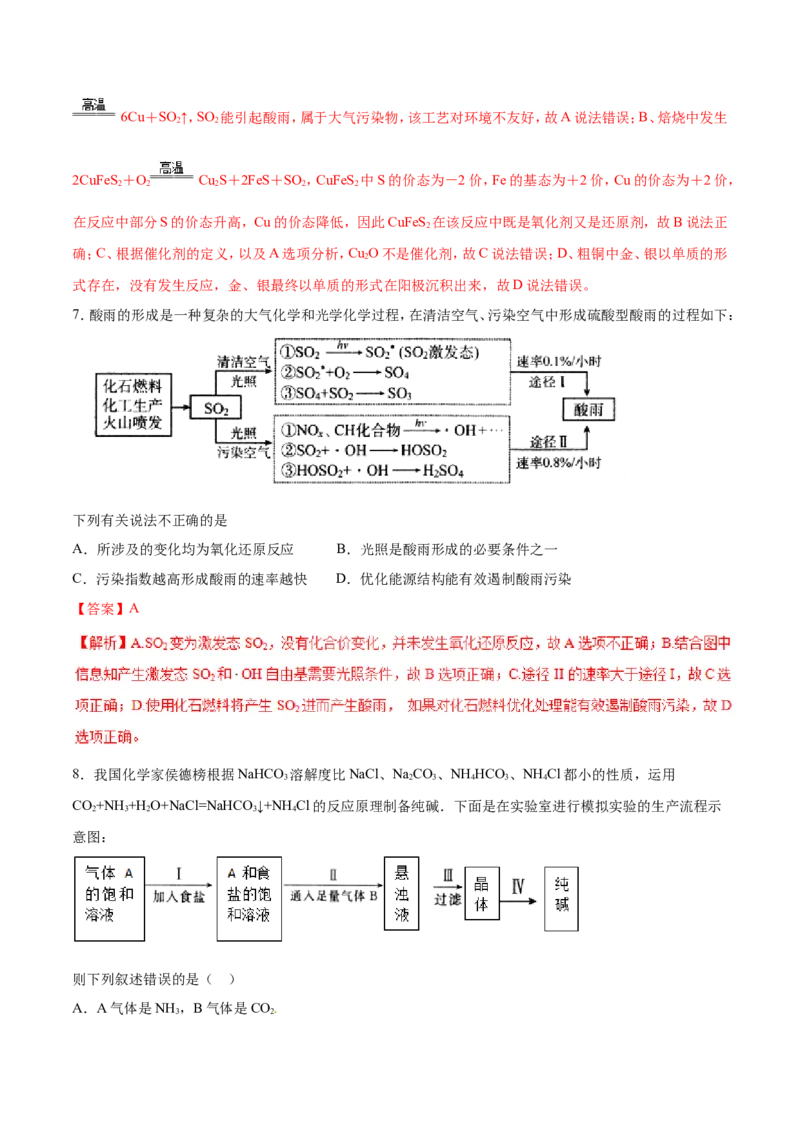
7.酸雨的形成是一种复杂的大气化学和光学化学过程,在清洁空气、污染空气中形成硫酸型酸雨的过程如下:
下列有关说法不正确的是
A.所涉及的变化均为氧化还原反应 B.光照是酸雨形成的必要条件之一
C.污染指数越高形成酸雨的速率越快 D.优化能源结构能有效遏制酸雨污染
【答案】A
8.我国化学家侯德榜根据NaHCO 溶解度比NaCl、NaCO、NH HCO 、NH Cl都小的性质,运用
3 2 3 4 3 4
CO+NH+H O+NaCl=NaHCO ↓+NHCl的反应原理制备纯碱.下面是在实验室进行模拟实验的生产流程示
2 3 2 3 4
意图:
则下列叙述错误的是( )
A.A气体是NH ,B气体是CO
3 2B.把纯碱及第Ⅲ步得到的晶体与某些固体酸性物质(如酒石酸)混合可制得发酵粉
C.纯碱可广泛地用于玻璃、制皂、造纸、纺织等工业中
D.第Ⅳ步操作是将晶体溶于水后加热、蒸发、结晶
【答案】D
9.某同学采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe O、SiO、Al O,不考虑其他杂质)制取七水合硫酸亚
2 3 2 2 3
铁(FeSO ·7H O),设计了如下流程:
4 2
下列说法不正确的是( )
A.溶解烧渣选用足量硫酸,试剂X选用铁粉
B.固体1中一定含有SiO,控制pH是为了使Al3+转化为Al(OH) ,进入固体2
2 3
C.从溶液2得到FeSO ·7H O产品的过程中,须控制条件防止其氧化和分解
4 2
D.若改变方案,在溶液1中直接加NaOH至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到
FeSO ·7H O
4 2
【答案】D
【解析】A、流程设计意图是用硫酸把Fe O、Al O,转化为硫酸盐,除去SiO,然后用铁粉还原Fe3+得到硫酸亚
2 3 2 3 2
铁,A正确;B、固体1为SiO,分离FeSO 和Al (SO ) 采用的是调控pH的方法,使Al3+转化为Al(OH) 沉淀
2 4 2 4 3 3
从而与FeSO 分离,B不正确;C、Fe2+容易被氧化,所以在得到FeSO ·7H O产品的过程中,要防止其被氧化
4 4 2
和分解,C正确;D、在溶液1中直接加过量的NaOH得到的是Fe(OH) 沉淀,但Fe(OH) 不稳定,很容易被氧
2 2
化为Fe(OH) ,这样的话,最终所得的产品不纯,混有较多的杂质Fe (SO ),D不正确。
3 2 4 3
10.中国是茶的故乡,为方便饮用,可通过以下方法制取罐装饮料茶,有关下述过程说法不正确的是A.操作①利用了物质的溶解性
B.操作③的方法属于过滤
C.加热杀菌的温度应在500°C左右
D.抗氧化剂的作用是延长饮料茶的保质期
【答案】C
11.以铜银合金(含少量铁)废料为原料回收银和铜的工艺流程如下:
下列说法正确的是
A.粗铜溶于过量稀硝酸,过滤、低温干燥得纯铜
B.电解时用粗银作阴极,硝酸银溶液为电解质溶液
C.用稀硫酸处理渣料时主要发生了氧化还原反应
D.从滤液B中可以提取绿矾(FeSO ·7H O)
4 2
【答案】D
【解析】A、由流程可知,粗铜中含有少量铁,铁和铜都能溶于过量的稀硝酸中,过滤后低温干燥得不到纯铜,
选项A错误;B、电解时,粗银作阳极,纯银作阴极,选项B错误;C、渣料的主要成分为氧化铜,还含有少量的
氧化铁,两种金属氧化物均能与稀硫酸反应,元素化合价均没有发生变化,没有发生氧氧化还原反应,选项C
错误;D、滤液B中的溶质是硫酸亚铁,采用蒸发浓缩、降温结晶、过滤、洗涤、干燥,可得到绿矾,选项D正确。
12.某电镀污泥含有碲化亚铜(Cu Te)、三氧化二铬(CrO)以及少量金等,某小组设计如下资源综合利用的方
2 2 3
案:已知:碲和硫位于同主族,煅烧时Cu Te发生的反应为Cu Te+2O 2CuO+TeO ,滤渣中TeO 溶于稀硫酸
2 2 2 2 2
发生的反应为TeO +H SO =TeOSO +H O。下列说法不正确的是
2 2 4 4 2
A.“高温”灼烧电镀污泥时铜碲和铬元素都被氧化
B.酸化NaCrO 溶液时可用浓盐酸
2 4
C.上述流程可以回收的金属单质有金和铜
D.滤液3可以循环利用
【答案】B
13.绿水青山是习近平总书记构建美丽中国的伟大构想,某工厂拟综合处理含NH +废水和工业废气(主要含
4
N、CO、SO 、NO、CO,不考虑其他成分),设计了如下流程:
2 2 2
下列说法正确的是
A.固体1中主要含有CaCO 、CaSO
3 3
B.X可以是空气,且需过量
C.捕获剂所捕获的气体主要是COD.处理含NH +废水时,发生的反应为:NH ++5NO-+4H+=6NO↑+4HO
4 4 2 2
【答案】C
【解析】A.固体还包括过量的Ca(OH) ,A错;B.通入空气不能过量,不然会生成NO -,B错;C.通过分析,气体
2 3
2为一氧化碳和氮气的混合气体,氮气无污染,所以捕获气体为一氧化碳,C项正确;D、铵根离子和亚硝酸根
离子发生氧化还原反应生成氮气,方程式为NH ++NO-=N ↑+2H O,D错。
4 2 2 2
14.用铁泥(主要成分为Fe O、FeO和少量Fe)制备纳米Fe O,的流程示意图如下:
2 3 3 4
下列叙述错误的是
A.为提高步骤①的反应速率,可采取搅拌、升温等措施
B.步骤②中,主要反应的离子方程式是2Fe3++Fe=3Fe2+
C.步骤④中,反应完成后剩余的HO 无需除去
2 2
D.步骤⑤中,“分离”包含的操作有过滤、洗涤
【答案】C
15.BHT是一种常用的食品抗氧化剂,合成方法有如下两种:
下列说法正确的是
A. 能与NaCO 溶液反应生成CO
2 3 2B. 与BHT互为同系物
C.BHT久置于空气中不会被氧化
D.两种方法的反应类型都是加成反应
【答案】B
【解析】酚羟基不能和碳酸钠反应产生CO,所以A不正确。BHT和苯酚的结构相似,属于同一类有机物,互
2
为同系物,B正确。酚羟基易被氧化,C正确。方法二是取代反应,D不正确,答案选BC。
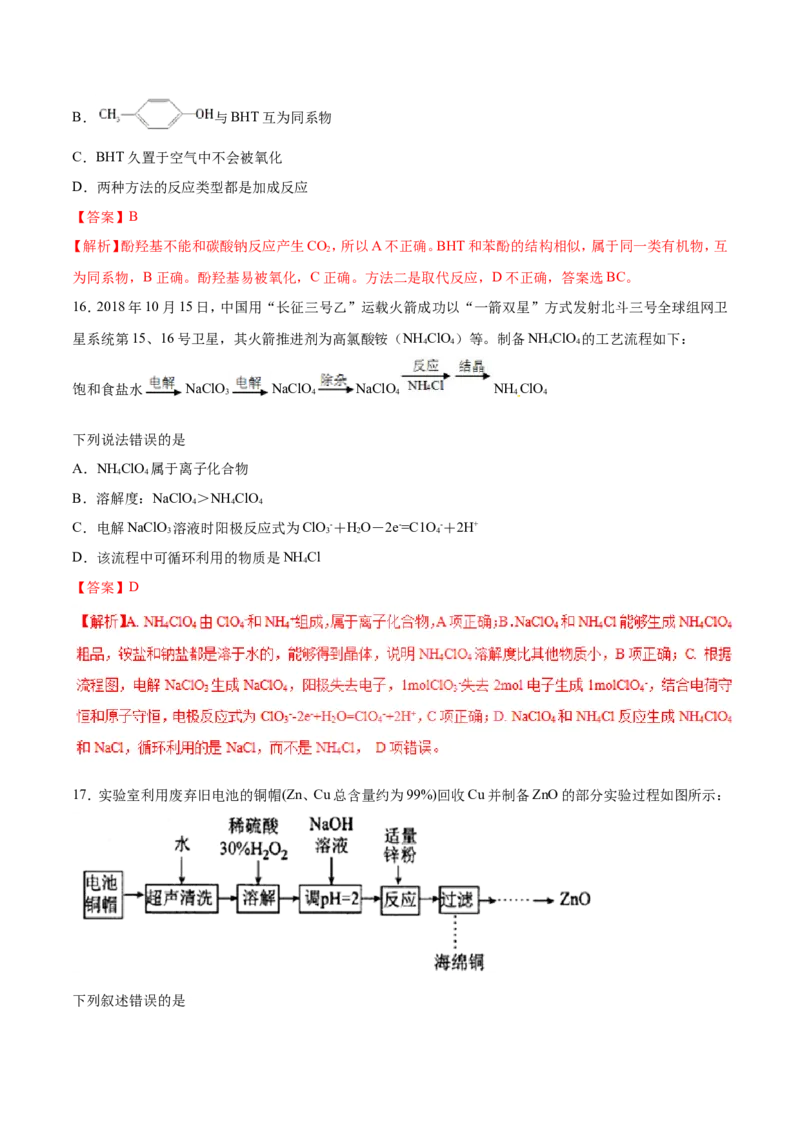
16.2018年10月15日,中国用“长征三号乙”运载火箭成功以“一箭双星”方式发射北斗三号全球组网卫
星系统第15、16号卫星,其火箭推进剂为高氯酸铵(NH ClO )等。制备NH ClO 的工艺流程如下:
4 4 4 4
饱和食盐水 NaClO NaClO NaClO NH ClO
3 4 4 4 4
下列说法错误的是
A.NH ClO 属于离子化合物
4 4
B.溶解度:NaClO>NH ClO
4 4 4
C.电解NaClO 溶液时阳极反应式为ClO -+HO-2e-=C1O -+2H+
3 3 2 4
D.该流程中可循环利用的物质是NH Cl
4
【答案】D
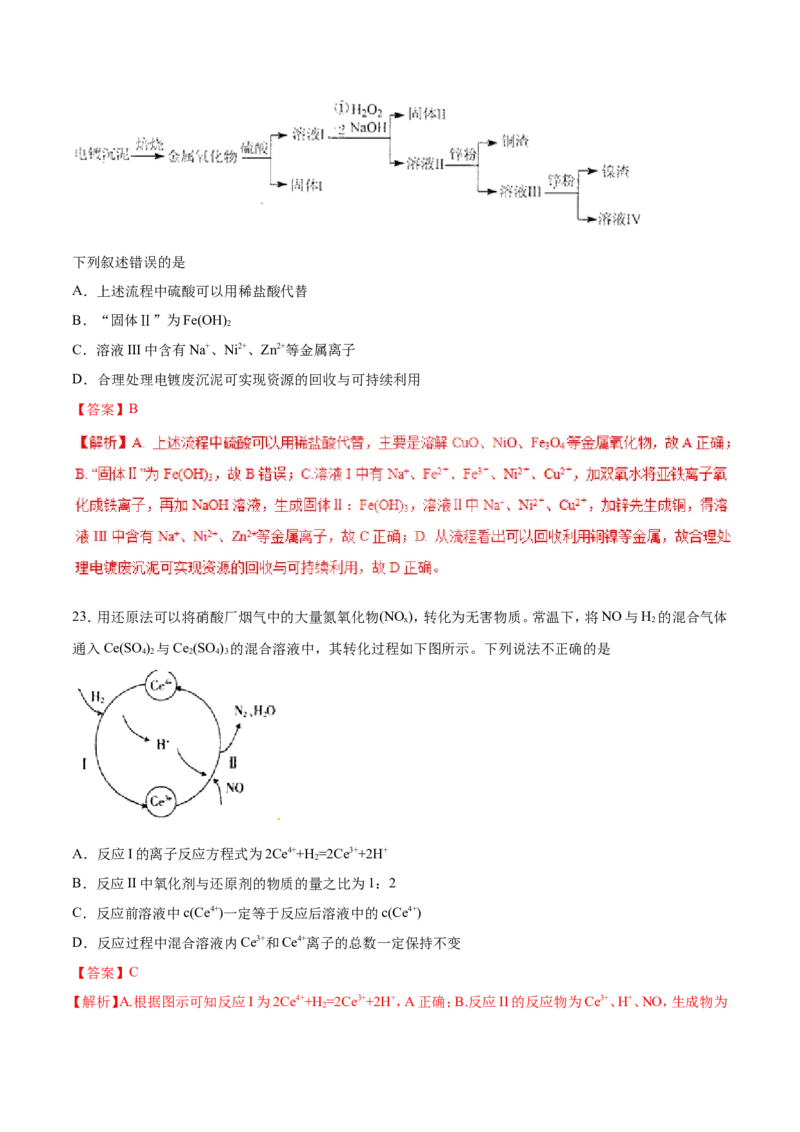
17.实验室利用废弃旧电池的铜帽(Zn、Cu总含量约为99%)回收Cu并制备ZnO的部分实验过程如图所示:
下列叙述错误的是
[来源:学科网]A.合理处理废弃旧电池的铜帽既有利于节约资源,又有利于保护环境
B.“溶解”操作中可用酸性条件下不断鼓入O 代替HO
2 2 2
C.加入锌粉反应的离子为Cu2+
D.“过滤”操作后直接将溶液蒸发结晶、高温灼烧得到ZnO
【答案】D
18.聚合硫酸铁(PFS)是水处理中重要的絮凝剂,以废铁屑为原料制备PFS的具体工艺流程如下:
下列说法不正确的是
A.步骤①,粉碎的目的是为了增大反应物接触面积,提高“酸浸”反应速率
B.步骤③,可以选择双氧水、氯气等氧化剂将Fe2+转化成Fe3+
C.步骤④,加稀硫酸调节pH在一定的范围内,让Fe3+部分水解形成碱式盐
D.步骤⑤,减压蒸发,有利于降低水的沸点防止产物分解
【答案】B
【解析】A.废铁屑粉碎后,使反应物接触面积增大,能够加快化学反应速率,故A正确;B.若使用氯气作氧化
剂,将Fe2+氧化成Fe3+的同时,引入了新的杂质离子Cl-,故B错误;C. 步骤④,加稀硫酸调节pH在一定的范
围内,Fe3+部分水解生成Fe(OH) 进而生成碱式盐,故C正确;D. 减压蒸发,可以防止温度过高,聚合硫酸铁
3
分解,故D正确。
19.硫酸亚铁是一种重要的化工原料,可以制备一系列物质(如图所示)。下列说法错误的是A.碱式硫酸铁水解能产生Fe(OH) 胶体,可用做净水剂
3
B.该温度下,(NH )Fe(SO ) 在水中的溶解度比FeSO 的大
4 2 4 2 4
C.可用KSCN溶液检验(NH )Fe(SO ) 是否被氧化
4 2 4 2
D.为防止NH HCO 分解,生产FeCO 需在较低温度下进行
4 3 3
【答案】B
20.过氧化钙晶体(CaO·8H O)常用作医药消毒剂,可以轻质碳酸钙为原料,按以下实验方法来制备。
2 2
下列有关说法正确的是
[来源:Zxxk.Com]
A.①煮沸的主要目的是为了除去溶解的CO
2
B.②的反应中HO 作氧化剂,氨水用来调节溶液的pH
2 2
C.②中结晶的颗粒较小,过滤时可用玻璃棒轻轻搅动
D.③醇洗的主要目的是为了减少晶体的损失
【答案】D21.港珠澳大桥水泥的使用量约198万吨。水泥熟料的主要成分为CaO、SiO,并含有一定量的铁、铝和镁等
2
金属的氧化物。实验室测定水泥样品中钙含量的过程如图所示:
下列叙述正确的是
A.水泥、玻璃、陶瓷为传统的硅酸盐材料,三者的原料都主要为SiO
2
B.沉淀A主要成分为SiO,沉淀B为Fe(OH) 、Al(OH)
2 3 3
C.为了加快溶解速率,使用盐酸代替硫酸处理草酸钙
[来源:学+科+网]
D.草酸钙易溶于水
【答案】B
【解析】A.水泥、玻璃、陶瓷均为硅酸盐工业产品,所以主要成分是硅酸盐,三者的原料不同,三者的原料并非
都主要为SiO,例如:陶瓷的主要原料有黏土等,水泥的主要原料有石灰石和黏土(铝硅酸盐),故A错误;B.
2
水泥样品的主要成分为CaO、SiO,并含有一定量的铁、铝和镁等金属的氧化物,加入氯化铵、盐酸和硝酸,由
2
于二氧化硅与酸不反应,则得到的沉淀A为SiO,滤液中含有Ca2+、Fe3+、Al3+、Mg2+等离子,加入氨水调节pH
2
到4~5之间,可生成Al(OH) 、Fe(OH) 沉淀,则沉淀B为Fe(OH) 、Al(OH) ,故B正确;C.使用盐酸代替硫酸
3 3 3 3
处理草酸钙,在溶液中剩余的盐酸也能被高锰酸钾氧化,从而干扰草酸的测定,进而使测得的钙的含量产生
误差,故C错误;D.草酸钙是难溶于水的白色固体,故D错误。
22.电镀废水沉泥中含Cu、Ni、Ag和Fe等多种元素的有机金属盐,采用焙烧一浸出—分离回收的工艺流程
可有效分离电镀废水沉泥中的金属,其流程如下:下列叙述错误的是
A.上述流程中硫酸可以用稀盐酸代替
B.“固体Ⅱ”为Fe(OH)
2
C.溶液III中含有Na+、Ni2+、Zn2+等金属离子
D.合理处理电镀废沉泥可实现资源的回收与可持续利用
【答案】B
23.用还原法可以将硝酸厂烟气中的大量氮氧化物(NO ),转化为无害物质。常温下,将NO与H 的混合气体
x 2
通入Ce(SO) 与Ce (SO ) 的混合溶液中,其转化过程如下图所示。下列说法不正确的是
4 2 2 4 3
A.反应I的离子反应方程式为2Ce4++H =2Ce3++2H+
2
B.反应II中氧化剂与还原剂的物质的量之比为1:2
C.反应前溶液中c(Ce4+)一定等于反应后溶液中的c(Ce4+)
D.反应过程中混合溶液内Ce3+和Ce4+离子的总数一定保持不变
【答案】C
【解析】A.根据图示可知反应I为2Ce4++H =2Ce3++2H+,A正确;B.反应II的反应物为Ce3+、H+、NO,生成物为
2Ce4+、N、HO,根据电子守恒、电荷守恒及原子守恒,可得反应方程式为 4Ce3++4H++2NO=4Ce4++N +2H O,在
2 2 2 2
该反应中NO是氧化剂,Ce3+是还原剂,故氧化剂与还原剂的物质的量的比为2:4=1:2,B正确;C.反应前后
溶液中n(Ce4+)的物质的量不变,但由于反应后溶液中水的物质的量增多,所以反应后溶液中c(Ce4+)减小,C
错误;D.由于反应前后各种元素的原子个数相等,根据Ce元素守恒可知反应过程中混合溶液内Ce3+和
Ce4+离子的总数不变,D正确。
24.练江整治已刻不容缓,其中以印染工业造成的污染最为严重。某工厂拟综合处理含NH + 废水和工业废气
4
(主要含N、CO、SO 、NO、CO),设计了如下工业流程:
2 2 2
下列说法错误的是
A.气体I中主要含有的气体有N、NO、CO
2
B.X在反应中作氧化剂,可通入过量的空气
C.处理含NH +废水时,发生离子方程式是:NH ++NO-=N ↑+2H O
4 4 2 2 2
D.捕获剂所捕获的气体主要是CO
【答案】B
25.利用食盐水制取ClO 的工业流程如图所示,装置①中的反应:NaCl+3H O NaClO+3H ↑,装置②中
2 2 3 2
的反应:2NaClO+4HCl 2ClO + Cl ↑+2NaCl+2HO。下列关于该流程说法不正确的是( )
3 2 2 2A.该流程中Cl、NaCl都可以循环利用
2
B.装置①中H 是阴极产物
2
C.装置②发生的反应中,Cl 是氧化产物,NaCl是还原产物
2
D.为了使H 完全转化为HCl,需要向装置③中补充Cl
2 2[来源:学科网ZXXK]
【答案】C