文档内容
专题 08 水溶液中的离子反应与平衡
目录
01考情透视·目标导航............................................................................................................................
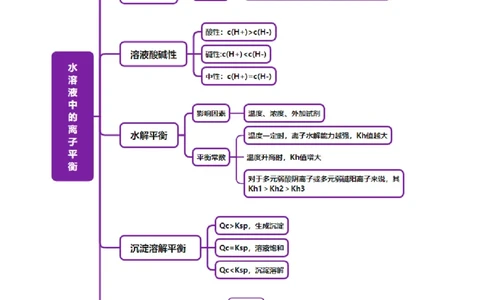
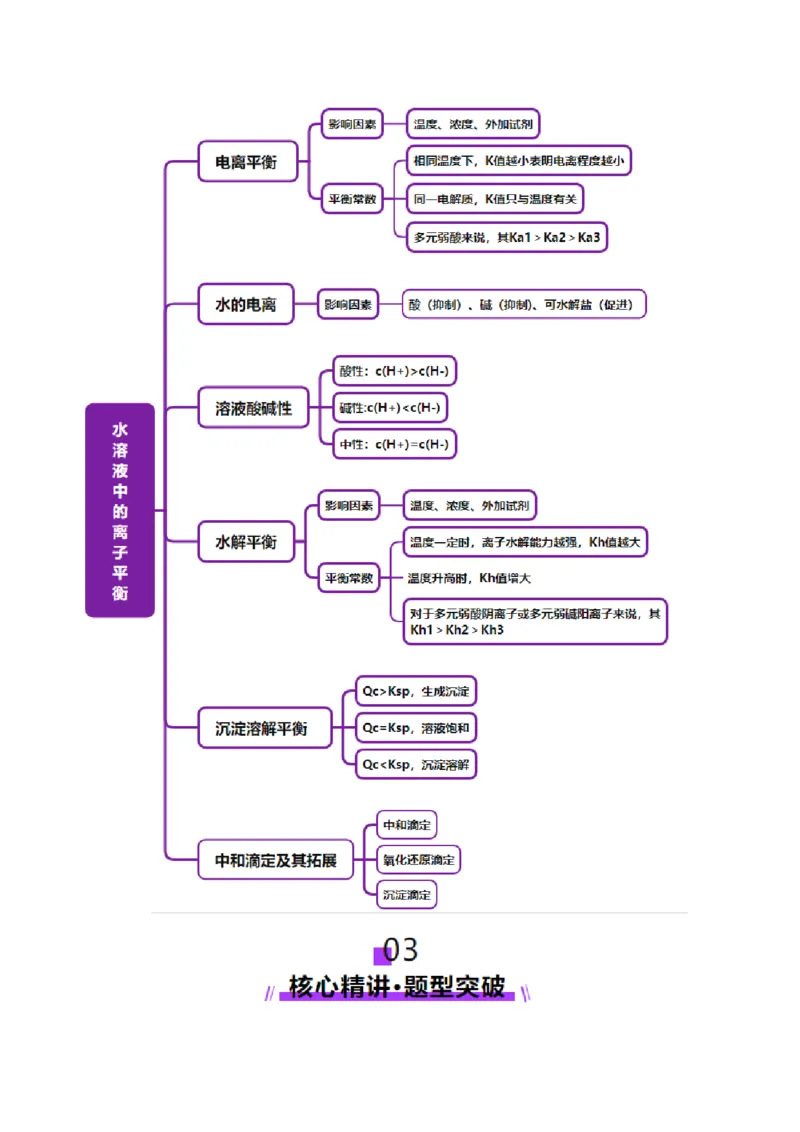
02知识导图·思维引航............................................................................................................................
03核心精讲·题型突破............................................................................................................................
题型一 电离平衡、水解平衡、沉淀溶解平衡及其应用....................................................................
【真题研析】...................................................................................................................................................................
【核心精讲】...................................................................................................................................................................
1.电解质溶液中的三大平衡.........................................................................................................................................
2.电离平衡常数.............................................................................................................................................................
3.水解平衡常数(K )......................................................................................................................................................
h
4.溶度积常数(K ).........................................................................................................................................................
sp
【命题预测】...................................................................................................................................................................
题型二 电离常数、水解常数、溶度积常数的综合应用...............................................................................
【真题研析】...................................................................................................................................................................
【核心精讲】...................................................................................................................................................................
1.电离常数的4大应用.................................................................................................................................................
2.K 、K、K 、K 、K 之间的关系............................................................................................................................
w a b sp h
3.电离常数与水解常数的关系.....................................................................................................................................
【命题预测】...................................................................................................................................................................
题型三 中和滴定及其拓展应用............................................................................................................
【真题研析】...................................................................................................................................................................
【核心精讲】...................................................................................................................................................................
1.中和滴定.....................................................................................................................................................................
2.氧化还原滴定.............................................................................................................................................................
3.沉淀滴定.....................................................................................................................................................................
【命题预测】...................................................................................................................................................................考点要求 考题统计 考情分析
2024·天津卷,12,3分;2024·安徽卷,7,3 近年高考命题选材,以多平
各平衡常 分;2024·浙江1月卷,15,3分;2024·福建 衡体系溶液的真实情景为素
数之间相 卷,7,4分;2024·江苏卷,16,15分;2023•浙 材,来考查学生系统处理复
互换算及 江省1月选考,15;2023•山东卷,15;2023•江 杂情境中化学问题的能力。
应用 苏卷,12,3分;2023•浙江省6月选考,15,3 常涉及的平衡有水、弱电解
分; 质的电离平衡,盐类水解平
衡,沉淀转化平衡,配合物
的络合平衡。预计2025年将
2023•山东卷,8,3分;2023•湖北省选择性考
中和滴定 在选择题某一选项中以图像
试,18,3分;2023•浙江省1月选考,20(5)
原理及拓 或者文字的形式考查,在填
(6);2023•湖北省选择性考试,18;2023•浙江省
展 空题中结合化学反应原理综
6月选考,20(4);2022•辽宁省选择性,17(7);
合考查。题型一 电离平衡、水解平衡、沉淀溶解平衡及其应用
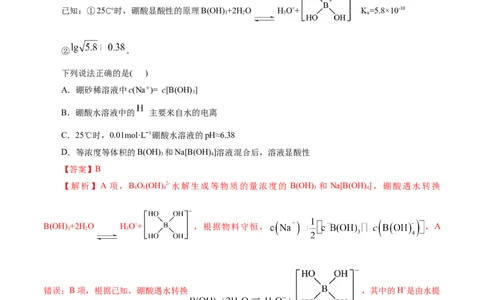
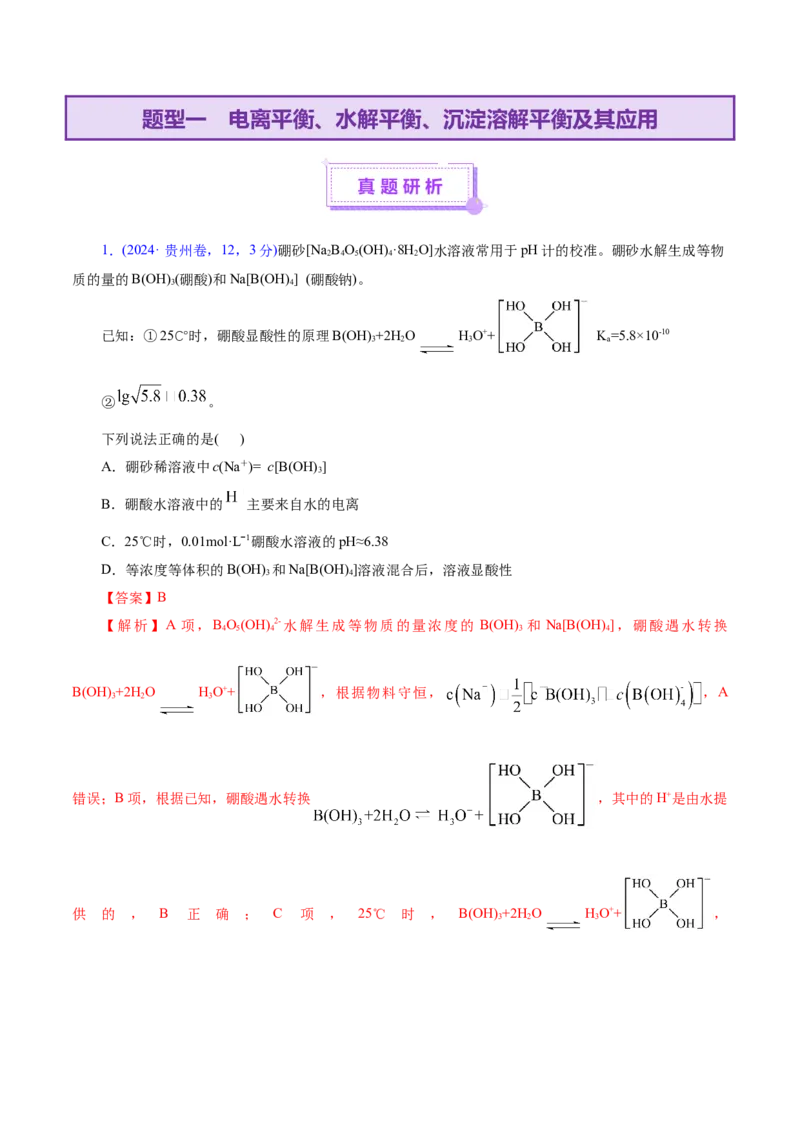
1.(2024· 贵州卷,12,3分)硼砂[Na B O(OH) ·8H O]水溶液常用于pH计的校准。硼砂水解生成等物
2 4 5 4 2
质的量的B(OH) (硼酸)和Na[B(OH) ] (硼酸钠)。
3 4
已知:①25℃时,硼酸显酸性的原理B(OH) +2H O HO++ K=5.8×10-10
3 2 3 a
② 。
下列说法正确的是( )
A.硼砂稀溶液中cNa+= c[B(OH) ]
3
B.硼酸水溶液中的 主要来自水的电离
C.25℃时,0.01mol·Lˉ1硼酸水溶液的pH≈6.38
D.等浓度等体积的B(OH) 和Na[B(OH) ]溶液混合后,溶液显酸性
3 4
【答案】B
【解析】A 项,B O(OH) 2-水解生成等物质的量浓度的 B(OH) 和 Na[B(OH) ],硼酸遇水转换
4 5 4 3 4
B(OH) +2H O HO++ ,根据物料守恒, ,A
3 2 3
错误;B项,根据已知,硼酸遇水转换 ,其中的H+是由水提
供 的 , B 正 确 ; C 项 , 25℃ 时 , B(OH) +2H O HO++ ,
3 2 3, , 因
, ,C错误;D项,B(OH) 的电离平衡常数为K=5.8×10-10,B(OH) -
3 a 4
的水解平衡常数 ,水解程度大于电离程度,显碱性,D错误;故选B。
2.(2022•湖北卷,12,3分)根据酸碱质子理论,给出质子(H+)的物质是酸,给出质子的能力越强,酸
性越强。已知:NH++NH=NH++N H,NH+CH COOH=N H++CH COO-,下列酸性强弱顺序正确的是(
2 5 3 4 2 4 2 4 3 2 5 3
)
A.NH+>NH>NH + B.NH+>CHCOOH>NH +
2 5 2 4 4 2 5 3 4
C.NH >NH>CHCOO- D.CHCOOH>NH+>NH +
3 2 4 3 3 2 5 4
【答案】D
【解析】根据复分解反应的规律,强酸能制得弱酸,根据酸碱质子理论,给出质子(H+)的物质是酸,
则反应NH+CH COOH=N H++CH COO-中,酸性:CHCOOH>NH+,反应NH++NH=NH++N H 中,
2 4 3 2 5 3 3 2 5 2 5 3 4 2 4
酸性:NH+>NH +,故酸性:CHCOOH>NH+>NH +,故选D。
2 5 4 3 2 5 4
3.(2022•全国乙卷,13,6分)常温下,一元酸 的K(HA)=1.0×10-3。在某体系中, 与A-离子不
a
能穿过隔膜,未电离的 可自由穿过该膜(如图所示)。
设溶液中c (HA)=c(HA)+c(A-),当达到平衡时,下列叙述正确的是( )
总
A.溶液Ⅰ中c(H+)=c(OH-)+c(A-)
B.溶液Ⅱ中的HA的电离度 为
C.溶液Ⅰ和Ⅱ中的c(HA)不相等
D.溶液Ⅰ和Ⅱ中的c (HA)之比为10-4
总
【答案】B
【解析】A项,常温下溶液I的pH=7.0,则溶液I中c(H+)=c(OH-)=1×10-7mol/L,c(H+)<c(OH-)+c(A-),A错误;B项,常温下溶液II的pH=1.0,溶液中c(H+)=0.1mol/L,K = =1.0×10-3,c
a 总
(HA)=c(HA)+c(A-),则 =1.0×10-3,解得 = ,B正确;C项,根据题意,未电离的
HA可自由穿过隔膜,故溶液I和II中的c(HA)相等,C错误;D项,常温下溶液I的pH=7.0,溶液I中
c(H+)=1×10-7mol/L,K = =1.0×10-3,c (HA)=c(HA)+c(A-), =1.0×10-3,溶
a 总
液I中c (HA)=(104+1)c(HA),溶液II的pH=1.0,溶液II中c(H+)=0.1mol/L,K = =1.0×10-3,c
总 a 总
(HA)=c(HA)+c(A-), =1.0×10-3,溶液II中c (HA)=1.01c(HA),未电离的HA可自由穿
总
过隔膜,故溶液I和II中的c(HA)相等,溶液I和II中c (HA)之比为
总
[(104+1)c(HA)]∶[1.01c(HA)]=(104+1)∶1.01≈104,D错误;故选B。
4.(2022·浙江省1月选考,17,2分)已知25℃时二元酸HA的K =1.3×10-7,K =7.1×10-15。下列说法
2 a1 a2
正确的是( )
A.在等浓度的NaA、NaHA溶液中,水的电离程度前者小于后者
2
B.向0.1mol·L-1的HA溶液中通入HCl气体(忽略溶液体积的变化)至pH=3,则HA的电离度为
2 2
0.013%
C.向HA溶液中加入NaOH溶液至pH=11,则c(A2-)>c(HA-)
2
D.取pH=a的HA溶液10mL,加蒸馏水稀释至100mL,则该溶液pH=a+1
2
【答案】B
【解析】A项,在等浓度的NaA、NaHA溶液中,A2-的水解程度大于HA-,水的电离程度前者大于后
2
者,故A错误;B项,向0.1mol·L-1的HA溶液中通入HCl气体(忽略溶液体积的变化)至pH=3,
2
,则HA的电离度 0.013%,故B正确;C项,
2向HA溶液中加入NaOH溶液至pH=11, ,则c(A2-)K 时,溶液过饱和,有沉淀析出,直至溶液饱和,达到新的平衡;当Q=K 时,溶液饱和,
c sp c sp
沉淀与溶解处于平衡状态;当QK (RCO),故向c(CO2-)=c(SO2-)的混合液中滴加RCl 溶液,
4 3 sp 4 sp 3 3 4 2
首先析出RCO 沉淀,A错误;B项,将浓度均为3×10-4.5mol•L-1的RCl 、NaCO 溶液等体积混合后,
3 2 2 3
c(R2+)=1.5×10-4.5mol•L-1、c(CO2-)=1.5×10-6mol•L-1,此时的离子积Q=c(R2+)•c(CO 2-)=1.5×10-6×1.5×10-
3 3
6=2.25×10-12
【答案】C
【解析】A项,NaS溶液中存在质子守恒:c(OH-)=c(H+)+c(HS-)+2c(H S),A错误;B项,向AgCl悬
2 2
浊液加入足量氨水,溶液变澄清,得到银氨溶液,离子方程式为AgCl+2NH•H O=[Ag(NH)]++Cl-+2H O,
3 2 3 2 2
B错误;C项,反应2AgCl+S2- Ag S+2Cl-的平衡常数K= = = =
2
=2×1028,当浓度商Q= <K时,反应正向移动,C正确;D项,根据题意沉淀发生转化,
即体系中不会生成AgCl沉淀,所以c(Ag+)< ,D错误;故选C。
11.氢氧化镁是常见难溶物,将过量氢氧化镁粉末置于水中达到溶解平衡:Mg(OH) (s) Mg2+
2
(aq)+ 2OH-(aq)。已知K [Mg(OH) ]=1.8×10-11,K (MgCO )=3.5×10-8;通常,溶液中某离子的浓度小于
sp 2 sp 3
1.0×10-5mol·L-1时,可以认为该离子已沉淀完全。下列有关说法不正确的是( )
A.滴入几滴稀硫酸,溶液的pH先下降后上升,最后保持一个稳定值
B.MgCO 的饱和溶液中c(Mg2+)>c(CO2-)
3 3
C.NaOH溶液可使MgCO 较彻底地转化为Mg(OH)
3 2
D.氢氧化镁可处理印染厂的酸性废水,处理后c(Mg2+)=1.8×10-3mol·L-1,此时溶液呈碱性
【答案】B
【解析】A项,滴入几滴稀硫酸后,氢离子和氢氧根离子反应生成水,氢氧根离子浓度降低,pH降低,
随后沉淀溶解平衡正向移动,氢氧根离子浓度增大,pH增大,A正确;B项,碳酸镁电离产生镁离子和碳
酸根离子,但是碳酸根离子会水解,故镁离子浓度大于碳酸根离子,B错误;C项,通过信息可知,氢氧
化镁的溶度积常数要小的多,故碳酸镁更加容易转化为氢氧化镁,则NaOH溶液可使MgCO 较彻底地转化
3
为Mg(OH) ,C正确;D项,处理后 ,则此时
2,氢氧根离子浓度较大,溶液显碱性,D
正确;故选B。
12.向工业废水中加入硫化物可以获得CuS、FeS纳米粒子[已知K (FeS)= 6.3×10-18,K (CuS)=
sp sp
1.3×10-36],下列说法正确的是( )
A.FeS固体不能用于去除工业废水中的Cu2+
B.向FeSO 和CuSO 混合溶液中加入NaS溶液,当两种沉淀共存时,
4 4 2
C.向CuS饱和溶液中加入CuCl 固体,CuS的溶解平衡逆向移动,滤液中一定存在
2
D.已知HS溶液中 ,可判断CuS易溶于稀盐酸
2
【答案】C
【解析】A项,根据K (FeS)>K (CuS)可知,FeS固体能用于去除工业废水中的Cu2+,故A错误;B
sp sp
项,向FeSO 和CuSO 混合溶液中加入NaS溶液,当两种沉淀共存时,
4 4 2
,故B错误;C项,CuS存在溶解平衡CuS(s) Cu2+(aq)
+S2−(aq),向CuS饱和溶液中加入CuCl 固体,铜离子浓度增大,因此CuS的溶解平衡逆向移动,根据溶度
2
积常数得到滤液中一定存在 ,故C正确;D项,若要溶解CuS+2H+= Cu2++H S,则
2
,平衡常数很小,反应几乎不能发生,可判断CuS难
溶于稀盐酸,故D错误。故选C。
题型二 电离常数、水解常数、溶度积常数的综合应用1.(2024·福建卷,7,4分)多卤离子I-、ICl-、IBr -在水溶液中的分解反应及平衡常数值如下:
3 2 2
离子 分解反应 平衡常数值
I-(aq) I-(aq)=I(aq)+I-(aq) 1.4×10-3
3 3 2
ICl-(aq) ICl-(aq)=ICl(aq) +Cl-(aq) 6.0×10-3
2 2
IBr -(aq) IBr -(aq)=IBr(aq) +Br-(aq) K
2 2
下列说法错误的是( )
.
A K<6.0×10-3 B.上述分解反应均为氧化还原反应
C.共价键极性:ICl>IBr D.BrCl-(aq)可分解为BrCl-(aq)和Cl-(aq)
2
【答案】B
【解析】A项,已知电负性Cl>Br,因此氯在化合物中更容易吸引电子,导致I-Cl比I-Br更容易断裂,
所以电离程度ICl->IBr -,K<6.0×10-3,A正确;B项,每个碘离子可以与一个碘分子结合,形成I-,这
2 2 3
个过程中,I-离子能够离解成碘和碘离子,形成平衡反应:I-+I I-,所以溶液中存在I-(aq)
3 2 3 3
I(aq)+I-(aq)的电离平衡,此变化不是氧化还原反应,ICl-、ICl中碘元素是+1价,氯元素是-1价,IBr -和
2 2 2
IBr中,碘元素是+1价,溴元素是-1价;三个变化过程中,各元素化合价都没有改变,不是氧化还原反应,
B错误;C项,同主族元素从上往下,电负性逐渐减小,因此氯的电负性大于溴的电负性,形成共价键的
两元素之间的电负性的差值越大,则键的极性越强,因此共价键极性的大小关系为ICl>IBr,C正确;D
项,已知电负性Cl>Br,因此氯在化合物中更容易吸引电子,导致Cl-Br容易断裂产生为BrCl-(aq)和Cl-
(aq),D正确;故选B。
2.(2024·天津卷,12,3分)甲胺(CHNH )水溶液中存在以下平衡:CHNH +H O CHNH +
3 2 3 2 2 3 3
+OH-。已知:25℃时,CHNH 的K =4.2×10-4,NH ·H O的K =1.8×10-5。下列说法错误的是( )
3 2 b 3 2 b
A.CHNH 的
3 2
B.CHNH 溶液中存在cCHNH ++cH+=cOH-
3 2 3 3
C.25℃时,0.1mol·L-1NH Cl溶液与0.1mol·L-1CHNH Cl溶液相比,NH Cl溶液中的cH+小
4 3 3 4
D.0.01mol·L-1 CHNH 溶液与相同浓度的CHNH Cl溶液以任意比例混合,混合液中存在
3 2 3 3
c(CHNH )+ c(CHNH +)=0.1mol·L-1
3 2 3 3
【答案】C
【解析】A项,由(CHNH )的电离方程式可知,CHNH 的 ,A正确;B
3 2 3 2项,由CHNH 的电离方程式及电荷守恒可知,CHNH 溶液中存在cCHNH ++cH+=cOH-,B正确;
3 2 3 2 3 3
C项,由CHNH 的K =4.2×10-4,NH ·H O的K =1.8×10-5,碱性CHNH >NH ·H O,由越弱越水解可得,
3 2 b 3 2 b 3 2 3 2
25℃时,0.1mol·L-1NH Cl溶液与0.1mol·L-1CHNH Cl溶液相比,NH Cl溶液中的cH+大,C错误;D项,
4 3 3 4
0.01mol·L-1 CHNH 溶液与相同浓度的CHNH Cl溶液以任意比例混合,由物料守恒得,混合液中存在
3 2 3 3
c(CHNH )+ c(CHNH +)=0.1mol·L-1,D正确;故选C。
3 2 3 3
3.(2024·浙江1月卷,15,3分)常温下、将等体积、浓度均为0.40mol·L-1 BaCl 溶液与新制HSO 溶
2 2 3
液混合,出现白色浑浊;再滴加过量的HO 溶液,振荡,出现白色沉淀。
2 2
已知:HSO K =1.4×10-2,K =6.0×10-8
2 3 a1 a2
K (BaSO)=5.0×10-10,K (BaSO)=1.1×10-10,
sp 3 sp 4
下列说法不正确的是( )
A. HSO 溶液中存在c(H+)>c(HSO -)>c(SO 2-)>c(OH-)
2 3 3 3
B.将0.40mol·L-1 HSO 溶液稀释到0.20mol·L-1,c(SO 2-)几乎不变
2 3 3
C.BaCl 溶液与HSO 溶液混合后出现的白色浑浊不含有BaSO
2 2 3 3
D.存在反应BaSO+ HSO +H O= BaSO↓+2H++H O是出现白色沉淀的主要原因
3 2 3 2 2 4 2
【答案】C
【解析】A项,亚硫酸是二元弱酸,存在二次电离,电离方程式为:HSO H++HSO -,HSO -
2 3 3 3
H++SO 2-,则溶液中c(H+)>c(HSO -)>c(SO 2-)>c(OH-),A正确;B项,亚硫酸根离子是其二级电
3 3 3
离产生的,则稀释的时候对氢离子的影响较大,稀释的时候,亚硫酸的浓度变为原来的一半,另外稀释的
平衡常数不变,对第二级电离影响很小,则稀释时亚硫酸根浓度基本不变,B正确;C项,加入双氧水之
前,生成的白色浑浊为BaSO 沉淀,C错误;D项,过氧化氢具有强氧化性,可以将+4价硫氧化为+6价硫
3
酸根离子,则存在反应,BaSO+H O= BaSO↓+H O,则出现白色沉淀的主要原因生成BaSO 沉淀,D正确;
3 2 2 4 2 4
故选C。
4.(2024·安徽卷,7,3分)地球上的生物氮循环涉及多种含氮物质,转化关系之一如下图所示(X、Y
均为氮氧化物),羟胺(NH OH)以中间产物的形式参与循环。常温常压下,羟胺易潮解,水溶液呈碱性,与
2
盐酸反应的产物盐酸羟胺([NH OH]Cl)广泛用子药品、香料等的合成。
3
已知25℃时,K(HNO)=7.2×10-4,K(NH ·H O)=1.8×10-5 ,K(NH OH)=8.7×10-9。
a 2 b 3 2 b 2下列有关物质结构或性质的比较中,正确的是( )
A.键角:NH >NO -
3 3
B.熔点: NH OH>[NH OH]Cl
2 3
C. 同浓度水溶液的pH:[NH OH]Cl>NH Cl
3 4
D.羟胺分子间氢键的强弱:
【答案】D
【解析】A项,NH 中N原子的价层电子对数= ,为sp3杂化,键角为107°,
3
NO -中N的价层电子对数= ,为sp2杂化,键角为120°,故键角:NH <NO -,A
3 3 3
错误;B项,NH OH为分子晶体,[NH OH]Cl为离子晶体,故熔点:NH OH<[NH OH]Cl,B错误;C项,
2 3 2 3
由题目信息可知,25℃下,K(NH ·H O)>K(NH OH),故NH OH的碱性比NH ·H O弱,故同浓度的水溶
b 3 2 b 2 2 3 2
液中,[NH OH]+的电离程度大于NH +的电离程度,同浓度水溶液的pH:[NH OH]Cl<NH Cl,C错误;D
3 4 3 4
项,O的电负性大于N,O-H键的极性大于N-H键,故羟胺分子间氢键的强弱 ,D
正确;故选D。
5.(2023•浙江省6月选考,15,3分)草酸(HC O)是二元弱酸。某小组做如下两组实验:
2 2 4
实验I:往20mL0.1mol·L-1NaHC O 溶液中滴加0.1mol·L-1NaOH溶液。
2 4
实验Ⅱ:往20mL0.1mol·L-1NaHC O 溶液中滴加0.1mol·L-1 CaCl 溶液。
2 4 2
[已知:HC O 的电离常数K =5.4×10-2,K =5.4×10-5,K (CaC O)= 2.4×10-9,溶液混合后体积变化忽
2 2 4 a1 a2 sp 2 4
略不计],下列说法正确的是
A.实验I可选用甲基橙作指示剂,指示反应终点
B.实验I中V(NaOH)=10mL时,存在c(C O2-)<c(HC O-)
2 4 2 4C.实验Ⅱ中发生反应Ca2++ HC O- =CaC O↓+H+
2 4 2 4
D.实验Ⅱ中V(CaCl)=80mL时,溶液中c(C O2-)=4.0×10-8mol·L-1
2 2 4
【答案】D
【解析】A项,NaHC O 溶液被氢氧化钠溶液滴定到终点时生成显碱性的草酸钠溶液,为了减小实验
2 4
误差要选用变色范围在碱性范围的指示剂,因此,实验I可选用酚酞作指示剂,指示反应终点,故A错误;
B项,实验I中V(NaOH)=10mL时,溶质是NaHC O、NaC O 且两者物质的量浓度相等,
2 4 2 2 4
,,则草酸氢根的电离程度大于草酸根的水解程度,因此存在c(C O2-)>
2 4
c(HC O-),故B错误;C项,实验Ⅱ中,由于开始滴加的氯化钙量较少而NaHC O 过量,因此该反应在初
2 4 2 4
始阶段发生的是Ca2++ 2HC O- =CaC O↓+H C O,该反应的平衡常数为
2 4 2 4 2 2 4
,因为平衡常数很大,说明反应能够完全进行,
当NaHC O 完全消耗后,HC O 再和CaCl 发生反应,故C错误;D项,实验Ⅱ中V(CaCl)=80mL时,溶
2 4 2 2 4 2 2
液中的钙离子浓度为 ,溶液中
,故D正确。故选D。
6.(2024·江苏卷,16,15分)贵金属银应用广泛。Ag与稀HNO 制得AgNO,常用于循环处理高氯废
3 3
水。
(1)沉淀Cl-。在高氯水样中加入KCrO 使CrO2-浓度约为5×10-3mol·L-1,当滴加AgNO 溶液至开始产生
2 4 4 3
Ag CrO 沉淀(忽略滴加过程的体积增加),此时溶液中Cl-浓度约为_______ mol·L-1。[已知:K (AgCl)=
2 4 sp
1.8×10-10,K (Ag CrO)= 2.0×10-12]
sp 2 4
(2)还原AgCl。在AgCl沉淀中埋入铁圈并压实,加入足量0.5mol·L-1盐酸后静置,充分反应得到Ag。
①铁将AgCl转化为单质Ag的化学方程式为_______。
②不与铁圈直接接触的AgCl也能转化为Ag的原因是_______。
③为判断AgCl是否完全转化,补充完整实验方案:取出铁圈,搅拌均匀,取少量混合物过滤,_______[实验中必须使用的试剂和设备:稀HNO、AgNO 溶液,通风设备]
3 3
(3)Ag的抗菌性能。纳米Ag表面能产生Ag+杀死细菌(如图所示),其抗菌性能受溶解氧浓度影响。
①纳米Ag溶解产生Ag+的离子方程式为_______。
②实验表明溶解氧浓度过高,纳米Ag的抗菌性能下降,主要原因是_______。
【答案】(1) 9×10-6
(2)①Fe+AgCl+2HCl= FeCl+Ag+H↑ ②形成了以Fe为负极,AgCl为正极,盐酸为电解质溶液的原
3 2
电池,正极AgCl得到电子,电极反应式为AgCl+ e-=Ag+Cl-,生成Ag ③洗涤,向最后一次洗涤液中
滴加硝酸银溶液,确保氯离子洗净,开启通风设备,向滤渣中加入足量稀 HNO ,搅拌,若固体完全溶解,
3
则AgCl完全转化,若固体未完全溶解,则AgCl未完全转化
(3)①4Ag+O+4H+=4Ag++2H O ②纳米Ag与氧气生成Ag O,使得Ag+浓度下降
2 2 2
【解析】(1) CrO 2-浓度约为 5×10-3mol·L-1,当滴加 AgNO 溶液至开始产生 Ag CrO 沉淀,此时
4 3 2 4
,
(2)①在足量0.5mol·L-1盐酸中静置,铁将AgCl转化为单质Ag,反应的化学方程式为:Fe+AgCl+2HCl=
FeCl+Ag+H↑;②不与铁圈直接接触的AgCl也能转化为Ag,是因为形成了以Fe为负极,AgCl为正极,
3 2
盐酸为电解质溶液的原电池,正极 AgCl得到电子,电极反应式为 AgCl+ e-=Ag+Cl-,生成Ag;③判断
AgCl是否完全转化,即检验混合物中是否含有AgCl,若AgCl完全转化,则剩余固体全部为银,可完全溶
于稀硝酸,若AgCl未完全转化,剩余AgCl不能溶于稀硝酸,则可用稀硝酸检验,稀硝酸参与反应可能会
产生氮氧化物,反应需在通风设备中进行,反应后的溶液中存在氯离子,若未将滤渣洗净,氯离子会干扰
实验,所以首先需要检验氯离子是否洗净,实验方案为:取出铁圈,搅拌均匀,取少量混合物过滤,洗涤,
向最后一次洗涤液中滴加AgNO 溶液,确保氯离子洗净,打开通风设备,向洗涤干净的滤渣中加入足量稀
3
HNO ,搅拌,若固体完全溶解,则AgCl完全转化,若固体未完全溶解,则AgCl未完全转化;(3)①纳米
3
Ag溶解时被氧化为Ag+,离子方程式为:4Ag+O+4H+=4Ag++2H O;②溶解氧浓度过高,纳米Ag与氧气
2 2
生成Ag O,使得Ag+浓度下降,抗菌性能下降。
21 .电离常数的 4 大应用
电离常数越大,酸性(或碱性)越强。如:常温下,CHCOOH的K=1.
3 a
判断弱酸(或弱 8×10-5,HCO 的K =4.3×10-7、K =5.6×10-11。
2 3 a1 a2
碱)的相对强弱
则酸性:CHCOOH>H CO>HCO
3 2 3
电离常数越大,对应的盐水解程度越小,碱性(或酸性)越弱。如:利用
判断盐溶液的酸
上面电离常数的数值可知等浓度的CHCOONa、NaHCO 、NaCO 溶液
性(或碱性)强弱 3 3 2 3
的pH由大到小的顺序为NaCO>NaHCO>CH COONa
2 3 3 3
一般符合“强酸制弱酸”规律。如:利用上面中电离常数的数值可知,
判断复分解反应
向NaCO 溶液中加入足量CHCOOH的离子方程式为CO+
能否发生 2 3 3
2CHCOOH===2CH COO-+HO+CO↑
3 3 2 2
弱电解质加水稀释时,能促进弱电解质的电离,溶液中离子和分子的浓
判断微粒浓度比 度会发生相应的变化,但电离常数不变,题目中经常利用电离常数来判
值的变化 断溶液中微粒浓度比值的变化情况。如把0.1 mol·L-1 CHCOOH溶液加
3
水稀释,==稀释时,c(H+)减小,K 值不变,则变大
a
2 . K 、 K 、 K 、 K 、 K 之间的关系
w a b sp h
(1)一元弱酸强碱盐:K =K /K;
h w a
(2)一元弱碱强酸盐:K =K /K ;
h w b
(3)多元弱碱强酸盐,如氯化铁:Fe3+(aq)+3HO(l) Fe(OH) (s)+3H+(aq),K =c3(H+)/c(Fe3+)。
2 3 h
将(K )3=c3(H+)×c3(OH-)与K =c(Fe3+)×c3(OH-)两式相除,消去c3(OH-)可得K =(K )3/K 。
w sp h w sp
(4)M(OH) 悬浊液中K 、K 、pH间关系,M(OH) (s) Mn+(aq)+nOH-(aq),K =c(Mn+)·cn(OH
n sp w n sp
-)=·cn(OH-)==()n+1。
3 . 电离常数与水解常数的关系
(1)对于一元弱酸HA,K 与K 的关系
a h
c(H+)·c(A-)
HA H++A-,K(HA)= ;
a c(HA)
c(OH-)·c(HA)
A-+H O HA+OH-,K (A-)= 。
2 h c(A-)
K 1.0×10-14
w
则K·K =c(H+)·c(OH-)=K ,故K = 。常温时K·K =K =1.0×10-14,K = 。
a h w h K a h w h K
a a
(2)对于二元弱酸HB,K (H B)、K (H B)与K (HB-)、K (B2-)的关系
2 a1 2 a2 2 h h
c(OH-)·c(H B) c(H+)·c(OH-)·c(H B) K
HB-+H O HB+OH-,K (HB-)= 2 = 2 = w
2 2 h c(HB-) c(H+)·c(HB-) K
a1
;
c(OH-)·c(HB-) c(H+)·c(OH-)·c(HB-) K
w
B2-+H O HB-+OH-,K (B2-)= = = 。
2 h c(B2-) c(H+)·c(B2-) K
a21.室温下,用过量0.5mol·L-1NaCO 溶液浸泡CaSO 粉末,一段时间后过滤,向滤渣中加稀醋酸,产
2 3 4
生气泡。(当溶液中剩余的离子浓度小于 时,化学上通常认为生成沉淀的反应已经完全进行了。
已知:K (CaSO)=5.0×10-5,K (CaCO)=3.0×10-9),下列说法正确的是( )
sp 4 sp 3
A.浸泡后CaSO 未完全转化为CaCO
4 3
B.0.5mol·L-1NaCO 溶液中存在:c(OH―)=c(H+)+c(HCO ―)+c(H CO)
2 3 3 2 3
C.反应CaSO+CO 2- CaCO +SO2-正向进行,需满足
4 3 3 4
D.过滤后所得清液中一定存在: 且
【答案】D
【 解 析 】 A 项 , 用 过 量 0.5mol·L-1NaCO 溶 液 浸 泡 CaSO 粉 末 , 则 浸 泡 后
2 3 4
,可以认为浸泡后 CaSO 完全转化为
4
CaCO ,A 错误; B 项,由质子守恒可知,0.5mol·L-1NaCO 溶液中存在:c(OH―)=c(H+)+c(HCO ―)
3 2 3 3
+2c(H CO),B错误;C项,CaSO+CO 2- CaCO +SO2-的 ,反应正
2 3 4 3 3 4
向进行,需满足 ,C 错误;D 项,过滤后所得清液为碳酸钙的饱和溶液,存在:
,且由于碳酸根离子浓度较大导致钙离子浓度很小,故存在 ,
D正确;故选D。
2.[新考法]印尼苏拉威西岛特产的椰子蟹具有异常坚硬的甲壳,这归功于摄入的椰子中的月桂酸
(C H COOH),在表面的角质层中形成难溶的月桂酸磷酸钙,存在如下平衡:Ca PO (OOCC H )(s)
11 23 3 4 11 23 33Ca2+(aq)+PO (aq)+3C H COO-(aq) K =7.3×10-35,已知CaCO 的K =2.8×10-9。下列说法不正确
11 23 sp 3 sp
的是( )
A.椰子蟹摄入月桂酸含量较高的椰肉有助于形成更加坚硬的甲壳
B.弱碱性的海水可以保护椰子蟹外壳,使其不易被腐蚀
C.将少量月桂酸磷酸钙投入适量1mol•L-1碳酸钠溶液中,可实现其与碳酸钙的转化
D.海水中CO 浓度升高,会腐蚀椰子蟹的外壳,使K 增大
2 sp
【答案】D
【解析】A项,由题干可知,月桂酸利于促进形成难溶的月桂酸磷酸钙,故椰子蟹摄入月桂酸含量较
高的椰肉有助于形成更加坚硬的甲壳,A正确;B项,弱碱性的海水利于月桂酸形成月桂酸根离子,使得
Ca PO (OOCC H )(s) 3Ca2+(aq)+PO3-(aq)+3C H COO-(aq)平衡逆向移动,利于保护椰子蟹外壳,
3 4 11 23 3 4 11 23
使其不易被腐蚀,B正确;C项,将少量月桂酸磷酸钙投入适量1mol•L-1碳酸钠溶液中,较高浓度的碳酸
根离子使得Ca PO (OOCC H )(s)转化为CaCO (s),实现其与碳酸钙的转化,C正确;D项,海水中CO
3 4 11 23 3 3 2
浓度升高,溶液酸性增强,使得月桂酸根离子转化为月桂酸,促使 Ca PO (OOCC H )(s) 3Ca2+(aq)
3 4 11 23 3
+PO3-(aq)+3C H COO-(aq)平衡正向移动,导致腐蚀椰子蟹的外壳,但不会使 K 增大,D错误;故选
4 11 23 sp
D。
3.常温下,向20mL0.1mol/LNaHCO 溶液中再加入少量的NaHCO 固体,一段时间后,少量气体X
3 3
从溶液底部固体中缓慢逸出,最终固体全部溶解,得到溶液Y,pH值为8.7。
已知:K (CaCO)=4.96×10-9 K (MgCO )=6.82×10-6,K [Mg(OH) ]=1.8×10-11
sp 3 sp 3 sp 2
HCO:pK =6.3、pK =10.3;Mg(OH) 沉淀范围:pH9.4~12.4。
2 3 a1 a2 2
下列说法正确的是( )
A.X气体是CO,饱和NaHCO 溶液的
2 3
B.因为K (MgCO )>K [Mg(OH) ],Mg(OH) 更难溶
sp 3 sp 2 2
C.向溶液Y中滴加MgCl 溶液,有Mg(OH) 生成
2 2
D.向0.1mol/L NaHCO 溶液中加入MgCl 溶液,无明显现象,但改为同浓度的CaCl 溶液,可生成沉
3 2 2
淀。
【答案】D
【解析】A项,在NaHCO 溶液中既存在水解平衡HCO -+H O⇌HCO+OH-、又存在电离平衡HCO -
3 3 2 2 3 3
⇌ H++ CO 2-,HCO -的水解平衡常数K = = =10-7.7>10-10.3,NaHCO 溶液呈碱性,向其中加入少
3 3 h 3
量NaHCO 固体,上述平衡正向移动,生成的 HCO 分解产生少量气体CO ,即X气体是CO ,同时有
3 2 3 2 2
CO2-生成,即溶液Y中含CO2-,由HCO 的K 、K 可知CO2-的水解能力大于HCO -,溶液Y的pH为
3 3 2 3 a1 a2 3 38.7,则饱和NaHCO 溶液的pH<8.7,A项错误;B项,MgCO 、Mg(OH) 不属于同类型的难溶电解质,
3 3 2
不能直接由 K 的大小判断溶解度的大小,K (MgCO )=6.82×10-6,饱和 MgCO 溶液的浓度 c(MgCO )=
sp sp 3 3 3
= mol/L= ×10-3mol/L,K [Mg(OH) ]=1.8×10-11,饱和 Mg(OH) 溶液的浓度
sp 2 2
c[Mg(OH) ]= = mol/L= ×10-4mol/L< ×10-3mol/L,Mg(OH) 更难溶,B
2 2
项错误;C项,Mg(OH) 沉淀的范围:pH9.4~12.4,即pH=9.4时Mg2+开始形成Mg(OH) 沉淀,Y溶液的
2 2
pH为8.7,故向溶液Y中滴加MgCl 溶液,没有Mg(OH) 生成,C项错误;D项,NaHCO 溶液中存在平
2 2 3
衡HCO - H++ CO 2-,由于K (CaCO) <K (MgCO ),说明Ca2+结合CO2-的能力比 Mg2+强,故向
3 3 sp 3 sp 3 3
0.1mol/LNaHCO 溶液中加入MgCl 溶液,无明显现象,但改为同浓度的CaCl 溶液,可生成沉淀,D项正
3 2 2
确;故选D。
4.(2025·浙江部分高中高三开学考试)硫化氢(H S)是二元弱酸。某小组做如下两组实验:
2
实验Ⅰ:往20mL 0.10mol·L-1NaHS溶液中滴加0.10mol·L-1NaOH溶液;
实验Ⅱ:往20mL 0.10mol·L-1NaHS溶液中滴加0.10mol·L-1 AgNO 溶液。
3
[已知:HS的电离平衡常数K =1.1×10-7,K =1.3×10-13,K (Ag S)=6.3×10-50;Ag++2NH
2 a1 a2 sp 2 3
[Ag(NH )]+ ,K=1.0×10-7.23,溶液混合后体积变化忽略不计]。
3 2
下列说法正确的是( )
A.实验I可选用甲基橙(变色的 范围 )作指示剂,指示反应终点
B.实验I中V(NaOH)=10mL时,存在c(Na+)>c(HS−)>c(S2−)
C.实验Ⅱ中发生的主要反应为2Ag++HS-=Ag S↓+H+
2
D.往实验Ⅱ反应产生的黑色沉淀中加入0.10mol·L-1氨水,黑色沉淀溶解,产生0.10mol·L-1
【答案】B
【解析】A项,实验I终点时为NaS溶液,为碱性,选用酚酞溶液做指示剂,A项错误;B项,实验I
2
中V(NaOH)=10mL时,为NaHS与NaS物质的量比1:1的混合溶液,HS-的电离平衡常数为1.3×10−13,
2
S2−水解平衡常数为 ,故HS-的电离程度小于S2−水解能力,存在
c(Na+)>c(HS−)>c(S2−),B项正确;C项,实验Ⅱ中发生的主要反应为2Ag++2HS-=Ag S↓+H S,C项错误;D
2 2
项,实验Ⅱ中存在Ag S(s) 2Ag+(aq)+ S2-(aq),故2c(Ag+)=c(S2−),K (Ag S)=
2 sp 2
6.3×10−50,c(Ag+)= ,Ag++2NH
3[Ag(NH )]+,K= 1.0×107.23,c[Ag(NH )+]=
3 2 3 2
,故Ag S不会溶解生成[Ag(NH )]+,D项错误;故选B。
2 3 2
5.(1)25 ℃时,HSO HSO+H+的电离常数K=1×10-2 mol·L-1,则该温度下NaHSO 水解反
2 3 a 3
应的平衡常数K =________ mol·L-1,若向NaHSO 溶液中加入少量的I,则溶液中 将
h 3 2
________(填“增大”、“减小”或“不变”)。
(2)已知25 ℃时,NH ·H O的电离平衡常数K =1.8×10-5 mol·L-1,该温度下1 mol·L-1的NH Cl溶液
3 2 b 4
中c(H+)=________ mol·L-1。(已知≈2.36)
(3)常温下,用NaOH溶液吸收SO 得到pH=9的NaSO 溶液,吸收过程中水的电离平衡________移
2 2 3
动(填“向左”、“向右”或“不”)。试计算溶液中 =________。(常温下HSO 的电离平衡常数
2 3
Ka=1.0×10-2,Ka=6.0×10-8)
1 2
【答案】(1)1×10-12 增大 (2)2.36×10-5 (3)向右 60
【解析】(1) , ==1×10-12
mol·L-1。HSO+HO HSO +OH-,当加入少量I 时,发生I+HSO+HO===2I-+3H++SO。根据
2 2 3 2 2 2
,由于c(OH-)减小,而K 不变,所以 增大。(2) =,
h
c(H+)≈c(NH ·H O),而c(NH)≈1 mol·L-1,所以c(H+)==≈2.36×10-5 mol·L-1。(3)NaOH电离出的OH-抑
3 2
制水的电离平衡,NaSO 电离出的 SO 水解促进水的电离平衡。SO+HO HSO+OH-,
2 3 2
==,所以 ==60。
6.[新题型](2025·浙江省新阵地教育联盟高三第一次联考,节选)已知溶洞的形成与下列反应有关:
①Ca2++2HCO- CaCO + H CO
3 3 2 3
②HCO HO+CO↑
2 3 2 2
(1)反应①的平衡常数为 。(用K 、K 、K (CaCO)表示)
a1 a2 sp 3
(2)以下能判断反应①达到平衡状态的是___________。
A.CO 气体压强保持不变 B.溶液的pH保持不变
2
C. 不变 D.v (H CO):v (HCO -)=2:1
正 2 3 逆 3
(3)当溶有碳酸氢钙的水从溶洞顶滴到洞底时渐渐形成了钟乳石,请解释可能的原因 。
(4)已知HCO 的K (H CO)=4.2×10-7,K (H CO)=5.6×10-11,K (CaCO)= 2.8×10-9,c(H+)=8.4×10-
2 3 a1 2 3 a2 2 3 sp 39mol·L-1 ,c(HCO -)=1×10-4mol·L-1,c(H CO)为 。当c(Ca2+)= mol·L-1¹时,开始产生
3 2 3
CaCO 沉淀。
3
【答案】(1) (2)AB
(3)由于水分的蒸发或压强减少,以及温度的变化上升都会使二氧化碳溶解度减小,使平衡②正移,导
致c(H CO)减少,使平衡①也正移而析出碳酸钙沉淀
2 3
(4) 2×10-6mol/L 4.2×10-3
【解析】(1)碳酸的一级电离为:HCO H++HCO-,二级电离为:HCO - H++CO 2-,
2 3 3 3 3
, ,且 K (CaCO)= c(Ca2+)·c(CO2-),反应①的平衡常数:
sp 3 3
, 根 据 以 上 三 个 平 衡 常 数 表 达 式 , 可 得 :
;(2)A项,碳酸分解产生二氧化
碳气体,CO 气体压强保持不变,说明CO 浓度不变,可进一步溶液中HCO 浓度不变,可以说明反应①
2 2 2 3
达到平衡状态,A符合题意;B项,溶液的pH保持不变,说明碳酸的电离已经达到平衡,即溶液中HCO
2 3
浓度不变,说明反应①达到平衡状态,B 符合题意;C 项,因 ,当
不变时,仅能说明CO2-的水解达到平衡,不能说明反应①达到平衡状态,C不符合题意;D
3
项,根据反应①,物质的反应速率之比等于其计量系数之比,则当v (H CO):v (HCO -)=1:2时,能说
正 2 3 逆 3
明反应①达到平衡状态,D不符合题意;故选AB。(3)当溶有碳酸氢钙的水从溶洞顶滴到洞底时渐渐形成
了钟乳石,可能的原因为:由于水分蒸发或压强减少,或温度的上升都会使二氧化碳溶解度减小,使平衡
②正移,导致 c(H CO)减少,使平衡①也正移而析出碳酸钙沉淀;(4)当 c(H+)=8.4×10-9mol·L-1,
2 3
c(HCO -)=1×10-4mol·L-1 , 则 ;
3, 当
时开始产生CaCO 沉淀,解得 。
3
题型三 中和滴定及其拓展应用
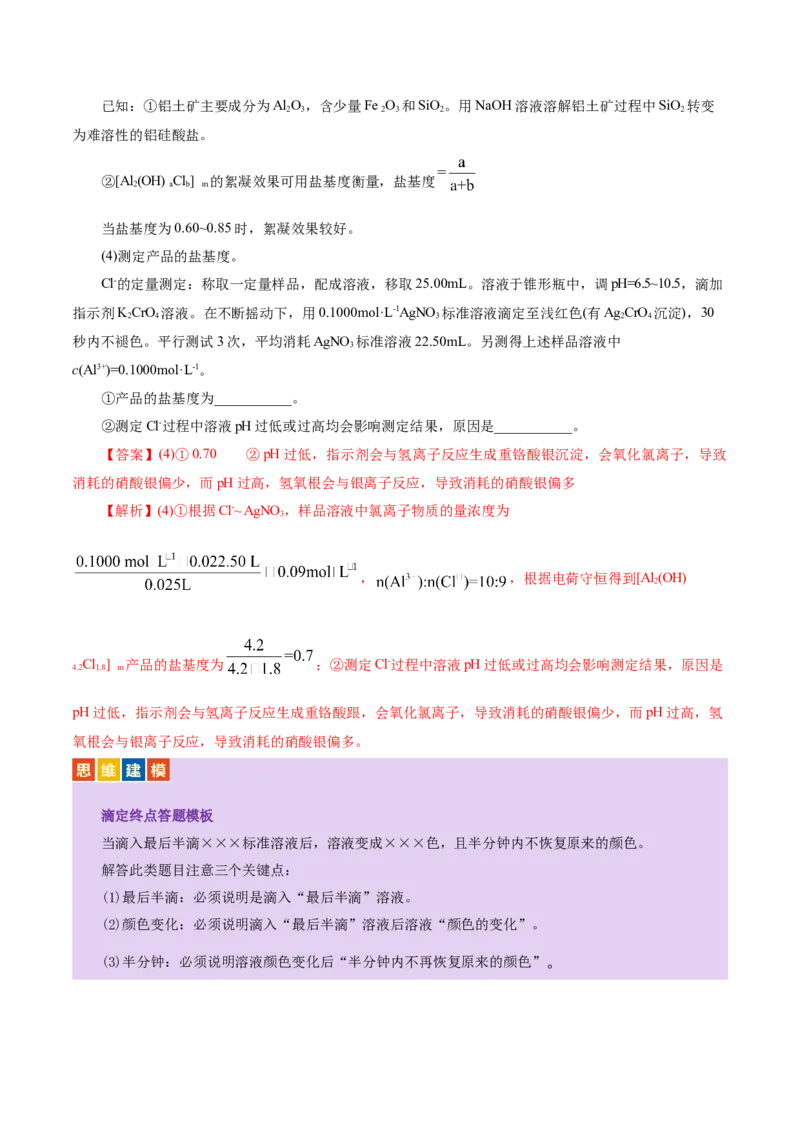
1.(2023•湖南卷,12,3分))常温下,用浓度为0.0200mol·L-1的NaOH标准溶液滴定浓度均为
0.0200mol·L-1的HCl和CHCOOH的混合溶液,滴定过程中溶液的 随 ( )的变化曲线如图所
3
示。下列说法错误的是( )
A.K(CHCOOH)约为10-4.76
a 3
B.点a:c(Na+)=c(Cl-)=c(CH COOH)+c(CH COO-)
3 3
C.点b:c(CHCOOH)d,故D错误;故选D。
2 . (2023• 山 东 卷 , 8 , 3 分 ) 一 定 条 件 下 , 乙 酸 酐 [(CH CO) O] 醇 解 反 应
3 2
[(CH CO) O+ROH→CH COOR+CH COOH]可进行完全,利用此反应定量测定有机醇(ROH)中的羟基含量,
3 2 3 3
实验过程中酯的水解可忽略。实验步骤如下:
①配制一定浓度的乙酸酐-苯溶液。
②量取一定体积乙酸酐-苯溶液置于锥形瓶中,加入 样品,充分反应后,加适量水使剩余乙酸
酐完全水解:(CHCO) O+HO→2CH COOH。
3 2 2 3
③加指示剂并用cmol·L-1NaOH-甲醇标准溶液滴定至终点,消耗标准溶液VmL。
1
④在相同条件下,量取相同体积的乙酸酐-苯溶液,只加适量水使乙酸酐完全水解;加指示剂并用
cmol·L-1NaOH-甲醇标准溶液滴定至终点,消耗标准溶液VmL。
2
对于上述实验,下列做法正确的是( )
A.进行容量瓶检漏时,倒置一次即可
B.滴入半滴标准溶液,锥形瓶中溶液变色,即可判定达滴定终点
C.滴定读数时,应单手持滴定管上端并保持其自然垂直
D.滴定读数时,应双手一上一下持滴定管
【答案】C
【解析】A项,进行容量瓶检漏时,倒置一次,然后玻璃塞旋转180度后再倒置一次,故A错误;B
项,滴入半滴标准溶液,锥形瓶中溶液变色,且半分钟内不变回原色,才是达到滴定终点,故B错误;C
项,滴定读数时,应单手持滴定管上端无刻度处,并保持其自然垂直,故C正确;D项,滴定读数时,应
单手持滴定管上端无刻度处,并保持其自然垂直,故D错误;故选C。
3.(2023•湖北省选择性考试,18)学习小组探究了铜的氧化过程及铜的氧化物的组成。回答下列问题:
(1)铜与浓硝酸反应的装置如下图,仪器A的名称为_______,装置B的作用为_______。(2)铜与过量HO 反应的探究如下:
2 2
实验②中
Cu溶解的离子方程式为_______;产生的气体为_______。比较实验①和②,从氧化还原角度说明 的作
用是_______。
(3)用足量NaOH处理实验②新制的溶液得到沉淀X,元素分析表明X为铜的氧化物,提纯干燥后的X
在惰性氛围下加热,mgX完全分解为ng黑色氧化物Y, 。X的化学式为_______。
(4)取含X粗品0.0500g(杂质不参加反应)与过量的酸性KI完全反应后,调节溶液至弱酸性。以淀粉为
指示剂,用0.1000mol·L-1 Na SO 标准溶液滴定,滴定终点时消耗NaSO 标准溶液15.00mL。(已知:
2 2 3 2 2 3
2Cu2++4I-=2CuI↓+I ,I+2S O2-=2I-+S O2-)标志滴定终点的现象是_______,粗品中X的相对含量为_______。
2 2 2 3 4 6
【答案】(1)①具支试管 ②防倒吸
(2)①Cu+H O+2H+= Cu2++2H O ②O ③既不是氧化剂,又不是还原剂
2 2 2 2
(3)CuO (4)①溶液蓝色消失,且半分钟不恢复原来的颜色 ② 72%
2
【解析】(1)由图可知,仪器A的名称为具支试管;铜和浓硝酸反应生成硝酸铜和二氧化氮,其中二氧
化氮易溶于水,需要防倒吸,则装置B的作用为防倒吸;(2)根据实验现象,铜片溶解,溶液变蓝,可知在
酸性条件下铜和过氧化氢发生反应,生成硫酸铜,离子方程式为:Cu+H O+2H+= Cu2++2H O;硫酸铜可以
2 2 2
催化过氧化氢分解生成氧气,则产生的气体为O ;在铜和过氧化氢的反应过程中,氢元素的化合价没有发
2
生变化,故从氧化还原角度说明 H+的作用是:既不是氧化剂,又不是还原剂;(3)在该反应中铜的质量
m(Cu)=n× ,因为 ,则m(O)= ,则X的化学式中铜原子和氧原子的物质的量之比为: ,则X为CuO ;(4)滴定结束的时候,单质碘消耗完,则标志滴定终
2
点的现象是:溶液蓝色消失,且半分钟不恢复原来的颜色;在CuO 中铜为+2价,氧为-1价,根据2Cu2+
2
+4I-=2CuI↓+I ,I+2S O2-=2I-+S O2-,可以得到关系式: CuO~2I ~4S O2-,则 n(CuO)= ×0.1mol/
2 2 2 3 4 6 2 2 2 3 2
L×0.015L=0.000375mol,粗品中X的相对含量为 。
4.(2023•浙江省6月选考,20节选)测定产品的盐基度。Cl-的定量测定:称取一定量样品,配成溶液,
移取 25.00mL。溶液于锥形瓶中,调 pH=6.5~10.5,滴加指示剂 KCrO 溶液。在不断摇动下,用
2 4
0.1000mol·L-1AgNO 标准溶液滴定至浅红色(有AgCrO 沉淀),30秒内不褪色。平行测试3次,平均消耗
3 2 4
AgNO 标准溶液22.50mL。另测得上述样品溶液中c(Al3+)=0.1000mol·L-1。
3
①产品的盐基度为___________。
②测定Cl-过程中溶液pH过低或过高均会影响测定结果,原因是___________。
【答案】①0.70 ②pH过低,指示剂会与氢离子反应生成重铬酸银沉淀,会氧化氯离子,导致消
耗的硝酸银偏少,而pH过高,氢氧根会与银离子反应,导致消耗的硝酸银偏多
【 解 析 】 ① 根 据 Cl-~ AgNO , 样 品 溶 液 中 氯 离 子 物 质 的 量 浓 度 为
3
, , 根 据 电 荷 守 恒 得 到 [Al (OH)
2
Cl ] 产品的盐基度为 ;②测定Cl-过程中溶液pH过低或过高均会影响测定结果,原因是
4.2 1.8 m
pH过低,指示剂会与氢离子反应生成重铬酸跟,会氧化氯离子,导致消耗的硝酸银偏少,而 pH过高,氢
氧根会与银离子反应,导致消耗的硝酸银偏多。
5.(2023•浙江省6月选考,20,10分))某研究小组用铝土矿为原料制备絮凝剂聚合氯化铝([Al (OH)
2
Cl] ,a=1~5)按如下流程开展实验。
a b m已知:①铝土矿主要成分为Al O,含少量Fe O 和SiO。用NaOH溶液溶解铝土矿过程中SiO 转变
2 3 2 3 2 2
为难溶性的铝硅酸盐。
②[Al (OH) Cl] 的絮凝效果可用盐基度衡量,盐基度
2 a b m
当盐基度为0.60~0.85时,絮凝效果较好。
(4)测定产品的盐基度。
Cl-的定量测定:称取一定量样品,配成溶液,移取25.00mL。溶液于锥形瓶中,调pH=6.5~10.5,滴加
指示剂KCrO 溶液。在不断摇动下,用0.1000mol·L-1AgNO 标准溶液滴定至浅红色(有AgCrO 沉淀),30
2 4 3 2 4
秒内不褪色。平行测试3次,平均消耗AgNO 标准溶液22.50mL。另测得上述样品溶液中
3
c(Al3+)=0.1000mol·L-1。
①产品的盐基度为___________。
②测定Cl-过程中溶液pH过低或过高均会影响测定结果,原因是___________。
【答案】(4)①0.70 ②pH过低,指示剂会与氢离子反应生成重铬酸银沉淀,会氧化氯离子,导致
消耗的硝酸银偏少,而pH过高,氢氧根会与银离子反应,导致消耗的硝酸银偏多
【解析】(4)①根据Cl-~ AgNO ,样品溶液中氯离子物质的量浓度为
3
, ,根据电荷守恒得到[Al (OH)
2
Cl ] 产品的盐基度为 ;②测定Cl-过程中溶液pH过低或过高均会影响测定结果,原因是
4.2 1.8 m
pH过低,指示剂会与氢离子反应生成重铬酸跟,会氧化氯离子,导致消耗的硝酸银偏少,而pH过高,氢
氧根会与银离子反应,导致消耗的硝酸银偏多。
滴定终点答题模板
当滴入最后半滴×××标准溶液后,溶液变成×××色,且半分钟内不恢复原来的颜色。
解答此类题目注意三个关键点:
(1)最后半滴:必须说明是滴入“最后半滴”溶液。
(2)颜色变化:必须说明滴入“最后半滴”溶液后溶液“颜色的变化”。
(3)半分钟:必须说明溶液颜色变化后“半分钟内不再恢复原来的颜色”。1 . 中和滴定
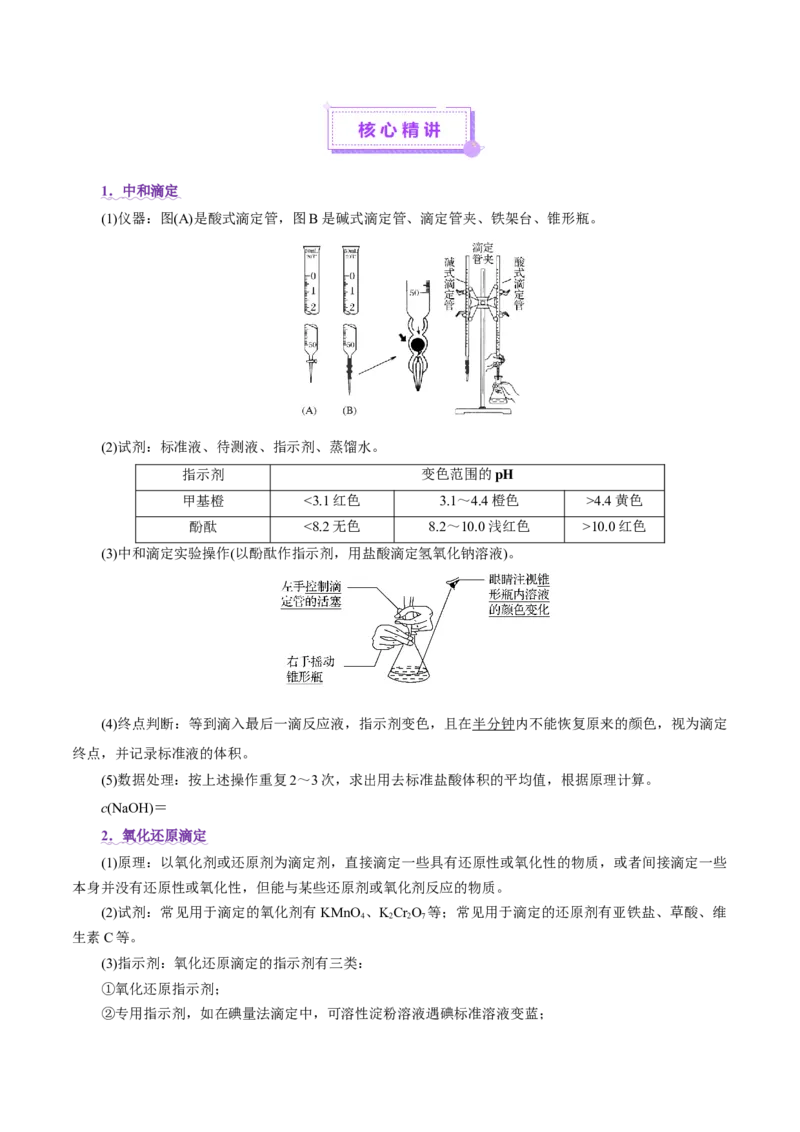
(1)仪器:图(A)是酸式滴定管,图B是碱式滴定管、滴定管夹、铁架台、锥形瓶。
(2)试剂:标准液、待测液、指示剂、蒸馏水。
指示剂 变色范围的pH
甲基橙 <3.1红色 3.1~4.4橙色 >4.4黄色
酚酞 <8.2无色 8.2~10.0浅红色 >10.0红色
(3)中和滴定实验操作(以酚酞作指示剂,用盐酸滴定氢氧化钠溶液)。
(4)终点判断:等到滴入最后一滴反应液,指示剂变色,且在半分钟内不能恢复原来的颜色,视为滴定
终点,并记录标准液的体积。
(5)数据处理:按上述操作重复2~3次,求出用去标准盐酸体积的平均值,根据原理计算。
c(NaOH)=
2 . 氧化还原滴定
(1)原理:以氧化剂或还原剂为滴定剂,直接滴定一些具有还原性或氧化性的物质,或者间接滴定一些
本身并没有还原性或氧化性,但能与某些还原剂或氧化剂反应的物质。
(2)试剂:常见用于滴定的氧化剂有KMnO 、KCr O 等;常见用于滴定的还原剂有亚铁盐、草酸、维
4 2 2 7
生素C等。
(3)指示剂:氧化还原滴定的指示剂有三类:
①氧化还原指示剂;
②专用指示剂,如在碘量法滴定中,可溶性淀粉溶液遇碘标准溶液变蓝;③自身指示剂,如高锰酸钾标准溶液滴定草酸时,滴定终点为溶液由无色变为浅红色。
3 . 沉淀滴定
(1)概念:沉淀滴定是利用沉淀反应进行滴定、测量分析的方法。生成沉淀的反应很多,但符合条件的
却很少,实际上应用最多的是银量法,即利用Ag+与卤素离子的反应来测定Cl-、Br-、I-浓度。
(2)原理:沉淀滴定所用的指示剂本身就是一种沉淀剂,滴定剂与被滴定物反应的生成物的溶解度要比
滴定剂与指示剂反应的生成物的溶解度小,否则不能用这种指示剂。如用AgNO 溶液测定溶液中Cl-的含
3
量时常以CrO为指示剂,这是因为AgCl比AgCrO 更难溶。
4
1.用标准的KOH溶液滴定未知浓度的盐酸,若测定结果偏低,其原因可能是( )
A.配制标准溶液的固体KOH中混有NaOH杂质
B.滴定到终点读数时,仰视滴定管的刻度,其他操作正确
C.盛装未知液的锥形瓶用蒸馏水洗过后再用未知液润洗
D.滴定到终点读数时,发现滴定管尖嘴处悬挂一滴溶液
【答案】A
【解析】A项将会使标准碱液的c(OH-)偏大,滴定时耗用的V(OH-)偏小,导致结果偏低,A项正确;
滴定终点时仰视读数,将使读取碱液的体积偏大,测定结果偏高,B项错误;用未知液润洗锥形瓶将使测
定结果偏高,C项错误;尖嘴处悬挂溶液将使读取的标准液体积偏大,测定结果偏高,D项错误。
2.如图是用EDTA(Na HY)标准溶液滴定法测定油菜样品中Ca2+含量的流程。下列说法正确的是( )
2 2
(已知:Ca2++H Y2-=CaY2-+2H+)
2
A.稀硝酸的作用是溶解,操作1是过滤
B.配制溶液用到的玻璃仪器有容量瓶、烧杯、玻璃棒
C.滴定过程中眼睛要注视滴定管内液面的变化
D.平行滴定三次,平均消耗23.30mLEDTA溶液,则测得Ca2+含量为0.155%
【答案】A
【解析】A项,油菜中本身含有较多磷元素,油菜灰中的钙元素可能以磷酸钙等难溶于水的钙盐形式
存在,可以用稀硝酸来溶解,因此稀硝酸的作用是溶解,操作1是为了把未溶解的固体和溶液分离开,为
过滤操作,A项正确;B项,由步骤知,配置100 mL溶液,需要用到的玻璃仪器有烧杯、玻璃棒、100
mL容量瓶、胶头滴管,B项错误;C项,滴定过程中眼睛应观察滴定所用锥形瓶中的颜色变化,而不是注
视滴定管内液面的变化,C项错误;D项,若平均消耗23.30 mL的EDTA溶液,由反应Ca2++H Y2-=CaY2-
2+2H+可知,100 mL济液中所含Ca2+的质量为m=0.0233 L ×0.005 mol/L× 40 g/mol× 10=0.0466 g,因此Ca2+含
量为0.0466 g÷3g× 100%=1.55%,D项错误;故选A。
3.一种测定水样中溴离子浓度的实验步骤如下:
①向锥形瓶中加入处理后的水样25.00mL,加入几滴NH Fe(SO ) 溶液。
4 4 2
②加入V mL c mol∙L−1AgNO 溶液(过量),充分摇匀。
1 1 3
③用c mol∙L−1KSCN标准溶液进行滴定,至终点时消耗标准溶液VmL 。
2 2
已知:K (AgBr)=7.7×10−13,Ag++SCN-= AgSCN(白色)↓,K (AgSCN)=1×10−12,下列说法不正确的是(
sp sp
)
A.滴定终点时,溶液变为红色
B.该水样中溴离子浓度为:c(Br-)= mol∙L−1
C.AgBr(s)+SCN-(aq) AgSCN(s)+Br-(aq)的平衡常数K=0.77
D.该实验需要严格控制水样的pH,若pH过高则测定结果将偏高
【答案】D
【解析】A项,加入几滴NH Fe(SO ) 指示剂,滴定终点时,KSCN过量,会与铁离子反应,因此溶液
4 4 2
变为红色,故A正确;B项,25mL溶液中Br-物质的量n(Br-)= V ×10−3 L×c mol∙L−1− V ×10−3 L×c
1 1 2 2
mol∙L−1=(V c − V c ) ×10−3 mol,因此该水样中溴离子浓度为:c(Br-)= mol∙L−1,故B正确;
1 1 2 2
C 项 , AgBr(s)+SCN - (aq) AgSCN(s)+Br - (aq) 的 平 衡 常 数
,故C正确;D项,该实验需要严格控制水样的pH,若pH
过高,银离子会与氢氧根反应,则得到的溴离子物质的量减少,则测定结果将偏低,故D错误。故选D。
4.一定条件下,乙酸酐[(CH CO) O]醇解反应
3 2
[(CH CO) O+ROH→CH COOR+CH COOH]可进行完全,利用此反应定量测定有机醇(ROH)中的羟基含
3 2 3 3
量,实验过程中酯的水解可忽略。实验步骤如下:
①配制一定浓度的乙酸酐-苯溶液。
②量取一定体积乙酸酐-苯溶液置于锥形瓶中,加入 样品,充分反应后,加适量水使剩余乙酸
酐完全水解:(CHCO) O+HO→2CH COOH。
3 2 2 3
③加指示剂并用cmol·L-1NaOH-甲醇标准溶液滴定至终点,消耗标准溶液VmL。
1④在相同条件下,量取相同体积的乙酸酐-苯溶液,只加适量水使乙酸酐完全水解;加指示剂并用
cmol·L-1NaOH-甲醇标准溶液滴定至终点,消耗标准溶液VmL。根据上述实验原理,下列说法正确的是
2
( )
A.可以用乙酸代替乙酸酐进行上述实验
B.若因甲醇挥发造成标准溶液浓度发生变化,将导致测定结果偏小
C.步骤③滴定时,不慎将锥形瓶内溶液溅出,将导致测定结果偏小
D.步骤④中,若加水量不足,将导致测定结果偏大
【答案】B
【解析】用cmol·L-1NaOH-甲醇标准溶液滴定乙酸酐完全水解生成的乙酸,消耗标准溶液 VmL,则消
2
耗NaOH的物质的量为(V ×c×10-3) mol,即乙酸酐的总物质的量为 ,ROH与乙酸酐反应
2
后剩余的乙酸酐的物质的量为 ,所以与 ROH 反应消耗的乙酸酐的物质的量为
。A项,乙酸与醇的酯化反应可逆,不能用乙酸代替乙酸酐进行上述实验,
A项错误;B项,若甲醇挥发,NaOH-甲醇溶液的浓度将偏大,滴定时消耗NaOH-甲醇溶液的体积偏小,
步骤④中所得V 偏小,而ROH的物质的量为 ,故将导致测定结果偏小,B
2
项正确;C项,步骤③滴定时,不慎将锥形瓶内溶液溅出,消耗NaOH-甲醇溶液的体积偏小即V 偏小,而
1
ROH的物质的量为 ,故将导致测定结果偏大,C项错误;D项,步骤④中,
若加水量不足,乙酸酐未完全水解,生成乙酸的物质的量偏小,消耗 NaOH-甲醇溶液的体积偏小即V 偏
2
小,而ROH的物质的量为 ,故将导致测定结果偏小,D项错误;故选B。
5.使用硫酸亚铁铵晶体[(NH )Fe(SO )·6H O]滴定法可以测定青铜中铬元素的含量。实验步骤如下:
4 2 4 2 2
步骤1:称量硫酸亚铁铵晶[(NH )Fe(SO )·6H O]溶于稀硫酸,加水稀释配成 1000 mL0.0200 mol/L
4 2 4 2 2
(NH )Fe(SO ) 标准溶液。
4 2 4 2步骤2:称取1.00 g青铜样品于250 mL维形瓶中,加入适量稀硝酸使其完全溶解,再加入适量过硫酸
[(NH )SO]溶液,加热煮沸,使样品中的铬元素完全转化为 HCrO ,冷却后加蒸馏水配制成250 mL溶液,
4 2 2 8 2 4
摇匀。
步骤3:取25 mL上述溶液置于锥形瓶中,加入硫酸酸化,滴入4滴N-苯代邻氨基苯甲酸指示剂,用
(NH )Fe(SO ) 标准溶液满淀至终点。重复上述操作 3次。测得消耗(NH )Fe(SO ) 标准溶液的体积分别为
4 2 4 2 4 2 4 2
18.90 mL、17.97 mL、18.03 mL。发生反应的离子方程式为:HCrO+Fe2++H+→Cr3++Fe3++H O (未配平)
2 4 2
下列说法不正确的是( )
A.在“步骤1”中,用到的玻璃仪器有1000 mL容量瓶、烧杯、玻璃棒、胶头滴管
B.在“步骤2”中,铜与硝酸反应的离子方程式为:3Cu+2NO-+8H+=3Cu2++2NO↑+4HO
3 2
C.青铜中铬元素的质量分数为6.344%
D.实验中,如果盛放(NH )Fe(SO ) 标准溶液的滴定管没有润洗,则测量结果将偏大
4 2 4 2
【答案】C
【解析】A项,在“步骤1”中配制溶液需要的玻璃仪器:1000 mL容量瓶、烧杯、玻璃棒、胶头滴管,
故A正确;B项,在“步骤2”中,铜与硝酸反应的离子方程式根据电子、电荷、原子守恒配平得方程式为:
3Cu+2NO-+8H+=3Cu2++2NO↑+4HO ,故B正确;C项,根据滴定过程(NH )Fe(SO ) 标准溶液的体积分别
3 2 4 2 4 2
为18.90 mL、17.97 mL、18.03 mL,因为第一组实验数据与第二、三组误差大而舍去,故平均消耗的溶液
体积为:V= ,反应关系式计算: ,
解得x=1.2×10-4mol,则铬元素的质量分数为: = 6.24%,故C不正确;D项,实验
中,如果盛放(NH )Fe(SO ) 标准溶液的滴定管没有润洗,实际标准液被稀释,导致滴加的体积偏大,在计
4 2 4 2
算时导致测量结果偏大,故D正确;故选C。
6.(2024·湖南高三联考)K Cr O(重铬酸钾)是一种常见的氧化剂。以铬渣(主要成分为Cr O、Fe O 等)
2 2 7 2 3 2 3
为原料制备KCr O 并测定其纯度。其步骤如下:
2 2 7
步骤1:铬渣粉碎和NaCO 均匀混合在空气中焙烧;
2 3
步骤2:用水浸取焙烧渣,过滤,得到水浸液(含NaCrO);
2 4
步骤3:向步骤2中水浸液加入BaCO ,过滤,得到BaCrO;
3 4
步骤4:向BaCrO 中加入NaHSO 溶液,过滤,得到浸出液(Na Cr O)和浸渣(BaSO);
4 4 2 2 7 4
步骤5:向步骤4中浸出液加入KCl粉末,蒸发浓缩、降温结晶、过滤,得到KCr O;
2 2 7
步骤6:准确称取mgK Cr O 产品溶于蒸馏水,加入适量稀硫酸,加入足量KI溶液(还原产物为
2 2 7Cr3+),用水稀释为250mL溶液,量取25.00mL稀释后溶液于锥形瓶中。用c mol•L-1NaSO 溶液滴定至终
2 2 3
点,消耗VmL滴定液。滴定反应为I+2S O2-=2I-+S O2-
2 2 3 4 6
下列叙述错误的是( )
A.步骤1中制备1molNa CrO 消耗0.75mol氧气
2 4
B.步骤3目的是除去杂质,富集铬元素
C.步骤6中KI作用是Cr O2-+6I-+14H+=2Cr3++3I +7H O
2 7 2 2
D.KCr O 产品纯度为w= %
2 2 7
【答案】D
【解析】A项,反应2Cr O+4NaCO+3O 4NaCrO+4CO 中生成1molNa CrO 消耗0.75molO,故
2 3 2 3 2 2 4 2 2 4 2
A正确;B项,利用步骤3将NaCrO 转化成BaCrO,滤去溶液,富集铬元素,故B正确;C项,加入KI
2 4 4
还原重铬酸钾,产物为Cr3+、I、HO,方程式为Cr O2-+6I-+14H+=2Cr3++3I +7H O,故C正确;D项,由
2 2 2 7 2 2
KCr O~3I ~6 Na SO 可知, ,故D错误;故选D。
2 2 7 2 2 2 3
7.(2025·湖南省部分学校高三联考,节选)高纯三氯氧磷POCl 是集成电路、太阳能电池生产的掺杂剂。
3
(4)实验室可通过以下实验步骤测定三氯氧磷产品中氯元素含量,可进一步计算三氯氧磷的质量分数
[假设产品中的杂质只有PCl 。已知:K (AgCl)=3.2×10-10,K (AgSCN)=2.0×10-12,Ag PO 呈黄色,难溶
3 sp sp 3 4
于水,溶于酸和氨水]。
步骤i:取ag产品置于盛有50.00mLNaOH溶液(足量)的水解瓶中,摇动至完全水解,将水解液“预处
理”并配成100.00mL溶液。
步骤ii:取10.00mL溶液于锥形瓶中,向其中加入cmol·L-1的AgNO 标准溶液VmL,使 完全沉淀,
1 3 1
再加入20mL硝基苯,振荡,使沉淀表面被有机物覆盖;然后加入几滴Fe(NO ) 溶液作指示剂,用
3 3
cmol·L-1NH SCN标准溶液滴定过量Ag+至终点,记下所用体积为VmL。
2 4 2
①步骤i中的“预处理”指的是 ;
②滴定终点的现象是 ;
③产品中三氯氧磷的百分含量为 %(填表达式);步骤ii中若忘记加入硝基苯,则所测
POCl 的含量将 (填“偏高”、“偏低”或“不变”)。
3
【答案】(4)向水解液加稀硝酸酸化 滴入最后半滴标准液,溶液变红色,且半分钟不变色
偏高【解析】(4)①为避免滴定过程中生成Ag PO 沉淀,应加稀硝酸酸化,排除PO 3-以及OH-对滴定实验
3 4 4
的干扰,故“预处理”指的是:向水解液加稀硝酸酸化。 ②用Fe(NO ) 做指示剂,用NH SCN标准溶液
3 3 4
滴定过量Ag+,当Ag+完全反应,Fe3++3SCN-=Fe(SCN) ,溶液变红色,达到滴定终点,故滴定终点为:滴入
3
最后半滴标准液,溶液变红色,且半分钟不变色。③根据元素守恒可得关系式:POCl ~3Cl-~3Ag+、
3
PCl ~3Cl-~3Ag+;与Cl-反应的Ag+的物质的量为
3
,则
,假设n(PCl )、n(POCl )的物质的量分别是x、
3 3
y,则 ,根据质量关系可得 ,解得
,所以POCl 的含量为: ;实验过程中
3
加入硝基苯的目的是使生成的AgCl沉淀与溶液隔离,避免滴定过程中SCN-与AgCl反应;根据硝基苯的
作用,若忘记此操作,则V 偏大,会导致所测POCl 的含量偏高。
2 3
8.(2025·浙江省强基联高三联考,节选)甘氨酸亚铁晶体[(NH CHCOO) Fe·2H O]是一种补铁剂。
2 2 2 2
(5)①准确称取甘氨酸亚铁晶体样品0.5600g于锥形瓶中,加3 mol·L-1HSO 溶液15mL将样品溶解完全
2 4
后,加入指示剂,立即用0.1000mol·L-1(NH )Ce(SO) 标准液滴定至终点,消耗标准液20.20mL(离子方程
4 2 4 3
式为Ce4++Fe2+=Fe3++Ce3+)。
②若步骤①操作中不加甘氨酸亚铁晶体样品,用0.1000mol·L-1(NH )Ce(SO) 标准液直接滴定至终点,
4 2 4 3
消耗标准液0.20mL。
甘氨酸亚铁晶体中铁元素的质量分数为 (用百分数表示)。
【答案】(5)20%
【解析】(5)由题意知,滴定消耗(NH )Ce(SO) 的体积为20.20mL-0.20mL=20.00mL,根据方程式的
4 2 4 3
比例关系可知,n(甘氨酸亚铁)= 0.1000mol·L-1×20×10-3L=2×10-3mol,则甘氨酸亚铁晶体中铁元素的质量分
数为 =20%。
9.(2025·浙江省强基联盟高三10月联考,节选)亚硝酰氯(NOCl,熔点-64.5℃,沸点-5. 5℃)为黄色气
体,易与水反应生成HNO 和HCl,常用作有机合成中间体。
2(4)制得的NOCl中可能含有少量NO 杂质,为测定产品纯度,进行如下实验:称取2.0000g样品溶于
2
50.00mLNaOH溶液中,加入几滴KCrO 溶液作指示剂,用足量硝酸酸化0.40mol·L-1AgNO 溶液滴定至终
2 4 3
点,消耗AgNO 溶液50.00mL。[已知:Ag CrO 为砖红色固体,K (AgCl)= 1.56×10-10,K (Ag CrO)=
3 2 4 sp sp 2 4
1.0×10-12]
①滴定终点的现象:当滴入最后半滴AgNO 标准溶液后, 。
3
②计算产品的纯度为 %(保留1位小数)。
【答案】(4) 出现砖红色沉淀,且半分钟内不变化 65.5
【解析】(4)①滴定中KCrO 溶液作指示剂,已知Ag CrO 为砖红色固体,滴定终点的现象为当滴人最
2 4 2 4
后半滴AgNO 标准溶液后,出现砖红色沉淀,且半分钟内不变化。②
3
,由关系 ,则样品纯度为
。
10.(2025·浙江省部分学校高三选考模拟,节选)(4)己二酸纯度测定
将0.5000g己二酸[HOOC(CH )COOH]样品配制成100mL溶液,每次取25.00mL试样溶液于锥形瓶中,
2 4
滴入几滴酚酞试液,用0.1000mol/LNaOH溶液滴定至终点,平均消耗NaOH溶液16.00mL (己二酸被完全
中和)。
①下列说法正确的是 。
A.用100mL容量瓶配制成溶液后,最好用25mL规格的量筒量取待测液于锥形瓶中
B.润洗滴定管时,待液体润湿全部滴定管内壁后,应将液体从滴定管上口倒入预置的烧杯中
C.接近滴定终点时,应控制活塞,改为滴加半滴标准溶液,直至溶液变为粉红色,且半分钟内不变
色
D.若滴定前滴定管尖嘴部分气泡未赶走,滴定后气泡消失,则测定结果偏高
②己二酸的纯度为 %。
【答案】(4) CD 93.44
【解析】(4)①A项,量筒只能读到小数点后一位,量取25.00mL待测液于锥形瓶中时,最好用25mL
规格的酸式滴定管,A不正确;B项,润洗滴定管时,滴定管内壁、橡皮管、尖嘴管都需要润洗,所以,
液体润湿全部滴定管内壁后,应将液体从滴定管下口流入预置的烧杯中,B不正确;C项,看到溶液变红
后又变为无色,表明接近滴定终点,此时应控制活塞,改为滴加半滴标准溶液,直至溶液变为粉红色,且
半分钟内不变色,C正确;D项,若滴定前滴定管尖嘴部分气泡未赶走,滴定后气泡消失,则读取的所用
标准液的体积偏大,测定结果偏高,D正确;故选CD;②由反应可以建立如下关系式:HOOC(CH )COOH——2NaOH,则己二酸的纯度为 ≈93.44%。
2 4
11.过氧化氢的水溶液适用于医用消毒、环境消毒和食品消毒。
Ⅰ.过氧化氢性质探究实验
(1)酸性条件下HO 可将Fe2+转化成Fe3+,由此说明HO 具有______性。
2 2 2 2
(2)已知HO 是一种二元弱酸,其中K =2.20×10-12、K =1.05×10-25,则HO 的电离方程式为______,
2 2 a1 a2 2 2
常温下,1mol∙L-1的HO 溶液的pH约为______。
2 2
Ⅱ.过氧化氢含量的测定实验。某兴趣小组同学用0.1000mol∙L-1的酸性高锰酸钾标准溶液滴定试样中的
过氧化氢,反应原理为2 MnO-+5H O+6H+=2Mn2++8H O+5O↑。
4 2 2 2 2
(3)滴定达到终点的现象是______。
(4)用移液管移取25.00mL试样置于锥形瓶中,重复滴定四次,每次消耗酸性高锰酸钾标准溶液的体积
如表所示:
第一 第三
第二次 第四次
次 次
V(KMnO 溶液)/mL 17.10 18.10 18.00 17.90
4
计算试样中过氧化氢的浓度为______mol∙L-1。
(5)若滴定前滴定管尖嘴处有气泡,滴定后消失,则测定结果______(填“偏高”“偏低”或“不变”)。
【答案】(1)氧化 (2)H O H++HO-、HO - H++O 2- 5.8
2 2 2 2 2
(3)锥形瓶内溶液恰好由无色变为浅紫色,且30秒内⇌溶液不褪色
(4)0.1800 (5)偏高
【解析】(1)酸性条件下,HO 可将Fe2+氧化为Fe3+,HO 转变为HO,化合价降低,体现了过氧化氢
2 2 2 2 2
的氧化性;(2)过氧化氢属于二元弱酸,分步电离,其电离的方程式为HO H++HO-、HO - H+
2 2 2 2
⇌
+O 2-;又K =2.20×10-12,K =1.05×10-25,K K ,以第一步电离为主,则K = =
2 a1 a2 a1 a2 a1
≫
=2.20×10-12,所以c(H+)≈1.48×10-6mol∙L-1,即pH≈5.8;(3)该实验是酸性高锰酸钾标准溶液滴定试样中的过
氧化氢,发生反应:2 MnO-+5H O+6H+=2Mn2++8H O+5O↑,若达到滴定终点,高锰酸钾恰好完全反应,
4 2 2 2 2
故滴定达到终点的现象是锥形瓶内溶液恰好由无色变为浅紫色,且30秒内溶液不褪色;(4)由于第一次数
据误差过大,故舍去;其他三组数据的平均值18.00mL,根据反应2 MnO-+5H O+6H+=2Mn2+
4 2 2
+8H O+5O↑,n(H O)=2.5×n(MnO -)=2.5×0.1000mol∙L-1×0.018L,c(H O)=
2 2 2 2 4 2 2mol∙L-1=0.1800mol∙L-1;(5)滴定前滴定管尖嘴处有气泡,导致消耗的标准液体积偏大,根据c V =c V ,
标 标 待 待
c = ,则测定结果偏高。
待
12.乙二酸俗名草酸,下面是化学学习小组的同学对草酸晶体(H C O·xHO)进行的探究性学习的过程,
2 2 4 2
请你参与并协助他们完成相关学习任务。
该组同学的研究课题是:探究测定草酸晶体(H C O·xHO)中的x值。通过查阅资料和网络查寻得,草
2 2 4 2
酸易溶于水,水溶液可以用酸性KMnO 溶液进行滴定:2MnO -+5HC O+6H+=2Mn2++5CO ↑+8H O。学习
4 4 2 2 4 2 2
小组的同学设计了如下步骤用滴定的方法测定x值。
①称取1.260 g纯草酸晶体,将其制成 水溶液为待测液。
②取 待测液放入锥形瓶中,再加入适量的稀HSO 。
2 4
③用浓度为 的酸性KMnO 标准溶液进行滴定,达到终点时消耗 。
4
(1)上述步骤②中使用的锥形瓶是否需要用待测液润洗_______,(填“是”或“否”)滴定时,将酸性
KMnO 标准液装入_______(填“酸式”或“碱式”)滴定管中。
4
(2)本实验滴定达到终点的标志是_______。
(3)通过上述数据,求得 _______。
(4)若滴定终点时俯视滴定管刻度,则由此测得的x值会_______(填偏“大”、“偏小”或“不变”)。
(5)根据上述实验计算的数据可信性不强,为了提高实验的准确性,请写出改进措施_______。
【答案】(1) 否 酸式
(2)当最后半滴KMnO 溶液滴入,溶液颜色恰好由无色变为浅红色,且半分钟不恢复至原来的颜色
4
(3)2
(4)偏大
(5)重复操作②③步骤2-3次,取平均值
【解析】(1)滴定实验中锥形瓶不能润洗,否则导致待测液体积偏大;酸性高锰酸钾溶液应用酸式滴定
管盛装;(2)滴定终点判断的方法:当最后半滴KMnO 溶液滴入,溶液颜色恰好由无色变为浅红色,且半
4
分钟不恢复至原来的颜色,故答案为:当最后半滴KMnO 溶液滴入,溶液颜色恰好由无色变为浅红色,且
4
半分钟不恢复至原来的颜色;(3)n(KMnO)= ×0.01L=0.001mol;结合反应可知n(H C O)=
4 2 2 4
n(KMnO)=0.0025mol,m(HC O)=0.0025mol×90g/mol=0.225g,m(HO)= 1.260 g× -0.225g =0.315-
4 2 2 4 20.225g=0.09g,n(H O)=0.005mol,n(H C O):n(H O)=1:2,则x=2;(4)若滴定终点时俯视滴定管刻度,导
2 2 2 4 2
致读数偏小,则所测n(H C O 偏小,n(H O)偏大,则x偏大;(5)定量实验只进行一次实验,数据可信性不
2 2 4 2
强,为了提高实验的准确性需重复操作②③步骤2-3次,取平均值。
13.烟道气中的NO 是主要的大气污染物之一,为了监测其含量,选用如下采样和检测方法。
x
将V L气样通入适量酸化的HO 溶液中,使NO 完全被氧化为NO,加水稀释至100.00 mL。量取
2 2 x
20.00 mL该溶液,加入V mL c mol·L-1 FeSO 标准溶液(过量),充分反应后,用c mol·L-1 KCr O 标
1 1 4 2 2 2 7
准溶液滴定剩余的Fe2+,终点时消耗KCr O 溶液V mL。
2 2 7 2
回答下列问题:
(1)滴定过程中发生下列反应:
3Fe2++NO+4H+===NO↑+3Fe3++2HO、Cr O+6Fe2++14H+===2Cr3++6Fe3++7HO
2 2 2
则气样中NO 折合成NO 的含量为________ mg·m-3。
x 2
(2)若FeSO 标准溶液部分变质,会使测定结果__________(填“偏高”“偏低”或“无影响”)。
4
【答案】(1) ×104 (2)偏高
【解析】(1)根据关系式:Cr O~6Fe2+,求得KCr O 标准溶液消耗n(Fe2+)=6cV×10-3 mol;则NO
2 2 2 7 2 2
消耗n(Fe2+)=(cV-6cV)×10-3 mol,根据关系式3Fe2+~NO得n(NO)=(cV-6cV)×10-3 mol,n(NO)
1 1 2 2 1 1 2 2 x
=n(NO )=n(NO)=(cV-6cV)×10-3 mol,V L气样中含m(NO )=(cV-6cV)×46× mg,所以气样中
2 1 1 2 2 2 1 1 2 2
NO 的含量为 mg·m-3= ×104 mg·m-3。
2