文档内容
专题验收评价
专题 09 化学反应速率与化学平衡
内容概览
A·常考题不丢分
【考点一 化学反应速率及其影响因素和相关计算】
【考点二 化学平衡及其影响因素】
【考点三 化学平衡常数及化学平衡相关计算】
【微专题 图像、图表题的信息提取与应用】
B·综合素养拿高分/拓展培优拿高分
C·挑战真题争满分
【考点一 化学反应速率及其影响因素和相关计算】
1.(2023·辽宁·校联考二模)某温度下,在2L恒容密闭容器中4molNH COONH(s),发生如下反应
2 4
,在0-1min内,CO 的生成速率为0.4mol•L-1•min-1,0-2min内,
2
CO 的生成速率为0.3mol•L-1•min-1,0-3min内,CO 的生成速率为0.2mol•L-1•min-1,下列说法错误的是
2 2
A.当混合气体的平均摩尔质量不变时,标志此反应达到了平衡状态
B.0-1min内,NH COONH(s)的反应速率为62.4g/min
2 4
C.30秒时,CO 的浓度大于0.2mol/L
2
D.2min时,再加入2molNH ,此时反应的V >V
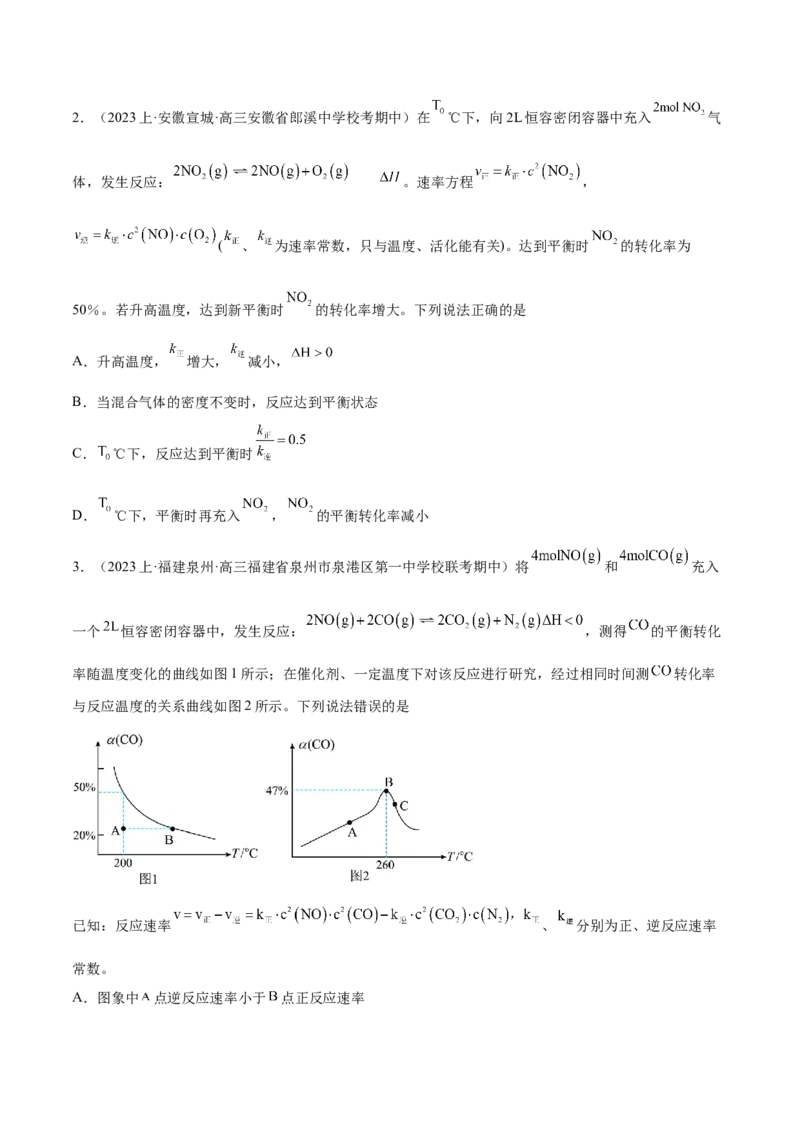
3 逆 正2.(2023上·安徽宣城·高三安徽省郎溪中学校考期中)在 ℃下,向2L恒容密闭容器中充入 气
体,发生反应: 。速率方程 ,
( 、 为速率常数,只与温度、活化能有关)。达到平衡时 的转化率为
50%。若升高温度,达到新平衡时 的转化率增大。下列说法正确的是
A.升高温度, 增大, 减小,
B.当混合气体的密度不变时,反应达到平衡状态
C. ℃下,反应达到平衡时
D. ℃下,平衡时再充入 , 的平衡转化率减小
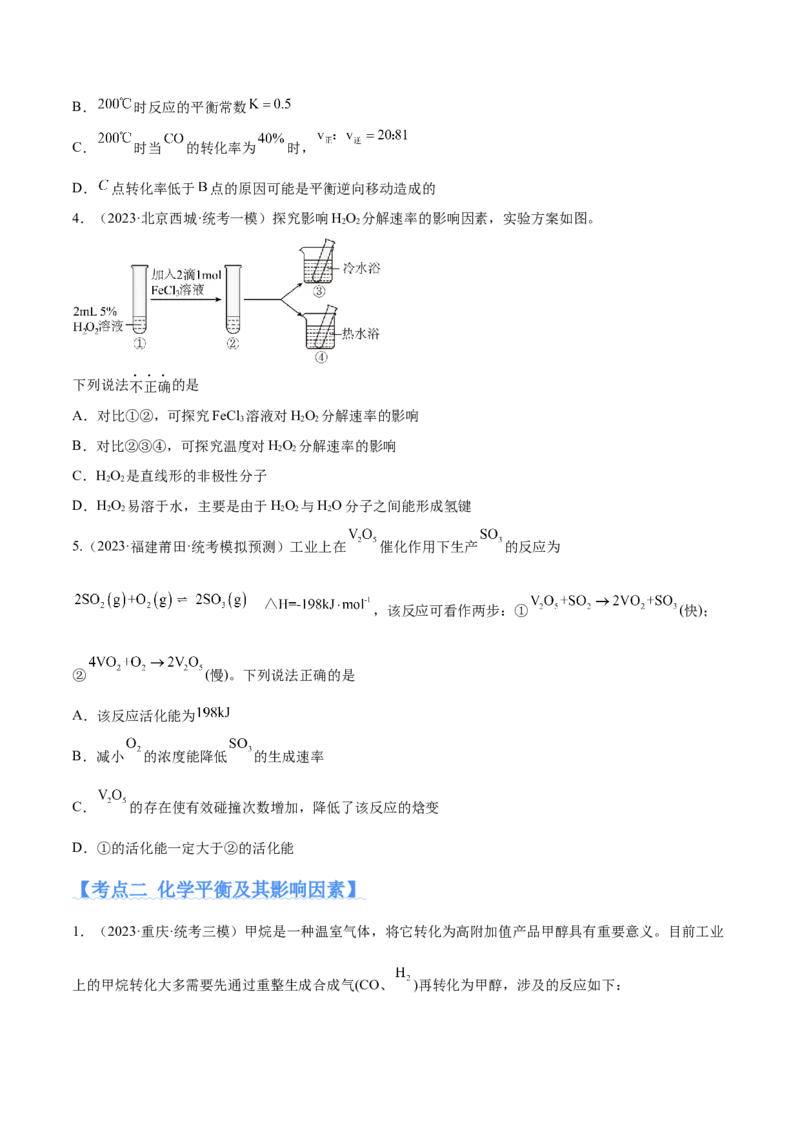
3.(2023上·福建泉州·高三福建省泉州市泉港区第一中学校联考期中)将 和 充入
一个 恒容密闭容器中,发生反应: ,测得 的平衡转化
率随温度变化的曲线如图1所示;在催化剂、一定温度下对该反应进行研究,经过相同时间测 转化率
与反应温度的关系曲线如图2所示。下列说法错误的是
已知:反应速率 、 分别为正、逆反应速率
常数。
A.图象中 点逆反应速率小于 点正反应速率B. 时反应的平衡常数
C. 时当 的转化率为 时,
D. 点转化率低于 点的原因可能是平衡逆向移动造成的
4.(2023·北京西城·统考一模)探究影响HO 分解速率的影响因素,实验方案如图。
2 2
下列说法不正确的是
A.对比①②,可探究FeCl 溶液对HO 分解速率的影响
3 2 2
B.对比②③④,可探究温度对HO 分解速率的影响
2 2
C.HO 是直线形的非极性分子
2 2
D.HO 易溶于水,主要是由于HO 与HO分子之间能形成氢键
2 2 2 2 2
5.(2023·福建莆田·统考模拟预测)工业上在 催化作用下生产 的反应为
,该反应可看作两步:① (快);
② (慢)。下列说法正确的是
A.该反应活化能为
B.减小 的浓度能降低 的生成速率
C. 的存在使有效碰撞次数增加,降低了该反应的焓变
D.①的活化能一定大于②的活化能
【考点二 化学平衡及其影响因素】
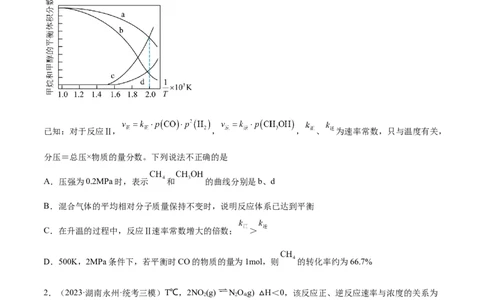
1.(2023·重庆·统考三模)甲烷是一种温室气体,将它转化为高附加值产品甲醇具有重要意义。目前工业
上的甲烷转化大多需要先通过重整生成合成气(CO、 )再转化为甲醇,涉及的反应如下:反应Ⅰ:
反应Ⅱ:
在密闭容器中通入3mol 和2mol ,假设只发生反应Ⅰ和Ⅱ,分别在0.2MPa和2MPa下进行反应,
其中 和 的平衡体积分数随温度变化如图所示。
已知:对于反应Ⅱ, , , 、 为速率常数,只与温度有关,
分压=总压×物质的量分数。下列说法不正确的是
A.压强为0.2MPa时,表示 和 的曲线分别是b、d
B.混合气体的平均相对分子质量保持不变时,说明反应体系已达到平衡
C.在升温的过程中,反应Ⅱ速率常数增大的倍数; >
D.500K,2MPa条件下,若平衡时CO的物质的量为1mol,则 的转化率约为66.7%
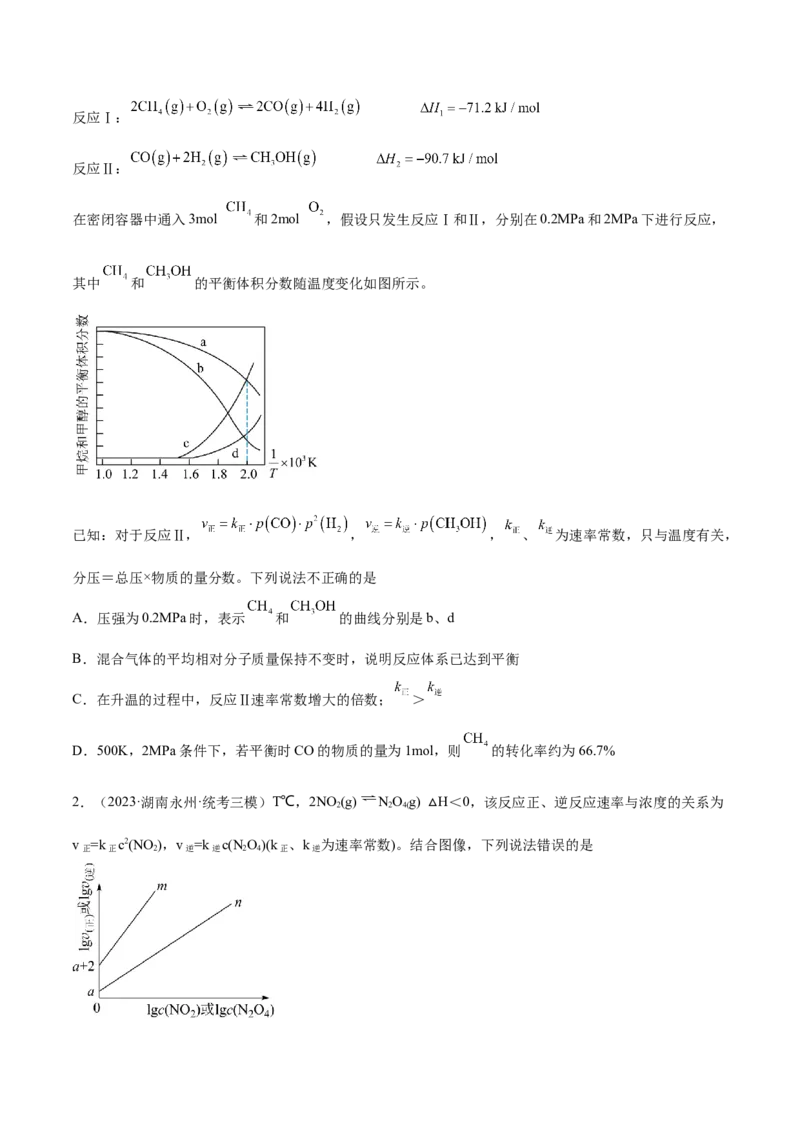
2.(2023·湖南永州·统考三模)T℃,2NO (g) NO g) H<0,该反应正、逆反应速率与浓度的关系为
2 2 4(
△
v =k c2(NO ),v =k c(NO)(k 、k 为速率常数)。结合图像,下列说法错误的是
正 正 2 逆 逆 2 4 正 逆A.图中表示lgv ~lgc(N O)的线是n
逆 2 4
B.当2 v(N O)=v (NO )时,说明反应达到平衡状态
正 2 4 逆 2
C.T℃时,向2L的容器中充入5molN O 气体和1molNO 气体,此时v <v
2 4 2 正 逆
D.T℃时,向刚性容器中充入一定量NO 气体,平衡后测得c(NO)为1.0mol•L-1,则平衡时,v 的数值为
2 2 4 正
10a
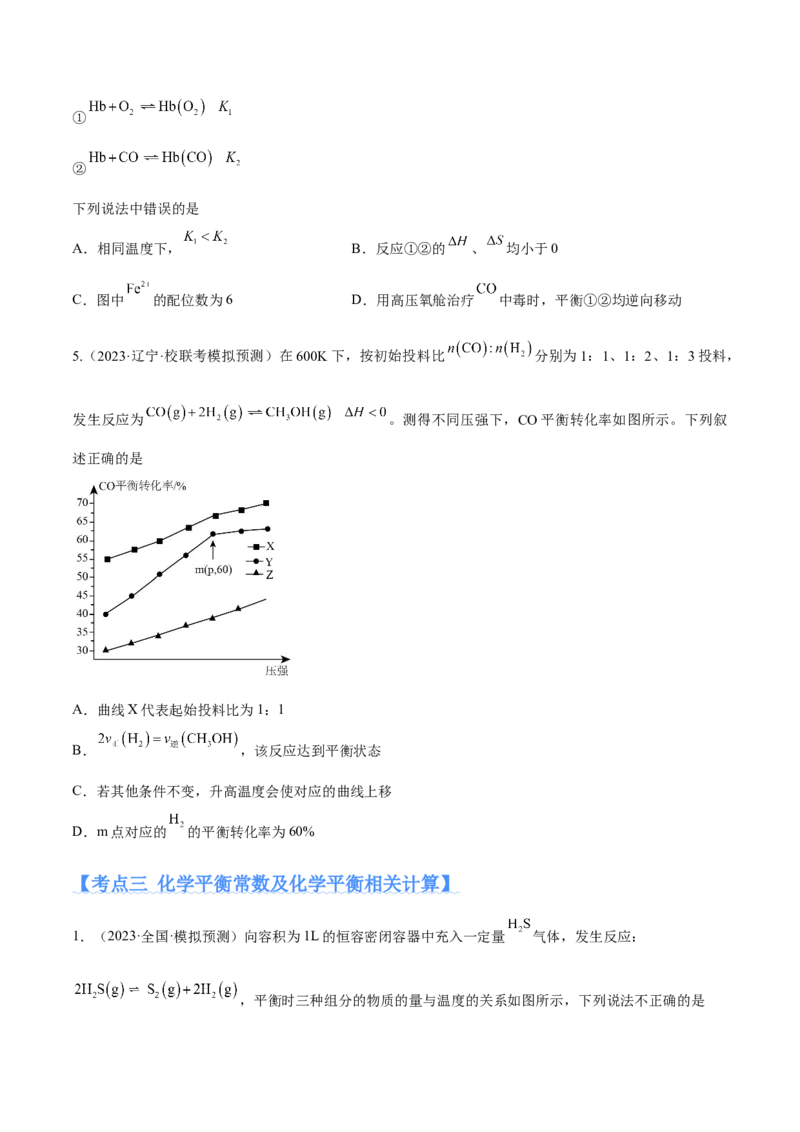
3.(2023·全国·模拟预测)CS 是一种重要的化工原料。工业上可以利用硫(S )与CH 制备CS,在2L恒
2 8 4 2
容密闭容器中S(s)受热分解成气态S,发生反应2S(g)+CH (g) CS(g)+2HS(g) H,一定条件下,平
8 2 2 4 2 2 1
衡时S 的体积分数、CH 的平衡转化率与温度的关系如图所示。下列说法正确的是 △
2 4
A.△H>0
1
B.某温度下,S(g)分解成气态S,当混合气体密度不变时,当CH(g)与S(g)的反应达到平衡状态
8 2 4 2
C.若容器内只发生反应S(s) 4S(g),平衡后恒温压缩体积,S(g)的浓度不变
8 2 2
D.若起始加入2molCH ,2min达到平衡时甲烷转化率为30%,则0~2min内HS的平均反应速率为
4 2
0.6mol•L-1•min-1
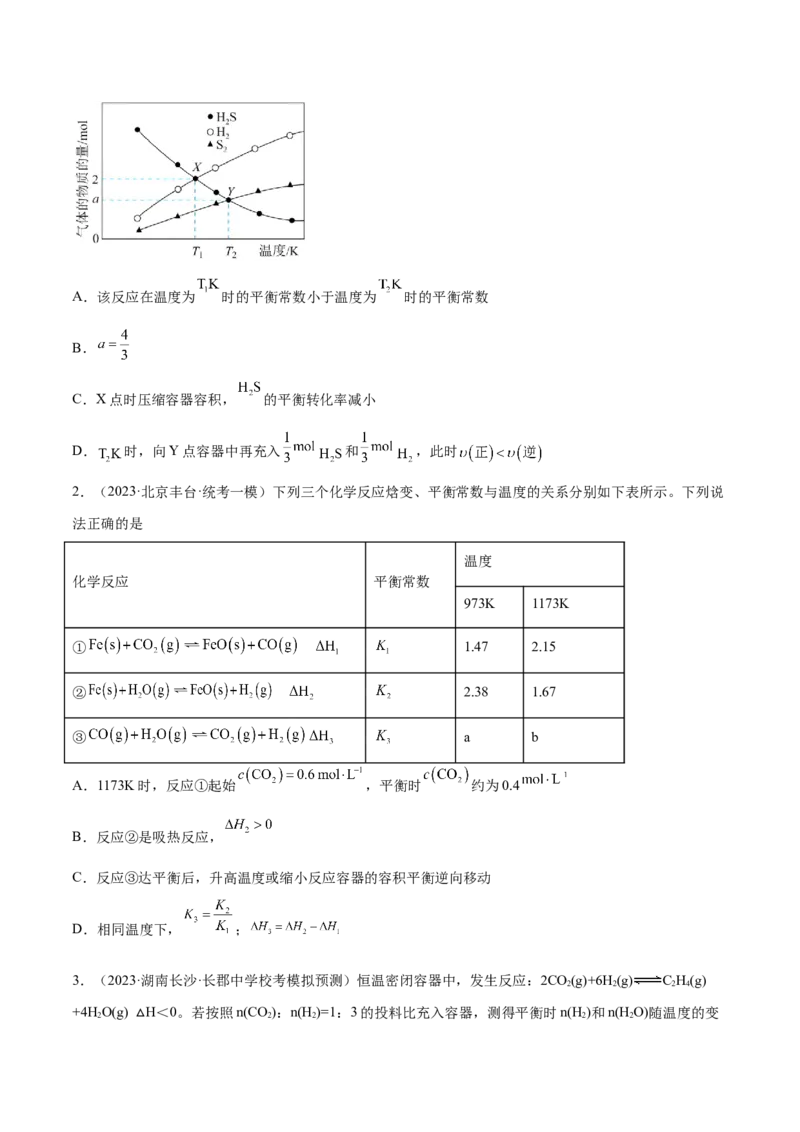
4.(2024·辽宁沈阳·统考一模)血红蛋白可与 结合,更易与 配位,血红蛋白与 配位示意如图所
示。血红蛋白 与 、 结合的反应可表示为①
②
下列说法中错误的是
A.相同温度下, B.反应①②的 、 均小于0
C.图中 的配位数为6 D.用高压氧舱治疗 中毒时,平衡①②均逆向移动
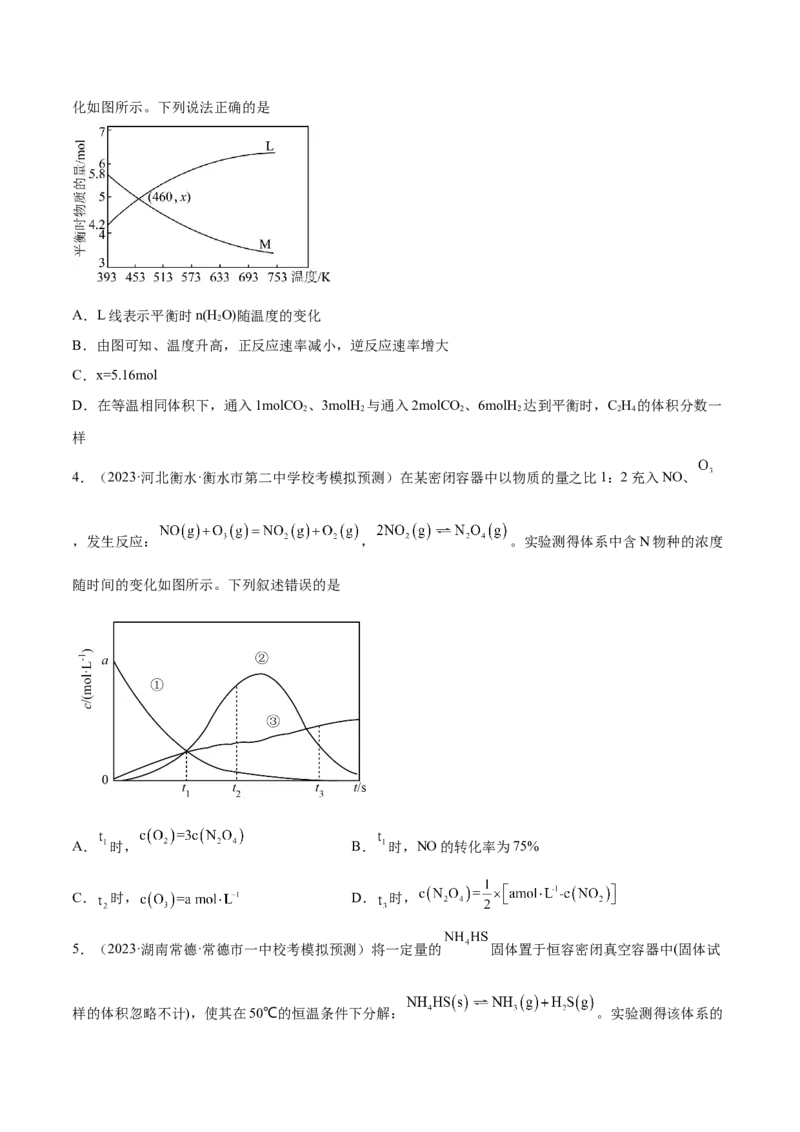
5.(2023·辽宁·校联考模拟预测)在600K下,按初始投料比 分别为1:1、1:2、1:3投料,
发生反应为 。测得不同压强下,CO平衡转化率如图所示。下列叙
述正确的是
A.曲线X代表起始投料比为1:1
B. ,该反应达到平衡状态
C.若其他条件不变,升高温度会使对应的曲线上移
D.m点对应的 的平衡转化率为60%
【考点三 化学平衡常数及化学平衡相关计算】
1.(2023·全国·模拟预测)向容积为1L的恒容密闭容器中充入一定量 气体,发生反应:
,平衡时三种组分的物质的量与温度的关系如图所示,下列说法不正确的是A.该反应在温度为 时的平衡常数小于温度为 时的平衡常数
B.
C.X点时压缩容器容积, 的平衡转化率减小
D. 时,向Y点容器中再充入 和 ,此时
2.(2023·北京丰台·统考一模)下列三个化学反应焓变、平衡常数与温度的关系分别如下表所示。下列说
法正确的是
温度
化学反应 平衡常数
973K 1173K
① 1.47 2.15
② 2.38 1.67
③ a b
A.1173K时,反应①起始 ,平衡时 约为0.4
B.反应②是吸热反应,
C.反应③达平衡后,升高温度或缩小反应容器的容积平衡逆向移动
D.相同温度下, ;
3.(2023·湖南长沙·长郡中学校考模拟预测)恒温密闭容器中,发生反应:2CO(g)+6H(g) C H(g)
2 2 2 4
+4H O(g) H<0。若按照n(CO):n(H )=1:3的投料比充入容器,测得平衡时n(H )和n(H O)随温度的变
2 2 2 2 2
△化如图所示。下列说法正确的是
A.L线表示平衡时n(H O)随温度的变化
2
B.由图可知、温度升高,正反应速率减小,逆反应速率增大
C.x=5.16mol
D.在等温相同体积下,通入1molCO 、3molH 与通入2molCO 、6molH 达到平衡时,C H 的体积分数一
2 2 2 2 2 4
样
4.(2023·河北衡水·衡水市第二中学校考模拟预测)在某密闭容器中以物质的量之比1:2充入NO、
,发生反应: , 。实验测得体系中含N物种的浓度
随时间的变化如图所示。下列叙述错误的是
A. 时, B. 时,NO的转化率为75%
C. 时, D. 时,
5.(2023·湖南常德·常德市一中校考模拟预测)将一定量的 固体置于恒容密闭真空容器中(固体试
样的体积忽略不计),使其在50℃的恒温条件下分解: 。实验测得该体系的压强如表所示:
时间/min 0 10 20 30 40 50 60 70
压强/kPa 0 0.66 1.28 1.78 2.20 2.50 2.50 2.50
已知: 为用各气体分压表示的平衡常数,分压=总压×物质的量分数。
下列有关说法正确的是
A.当混合气体的平均摩尔质量不再随时间变化时,反应达到平衡
B.0~10 min,用HS的压强变化表示该反应的平均反应速率为
2
C.50℃时, 的分解反应的压强平衡常数
D.50℃时,若在65 min时将容器的容积压缩至原来的 ,再次达到平衡时,体系的压强大于2.50 kPa
【微专题 图像、图表题的信息提取与应用】
1.(2023·天津南开·统考一模)已知: 现将三个相同容积的密闭容器中按
不同方式投入反应物发生反应。相关数据见下表:
容器1 容器2 容器3
反应温度(°C) 400 400 500
起始量 lmol 、1mol (g) 2mol HI lmol 、1mol (g)
平衡浓度
平衡转化率
平衡常数
下列各项关系不正确的是
A. B.
C. D.
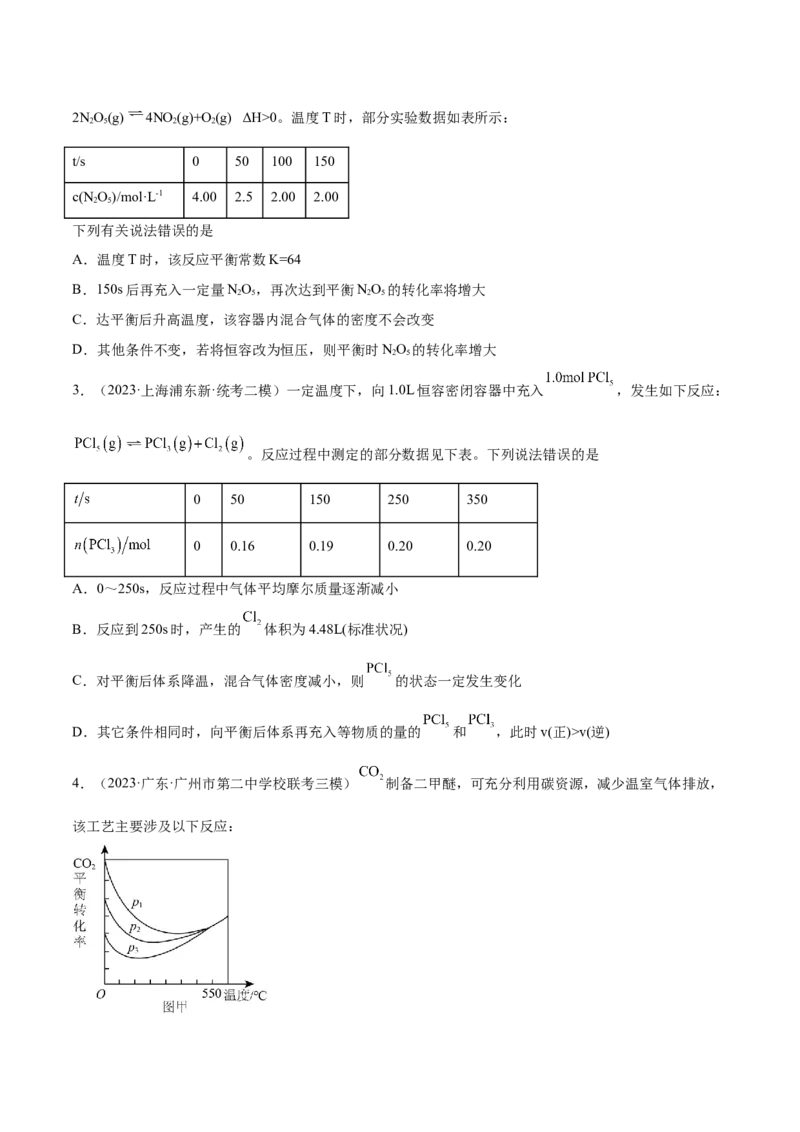
2.(2023·湖北·校联考模拟预测)在恒温恒容条件下,向某容器中充入一定量的NO 气体发生下列反应:
2 52NO(g) 4NO (g)+O(g) ΔH>0。温度T时,部分实验数据如表所示:
2 5 2 2
t/s 0 50 100 150
c(NO)/mol·L-1 4.00 2.5 2.00 2.00
2 5
下列有关说法错误的是
A.温度T时,该反应平衡常数K=64
B.150s后再充入一定量NO,再次达到平衡NO 的转化率将增大
2 5 2 5
C.达平衡后升高温度,该容器内混合气体的密度不会改变
D.其他条件不变,若将恒容改为恒压,则平衡时NO 的转化率增大
2 5
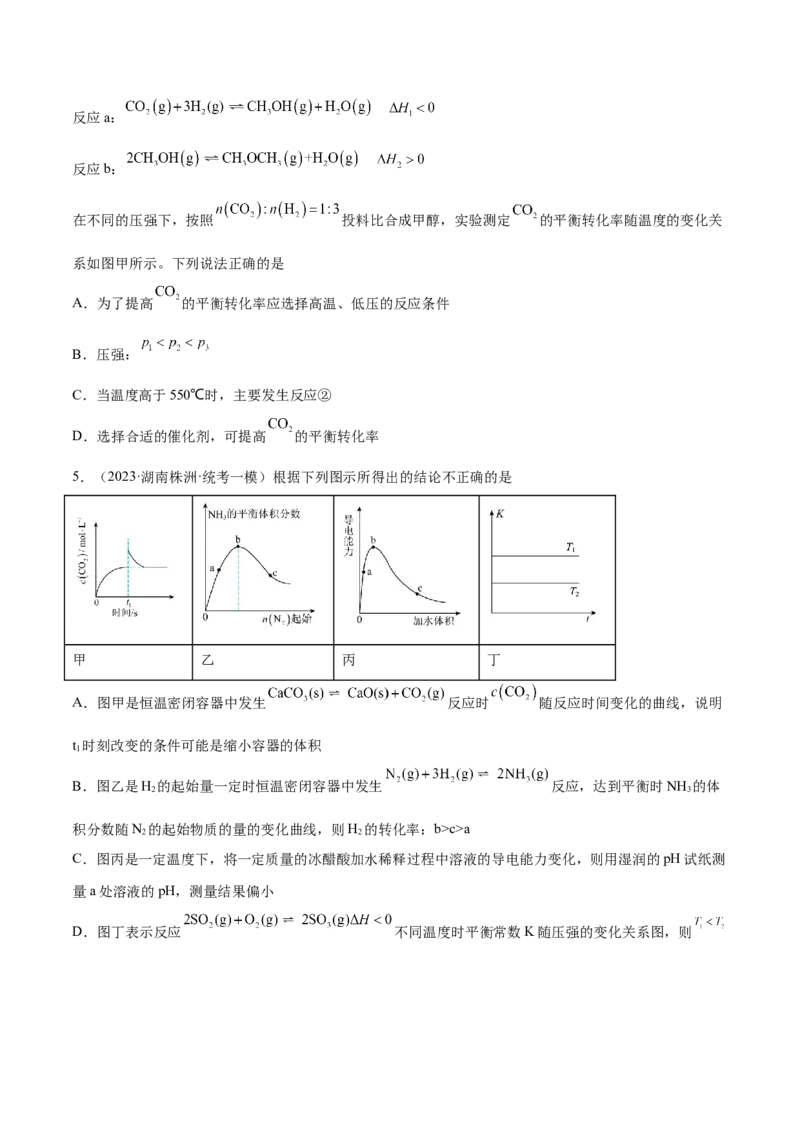
3.(2023·上海浦东新·统考二模)一定温度下,向1.0L恒容密闭容器中充入 ,发生如下反应:
。反应过程中测定的部分数据见下表。下列说法错误的是
0 50 150 250 350
0 0.16 0.19 0.20 0.20
A.0~250s,反应过程中气体平均摩尔质量逐渐减小
B.反应到250s时,产生的 体积为4.48L(标准状况)
C.对平衡后体系降温,混合气体密度减小,则 的状态一定发生变化
D.其它条件相同时,向平衡后体系再充入等物质的量的 和 ,此时v(正)>v(逆)
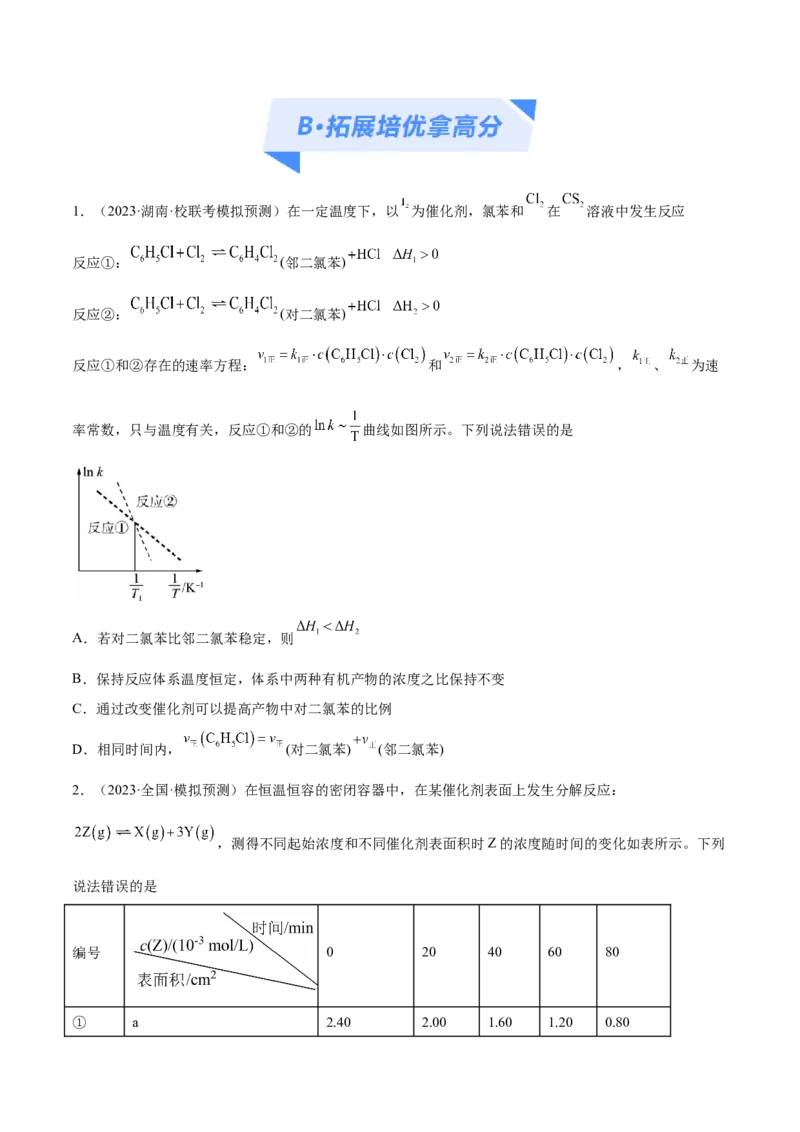
4.(2023·广东·广州市第二中学校联考三模) 制备二甲醚,可充分利用碳资源,减少温室气体排放,
该工艺主要涉及以下反应:反应a:
反应b:
在不同的压强下,按照 投料比合成甲醇,实验测定 的平衡转化率随温度的变化关
系如图甲所示。下列说法正确的是
A.为了提高 的平衡转化率应选择高温、低压的反应条件
B.压强:
C.当温度高于550℃时,主要发生反应②
D.选择合适的催化剂,可提高 的平衡转化率
5.(2023·湖南株洲·统考一模)根据下列图示所得出的结论不正确的是
甲 乙 丙 丁
A.图甲是恒温密闭容器中发生 反应时 随反应时间变化的曲线,说明
t 时刻改变的条件可能是缩小容器的体积
1
B.图乙是H 的起始量一定时恒温密闭容器中发生 反应,达到平衡时NH 的体
2 3
积分数随N 的起始物质的量的变化曲线,则H 的转化率:b>c>a
2 2
C.图丙是一定温度下,将一定质量的冰醋酸加水稀释过程中溶液的导电能力变化,则用湿润的pH试纸测
量a处溶液的pH,测量结果偏小
D.图丁表示反应 不同温度时平衡常数K随压强的变化关系图,则1.(2023·湖南·校联考模拟预测)在一定温度下,以 为催化剂,氯苯和 在 溶液中发生反应
反应①: (邻二氯苯)
反应②: (对二氯苯)
反应①和②存在的速率方程: 和 , 、 为速
率常数,只与温度有关,反应①和②的 曲线如图所示。下列说法错误的是
A.若对二氯苯比邻二氯苯稳定,则
B.保持反应体系温度恒定,体系中两种有机产物的浓度之比保持不变
C.通过改变催化剂可以提高产物中对二氯苯的比例
D.相同时间内, (对二氯苯) (邻二氯苯)
2.(2023·全国·模拟预测)在恒温恒容的密闭容器中,在某催化剂表面上发生分解反应:
,测得不同起始浓度和不同催化剂表面积时Z的浓度随时间的变化如表所示。下列
说法错误的是
编号 0 20 40 60 80
① a 2.40 2.00 1.60 1.20 0.80② a 1.20 0.80 0.40 x
③ 2a 2.40 1.60 0.80 0.40 0.40
A.实验①,100 min时反应达到平衡状态
B.实验②,60 min时反应处于平衡状态
C.相同条件下,增大催化剂的表面积,Z的平衡转化率不变
D.相同条件下,增加Z的浓度,反应速率增大
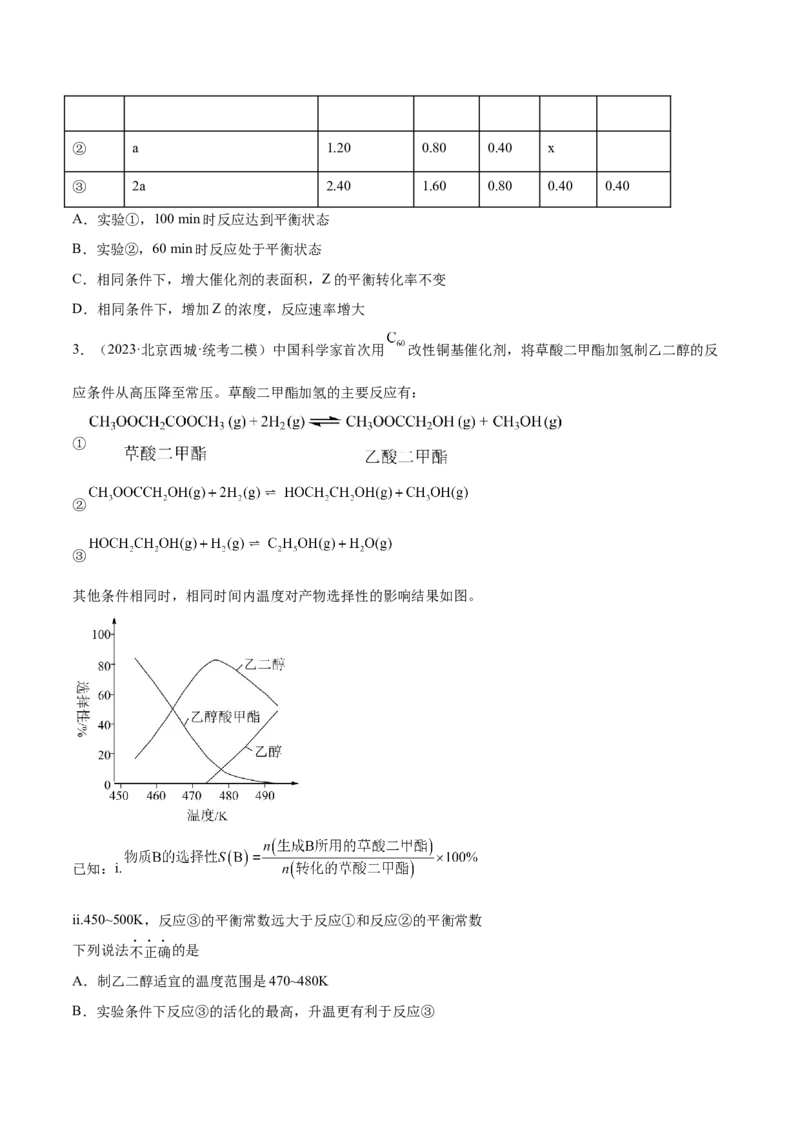
3.(2023·北京西城·统考二模)中国科学家首次用 改性铜基催化剂,将草酸二甲酯加氢制乙二醇的反
应条件从高压降至常压。草酸二甲酯加氢的主要反应有:
①
②
③
其他条件相同时,相同时间内温度对产物选择性的影响结果如图。
已知:i.
ii.450~500K,反应③的平衡常数远大于反应①和反应②的平衡常数
下列说法不正确的是
A.制乙二醇适宜的温度范围是470~480K
B.实验条件下反应③的活化的最高,升温更有利于反应③C.减压可提高乙二醇的平衡产率
D.铜基催化剂用 改性后反应速率增大,可以降低反应所需的压强
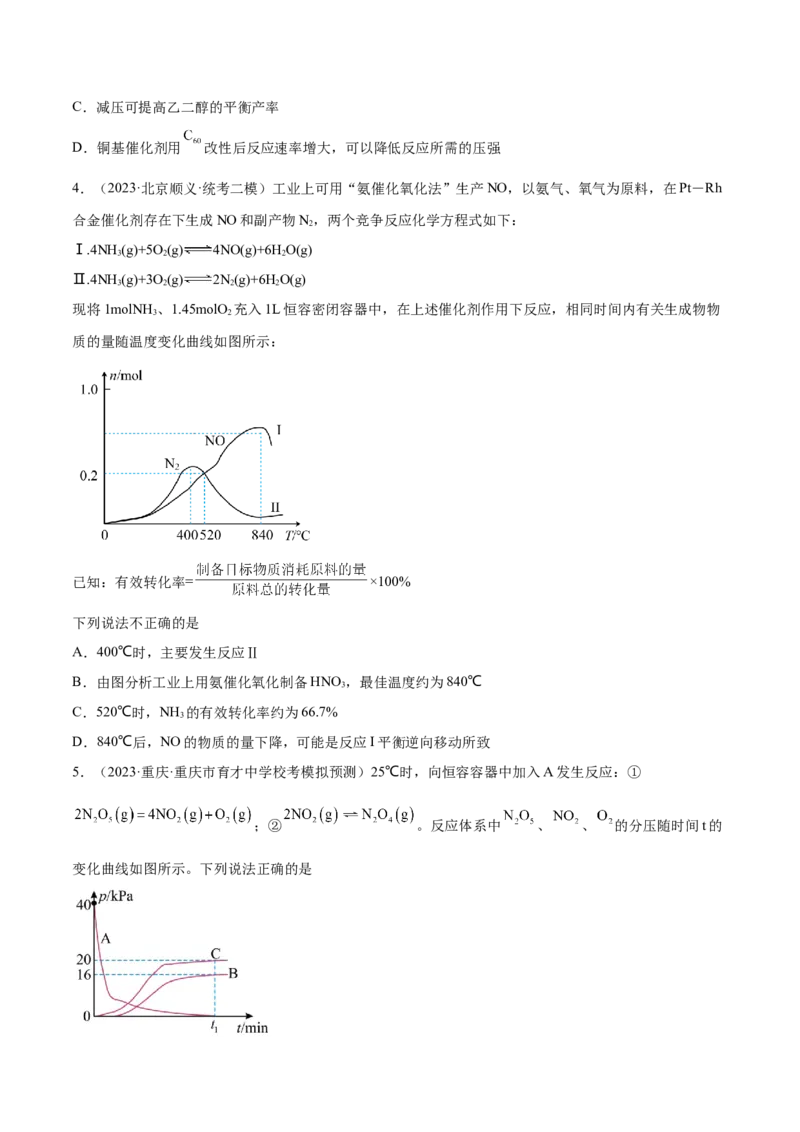
4.(2023·北京顺义·统考二模)工业上可用“氨催化氧化法”生产NO,以氨气、氧气为原料,在Pt-Rh
合金催化剂存在下生成NO和副产物N,两个竞争反应化学方程式如下:
2
Ⅰ.4NH(g)+5O(g) 4NO(g)+6H O(g)
3 2 2
Ⅱ.4NH(g)+3O(g) 2N(g)+6HO(g)
3 2 2 2
现将1molNH 、1.45molO 充入1L恒容密闭容器中,在上述催化剂作用下反应,相同时间内有关生成物物
3 2
质的量随温度变化曲线如图所示:
已知:有效转化率= ×100%
下列说法不正确的是
A.400℃时,主要发生反应Ⅱ
B.由图分析工业上用氨催化氧化制备HNO,最佳温度约为840℃
3
C.520℃时,NH 的有效转化率约为66.7%
3
D.840℃后,NO的物质的量下降,可能是反应I平衡逆向移动所致
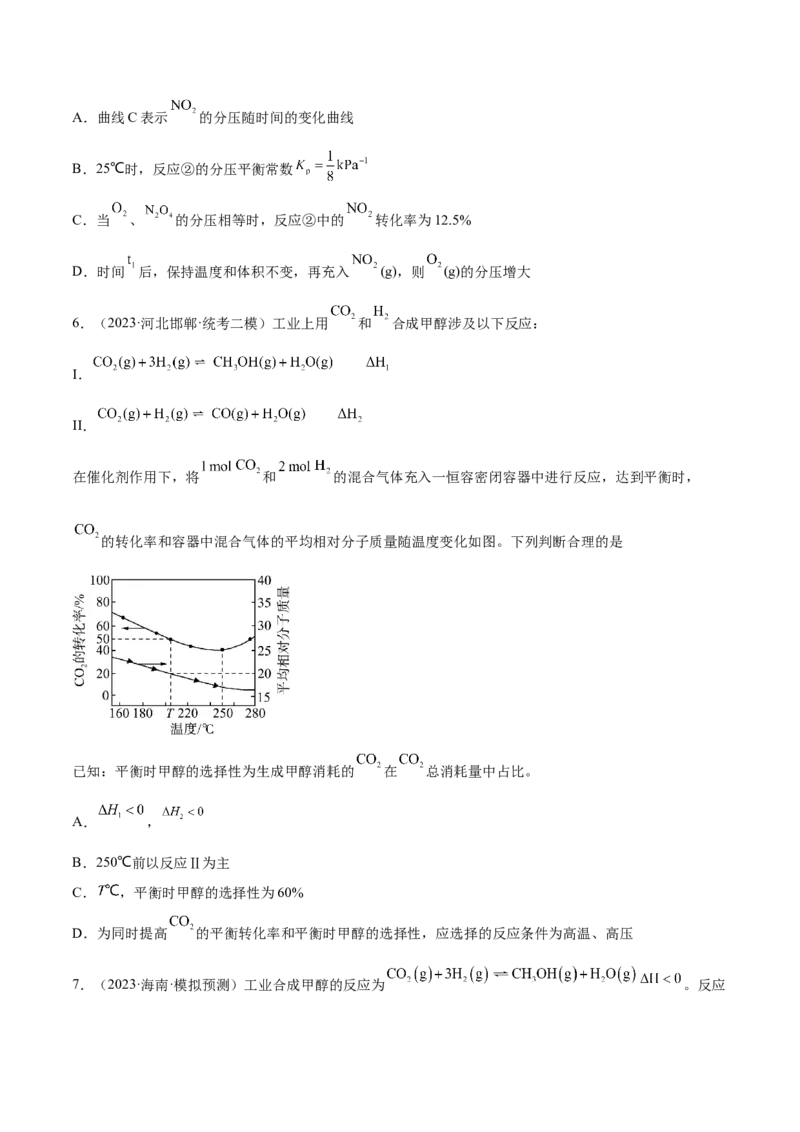
5.(2023·重庆·重庆市育才中学校考模拟预测)25℃时,向恒容容器中加入A发生反应:①
;② 。反应体系中 、 、 的分压随时间t的
变化曲线如图所示。下列说法正确的是A.曲线C表示 的分压随时间的变化曲线
B.25℃时,反应②的分压平衡常数
C.当 、 的分压相等时,反应②中的 转化率为12.5%
D.时间 后,保持温度和体积不变,再充入 (g),则 (g)的分压增大
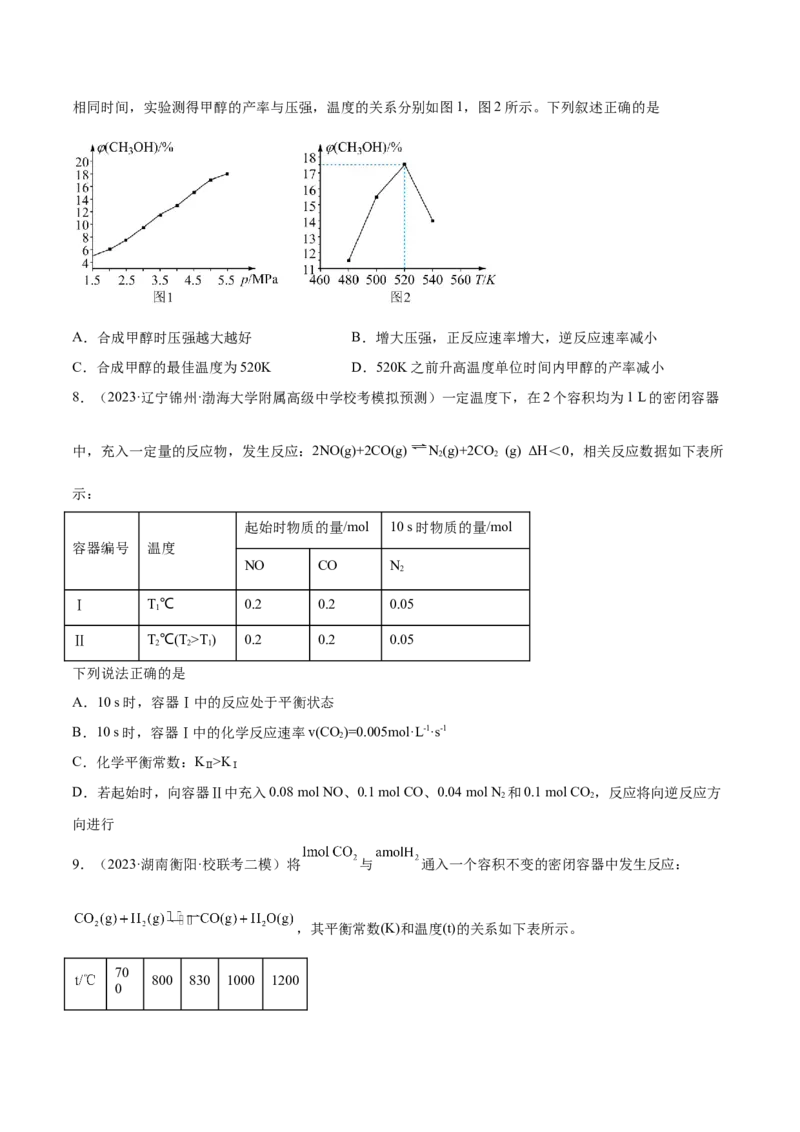
6.(2023·河北邯郸·统考二模)工业上用 和 合成甲醇涉及以下反应:
I.
II.
在催化剂作用下,将 和 的混合气体充入一恒容密闭容器中进行反应,达到平衡时,
的转化率和容器中混合气体的平均相对分子质量随温度变化如图。下列判断合理的是
已知:平衡时甲醇的选择性为生成甲醇消耗的 在 总消耗量中占比。
A. ,
B.250℃前以反应Ⅱ为主
C. ,平衡时甲醇的选择性为60%
D.为同时提高 的平衡转化率和平衡时甲醇的选择性,应选择的反应条件为高温、高压
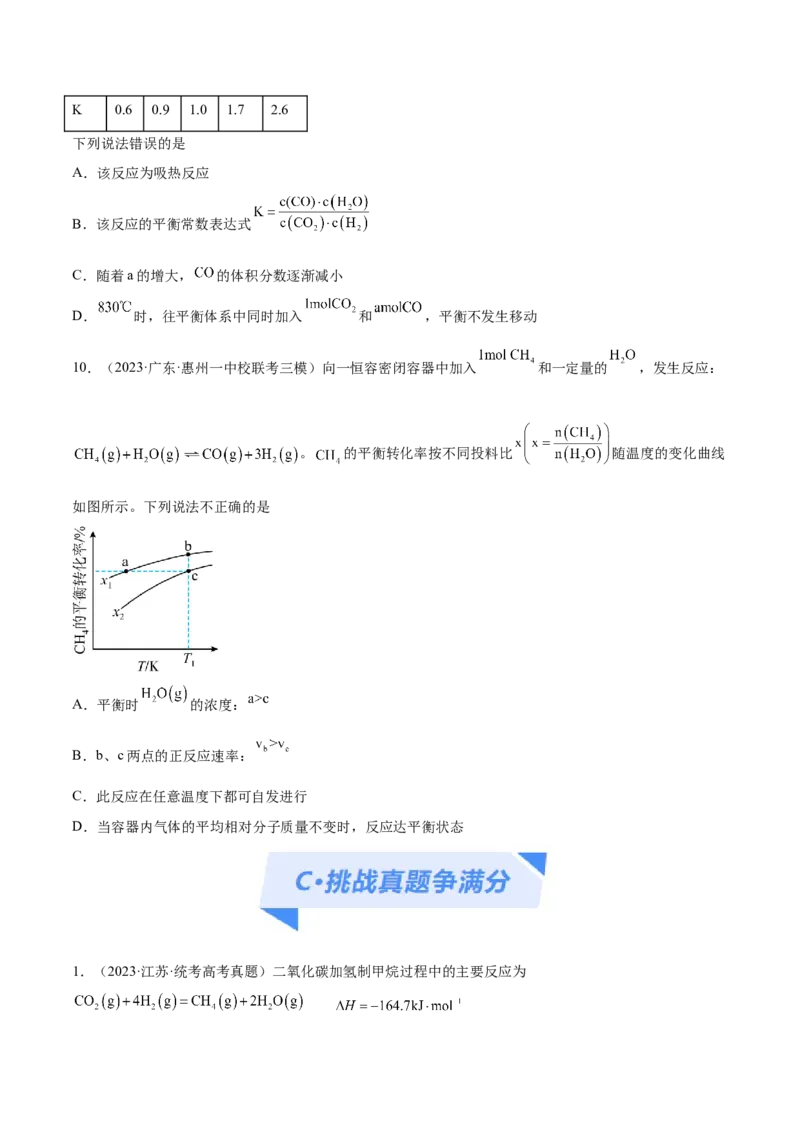
7.(2023·海南·模拟预测)工业合成甲醇的反应为 。反应相同时间,实验测得甲醇的产率与压强,温度的关系分别如图1,图2所示。下列叙述正确的是
A.合成甲醇时压强越大越好 B.增大压强,正反应速率增大,逆反应速率减小
C.合成甲醇的最佳温度为520K D.520K之前升高温度单位时间内甲醇的产率减小
8.(2023·辽宁锦州·渤海大学附属高级中学校考模拟预测)一定温度下,在2个容积均为1 L的密闭容器
中,充入一定量的反应物,发生反应:2NO(g)+2CO(g) N(g)+2CO (g) ΔH<0,相关反应数据如下表所
2 2
示:
起始时物质的量/mol 10 s时物质的量/mol
容器编号 温度
NO CO N
2
Ⅰ T℃ 0.2 0.2 0.05
1
Ⅱ T℃(T >T) 0.2 0.2 0.05
2 2 1
下列说法正确的是
A.10 s时,容器Ⅰ中的反应处于平衡状态
B.10 s时,容器Ⅰ中的化学反应速率v(CO)=0.005mol·L-1·s-1
2
C.化学平衡常数:K >K
Ⅱ Ⅰ
D.若起始时,向容器Ⅱ中充入0.08 mol NO、0.1 mol CO、0.04 mol N 和0.1 mol CO ,反应将向逆反应方
2 2
向进行
9.(2023·湖南衡阳·校联考二模)将 与 通入一个容积不变的密闭容器中发生反应:
,其平衡常数(K)和温度(t)的关系如下表所示。
70
800 830 1000 1200
0K 0.6 0.9 1.0 1.7 2.6
下列说法错误的是
A.该反应为吸热反应
B.该反应的平衡常数表达式
C.随着a的增大, 的体积分数逐渐减小
D. 时,往平衡体系中同时加入 和 ,平衡不发生移动
10.(2023·广东·惠州一中校联考三模)向一恒容密闭容器中加入 和一定量的 ,发生反应:
。 的平衡转化率按不同投料比 随温度的变化曲线
如图所示。下列说法不正确的是
A.平衡时 的浓度:
B.b、c两点的正反应速率:
C.此反应在任意温度下都可自发进行
D.当容器内气体的平均相对分子质量不变时,反应达平衡状态
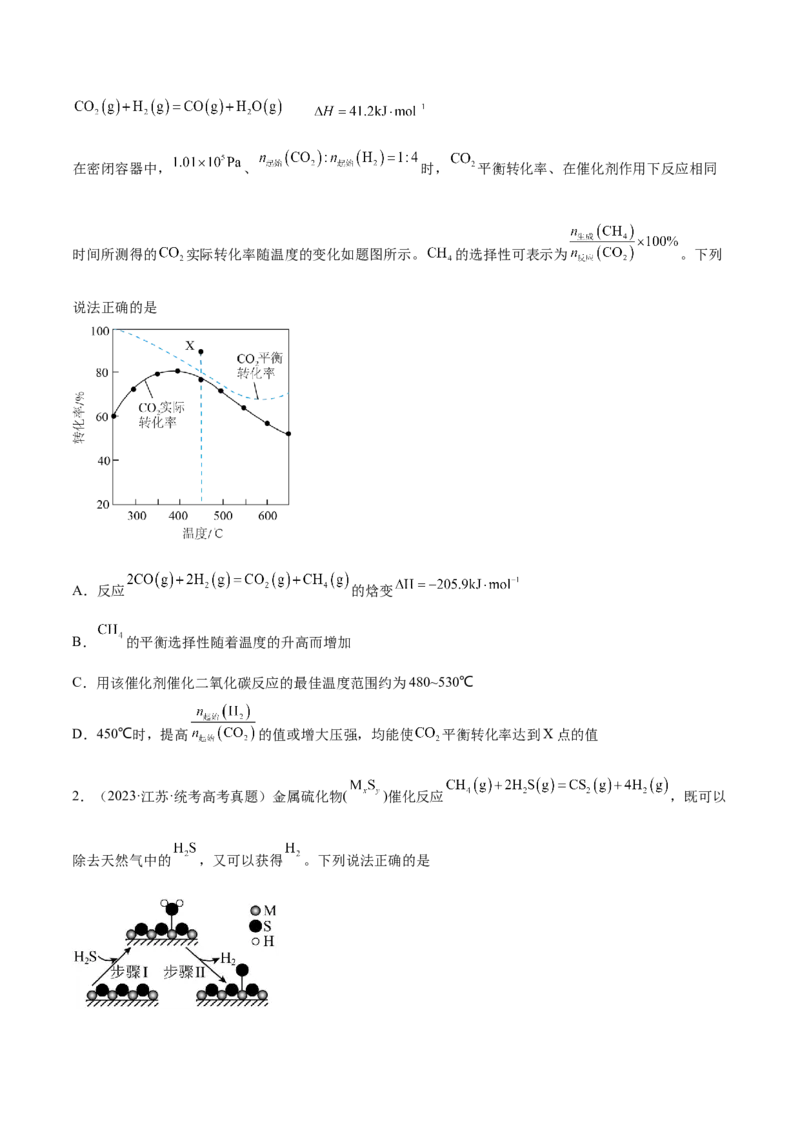
1.(2023·江苏·统考高考真题)二氧化碳加氢制甲烷过程中的主要反应为在密闭容器中, 、 时, 平衡转化率、在催化剂作用下反应相同
时间所测得的 实际转化率随温度的变化如题图所示。 的选择性可表示为 。下列
说法正确的是
A.反应 的焓变
B. 的平衡选择性随着温度的升高而增加
C.用该催化剂催化二氧化碳反应的最佳温度范围约为480~530℃
D.450℃时,提高 的值或增大压强,均能使 平衡转化率达到X点的值
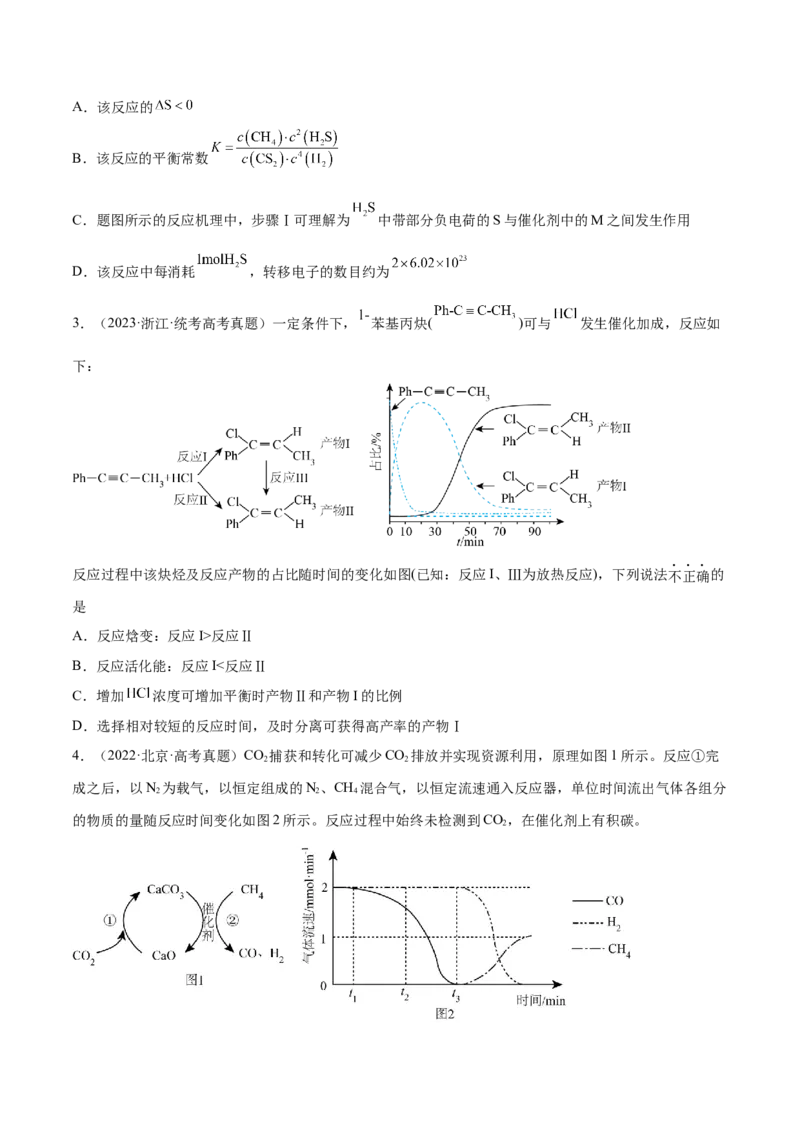
2.(2023·江苏·统考高考真题)金属硫化物( )催化反应 ,既可以
除去天然气中的 ,又可以获得 。下列说法正确的是A.该反应的
B.该反应的平衡常数
C.题图所示的反应机理中,步骤Ⅰ可理解为 中带部分负电荷的S与催化剂中的M之间发生作用
D.该反应中每消耗 ,转移电子的数目约为
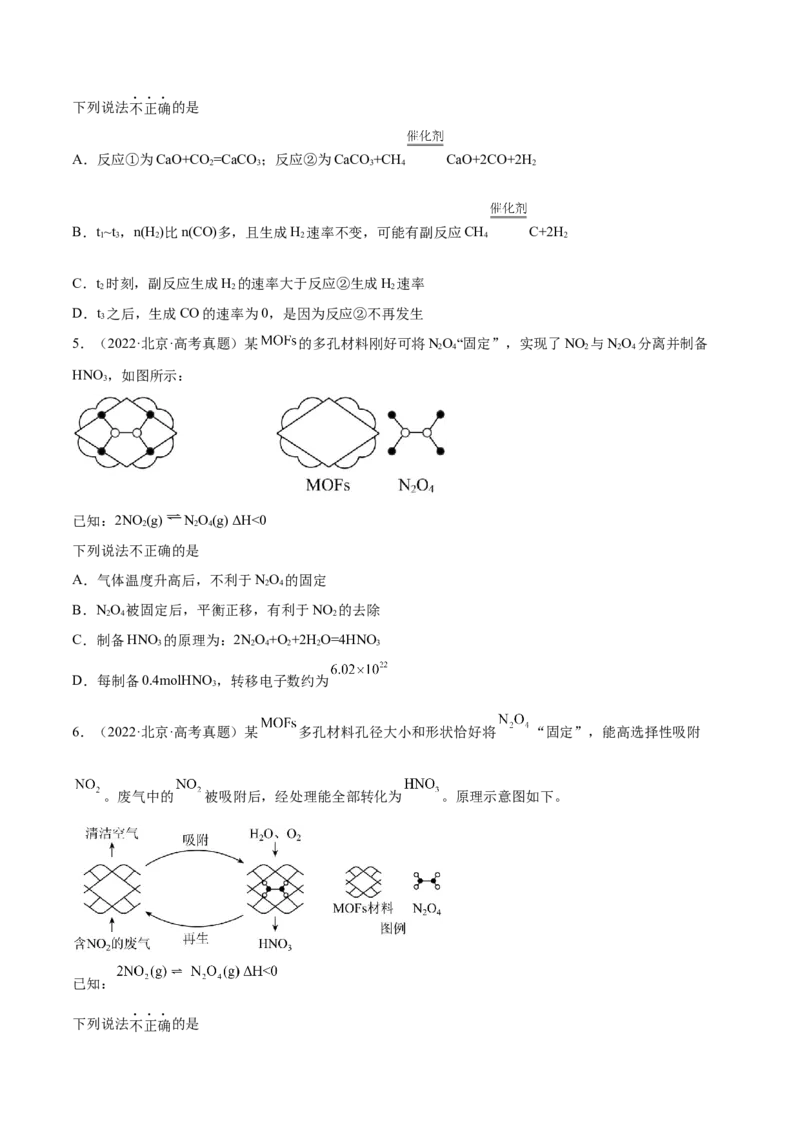
3.(2023·浙江·统考高考真题)一定条件下, 苯基丙炔( )可与 发生催化加成,反应如
下:
反应过程中该炔烃及反应产物的占比随时间的变化如图(已知:反应I、Ⅲ为放热反应),下列说法不正确的
是
A.反应焓变:反应I>反应Ⅱ
B.反应活化能:反应I<反应Ⅱ
C.增加 浓度可增加平衡时产物Ⅱ和产物I的比例
D.选择相对较短的反应时间,及时分离可获得高产率的产物Ⅰ
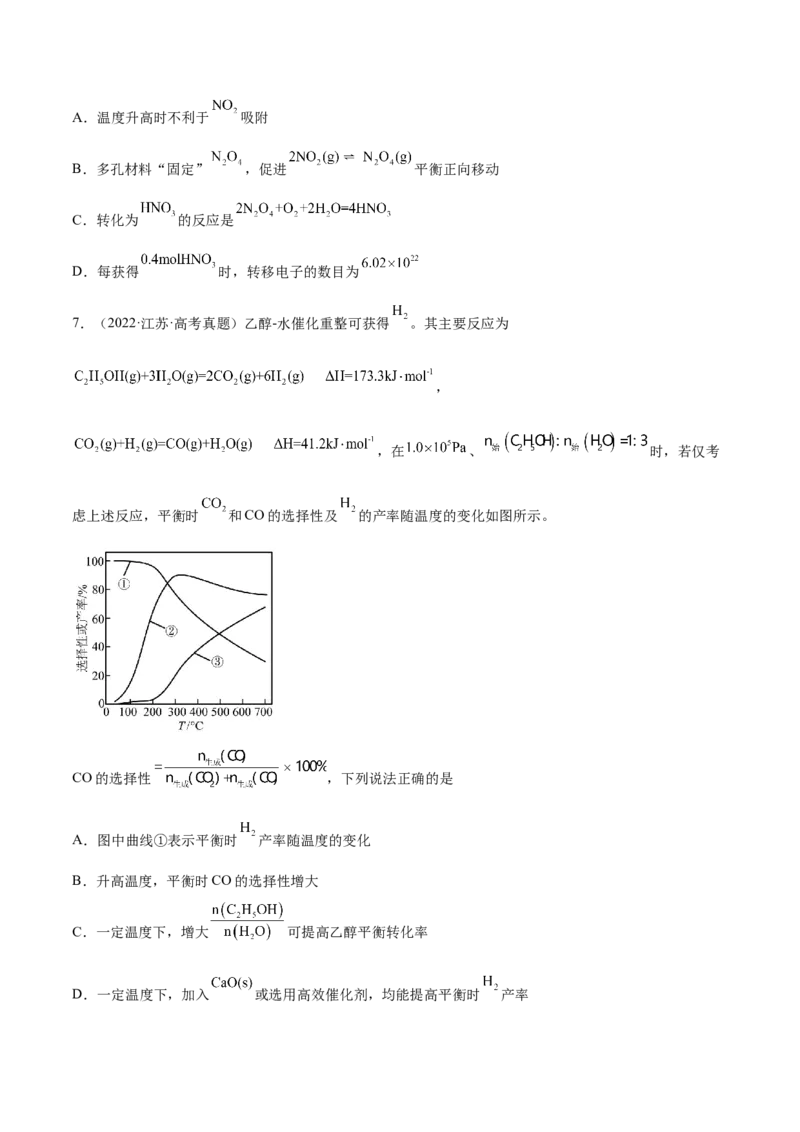
4.(2022·北京·高考真题)CO 捕获和转化可减少CO 排放并实现资源利用,原理如图1所示。反应①完
2 2
成之后,以N 为载气,以恒定组成的N、CH 混合气,以恒定流速通入反应器,单位时间流出气体各组分
2 2 4
的物质的量随反应时间变化如图2所示。反应过程中始终未检测到CO,在催化剂上有积碳。
2下列说法不正确的是
A.反应①为CaO+CO =CaCO ;反应②为CaCO +CH CaO+2CO+2H
2 3 3 4 2
B.t~t,n(H )比n(CO)多,且生成H 速率不变,可能有副反应CH C+2H
1 3 2 2 4 2
C.t 时刻,副反应生成H 的速率大于反应②生成H 速率
2 2 2
D.t 之后,生成CO的速率为0,是因为反应②不再发生
3
5.(2022·北京·高考真题)某 的多孔材料刚好可将NO“固定”,实现了NO 与NO 分离并制备
2 4 2 2 4
HNO,如图所示:
3
已知:2NO (g) NO(g) ΔH<0
2 2 4
下列说法不正确的是
A.气体温度升高后,不利于NO 的固定
2 4
B.NO 被固定后,平衡正移,有利于NO 的去除
2 4 2
C.制备HNO 的原理为:2NO+O +2H O=4HNO
3 2 4 2 2 3
D.每制备0.4molHNO ,转移电子数约为
3
6.(2022·北京·高考真题)某 多孔材料孔径大小和形状恰好将 “固定”,能高选择性吸附
。废气中的 被吸附后,经处理能全部转化为 。原理示意图如下。
已知:
下列说法不正确的是A.温度升高时不利于 吸附
B.多孔材料“固定” ,促进 平衡正向移动
C.转化为 的反应是
D.每获得 时,转移电子的数目为
7.(2022·江苏·高考真题)乙醇-水催化重整可获得 。其主要反应为
,
,在 、 时,若仅考
虑上述反应,平衡时 和CO的选择性及 的产率随温度的变化如图所示。
CO的选择性 ,下列说法正确的是
A.图中曲线①表示平衡时 产率随温度的变化
B.升高温度,平衡时CO的选择性增大
C.一定温度下,增大 可提高乙醇平衡转化率
D.一定温度下,加入 或选用高效催化剂,均能提高平衡时 产率8.(2022·海南·统考高考真题)某温度下,反应CH=CH (g)+HO(g) CHCHOH(g)在密闭容器中达到平
2 2 2 3 2
衡,下列说法正确的是
A.增大压强, ,平衡常数增大
B.加入催化剂,平衡时 的浓度增大
C.恒容下,充入一定量的 ,平衡向正反应方向移动
D.恒容下,充入一定量的 , 的平衡转化率增大
9.(2022·湖南·高考真题)甲基丙烯酸甲酯是合成有机玻璃的单体。
旧法合成的反应:
新法合成的反应:
下列说法错误的是(阿伏加德罗常数的值为 )
A. 的电子式为
B.新法没有副产物产生,原子利用率高
C. 的 溶液中 的微粒数小于
D. 的作用是降低反应的活化能,使活化分子数目增多,百分数不变
10.(2021·江苏·高考真题)NH 与O 作用分别生成N、NO、NO的反应均为放热反应。工业尾气中的
3 2 2 2
NH 可通过催化氧化为N 除去。将一定比例的NH 、O 和N 的混合气体以一定流速通过装有催化剂的反
3 2 3 2 2
应管,NH 的转化率、生成N 的选择性[ 100%]与温度的关系如图所示。
3 2下列说法正确的是
A.其他条件不变,升高温度,NH 的平衡转化率增大
3
B.其他条件不变,在175~300 ℃范围,随温度的升高,出口处N 和氮氧化物的量均不断增大
2
C.催化氧化除去尾气中的NH 应选择反应温度高于250 ℃
3
D.高效除去尾气中的NH ,需研发低温下NH 转化率高和N 选择性高的催化剂
3 3 2