文档内容
专题 12 物质结构与性质综合(题型突破)
(考试时间:75分钟 试卷满分:100分)
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一项是符合题目要求的)
1.含有N-、N+的材料Pb(N )、NAsF 可以用于炸药。下列说法正确的是( )
3 5 3 2 5 6
A.Pb属于d区元素
B.基态As原子的d轨道与p轨道上的电子数之比为3:2
C.N-的空间构型为直线形
3
D.基态F原子中,核外电子的空间运动状态有9种
【答案】C
【解析】A项,铅元素的原子序数为82,价电子排布式为6s26p2,处于元素周期表的p区,故A错误;
B项,砷元素的原子序数为33,电子排布式为1s22s22p63s23p63d104s24p3,则原子的d轨道与p轨道上的电子
数之比为10:15=2:3,故B错误;C项,等电子体具有相同的空间构型,N-离子与二氧化碳分子的原子
3
个数都为3、价电子数都为16,互为等电子体,二氧化碳的空间构型为直线形,则N-离子的空间构型为直
3
线形,故C正确;D项,核外电子的空间运动状态与原子轨道的数目相同,氟元素的原子序数为9,电子
排布式为1s22s22p5,氟原子的原子轨道数目为5,则核外电子的空间运动状态有5种,故D错误;故选C。
2.(2024·江苏苏州高三期中)Na、Mg、Al均为第三周期元素。下列说法正确的是( )
A.离子半径:r(Na+)<r(Mg2+)<r(Al3+) B.第一电离能:I(Na)> I (Mg)> I (Al)
1 1 1
C.还原性:Na>Mg>Al D.碱性:NaOH<Mg(OH) <Al(OH)
2 3
【答案】C
【解析】A项,三种离子核外电子排布相同半径随核电荷数增大而减小,故A错误;B项,同周期元
素第一电离能总体趋势:核电荷数越大,第一电离能越大,故B错误;C项,同周期元素,核电荷数越大
金属性越弱,对应单质还原性越弱,故C正确;D项,金属性Na>Mg>Al,其对应最高价氧化物水化物
碱性越弱,碱性:NaOH>Mg(OH) >Al(OH) ,故D错误;故选C。
2 3
3.(2024·山东淄博高三期中检测)下列关于物质结构和性质的说法正确的是( )
A.键角:HS>PH>SiH B.熔点:CsCl>KCl>NaCl
2 3 4
C.NO -、NO -的VSEPR模型相同 D.酸性:CHCOOH>CCl COOH>CF COOH
3 2 3 3 3
【答案】C
【解析】A项,孤电子对对成键电子对的作用力大于成键电子对之间的作用力,硫化氢含有两对孤电子对,磷化氢含有一个孤电子对,硅烷没有孤电子对,所以键角HS<PH <SiH,故A错误;B项,离子
2 3 4
化合物晶格能越大熔点越高,离子所带电荷相同原子离子半径越小晶格能越大熔点越高,熔点:CsCl<
KCl<NaCl,故B错误;C项,N-价层电子对数= 是sp3杂化, NO -价层电子对数=
3 2
是sp3杂化,所以它们VSEPR模型相同,故C正确;D项,H的电负性小于氯原子,氯
原子小于氟原子,电负性越强羟基上的氢原子越容易电离,酸性越强,所以酸性:CHCOOH<CCl COOH
3 3
<CFCOOH,故D错误;故选C。
3
4.实验室中利用CoCl 制取配合物[Co(NH )]Cl 的反应为2CoCl + 10NH + 2NH Cl+H O
2 3 6 3 2 3 4 2 2
=2[Co(NH)]Cl +2H O。下列叙述正确的是( )
3 6 3 2
A.Co2+的价电子排布图为 B.1 mol [Co(NH)]3+中含σ键为18 mol
3 6
C.HO 中氧原子采用sp3杂化 D.氨分子间存在氢键,因而NH 易溶于水
2 2 3
【答案】C
【解析】A项,Co原子核外有27个电子,基态Co原子的核外电子排布式为1s22s22p63s23p63d74s2,
Co2+的价电子排布式为3d7,价电子排布图为 ,A项错误;B项,1个
[Co(NH )]3+中1个Co3+与6个N原子形成6个配位键,配位键属于σ键,每个NH 中含3个N—Hσ键,
3 6 3
1mol[Co(NH)]3+中含有(6+6×3)mol=24molσ键,B项错误;C项,HO 的结构式为H—O—O—H,每个O
3 6 2 2
形成2个σ键,每个O还有两对孤电子对,即O原子的价层电子对数为4,O原子采用sp3杂化,C项正确;
D项,NH 易溶于水是由于NH 与HO分子间存在氢键、NH 分子和HO分子都是极性分子、NH 能与
3 3 2 3 2 3
HO反应,不是由于氨分子间存在氢键,D项错误;故选C。
2
5.(2024·山东菏泽高三期中)H、C、N、O、V(钒)五种元素形成的某分子结构如图所示,下列说法错
误是( )A.该分子中不存在氢键
B.B.基态V原子的价电子轨道表示式为
C.基态O原子中有3种能量不同的电子
D.该分子中的碳原子全部是sp2杂化
【答案】B
【解析】A项,该分子中不存在与电负性较大的原子相连的氢原子,分子中不存在氢键,故A正确;
B项,基态V原子价层电子轨道表示式为 ,故B错误;C项,基态O原子有1s、
2s、2p三种能量不同的电子,故C正确;D项,从结构来看,高分子中所有碳原子都是形成三个δ键,都
是sp2杂化,故D正确;故选B。
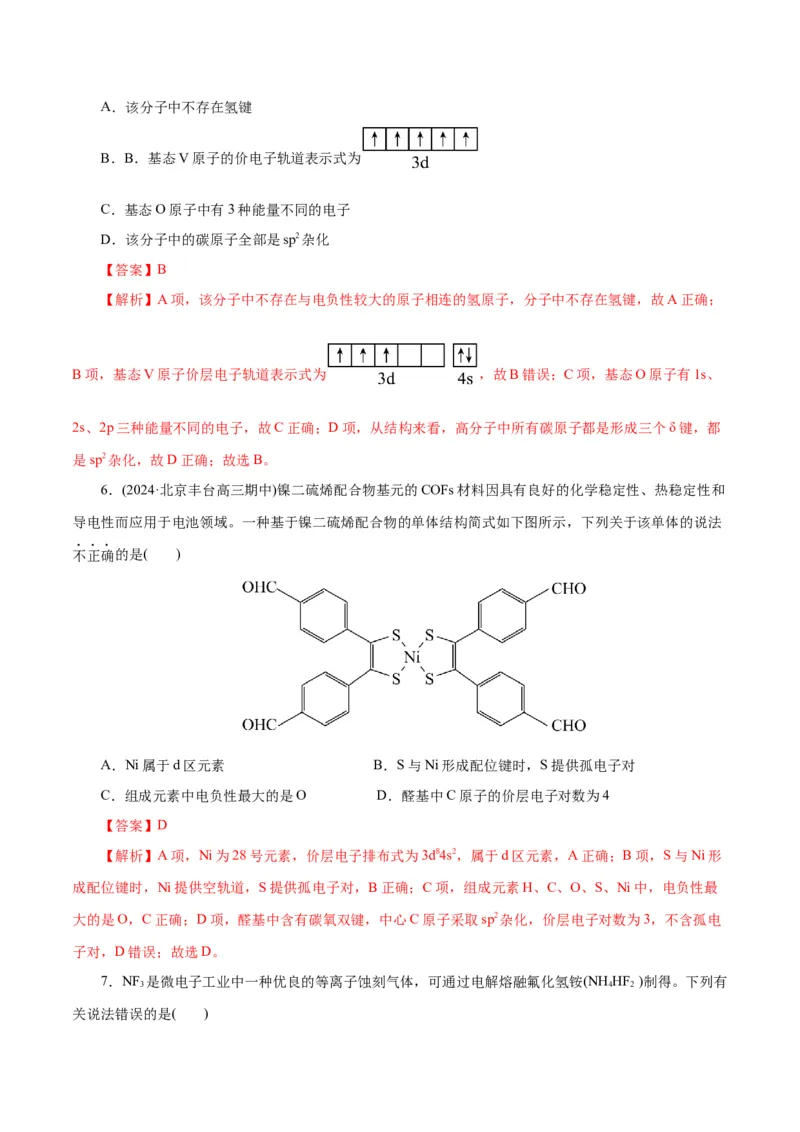
6.(2024·北京丰台高三期中)镍二硫烯配合物基元的COFs材料因具有良好的化学稳定性、热稳定性和
导电性而应用于电池领域。一种基于镍二硫烯配合物的单体结构简式如下图所示,下列关于该单体的说法
不正确的是( )
A.Ni属于d区元素 B.S与Ni形成配位键时,S提供孤电子对
C.组成元素中电负性最大的是O D.醛基中C原子的价层电子对数为4
【答案】D
【解析】A项,Ni为28号元素,价层电子排布式为3d84s2,属于d区元素,A正确;B项,S与Ni形
成配位键时,Ni提供空轨道,S提供孤电子对,B正确;C项,组成元素H、C、O、S、Ni中,电负性最
大的是O,C正确;D项,醛基中含有碳氧双键,中心C原子采取sp2杂化,价层电子对数为3,不含孤电
子对,D错误;故选D。
7.NF 是微电子工业中一种优良的等离子蚀刻气体,可通过电解熔融氟化氢铵(NH HF )制得。下列有
3 4 2
关说法错误的是( )A.NF 的空间构型为平面三角形
3
B.相关元素电负性由大到小的顺序为F>N>H
C.NF 和NH HF 中N原子的杂化方式均为sp3
3 4 2
D.NH HF 晶体中微粒间的作用有离子键、共价键、配位键、氢键
4 2
【答案】A
【解析】A项,NF 分子中N的周围形成3个σ键,孤电子对数= ,故其价层电子对为4,
3
故其的空间构型为三角锥形,A项错误;B项,同一周期从左往右元素的电负性依次增大,同一主族从上
往下依次减小,故相关元素电负性由大到小的顺序为,B项正确;C项,NF 分子中N的周围形成3个σ键,
3
孤电子对数= ,故其价层电子对为4,NH HF 中NH +周围有4个σ键,孤电子对数=
4 2 4
,故其价层电子对为4,NF 和NH HF 中N原子的杂化方式均为sp3,C项正确;D项,
3 4 2
NH HF 晶体中NH +与HF -微粒内存在共价键和配位键,微粒间存在离子键,且HF -与HF -微粒间存在氢
4 2 4 2 2 2
键,D项正确;故选A。
8.(2024·山东临沂市高三教学质量检测考试)六硝基合钴酸钾{K [Co(NO )]}是一种黄色难溶物。检验
3 2 6
K+或Co2+的反应原理如下:CoCl+NaNO +KCl+HCl→K[Co(NO )]↓+NO↑+NaCl+H O(未配平)。下列说法
2 2 3 2 6 2
错误的是( )
A.将上述反应设计成原电池,正极产物为NO
B.配合物K[Co(NO )]中配位原子是氧原子
3 2 6
C.基态Co原子的价层电子中,成对电子数与未成对电子数之比为2:1
D.上述反应的离子方程式为CoCl+7NO -+3K++2H+=K[Co(NO )]↓+NO↑+HO
2 2 3 2 6 2
【答案】B
【解析】A.原电池正极得到电子,CoCl+NaNO +KCl+HCl→K[Co(NO )]↓+NO↑+NaCl+H O,该反应
2 2 3 2 6 2
中亚硝酸根得到电子生成NO,设计成原电池,正极产物为NO,故A正确;B项,氮原子电负性小于氧原
子,配合物K[Co(NO )]中配位原子是氮原子,Co提供空轨道,故B错误;C项,基态Co原子的价层电
3 2 6
子中,价层电子排布图为: ,成对电子数与未成对电子数之比为2:1,故C正确;D
项,上述反应的离子方程式为CoCl+7NO -+3K++2H+=K[Co(NO )]↓+NO↑+HO,故D正确;故选B。
2 2 3 2 6 29.(2024·安徽六安一中高三质检)在《是真的吗》节目《盐里面加进了亚铁氰化钾》案例中:有一位
老教授食用了添加抗结剂亚铁氰化钾的食盐后,肾脏受到严重危害。亚铁氰化钾K[Fe(CN)]俗名黄血盐,
4 6
制备方法为Fe+6HCN+2KCO= K[Fe(CN)]+H ↑+2CO ↑+2H O。设N 为阿伏加德罗常数的数值,下列说法
2 3 4 6 2 2 2 A
正确的是( )
A.27gHCN分子中含有π键数目为N
A
B.配合物K[Fe(CN)]的中心离子价电子排布式为3d6,该中心离子的配位原子数为12
4 6
C.每生成1 CO 时,反应过程中转移电子数目为4N
2 A
D.1L1 的KCO 溶液,阳离子数目大于2N
2 3 A
【答案】D
【解析】A项,27gHCN的物质的量为1mol,其结构式为:H-C≡N,则27gHCN分子中含有π键数目为
2N ,故A错误;B项,配合物K[Fe(CN)]的中心离子为Fe2+,其价电子排布式为3d6,该中心离子的配体
A 4 6
为CN-,配位数为6,故B错误;C项,该反应中,铁由0价升高到+2价,两个+1价氢变为0价,则转移2
个电子,故每生成1molCO 时,反应过程中转移电子数目为N ,故C错误;D项,1L 1 mol•L-1 KCO 溶
2 A 2 3
液中,阳离子有K+和H+,其中钾离子的物质的量为2mol,则溶液中阳离子数目大于2N ,故D正确;故
A
选D。
10.(2024·江苏南京金陵中学高三期中)NH 是一种重要的化工原料,向NiSO 溶液中通NH 可制
3 4 3
[Ni(NH )]SO ,肼(N H)是一种火箭燃料推进剂,其燃烧热为624 kJ·mol-1,下列说法正确的是( )
3 6 4 2 4
A.[Ni(NH )]SO 、NH 中的 键角:前者大于后者
3 6 4 3
B.基态 核外电子排布式为 [Ar]3d64s2
C.表示肼燃烧热的热化学方程式:NH (g)+ O(g) N (g)+ 2HO(g) ΔH=-624 kJ·mol-1
2 4 2 2 2
D.[Ni(NH )]SO 中含有化学键有离子键、共价键、氢键、配位键
3 6 4
【答案】A
【解析】A项,NH 分子中N原子有一对孤电子对,[Ni(NH )]SO 中N原子孤电子对于Ni形成配位键,
3 3 6 4
斥力减小,键角增大,所以键角:前者小于后者,A正确;B项,Ni原子序数为28,则基态核外电子排布
式为 [Ar]3d8,B错误;C项,表示肼燃烧热的热化学方程式:NH (g)+ O (g) N (g)+ 2H O(g)
2 4 2 2 2
ΔH=-624 kJ·mol-1,C错误;D项,[Ni(NH )]SO 中含有化学键有离子键、共价键、配位键,但无
3 6 4
氢键,D错误;故选A。
11.(2024·江苏泰州高三期中)海洋是一个巨大的化学资源宝库,含有80多种元素,其中含有较高的钠
和氯元素。化学家常用廉价氯化钠为原料制备纯碱,也可用于电解方法获得金属钠、氯气、氢气等,并进一步将其转化为生产、生活和科学实验中用途更为广泛的新物质,如ClO 、NaO、NaClO等。下列说法
2 2 2
正确的是( )
A.键角:ClO ->ClO -
3 4
B.酸性:CClCOOH>CHCOOH
3 3
C.侯氏制碱的反应:2NaCl+2NH +CO +H O=NaCO+2NHCl
3 2 2 2 3 4
D.电解饱和食盐水时,若两极共产生气体 (标准状况下),转移电子数为
【答案】B
【解析】A项,ClO -中价电子对数为4,但有一对孤电子对,ClO -中价电子对数为4,没有孤电子对,
3 4
所以键角应为:ClO -<ClO -,A项错误;B项,氯原子是吸电子基团,会增加羧基中氧氢键的极性,使酸
3 4
性增强,B项正确;C项,侯氏制碱法第一步反应应生成碳酸氢钠和氯化铵,C项错误;D项,电解饱和
食盐水时,两极分别产生氢气和氯气,且产生气体体积比为1:1,所以每极各有11.2L气体(标准状况下),
即0.5mol气体,每生成1mol气体转移2mol电子,所以转移的电子数应为1mol,D项错误;故选B。
12.铜有Cu(Ⅰ)和Cu(Ⅱ)两种离子,铜的离子是人体内多种酶的辅因子,人工模拟酶是当前研究的热
点。铜的离子可与多种配体形成配位化合物,有一种配离子结构如图。下列有关说法中错误的是( )
A.该配离子中所含基态铜离子的价层电子排布图为
B.该离子的配体中,N原子采用了sp2和sp3两种杂化方式
C.该配离子中铜的配位数和所含配位键的数目均为4
D.从核外电子排布角度分析,稳定性:Cu(Ⅰ)<Cu(Ⅱ)
【答案】D
【解析】A项,该配离子中铜离子为+1价,所以价层电子排布图为 ,A正确;B项,
该离子的配体中,N原子采用了sp2和sp3两种杂化方式,B正确;C项,由图可知铜离子配位数和每个离子所含配位键数均为4,C正确;D项,由于Cu(Ⅰ)的3d轨道全充满,所以更稳定,故D错误。故选D。
13.某种硫化橡胶的部分结构如图所示。下列说法错误的是( )
A.图中元素位于s区和p区的种数之比为1:2
B.基态硫原子和碳原子最高能级电子云轮廓图均为哑铃形
C.图中的硫原子和碳原子共有两种杂化方式
D.图示结构中含有σ键、π键和氢键等作用力
【答案】D
【解析】A项,位于s区的元素有H元素,位于p区的元素有C、S元素,则图中元素位于s区和p区
的种数之比为1:2,A正确;B项,p能级的电子电子云轮廓图为哑铃形,s能级的电子电子云轮廓图为球
形,基态S原子最高能级为3p能级、基态C原子最高能级为2p能级,所以电子云轮廓图都是哑铃形,B
正确;C项,连接双键的碳原子采用sp2杂化,价层电子对数是4的碳原子、硫原子采用sp3杂化,所以
C、S原子共有两种杂化方式,C正确;D项,图中不存在氢键,存在σ键、π键,D错误;故选D。
14.照相底片定影并回收定影液硫代硫酸钠和银,经历如下过程,下列说法不正确的是( )
A.Na[Ag(S O)]晶体中所含的作用力只有离子键、配位键
3 2 3 2
B.SO2-与SO 2-是等电子体,结构相似,相当于SO 2-中O被一个S原子替换
2 3 4 4
C.该过程中与Ag+结合能力:S2->SO2->Br---
2 3
D.副产物SO 的键角小于 的原因:SO 分子中S的孤电子对对成键电子对的排斥作用使键角变小
2 2
【答案】A
【解析】A项,Na[Ag(S O)]晶体中所含的作用力含有离子键、配位键、共价键,A错误;B项,等
3 2 3 2
电子体是指价电子数和原子数相同的分子、离子或原子团;SO2-与SO 2-是等电子体,结构相似,相当于
2 3 4
SO 2-中O被一个S原子替换,B正确;C项,反应中溴化银转化为[Ag(S O)]3+、[Ag(S O)]3+转化AgS,
4 2 3 2 2 3 2 2
故该过程中与Ag+结合能力:S2->SO2->Br--,C正确;D项,SO 分子中S含有孤电子对,副产物SO 的
2 3 2 2
键角小于 的原因是SO 分子中S的孤电子对对成键电子对的排斥作用使键角变小,D正确;故选A。
2
15.(2024·重庆八中质检)前四周期元素M、Q、W、X、Y、Z原子序数依次增大。M的单质常用作保护气,W是元素周期表中电负性最大的元素,X与Y形成化合物的化学式为YX且其焰色试验为紫色(透过
蓝色钴玻璃),Z的原子序数为28,Q和Y形成的一种化合物甲的晶胞在xy平面、xz平面、yz平面上的投
影图甲所示。W、Y、Z三种元素组成的化合物乙的晶体结构如图乙所示。
下列关于化合物乙的说法不正确的是( )
A.该晶体中Z的化合价为+2
B.与Z等距最近的W有6个
C.图中A、B原子间的距离为
D.图中B的原子分数坐标可表示为
【答案】D
【解析】根据题干信息分析,M为N元素,W为F元素,由于前四周期元素M、Q、W、X、Y、Z原
子序数依次增大,因此Q为O元素,X与Y形成化合物的化学式为YX且其焰色试验为紫色(透过蓝色钴
玻璃),故Y为K元素,X为Cl元素,Z的原子序数为28,Z为Ni元素;根据均摊法 ,
, ,则化合物乙的化学式为KNiF。A项,根据以上分析化合物乙的化学式为
2 4
KNiF,因此Ni的化合价为+2,A正确; B项,以体心的Ni原子分析,看图可知与Ni等距最近的W原
2 4
子有6个,B正确;C项,根据图中信息可知,图中A、B原子间的距离为
pm,C正确; D项,由于 ,因此图中B的原子分数坐标不能表示为 ,D错误;故选D。
二、非选择题(本题包括4小题,共55分)
16.(12分)含氮化合物在生活中占有重要地位。请回答:
(1)CN-可通过配位键与Co3+形成[Co(CN) ]3-。形成该配合物时,基态 的价层电子发生重排提供两
6
个空轨道,则重排后的Co3+价电子排布图为___________;CO 的金属配合物也已经制备成功,但为数不多,
2
如[Ni(PH )CO],已知该配合物的配位数与[[Ni(CO) ]]的配位数相同,测得其中存在两种碳氧键的键长,
3 2 2 4
一个为0.117mm,另一个为0.122nm。请画出[Ni(PH )CO]的结构示意图:___________。
3 2 2
(2)NF 和NH 是常见含氮化合物,其VSEPR构型均为___________,其中二者相比较,键角更大的是
3 3
___________。
(3)N、P、As同属于ⅤA族,下列说法正确的是___________。
A.原子半径:r(N) >r(P) >r(As)且电负性:N>P>As
B.N、P、As的最高价氧化物水化物的酸性依次减弱
C.简单氢化物的还原性:NH >PH >AsH
3 3 3
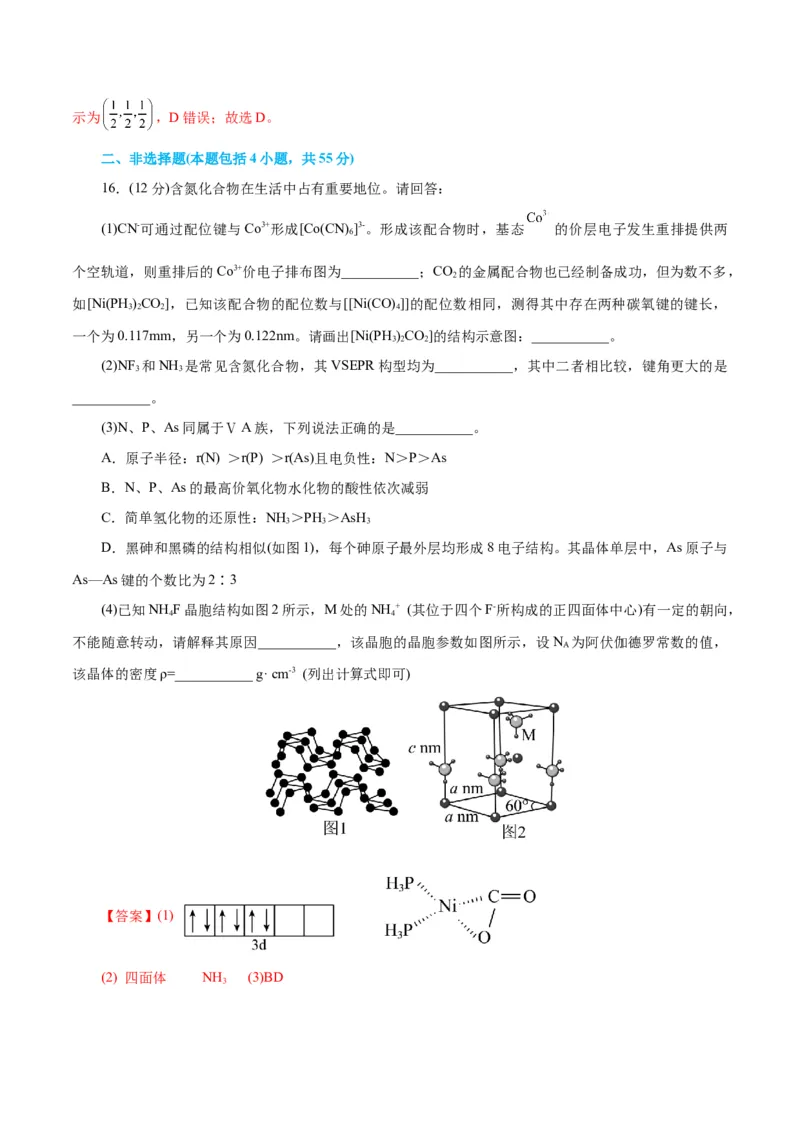
D.黑砷和黑磷的结构相似(如图1),每个砷原子最外层均形成8电子结构。其晶体单层中,As原子与
As—As键的个数比为2∶3
(4)已知NH F晶胞结构如图2所示,M处的NH + (其位于四个F-所构成的正四面体中心)有一定的朝向,
4 4
不能随意转动,请解释其原因___________,该晶胞的晶胞参数如图所示,设N 为阿伏伽德罗常数的值,
A
该晶体的密度ρ=___________ g· cm-3 (列出计算式即可)
【答案】(1)
(2) 四面体 NH (3)BD
3(4) NH+与F-形成N—H…F氢键,氢键具有方向性;
4
【解析】(1)基态Co3+的价层电子排布式为3d6,CN-可通过配位键与Co3+形成[Co(CN) ]3-,形成配合物
6
时,基态 Co3+的价层电子发生重排提供两个空轨道,则 重排后的 Co3+价电子排布图为
;[Ni(CO) ]的配位数为4,[Ni(PH )CO]的配位数与[Ni(CO) ]的配位数相同,
4 3 2 2 4
[Ni(PH )CO]的配位数也为4,测得其中存在两种碳氧键的键长,一个为0.117mm,另一个为0.122nm,说
3 2 2
明Ni与2个PH 分子中的P原子、CO 分子中的碳原子和 1个O原子形成配位键,其结构示意图为:
3 2
;(2)NF 和NH 分子中中心N原子的σ键电子对数都为3、孤电子对数都为1,价
3 3
层电子对数都为4,VSEPR模型都为四面体形;空间构型都为三角锥形,由于电负性 F>N>H,则NF 分
3
子中成键电子对离 N原子更远,两个N—F键之间的斥力减小,故 NF 中的键角更小,键角更大的是
3
NH ;(3)A项,同主族从上到下原子半径逐渐增大、电负性逐渐减小,原子半径:r(N) <r(P) <r(As),电
3
负性:N>P>As,A项错误;B项,同主族从上到下元素的非金属性逐渐减弱,最高价氧化物水化物的酸
性逐渐减弱,N、P、As的最高价氧化物水化物的酸性逐渐减弱,B项正确;C项,同主族从上到下元素的
非金属性逐渐减弱,简单氢化物的还原性逐渐增强,即简单氢化物的还原性:NH <PH <AsH ,C项错误;
3 3 3
D项,黑砷和黑磷的结构相似,每个砷原子最外层均形成8电子结构,由图可知,晶体单层中,每个As原
子形成3个As—As键,以As—As键形成六元环,每个As原子被3个六元环共有,每个As—As键被2个
六元环共有,则晶体单层中As原子与As—As键的个数比为2∶3,D项正确;故选BD。(4)M处的NH +
4
(其位于四个F-所构成的正四面体中心)有一定的朝向,不能随意转动,其原因是:NH +与F-形成N—H…F
4
氢键,氢键具有方向性;由图可知晶胞中含F-、NH +的个数都为2,晶胞的质量为 ,晶胞的体积为
4
(a×10-7cm)×(a×10-7cm)×(c×10-7cm)= a2c×10-21cm3 , 该 晶 体 的 密 度 ρ= ÷( a2c×10-21cm3)=g/cm3。
17.(13分)中国科学院朱庆山团队研究六方相砷化镍(NiAs)型到正交相磷化锰(MnP)型结构转变,实现
了对锂硫催化剂的精确设计。回答下列问题:
(1)Li、P、S三种元素中,电负性最小的是___________。第三周期元素中第一电离能比P大的元素有
___________种。
(2)基态S原子核外有___________个电子自旋状态相同。基态As原子的电子排布式为___________。
(3)PH 、AsH 中沸点较高的是___________,其主要原因是___________。
3 3
(4)Mn的一种配合物化学式为[Mn(CO) (CHCN)],该配合物中锰原子的配位数为___________。
5 3
(5)CH CN中C原子的杂化类型为___________。
3
(6)等物质的量的CHCN和CO中,π键数目之比___________。
3
(7)NiAs的一种晶胞结构如图所示。若阿伏加德罗常数的值为N ,晶体的密度为ρ g/cm3,则该晶胞中
A
最近的砷原子之间的距离为 ___________pm。
【答案】(1) Li 2 (2) 9或7 [Ar]3d104s24p3
(3) AsH 两者均为分子晶体,AsH 相对分子质量大,范德华力强,沸点高
3 3
(4)6 (5)sp3、sp (6)1∶1 (7)
【解析】(1)Li、P、S中,Li为金属元素,容易失去电子,电负性最小;一般情况下同一周期的元素,
原子序数越大,元素的第一电离能也越大,但第 VA的元素由于其处于p轨道的半充满的稳定状态,其第
一电离能大于同周期相邻元素,第一电离能P>S,故第三周期元素中第一电离能大于磷的元素有 Cl、Ar;
所以第三周期元素中第一电离能比P大的元素有2种;(2)基态S元素电子排布式为1s22s22p3s23p4;有7个
或9个电子自旋状态相同;基态As原子的电子排布式为[Ar]3d104s24p3;(3)PH 、AsH 均为分子晶体,相
3 3
对分子质量大,范德华力强,沸点高所以沸点较高的是 AsH ;(4)Mn 的一种配合物化学式为
3
[Mn(CO) (CHCN)],该配合物中与锰原子的配位有CO和CHCN,配位数为6;(5)CH CN中有两个C原子,
5 3 3 3分别连接有4个和2个 键,杂化类型为sp3、sp;(6)CH CN和CO均含有2个π键,等物质的量的CHCN
3 3
和CO中,π键数目之比1:1;(7)该晶胞中含有Ni3+个数为 ,含有As3-为4;即含有4个
NiAs,其质量为 ,设其棱长为acm,所以 ,As3-位于其八分之一晶胞的
中 心 , 两 个 As3- 之 间 的 距 离 相 当 于 面 对 角 线 长 度 的 一 半 ; 所 以 两 个 As3- 之 间 为
。
18.(15分)022年诺贝尔化学奖授予美国科学家卡罗琳·贝尔托齐、卡尔·巴里·沙普利斯和丹麦科学家
莫滕·梅尔达尔,以表彰他们在发展点击化学和生物正交化学方面的贡献。点击化学的代表反应为 Cu催化
的叠氮一炔基Husigen环加成反应,NaN₃、SO₂F₂、FSO₂N₂等均是点击化学中常用的无机试剂。回答下列
问题:
(1)氮原子激发态的电子排布式有___________,其中能量最高的是_______(填标号)。
a.1s²2s²2p²3p¹ b.1s²2s²2p4 c.1s²2s²2p²3s¹ d.1s²2s²2p³
(2)N、O、F的第一电离能最小的是___________,SO₂F₂分子结构如图1所示,已知键角α为124°,β
为96°,则α>β的原因主要是___________。
(3)叠氮化物能与Fe³⁺、Cu²⁺及Co³⁺等形成配合物,如:[Co(N₃)(NH₃)₅]SO₄,该配合物中Co³⁺的配位数
为___________。HN 分子的空间结构如图2所示(图中键长单位为10⁻10m)。
3
已知:①典型N-N、N=N和N≡N的键长分别为1.40×10⁻10m、1.20×10⁻10m和1.09×10⁻10m;②甲酸根的
两个碳氧键键长相同,处于典型碳氧单键键长和碳氧双键键长之间,其结构可以用两个极端电子式()的平均杂化体来表示。试画出HN 分子的两个极端电子式___________;
3
“ ”中N原子的杂化方式为___________。
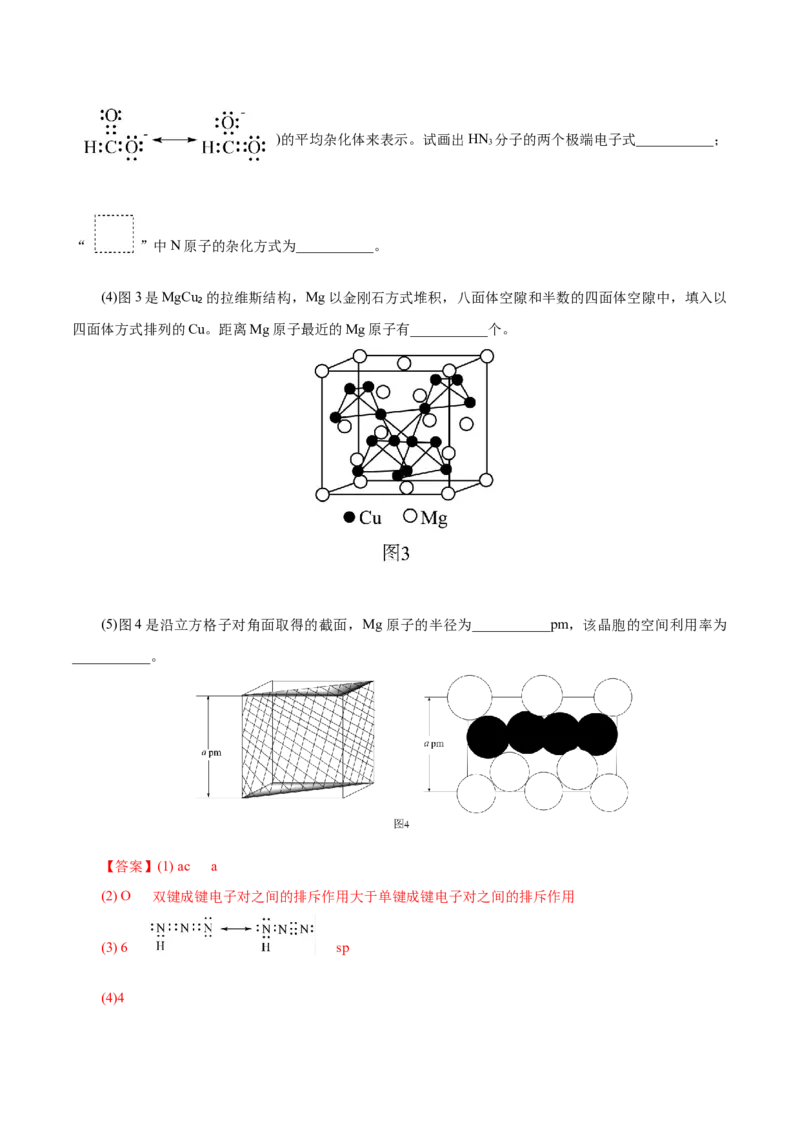
(4)图3是MgCu₂的拉维斯结构,Mg以金刚石方式堆积,八面体空隙和半数的四面体空隙中,填入以
四面体方式排列的Cu。距离Mg原子最近的Mg原子有___________个。
(5)图4是沿立方格子对角面取得的截面,Mg原子的半径为___________pm,该晶胞的空间利用率为
___________。
【答案】(1) ac a
(2) O 双键成键电子对之间的排斥作用大于单键成键电子对之间的排斥作用
(3) 6 sp
(4)4(5)
【解析】(1)激发态是基态原子吸收能量,较低能级的电子跃迁到更高能级而来,跃迁的能级越高、数
量越多,能量越高;基态N原子的电子排布式为1s²2s²2p³,1s²2s²2p²3p¹是2p能级电子跃迁到3p能级,
1s²2s²2p²3s¹是2p能级电子跃迁到3s能级,因此处于激发态的是ac,由于3p能级的能量高于3s能级,因
此a中激发态能量更高。(2)同周期主族元素第一电离能从左到右增大,但是由于Ⅱ A、ⅤA族元素核外电
子最高能级分别处于全满和半满状态,比较稳定,第一电离能高于相邻元素,即第一电离能F>N>O,最
小的为O;由图示结构式可知,S、O之前为共价双键,S、F之间为共价单键,双键成键电子对之间的排
斥作用大于单键成键电子对之间的排斥作用,因此键角α>β。(3)由[Co(N₃)(NH₃)₅]SO₄化学式可知,内界中
有5个NH 和1个N-,故其配位数为6;参考甲酸根的两个极端电子式可知书写规律为尽可能的让其中一
3 3
个成键最多或最少,电子偏向其中一极,则为两种极端形式,参考这个规律,可让 HN 中最右侧原子最多
3
成三键和最少成双键,其余氮按照八电子理论补齐化学键来表示,两种极端电子式为
;由图二结构式可知,三个氮原子呈直线型,则中间氮原子的杂化方式为
sp杂化。(4)以上表面面心处的Mg为例,距离其最近的Mg为位于下方四面体空隙中的两个Mg以及相应
的上方四面体空隙中的两个,共4个。(5)由晶胞结构及截面图可知,Mg原子之间的最近距离为晶胞体对
角线的四分之一,即为两个半径的长度,换言之,Mg原子半径为体对角线的八分之一,晶胞参数为a,则
Mg的半径为 ,铜原子半径为面对角线的八分之一,即 ,晶胞体积为a3,Mg原子个数为8,体积
为 ,Cu原子个数为16,体积为 ,空间利用率为( + )÷a3= 。
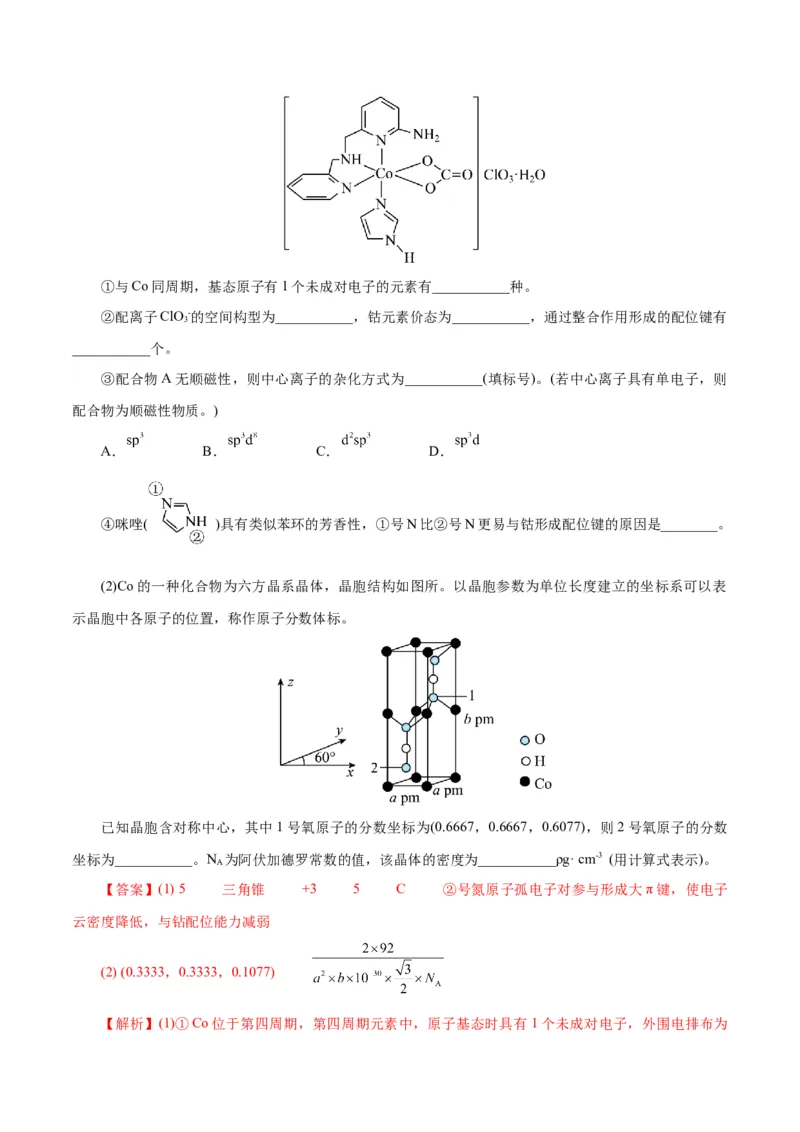
19.(15分)Co元素的某些化合物在电池、光电材料、催化剂等方面有广泛应用。回答下列问题:
(1)一种具有光催化作用的配合物A结构简式如图所示:①与Co同周期,基态原子有1个未成对电子的元素有___________种。
②配离子ClO -的空间构型为___________,钴元素价态为___________,通过整合作用形成的配位键有
3
___________个。
③配合物A无顺磁性,则中心离子的杂化方式为___________(填标号)。(若中心离子具有单电子,则
配合物为顺磁性物质。)
A. B. C. D.
④咪唑( )具有类似苯环的芳香性,①号N比②号N更易与钴形成配位键的原因是________。
(2)Co的一种化合物为六方晶系晶体,晶胞结构如图所。以晶胞参数为单位长度建立的坐标系可以表
示晶胞中各原子的位置,称作原子分数体标。
已知晶胞含对称中心,其中1号氧原子的分数坐标为(0.6667,0.6667,0.6077),则2号氧原子的分数
坐标为___________。N 为阿伏加德罗常数的值,该晶体的密度为___________ρg· cm-3 (用计算式表示)。
A
【答案】(1) 5 三角锥 +3 5 C ②号氮原子孤电子对参与形成大π键,使电子
云密度降低,与钻配位能力减弱
(2) (0.3333,0.3333,0.1077)
【解析】(1)①Co位于第四周期,第四周期元素中,原子基态时具有1个未成对电子,外围电排布为4s1或 4s24p1或 4s24p5、3dl04s1、3d14s2,共有 5 种元素;②配离子 ClO -中心原子价层电子对数为 3+
3
=4,且含有1个孤电子对,空间构型为三角锥形,由配合物A结构简式可知Co原子和N原
子形成4个配位键,和O原子形成2个共价键,ClO -带1个单位负电荷,则钴元素价态为+3价,整合是指
3
具有以下两个或多个配位原子的多齿配体与同一金属进行离子相互之间没有形成螯合环,通过整合作用形
成的配位键有5个;③由配合物A结构简式可知Co原子形成6个配位键,Co原子的价层电子对数为6,
杂化方式为 ,故选C;④②号氮原子孤电子对参与形成大π键,使电子云密度降低,与钻配位能力减
弱。(2)根据1号氧原子的分数坐标为(0.6667,0.6667,0.6077),2号氧原子、1号氧原子和晶胞含对称中心,
根据对称关系可知2号氧原子的分数坐标为(0.3333,0.3333,0.1077),晶胞中O原子个数为4,H原子个
数为2,Co原子个数为8 +4 =2,则该晶体的密度为 = 。