文档内容
合格演练测评(四)
(离子反应)
姓名: 班级: 正确率:
题号 1 2 3 4 5 6 7 8 9 10
答案
题号 11 12 13 14 15 16 17 18 19 20
答案
一、单项选择题
1.物质的量浓度都为0.1 mol·L-1的下列物质的水溶液,酸性最强的是( )
A.CHCHOH B.HSO
3 2 2 4
C.CHCOOH D.NaCl
3
解析:A项,CHCHOH溶液呈中性,不符合题意;B项,硫酸为强酸,溶于水后可完全电离,1个硫酸可电
3 2
离出2个氢离子,所以0.1 mol·L-1硫酸中氢离子浓度是0.2 mol·L-1,酸性最强,符合题意;C项,醋酸为
弱酸,溶于水后部分电离,所以醋酸溶液中氢离子浓度小于0.1 mol·L-1,不符合题意;D项,氯化钠溶液呈
中性,不符合题意。
答案:B
2.下列物质可以导电的是( )
A.甲苯 B.NaCl 固体
C.氯化钠溶液 D.酒精
答案:C
3.常温下溶液pH大于7的是( )
A.氯化钠溶液 B.稀硫酸
C.醋酸溶液 D.纯碱溶液
答案:D
4.下列离子在含有0.1 mol·L-1 SO的溶液中不能大量存在的是( )A.Al3+ B.Cu2+
C.Fe3+ D.Ba2+
解析:Ba2+与SO能产生白色沉淀BaSO,故不能大量共存。
4
答案:D
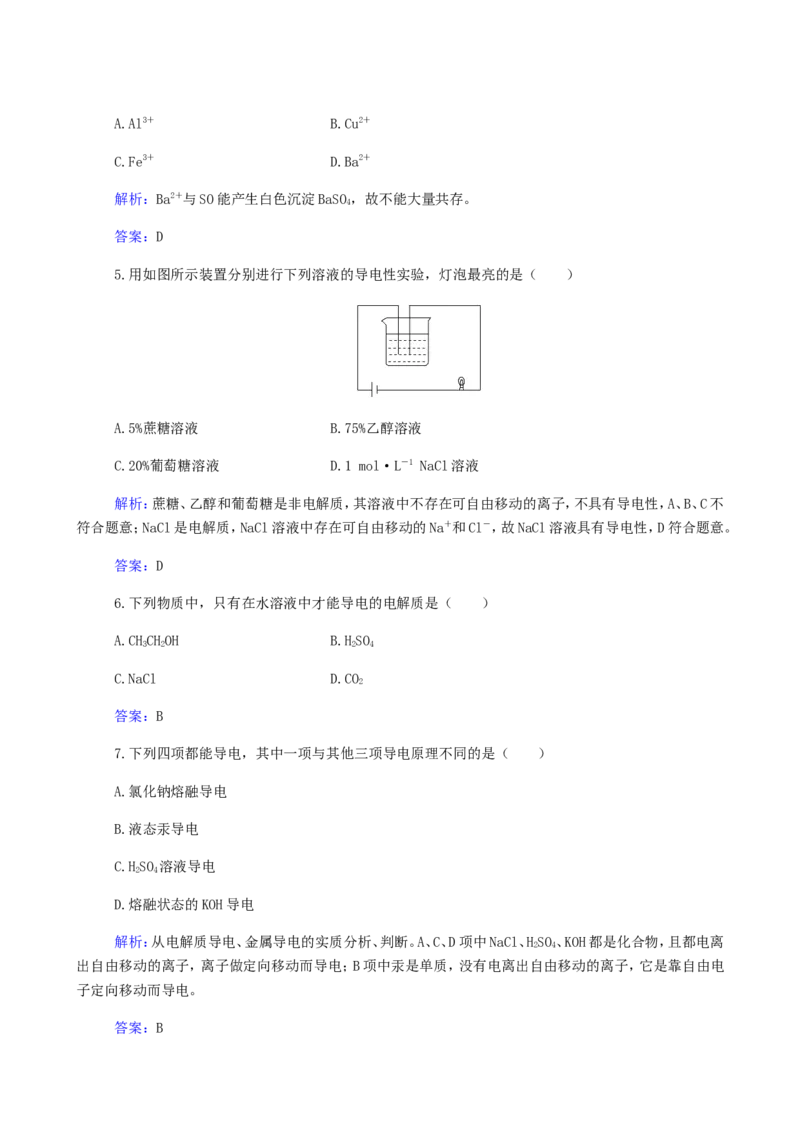
5.用如图所示装置分别进行下列溶液的导电性实验,灯泡最亮的是( )
A.5%蔗糖溶液 B.75%乙醇溶液
C.20%葡萄糖溶液 D.1 mol·L-1 NaCl溶液
解析:蔗糖、乙醇和葡萄糖是非电解质,其溶液中不存在可自由移动的离子,不具有导电性,A、B、C不
符合题意;NaCl是电解质,NaCl溶液中存在可自由移动的Na+和Cl-,故NaCl溶液具有导电性,D符合题意。
答案:D
6.下列物质中,只有在水溶液中才能导电的电解质是( )
A.CHCHOH B.HSO
3 2 2 4
C.NaCl D.CO
2
答案:B
7.下列四项都能导电,其中一项与其他三项导电原理不同的是( )
A.氯化钠熔融导电
B.液态汞导电
C.HSO 溶液导电
2 4
D.熔融状态的KOH导电
解析:从电解质导电、金属导电的实质分析、判断。A、C、D项中NaCl、HSO、KOH都是化合物,且都电离
2 4
出自由移动的离子,离子做定向移动而导电;B项中汞是单质,没有电离出自由移动的离子,它是靠自由电
子定向移动而导电。
答案:B8.能够用来鉴别BaCl、NaCl、NaCO 三种物质的试剂是( )
2 2 3
A.AgNO 溶液 B.稀硫酸
3
C.稀盐酸 D.稀硝酸
答案:B
9.在水溶液中能够大量共存的是( )
A.Na+、Cl-、NO B.Ag+、Cl-、NO
C.NH、OH-、SO D.Na+、Fe2+、OH-
答案:A
10.向下列各物质的水溶液中滴加稀硫酸或MgCl 溶液时,均有白色沉淀生成的是( )
2
A.BaCl B.KOH
2
C.NaCO D.Ba(OH)
2 3 2
解析:D项,中滴加稀硫酸有BaSO 沉淀生成,滴加MgCl 溶液有Mg(OH) 沉淀生成。
4 2 2
答案:D
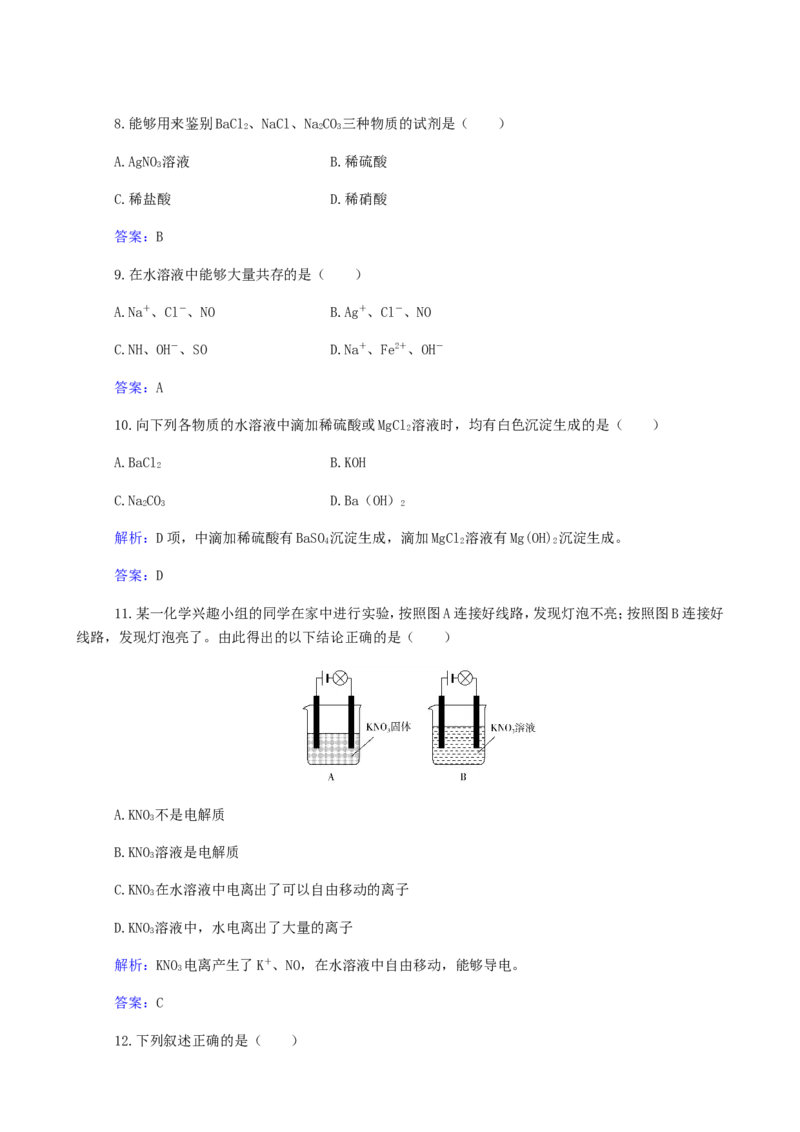
11.某一化学兴趣小组的同学在家中进行实验,按照图A连接好线路,发现灯泡不亮;按照图B连接好
线路,发现灯泡亮了。由此得出的以下结论正确的是( )
A.KNO 不是电解质
3
B.KNO 溶液是电解质
3
C.KNO 在水溶液中电离出了可以自由移动的离子
3
D.KNO 溶液中,水电离出了大量的离子
3
解析:KNO 电离产生了K+、NO,在水溶液中自由移动,能够导电。
3
答案:C
12.下列叙述正确的是( )A.凡是盐,在离子方程式中都要以离子形式表示
B.离子互换反应总是向着溶液中反应物离子浓度减小的方向进行
C.酸碱中和反应的实质是H+与OH-结合生成水,故所有的酸碱中和反应的离子方程式都可写成H++
OH-===HO的形式
2
D.复分解反应必须同时具备离子反应发生的三个条件才能进行
解析:只有可溶且易电离的盐在离子方程式中才可以写成离子形式;离子反应的实质是离子的浓度或
数目减小;H++OH-===HO表示的是可溶性强酸(或强酸酸式盐)与可溶性强碱反应生成水和可溶性盐的一
2
类反应;复分解反应只要满足三个条件之一即可发生。
答案:B
13.下列反应的离子方程式能用H++OH-===HO来表示的是( )
2
A.氢氧化镁和稀盐酸反应
B.澄清石灰水和稀硝酸反应
C.Ba(OH) 溶液滴入稀硫酸中
2
D.二氧化碳通入澄清石灰水中
答案:B
14.下列反应的离子方程式正确的是( )
A.向NaOH溶液中加入铝粉来制备H:Al+2OH-+2HO===
2 2
AlO+3H↑
2
B.用胃舒平治疗胃酸过多:Al(OH)+3H+===Al3++3HO
3 2
C.实验室用氢氧化钠溶液吸收Cl:Cl+OH-===Cl-+ClO-+
2 2
HO
2
D.碳酸钡溶于醋酸中:BaCO+2H+===Ba++HO+CO↑
3 2 2
解析:Al与NaOH反应的离子方程式:2Al+2OH-+2HO=== 2AlO+3H↑,A项错误;用胃舒平治疗胃酸
2 2
过多的离子反应为Al(OH)+3H+===Al3++3HO,B项正确;C项,离子方程式中电荷不守恒,原子个数不守恒,
3 2
应改为Cl+2OH-===Cl-+ClO-+HO,错误;醋酸为弱酸,离子方程式中不能拆为离子形式,应改为BaCO+
2 2 3
2CHCOOH===Ba2++HO+CO↑+2CHCOO-,D项错误。
3 2 2 3
答案:B15.下列离子方程式正确的是( )
A.金属钠与水反应:Na+HO===Na++OH-+H↑
2 2
B.将铁投入氯化铁溶液中:Fe+Fe3+===2Fe2+
C.铝和稀硫酸反应:2Al+6H+===2Al3++3H↑
2
D.氢氧化钡溶液与稀硫酸溶液混合:Ba2++SO===BaSO↓
4
解析:A项,H原子个数不守恒;B项,电荷不守恒;D项,不符合反应事实(应有HO生成)。
2
答案:C
16.下列离子反应方程式,书写正确的是( )
A.向碳酸钠溶液中加盐酸:CO+2H+===HO+CO↑
2 2
B.向稀硫酸溶液中投入铁粉:2Fe+6H+===2Fe3++3H↑
2
C.向盐酸中投入碳酸钙:CO+2H+===HO+CO↑
2 2
D.氢氧化钡溶液中加入硫酸:H++OH-===HO
2
答案:A
17.在下列离子反应中,不能用离子方程式:Ba2++SO=== BaSO↓来表示的是( )
4
A.Ba(NO)+HSO===BaSO↓+2HNO
3 2 2 4 4 3
B.Ba(OH)+NaSO===BaSO↓+2NaOH
2 2 4 4
C.Ba(OH)+HSO===BaSO↓+2HO
2 2 4 4 2
D.BaCl+HSO===BaSO↓+2HCl
2 2 4 4
答案:C
18.水溶液中能大量共存的一组离子是( )
A.NH、Ba2+、Br-、CO
B.Cl-、SO、Fe2+、H+
C.K+、Na+、SO、MnO
D.Na+、H+、NO、HCO
答案:C19.某溶液中存在大量的H+、Cl-、SO,该溶液中还可能大量存在的是( )
A.HCO B.Ba2+
C.Al3+ D.Ag+
解析:C HCO和H+反应生成二氧化碳,故A错误;Ba2+和SO反应生成硫酸钡沉淀,故B错误;Ag+和Cl
-反应生成氯化银沉淀,故D错误。
答案:C
20.在碱性强的溶液中,能大量共存的无色溶液是( )
A.Na+、Cu2+、Cl-、SO
B.Mg2+、Ba2+、NO、Cl-
C.K+、Na+、SO、CO
D.K+、Ag+、HCO、Br-
解析:C碱性强的溶液中肯定存在大量的OH-。A项中Cu2+有色且能与OH-反应生成沉淀;B项中Mg2+
能与OH-反应生成沉淀;D项中Ag+、HCO- 均可与OH-反应。
3
答案:C
二、非选择题
21.描述下列反应的现象并写出反应的离子方程式。
(1)向FeCl 溶液中滴加NaOH溶液,现象:___________
3
_____________________________________________________,
离子方程式:________________________________________。
(2)向NaHCO 溶液中滴加稀HSO,现象:___________
3 2 4
____________________________________________________,
离子方程式:________________________________________。
(3)稀HNO 和Ba(OH) 溶液混合,现象:___________
3 2
_____________________________________________________,
离子方程式:________________________________________。
解析:从离子反应的现象和本质(离子浓度的变化)去分析。答案:(1)生成红褐色沉淀
Fe3++3OH-===Fe(OH)↓
3
(2)生成无色无味气体
HCO+H+ ===CO↑+HO
2 2
(3)观察不到明显现象
H++OH-===HO
2
22.写出下列物质在水溶液中的电离方程式:
(1)①Ba(OH):_________________________________。
2
②KHSO:_________________________________________。
4
③HNO:___________________________________________。
3
④NaCO:__________________________________________。
2 3
(2)上述物质按酸、碱、盐分类,其中,属于酸的是 ,属于碱的是 ,属于盐的是
。
答案:(1)①Ba(OH)===Ba2++2OH-
2
②KHSO===K++H++SO
4
③HNO===H++NO
3
④NaCO===2Na++CO
2 3
(2)③ ① ②④
23.有一包白色固体,可能含有NaCO、KNO、KCl、BaCl 和CuSO,按下列步骤做实验。
2 3 3 2 4
①将该固体溶于水得无色溶液。
②向溶液中加入AgNO 溶液,得到白色沉淀,再加稀HNO,白色沉淀部分溶解并有气泡产生,把气体通
3 3
入澄清石灰水,石灰水变浑浊。
根据上述现象判断:
(1)一定存在的物质是_______________________________。
(2)一定不存在的物质是___________________________。
(3)可能存在的物质是_______________________________。解析:无色溶液可排除CuSO 固体;通过实验②白色沉淀部分溶解并有气泡产生可确定溶液中含有CO
4
和Cl-,同时排除Ba2+的存在。由此肯定固体中含有NaCO 和KCl,不存在BaCl 固体。
2 3 2
答案:(1)NaCO、KCl
2 3
(2)BaCl、CuSO
2 4
(3)KNO
3