文档内容
专题 41 工艺流程
(建议完成时间:45分钟 实际完成时间:_______分钟)
1.(2023·陕西渭南·统考模拟预测)铍及其化合物用途广泛,以绿柱石(主要组成是 ,
还含少量铁元素)和方解石(主要成分是 )为原料生产铍的工艺流程如图所示:
已知:铝铵矾 在不同温度下的溶解度如下表:
温度/℃ 0 10 20 30 40 60
溶解度/g 2.10 5.00 7.74 10.9 14.9 26.7
回答下列问题:
(1)绿柱石中Be元素的化合价为 。“熔炼”中生成气体的电子式为 。
(2)滤渣1中除 及难溶性硅酸盐外,还含有 (填化学式);“转化”后,要得到铝铵矾晶体,在中学实
验室中可采取的操作是 、 、过滤、洗涤、干燥。
(3)加 时,溶液中发生反应的离子方程式是 。
(4)“沉铍”时,若选用氢氧化钠溶液可能造成的影响是 ,所得母液中的主要溶质可返回到 工序循环利
用。
(5)“沉铍”时加入氨水调节pH至7.5,列式并计算说明此时溶液中的铍离子是否沉淀完全 。(已知:该条
件下, ;离子浓度 时,可认为离子沉淀完全)
(6)无水 可用作聚合反应的催化剂。 、 与足量C在600~800℃制备 的化学方程式为 。
【答案】(1)+2
(2)CaSO 蒸发浓缩 冷却结晶
4
(3)2Fe2++H O+2H+=2Fe3++2H O
2 2 2
(4)Be(OH) 能溶于过量的NaOH溶液中[或Be(OH) +2OH-= + 2H O] 转化
2 2 2
(5)c(Be2+)= =1.6×10-9<10-5 mol·L-1, 所以Be2+沉淀完全
(6)BeO+Cl +C CO+BeCl
2 2
【分析】以绿柱石(主要组成是3BeO·Al O·6SiO,还含少量铁元素)和方解石(主要成分是CaCO )为原料生
2 3 2 3
1
原创精品资源学科网独家享有版权,侵权必究!产铍,将绿柱石和方解石在高温下熔炼,再硫酸酸浸生成硫酸铝、硫酸铍和硅酸,滤渣1中除SiO 及难溶
2
性硅酸盐外,还含有CaSO,滤液滴加硫酸铵生成铝铵矾晶体,过滤后向滤液中加入HO 溶液,将Fe2+氧
4 2 2
化为Fe3+,调pH使Fe3+转化为氢氧化铁,过滤后滴加氨水生成氢氧化铍,除杂煅烧生成氧化铍,最终得到
单质铍。
【解析】(1)3BeO·Al O·6SiO 种O是-2价,根据化合价代数和为零可知,Be的化合价为+2,“熔炼”
2 3 2
中CaCO 受热分解产生CO 气体,CO 的电子式为 。
3 2 2
(2)由分析可知,滤渣1中除SiO 及难溶性硅酸盐外,还含有CaSO;“转化”后,要得到铝铵矾晶体,
2 4
在中学实验室中可采取的操作是蒸发浓缩、冷却结晶、过滤、 洗涤、干燥。
(3)向滤液中加入HO 溶液的目的是:将Fe2+氧化为Fe3+,发生反应的离子方程式是:2Fe2++H O+2H+=
2 2 2 2
2Fe3++2H O。
2
(4)Be和Al的化学性质有相似的地方,“沉铍”时,若选用氢氧化钠溶液可能造成的影响是Be(OH) 能
2
溶于过量的NaOH溶液中[或Be(OH) +2OH-= + 2H O],所得母液中含有(NH )SO ,可返回到转化
2 2 4 2 4
工序循环利用。
(5)“沉铍”时加入氨水调节pH至7.5,溶液中c(OH-)= ,溶液中c(Be2+)=
=1.6×10-9<10-5 mol·L-1, 所以Be2+沉淀完全。
(6)BeO、 与足量C在600~800°C生成BeCl 同时生成CO,化学方程式为BeO+Cl +C
2 2
CO+BeCl 。
2
2.(2023·福建泉州·福建省永春第一中学校考模拟预测)工厂的含砷废水必须经过一定的处理。 某厂用
某含砷废水(含HAsO、HSO 、及少量Fe3+、Cu2+、Bi2+ )提取三氧化二砷(俗称砒霜,分子式:As O)的流
2 2 4 2 3
程如图:
已知:K [Fe(OH) ]=2.8 ×10-39,K [Cu(OH) ]=2.2 ×10-22,K [Bi(OH) ]=4.4 ×10-31。
sp 3 sp 2 sp 3
回答下列问题:
(1)滤渣a的成分是 (写化学式)。
(2)“沉淀”时,CuSO 溶液必须过量的原因是 。
4
(3)写出“还原”时Cu(AsO ) 与HO、SO 发生反应的化学方程式: 。
2 2 2 2
(4)红色还原渣(不溶于水)“氧化”时反应的离子方程式为 。
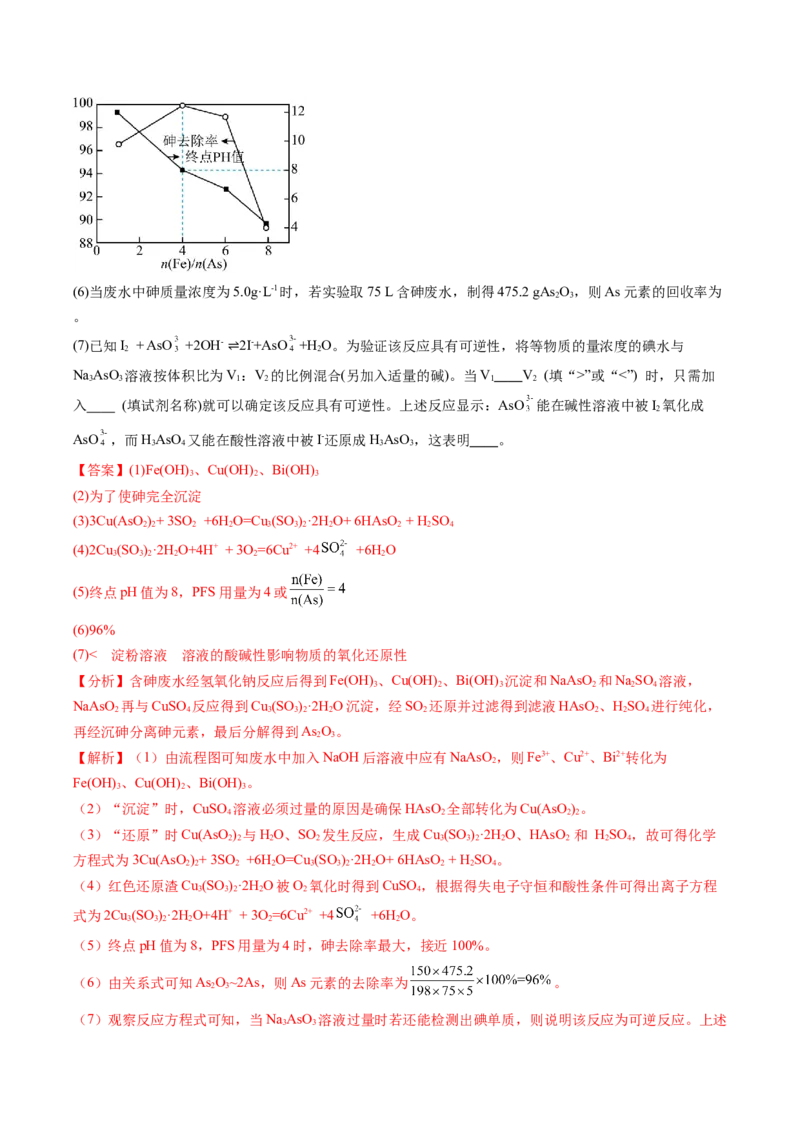
(5)“沉砷”后废水中残留的砷可用PFS(聚铁)进一步去除,用石灰乳调节废水的pH值,通入空气,PFS用
量[以 表示]、终点pH值与砷去除率的关系如图所示。PFS除砷的最佳条件是 。(6)当废水中砷质量浓度为5.0g·L-1时,若实验取75 L含砷废水,制得475.2 gAs O,则As元素的回收率为
2 3
。
(7)已知I + AsO +2OH- 2I-+AsO +H O。为验证该反应具有可逆性,将等物质的量浓度的碘水与
2 2
Na
3
AsO
3
溶液按体积比为V⇌1 :V
2
的比例混合(另加入适量的碱)。当V
1
V
2
(填“>”或“<”) 时,只需加
入 (填试剂名称)就可以确定该反应具有可逆性。上述反应显示:AsO 能在碱性溶液中被I 氧化成
2
AsO ,而HAsO 又能在酸性溶液中被I-还原成HAsO ,这表明 。
3 4 3 3
【答案】(1)Fe(OH) 、Cu(OH) 、Bi(OH)
3 2 3
(2)为了使砷完全沉淀
(3)3Cu(AsO )+ 3SO +6H O=Cu (SO )·2H O+ 6HAsO + H SO
2 2 2 2 3 3 2 2 2 2 4
(4)2Cu (SO )·2H O+4H+ + 3O =6Cu2+ +4 +6H O
3 3 2 2 2 2
(5)终点pH值为8,PFS用量为4或
(6)96%
(7)< 淀粉溶液 溶液的酸碱性影响物质的氧化还原性
【分析】含砷废水经氢氧化钠反应后得到Fe(OH) 、Cu(OH) 、Bi(OH) 沉淀和NaAsO 和NaSO 溶液,
3 2 3 2 2 4
NaAsO 再与CuSO 反应得到Cu (SO )·2H O沉淀,经SO 还原并过滤得到滤液HAsO、HSO 进行纯化,
2 4 3 3 2 2 2 2 2 4
再经沉砷分离砷元素,最后分解得到As O。
2 3
【解析】(1)由流程图可知废水中加入NaOH后溶液中应有NaAsO,则Fe3+、Cu2+、Bi2+转化为
2
Fe(OH) 、Cu(OH) 、Bi(OH) 。
3 2 3
(2)“沉淀”时,CuSO 溶液必须过量的原因是确保HAsO 全部转化为Cu(AsO )。
4 2 2 2
(3)“还原”时Cu(AsO ) 与HO、SO 发生反应,生成Cu (SO )·2H O、HAsO 和 HSO ,故可得化学
2 2 2 2 3 3 2 2 2 2 4
方程式为3Cu(AsO )+ 3SO +6H O=Cu (SO )·2H O+ 6HAsO + H SO 。
2 2 2 2 3 3 2 2 2 2 4
(4)红色还原渣Cu (SO )·2H O被O 氧化时得到CuSO ,根据得失电子守恒和酸性条件可得出离子方程
3 3 2 2 2 4
式为2Cu (SO )·2H O+4H+ + 3O =6Cu2+ +4 +6H O。
3 3 2 2 2 2
(5)终点pH值为8,PFS用量为4时,砷去除率最大,接近100%。
(6)由关系式可知As O~2As,则As元素的去除率为 。
2 3
(7)观察反应方程式可知,当NaAsO 溶液过量时若还能检测出碘单质,则说明该反应为可逆反应。上述
3 3反应显示:AsO 能在碱性溶液中被I 氧化成AsO ,而HAsO 又能在酸性溶液中被I-还原成HAsO ,这
2 3 4 3 3
表明溶液的酸碱性影响物质的氧化还原性。
3.(2023·全国·校联考一模)在照相底片的定影过程中,未曝光的溴化银(AgBr)常用硫代硫酸钠(Na SO)
2 2 3
溶解。从废定影液{主要含有[Ag(S O)]3-、Br-等}中回收Ag并制取催化剂PdAg@Cu O的流程如图所示:
2 3 2 2
已知:① 的结构如图所示: ;
② 。
请回答下列问题:
(1)写出NaSO 溶液溶解AgBr生成 的离子方程式: ,该反应的化学平衡常数为
2 2 3
。
(2)在 配合反应中,作配位原子的不可能是 (填字母)。
a. 中的中心S原子 b. 中的端基S原子
(3)向滤液1中通入足量氯气后,通过一系列操作可分离出Br 。通入足量氯气后,Cl 发生的氧化还原反应
2 2
主要有 、 、 。
(4)“酸溶”过程中产生的有害气体是 (填化学式),实验室消除该有害气体的方法为 。
(5)操作 的目的是 。
(6)在制备PdAg@Cu O的反应中,NH OH被氧化成无污染物(N ),若获得0.5molPdAg@Cu O,理论上至少
2 2 2 2
需要NH OH g。
2
【答案】(1)AgBr+2 =[Ag(S O)]3-+Br- 16
2 3 2
(2)a
(3) +4Cl+5H O=2 +8Cl-+10H+
2 2
(4)NO 将NO与足量O 混合通入NaOH溶液中
2
(5)除去Ag中混有的铁粉
(6)33
【分析】废定影液{主要含有[Ag(S O)]3-、Br-等}中加入NaS溶液,与[Ag(S O)]3-反应生成Ag S沉淀,过
2 3 2 2 2 3 2 2
滤后,所得滤液中含有Br-、S2-、 ;将Ag S通入空气焙烧,生成粗银和SO ;将粗银放入稀硝酸中溶
2 2
解,生成AgNO 等,加入盐酸将银转化为AgCl沉淀;加入铁粉,将AgCl还原为Ag,过滤所得的Ag中
3混有Fe,加入足量盐酸溶解Fe、过滤、洗涤、干燥,得纯银;纯银与KPdCl 、PVP混合后,得到PdAg,
2 4
再与CuCl 、NaOH、NH OH、HCl混合后,得到PdAg@Cu O。
2 2 2
【解析】(1)NaSO 溶液溶解AgBr生成 和NaBr,离子方程式:AgBr+2
2 2 3
=[Ag(S O)]3-+Br-,该反应的化学平衡常数为K= =K ∙K (AgBr)=3.2×10-
2 3 2 稳 sp
13×5.0×1013=16。
(2)在 配合反应中, 中的中心S原子不存在孤电子对,不能作配位
原子, 中的端基S原子存在孤电子对,可作配位原子,则配原子不可能是a。
(3)向滤液1中通入足量氯气后,通过一系列操作可分离出Br 。通入足量氯气后,Cl 发生的氧化还原反
2 2
应主要有 、 、 +4Cl+5H O=2 +8Cl-
2 2
+10H+。
(4)“酸溶”过程中,粗银与稀硝酸反应,生成AgNO 等,产生的有害气体是NO,实验室消除该有害气
3
体的方法为:将NO与足量O 混合通入NaOH溶液中。
2
(5)加入过量的铁粉后,AgCl全部被还原为Ag,此时Ag中混有过量的铁。往固体混合物中加入足量盐
酸,将Fe溶解后过滤、洗涤、干燥,则操作 的目的是:除去Ag中混有的铁粉。
(6)在制备PdAg@Cu O的反应中,NH OH被氧化成无污染物(N ),依据得失电子守恒,可得出关系式:
2 2 2
2NH OH——Cu O,若获得0.5molPdAg@Cu O,理论上至少需要NH OH的物质的量为0.5mol×2=1mol,
2 2 2 2
质量为1mol×33g/mol=33g。
4.(2023·河北唐山·统考模拟预测)一种用方铅矿(PbS,含少量FeS)和软锰矿(MnO ,含少量铁、锌的氧
2
化物)联合制备PbSO 和MnO 的工艺流程如下:
4 3 4
已知:(1)PbCl 难溶于冷水,易溶于热水;
2
(2)25℃时,部分难溶物的K
sp
物质 FeS ZnS MnS PbS PbCl PbSO
2 4
K 6.0×10-18 1.2×10-23 2×10-13 8×10-28 1.6×10-5 1.6×10-8
sp
回答下列问题:(1)“浸取”中,加入饱和NaCl溶液的作用是 。
(2)滤液X中的金属阳离子主要有Mn2+、Zn2+、Pb2+、Fe2+。加入NaS调pH时,杂质离子的沉淀顺序是
2
。
(3)“转化”环节中,当溶液中 时,c(Cl-)= mol/L。流程中,可循环利用的物质
是 (填化学式)。
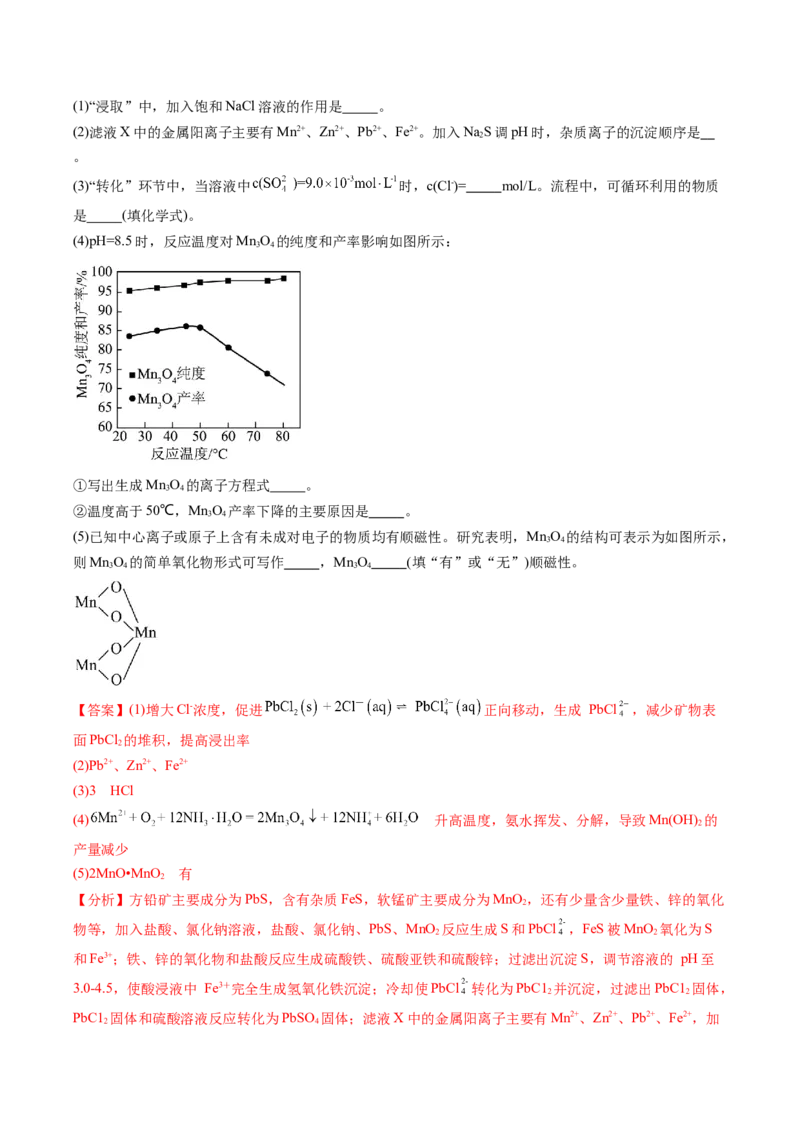
(4)pH=8.5时,反应温度对MnO 的纯度和产率影响如图所示:
3 4
①写出生成MnO 的离子方程式 。
3 4
②温度高于50℃,MnO 产率下降的主要原因是 。
3 4
(5)已知中心离子或原子上含有未成对电子的物质均有顺磁性。研究表明,MnO 的结构可表示为如图所示,
3 4
则MnO 的简单氧化物形式可写作 ,MnO (填“有”或“无”)顺磁性。
3 4 3 4
【答案】(1)增大Cl-浓度,促进 正向移动,生成 PbCl ,减少矿物表
面PbCl 的堆积,提高浸出率
2
(2)Pb2+、Zn2+、Fe2+
(3)3 HCl
(4) 升高温度,氨水挥发、分解,导致Mn(OH) 的
2
产量减少
(5)2MnO•MnO 有
2
【分析】方铅矿主要成分为PbS,含有杂质FeS,软锰矿主要成分为MnO ,还有少量含少量铁、锌的氧化
2
物等,加入盐酸、氯化钠溶液,盐酸、氯化钠、PbS、MnO 反应生成S和PbCl ,FeS被MnO 氧化为S
2 2
和Fe3+;铁、锌的氧化物和盐酸反应生成硫酸铁、硫酸亚铁和硫酸锌;过滤出沉淀S,调节溶液的 pH至
3.0-4.5,使酸浸液中 Fe3+完全生成氢氧化铁沉淀;冷却使PbCl 转化为PbC1 并沉淀,过滤出PbC1 固体,
2 2
PbC1 固体和硫酸溶液反应转化为PbSO 固体;滤液X中的金属阳离子主要有Mn2+、Zn2+、Pb2+、Fe2+,加
2 4入硫化钠溶液调pH时,根据溶度积可得,Pb2+、Zn2+、Fe2+依次沉淀,过滤除去滤渣,滤液中有氯化锰,
加入氨水并通通入氧气,得到产品 MnO。
3 4
【解析】(1)根据分析及题目信息,PbCl 难溶于冷水,易溶于热水,且存在平衡
2
,则“浸取”中,加入饱和NaCl溶液的作用是:增大Cl-浓度,促
进 正向移动,生成 PbCl ,减少矿物表面PbCl 的堆积,提高浸出率。
2
(2)根据分析及题目中25℃时,部分难溶物的K ,加入硫化钠溶液调pH时, Pb2+、Zn2+、Fe2+依次沉淀,
sp
生成对应硫化物。
(3)“转化”环节中,发生反应PbC1 (s)+ (aq) PbSO (s)+2Cl-(aq),当溶液中
2 4
时, ,则c(Cl-)= =3 。“转化”环节中,
生成了HCl,根据流程及分析,HCl可循环利用。
(4)①氯化锰、氨水、氧气反应生成MnO、氯化铵、水,反应方程式为
3 4
,离子方程式为
。
②根据pH=8.5时,反应温度对MnO 的纯度和产率影响图像可得,温度高于50℃,MnO 产率下降,其
3 4 3 4
主要原因是升高温度,氨水挥发、分解,导致Mn(OH) 的产量减少。
2
(5)根据MnO 的结构图可得,MnO 的简单氧化物形式可写作2MnO•MnO ;中心离子或原子上含有未
3 4 3 4 2
成对电子的物质均有顺磁性,锰原子的价层电子排布为3d54s2,含有未成对电子,故MnO 有顺磁性。
3 4
5.(2023·黑龙江大庆·统考一模)高铁酸钾 是新型多功能水处理剂,其生产工艺如图所示:
已知:① 与 溶液反应的产物与反应温度有关,温度较低时产物为 和 ;温度较
高时产物为 和 。
②同一条件下,溶液的碱性越强,高铁酸盐的稳定性越高。
回答下列问题:
(1)写出 与 溶液在较高温度下反应的离子方程式: 。
(2)向“溶液Ⅰ”中加入 固体起到的作用有降低 的溶解度、 、 ;
(3) 晶胞结构如图,设晶胞边长为apm,N 为阿伏加德罗常数的值,则距离最近的 间的距离为
A
,该晶体的密度为 。(列出计算式)(4)配制 溶液时,将 固体溶解在 水中(水的密度近似为 ),所得溶液的密度为
,则该溶液的物质的量浓度为 。(保留3位有效数字)
(5)步骤③发生的反应中氧化剂与还原剂的物质的量之比n(氧化剂)∶n(还原剂) 。对“湿产品”进行
“洗涤、干燥”时,洗涤剂最好选用 (填标号)溶液和异丙醇。
A. B. C.
【答案】(1)
(2)使 完全反应生成 增强溶液的碱性
(3) (未化成最简的计算式 也可)
(4)10.2
(5) C
【分析】过量的氯气和氢氧化钠生成氧化性物质次氯酸钠,加入氢氧化钠使得溶液显碱性,除去氯化钠后
加入硝酸铁溶液,发生氧化还原反应生成 ,加入饱和氢氧化钾溶液析出 晶体。
【解析】(1) 与NaOH溶液在较高温度下反应,产物为NaCl、 和 ,反应中部分氯化合价
由0变为-1、部分由0变为+5,根据电子守恒可知,离子方程式 ;
(2)由流程可知,步骤①氯气过量,步骤③需要碱性条件,故向“溶液Ⅰ”中加入NaOH固体起到的作
用有降低NaCl的溶解度、使氯气完全反应生成NaClO 、增强溶液的碱性;
(3)由图可知,距离最近的 间的距离为面对角线的二分之一,为 pm;根据“均摊法”,晶胞中
含 个Cl-、 个Na,则晶体密度为 ;
(4)利用公式 ,可得 ;
(5)步骤③发生反应为铁离子和次氯酸根离子发生氧化还原反应生成高铁酸根离子和氯离子、水,离子
方程式为 , 是还原剂, 是氧化剂,所以氧化剂和还原剂的物质的量之比为3∶2;根据已知条件可知,洗涤剂不能选用水解呈酸性的 溶液和 溶液,
应选用水解呈碱性的 溶液,故选C。
6.(2023·黑龙江大庆·统考二模)水滑石具有特殊的层状结构,在催化、吸附等方面用途广泛,是一类极
具有研究潜质和使用价值的新材料。共沉淀法制备镁铝水滑石的工业生产流程如图所示。
请回答以下问题:
(1)基态镁原子的核外电子排布式为 。
(2)A1(NO) 力受热易分解,在实验室中需低温密封保存,Al(NO ) 在一定温度下分解的产物有氧化铝和物
3 3 3 3
质的量之比为4:1的两种气体,其中一种气体是单质,则该化学反应方程式为 ;反应釜中,NaCO
2 3
与Al(NO ) 在溶液中发生反应的离子方程式为 。
3 3
(3)陈化是沉淀反应完毕后,将初生的沉淀与母液一起放置一段时间,此过程中随着小晶粒的溶解,被吸附、
吸留和包藏在沉淀内部的杂质重新进入溶液,可提高沉淀的纯度。已知: ,
,则NaCO 与Mg(NO) 在溶液中反应生成沉淀的主要成分为 (填化学式)。
2 3 3 2
(4)检验洗涤液中是否含有钠离子的方法是 。
(5)控制烘干温度为100℃,不能高于此温度的原因是 。
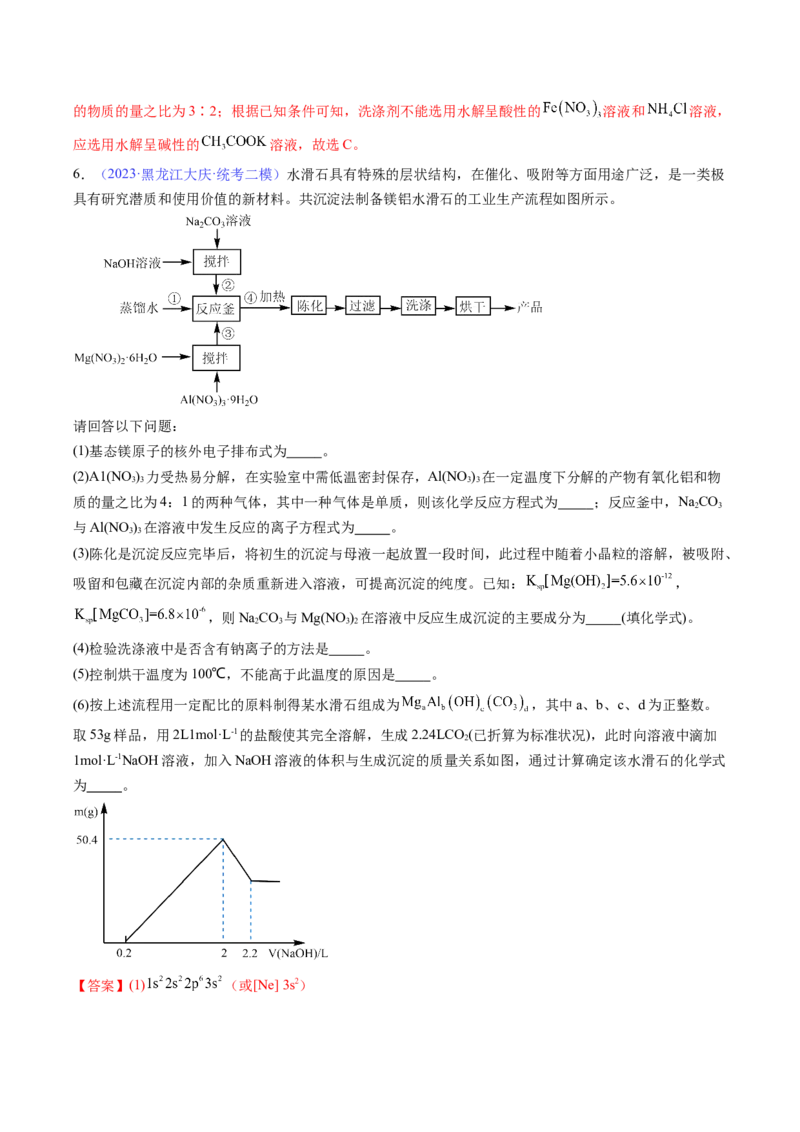
(6)按上述流程用一定配比的原料制得某水滑石组成为 ,其中a、b、c、d为正整数。
取53g样品,用2L1mol·L-1的盐酸使其完全溶解,生成2.24LCO (已折算为标准状况),此时向溶液中滴加
2
1mol·L-1NaOH溶液,加入NaOH溶液的体积与生成沉淀的质量关系如图,通过计算确定该水滑石的化学式
为 。
【答案】(1) (或[Ne] 3s2)(2)
(3)
(4)焰色试验
(5)温度过高,导致产物分解
(6)
【分析】本题流程是以碳酸钠、氢氧化钠、硝酸镁、硝酸铝为原料制备水滑石;首先将碳酸钠溶液和氢氧
化钠溶液混合搅拌,硝酸镁和硝酸钠混合搅拌,将两者与蒸馏水加入反应釜中,加热生成氢氧化铝和氢氧
化镁沉淀,经陈化后析出水滑石,再进行过滤、洗涤、烘干,获得水滑石产品。
【解析】(1)Mg为12号元素,基态镁原子的核外电子排布式为 ;
(2)Al(NO ) 在一定温度下分解的产物有氧化铝和物质的量之比为4:1的两种气体,其中一种气体是单
3 3
质,根据氧化还原反应的电子得失守恒可确定物质的量之比为4:1的两种气体为二氧化氮和氧气,则
Al(NO ) 在一定温度下分解的化学方程式为 ;碳酸钠和硝酸铝在溶
3 3
液中发生彻底的双水解,其离子方程式为 ;
(3)由 、 可知,氢氧化镁溶解度小于碳酸镁,所以NaCO
2 3
与Mg(NO) 在溶液中反应生成沉淀的主要成分为 ;
3 2
(4)钠离子的检验通常采用焰色试验,火焰呈黄色则说明洗涤液中含钠离子;
(5)控制烘干温度为100℃,不能高于此温度的原因为温度过高,导致产物分解;
(6)取53g样品,用盐酸使其完全溶解,生成2.24LCO (已折算为标准状况),即0.1molCO,则含0.1mol
2 2
,根据加入1mol·L-1NaOH溶液的体积与生成沉淀的质量关系图可知,53g样品含0.2molAl3+,Mg2+为
,由电荷守恒可知,53g样品含1.6molOH-,则
a∶b∶c∶d=0.6∶0.2∶1.6∶0.1=6∶2∶16∶1,故该水滑石的化学式为 。
7.(2023·山西晋城·晋城市第一中学校校考模拟预测) 作为一种新型锂电池正极材料受到广泛关
注。由菱锰矿( ,含有少量 、 、 、 等元素)制备 的流程如下:
已知: , , 。
回答下列问题:
(1)硫酸溶矿主要反应的化学方程式为 。为提高溶矿速率,可采取的措施 (举1例)。
(2)加入少量 的作用是 。(3)溶矿反应完成后,反应器中溶液 ,此时 ;用石灰乳调节至 ,除去
的金属离子是 。
(4)加入少量 溶液除去 ,生成的沉淀有 。
(5)在电解槽中,发生电解反应的离子方程式为 。
(6)煅烧窑中,生成 反应的化学方程式是 。
【答案】(1) 粉碎矿石、适当增大硫酸的浓度、适当升高温度等
(其中一条)
(2)将 氧化为 ,便于形成 沉淀而除去
(3)
(4) 和
(5)
(6)
【分析】菱锰矿( ,含有少量 、 、 、 等元素),加入稀硫酸和 ,溶液中含有 、
、 ,加入石灰乳调节 ,除去 ,加入少量 溶液形成 沉淀除去 ,将所得溶液电
解, ,得到 ,最后在煅烧窑中加入碳酸锂反应后生成产品 、
和 。
【解析】(1)硫酸溶矿主要反应的化学方程式为 ,可以通过粉碎矿
石、适当增大硫酸的浓度、适当升高温度等措施加快反应速率;
(2)加入少量 的作用是将 氧化为 ,便于形成 沉淀而除去;
(3)溶矿反应完成后,反应器中溶液 , , ,此时
;用石灰乳调节至 , ,
, ,所以除去的金属离子是 ;
(4)加入少量 溶液除去 ,生成的沉淀为 ,还有 ;
(5)在电解槽中,发生电解反应的离子方程式为 ;
(6)在煅烧窑中加入碳酸锂、 和 反应后可制备产品 ,反应的方程式为:
。8.(2023·四川南充·统考模拟预测)某催化剂主要含Ni、Ni(OH) 、NiS及少量Zn、Fe、CuO、CaO、SiO
2 2
等杂质,从中制备金属Ni的工艺流程如下:
物质 NiS ZnS CuS FeS CaF
2
(2
0℃)
回答下列问题:
(1)为提高废镍催化剂的浸出速率,可采取的措施有 (答一条即可)。
(2)反应 的平衡常数K= 。滤渣1的成分除CuS外还有 。
(3)NaClO氧化 为 的离子方程式为 。
(4)室温下用有机萃取剂HDEHP萃取金属离子的萃取率随溶液pH的变化如下左图。“萃取”时应调节溶
液pH的最佳范围是 。
(5)若用NaCO 溶液“沉镍”会产生 。为测定其组成,进行下列实验:称取干燥
2 3
沉淀样品3.41g,隔绝空气加热,剩余固体质量随温度变化的曲线如上图所示(300~480℃、500~750℃条件
下加热,收集到的气体产物均各只有一种,750℃以上残留固体为NiO)。则样品的化学式为 。
(6)“分解”时通N 的作用是 。
2
【答案】(1)将废镍催化剂进行粉碎或适当升高温度
(2)1010 CaSO、SiO
4 2
(3)2H++ClO-+2Fe2+=2Fe3++Cl-+H O
2
(4)3~4或3<pH<4
(5)NiCO ·2Ni(OH) ·2H O
3 2 2
(6)作保护气,防止Ni被氧化
【分析】废镍催化剂利用硫酸酸浸,二氧化硅不溶,硫酸钙微溶,生成的铜离子结合硫离子转化为CuS沉淀,过滤,浸取液中含有Zn2+、Fe2+、Ni2+等,加入次氯酸钠氧化亚铁离子为铁离子,加入NiO调节pH
沉淀铁离子,加入NaF沉淀锌离子,加入萃取剂萃取除镍离子以外的其它离子,分液后加入草酸钠沉淀镍
离子,最后草酸镍热分解得到金属镍,据此解答。
【解析】(1)依据外界条件对反应速率的影响可判断为提高废镍催化剂的浸出速率,可采取的措施有将
废镍催化剂进行粉碎或适当升高温度等。
(2)反应 的平衡常数K= 。根据以上分析可
知滤渣1的成分除CuS外还有CaSO、SiO。
4 2
(3)NaClO氧化 为 的离子方程式为2H++ClO-+2Fe2+=2Fe3++Cl-+H O。
2
(4)根据图像可知pH在3~4时镍的萃取率最低,其余金属阳离子的萃取率高,所以“萃取”时应调节
溶液pH的最佳范围是3~4或3<pH<4。
(5)300~480℃、500~750℃条件下加热,收集到的气体产物均各只有一种,加热时首先失去的是结晶
水,结晶水的质量是3.41g-2.69g=0.72g,物质的量是0.04mol,第二次生成的气体是二氧化碳,质量是
2.69g-2.25g=0.44g,物质的量是0.01mol,最终得到的是2.25gNiO,物质的量是0.03mol,因此x:y:z=
0.01:0.02:0.02=1:2:2,所以样品的化学式为NiCO·2Ni(OH) ·2H O。
3 2 2
(6)氮气性质稳定,为防止生成的镍被氧化,“分解”时通N 的作用是作保护气,防止Ni被氧化。
2
9.(2023·江西·校联考模拟预测)碲(Te)是重要的稀有元素,被誉为“现代高新技术材料的维生素”。一
种从碲化镉废料中(主要成分为CdTe、CdS、SiO)回收Te和Cd的工艺流程如图所示。
2
已知:室温下,饱和HS溶液的浓度为0.01mol·L-1,Ka=1.6×10-7,Ka=6.25×10-15;K (CdS)=1×10-26;K
2 1 2 sp sp
【Cd(OH) 】=5.3×10-15。
2
回答下列问题:
(1)“氧化浸出”时,温度控制在80℃的原因是 。“氧化浸出”过程中CdTe反应的离子方程式为
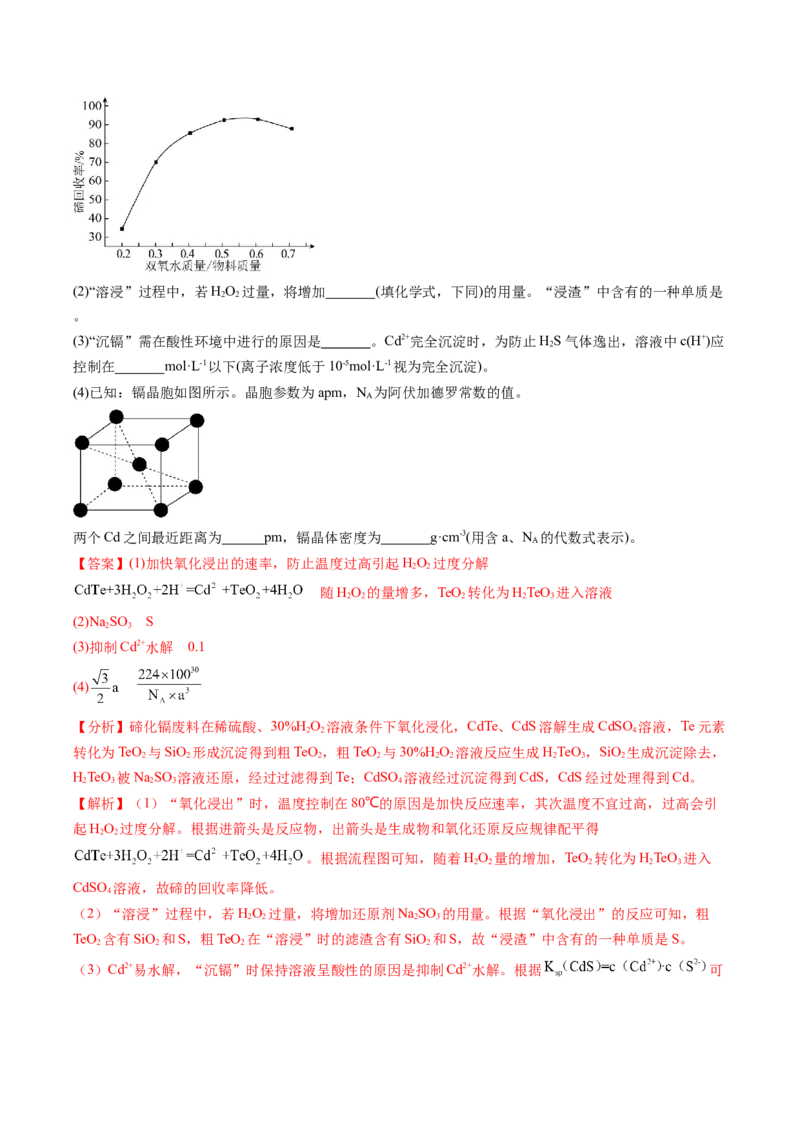
,其他条件不变,该过程中双氧水与物料质量比对碲回收率的影响如图所示。质量比高于0.6时,碲回收
率降低的原因是 。(2)“溶浸”过程中,若HO 过量,将增加 (填化学式,下同)的用量。“浸渣”中含有的一种单质是
2 2
。
(3)“沉镉”需在酸性环境中进行的原因是 。Cd2+完全沉淀时,为防止HS气体逸出,溶液中c(H+)应
2
控制在 mol·L-1以下(离子浓度低于10-5mol·L-1视为完全沉淀)。
(4)已知:镉晶胞如图所示。晶胞参数为apm,N 为阿伏加德罗常数的值。
A
两个Cd之间最近距离为 pm,镉晶体密度为 g·cm-3(用含a、N 的代数式表示)。
A
【答案】(1)加快氧化浸出的速率,防止温度过高引起HO 过度分解
2 2
随HO 的量增多,TeO 转化为HTeO 进入溶液
2 2 2 2 3
(2)NaSO S
2 3
(3)抑制Cd2+水解 0.1
(4)
【分析】碲化镉废料在稀硫酸、30%H O 溶液条件下氧化浸化,CdTe、CdS溶解生成CdSO 溶液,Te元素
2 2 4
转化为TeO 与SiO 形成沉淀得到粗TeO ,粗TeO 与30%H O 溶液反应生成HTeO ,SiO 生成沉淀除去,
2 2 2 2 2 2 2 3 2
HTeO 被NaSO 溶液还原,经过过滤得到Te;CdSO 溶液经过沉淀得到CdS,CdS经过处理得到Cd。
2 3 2 3 4
【解析】(1)“氧化浸出”时,温度控制在80℃的原因是加快反应速率,其次温度不宜过高,过高会引
起HO 过度分解。根据进箭头是反应物,出箭头是生成物和氧化还原反应规律配平得
2 2
。根据流程图可知,随着HO 量的增加,TeO 转化为HTeO 进入
2 2 2 2 3
CdSO 溶液,故碲的回收率降低。
4
(2)“溶浸”过程中,若HO 过量,将增加还原剂NaSO 的用量。根据“氧化浸出”的反应可知,粗
2 2 2 3
TeO 含有SiO 和S,粗TeO 在“溶浸”时的滤渣含有SiO 和S,故“浸渣”中含有的一种单质是S。
2 2 2 2
(3)Cd2+易水解,“沉镉”时保持溶液呈酸性的原因是抑制Cd2+水解。根据 可得Cd2+完全沉淀时,c(S2-)=10-21mol·L-1,又根据 得,Cd2+完全沉淀时,为防止HS气
2
体逸出,溶液中c(H+)应控制在0.1mol·L-1以下。
(4)体心立方晶胞中体对角线上3个粒子相切,棱上粒子不相切。两个镉最近距离为 pm。1个晶胞
含2个镉,晶体密度为 。
10.(2023·广西柳州·柳州高级中学校联考模拟预测)高纯氯化锰(MnCl )在电子技术和精细化工领域有重
2
要应用。一种由粗锰粉(含磷酸盐、硅酸盐、铁、铅等)制备高纯氯化锰的工艺流程如图所示(部分操作和条
件略)。
已知:生成氢氧化物沉淀的pH:
Fe(OH) Fe(OH) Mn(OH) Pb(OH)
2 3 2 2
开始沉淀时 6.3 1.5 8.1 6.5
完全沉淀时 8.3 2.8 10.1 8.5
注:金属离子的起始浓度为0.1mol•L﹣1;当离子的浓度小于等于10﹣5mol•L﹣1时沉淀完全。
回答下列问题:
(1)将粗锰粉磨碎的目的是 。
(2)步骤1和步骤2除去了磷酸盐和硅酸盐。非金属性P Si(填写“大于”“小于”),从原子结构角度
解释非金属性不同的原因是 。
(3)所得滤液甲中的金属离子主要含有Mn2+、Fe2+和Pb2+等,且Pb2+不被HO 氧化。加入HO 目的是 。
2 2 2 2
(用离子方程式表示)。步骤4加入MnCO 得到沉淀的主要成分是 。
3
(4)已知PbS的K =8×10﹣28,MnS的K =2×10﹣10.步骤5的目的是除去Pb2+,反应的离子方程式是 ,
sp sp
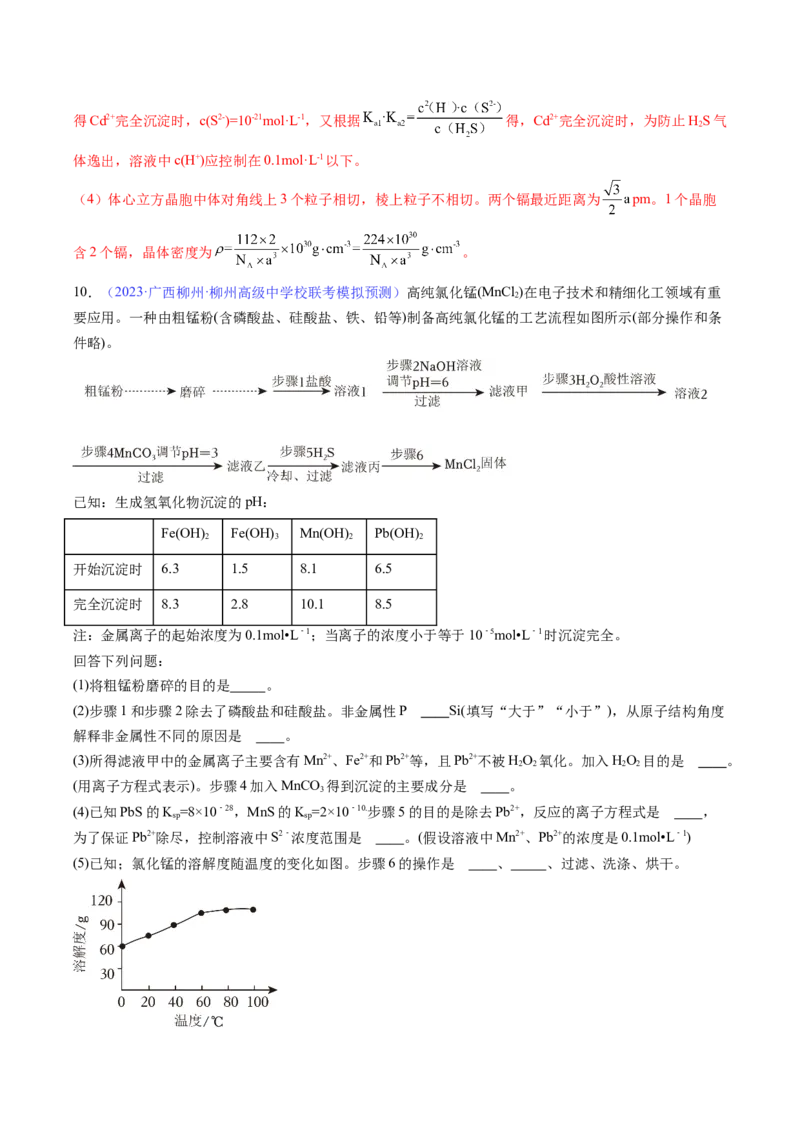
为了保证Pb2+除尽,控制溶液中S2﹣浓度范围是 。(假设溶液中Mn2+、Pb2+的浓度是0.1mol•L﹣1)
(5)已知;氯化锰的溶解度随温度的变化如图。步骤6的操作是 、 、过滤、洗涤、烘干。【答案】(1)增大接触面积,加快反应速率
(2)大于 P元素原子半径较小,得电子能力强,非金属性强
(3)2Fe2++H O+2H+=2Fe3++2H O Fe(OH)
2 2 2 3
(4)Pb2++H S=PbS↓+2H+ 8×10﹣23mol/LH SiO,则得非金属性:P>Si,
3 4 2 3
故答案为:大于;P元素原子半径较小,得电子能力强,非金属性强;
(3)通过分析可知,过氧化氢的作用是将溶液中的Fe2+氧化为Fe3+,便于调节pH将其转化为Fe(OH) 沉
3
淀除去,反应的离子方程式为:2Fe2++H O+2H+=2Fe3++2H O,通过分析可知加入MnCO 相关反应的离子
2 2 2 3
方程式为:MnCO +2H+=Mn2++H O+CO↑,Fe3++3H O Fe(OH) +3H+,作用为调节溶液的pH以便于
3 2 2 2 3
Fe3+沉淀;
⇌
故答案为:2Fe2++H O+2H+=2Fe3++2H O;Fe(OH) ;
2 2 2 3
(4)已知PbS的K =3×10﹣28,MnS的K =2×10﹣10,步骤5的目的是除去Pb2+,反应的离子方程式为:
sp sp
Pb2++H S═PbS↓+2H+,为了保证Pb2+除尽,K =c(Pb2+)×c(S2﹣)=8×10﹣28,c(S2﹣)= mol/L=8×10﹣
2 sp
23mol/L,K =c(Mn2+)×c(S2﹣)=2×10﹣10,c(S2﹣)= mol/L=2×10﹣9mol/L,控制溶液中S2﹣浓度范围是:
sp
8×10﹣23mol/L