文档内容
4.2 元素周期律
【题组一 同周期、同主族的递变规律】
1.(2019·广东湛江·期末)下列关于元素性质的有关叙述中不正确的是
A.C、N、O、F的原子半径依次减小
B.KOH、NaOH、LiOH的碱性逐渐减弱
C.P、S、Cl、Ar的最高正价依次升高
D.Na、Mg、Al、Si的最外层电子数依次增加
【答案】C
【解析】A.C、N、O、F位于周期表同一周期,同周期元素从左到右原子半径逐渐减小,
A正确;
B.Li、Na、K位于同一主族,同一主族元素从上到下元素的金属性逐渐增强,金属性越强,其最高价氧
化物对应的水化物的碱性越强,KOH、NaOH、LiOH的碱性逐渐减弱,B正确;
C.P、S、Cl的最高正价依次升高,Ar为惰性气体,化合价一般为0,C错误;
D.Na、Mg、Al、Si的最外层电子数依次为1、2、3、4,依次增加,D正确;
故合理选项是C。
2.(2020·云南省保山第九中学月考)下列说法错误的是
A.原子半径:F<Mg<K B.稳定性:PH >HS>NH
3 2 3
C.酸性:HPO <HSO <HClO D.碱性:Al(OH) <Mg(OH) <KOH
3 4 2 4 4 3 2
【答案】B
【解析】A、半径的比较:一看电子层数,电子层数越多,半径越大,二看原子序数,电子层数相等,半
径随原子序数的递增而减小,即K>Mg>F,故说法正确;
B、非金属性越强,其氢化物越稳定,同主族从上到下,非金属性减弱,同周期从左向右非金属性增强,
稀有气体除外,非金属性:N>P,即NH >PH,故说法错误;
3 3
C、非金属性越强,其最高价氧化物对应水化物的酸性越强,同周期从左向右非金属性增强,稀有气体除
外,故说法正确;
D、金属性越强,其最高价氧化物对应水化物的碱性越强,同周期从左向右金属性减弱,故说法正确。
答案选B。
3.(2020·全国高一课时练习)下列证据及结论均正确的是( )
证据 结论
A HF、HCl、HBr、HI的酸性逐渐增强 F、Cl、Br、I的非金属性依次增强B HF、HCl、HBr、HI的稳定性逐渐增强 F、Cl、Br、I得电子能力依次增强
、 、 、 的酸性逐渐 、 、 、 的氧化性依次减
C
增强 弱
D 原子最外层电子数相同,电子层数依次增多 F、Cl、Br、I原子半径依次增大
【答案】D
【解析】A.元素最高价氧化物对应水化物的酸性强弱能说明元素非金属性的强弱,氢化物的酸性强弱则
不能,故结论错误,A项不符合;
B.HF、HCl、HBr、HI的稳定性逐渐减弱,说明F、Cl、Br、I得电子能力依次减弱,故证据及结论均错
误,B项不符合;
C.F没有 , 、 、 的酸性逐渐减弱,故证据错误,C项不符合;
D.卤族元素随着原子序数的递增,原子最外层电子数相同,电子层数依次增多,则原子半径依次增大,
故证据及结论均正确,D项符合;
故选D。
4.(2020·浙江高一期中)如图是部分短周期元素原子序数与主要化合价的关系图,X、Y、Z、W、R是
其中的五种元素。下列说法不正确的是
A.离子半径:Y>X
B.33号砷元素与Q同族
C.最高价氧化物的水化物的酸性:R>W
D.单质与水(或酸)反应的剧烈程度:Y>Z
【答案】A
【解析】A.电子层数相同,质子数越多半径越小,离子半径:O2->Na+ ,故A错误;
B.33号砷元素最外层有5个电子,属于ⅤA族元素;Q是P元素,属于ⅤA族元素,故B正确;
C.非金属性Cl>S,最高价氧化物的水化物的酸性HClO>H SO ,故C正确;
4 2 4D.金属性Na>Al,与水(或酸)反应的剧烈程度Na>Al,故D正确;
选A。
5.(2020·福建南安华侨中学月考)下列各组元素中原子序数按由小到大顺序排列的是( )
A.Be、C、B B.Li、O、Cl C.Al、S、Si D.C、S、Mg
【答案】B
【解析】A. Be、C. B的原子序数分别为:4、6、5;
B. Li、O、Cl的原子序数分别是3、8、17;
C. Al、S、Si的原子序数分别是13、16、14;
D. C. S、Mg的原子序数分别是6、16、12;
故选:B。
6.(2020·全国课时练习)下列关于物质性质变化的比较,不正确的是( )
A.离子半径大小:S2->O2->Na+
B.气态氢化物稳定性:HBr<HCl<HF
C.碱性强弱:KOH>NaOH>LiOH
D.还原性强弱:F->Cl->Br->I-
【答案】D
【解析】A、核外电子排布相同的离子,核电荷数越大,离子半径越小,所以O2->Na+;电子层数多的离
子,半径越大,因此离子半径大小S2->O2->Na+,A正确;
B、非金属性F>Cl>Br,气态氢化物的稳定性为HBr<HCl<HF,B正确;
C、金属性K>Na>Li,对应最高价氧化物的水化物的碱性为KOH>NaOH>LiOH,C正确;
D、非金属性F>Cl>Br>I,对应离子的还原性为F-<Cl-<Br-<I-,D错误;
正确选项D。
7.(2020·全国课时练习)三种短周期元素 、 、 在周期表中的位置关系如图所示,则下列叙述不正
确的是( )
A. 在自然界中以化合态形式存在
B. 的最高价氧化物对应的水化物是强酸
C. 的气态氢化物的稳定性强于 的气态氢化物的稳定性D. 、 形成的化合物可用于制作光导纤维
【答案】B
【解析】A. 硅在自然界中以化合态形式存在,故A正确;
B. 氧没有对应的酸,故B错误;
C. 元素的非金属性越强,其气态氢化物的稳定性越强,由于氧的非金属性强于硅,所以HO的稳定性强
2
于SiH,故C正确;
4
D. 二氯化硅可用于制作光导钎维,故D正确;
故答案为B。
8.(2020·全国课时练习)下列对 、 、 三种元素的判断不正确的是( )
A.单质的还原性逐渐减弱
B.原子的失电子能力逐渐增强
C.对应阳离子的氧化性逐渐增强
D.最高价氧化物对应水化物的碱性逐渐减弱
【答案】B
【解析】Na、Mg、Al三种元素原子的电子层数相同,最外层电子数逐渐增多,导致它们的失电子能力逐
渐减弱,即元素的金属性逐渐减弱,则单质的还原性逐渐减弱,还原性越弱失电子的能力越弱,对应阳离
子的氧化性逐渐增强,最高价氧化物对应水化物的碱性逐渐减弱,故答案为B。
9.(2020·全国课时练习)下列结论正确的是( )
①粒子半径:S2->Cl>S ②气态氢化物的热稳定性:HF>HCl>PH
3
③离子还原性:S2->Cl->Br->I- ④单质氧化性:Cl>S
2
⑤酸性:HSO >HClO ⑥碱性:KOH>NaOH>Mg(OH)
2 4 4 2
A.① B.③⑥ C.②④⑥ D.①③④
【答案】C
【解析】①氯和硫都为第三周期元素,氯原子半径小于硫原子,①错误;
②非金属的非金属性越强,其气态氢化物越稳定,非金属性F>Cl>P,②正确;
③非金属性越强,其阴离子的还原性越弱,故还原性应为S2->I->Br->Cl-,③错误;
④氯气的氧化性强于硫,④正确;
⑤非金属的非金属性越强,其最高价氧化物对应水化物的酸性越强,则高氯酸的酸性强于硫酸,⑤错误;
⑥元素的金属性越强,对应的氢氧化物的碱性越强,碱性KOH>NaOH>Mg(OH) ,⑥正确;
2
综上所述,②④⑥正确,答案为C。
【题组二 粒子半径大小的比较】1.(2020·北京密云·高一期末)下列元素的原子半径最大的是( )
A.Mg B.N C.O D.Cl
【答案】A
【解析】根据层多径大原则,N、O两个电子层,Mg、Cl三个电子层,则Mg、Cl半径比N、O半径大,
根据同电子层结构核多径小原则,Mg半径大于Cl半径,因此Mg半径最大,故A符合题意。
综上所述,答案为A。
2.(2020·全国高一课时练习)下列离子中半径最大的是( )
A.Na+ B.Mg2+ C.O2- D.F-
【答案】C
【解析】Na+、Mg2+、O2- 和F-离子核外电子排布都是2、8的电子层结构。对于电子层结构相同的离子
来说,核电荷数越大,离子半径就越小,所以离子半径最大的是O2-,选C。
3.(2019·乾安县第七中学高一月考)下列各组微粒半径大小的比较中,错误的是( )
A.K>Na>Li B.Mg2+>Na+>F﹣
C.Na+>Mg2+>Al3+ D.Cl﹣>F﹣>F
【答案】B
【解析】A.同主族自上而下原子半径增大,故原子半径K>Na>Li,A正确;
B.核外电子排布相同,核电荷数越大离子半径越小,故离子半径F->Na+>Mg2+,B错误;
C.核外电子排布相同,核电荷数越大离子半径越小,故离子半径Na+>Mg2+>Al3+,C正确;
D.最外层电子数相同,电子层越多离子半径越大,阴离子半径大于相应的原子半径,故半径Cl->F->F,
D正确;答案选B。
4.(2020·全国高一课时练习)下列有关原子半径的叙述正确的是( )
A.原子半径:
B.原子半径:
C.简单阴离子半径:
D.原子半径:
【答案】AC
【解析】A.同周期: ,同主族: ,所以 ,故选A;B.同周期: 、 ,故B不选;
C.核外电子排布相同的离子,核电荷数越大,离子半径越小,同周期: ,故选C;
D.同周期从左到右,原子半径减小,所以 ,故D不选。
答案选AC
5.(2020·北京八中乌兰察布分校期末)X、Y、Z均为元素周期表中前20号元素,Xa+、Yb-、Z(b+1)-简单
离子的电子层结构相同,下列说法正确的是( )
A.已知 Xa+与 Yb-,得m+a=n-b
m n
B.离子半径:Yb->Z(b+1)->Xa+
C.Z(b+1)-的还原性一定大于Yb-
D.气态氢化物的稳定性H Z一定大于HY
b+1 b
【答案】C
【解析】A.因为 Xa+与 Yb-的电子层结构相同,所以:m-a=n+b,A错误;
m n
B.由上面分析可知,原子序数:Z<Y<X,层同看序数,序小半径大,所以,离子半径大小关系为:Z(b+
1)- > Yb-> Xa+,B 错误;
C.Y和Z位于同一周期,Y在右边,所以Y的非金属性强于Z,Y单质的氧化性强于Z单质, Z(b+1)-的还
原性强于Yb-,C正确;
D.由C可知,Y的非金属性强于Z,所以,气态氢化物的稳定性H Z一定小于HY,D错误。
b+1 b
答案选C。
6.(2020·全国课时练习)已知1~18号元素中某四种元素的离子 、 、 、 具有相同的电
子层结构,则下列说法正确的是( )
A.四种元素位于同一周期
B.离子的氧化性:
C.气态氢化物的稳定性:
D.
【答案】D【解析】A.因为 、 、 、 具有相同的电子层结构,所以 、 比 、 多一个电子
层,四种元素不全在同一周期,且 ,A项错误;
B. 、 位于同—周期, ,则其单质的还原性: ,对应离子的氧化性: ,B
项错误;
C. 、 位于同一周期, ,非金属性: ,则气态氧化物的稳定性: ,C项错误;
D. 、 的核外电子数相等,则有 ,即 ,D项正确;
故答案为D。
A2+ B+ D−
7.(2020·全国课时练习)已知第一、二、三周期元素A、B、C、D的离子a 、b 、 、d 具有
相同的电子层结构。则下列叙述正确的是( )
A.原子半径: B.原子序数:
C.原子的最外层电子数: D.离子半径:
【答案】D
【解析】根据题意可推知A为Mg,B为Na,C为N,D为F,据此解题:
A.原子半径: ,A错误;
B.原子序数: ,B错误;
C.最外层电子数: ,C错误;
D. 、 、 、 的电子层结构相同,核电荷数越大,离子半径越小,故离子半径;
,D正确;
故答案为:D。
8.(2020·全国高一单元测试)下列粒子半径大小的比较正确的是( )
A.原子半径:B.原子半径:
C.离子半径:
D.第三周期元素简单离子的半径从左到右逐渐减小
【答案】B
【解析】A.F与Cl属于同一主族元素,随着电子层数的递增,原子半径逐渐增大,所以原子半径:
,故A错误;
B. 、 、 属于同一周期元素,随着原子序数的递增,原子半径逐渐减小,故B正确;
C.电子排布相同的离子,核电荷数越大,离子半径越小,故C错误;
D.第三周期元素简单阳离子的半径从左到右逐渐减小,但简单阴离子的半径大于简单阳离子的半径,故
D错误;
答案选B。
【题组三 周期表(律)的应用】
1.(2020·全国课时练习)短周期主族元素X、Y、Z、W的原子序数依次增大,Y在短周期中原子半径最
大,Z是地壳中含量最高的金属元素,X和W同主族,W的最高正化合价与最低负化合价的代数和为4。
下列说法正确的是( )
A.简单气态氢化物的稳定性:X<W
B.原子半径由小到大的顺序:r(X)<r(Z)<r(W)
C.最高价氧化物对应水化物的碱性:Y>Z
D.X与Y只能形成一种化合物
【答案】C
【解析】A.同主族从上至下非金属性逐渐减弱,非金属性O>S,简单氢化物稳定性:HO>HS,故A错
2 2
误;
B.Al、S核外电子层数较O多,因此O原子半径最小,Al与S同周期,从左至右原子半径逐渐减小,因
此原子半径:r(Al)>r(S)>r(O),故B错误;
C.因金属性:Na>Al,因此高价氧化物对应水化物的碱性:NaOH>Al(OH) ,故C正确;
3
D.O与Na能够形成NaO、NaO 等化合物,故D错误;
2 2 2
故答案为C。
2.(2020·全国课时练习)下列与有关非金属元素的叙述以及推理结果不正确的是( )①非金属性 ,故将 通入NaCl溶液中,发生的反应为
②非金属性 ,故酸性:
③非金属性 ,故前者的气态氢化物稳定性更强
④非金属性 ,故 与 化合比 与 化合容易
A.②③ B.③④ C.①④ D.①②
【答案】D
【解析】①将 通入NaCl溶液中, 与水反应生成HF和 ,不与NaCl发生置换反应,故①错误;②
元素非金属性强弱与氢化物水溶液酸性的强弱无关,故②错误;③元素非金属性越强,气态氢化物越稳定,
非金属性 ,因此前者的气态氢化物稳定性更强,故③正确;④元素非金属性越强,与氢气反应越容
易,故 与 化合比 与 化合容易,故④正确,因①②错误;故D正确。
综上所述,答案为D。
3.(2020·全国课时练习)W、X、Y、Z是原子序数依次增大的短周期元素。M、n、p是由这些元素组成
的二元化合物,r是元素Y的常见单质,能使带火星的木条复燃,q为一元强碱,q、s的焰色均呈黄色。上
述物质的转化关系如图所示。下列说法正确的是( )
A.原子半径:
B.Y的简单氢化物的稳定性比X的弱
C.元素非金属性:
D.由W、X、Y、Z四种元素只能组成一种化合物
【答案】C
【解析】A.C、O位于同一周期,C的原子半径大于O,故原子半径: ,A错误;
B.C、O为同周期元素,元素非金属性 ,其简单氢化物的稳定性 ,B错误;
C.C、O为同周期元素,元素非金属性 ,C正确;D.由W、X、Y、Z四种元素可组成 、 等多种化合物,D错误;
故答案为:C。
4.(2020·全国课时练习)今年是门捷列夫发现元素周期律150周年。如表是元素周期表的一部分,W、
X、Y、Z为短周期主族元素,W与X的最高化合价之和为8。下列说法错误的是( )
W
X Y Z
A.原子半径: B.常温常压下,W单质为气态
C.气态氢化物热稳定性: D.X的最高价氧化物的水化物是强碱
【答案】D
【解析】A.X为Al,W为N,原子的电子层数越多,半径越大,原子半径 ,故A正确;
B.W为N,常温常压下,氮气呈气态,故B正确;
C.W和Z分别为N和P,非金属性越强,其简单气态氢化物的稳定性越强,非金属性 ,可知气态
氢化物热稳定性 ,故C正确;
D.Al的最高价氧化物对应的水化物 是典型的两性氢氧化物,并非强碱,故D错误;
答案选D。
5.(2020·全国课时练习)甲、乙、丙三种溶液各含有一种 ( 为 或 )离子,向甲中加淀粉
溶液和氯水,则溶液变为橙色,再加乙溶液,颜色无明显变化。则甲、乙、丙依次含有( )
A. B.
C. D.
【答案】A
【解析】向甲中加入淀粉溶液和新制氯水,溶液变为橙色而不是蓝色,说明甲中含Br-,发生的反应为:
2Br-+Cl=Br +2Cl-;再加入乙溶液,颜色无明显变化,说明乙溶液中含有Cl-,丙溶液含I-,甲含Br-,乙含
2 2Cl-,故答案为:A。
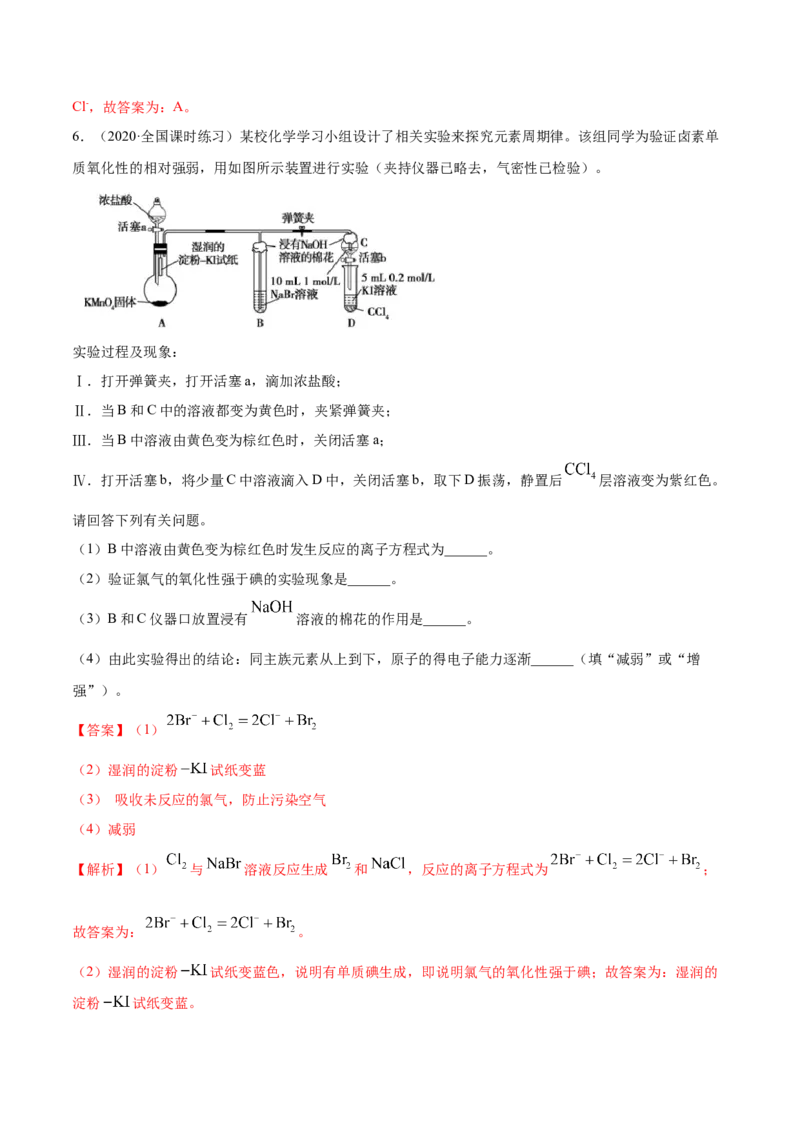
6.(2020·全国课时练习)某校化学学习小组设计了相关实验来探究元素周期律。该组同学为验证卤素单
质氧化性的相对强弱,用如图所示装置进行实验(夹持仪器已略去,气密性已检验)。
实验过程及现象:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸;
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹;
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a;
Ⅳ.打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下D振荡,静置后 层溶液变为紫红色。
请回答下列有关问题。
(1)B中溶液由黄色变为棕红色时发生反应的离子方程式为______。
(2)验证氯气的氧化性强于碘的实验现象是______。
(3)B和C仪器口放置浸有 溶液的棉花的作用是______。
(4)由此实验得出的结论:同主族元素从上到下,原子的得电子能力逐渐______(填“减弱”或“增
强”)。
【答案】(1)
(2)湿润的淀粉 试纸变蓝
(3) 吸收未反应的氯气,防止污染空气
(4)减弱
【解析】(1) 与 溶液反应生成 和 ,反应的离子方程式为 ;
故答案为: 。
(2)湿润的淀粉 试纸变蓝色,说明有单质碘生成,即说明氯气的氧化性强于碘;故答案为:湿润的
淀粉 试纸变蓝。(3)B和C仪器口放置浸有 溶液的棉花的作用是吸收未反应的氯气,防止其对空气造成污染;故
答案为:吸收未反应的氯气,防止污染空气。
(4)由实验可知氯气的氧化性强于溴,而溴的氧化性强于碘,所以同主族元素从上到下,原子的得电子
能力逐渐减弱;故答案为:减弱。
7.(2020·全国课时练习)某校化学兴趣小组同学为探究元素周期律,设计了如下一系列实验。
Ⅰ.(1)将物质的量均为1 mol的钠、钾、镁、铝分别投入足量的0.1 mol/L的盐酸中,试预测实验结果:
________与盐酸反应最剧烈,________与盐酸反应最慢。
(2)将NaOH溶液与NH Cl溶液混合,反应生成NH ·H O,从而验证NaOH的碱性强于NH ·H O的碱性,继
4 3 2 3 2
而可以验证Na的金属性强于N的金属性,你认为此设计是否合理,并说明理由_______。
Ⅱ.利用如所示装置可以验证元素的非金属性的变化规律。
已知:MnO +4HCl(浓) MnCl +Cl↑+2H O,
2 2 2 2
2KMnO +16HCl(浓)=2KCl+2MnCl +5Cl↑+8H O。
4 2 2 2
(3)仪器A的名称为______,D的作用是__________。
(4)实验室中现有药品NaS、KMnO 、浓盐酸、MnO ,请选择合适药品设计实验,验证氯的非金属性强于
2 4 2
硫的非金属性。装置A、B、C中所装药品分别为_________、_________、_________,装置C中的实验现
象为有淡黄色沉淀生成,则反应的离子方程式为___________。
(5)若要证明非金属性C>Si,则A中应加入________溶液,B中应加入NaCO,C中应加入______溶液,
2 3
装置C中的现象为________。
【答案】(1)钾 铝
(2) 不合理,用碱性强弱来判断元素的金属性强弱时,一定要用元素的最高价氧化物对应水化物的碱性
强弱进行判断,NH •H O不是N元素的最高价氧化物对应水化物
3 2
(3) 分液漏斗 防止倒吸
(4) 浓盐酸 KMnO Na S S2-+Cl=S↓+2Cl-
4 2 2
(5) 硫酸 NaSiO 有白色胶状沉淀产生
2 3【解析】I.(1)同一周期元素,元素的金属性随着原子序数增大而减弱,元素的金属性越强;同一主族,
原子序数越大,元素的金属性越强,其单质与酸或水反应越剧烈,所以元素金属性:K>Na>Mg>Al,则
K与盐酸反应最剧烈、Al与盐酸反应速率最慢;
(2)将NaOH溶液与NH Cl溶液混合生成NH •H O,可说明碱性NaOH>NH •H O,但不能说明元素的金属
4 3 2 3 2
性:Na>N,因为要验证金属性的强弱,必须通过比较最高价氧化物所对应的水化物的碱性来进行比较,
而NH •H O不是N的最高价氧化物的水化物,
3 2
故答案为:不合理,用碱性强弱比较金属性强弱时,一定要用元素的最高价氧化物的水化物的碱性强弱比
较,而NH •H O不是氮元素的最高价氧化物的水化物.
3 2
II.(3)根据装置图可知仪器A为分液漏斗,球形干燥管D的作用是防止倒吸,可避免C中液体进入锥形瓶
中;
(4)要设计实验验证非金属性:Cl>S,可根据活动性强的单质能够将活动性弱的从化合物中置换出来验证,
即利用Cl 与NaS的氧化还原反应可验证,则装置A、B、C中所装药品应分别为浓盐酸、KMnO 、NaS
2 2 4 2
溶液,在B中反应制取Cl,在装置C中发生反应:S2-+Cl=S↓+2Cl-,故装置C中的实验现象为:有淡黄色
2 2
沉淀生成;
(5)若要证明元素的非金属性:C>Si,可通过CO 和NaSiO 在溶液中发生复分解反应生成难溶性的硅酸来
2 2 3
证明,A中可以加无挥发性的HSO ,B中加NaCO 溶液,二者反应制取CO,然后将反应产生的CO 通
2 4 2 3 2 2
入C中的NaSiO 溶液中,发生反应:NaSiO+CO +H O=HSiO↓+Na CO,因此会看到:产生白色胶状沉
2 3 2 3 2 2 2 3 2 3
淀,从而可以证明酸性:HCO>HSiO,则元素的非金属性:C>Si。
2 3 2 3