文档内容
4.2.2电解池原理的应用(分层作业)
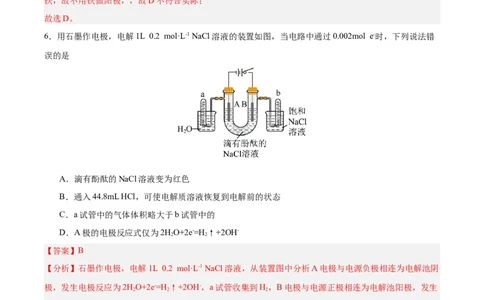
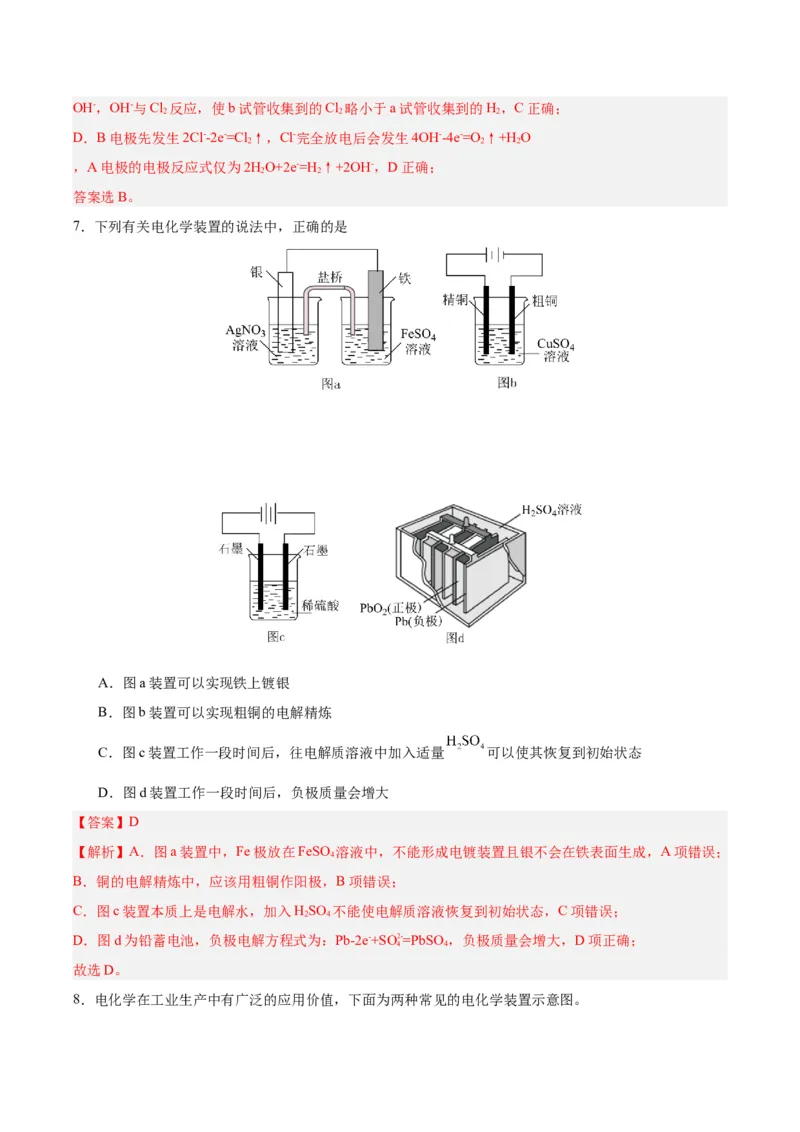
1.下列有关四个实验装置的叙述错误的是
A.图I所示装置工作时,盐桥中的阳离子移向 溶液
B.图Ⅱ所示的金属防护法称为外加电流法
C.图Ⅲ可以比较K (AgCl)、K (AgBr)的相对大小
sp sp
D.图Ⅳ所示装置工作时,溶液a是烧碱溶液
【答案】D
【解析】A.盐桥中的阳离子移向正极CuSO 溶液,A正确;
4
B.图Ⅱ中有外加直流电源,称为外加电流法,B正确
C.向氯离子和溴离子浓度均为0.1mol/L的溶液中滴入硝酸银溶液,若先生成淡黄色的溴化银沉淀,说明
K (AgCl)>K (AgBr),C正确;
sp sp
D.图Ⅳ所示装置工作时,右侧为阴极,阴极放氢生碱,得到NaOH溶液,故右侧溶液是烧碱溶液,D错
误;
故选D。
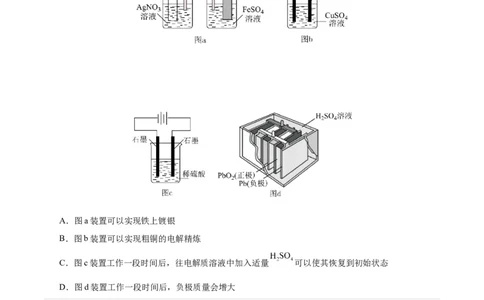
2.(双选)金属镍有广泛的用途,粗镍中含有Fe、Zn、Cu、Pt等杂质,可用电解法制得高纯度的镍。下
列叙述正确的是(已知氧化性:Fe2+a %,C
项正确;
D.阳极上亚硫酸根离子在酸辛条件下失电子发生氧化反应,故电极反应方程式为:SO2- +HO-2e-=SO2- +
3 2 4
2H+,D项错误;
答案选C。
18.请回答下列问题:
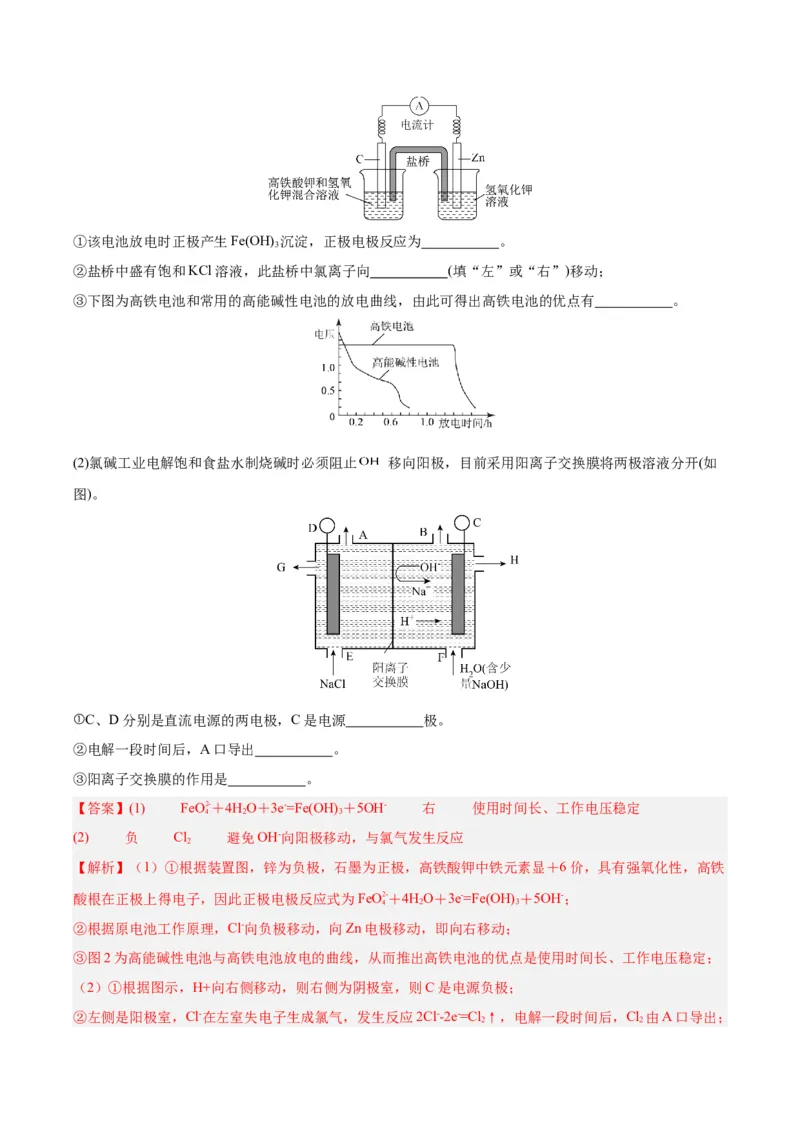
(1)高铁酸钾( )不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。下图所示是高铁电池
的模拟实验装置。①该电池放电时正极产生Fe(OH) 沉淀,正极电极反应为 。
3
②盐桥中盛有饱和KCl溶液,此盐桥中氯离子向 (填“左”或“右”)移动;
③下图为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有 。
(2)氯碱工业电解饱和食盐水制烧碱时必须阻止 移向阳极,目前采用阳离子交换膜将两极溶液分开(如
图)。
①C、D分别是直流电源的两电极,C是电源 极。
②电解一段时间后,A口导出 。
③阳离子交换膜的作用是 。
【答案】(1) FeO2- +4HO+3e-=Fe(OH) +5OH- 右 使用时间长、工作电压稳定
4 2 3
(2) 负 Cl 避免OH-向阳极移动,与氯气发生反应
2
【解析】(1)①根据装置图,锌为负极,石墨为正极,高铁酸钾中铁元素显+6价,具有强氧化性,高铁
酸根在正极上得电子,因此正极电极反应式为FeO2- +4HO+3e-=Fe(OH) +5OH-;
4 2 3
②根据原电池工作原理,Cl-向负极移动,向Zn电极移动,即向右移动;
③图2为高能碱性电池与高铁电池放电的曲线,从而推出高铁电池的优点是使用时间长、工作电压稳定;
(2)①根据图示,H+向右侧移动,则右侧为阴极室,则C是电源负极;
②左侧是阳极室,Cl-在左室失电子生成氯气,发生反应2Cl--2e-=Cl↑,电解一段时间后,Cl 由A口导出;
2 2③若不采用阳离子交换膜,OH-会向阳极移动,氯气和氢氧根离子反应生成氯离子和次氯酸根离子,故使
用阳离子交换膜可以避免OH-向阳极移动,与氯气发生反应。
19.电池的发明和应用是化学家们对人类社会的重要贡献之一。每一次化学电池技术的突破,都带来了电
子设备革命性的发展。最近,我国在甲烷燃料电池的相关技术上获得了新突破,原理如下图所示:
(1)甲烷燃料应从 口通入(图1),发生的电极反应式 。
(2)以石墨做电极电解NaSO 溶液,如图2所示,电解开始后在 的周围(填“阴极”或“阳
2 4
极”)先出现红色,该极的电极反应式为 。。
(3)以CuSO 溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是
4
___________。
A.利用阳极泥可回收Ag、Pt、Au等金属
B.粗铜接电源正极,发生氧化反应
C.溶液中Cu2+向阳极移动
D.电能全部转化为化学能
(4)人工肾脏可采用间接电化学方法除去代谢产物中的尿素[CO(NH)],原理如图。
2 2①电源的正极为 (填“A”或“B”)。
②电解结束后,阴极室溶液的pH与电解前相比将 (填“增大”、“减小”、“不变”);若收
集到H2.24L(标准状况),则通过质子交换膜的H+数目为 (忽略气体的溶解)。
2
【答案】(1) b CH —8e—+2H O=CO+8H+
4 2 2
(2) 阴极 2HO+2e—= H ↑+ 2OH—
2 2
(3)AB
(4) A 不变 0.2N
A
【解析】(1)由氢离子的移动方向可知,左侧电极燃料电池的负极,水分子作用下甲烷在负极失去电子
发生氧化反应生成二氧化碳和氢离子,电极反应式为CH—8e—+2H O=CO+8H+,则甲烷燃料应从b口通
4 2 2
入,故答案为:b;CH—8e—+2H O=CO+8H+;
4 2 2
(2)以石墨做电极电解硫酸钠溶液时,水分子在阴极得到电子发生还原反应生成氢气和氢氧根离子,使
滴入酚酞试液的阴极区溶液变红色,电极反应式为2HO+2e—= H ↑+ 2OH—,故答案为:阴极;2HO+2e—=
2 2 2
H↑+ 2OH—;
2
(3)精炼铜时,与直流电源正极相连的粗铜做精炼池的阳极,铝、锌、铜在阳极失去电子发生氧化反应
生成金属阳离子,银、铂、金不能放电,在阳极形成阳极泥,精铜做阴极,铜离子在阴极得到电子发生还
原反应生成铜。
A.由分析可知,银、铂、金不能放电,在阳极形成阳极泥,所以利用阳极泥可回收银、铂、金等金属,
故A正确;
B.由分析可知,与直流电源正极相连的粗铜做精炼池的阳极,故B正确;
C.精炼池工作时,溶液中阳离子铜离子向阴极移动,故C错误;
D.精炼池工作时,电能会转化为化学能和热能,不可能完全转化为化学能,故D错误;
故选AB;(4)由图可知,与直流电源A极相连的左侧电极逸出氯气可知,A极为正极,左侧电极为阳极,氯离子
在阳极失去电子发生氧化反应生成氯气,氯气与尿素溶液反应生成氮气、二氧化碳和盐酸,反应的化学方
程式为CO(NH)+3Cl+H O=N+CO +6HCl,溶液中的氢离子通过质子交换膜进入阴极室,右侧电极为阴极,
2 2 2 2 2 2
水分子在阴极得到电子发生还原反应生成氢气和氢氧根离子,电极反应式为2HO+2e—= H ↑+ 2OH—,放电
2 2
生成的氢氧根离子与进入阴极室的氢离子反应生成水;
①由分析可知,A极为电源的正极,故答案为:A;
②由分析可知,放电生成的氢氧根离子与进入阴极室的氢离子反应生成水,所以阴极室中电解前后溶液的
2.24L
pH不变,则标准状况下阴极生成2.24L时,通过质子交换膜的氢离子数目为 ×2×N mol—
22.4L/mol A
1=0.2N ,故答案为:不变;0.2N 。
A A