文档内容
由于第一节内容后连的比较多,所以这一节内容就是个概念形
成和具体应用的一节,所以内容较少,结合上一节内容一起看
才能体会元素周期表和元素周期律的真正含义
1、粒子半径大小的比较
影响粒子半径大小的因素有:
①电子层数的多少;
②原子核对核外电子的吸引力的大小;
③核外电子的多少。
(1)同周期、同主族原子半径的比较
①同一周期,从左到右,核电荷数依次增大,
原子半径依次减小。如
r(Na)>r(Mg)>r(Al)>r(Si)>r(P)>r(S)>r(Cl)。
②同一主族,自上而下,电子层数依次增多,
原子半径依次增大。如r(Li)r(O)。
②电子层数相同时看核电荷数,荷少径大,
如r(F-)>r(Na+)。
③电子层数、核电荷数都相同时看电子数,
电子数多的半径大,如r(Cl-)>r(Cl)、r(Fe2+)>r(Fe3+)。
1.下列各组微粒半径大小的比较中,错误的是( )
A.K>Na>Li B.Mg2+>Na+>F﹣
C.Na+>Mg2+>Al3+ D.Cl﹣>F﹣>F
【答案】B
详解:A.同主族自上而下原子半径增大,
故原子半径K>Na>Li,A正确;
B.核外电子排布相同,核电荷数越大离子半径越小,
故离子半径F->Na+>Mg2+,B错误;C.核外电子排布相同,核电荷数越大离子半径越小,
故离子半径Na+>Mg2+>Al3+,C正确;
D.最外层电子数相同,电子层越多离子半径越大,
阴离子半径大于相应的原子半径,故半径Cl->F->F,D正确;
2、 主族元素主要化合价的确定
(1)主族元素的最高化合价=族序数(O、F除外)。
(2)非金属元素最低负价=8-原子的最外层电子数(H除外)。
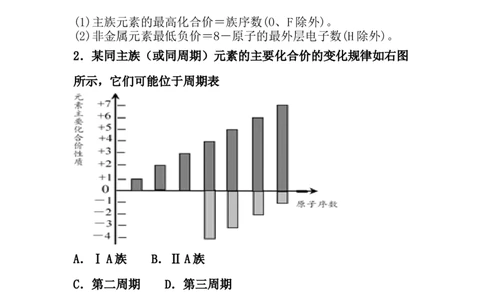
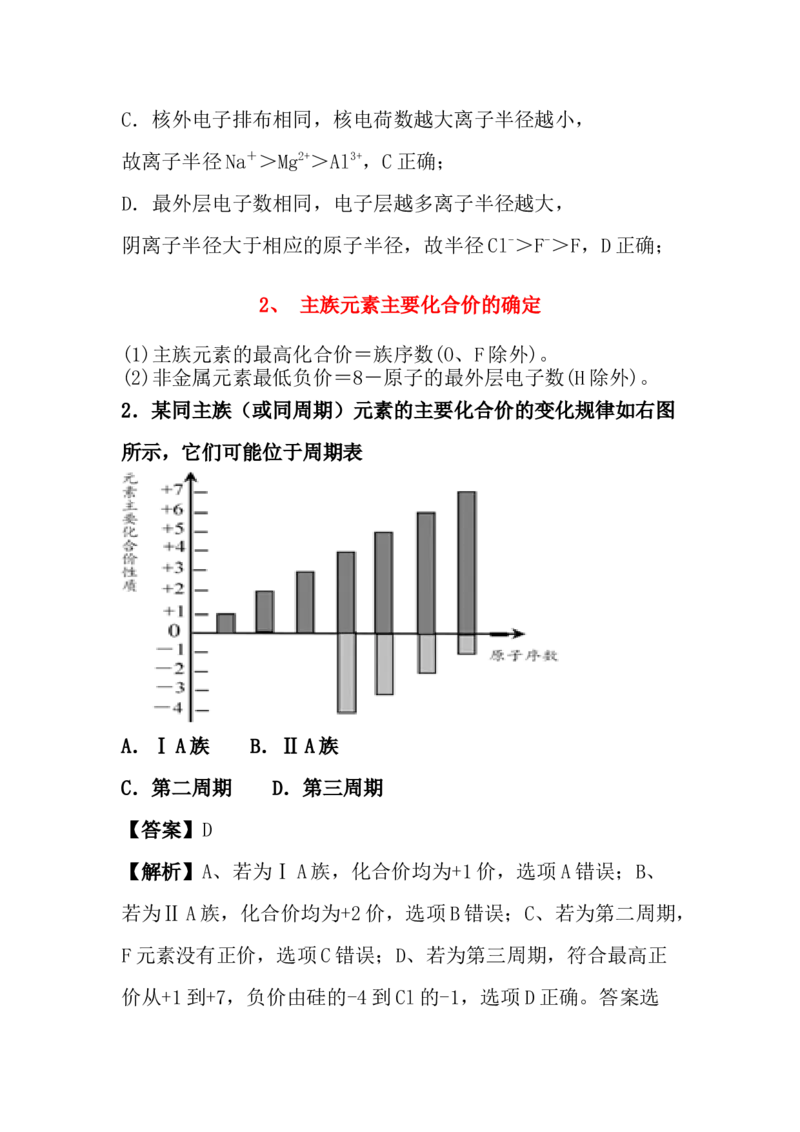
2.某同主族(或同周期)元素的主要化合价的变化规律如右图
所示,它们可能位于周期表
A.ⅠA族 B.ⅡA族
C.第二周期 D.第三周期
【答案】D
【解析】A、若为ⅠA族,化合价均为+1价,选项A错误;B、
若为ⅡA族,化合价均为+2价,选项B错误;C、若为第二周期,
F元素没有正价,选项C错误;D、若为第三周期,符合最高正
价从+1到+7,负价由硅的-4到Cl的-1,选项D正确。答案选D。
3. 元素周期律的具体应用
(1)预测未知元素的性质
依据:同主族元素性质的递变规律。
如已知卤族元素的性质递变规律,可推知未知元素砹(At)应
为有色固体,与氢难化合,HAt不稳定,水溶液呈酸性,AgAt
不溶于水等。
3.1.(2019·衡水高一检测)原子序数为114的元素位于第七周
期第ⅣA族,称为类铅元素。下面关于它的原子结构和性质的说
法正确的是 ( )
A.类铅元素原子的最外层电子数为6
B.其常见价态为+2、+3、+4
C.它的金属性比铅强
D.它的原子半径比铅小
【解析】选 C。114 号元素位于第Ⅳ A 族,最外层电子数应该是
4,A 项错;C、Si、Pb 的常见正价有+2、+4 价,没有+3 价,B 项错;
同主族元素的金属性由上至下逐渐增强,C 项正确;该元素的电
子层数比Pb多,原子半径比Pb大,D项错
(2)比较元素的性质
依据:元素周期律。
如比较H SO 和H SeO 的酸性强弱,因为S、Se同主族,自上
2 4 2 4
至下,元素的非金属性减弱,最高价氧化物对应的水化物酸性
减弱,故酸性:H SO >H SeO 。
2 4 2 4
3.2(2019·临沂高一检测)门捷列夫对化学这一学科发展的最大
贡献在于发现了化学元素周期律。下列事实不能用元素周期律
解释的只有 ( )A.碱性:KOH>Ca(OH) >Mg(OH)
2 2
B.稳定性:H O>H S>H Se
2 2 2
C.挥发性:HNO >H PO >H SO
3 3 4 2 4
D.原子半径:P>S>Cl
【解析】选 C。元素的金属性越强,其原子失电子能力越强,其
最高价氧化物对应的水化物碱性越强,金属性 K>Ca>Mg,则碱
性:KOH>Ca(OH) >Mg(OH) ,A 可以;元素的非金属性越强,其对应
2 2
的气态氢化物越稳定,同主族元素非金属性 O>S>Se,则稳定
性:H O>H S>H Se,B 可以;挥发性与物质的结构无关,C 不可以;同
2 2 2
周期元素从左到右原子半径逐渐减小,D可以。
4. 元素的“位”“构”“性”间的关系
(1)原子结构――→元素在周期表中的位置:
结构位置
(2)原子结构――→元素的化学性质
结构 性质
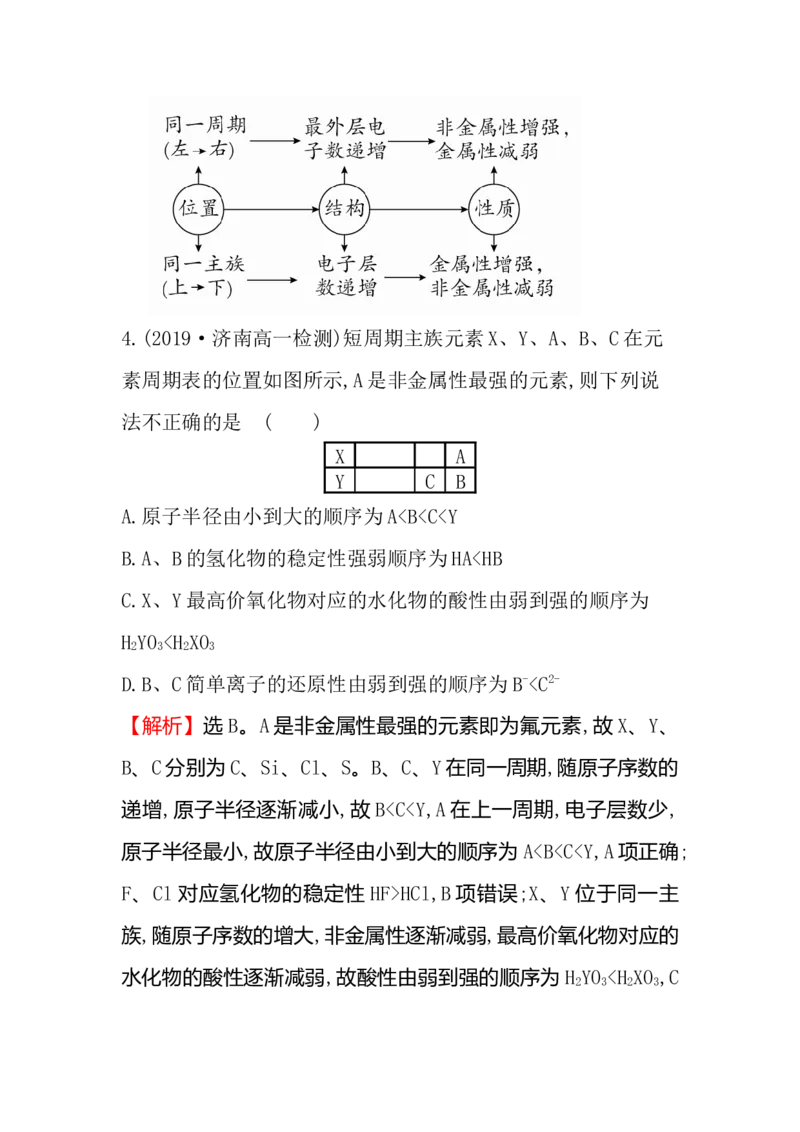
(3)位置――→原子结构和元素性质4.(2019·济南高一检测)短周期主族元素X、Y、A、B、C在元
素周期表的位置如图所示,A是非金属性最强的元素,则下列说
法不正确的是 ( )
X A
Y C B
A.原子半径由小到大的顺序为AHCl,B 项错误;X、Y 位于同一主
族,随原子序数的增大,非金属性逐渐减弱,最高价氧化物对应的
水化物的酸性逐渐减弱,故酸性由弱到强的顺序为 H YO