文档内容
4.2 元素周期律
【题组一 同周期、同主族的递变规律】
1.(2019·广东湛江·期末)下列关于元素性质的有关叙述中不正确的是
A.C、N、O、F的原子半径依次减小
B.KOH、NaOH、LiOH的碱性逐渐减弱
C.P、S、Cl、Ar的最高正价依次升高
D.Na、Mg、Al、Si的最外层电子数依次增加
2.(2020·云南省保山第九中学月考)下列说法错误的是
A.原子半径:F<Mg<K B.稳定性:PH >HS>NH
3 2 3
C.酸性:HPO <HSO <HClO D.碱性:Al(OH) <Mg(OH) <KOH
3 4 2 4 4 3 2
3.(2020·全国高一课时练习)下列证据及结论均正确的是( )
证据 结论
A HF、HCl、HBr、HI的酸性逐渐增强 F、Cl、Br、I的非金属性依次增强
B HF、HCl、HBr、HI的稳定性逐渐增强 F、Cl、Br、I得电子能力依次增强
、 、 、 的酸性逐渐 、 、 、 的氧化性依次减
C
增强 弱
D 原子最外层电子数相同,电子层数依次增多 F、Cl、Br、I原子半径依次增大
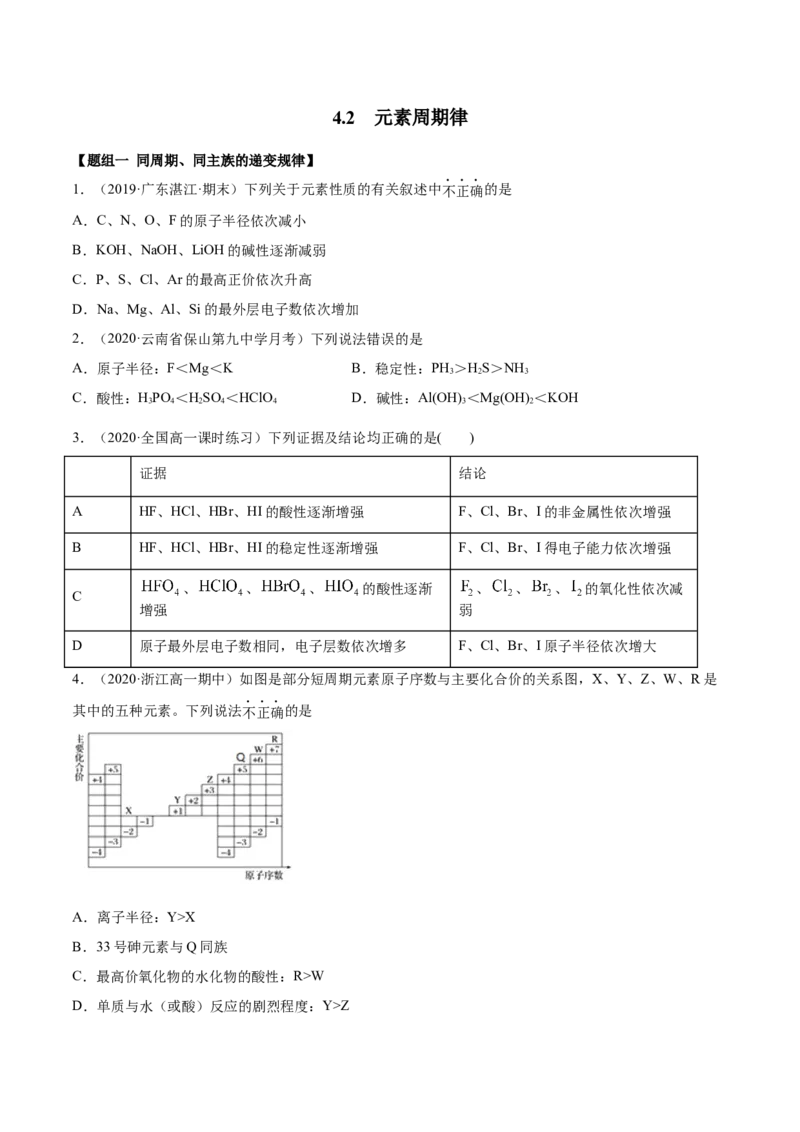
4.(2020·浙江高一期中)如图是部分短周期元素原子序数与主要化合价的关系图,X、Y、Z、W、R是
其中的五种元素。下列说法不正确的是
A.离子半径:Y>X
B.33号砷元素与Q同族
C.最高价氧化物的水化物的酸性:R>W
D.单质与水(或酸)反应的剧烈程度:Y>Z5.(2020·福建南安华侨中学月考)下列各组元素中原子序数按由小到大顺序排列的是( )
A.Be、C、B B.Li、O、Cl C.Al、S、Si D.C、S、Mg
6.(2020·全国课时练习)下列关于物质性质变化的比较,不正确的是( )
A.离子半径大小:S2->O2->Na+
B.气态氢化物稳定性:HBr<HCl<HF
C.碱性强弱:KOH>NaOH>LiOH
D.还原性强弱:F->Cl->Br->I-
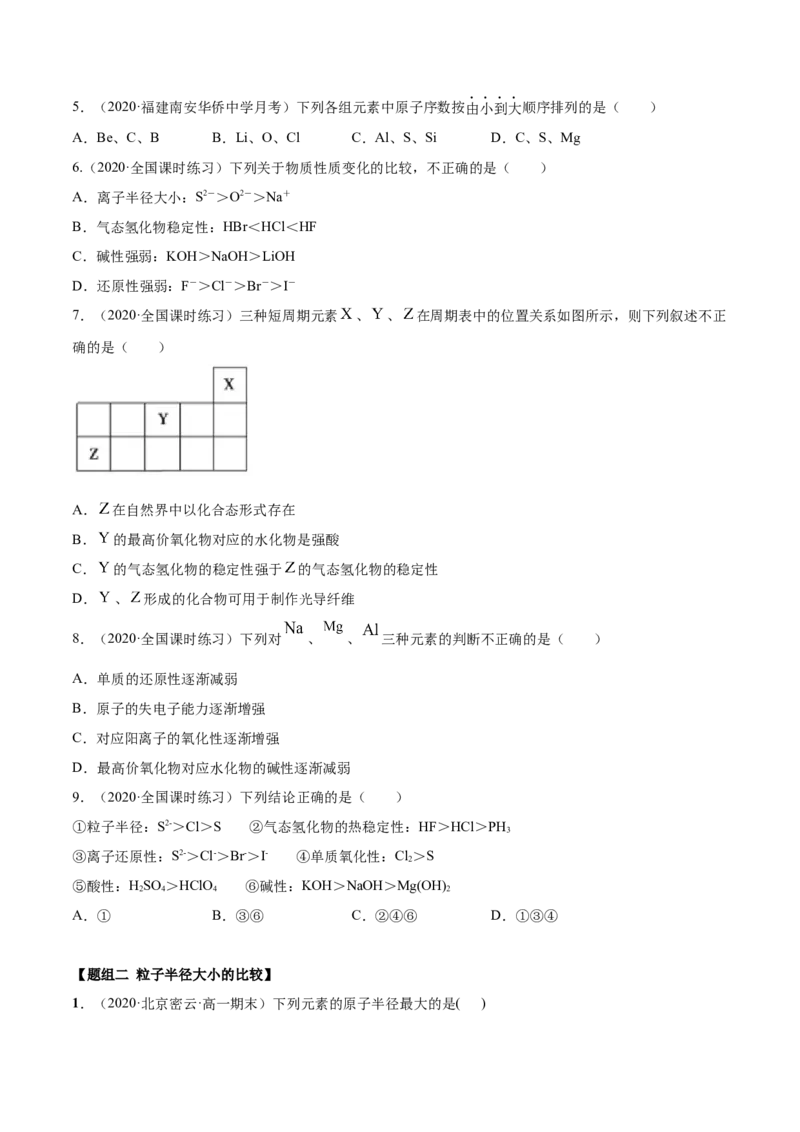
7.(2020·全国课时练习)三种短周期元素 、 、 在周期表中的位置关系如图所示,则下列叙述不正
确的是( )
A. 在自然界中以化合态形式存在
B. 的最高价氧化物对应的水化物是强酸
C. 的气态氢化物的稳定性强于 的气态氢化物的稳定性
D. 、 形成的化合物可用于制作光导纤维
8.(2020·全国课时练习)下列对 、 、 三种元素的判断不正确的是( )
A.单质的还原性逐渐减弱
B.原子的失电子能力逐渐增强
C.对应阳离子的氧化性逐渐增强
D.最高价氧化物对应水化物的碱性逐渐减弱
9.(2020·全国课时练习)下列结论正确的是( )
①粒子半径:S2->Cl>S ②气态氢化物的热稳定性:HF>HCl>PH
3
③离子还原性:S2->Cl->Br->I- ④单质氧化性:Cl>S
2
⑤酸性:HSO >HClO ⑥碱性:KOH>NaOH>Mg(OH)
2 4 4 2
A.① B.③⑥ C.②④⑥ D.①③④
【题组二 粒子半径大小的比较】
1.(2020·北京密云·高一期末)下列元素的原子半径最大的是( )A.Mg B.N C.O D.Cl
2.(2020·全国高一课时练习)下列离子中半径最大的是( )
A.Na+ B.Mg2+ C.O2- D.F-
3.(2019·乾安县第七中学高一月考)下列各组微粒半径大小的比较中,错误的是( )
A.K>Na>Li B.Mg2+>Na+>F﹣
C.Na+>Mg2+>Al3+ D.Cl﹣>F﹣>F
4.(2020·全国高一课时练习)下列有关原子半径的叙述正确的是( )
A.原子半径:
B.原子半径:
C.简单阴离子半径:
D.原子半径:
5.(2020·北京八中乌兰察布分校期末)X、Y、Z均为元素周期表中前20号元素,Xa+、Yb-、Z(b+1)-简单
离子的电子层结构相同,下列说法正确的是( )
A.已知 Xa+与 Yb-,得m+a=n-b
m n
B.离子半径:Yb->Z(b+1)->Xa+
C.Z(b+1)-的还原性一定大于Yb-
D.气态氢化物的稳定性H Z一定大于HY
b+1 b
6.(2020·全国课时练习)已知1~18号元素中某四种元素的离子 、 、 、 具有相同的电
子层结构,则下列说法正确的是( )
A .四种元素位于同一周期
B.离子的氧化性:
C.气态氢化物的稳定性:
D.
A2+ B+ D−
7.(2020·全国课时练习)已知第一、二、三周期元素A、B、C、D的离子a 、b 、 、d 具有相同的电子层结构。则下列叙述正确的是( )
A.原子半径: B.原子序数:
C.原子的最外层电子数: D.离子半径:
8.(2020·全国高一单元测试)下列粒子半径大小的比较正确的是( )
A.原子半径:
B.原子半径:
C.离子半径:
D.第三周期元素简单离子的半径从左到右逐渐减小
【题组三 周期表(律)的应用】
1.(2020·全国课时练习)短周期主族元素X、Y、Z、W的原子序数依次增大,Y在短周期中原子半径最
大,Z是地壳中含量最高的金属元素,X和W同主族,W的最高正化合价与最低负化合价的代数和为4。
下列说法正确的是( )
A.简单气态氢化物的稳定性:X<W
B.原子半径由小到大的顺序:r(X)<r(Z)<r(W)
C.最高价氧化物对应水化物的碱性:Y>Z
D.X与Y只能形成一种化合物
2.(2020·全国课时练习)下列与有关非金属元素的叙述以及推理结果不正确的是( )
①非金属性 ,故将 通入NaCl溶液中,发生的反应为
②非金属性 ,故酸性:
③非金属性 ,故前者的气态氢化物稳定性更强
④非金属性 ,故 与 化合比 与 化合容易
A.②③ B.③④ C.①④ D.①②
3.(2020·全国课时练习)W、X、Y、Z是原子序数依次增大的短周期元素。M、n、p是由这些元素组成
的二元化合物,r是元素Y的常见单质,能使带火星的木条复燃,q为一元强碱,q、s的焰色均呈黄色。上
述物质的转化关系如图所示。下列说法正确的是( )A.原子半径:
B.Y的简单氢化物的稳定性比X的弱
C.元素非金属性:
D.由W、X、Y、Z四种元素只能组成一种化合物
4.(2020·全国课时练习)今年是门捷列夫发现元素周期律150周年。如表是元素周期表的一部分,W、
X、Y、Z为短周期主族元素,W与X的最高化合价之和为8。下列说法错误的是( )
W
X Y Z
A.原子半径: B.常温常压下,W单质为气态
C.气态氢化物热稳定性: D.X的最高价氧化物的水化物是强碱
5.(2020·全国课时练习)甲、乙、丙三种溶液各含有一种 ( 为 或 )离子,向甲中加淀粉
溶液和氯水,则溶液变为橙色,再加乙溶液,颜色无明显变化。则甲、乙、丙依次含有( )
A. B.
C. D.
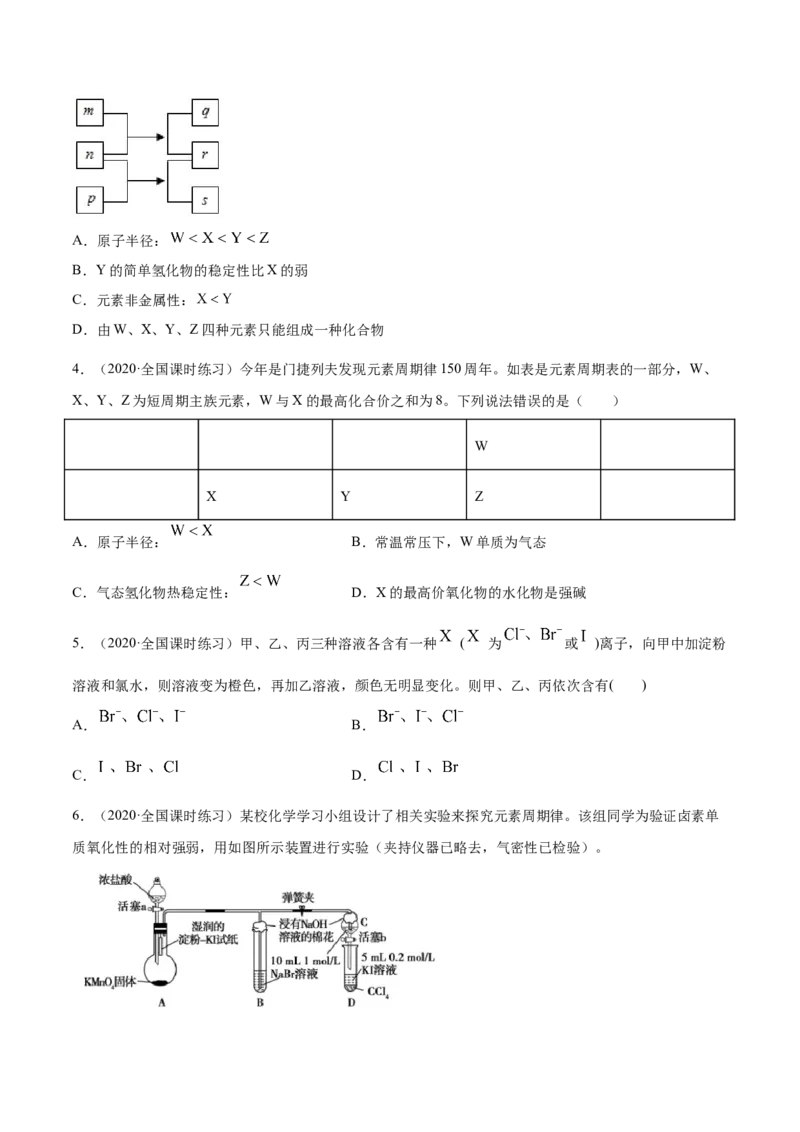
6.(2020·全国课时练习)某校化学学习小组设计了相关实验来探究元素周期律。该组同学为验证卤素单
质氧化性的相对强弱,用如图所示装置进行实验(夹持仪器已略去,气密性已检验)。实验过程及现象:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸;
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹;
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a;
Ⅳ.打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下D振荡,静置后 层溶液变为紫红色。
请回答下列有关问题。
(1)B中溶液由黄色变为棕红色时发生反应的离子方程式为______。
(2)验证氯气的氧化性强于碘的实验现象是______。
(3)B和C仪器口放置浸有 溶液的棉花的作用是______。
(4)由此实验得出的结论:同主族元素从上到下,原子的得电子能力逐渐______(填“减弱”或“增
强”)。
7.(2020·全国课时练习)某校化学兴趣小组同学为探究元素周期律,设计了如下一系列实验。
Ⅰ.(1)将物质的量均为1 mol的钠、钾、镁、铝分别投入足量的0.1 mol/L的盐酸中,试预测实验结果:
________与盐酸反应最剧烈,________与盐酸反应最慢。
(2)将NaOH溶液与NH Cl溶液混合,反应生成NH ·H O,从而验证NaOH的碱性强于NH ·H O的碱性,继
4 3 2 3 2
而可以验证Na的金属性强于N的金属性,你认为此设计是否合理,并说明理由_______。
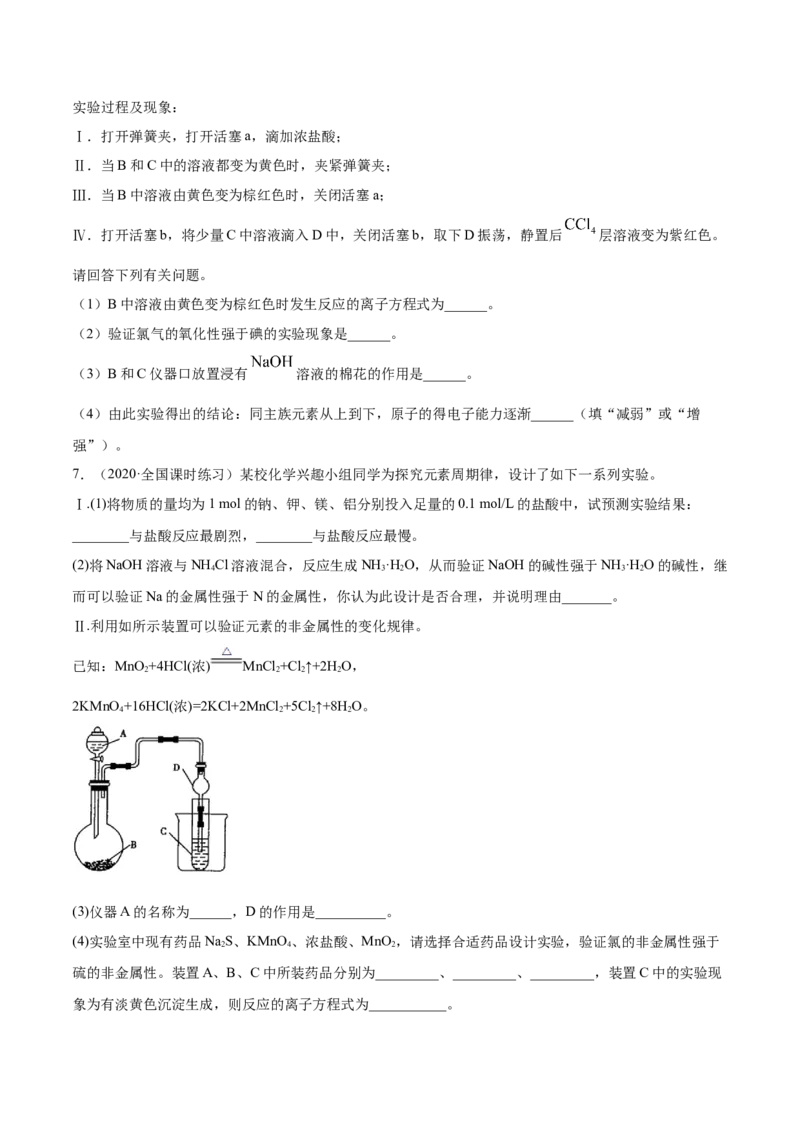
Ⅱ.利用如所示装置可以验证元素的非金属性的变化规律。
已知:MnO +4HCl(浓) MnCl +Cl↑+2H O,
2 2 2 2
2KMnO +16HCl(浓)=2KCl+2MnCl +5Cl↑+8H O。
4 2 2 2
(3)仪器A的名称为______,D的作用是__________。
(4)实验室中现有药品NaS、KMnO 、浓盐酸、MnO ,请选择合适药品设计实验,验证氯的非金属性强于
2 4 2
硫的非金属性。装置A、B、C中所装药品分别为_________、_________、_________,装置C中的实验现
象为有淡黄色沉淀生成,则反应的离子方程式为___________。(5)若要证明非金属性C>Si,则A中应加入________溶液,B中应加入NaCO,C中应加入______溶液,
2 3
装置C中的现象为________。