文档内容
合格演练测评(九)
(硫、氮及其化合物)
姓名: 班级: 正确率:
题号 1 2 3 4 5 6 7 8 9 10
答案
题号 11 12 13 14 15 16 17 18 19 20
答案
一、单项选择题
1.下列关于氨气的说法中,正确的是( )
A.氨可以用浓硫酸干燥
B.氨溶于水显弱碱性,因此氨气可使湿润的酚酞试纸变蓝
C.氨本身没有毒,故发生液氨大量泄漏时,人们也不必采取任何防范措施
D.用水吸收NH 用如图所示的装置可防止倒吸
3
答案:D
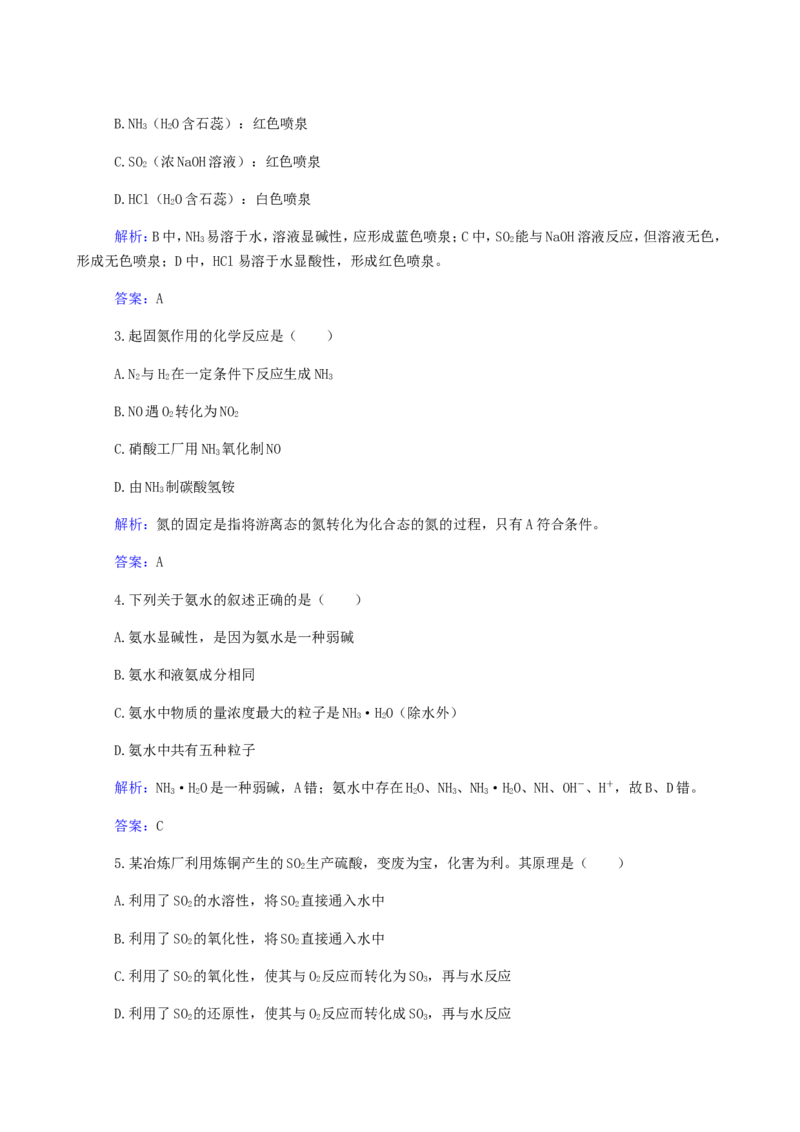
2.如图装置中,干燥烧瓶内盛有某种气体,烧杯和胶头滴管内盛放某种溶液。挤压胶头滴管的胶头,
下列与实验事实相符的是( )
A.CO(浓NaOH溶液):无色喷泉
2B.NH(HO含石蕊):红色喷泉
3 2
C.SO(浓NaOH溶液):红色喷泉
2
D.HCl(HO含石蕊):白色喷泉
2
解析:B中,NH 易溶于水,溶液显碱性,应形成蓝色喷泉;C中,SO 能与NaOH溶液反应,但溶液无色,
3 2
形成无色喷泉;D中,HCl易溶于水显酸性,形成红色喷泉。
答案:A
3.起固氮作用的化学反应是( )
A.N 与H 在一定条件下反应生成NH
2 2 3
B.NO遇O 转化为NO
2 2
C.硝酸工厂用NH 氧化制NO
3
D.由NH 制碳酸氢铵
3
解析:氮的固定是指将游离态的氮转化为化合态的氮的过程,只有A符合条件。
答案:A
4.下列关于氨水的叙述正确的是( )
A.氨水显碱性,是因为氨水是一种弱碱
B.氨水和液氨成分相同
C.氨水中物质的量浓度最大的粒子是NH·HO(除水外)
3 2
D.氨水中共有五种粒子
解析:NH·HO是一种弱碱,A错;氨水中存在HO、NH、NH·HO、NH、OH-、H+,故B、D错。
3 2 2 3 3 2
答案:C
5.某冶炼厂利用炼铜产生的SO 生产硫酸,变废为宝,化害为利。其原理是( )
2
A.利用了SO 的水溶性,将SO 直接通入水中
2 2
B.利用了SO 的氧化性,将SO 直接通入水中
2 2
C.利用了SO 的氧化性,使其与O 反应而转化为SO,再与水反应
2 2 3
D.利用了SO 的还原性,使其与O 反应而转化成SO,再与水反应
2 2 3解析:利用SO 生产硫酸发生的反应为:2SO+O2SO(被氧气氧化,体现还原性),SO+HO===HSO。
2 2 2 3 3 2 2 4
答案:D
6.香烟烟雾中往往含有CO和SO 气体,下列关于这两种气体的说法正确的是( )
2
A.两者都污染环境,危害健康
B.两者都是形成酸雨的主要物质
C.两者都能使品红溶液褪色
D.两者都易溶于水
解析:CO不能生成酸,不会形成酸雨,难溶于水,无漂白性,不能使品红溶液褪色,只有A选项正确。
答案:A
7.下列溶液中能够区别SO 和CO 气体的是( )
2 2
①澄清石灰水 ②HS溶液 ③酸性KMnO 溶液
2 4
④新制氯水 ⑤品红溶液
A.①②③ B.②③④
C.除①外 D.全部
解析:SO 和CO 都属于酸性氧化物,都能使澄清石灰水变浑浊。SO 具有氧化性,能将HS氧化成硫单
2 2 2 2
质(出现淡黄色浑浊);SO 具有还原性,能被酸性KMnO 溶液和新制氯水氧化(溶液褪色);SO 具有漂白性,能
2 4 2
使品红溶液褪色。而CO 没有这些性质。所以可以用②③④⑤来区别SO 和CO。
2 2 2
答案:C
8.下列关于硫酸的叙述正确的是( )
A.浓硫酸具有吸水性
B.稀硫酸可用铁罐贮存
C.稀硫酸能使蔗糖脱水
D.SO 溶于水,可得到稀硫酸
2
答案:A
9.下列物质中,硫元素的化合价为+4的是( )
A.NaSO B.SO
2 3 3C.NaSO D.HSO
2 4 2 4
答案:A
10.检验氨气可选用( )
A.湿润的蓝色石蕊试纸
B.干燥的红色石蕊试纸
C.干燥的蓝色石蕊试纸
D.湿润的红色石蕊试纸
解析:氨气溶于水显碱性,故氨气能使红色石蕊试纸变蓝,可用湿润的红色石蕊试纸检验氨气,D项正
确。
答案:D
11.将某无色气体X通入品红溶液,溶液褪色;加热,溶液又变红色。X可能是( )
A.O B.SO
2 2
C.Cl D.CO
2 2
解析:SO 与品红化合生成不稳定的无色物质,加热又分解,恢复红色。
2
答案:B
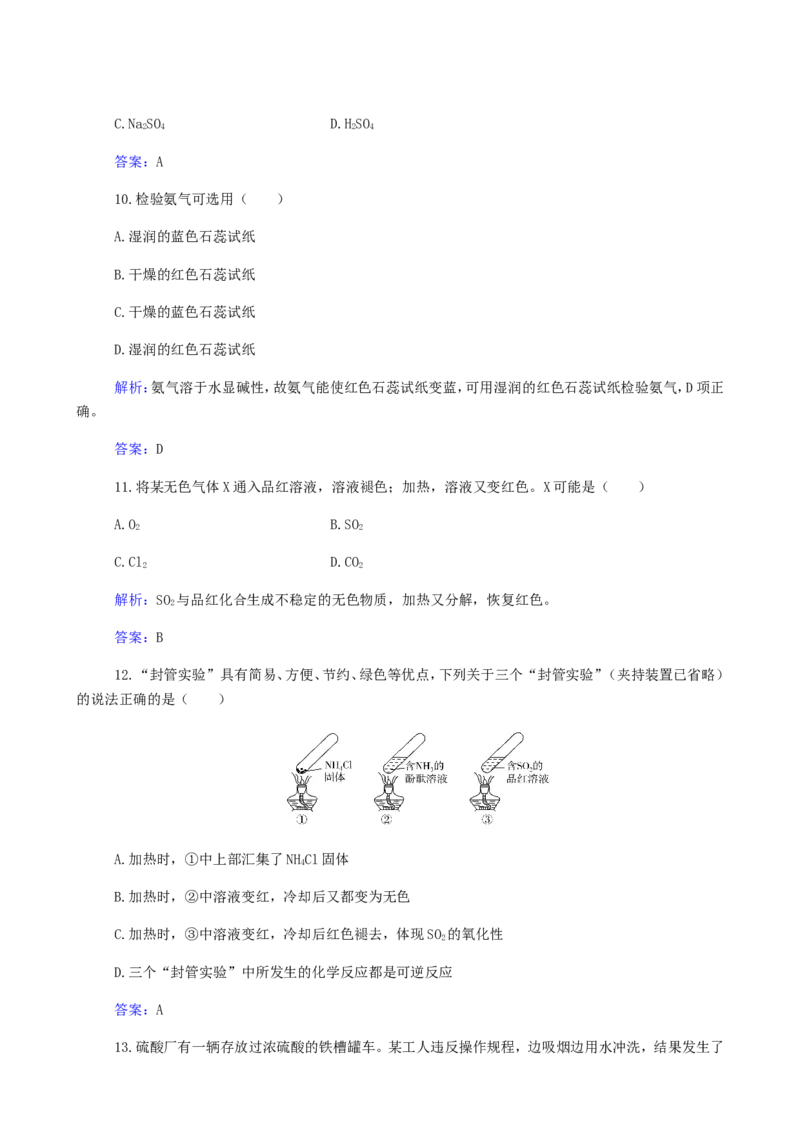
12.“封管实验”具有简易、方便、节约、绿色等优点,下列关于三个“封管实验”(夹持装置已省略)
的说法正确的是( )
A.加热时,①中上部汇集了NHCl固体
4
B.加热时,②中溶液变红,冷却后又都变为无色
C.加热时,③中溶液变红,冷却后红色褪去,体现SO 的氧化性
2
D.三个“封管实验”中所发生的化学反应都是可逆反应
答案:A
13.硫酸厂有一辆存放过浓硫酸的铁槽罐车。某工人违反操作规程,边吸烟边用水冲洗,结果发生了爆炸事故。下列对引起爆炸的原因分析正确的是( )
A.浓硫酸遇明火爆炸
B.浓硫酸遇水发热,爆炸
C.铁与水反应产生氢气,接触空气,遇明火爆炸
D.稀释后的硫酸与铁反应,产生的氢气接触空气,遇明火爆炸
答案:D
14.下列有关二氧化硫的说法中,错误的是( )
A.二氧化硫能使品红溶液褪色
B.二氧化硫是无色、无味有毒气体
C.二氧化硫可以形成酸雨
D.二氧化硫不可用于漂白食物
答案:B
15.下列气体遇空气变红棕色的是( )
A.SO B.Cl
2 2
C.CO D.NO
2
解析:2NO+O===2NO,NO 呈红棕色。
2 2 2
答案:D
16.工业上用洗净的废铜屑作原料制备硝酸铜,为节约原料和防止污染,宜采取的方法是( )
A.Cu+HNO(浓)→Cu(NO)
3 3 2
B.Cu+HNO(稀)→Cu(NO)
3 3 2
C.Cu→CuO→Cu(NO)
3 2
D.Cu→CuSO→Cu(NO)
4 3 2
解析:利用Cu+HNO(浓)→Cu(NO) 制取Cu(NO),既浪费HNO、又会产生污染气体NO,故不选A;利
3 3 2 3 2 3 2
用 Cu+HNO(稀)→Cu(NO) 制取 Cu(NO) ,既浪费 HNO 、又会产生污染气体 NO,故不选 B;利用
3 3 2 3 2 3
Cu→CuO→Cu(NO) 制取Cu(NO) ,能充分利用HNO ,且无污染,故选C;利用Cu→CuSO→Cu(NO) 制取
3 2 3 2 3 4 3 2
Cu(NO),该过程生成有毒气体SO 且浪费浓硫酸、硝酸钡,故不选D。
3 2 2答案:C
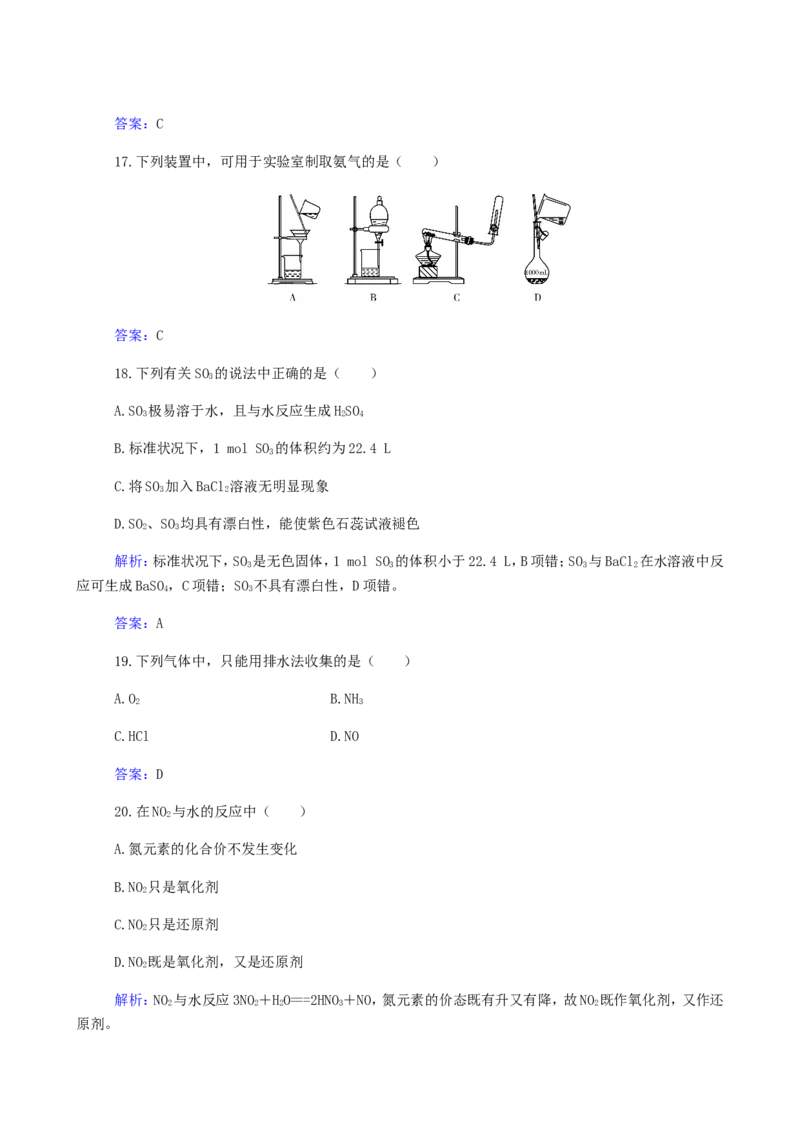
17.下列装置中,可用于实验室制取氨气的是( )
答案:C
18.下列有关SO 的说法中正确的是( )
3
A.SO 极易溶于水,且与水反应生成HSO
3 2 4
B.标准状况下,1 mol SO 的体积约为22.4 L
3
C.将SO 加入BaCl 溶液无明显现象
3 2
D.SO、SO 均具有漂白性,能使紫色石蕊试液褪色
2 3
解析:标准状况下,SO 是无色固体,1 mol SO 的体积小于22.4 L,B项错;SO 与BaCl 在水溶液中反
3 3 3 2
应可生成BaSO,C项错;SO 不具有漂白性,D项错。
4 3
答案:A
19.下列气体中,只能用排水法收集的是( )
A.O B.NH
2 3
C.HCl D.NO
答案:D
20.在NO 与水的反应中( )
2
A.氮元素的化合价不发生变化
B.NO 只是氧化剂
2
C.NO 只是还原剂
2
D.NO 既是氧化剂,又是还原剂
2
解析:NO 与水反应3NO+HO===2HNO+NO,氮元素的价态既有升又有降,故NO 既作氧化剂,又作还
2 2 2 3 2
原剂。答案:D
二、非选择题
21.某化学实验小组同学利用以下实验装置制取氨气,并探究氨气的性质(部分仪器已略去)。请回答:
(1)实验室制备氨气的化学方程式为____________
____________________________________________________。
(2)用装置B收集氨气时,应选择氨气的进气口是 (填“a”或“b”),并说明选择的理由是
__________________
_____________________________________________________。
(3)打开装置B中的止水夹c,若观察到烧瓶内产生了红色喷泉,则说明氨气具有的性质是
____________________________
___________________________________________________。
(4)为防止环境污染,以下装置(盛放的液体均为水)可用于吸收多余氨气的是 (填序号)。
解析:(1)实验室制取氨气的方程式为2NHCl+Ca(OH)=====CaCl+2NH↑+2HO。(2)氨气比空气的
4 2 2 3 2
密度小,可用向下排空气法收集,导气管要伸入烧瓶底部。(3)能形成喷泉,证明氨气极易溶于水,酚酞变红,
说明氨气的水溶液显碱性。(4)①不利于氨气的吸收,②、④能防止倒吸,③易发生倒吸。
答案:(1)2NHCl+Ca(OH)=====CaCl+2NH↑+2HO (2)a 氨气密度比空气密度小 (3)极易溶于
4 2 2 3 2
水与水反应生成碱 (4)②④
22.某无色气体A中可能含有Cl、SO、CO、HCl气体中的一种或几种。
2 2 2
(1)将此气体通入氯水后溶液变得无色透明。(2)将得到的溶液分为两份:①其中一份取出少量在试管中,加入用盐酸酸化的BaCl 溶液,出现白色
2
沉淀。
②另一份取出少量加入用硝酸酸化的AgNO 溶液,也得到白色沉淀。
3
试回答:
(1)气体A中肯定含有的气体是 ,理由是_________
____________________________________________________。
(2)气体A中肯定不存在的气体是 ,理由是_______
____________________________________________________。
(3)气体A中不一定存在的气体是 。
解析:无色气体说明一定不含Cl;①实验说明一定含SO,②实验说明含Cl-,但氯水中含Cl-,不确
2 2
定含HCl。
答案:(1)SO 气体通入氯水后溶液变得无色透明,且加入用盐酸酸化的BaCl 溶液,出现白色沉淀
2 2
(2)Cl Cl 为黄绿色气体 (3)CO,HCl
2 2 2
23.观察如图装置,回答下列问题:
(1)在⑥中发生的化学反应方程式为_____________________
____________________________________________________。
(2)①中的实验现象为紫色石蕊试液 ,此实验证明SO 是 气体。
2
(3)②中的品红溶液 ,证明SO 有 性。
2
(4)③中实验现象是_________________________________,
证明SO 有 性。
2
(5)④中实验现象是_________________________________,
证明SO 有 性。
2(6)⑤中反应的离子方程式为________________________
___________________________________________________。
解析:NaSO 和浓HSO 反应生成SO 气体,SO 为酸性气体,能使紫色石蕊试液变红。由于具有漂白性,
2 3 2 4 2 2
能使品红溶液褪色。SO 具有氧化性,与HS反应生成S单质。SO 具有还原性,能使酸性KMnO 溶液褪色。因
2 2 2 4
SO 有毒,应用NaOH溶液吸收。
2
答案:(1)NaSO+HSO(浓)===NaSO+SO↑+HO (2)变红色 酸性 (3)褪色 漂白 (4)有淡黄
2 3 2 4 2 4 2 2
色沉淀生成 氧化 (5)酸性KMnO 溶液褪色 还原 (6)SO+2OH-===SO+HO
4 2 2