文档内容
专题一 物质的分类与转化 基础过关检测
考试时间:70分钟 卷面分值:100分
学校:___________姓名:___________班级:___________考号:___________
注意事项:
1.答题前,务必将自己的姓名、考号填写在答题卡规定的位置上。
2.答选择题时,必须使用2B铅笔将答题卡上对应题目的答案标号涂黑。如需改动,用
橡皮擦擦干净后,再选涂其它答案标号。
3.答非选择题时,必须将答案书写在专设答题页规定的位置上。
4.所有题目必须在答题卡上作答。在试题卷上答题无效。
5.考试结束后,只交试卷答题页。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 S-32 Cl-35.5
一、选择题(本题含16小题,每题3分,共48分。每题只有一个选项符合题意)
1.(2022·浙江·模拟预测)下列抗疫物资中,主要成分属于盐的是
A.医用酒精 B.漂粉精 C.塑料护目镜 D.医用橡胶手套
2.(2022秋·福建厦门·高三厦门市湖滨中学校考期中)分类是认识和研究物质及其变
化的一种常用的科学方法。下列说法正确的是
A.烧碱和纯碱均属于碱
B. 溶液与淀粉溶液不可以利用丁达尔效应区分
C. 能电离出 ,所以 属于酸
D.“熬胆矾铁釜,久之亦化为铜”中的反应是氧化还原反应
3.(2022·湖南岳阳·统考模拟预测)下列物质的分类正确的是
A.共价化合物:HO、HT、HSO
2 2 4
B.强电解质:AgCl、Ca(OH) 、AlCl
2 3
C.同系物:乙烯、1,3-丁二烯、足球烯
D.天然高分子化合物:淀粉、蛋白质、油脂
4.下列逻辑关系图示中正确的是
A. B. C. D.A.A B.B C.C D.D
5.(2023·辽宁·校联考一模)胶体金具有比较良好的性能,现在制备出了一种直径为
10.0nm的一种胶体金,金的密度为19.3g cm-3,则一个胶体粒子中含有的金原子的数目
约为
A. B. C. D.
6.(2022·全国·高三专题练习)下列有关物质分类或归类中,正确的是
①胶体:碳纳米管(具有纳米尺度的直径)、氢氧化铁胶体、淀粉溶液
②纯净物:硝酸、液氯、冰水混合物
③化合物:CaCl 、NaOH、HCl、HD
2
④共价晶体:金刚石、NaO、BN、SiO
2 2
⑤电解质:明矾[KAl(SO)•12H O]、石膏、硫酸、纯碱
4 2 2
⑥同素异形体:C 、C 、金刚石、石墨烯
60 70
A.②⑤⑥ B.①③⑥ C.①⑤⑥ D.③⑤⑥
7.(2022·全国·高三专题练习)“矾”是一类金属硫酸盐的结晶水合物,在生活和生
产中有着重要应用,下列有关“矾”的说法正确的是
A.蓝矾(CuSO ·5H O)是一种纯净物,可用于检验酒精中是否含有水
4 2
B.明矾[KAl(SO)·12H O]常用于净水,其水溶液显中性
4 2 2
C.铁铵矾[NH Fe(SO )·12H O]是一种媒染剂,其中Fe的化合价为+3价
4 4 2 2
D.皓矾(ZnSO·7H O)常用作医学收敛剂,铁单质与其溶液反应能置换出Zn
4 2
8.铁元素是重要的金属元素,含有铁元素的物质,在人类的生产生活中有着重要的应
用。 是炼铁工业中的主反应。
在指定条件下,下列选项所示的物质间转化能实现的是
A.
B. (胶体)
试卷第2页,共8页C.
D.
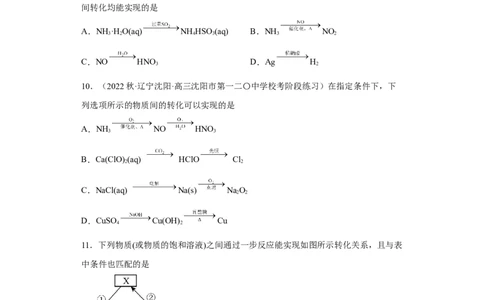
9.(2022·全国·高三专题练习)氮及其化合物在生产生活中具有广泛的应用。氨气可
用于生产氮肥和处理NO 等气体,氨水可用于吸收SO ,NO 可用于制取硝酸,硝酸可
x 2 x
洗涤试管上的银镜。NO 能与悬浮在大气中海盐粒子相互作用,反应为
2
2NO +NaCl=NaNO +ClNO(ClNO中N为中心原子,各原子均达到8电子稳定结构)。
2 3
NO能被FeSO 溶液吸收生成[Fe(NO)HO) ]SO 。在给定条件下,下列选项所示的物质
4 2 5 4
间转化均能实现的是
A.NH ·H O(aq) NH HSO (aq) B.NH NO
3 2 4 3 3 2
C.NO HNO D.Ag H
3 2
10.(2022秋·辽宁沈阳·高三沈阳市第一二〇中学校考阶段练习)在指定条件下,下
列选项所示的物质间的转化可以实现的是
A.NH NO HNO
3 3
B.Ca(ClO) (aq) HClO Cl
2 2
C.NaCl(aq) Na(s) NaO
2 2
D.CuSO Cu(OH) Cu
4 2
11.下列物质(或物质的饱和溶液)之间通过一步反应能实现如图所示转化关系,且与表
中条件也匹配的是
选项 X Y Z 箭头上为反应条件或试剂
A Fe FeCl FeCl ①通入少量Cl
2 3 2
B NaCO NaCl NaHCO ③先通NH 、再通CO
2 3 3 3 2
C Na NaOH NaCl ②电解饱和食盐水D Si NaSiO HSiO ②加热
2 3 2 3
A.A B.B C.C D.D
12.在给定条件下,下列选项所示的物质间转化均能实现的是
A.
B.
C.FeS SO (g) HSO (aq)
2 3 2 4
D.
13.(2022秋·宁夏石嘴山·高三平罗中学校考阶段练习)在给定条件下,下列物质间
的转化均能一步实现的是
A.
B.
C.
D.
14.(2022·江苏·模拟预测)在指定条件下,下列选项所示的物质间转化能实现的是
A.CO(g) NaHCO (aq)
2 3
B.CO(g) NaCO(s)
2 2 3
C.CO(g) Mg(s)
D.CO(g) N(g)
2
15.(2023秋·湖南株洲·高三校考期末)关于分散系,下列叙述中不正确的是
A.直径介于 之间的微粒称为胶体
B.电泳现象不可证明胶体带电荷,因为胶体表面积较大,胶体粒子能吸附电荷而带电
C.利用丁达尔效应可以区别溶液与胶体
D.放电影时,放映机到银幕间光柱的形成也是因为丁达尔效应
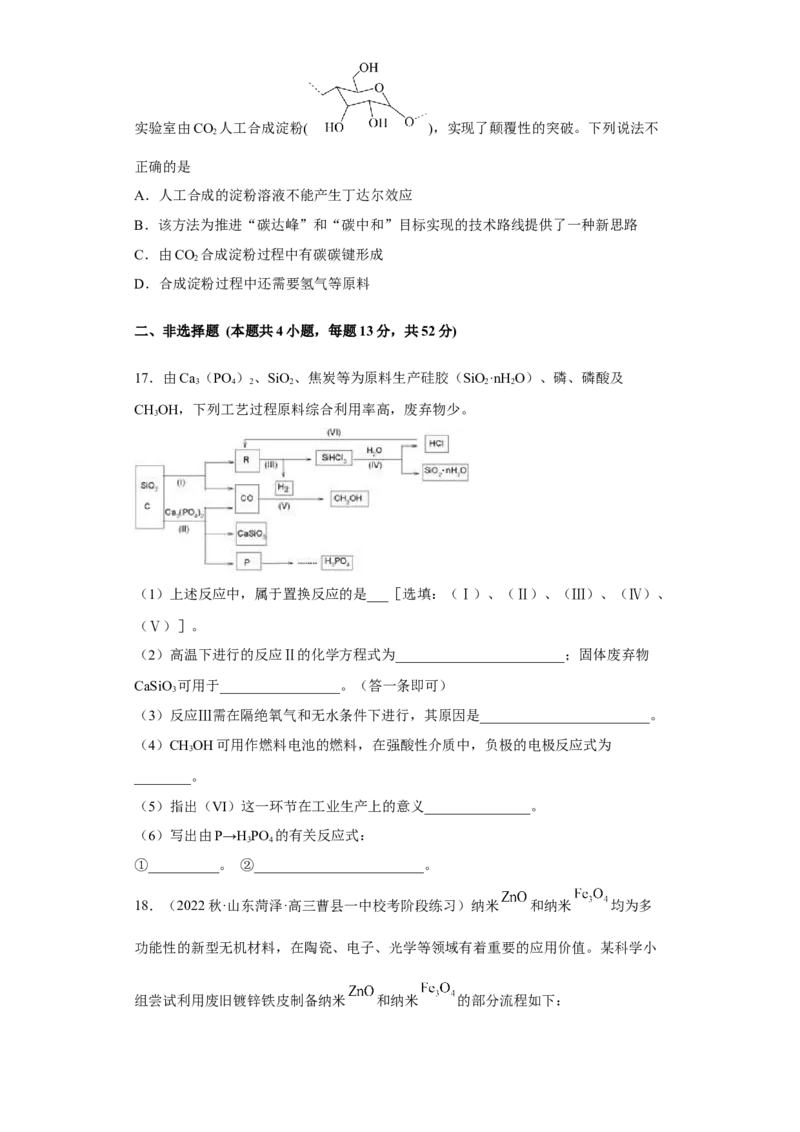
16.(2021秋·陕西汉中·高三校联考阶段练习)2021年9月,我国科学家宣布首次在
试卷第4页,共8页实验室由CO 人工合成淀粉( ),实现了颠覆性的突破。下列说法不
2
正确的是
A.人工合成的淀粉溶液不能产生丁达尔效应
B.该方法为推进“碳达峰”和“碳中和”目标实现的技术路线提供了一种新思路
C.由CO 合成淀粉过程中有碳碳键形成
2
D.合成淀粉过程中还需要氢气等原料
二、非选择题 (本题共4小题,每题13分,共52分)
17.由Ca (PO )、SiO、焦炭等为原料生产硅胶(SiO·nH O)、磷、磷酸及
3 4 2 2 2 2
CHOH,下列工艺过程原料综合利用率高,废弃物少。
3
(1)上述反应中,属于置换反应的是___[选填:(Ⅰ)、(Ⅱ)、(Ⅲ)、(Ⅳ)、
(Ⅴ)]。
(2)高温下进行的反应Ⅱ的化学方程式为________________________;固体废弃物
CaSiO 可用于_________________。(答一条即可)
3
(3)反应Ⅲ需在隔绝氧气和无水条件下进行,其原因是________________________。
(4)CHOH可用作燃料电池的燃料,在强酸性介质中,负极的电极反应式为
3
________。
(5)指出(VI)这一环节在工业生产上的意义_______________。
(6)写出由P→H PO 的有关反应式:
3 4
①__________。 ②________________________。
18.(2022秋·山东菏泽·高三曹县一中校考阶段练习)纳米 和纳米 均为多
功能性的新型无机材料,在陶瓷、电子、光学等领域有着重要的应用价值。某科学小
组尝试利用废旧镀锌铁皮制备纳米 和纳米 的部分流程如下:已知:Zn及其化合物的性质与Al及其化合物的性质相似。
请回答下列问题:
(1)铁皮镀锌在金属的电化学防护中属于_______法。
(2)调节滤液pH时,pH不能太低的原因为_______(用离子方程式表示)。
(3)向“碱浸”后得到的滤渣中加入过量稀硫酸时,硫酸不能过量太多的原因为_______。
(4)写出“氧化”阶段的离子方程式:_______;“加热沉铁”阶段需要持续通入 ,
其原因为_______。
(5)若“分离”阶段在实验室中进行,可选用的实验装置为_______(填字母)。
19.(2020秋·宁夏固原·高三固原一中校考阶段练习)氟化铬可用作毛织品防蛀剂、
卤化催化剂、大理石硬化及着色剂。以铬云母矿石(含4.5%Cr O,还含Fe O、FeO、
2 3 2 3
MgO、SiO)为原料制备氟化铬的工艺流程如下。
2
下表列出了相关金属离子生成氢氧化物沉淀的pH:
氢氧化物 Fe(OH) Mg(OH) Cr(OH) Fe(OH)
3 2 3 2
开始沉淀的pH 2.3 8.8 4.9 7.5
沉淀完全的pH 4.1 10.4 6.8 9.7
请回答下列问题:
(1)Fe O、MgO、FeO、SiO 中属于碱性氧化物的有___种。
2 3 2
(2)将铬云母矿石粉碎的目的是___。
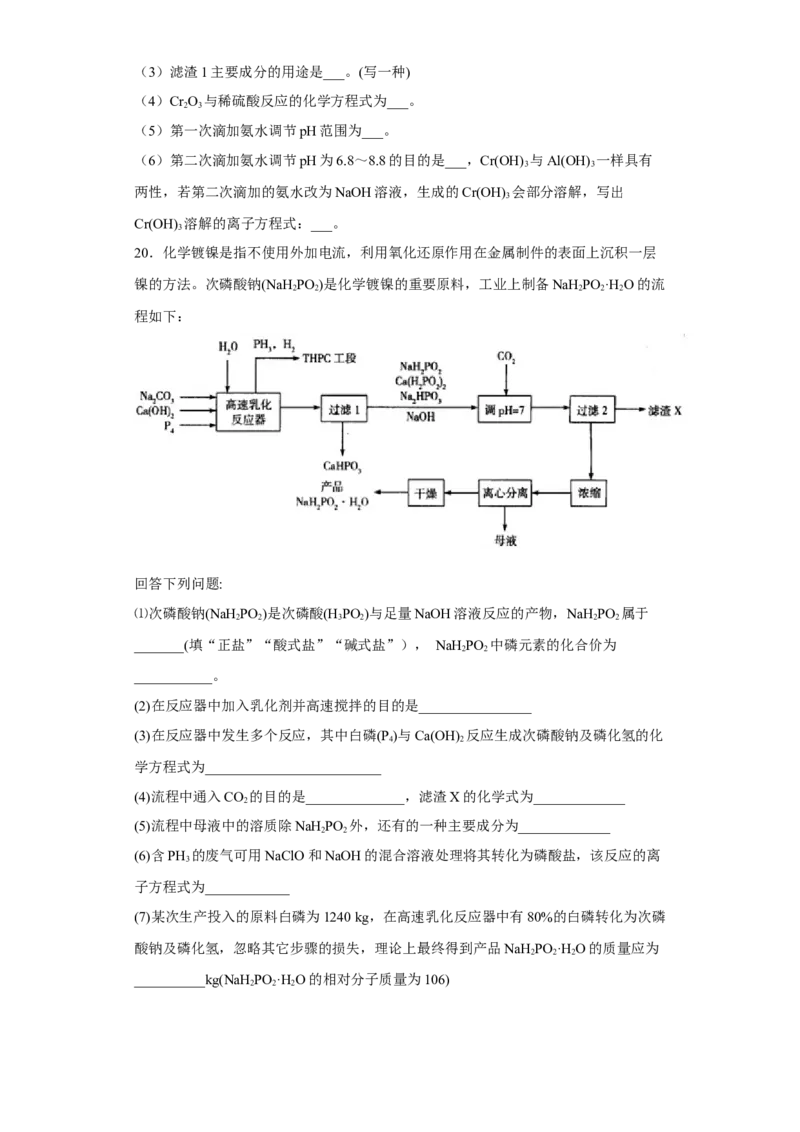
试卷第6页,共8页(3)滤渣1主要成分的用途是___。(写一种)
(4)Cr O 与稀硫酸反应的化学方程式为___。
2 3
(5)第一次滴加氨水调节pH范围为___。
(6)第二次滴加氨水调节pH为6.8~8.8的目的是___,Cr(OH) 与Al(OH) 一样具有
3 3
两性,若第二次滴加的氨水改为NaOH溶液,生成的Cr(OH) 会部分溶解,写出
3
Cr(OH) 溶解的离子方程式:___。
3
20.化学镀镍是指不使用外加电流,利用氧化还原作用在金属制件的表面上沉积一层
镍的方法。次磷酸钠(NaH PO )是化学镀镍的重要原料,工业上制备NaH PO ·H O的流
2 2 2 2 2
程如下:
回答下列问题:
⑴次磷酸钠(NaH PO )是次磷酸(H PO )与足量NaOH溶液反应的产物,NaH PO 属于
2 2 3 2 2 2
_______(填“正盐”“酸式盐”“碱式盐”), NaH PO 中磷元素的化合价为
2 2
___________。
(2)在反应器中加入乳化剂并高速搅拌的目的是________________
(3)在反应器中发生多个反应,其中白磷(P )与Ca(OH) 反应生成次磷酸钠及磷化氢的化
4 2
学方程式为_________________________
(4)流程中通入CO 的目的是______________,滤渣X的化学式为_____________
2
(5)流程中母液中的溶质除NaH PO 外,还有的一种主要成分为_____________
2 2
(6)含PH 的废气可用NaClO和NaOH的混合溶液处理将其转化为磷酸盐,该反应的离
3
子方程式为____________
(7)某次生产投入的原料白磷为1240 kg,在高速乳化反应器中有80%的白磷转化为次磷
酸钠及磷化氢,忽略其它步骤的损失,理论上最终得到产品NaH PO ·H O的质量应为
2 2 2
__________kg(NaH PO ·H O的相对分子质量为106)
2 2 2试卷第8页,共8页