文档内容
晶体类型与性质 晶体结构
(一)常见的几种典型晶体的主要性质
化学式 晶体类型 微粒间作用力 熔、沸点
CO 分子晶体 分子间作用力 较低
2
分子间作
H O(冰) 分子晶体 较低
2
用力和氢键
NaCl 离子晶体 离子键 较高
CsCl 离子晶体 离子键 较高
C(金刚石) 共价晶体 共价键 很高
SiO 共价晶体 共价键 高
2
(二)晶体结构与晶胞计算
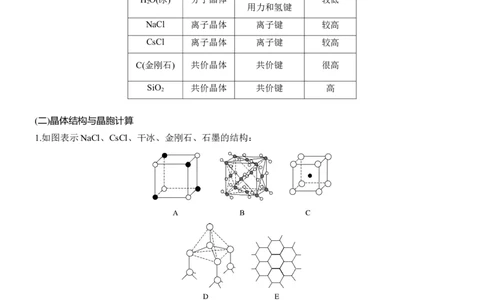
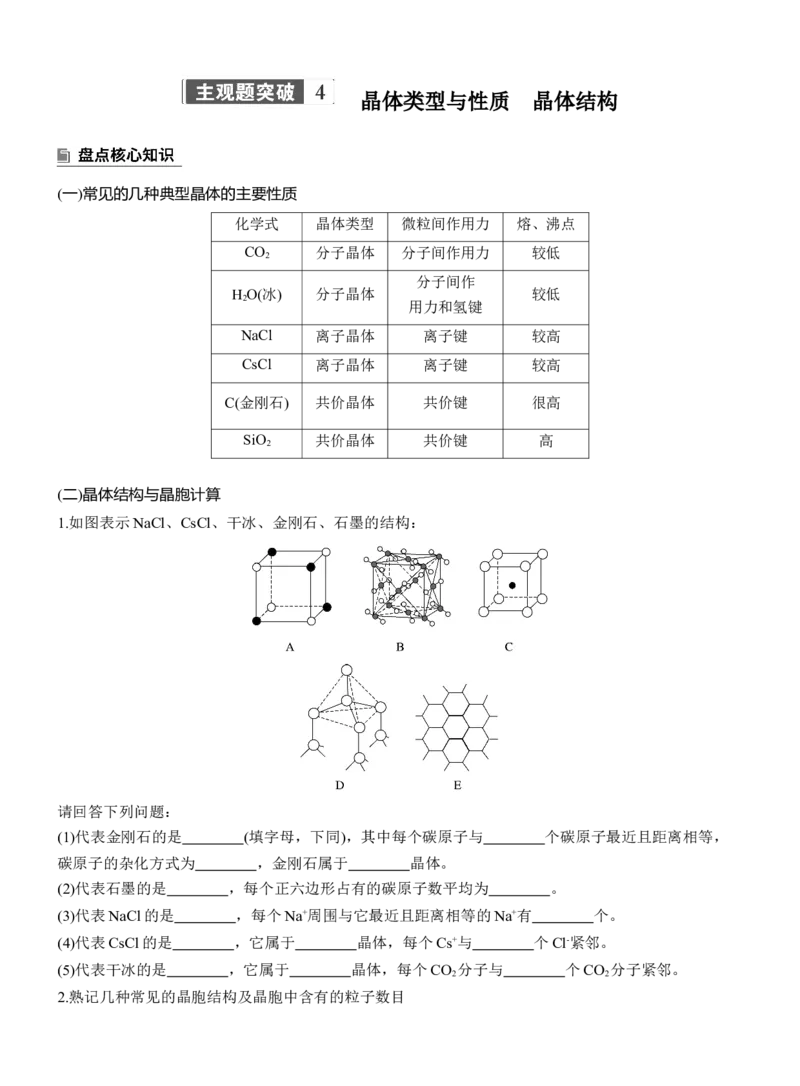
1.如图表示NaCl、CsCl、干冰、金刚石、石墨的结构:
请回答下列问题:
(1)代表金刚石的是 (填字母,下同),其中每个碳原子与 个碳原子最近且距离相等,
碳原子的杂化方式为 ,金刚石属于 晶体。
(2)代表石墨的是 ,每个正六边形占有的碳原子数平均为 。
(3)代表NaCl的是 ,每个Na+周围与它最近且距离相等的Na+有 个。
(4)代表CsCl的是 ,它属于 晶体,每个Cs+与 个Cl-紧邻。
(5)代表干冰的是 ,它属于 晶体,每个CO 分子与 个CO 分子紧邻。
2 2
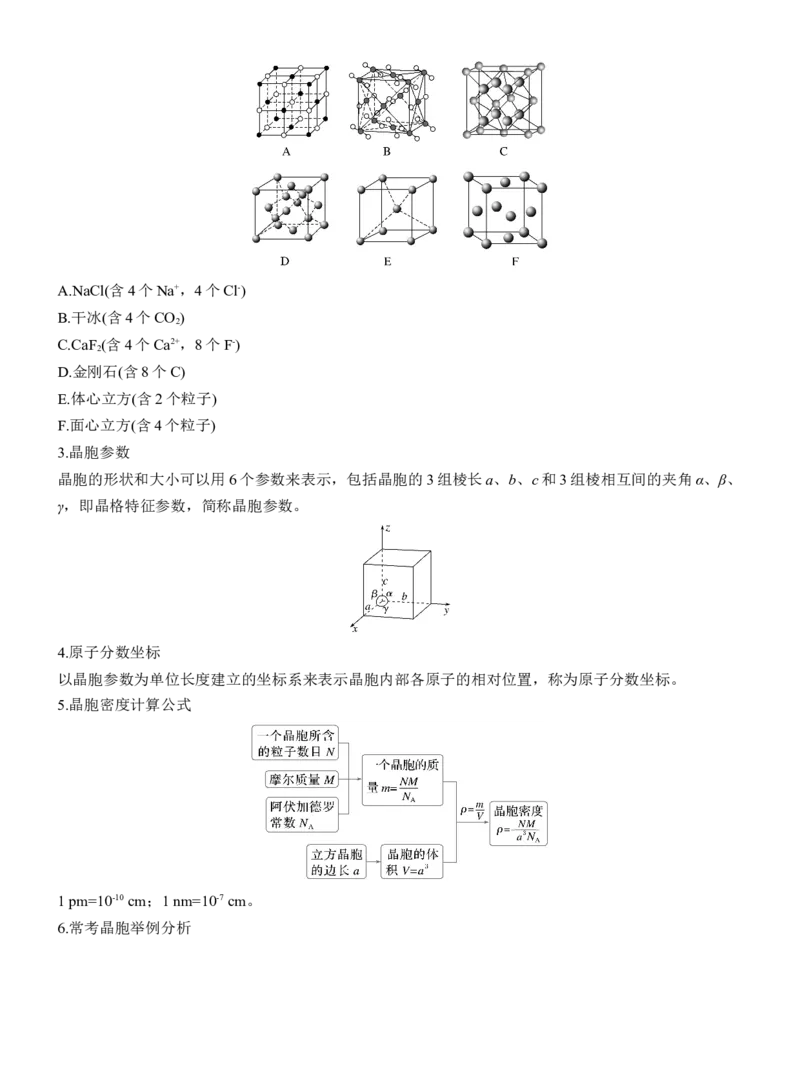
2.熟记几种常见的晶胞结构及晶胞中含有的粒子数目A.NaCl(含4个Na+,4个Cl-)
B.干冰(含4个CO )
2
C.CaF (含4个Ca2+,8个F-)
2
D.金刚石(含8个C)
E.体心立方(含2个粒子)
F.面心立方(含4个粒子)
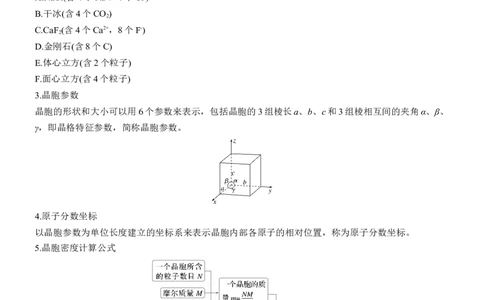
3.晶胞参数
晶胞的形状和大小可以用6个参数来表示,包括晶胞的3组棱长a、b、c和3组棱相互间的夹角α、β、
γ,即晶格特征参数,简称晶胞参数。
4.原子分数坐标
以晶胞参数为单位长度建立的坐标系来表示晶胞内部各原子的相对位置,称为原子分数坐标。
5.晶胞密度计算公式
1 pm=10-10 cm;1 nm=10-7 cm。
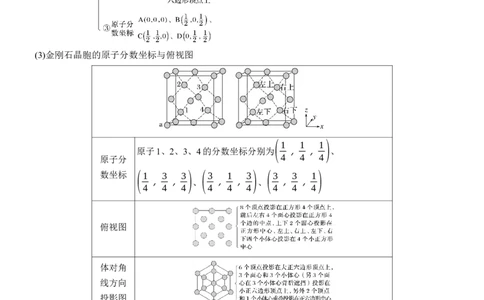
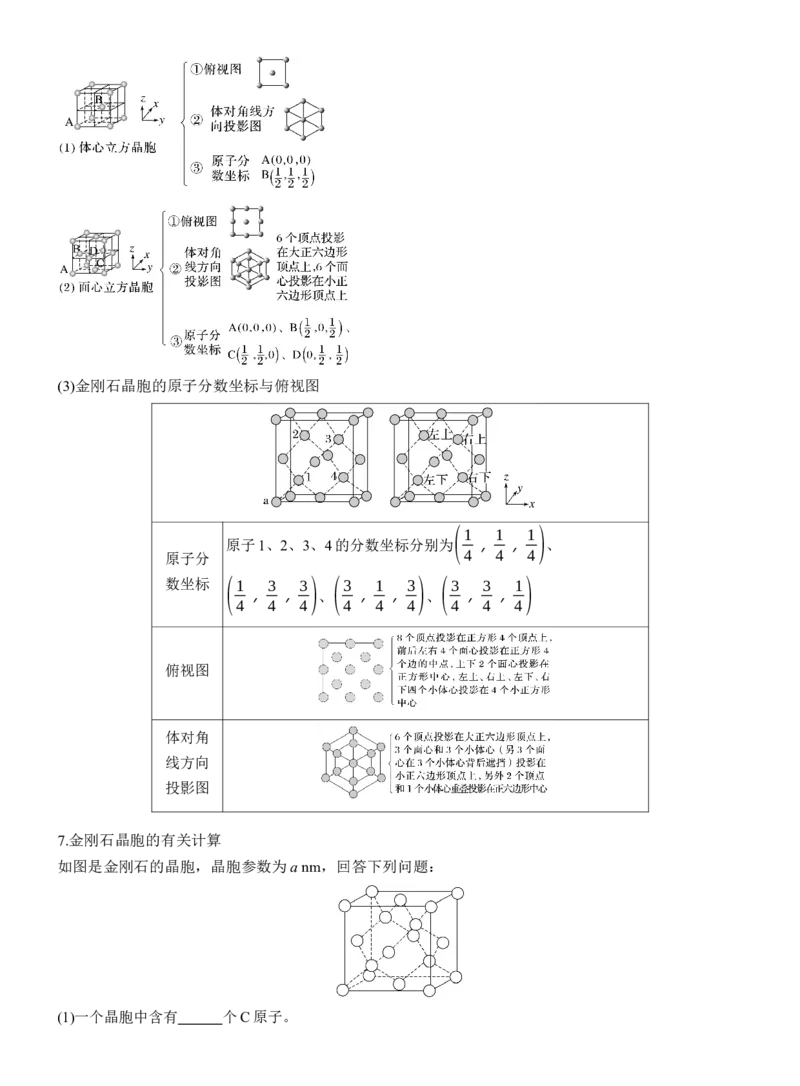
6.常考晶胞举例分析(3)金刚石晶胞的原子分数坐标与俯视图
(1 1 1)
原子1、2、3、4的分数坐标分别为 , , 、
原子分 4 4 4
数坐标 (1 3 3) (3 1 3) (3 3 1)
, , 、 , , 、 , ,
4 4 4 4 4 4 4 4 4
俯视图
体对角
线方向
投影图
7.金刚石晶胞的有关计算
如图是金刚石的晶胞,晶胞参数为a nm,回答下列问题:
(1)一个晶胞中含有 个C原子。(2)1 mol金刚石含有 mol C—C。
(3)最近的C原子之间距离为 nm(用a表示)。
(4)每个C原子的半径为 nm(用a表示)。
(5)晶胞密度为 g·cm-3。
(6)空间利用率为 。
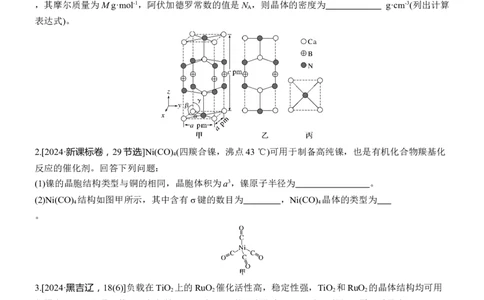
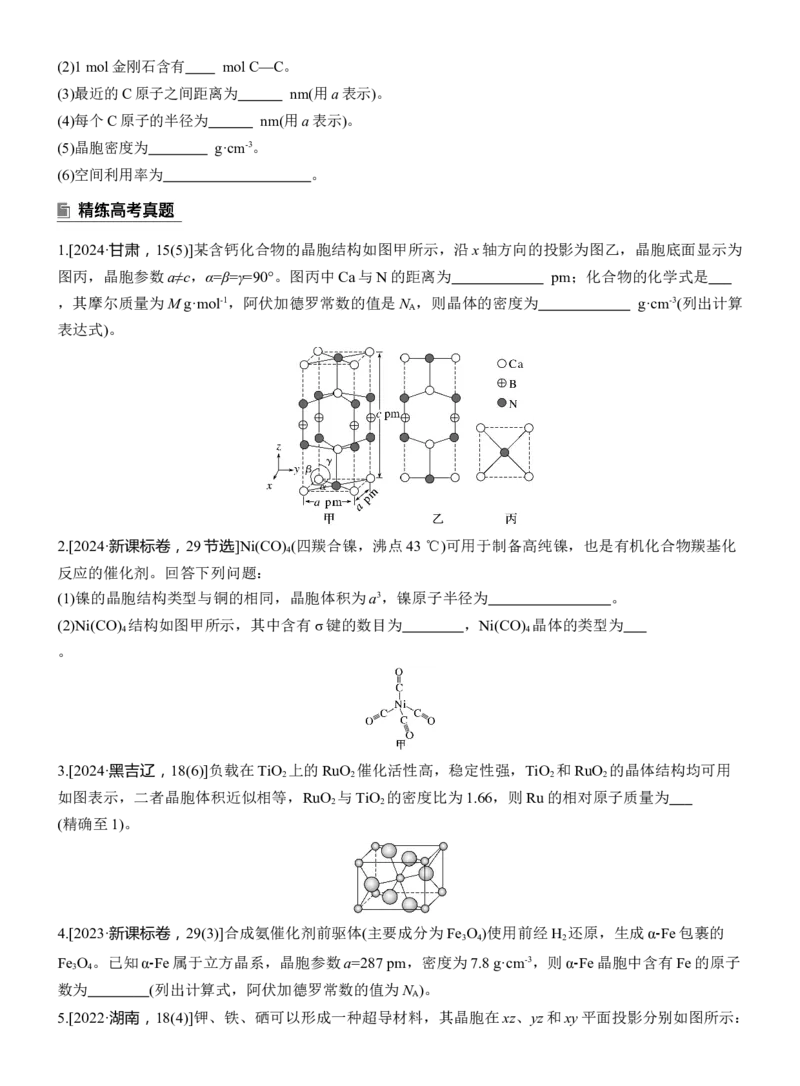
1.[2024·甘肃,15(5)]某含钙化合物的晶胞结构如图甲所示,沿x轴方向的投影为图乙,晶胞底面显示为
图丙,晶胞参数a≠c,α=β=γ=90°。图丙中Ca与N的距离为 pm;化合物的化学式是
,其摩尔质量为M g·mol-1,阿伏加德罗常数的值是N ,则晶体的密度为 g·cm-3(列出计算
A
表达式)。
2.[2024·新课标卷,29节选]Ni(CO) (四羰合镍,沸点43 ℃)可用于制备高纯镍,也是有机化合物羰基化
4
反应的催化剂。回答下列问题:
(1)镍的晶胞结构类型与铜的相同,晶胞体积为a3,镍原子半径为 。
(2)Ni(CO) 结构如图甲所示,其中含有σ键的数目为 ,Ni(CO) 晶体的类型为
4 4
。
3.[2024·黑吉辽,18(6)]负载在TiO 上的RuO 催化活性高,稳定性强,TiO 和RuO 的晶体结构均可用
2 2 2 2
如图表示,二者晶胞体积近似相等,RuO 与TiO 的密度比为1.66,则Ru的相对原子质量为
2 2
(精确至1)。
4.[2023·新课标卷,29(3)]合成氨催化剂前驱体(主要成分为Fe
3
O
4
)使用前经H
2
还原,生成α⁃Fe包裹的
Fe
3
O
4
。已知α⁃Fe属于立方晶系,晶胞参数a=287 pm,密度为7.8 g·cm-3,则α⁃Fe晶胞中含有Fe的原子
数为 (列出计算式,阿伏加德罗常数的值为N )。
A
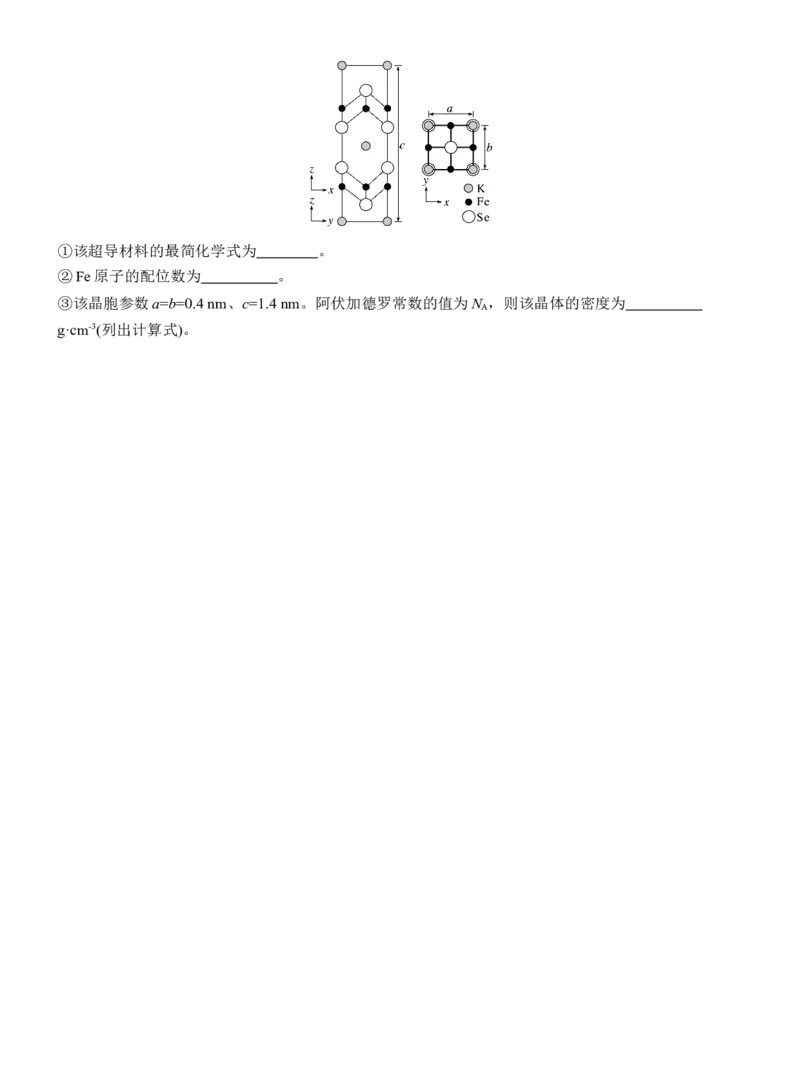
5.[2022·湖南,18(4)]钾、铁、硒可以形成一种超导材料,其晶胞在xz、yz和xy平面投影分别如图所示:①该超导材料的最简化学式为 。
②Fe原子的配位数为 。
③该晶胞参数a=b=0.4 nm、c=1.4 nm。阿伏加德罗常数的值为N ,则该晶体的密度为
A
g·cm-3(列出计算式)。答案精析
盘点核心知识
(二)
1.(1)D 4 sp3 共价 (2)E 2 (3)A 12
(4)C 离子 8 (5)B 分子 12
√3 √3 8×12
7.(1)8 (2)2 (3) a (4) a (5)
4 8 N a3×10-21
A
√3π
(6) ×100%
16
精练高考真题
√2 M
1. a Ca N B ×1030
2 3 3 N a2c
A
1 1 1 1
解析 由均摊法可知,晶胞中Ca的个数为8× +2=3,N的个数为8× +2× =3,B的个数为4× =1,则化
8 4 2 4
合物的化学式是Ca N B;其摩尔质量为M g·mol-1,阿伏加德罗常数的值是N ,晶胞体积为a2c×10-30 cm3,
3 3 A
M
则晶体的密度为 ×1030g·cm-3。
N a2c
A
√2
2.(1) a (2)8 分子晶体
4
解析 (1)铜的晶胞结构示意图为 ,镍的晶胞结构类型与铜的相同,则镍原子半径为晶胞面对
1 √2
角线长度的 ,因为晶胞体积为a3,所以晶胞棱长为a,面对角线长度为√2a,则镍原子半径为 a。(2)单
4 4
键均为σ键,双键含有1个σ键和1个π键,三键含有1个σ键和2个π键,由Ni(CO) 的结构可知,4个
4
配体CO与中心原子Ni形成的4个配位键均为σ键,而每个配体CO中含有1个σ键和2个π键,因此1个
Ni(CO) 分子中含有8个σ键。Ni(CO) 的沸点为43 ℃,因此其晶体类型为分子晶体。
4 4
3.101
M(Ru)+32
解析 由于二者的晶体结构相似,体积近似相等,则其密度之比等于摩尔质量之比,故
M(Ti)+32
=1.66,则Ru的相对原子质量约为101。
7.8×2873N
4. A
56×1030解析 已知α⁃Fe属于立方晶系,晶胞参数a=287 pm,密度为7.8 g·cm-3,设其晶胞中含有Fe的原子数为
56x 7.8×2873N
x,则α⁃Fe晶体密度ρ=
N ×(287×10-10 ) 3
g·cm-3=7.8 g·cm-3,解得x=
56×1030
A 。
A
2×(39+56×2+79×2)
5.①KFe Se ②4 ③
2 2 N ×0.4×0.4×1.4×10-21
A
1
解析 ①由平面投影图可知,晶胞中位于顶角和体心的钾原子个数为8× +1=2,位于棱上和体内的硒原子
8
1 1
4 2
的个数为8× +2=4,位于面上的铁原子个数为8× =4,该物质的晶胞结构如图所示: ,则超导
材料的最简化学式为KFe Se 。②由平面投影图可知,铁原子的配位数为4。③晶体的密度为
2 2
2×(39+56×2+79×2)
g·cm-3。
N ×0.4×0.4×1.4×10-21
A