文档内容
绝密★启用前|考试研究中心命制
2020-2021 学年下学期期中测试卷 01
高一化学
(考试时间:90分钟 试卷满分:100分)
测试范围:人教版2019必修第二册第五、六章
A.将集有氨气的试管倒扣于水槽中,液体迅速充满试管,说明氨气极易溶于水
第Ⅰ卷(选择题 共 48 分)
B.充分反应后,锥形瓶内有 NO 存在
一、选择题:本题共16个小题,每小题3分。在每小题给出的四个选项中,只有一项是符合题目要求的。 C.加热NH 4 HCO 3 固体,观察到固体逐渐减少,试管口有液滴产生,说明NH 4 HCO 3 具有热不稳定性
1.下列有关说法中正确的是( ) D.将红热的Pt丝伸入如上图所示的锥形瓶中,瓶口出现少量的红棕色气体,说明氨气催化氧化的产物中
有NO
A.“司南之杓(勺),投之于地,其柢(勺柄)指南”中“杓”的材质是 2
5.下列叙述中正确的是 ( )
B.商朝的“司母戊鼎”是我国最早使用的铁制品之一
①NH 易液化,液氨常用作制冷剂
C.氯气和二氧化硫均可作为漂白剂,若两者同时使用,漂白效果会更好 3
②可用铁、铝制容器盛装浓硝酸和稀硝酸
D.小苏打是制作面包等糕点的膨松剂,也可用于治疗胃酸过多
③利用氨气极易溶于水,氨气可做喷泉实验
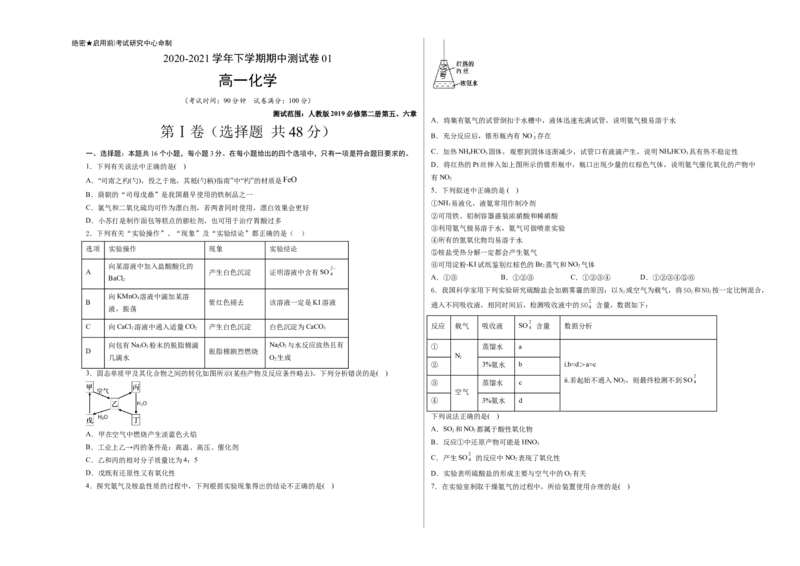
2.下列有关“实验操作”、“现象”及“实验结论”都正确的是( )
④所有的氮氧化物均易溶于水
选项 实验操作 现象 实验结论
⑤铵盐受热分解一定都会产生氨气
向某溶液中加入盐酸酸化的 ⑥可用淀粉-KI试纸鉴别红棕色的Br 2 蒸气和NO 2 气体
A 产生白色沉淀 证明溶液中含有SO
BaCl A.①③ B.①②③ C.①②③④ D.①②③④⑤⑥
2
6.我国科学家用下列实验研究硫酸盐会加剧雾霾的原因:以N 或空气为载气,将SO 和NO 按一定比例混合,
2 2 2
向KMnO 溶液中滴加某溶
4
B 紫红色褪去 该溶液一定是KI溶液
通入不同吸收液,相同时间后,检测吸收液中的SO 含量,数据如下:
液,振荡
C 向CaCl 溶液中通入适量CO 产生白色沉淀 白色沉淀为CaCO 反应 载气 吸收液 SO 含量 数据分析
2 2 3
向包有Na 2 O 2 粉末的脱脂棉滴 Na 2 O 2 与水反应放热且有 ① 蒸馏水 a
D 脱脂棉剧烈燃烧
几滴水 O 2 生成 N 2
② 3%氨水 b ⅰ.b≈d>a≈c
3.固态单质甲及其化合物之间的转化如图所示(某些产物及反应条件略去)。下列分析错误的是( )
ⅱ.若起始不通入NO ,则最终检测不到SO
③ 蒸馏水 c 2
空气
④ 3%氨水 d
下列说法正确的是( )
A.SO 和NO 都属于酸性氧化物
2 2
A.甲在空气中燃烧产生淡蓝色火焰
B.反应①中还原产物可能是HNO
3
B.工业上乙→丙的条件是:高温、高压、催化剂
C.产生SO 的反应中NO 表现了氧化性
C.乙和丙的相对分子质量比为4:5 2
D.戊既有还原性又有氧化性 D.实验表明硫酸盐的形成主要与空气中的O 有关
2
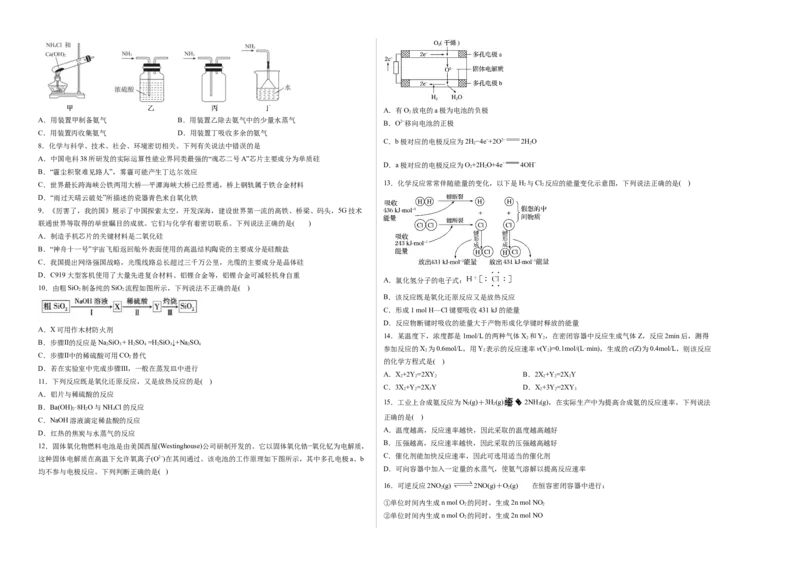
4.探究氨气及铵盐性质的过程中,下列根据实验现象得出的结论不正确的是( ) 7.在实验室制取干燥氨气的过程中,所给装置使用合理的是( )A.有O 放电的a极为电池的负极
2
A.用装置甲制备氨气 B.用装置乙除去氨气中的少量水蒸气
B.O2−移向电池的正极
C.用装置丙收集氨气 D.用装置丁吸收多余的氨气
C.b极对应的电极反应为2H−4e−+2O2− 2HO
8.化学与科学、技术、社会、环境密切相关。下列有关说法中错误的是 2 2
A.中国电科38所研发的实际运算性能业界同类最强的“魂芯二号A”芯片主要成分为单质硅
D.a极对应的电极反应为O+2H O+4e− 4OH−
2 2
B.“霾尘积聚难见路人”,雾霾可能产生丁达尔效应
C.世界最长跨海峡公铁两用大桥—平潭海峡大桥已经贯通,桥上钢轨属于铁合金材料 13.化学反应常常伴随能量的变化,以下是H 2 与Cl 2 反应的能量变化示意图,下列说法正确的是( )
D.“雨过天晴云破处”所描述的瓷器青色来自氧化铁
9.《厉害了,我的国》展示了中国探索太空,开发深海,建设世界第一流的高铁、桥梁、码头,5G技术
联通世界等取得的举世瞩目的成就。它们与化学有着密切联系。下列说法正确的是( )
A.制造手机芯片的关键材料是二氧化硅
B.“神舟十一号”宇宙飞船返回舱外表面使用的高温结构陶瓷的主要成分是硅酸盐
C.我国提出网络强国战略,光缆线路总长超过三千万公里,光缆的主要成分是晶体硅
D.C919大型客机使用了大量先进复合材料、铝锂合金等,铝锂合金可减轻机身自重
A.氯化氢分子的电子式:
10.由粗SiO 制备纯的SiO 流程如图所示,下列说法不正确的是( )
2 2
B.该反应既是氧化还原反应又是放热反应
C.形成1 mol H—Cl键要吸收431 kJ的能量
D.反应物断键时吸收的能量大于产物形成化学键时释放的能量
A.X可用作木材防火剂
14.某温度下,浓度都是1mol/L的两种气体X 和Y,在密闭容器中反应生成气体Z,反应2min后,测得
2 2
B.步骤Ⅱ的反应是NaSiO + H SO =H SiO↓+Na SO
2 3 2 4 2 3 2 4
参加反应的X 为0.6mol/L,用Y 表示的反应速率v(Y )=0.1mol/(L·min),生成的c(Z)为0.4mol/L,则该反应
2 2 2
C.步骤Ⅱ中的稀硫酸可用CO 替代
2
的化学方程式是( )
D.若在实验室中完成步骤Ⅲ,一般在蒸发皿中进行
A.X+2Y =2XY B.2X+Y =2X Y
2 2 2 2 2 2
11.下列反应既是氧化还原反应,又是放热反应的是( )
C.3X+Y =2X Y D.X+3Y =2XY
2 2 3 2 2 3
A.铝片与稀硫酸的反应
15.工业上合成氨反应为N(g)+3H(g) 2NH (g),在实际生产中为提高合成氨的反应速率,下列说法
2 2 3
B.Ba(OH) ·8H O与NH Cl的反应
2 2 4
正确的是( )
C.NaOH溶液滴定稀盐酸的反应
A.温度越高,反应速率越快,因此采取的温度越高越好
D.红热的焦炭与水蒸气的反应
B.压强越高,反应速率越快,因此采取的压强越高越好
12.固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的。它以固体氧化锆−氧化钇为电解质,
C.催化剂能加快反应速率,因此可选用适当的催化剂
这种固体电解质在高温下允许氧离子(O2−)在其间通过。该电池的工作原理如下图所示,其中多孔电极a、b
D.可向容器中加入一定量的水蒸气,使氨气溶解以提高反应速率
均不参与电极反应。下列判断正确的是( )
16.可逆反应2NO (g) 2NO(g)+O(g) 在恒容密闭容器中进行:
2 2
①单位时间内生成n mol O 的同时,生成2n mol NO
2 2
②单位时间内生成n mol O 的同时,生成2n mol NO
2③用NO 、NO和O 的物质的量浓度变化表示的反应速率之比为2∶2∶1
2 2
④混合气体的颜色不再改变
⑤混合气体的密度不再改变
⑥混合气体的压强不再改变
⑦混合气体的平均相对分子质量不再改变
可说明该反应达到化学平衡状态的是( )
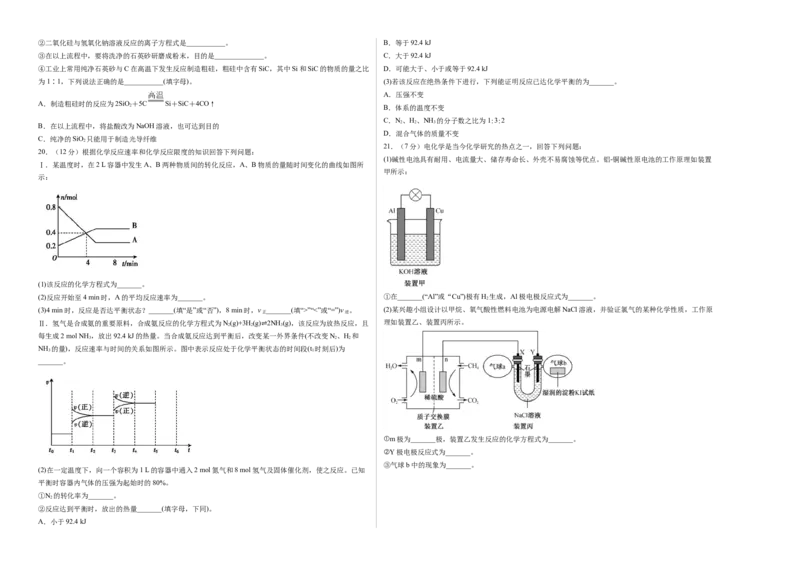
(1)检查装置气密性后,将燃烧匙中的木炭在酒精灯上加热至红热状态,立即伸入三颈瓶中,并塞紧瓶塞,
A.①④⑥⑦ B.②③④⑥ 滴加浓硝酸,可观察到三颈瓶中产生红棕色的气体,产生该气体的化学反应方程式是___________。
C.①④⑤⑦ D.①②⑥⑦ (2)装置C中盛有Ba(OH) 溶液,反应一段时间后可观察到C中出现白色沉淀,该白色沉淀为
2
___________(写化学式)。其中的Ba(OH) 溶液___________(填“能”或“不能”)用Ca(OH) 溶液代替,理
2 2
第 II 卷(非选择题 共 52 分) 由___________。
(3)装置D中收集到了无色气体,部分同学认为是NO,还有部分同学认为是O
2。
二、非选择题:包括第17题~第21题5个大题,共52分。 ①下列对该气体的检验方法合适的是___________(填字母)。
17.(12分)根据要求完成下列各小题实验目的。(a、b为弹簧夹,(加热及固定装置已略去) A.敞口观察集气瓶内气体的颜色变化
B.将润湿的蓝色石蕊试纸伸入集气瓶内,观察试纸是否变红
C.将带火星的木条伸入集气瓶中,观察木条是否复燃
②如果集气瓶中收集到的无色气体是氧气,则氧气的来源是___________。
(4)若将木炭改为铜片,再用等质量的铜片分别与等体积的浓硝酸、稀硝酸(硝酸均过量)反应时,发现反应后
所得溶液前者呈绿色,后者呈蓝色。针对此现象,同学们进行讨论,提出两种意见:①认为两溶液所显颜
色不同是由Cu2+浓度的差异引起的。②认为前者溶液呈绿色,是因为生成红棕色NO 溶解于溶液中引起的。
2
你认为上述意见___________(填“①”或“②”)合理(注:若填①,下题中只答Ⅰ;若填②,下题中只答Ⅱ)。
Ⅰ.如果你认为①合理,理由是___________。
Ⅱ.如果你认为②合理,请设计一个简单的实验进行验证___________ 。
19.(8分)我国考古学家对“南澳一号”沉船进行了考古探索,从沉船中发现了大量宋代精美瓷器,体现
(1)验证碳、硅非金属性的相对强弱。(已知酸性:亚硫酸>碳酸)
了灿烂的中华文明。青花瓷胎体的原料——高岭土[AlSi O(OH) ],可掺进瓷石制胎,青花瓷釉料的成分主
①连接仪器、___________、加药品后,打开a关闭b,然后滴入浓硫酸,加热。 2 2 5 x
要是钾长石(KAlSi O),在1300 ℃左右一次烧成的釉可形成精美的青花瓷。
②铜与浓硫酸反应的化学方程式是___________。装置A中试剂是___________。 3 8
(1)下列说法正确的是___________(填字母)。
③能说明碳的非金属性比硅强的实验现象是___________。
A.高岭土分子中x=2
(2)验证SO 的氧化性、还原性和酸性氧化物的通性。
2
B.钾长石能完全溶解在盐酸中形成澄清的溶液
①在(1)①操作后打开b,关闭a。
C.烧制青花瓷过程中发生了复杂的物理变化和化学变化
②一段时间后,HS溶液中的现象是___________,化学方程式是___________。
2
D.青花瓷、玻璃、水泥都属于硅酸盐产品
③BaCl 溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
2
(2)在“南澳一号”考古直播过程中,需用高纯度SiO 制造的光纤。下图是用海边的石英砂(含氯化钠、氧化
2
滴加的溶液 氯水 氨水
铝等杂质)制备二氧化硅粗产品的工艺流程。
沉淀的化学式 ___________ ___________
写出其中SO 显示还原性生成沉淀的离子方程式___________。
2
18.(13分)某化学学习小组采用下列装置,对浓硝酸与木炭的反应进行探究。
①洗涤石英砂的目的是___________。②二氧化硅与氢氧化钠溶液反应的离子方程式是___________。 B.等于92.4 kJ
③在以上流程中,要将洗净的石英砂研磨成粉末,目的是______________。 C.大于92.4 kJ
④工业上常用纯净石英砂与C在高温下发生反应制造粗硅,粗硅中含有SiC,其中Si和SiC的物质的量之比 D.可能大于、小于或等于92.4 kJ
为1∶1,下列说法正确的是___________(填字母)。 (3)若该反应在绝热条件下进行,下列能证明反应已达化学平衡的为_______。
A.压强不变
A.制造粗硅时的反应为2SiO+5C Si+SiC+4CO↑
2 B.体系的温度不变
C.N、H、NH 的分子数之比为1:3:2
2 2 3
B.在以上流程中,将盐酸改为NaOH溶液,也可达到目的
D.混合气体的质量不变
C.纯净的SiO 只能用于制造光导纤维
2
21.(7分)电化学是当今化学研究的热点之一,回答下列问题:
20.(12分)根据化学反应速率和化学反应限度的知识回答下列问题:
(1)碱性电池具有耐用、电流量大、储存寿命长、外壳不易腐蚀等优点。铝-铜碱性原电池的工作原理如装置
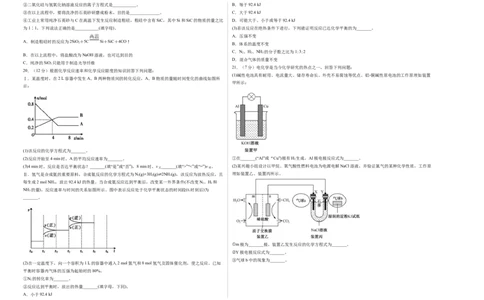
Ⅰ.某温度时,在2 L容器中发生A、B两种物质间的转化反应,A、B物质的量随时间变化的曲线如图所
甲所示:
示:
(1)该反应的化学方程式为_______。
(2)反应开始至4 min时,A的平均反应速率为_______。 ①在_______(“Al”或“Cu”)极有H 生成,Al极电极反应式为_______。
2
(3)4 min时,反应是否达平衡状态?_______(填“是”或“否”),8 min时,v _______(填“>”“<”或“=”)v 。 (2)某兴趣小组设计以甲烷、氧气酸性燃料电池为电源电解NaCl溶液,并验证氯气的某种化学性质,工作原
正 逆
Ⅱ.氢气是合成氨的重要原料,合成氨反应的化学方程式为N(g)+3H(g) 2NH (g),该反应为放热反应,且 理如装置乙、装置丙所示。
2 2 3
每生成2 mol NH ,放出92.4 kJ的热量。当合成氨反应达到平衡后,改变某一外界条件(不改变N、H 和
3 ⇌ 2 2
NH 的量),反应速率与时间的关系如图所示。图中表示反应处于化学平衡状态的时间段(t 时刻后)为
3 1
_______。
①m极为_______极,装置乙发生反应的化学方程式为_______。
②Y极电极反应式为_______。
③气球b中的现象为_______。
(2)在一定温度下,向一个容积为1 L的容器中通入2 mol氮气和8 mol氢气及固体催化剂,使之反应。已知
平衡时容器内气体的压强为起始时的80%。
①N 的转化率为_______。
2
②反应达到平衡时,放出的热量_______(填字母,下同)。
A.小于92.4 kJ