文档内容
化工流程中的有关计算
1.K 计算
sp
(1)判断能否沉淀。
(2)判断能否沉淀完全。
(3)计算某一离子的浓度。
(4)沉淀生成和沉淀完全时pH的计算。
(5)用化学平衡常数与溶度积计算沉淀转化。
2.产率、纯度的计算
(1)计算公式
纯净物的质量
纯度= ×100%
混合物的质量
产物的实际产量
产物的产率= ×100%
产物的理论产量
(2)计算的关键在于运用守恒或关系式法结合实验原理找到计算的关系,确定数量关系。
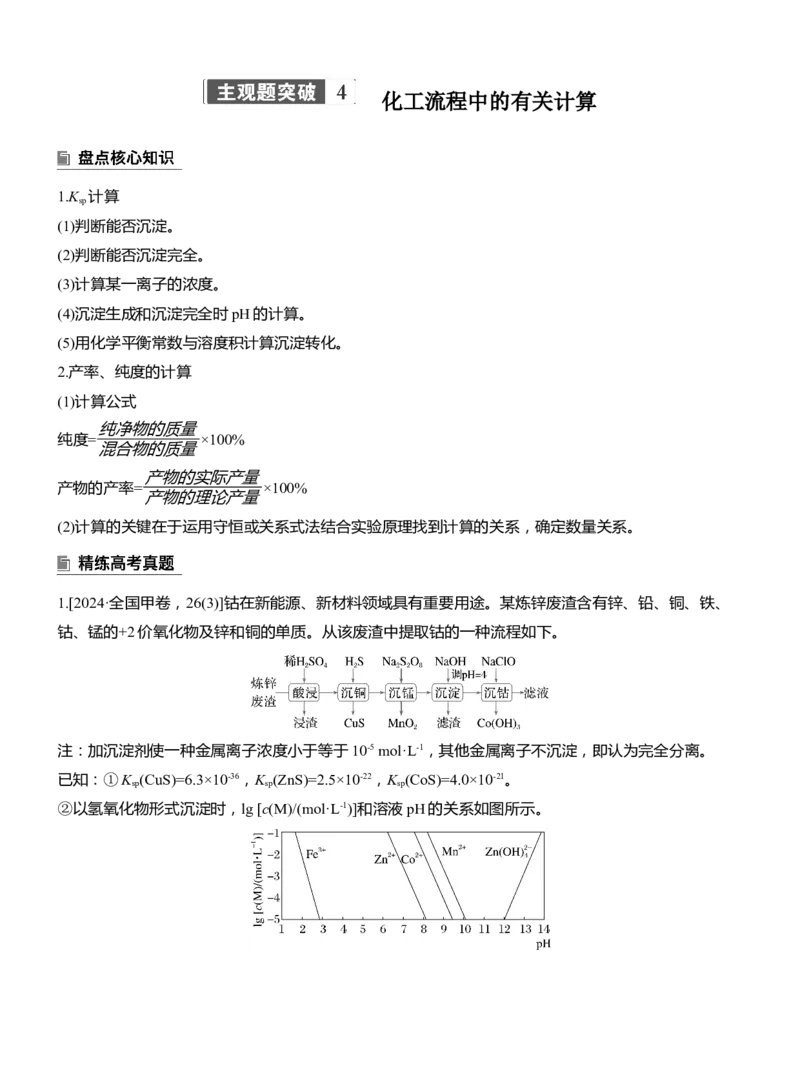
1.[2024·全国甲卷,26(3)]钴在新能源、新材料领域具有重要用途。某炼锌废渣含有锌、铅、铜、铁、
钴、锰的+2价氧化物及锌和铜的单质。从该废渣中提取钴的一种流程如下。
注:加沉淀剂使一种金属离子浓度小于等于10-5 mol·L-1,其他金属离子不沉淀,即认为完全分离。
已知:①K (CuS)=6.3×10-36,K (ZnS)=2.5×10-22,K (CoS)=4.0×10-21。
sp sp sp
②以氢氧化物形式沉淀时,lg [c(M)/(mol·L-1)]和溶液pH的关系如图所示。假设“沉铜”后得到的滤液中c(Zn2+)和c(Co2+)均为0.10 mol·L-1,向其中加入Na S至Zn2+沉淀完全,此
2
时溶液中c(Co2+)= mol·L-1,据此判断能否实现Zn2+和Co2+的完全分离? (填“能”
或“不能”)。
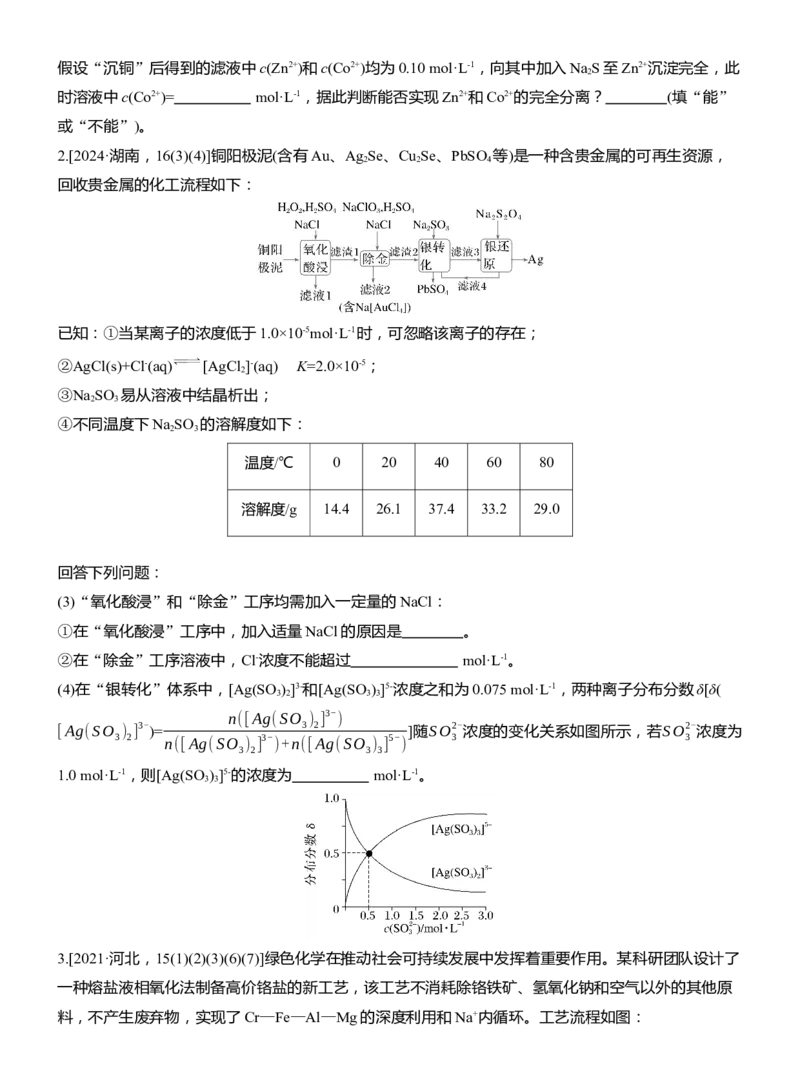
2.[2024·湖南,16(3)(4)]铜阳极泥(含有Au、Ag Se、Cu Se、PbSO 等)是一种含贵金属的可再生资源,
2 2 4
回收贵金属的化工流程如下:
已知:①当某离子的浓度低于1.0×10-5mol·L-1时,可忽略该离子的存在;
②AgCl(s)+Cl-(aq) [AgCl ]-(aq) K=2.0×10-5;
2
③Na SO 易从溶液中结晶析出;
2 3
④不同温度下Na SO 的溶解度如下:
2 3
温度/℃ 0 20 40 60 80
溶解度/g 14.4 26.1 37.4 33.2 29.0
回答下列问题:
(3)“氧化酸浸”和“除金”工序均需加入一定量的NaCl:
①在“氧化酸浸”工序中,加入适量NaCl的原因是 。
②在“除金”工序溶液中,Cl-浓度不能超过 mol·L-1。
(4)在“银转化”体系中,[Ag(SO ) ]3-和[Ag(SO ) ]5-浓度之和为0.075 mol·L-1,两种离子分布分数δ[δ(
3 2 3 3
n([Ag(SO ) ] 3- )
[Ag(SO ) ] 3- )= 3 2 ]随SO2- 浓度的变化关系如图所示,若SO2- 浓度为
3 2 n([Ag(SO ) ] 3- )+n([Ag(SO ) ] 5- ) 3 3
3 2 3 3
1.0 mol·L-1,则[Ag(SO ) ]5-的浓度为 mol·L-1。
3 3
3.[2021·河北,15(1)(2)(3)(6)(7)]绿色化学在推动社会可持续发展中发挥着重要作用。某科研团队设计了
一种熔盐液相氧化法制备高价铬盐的新工艺,该工艺不消耗除铬铁矿、氢氧化钠和空气以外的其他原
料,不产生废弃物,实现了Cr—Fe—Al—Mg的深度利用和Na+内循环。工艺流程如图:回答下列问题:
(1)高温连续氧化工序中被氧化的元素是 (填元素符号)。
(2)工序①的名称为 。
(3)滤渣Ⅰ的主要成分是 (填化学式)。
(6)热解工序产生的混合气体最适宜返回工序 (填“①”“②”“③”或“④”)参与内循环。
(7)工序④溶液中的铝元素恰好完全转化为沉淀的pH为 (通常认为溶液中离子浓度小于10-5
-
mol·L-1为沉淀完全;Al(OH) +OH- Al(OH) K=100.63;K =10-14,K [Al(OH) ]=10-33)。
3 4 w sp 3答案精析
精练高考真题
1.1.6×10-4 不能
解析 假设“沉铜”后得到的滤液中c(Zn2+)和c(Co2+)均为0.10 mol·L-1,向其中加入Na S至Zn2+沉淀完全,
2
2.5×10-22 4.0×10-21
此时溶液中c(S2-)= mol·L-1=2.5×10-17 mol·L-1,则c(Co2+)= mol·L-1=1.6×10-4 mol·L-1,说
10-5 2.5×10-17
明大部分Co2+也转化为硫化物沉淀,不能实现Zn2+和Co2+的完全分离。
2.(3)①使银元素转化为AgCl沉淀 ②0.5 (4)0.05
解析 (3)①在“氧化酸浸”工序中,加入适量NaCl的原因是使银元素转化为AgCl沉淀。②由题目可知
AgCl(s)+Cl-(aq) [AgCl ]-(aq),在“除金”工序溶液中,若Cl-加入过多,AgCl则会转化为[AgCl ]-,当某
2 2
离子的浓度低于1.0×10-5 mol·L-1时,可忽略该离子的存在,为了不让AgCl发生转化,则令
c([AgCl ] - )
c([AgCl ]-)=1.0×10-5 mol·L-1,由K= 2 =2.0×10-5,可得c(Cl-)=0.5 mol·L-1,即Cl-浓度不能超过0.5
2 c(Cl-
)
mol·L-1。(4)在“银转化”体系中,[Ag(SO ) ]3-和[Ag(SO ) ]5-浓度之和为0.075 mol·L-1,溶液中存在平衡关
3 2 3 3
系:[Ag(SO )
]3-+SO2-
[Ag(SO )
]5-,当c(SO2-
)=0.5 mol·L-1时,此时c([Ag(SO ) ]3-)=c([Ag(SO ) ]5-)=0.037
3 2 3 3 3 3 3 2 3 3
c([Ag(SO ) ] 5- ) 0.037 5
5 mol·L-1,则K=
3 3
=
=2,当c(SO2-
)=1 mol·L-1时,K=
c([Ag(SO ) ] 3- )·c(SO2- ) 0.037 5×0.5 3
3 2 3
c([Ag(SO ) ] 5- ) c([Ag(SO ) ] 5- )
3 3 = 3 3 =2,解得c([Ag(SO ) ]5-)=0.05 mol·L-1。
c([Ag(SO ) ] 3- )·c(SO2- ) 0.075-c([Ag(SO ) ] 5- ) 3 3
3 2 3 3 3
3.(1)Fe、Cr (2)溶解浸出 (3)MgO、Fe O
2 3
(6)② (7)8.37
解析 (2)工序①为将氧化后的固体加水溶解浸出可溶性物质。
(6)热解工序产生的混合气体为二氧化碳和水蒸气,将混合气体通入滤渣Ⅰ中可以将氧化镁转化为碳酸氢镁
溶液,则混合气体最适宜返回的工序为工序②。
-
(7)工序④溶液中的铝元素恰好完全转化为沉淀的反应为Al(OH) +H+ Al(OH) ↓+H O,反应的平衡常数
4 3 2
1 c(OH- ) 1
-
为K = = = =1013.37,当c[Al(OH) ]为10-5 mol·L-1时,
1 c[Al(OH) - ]·c(H+ ) c[Al(OH) - ]·c(H+ )·c(OH- ) K·K 4
4 4 w
1 1
溶液中氢离子浓度为 = mol·L-1=10-8.37 mol·L-1,则溶液的pH为8.37。
c[Al(OH) - ]·K 10-5×1013.37
4 1