文档内容
专题六 能力提升检测卷
(本卷共20小题,满分100分,考试用时75分钟)
可能用到的相对原子质量:H 1 Li 7 B 11 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Cl 35.5 K 39
Ca 40 Cr 52 Mn 55 Fe 56 Ni 59 Cu 64 La 139
第I卷 (选择题共50分)
一、选择题:本题共10个小题,每小题3分,共30分,在每小题给出的四个选项中,只有一项是符
合题目要求的。
1.已知:①2H(g)+O(g)===2H O(g) ΔH=-483.6 kJ·mol-1
2 2 2
②H(g)+S(g)===H S(g) ΔH=-20.1 kJ·mol-1
2 2
下列判断正确的是( )
A.1 mol氢气完全燃烧生成液态水吸收热量241.8 kJ
B.1 mol H O(g)和1 mol H S(g)的能量相差221.7 kJ
2 2
C.由①②知,水的热稳定性强于硫化氢
D.若反应②中改用固态硫,则1 mol S(s)完全反应放出的热量小于20.1 kJ
2.下列热化学方程式正确的是( )
选项 已知条件 热化学方程式
A H 的燃烧热为a kJ·mol-1 H+Cl===2HCl ΔH=-a kJ·mol-1
2 2 2
1 mol SO 、0.5 mol O 完全反应,放出热量 2SO (g)+O(g)2SO (g) ΔH=-
2 2 2 2 3
B
98.3 kJ 98.3 kJ·mol-1
H+(aq)+OH-(aq)===H O(l) HSO (aq)+Ba(OH) (aq)===BaSO (s)
2 2 4 2 4
C
ΔH=-57.3 kJ·mol-1 +2HO(l) ΔH=-114.6 kJ·mol-1
2
P(白磷,s)===4P(红磷,s) ΔH=-
4
D 31 g白磷比31 g红磷能量多b kJ
4b kJ·mol-1
3.十氢萘是具有高储氢密度的氢能载体,经历“十氢萘(C H )→四氢萘(C H )→萘(C H)”的脱氢过
10 18 10 12 10 8
程释放氢气。已知:
Ⅰ.C H (l)===C H (l)+3H(g) ΔH
10 18 10 12 2 1
Ⅱ.C H (l)===C H(l)+2H(g) ΔH
10 12 10 8 2 2
假设某温度下,ΔH>ΔH>0。下列“C H (l)→C H (l)→C H(l)”的“能量—反应过程”示意图正确
1 2 10 18 10 12 10 8
的是( )
4.已知:2H(g)+O(g)===2H O(g) ΔH
2 2 2 13H(g)+Fe O(s)===2Fe(s)+3HO(g) ΔH
2 2 3 2 2
2Fe(s)+O(g)===Fe O(s) ΔH
2 2 3 3
2Al(s)+O(g)===AlO(s) ΔH
2 2 3 4
2Al(s)+Fe O(s)===AlO(s)+2Fe(s) ΔH
2 3 2 3 5
下列关于上述反应焓变的判断正确的是( )
A.ΔH<0,ΔH>0
1 3
B.ΔH<0,ΔH<ΔH
5 4 3
C.ΔH=ΔH+ΔH
1 2 3
D.ΔH=ΔH+ΔH
3 4 5
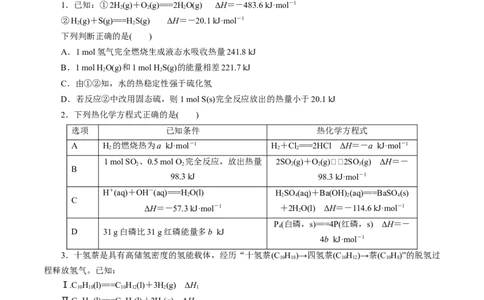
5.燃料电池对新能源的发展有划时代的意义。甲池是一种氢氧燃料电池,乙池是高分子膜电解池(苯、
环己烷均为气态)。已知D中进入10 mol混合气体(其中苯物质的量分数为20%,杂质不参与反应),C中出
来含苯的物质的量分数为10%的混合气体(不含H)。
2
下列说法不正确的是
A.甲池中F极为正极 B.乙池中流经水溶液的电子为6N
A
C.乙池中苯发生还原反应 D.甲池中G极发生:H-2e-=2H+
2
6.三室式电渗析法处理含NaSO 废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜。在
2 4
直流电场的作用下,两膜中间的Na+和SO 可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔
室。下列叙述正确的是
A.通电后中间隔室的Na+向正极迁移
B.正极反应为2HO+2e-=H ↑+2OH-,正极区溶液pH降低
2 2C.当电路中通过2mol电子的电量时,会有1mol的O 生成
2
D.该法在处理含NaSO 废水时可以得到NaOH和HSO 产品
2 4 2 4
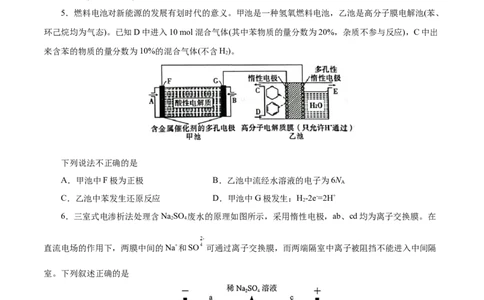
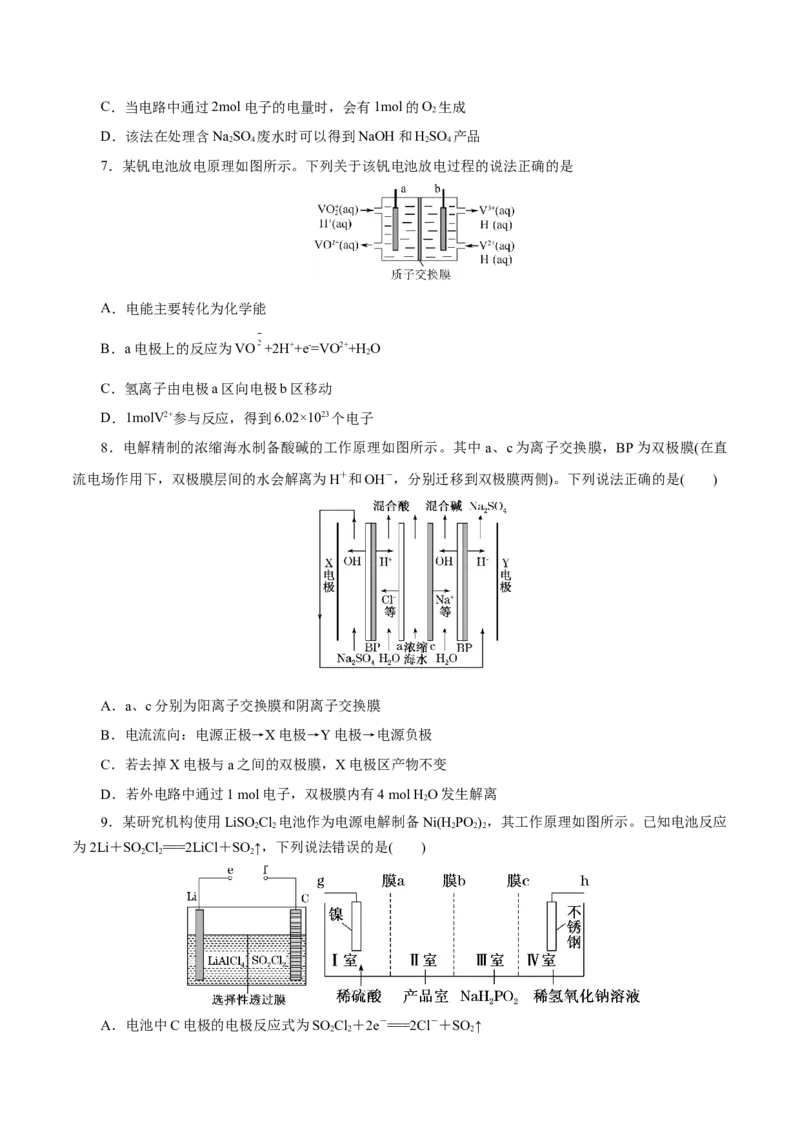
7.某钒电池放电原理如图所示。下列关于该钒电池放电过程的说法正确的是
A.电能主要转化为化学能
B.a电极上的反应为VO +2H++e-=VO2++H O
2
C.氢离子由电极a区向电极b区移动
D.1molV2+参与反应,得到6.02×1023个电子
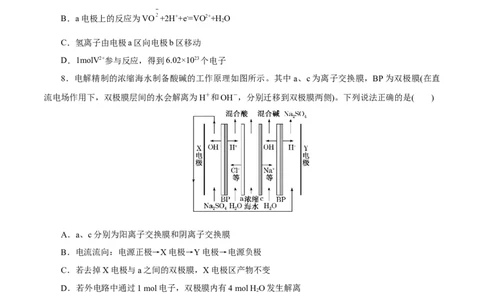
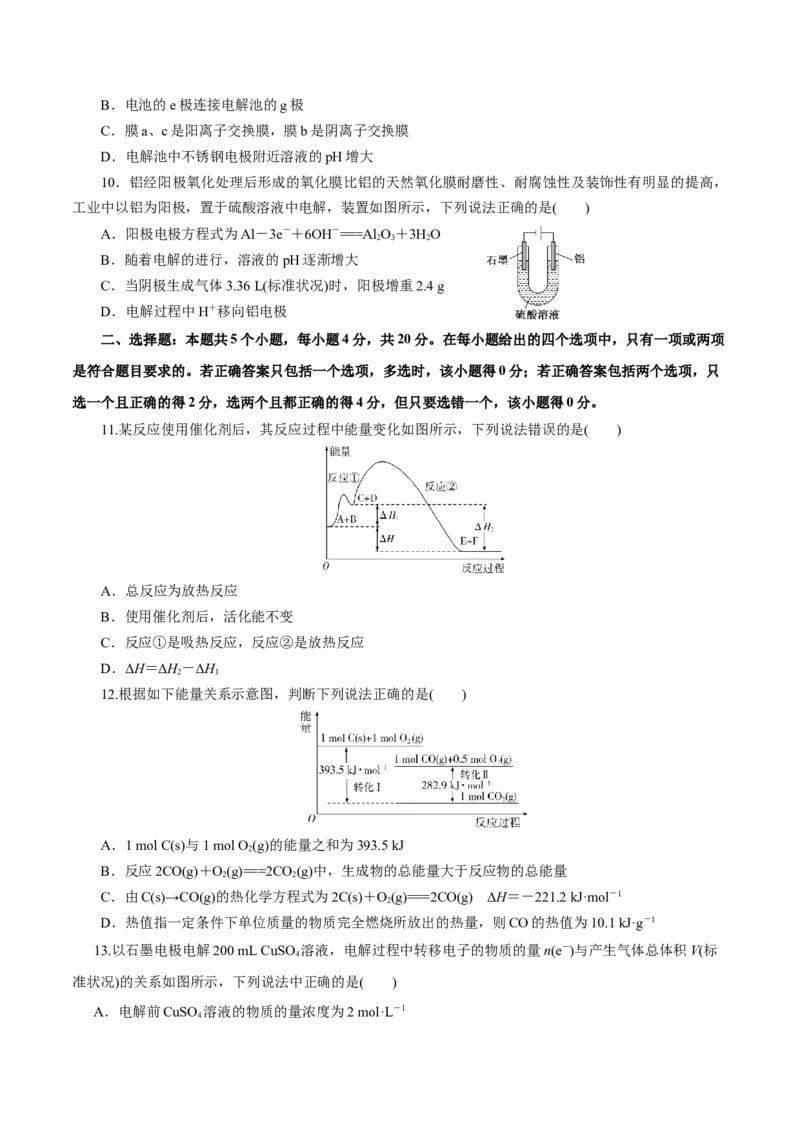
8.电解精制的浓缩海水制备酸碱的工作原理如图所示。其中a、c为离子交换膜,BP为双极膜(在直
流电场作用下,双极膜层间的水会解离为H+和OH-,分别迁移到双极膜两侧)。下列说法正确的是( )
A.a、c分别为阳离子交换膜和阴离子交换膜
B.电流流向:电源正极→X电极→Y电极→电源负极
C.若去掉X电极与a之间的双极膜,X电极区产物不变
D.若外电路中通过1 mol电子,双极膜内有4 mol H O发生解离
2
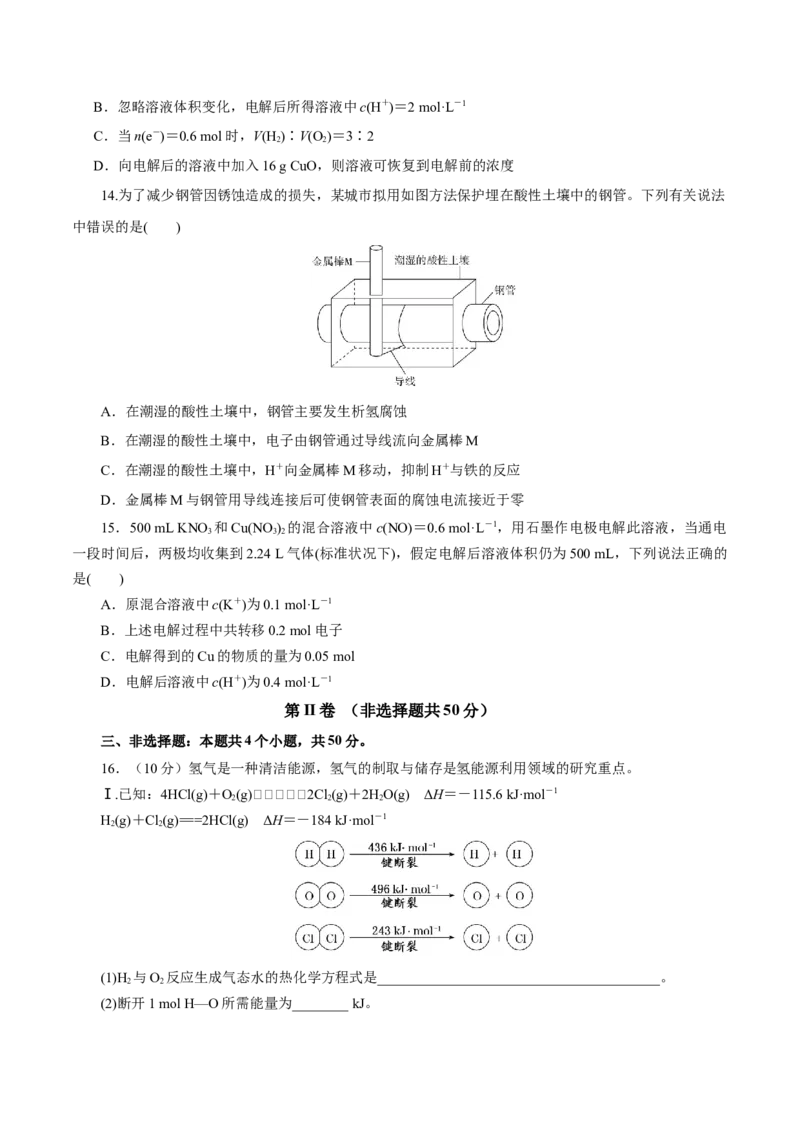
9.某研究机构使用LiSO Cl 电池作为电源电解制备Ni(H PO ) ,其工作原理如图所示。已知电池反应
2 2 2 2 2
为2Li+SO Cl===2LiCl+SO ↑,下列说法错误的是( )
2 2 2
A.电池中C电极的电极反应式为SO Cl+2e-===2Cl-+SO ↑
2 2 2B.电池的e极连接电解池的g极
C.膜a、c是阳离子交换膜,膜b是阴离子交换膜
D.电解池中不锈钢电极附近溶液的pH增大
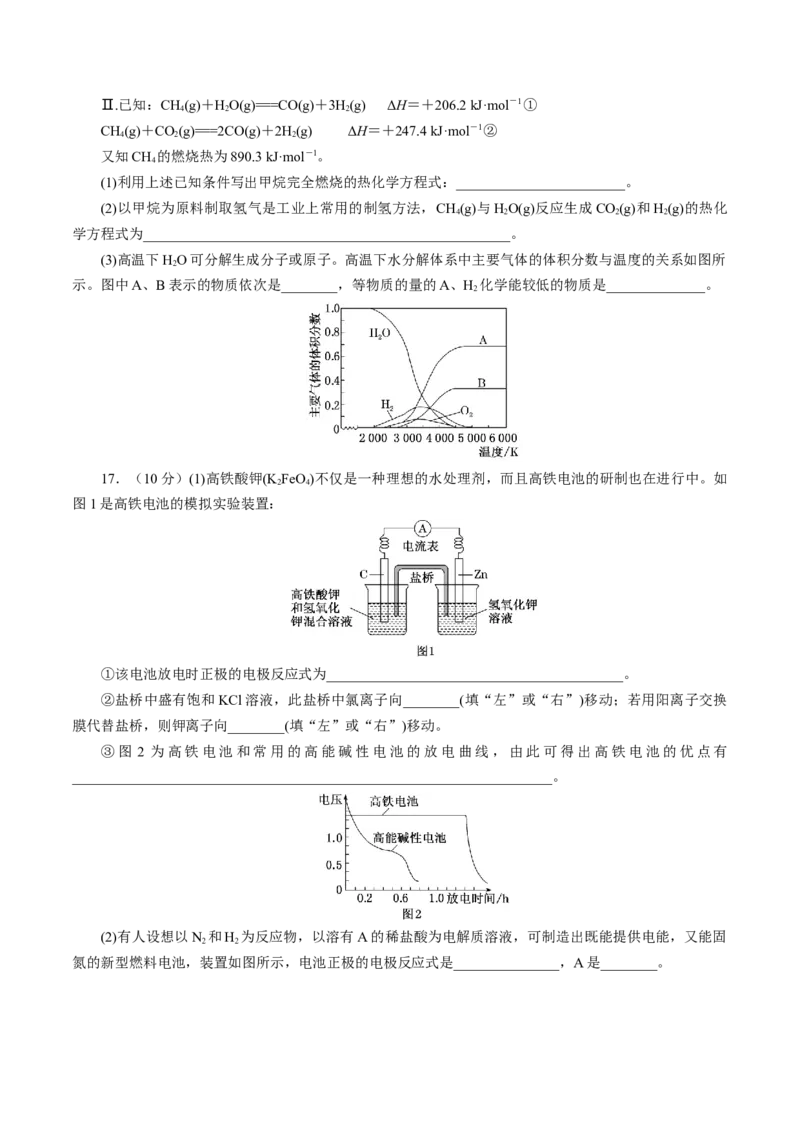
10.铝经阳极氧化处理后形成的氧化膜比铝的天然氧化膜耐磨性、耐腐蚀性及装饰性有明显的提高,
工业中以铝为阳极,置于硫酸溶液中电解,装置如图所示,下列说法正确的是( )
A.阳极电极方程式为Al-3e-+6OH-===AlO+3HO
2 3 2
B.随着电解的进行,溶液的pH逐渐增大
C.当阴极生成气体3.36 L(标准状况)时,阳极增重2.4 g
D.电解过程中H+移向铝电极
二、选择题:本题共5个小题,每小题4分,共20分。在每小题给出的四个选项中,只有一项或两项
是符合题目要求的。若正确答案只包括一个选项,多选时,该小题得0分;若正确答案包括两个选项,只
选一个且正确的得2分,选两个且都正确的得4分,但只要选错一个,该小题得0分。
11.某反应使用催化剂后,其反应过程中能量变化如图所示,下列说法错误的是( )
A.总反应为放热反应
B.使用催化剂后,活化能不变
C.反应①是吸热反应,反应②是放热反应
D.ΔH=ΔH-ΔH
2 1
12.根据如下能量关系示意图,判断下列说法正确的是( )
A.1 mol C(s)与1 mol O (g)的能量之和为393.5 kJ
2
B.反应2CO(g)+O(g)===2CO (g)中,生成物的总能量大于反应物的总能量
2 2
C.由C(s)→CO(g)的热化学方程式为2C(s)+O(g)===2CO(g) ΔH=-221.2 kJ·mol-1
2
D.热值指一定条件下单位质量的物质完全燃烧所放出的热量,则CO的热值为10.1 kJ·g-1
13.以石墨电极电解200 mL CuSO 溶液,电解过程中转移电子的物质的量n(e-)与产生气体总体积V(标
4
准状况)的关系如图所示,下列说法中正确的是( )
A.电解前CuSO 溶液的物质的量浓度为2 mol·L-1
4B.忽略溶液体积变化,电解后所得溶液中c(H+)=2 mol·L-1
C.当n(e-)=0.6 mol时,V(H )∶V(O )=3∶2
2 2
D.向电解后的溶液中加入16 g CuO,则溶液可恢复到电解前的浓度
14.为了减少钢管因锈蚀造成的损失,某城市拟用如图方法保护埋在酸性土壤中的钢管。下列有关说法
中错误的是( )
A.在潮湿的酸性土壤中,钢管主要发生析氢腐蚀
B.在潮湿的酸性土壤中,电子由钢管通过导线流向金属棒M
C.在潮湿的酸性土壤中,H+向金属棒M移动,抑制H+与铁的反应
D.金属棒M与钢管用导线连接后可使钢管表面的腐蚀电流接近于零
15.500 mL KNO 和Cu(NO ) 的混合溶液中c(NO)=0.6 mol·L-1,用石墨作电极电解此溶液,当通电
3 3 2
一段时间后,两极均收集到2.24 L气体(标准状况下),假定电解后溶液体积仍为500 mL,下列说法正确的
是( )
A.原混合溶液中c(K+)为0.1 mol·L-1
B.上述电解过程中共转移0.2 mol电子
C.电解得到的Cu的物质的量为0.05 mol
D.电解后溶液中c(H+)为0.4 mol·L-1
第II卷 (非选择题共50分)
三、非选择题:本题共4个小题,共50分。
16.(10分)氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究重点。
Ⅰ.已知:4HCl(g)+O(g)2Cl(g)+2HO(g) ΔH=-115.6 kJ·mol-1
2 2 2
H(g)+Cl(g)===2HCl(g) ΔH=-184 kJ·mol-1
2 2
(1)H 与O 反应生成气态水的热化学方程式是________________________________________。
2 2
(2)断开1 mol H—O所需能量为________ kJ。Ⅱ.已知:CH(g)+HO(g)===CO(g)+3H(g) ΔH=+206.2 kJ·mol-1①
4 2 2
CH(g)+CO(g)===2CO(g)+2H(g) ΔH=+247.4 kJ·mol-1②
4 2 2
又知CH 的燃烧热为890.3 kJ·mol-1。
4
(1)利用上述已知条件写出甲烷完全燃烧的热化学方程式:________________________。
(2)以甲烷为原料制取氢气是工业上常用的制氢方法,CH(g)与HO(g)反应生成CO(g)和H(g)的热化
4 2 2 2
学方程式为____________________________________________________。
(3)高温下HO可分解生成分子或原子。高温下水分解体系中主要气体的体积分数与温度的关系如图所
2
示。图中A、B表示的物质依次是________,等物质的量的A、H 化学能较低的物质是______________。
2
17.(10分)(1)高铁酸钾(K FeO)不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。如
2 4
图1是高铁电池的模拟实验装置:
①该电池放电时正极的电极反应式为__________________________________________。
②盐桥中盛有饱和KCl溶液,此盐桥中氯离子向________(填“左”或“右”)移动;若用阳离子交换
膜代替盐桥,则钾离子向________(填“左”或“右”)移动。
③图 2 为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有
____________________________________________________________________。
(2)有人设想以N 和H 为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固
2 2
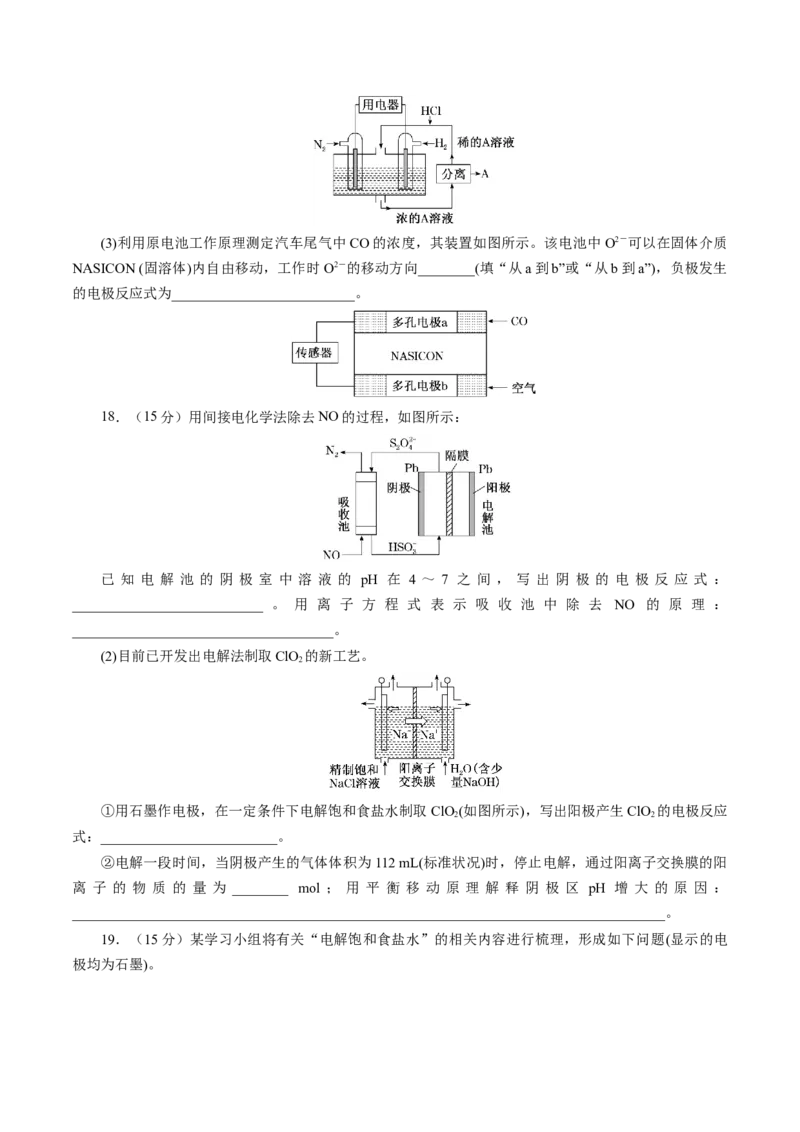
氮的新型燃料电池,装置如图所示,电池正极的电极反应式是_______________,A是________。(3)利用原电池工作原理测定汽车尾气中CO的浓度,其装置如图所示。该电池中O2-可以在固体介质
NASICON (固溶体)内自由移动,工作时O2-的移动方向________(填“从a到b”或“从b到a”),负极发生
的电极反应式为__________________________。
18.(15分)用间接电化学法除去NO的过程,如图所示:
已 知 电 解 池 的 阴 极 室 中 溶 液 的 pH 在 4 ~ 7 之 间 , 写 出 阴 极 的 电 极 反 应 式 :
___________________________ 。 用 离 子 方 程 式 表 示 吸 收 池 中 除 去 NO 的 原 理 :
_____________________________________。
(2)目前已开发出电解法制取ClO 的新工艺。
2
①用石墨作电极,在一定条件下电解饱和食盐水制取 ClO (如图所示),写出阳极产生ClO 的电极反应
2 2
式:_________________________。
②电解一段时间,当阴极产生的气体体积为112 mL(标准状况)时,停止电解,通过阳离子交换膜的阳
离 子 的 物 质 的 量 为 ________ mol ; 用 平 衡 移 动 原 理 解 释 阴 极 区 pH 增 大 的 原 因 :
____________________________________________________________________________________。
19.(15分)某学习小组将有关“电解饱和食盐水”的相关内容进行梳理,形成如下问题(显示的电
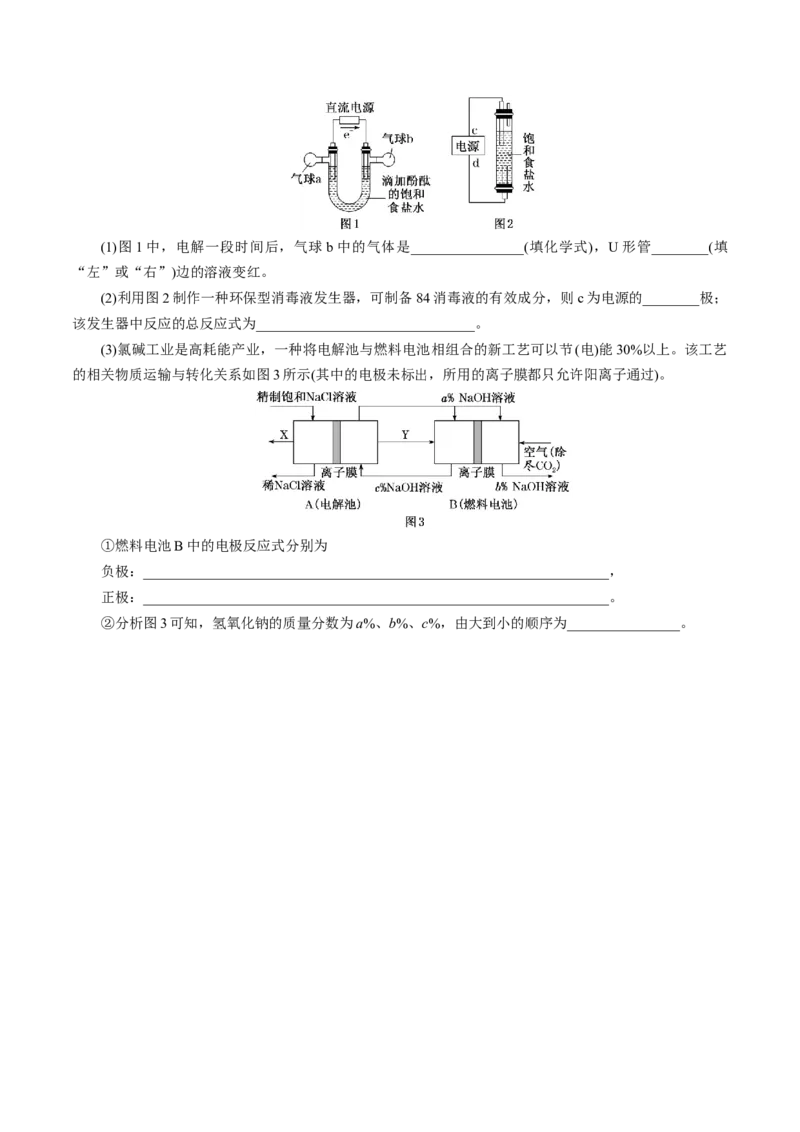
极均为石墨)。(1)图1中,电解一段时间后,气球b中的气体是________________(填化学式),U形管________(填
“左”或“右”)边的溶液变红。
(2)利用图2制作一种环保型消毒液发生器,可制备84消毒液的有效成分,则c为电源的________极;
该发生器中反应的总反应式为_______________________________。
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。该工艺
的相关物质运输与转化关系如图3所示(其中的电极未标出,所用的离子膜都只允许阳离子通过)。
①燃料电池B中的电极反应式分别为
负极:__________________________________________________________________,
正极:__________________________________________________________________。
②分析图3可知,氢氧化钠的质量分数为a%、b%、c%,由大到小的顺序为________________。