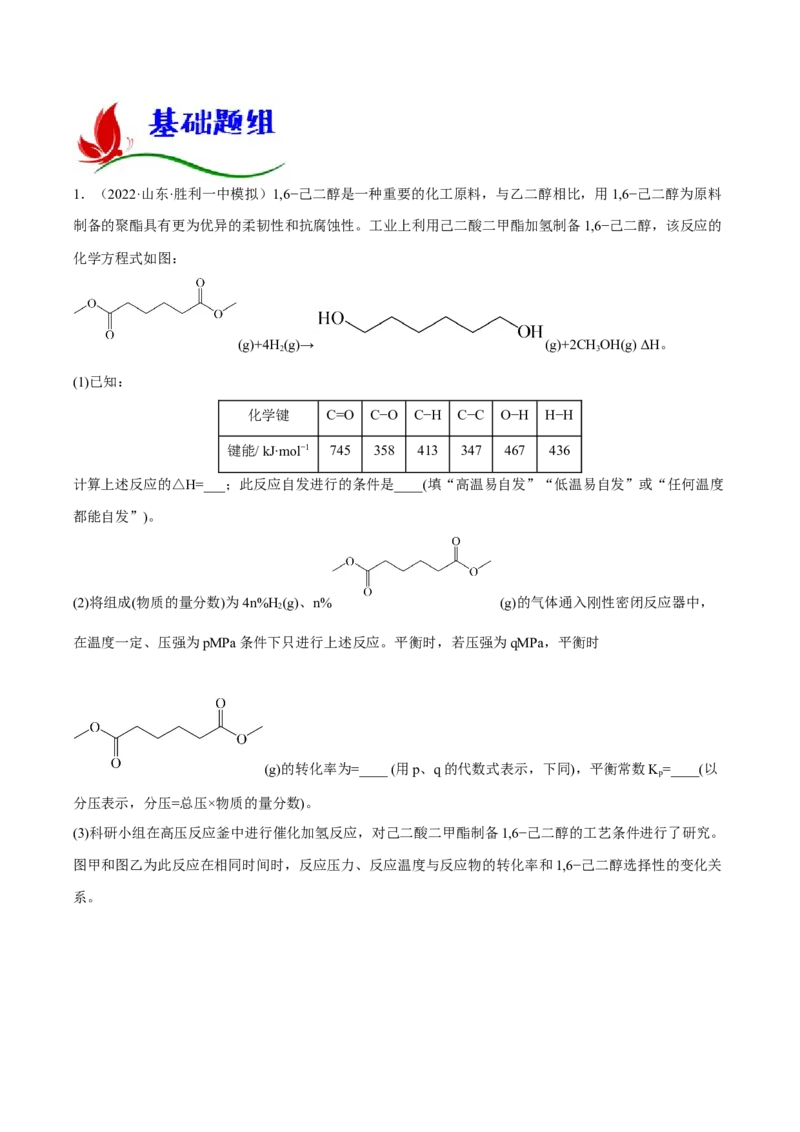
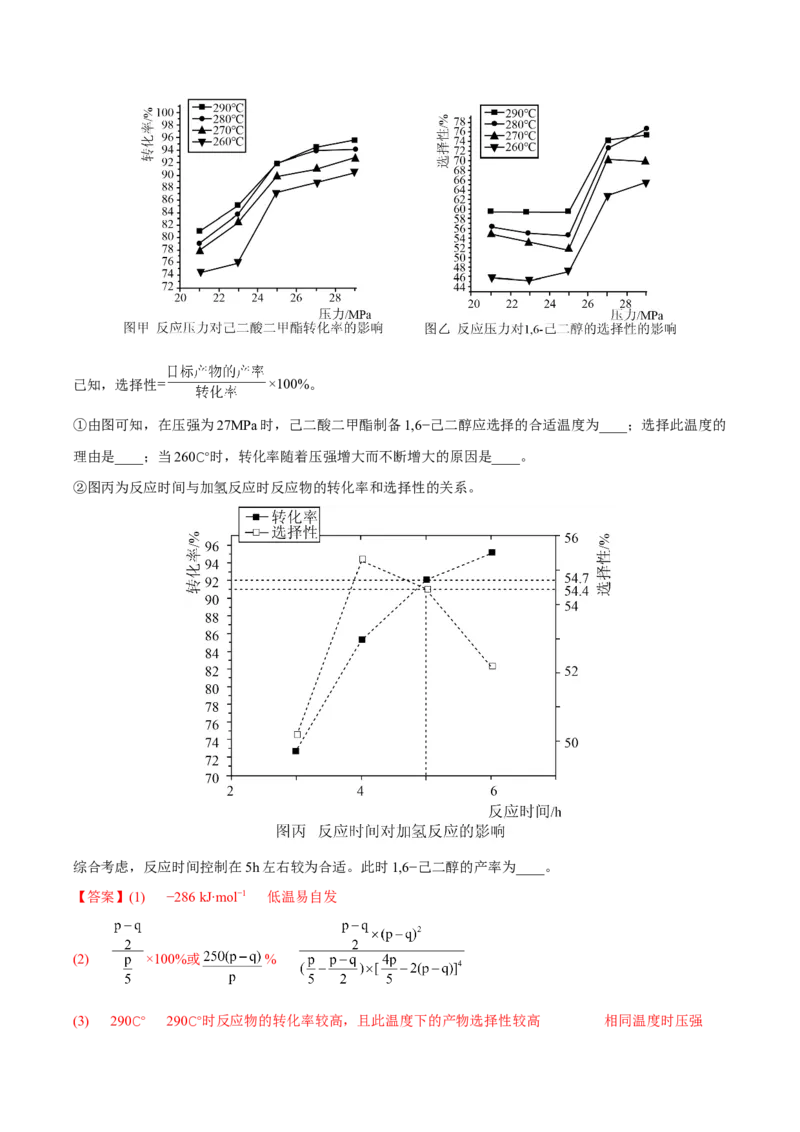
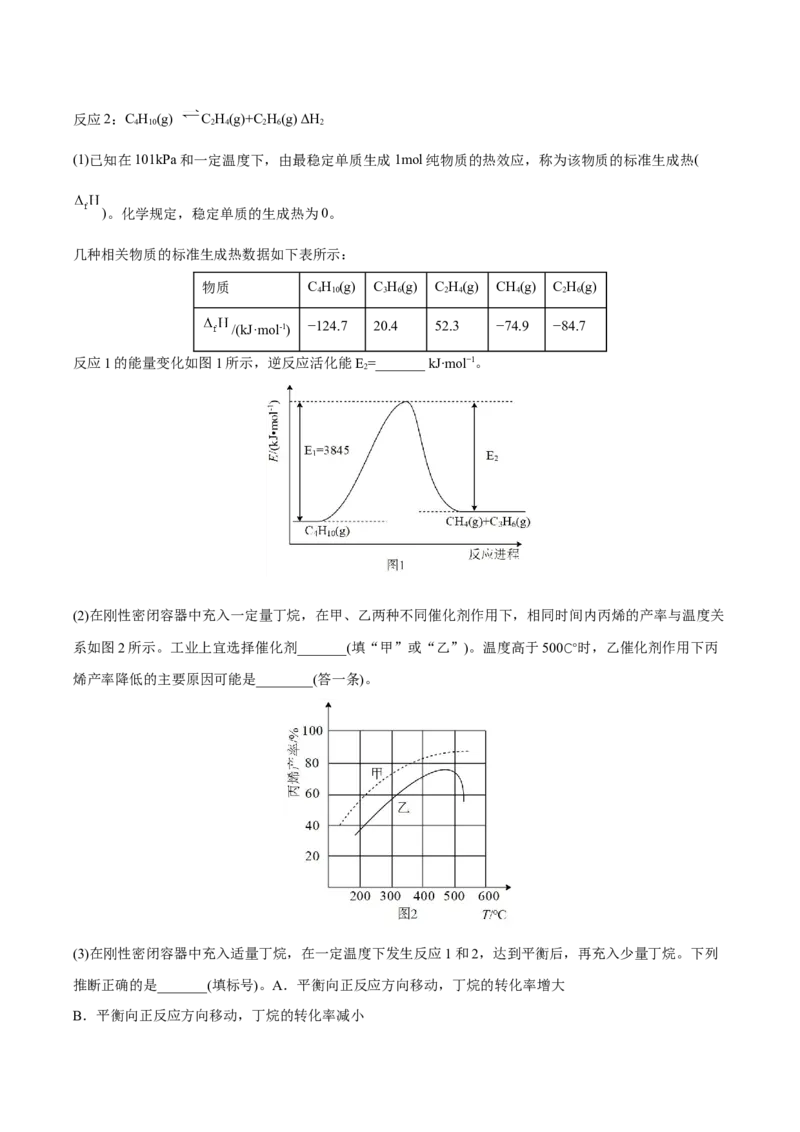
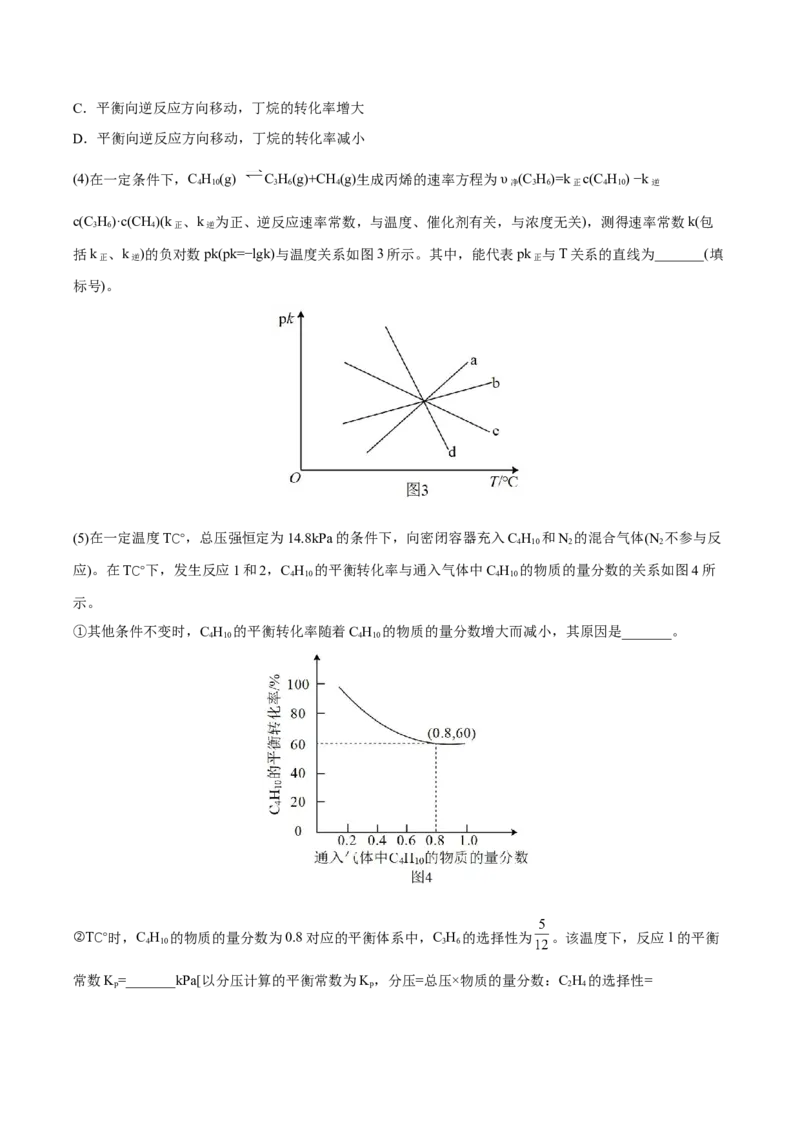
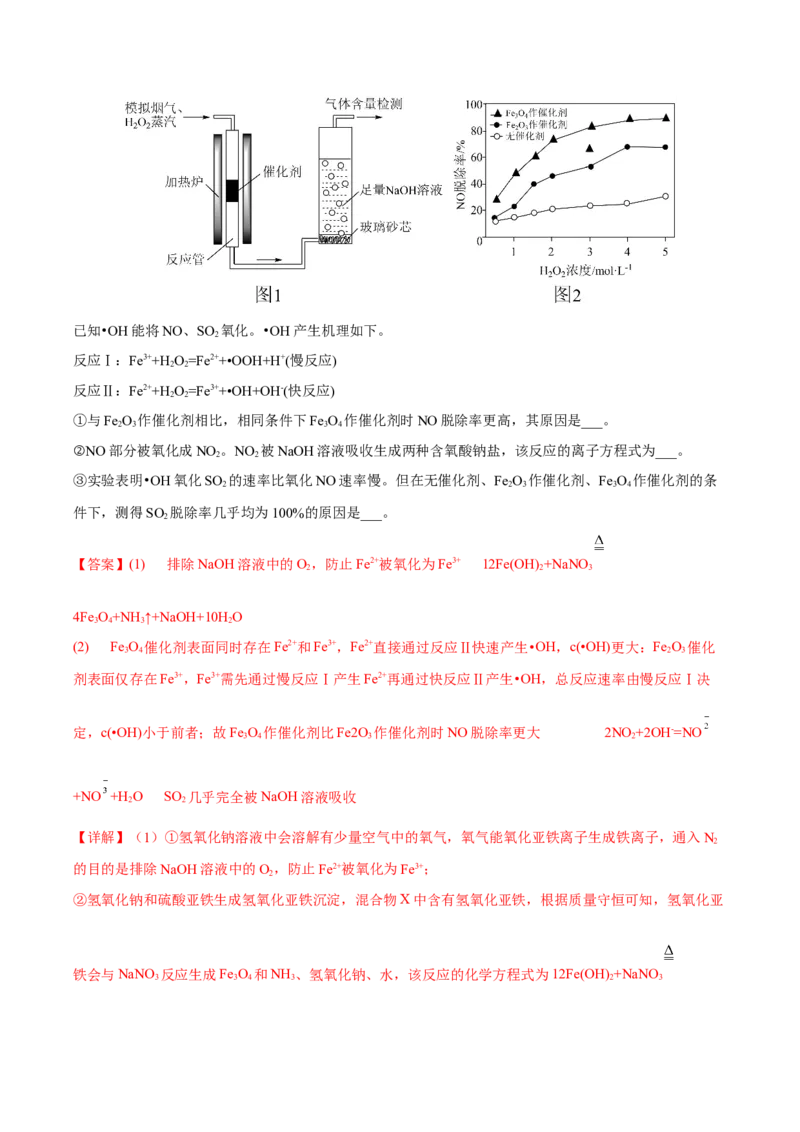
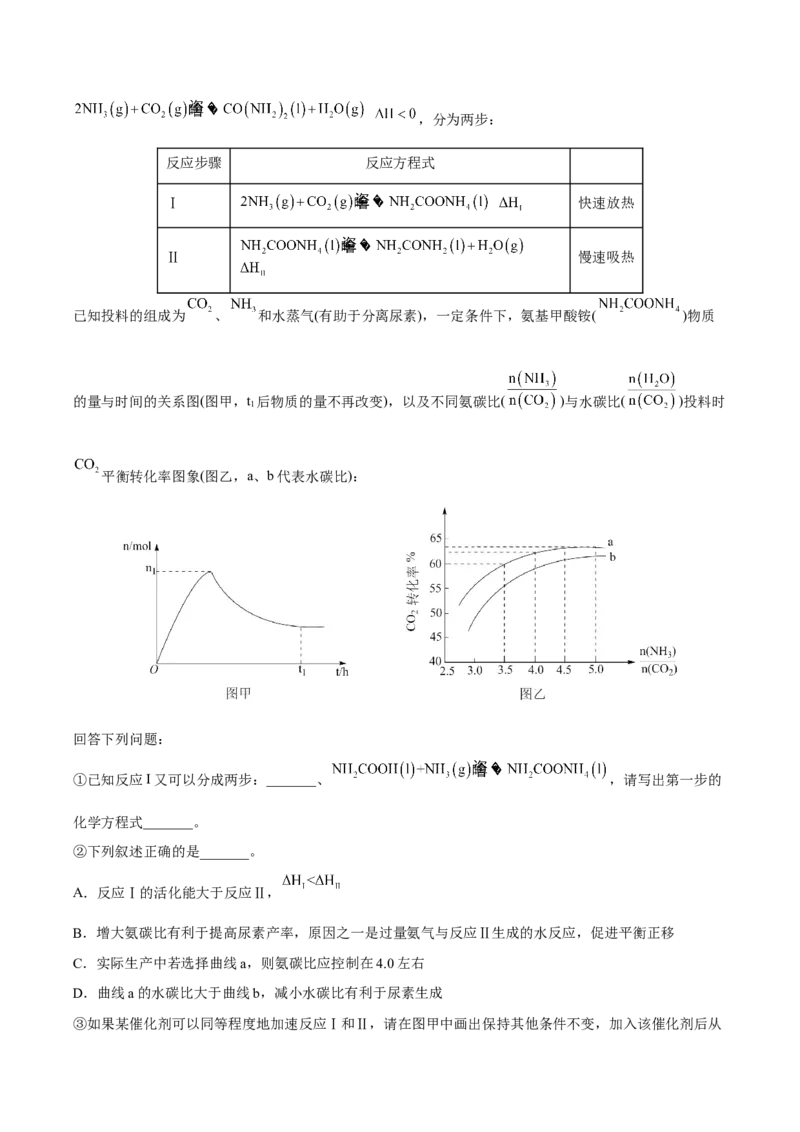
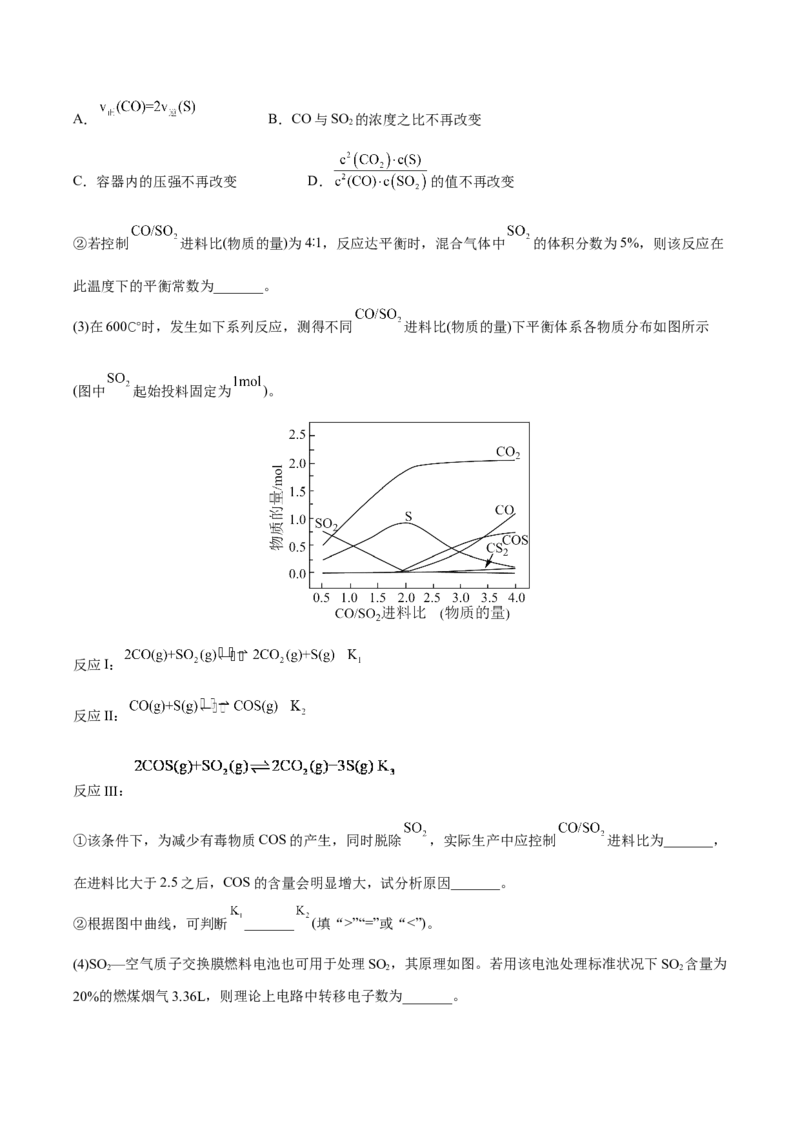
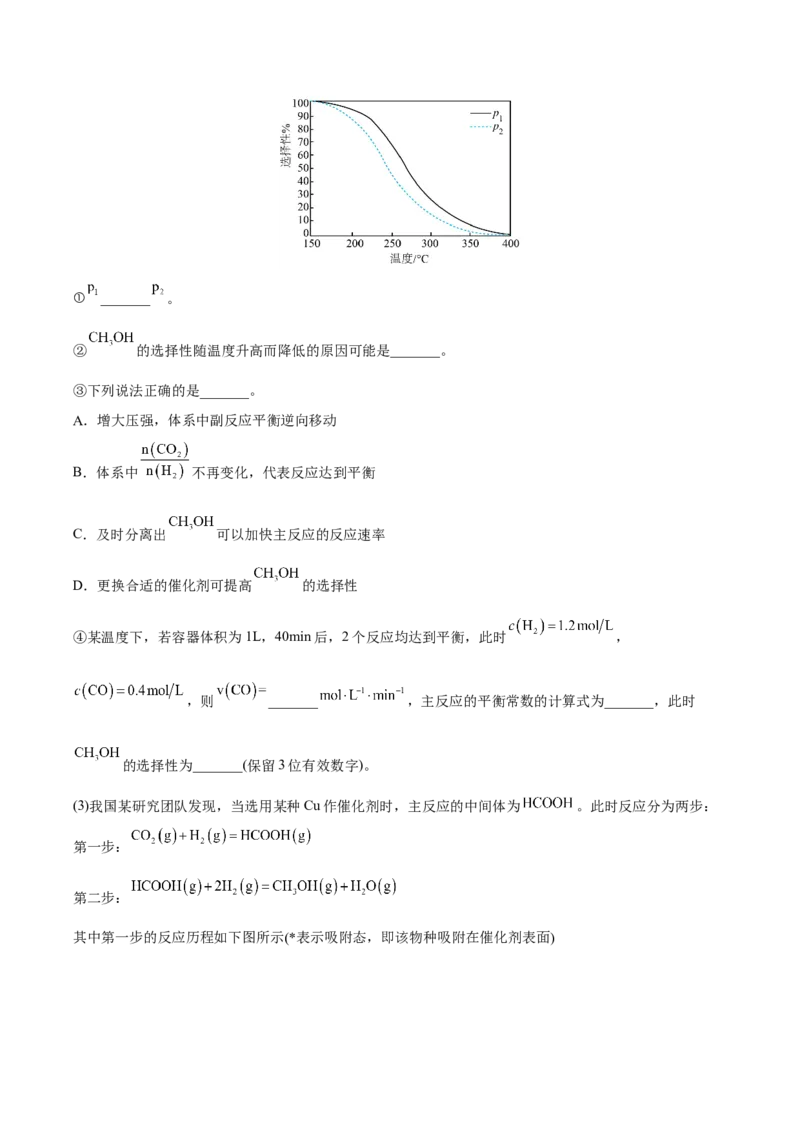
文档内容
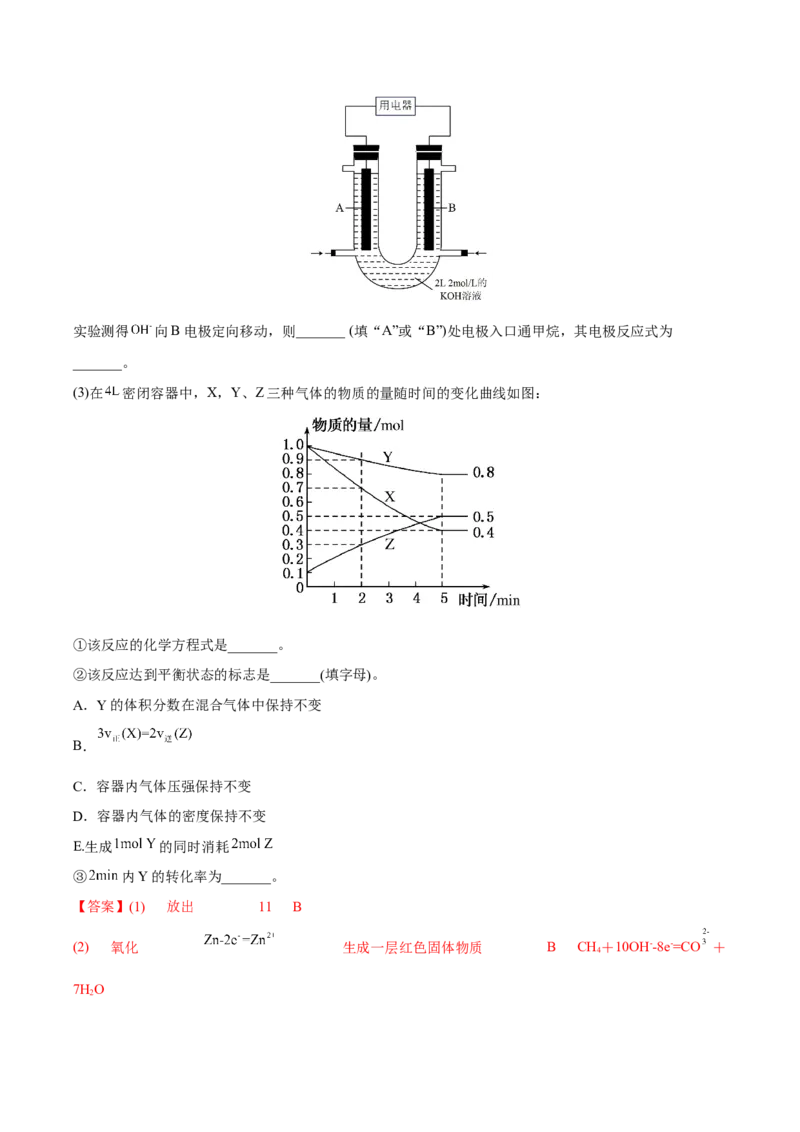
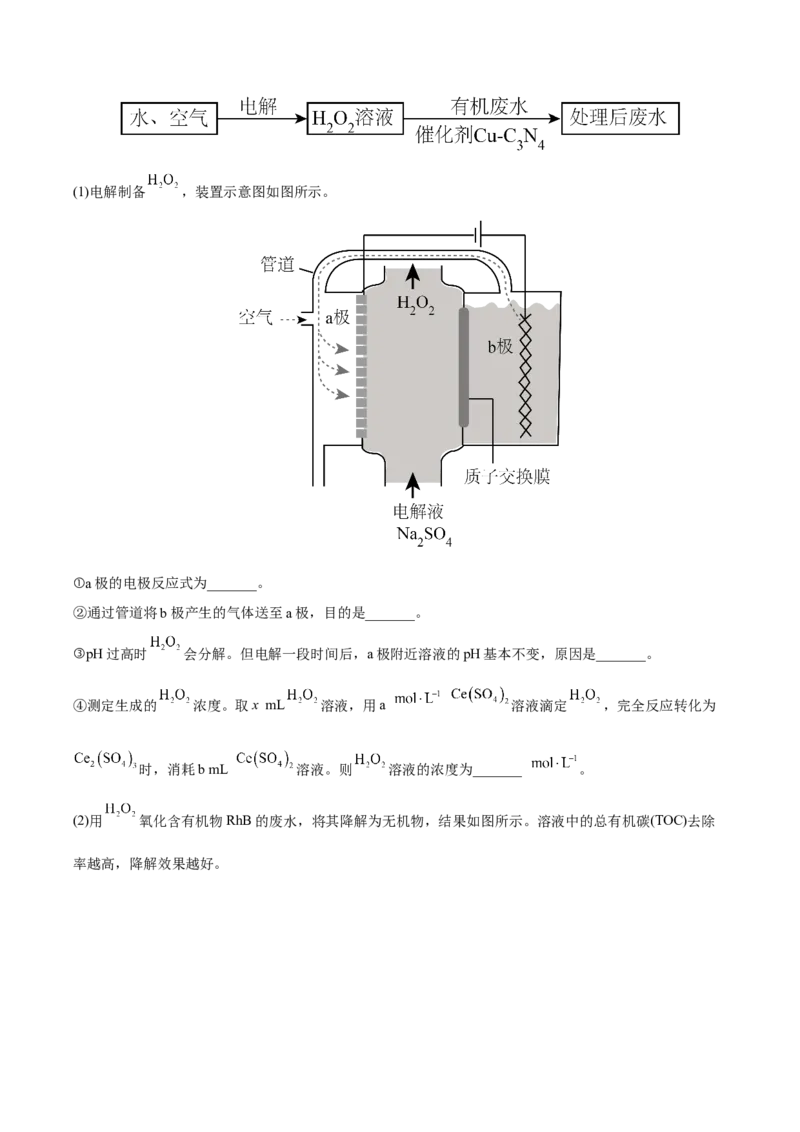
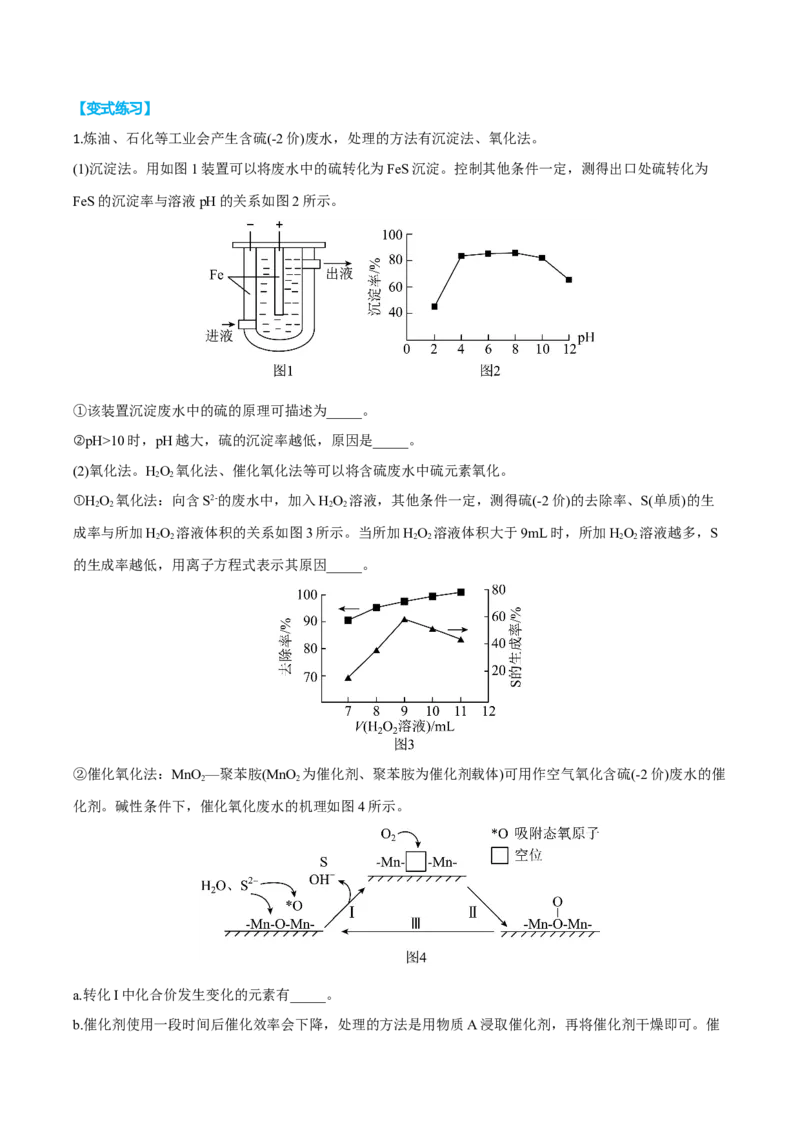
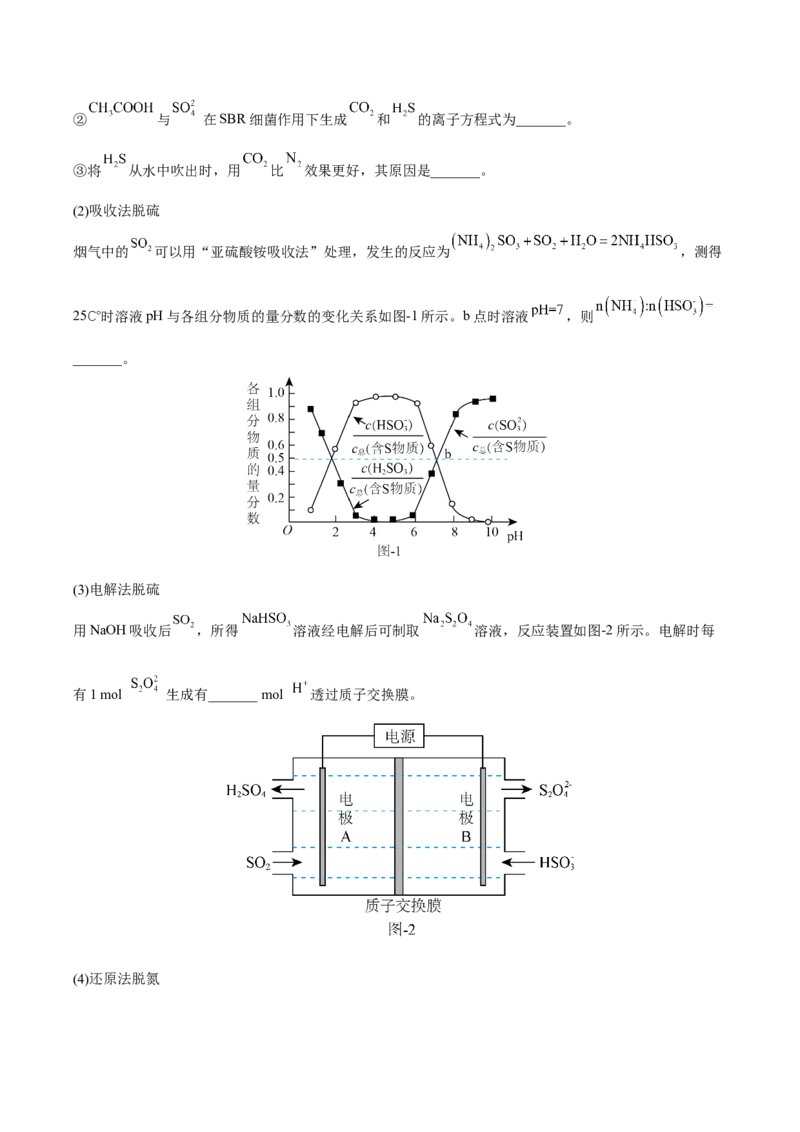
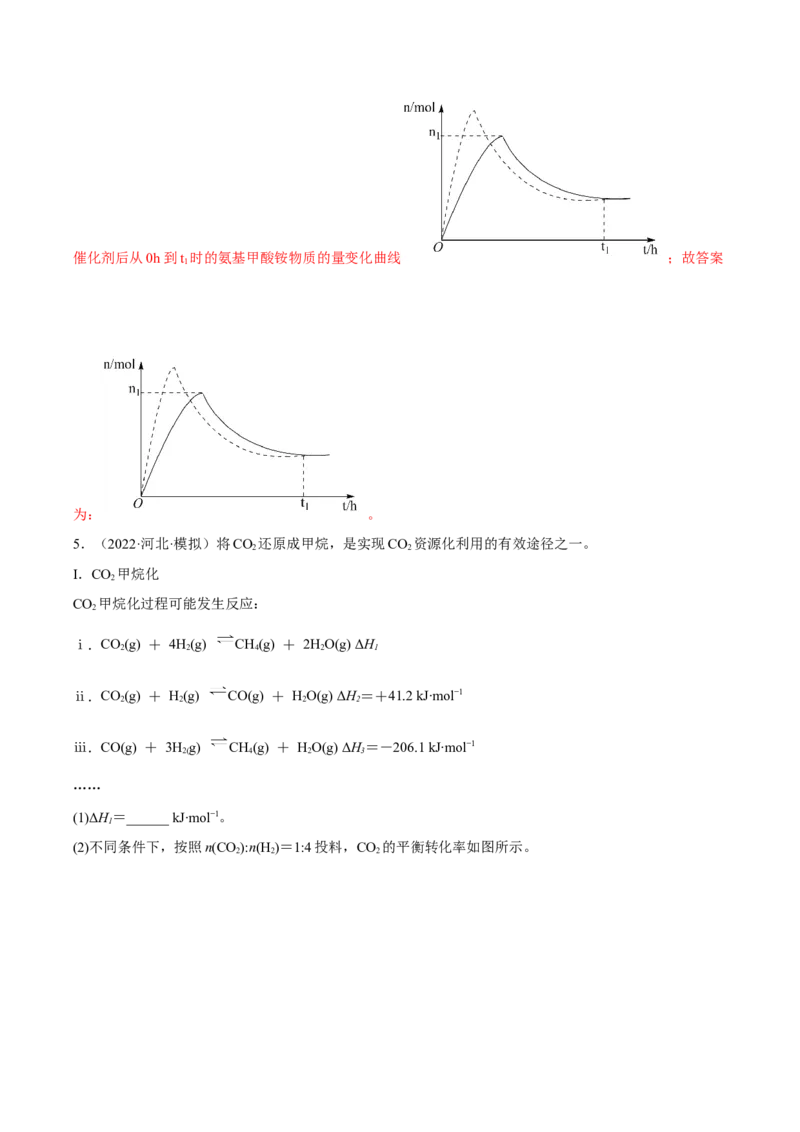
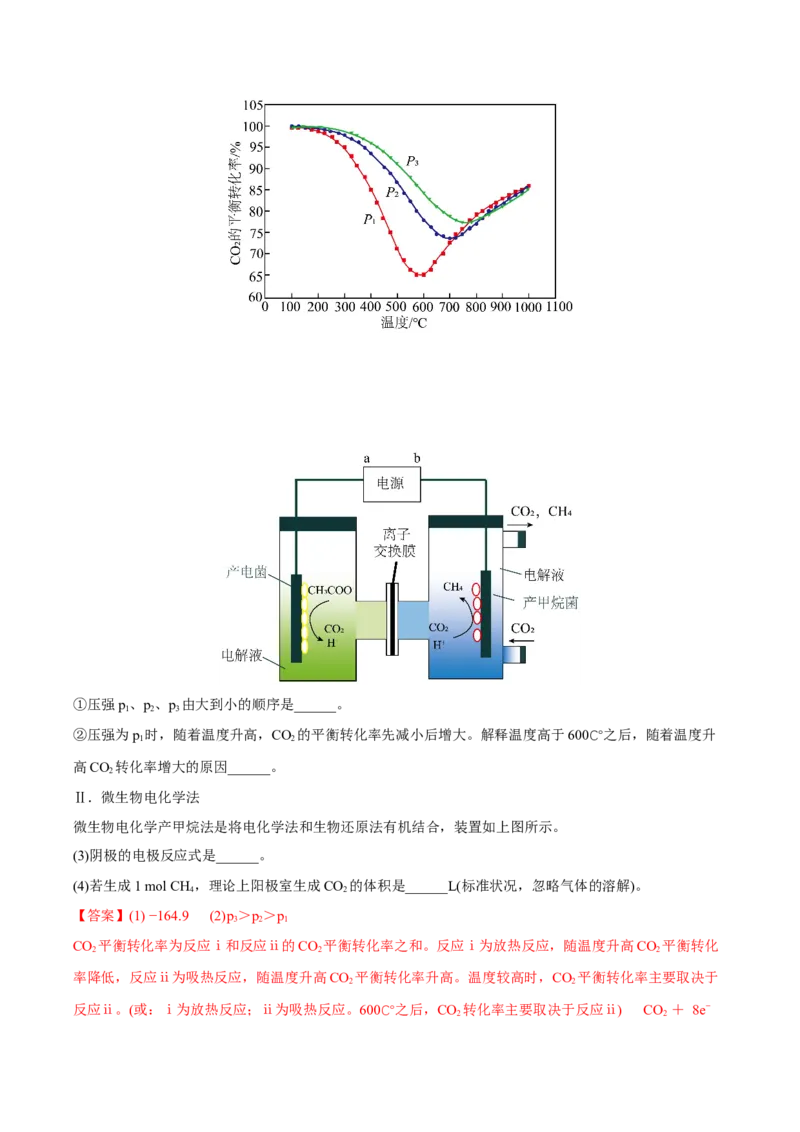
”“<”或“=”)。 1 2 Ⅱ.微生物燃料电池是一种利用微生物将化学能直接转化成电能的装置。已知某种甲醇( )微生物燃 料电池(如图所示)中,电解质溶液呈酸性。 (3)该电池中,外电路电流的流动方向为_______(填“从A到B”或“从B到A”)。 (4)B电极附近氧气发生的电极反应为_______。 (5)该燃料电池的总反应为_______。 Ⅲ.某可逆反应在体积为2L的恒温恒容密闭容器中进行,0~3min各物质的物质的量的变化情况如图所示 (A、C均为气体,B为固体)。 (6)该反应的化学方程式为_______。 (7)下列说法错误的是_______(填标号)。A.2min内A表示的反应速率为 B.增加B的物质的量,可使反应速率加快 C.当容器内混合气体的密度保持不变时,该反应达到平衡状态 D.当容器内压强保持不变时,该反应达到平衡状态 【答案】(1)吸热 (2) 92.4 > (3)从B到A (4) (5) (6) (7)BD 【解析】(1)反应的焓变为反应物的键能和减去生成物的键能和, 焓变为 6×391kJ-945.6kJ-3×436kJ=92.4kJ,焓变大于零,为吸热反应; (2)根据(1)分析可知, ,∆H=-92.4kJ/mol,则Q 为92.4k kJ。实际生产 1 中,反应为可逆反应,进行不完全,Q> Q 。 1 2 (3)由图可知,氧气在B极发生还原反应,为正极,则A为负极;外电路电流由正极流向负极,故流向 为从B到A; (4)氧气在B极得到电子,发生还原反应生成水, ; (5)该燃料电池中甲醇在负极发生氧化反应,总反应为甲醇和氧气生成二氧化碳和水, ; (6)由图可知,反应的ABC的物质的量比为(5mol-3mol):(2mol-1mol):(4mol-2mol)=2:1:2,且 反应后各物质共存,为可逆反应,故该反应的化学方程式为 ; (7)A.2min内A表示的反应速率为 ,A正确;B.B是固体,增加固体的物质的量,反应速率不变,B错误; C.容器内混合气体的质量是变量,则混合气体的密度也是变量,当变量保持不变时,该反应达到平衡状 态,C正确; D.该反应中气体物质的量始终保持不变,恒温恒容条件下,容器内的体压强是常量,也始终保持不变, 常量保持不变时,该反应可能达到平衡状态,也可能未达到平衡状态,D错误。 故选BD。 【变式练习】 1.回答下列问题: (1)化学反应的过程都是旧键断裂、新键形成的过程。对于反应: ,已知断开 键, 键分别需要吸收的能量是 和 ,形成 键需要放出的能量是 。 ① 和 完全反应共_______(填“放出”或“吸收”)能量_______ 。 ②如图,能够反映该反应能量变化的图象是_______(填“A”或“B”)。 (2)①如图所示,在银锌原电池中,以硫酸铜为电解质溶液,锌电极上发生的是_______ (填“氧化”或“还 原”)反应,电极反应式为_______。银片上观察到的现象是_______。 ②将 设计成燃料电池,其能量利用率更高,装置如图所示(A、B为多孔碳棒)。实验测得 向B电极定向移动,则_______ (填“A”或“B”)处电极入口通甲烷,其电极反应式为 _______。 (3)在 密闭容器中,X,Y、Z三种气体的物质的量随时间的变化曲线如图: ①该反应的化学方程式是_______。 ②该反应达到平衡状态的标志是_______(填字母)。 A.Y的体积分数在混合气体中保持不变 B. C.容器内气体压强保持不变 D.容器内气体的密度保持不变 E.生成 的同时消耗 ③ 内Y的转化率为_______。 【答案】(1) 放出 11 B (2) 氧化 生成一层红色固体物质 B CH+10OH--8e-=CO + 4 7HO 2(3) 3X+Y 2Z AC 60% 【详解】(1)①反应的焓变等于反应物的键能和减去生成物的键能和; 反应的焓变为 + -2× =-11kJ/mol;则 和 完全反应共放出能量11 。 ②该反应为放热反应,生成物能量低于反应物的能量,能够反映该反应能量变化的图象是B; (2)①在银锌原电池中,以硫酸铜为电解质溶液,锌较为活泼,为负极,锌电极上发生的是氧化反应, 电极反应式为 。银片为正极,铜离子放电生成铜单质,观察到的现象是生成一层红色固体物 质; ②将 设计成燃料电池,甲烷发生氧化反应为负极,氧气发生还原反应为正极,反应中阴离子向负极运 动;实验测得 向B电极定向移动,则B处电极入口通甲烷,其电极反应式为CH+10OH--8e-=CO + 4 7HO; 2 (3)①由图可知,反应达到平衡时,反应的YXZ的物质的量分别为0.2mol、0.6mol、0.4mol,则三者的 系数比为1:3:2,该反应的化学方程式是3X+Y 2Z; ②A.Y的体积分数在混合气体中保持不变,说明平衡不再移动,达到平衡,A正确; B.化学反应速率之比=计量数之比, ,此时正逆反应速率不相等,没有达到平衡,B错 误; C.反应为气体分子数改变的反应,容器内气体压强保持不变,达到平衡,C正确; D.容器体积和气体质量始终不变,则混合气体的密度始终不变,因此不能说明反应已达平衡;D错误; E.生成 的同时消耗 ,描述的都是逆反应,不能确定是否达到平衡,E错误; 故选AC; ③由图可知, 内Y反应的物质的量为0.6mol,转化率为 。 2.(2022·北京海淀·高三期末)传统方法制备 会产生大量副产物,研究者通过更环保的电解法,使 用空气和水制备 ,并用其处理有机废水,过程如下。(1)电解制备 ,装置示意图如图所示。 ①a极的电极反应式为_______。 ②通过管道将b极产生的气体送至a极,目的是_______。 ③pH过高时 会分解。但电解一段时间后,a极附近溶液的pH基本不变,原因是_______。 ④测定生成的 浓度。取x mL 溶液,用a 溶液滴定 ,完全反应转化为 时,消耗b mL 溶液。则 溶液的浓度为_______ 。 (2)用 氧化含有机物RhB的废水,将其降解为无机物,结果如图所示。溶液中的总有机碳(TOC)去除 率越高,降解效果越好。①20min时,RhB残留量已接近0。这段时间内RhB的平均降解速率=_______。 ②降解过程中,随着TOC去除率接近100%,溶液的pH降至5.6,请结合化学用语解释原因:_______。 【答案】(1) O+2H O+2e−= H O+2OH− 将b极产生的氧气循环利用,用于制备HO 反应中转移等 2 2 2 2 2 2 量的电子,阴极产生OH-与阳极产生H+的物质的量相等,阳极产生H+通过质子交换膜移至a极附近与OH- 反应 (2) HO 氧化有机物时,有机物中碳元素转化为CO,CO+H O HCO, 2 2 2 2 2 2 3 HCO H++HCO ,使溶液呈酸性,pH降低到5.6 2 3 【分析】(1)①氧气在a极得电子,化合价降低,发生还原反应生成过氧化氢,故a极的电极反应式为 O+2H O+2e−= H O+2OH−; 2 2 2 2 ②b极为阳极,发生氧化反应,生成氧气,故通过管道将b极产生的气体送至a极,目的是将b极产生的氧 气循环利用,用于制备HO; 2 2 ③电解时a极生成OH-,pH升高,b极生成H+,pH降低,H+能通过质子交换膜移动到a极,中和OH-,保 持a极附近溶液的pH不变,故为原因为:反应中转移等量的电子,阴极产生OH-与阳极产生H+的物质的 量相等,阳极产生H+通过质子交换膜移至a极附近与OH-反应; ④H O 和Ce(SO) 反应,Ce(SO) 做氧化剂,HO 做还原剂,根据电子守恒有如下关系,HO 2 2 4 2 4 2 2 2 2 2 ~2Ce(SO ),则HO 的浓度为 ; 4 2 2 2 (2)①20min时,RhB残留量已接近0;根据速率公式有,; ②H O 氧化有机物时,有机物中碳元素转化为CO,CO+H O HCO,HCO H++HCO ,使溶液呈 2 2 2 2 2 2 3 2 3 酸性,pH降低到5.6。 3.(2022·辽宁大连·二模)我国提出2060年前实现碳中和,为有效降低大气CO 中的含量,以CO 为原 2 2 料制备甲烷、戊烷、甲醇等能源物质具有较好的发展前景。CO 在固体催化剂表面加氢合成甲烷过程中发 2 生如下反应: Ⅰ.主反应: Ⅱ.副反应: (1)已知:Ⅲ. Ⅳ. 则 _______ (2)CO 加氢合成甲烷时,通常控制温度为 左右,其可能的原因为_______ 2 A.反应速率快 B.平衡转化率高 C.催化剂活性高 D.主反应催化剂选择性好 (3) 时,向1L恒容密闭容器中充入 和 ,初始压强为p, 时主、副反应都达到 平衡状态,测得 ,体系压强为 ,则 内 _______,平衡时 选择 性=_______( 选择性 ,计算保留三位有效数字) (4)以 催化加氢合成的甲醇为原料,在催化剂作用下可以制取丙烯,反应的化学方程式为 。该反应的Arrhenius经验公式的实验数据如图中曲线a所示,已知 Arhenius经验公式 ( 为活化能,k为速率常数,R和C为常数)。则该反应的活化能_______ 。当改变外界条件时,实验数据如图中的曲线b所示,则实验可能改变的外界条件是 _______。 【答案】(1) (2)ACD (3) 66.7% (4) 64 使用更高效的催化剂或增大催化剂的比表面积 【解析】(1)根据盖斯定律反应Ⅲ的2倍减去反应Ⅰ得到Ⅳ,则 ;故答案为: 。 (2)CO 加氢合成甲烷时,也有副产物发生,主反应是放热反应,副反应是吸热反应,通常控制温度为 2 左右,此时催化剂的活性高,反应速率快,由于有副反应发生,因此应是主反应催化剂选择性好, 而温度高,对副反应平衡正向移动,对主反应平衡逆向移动;故答案为:ACD。 (3) 时,向1L恒容密闭容器中充入 和 ,初始压强为p, 时主、副反应都达到 平衡状态,测得 ,体系压强为 ,建立三段式, ,2x+y=5,根据物质的量之比等于压强之比得 到 ,解得x=2,y=1,则 内 ,平衡时 选择性 ;故答案为: ;66.7%。 (4)根据题意和a曲线上两点得到8.0 =−3.2×103×Ea +C,1.6 =−3.3×10−3×Ea +C,两者方程式相减得到Ea=64 ,则该反应的活化能 64 。当改变外界条件时, 实验数据如图中的曲线b所示,斜率降低,说明活化能降低,则实验可能改变的外界条件是使用更高效的 催化剂或增大催化剂的比表面积;故答案为:64;使用更高效的催化剂或增大催化剂的比表面积。 探究三 化学能与电能 (2022·天津天津·高三期中)甲醇的结构决定了其性质及其应用。请按要求回答下列问题。 (1)甲醇、乙烷沸点分别为65℃、-89℃,对比分析推测乙醇比丙烷沸点____(填“高很多”或“低很多”或 “等于”),你的推测依据是____。 (2)甲醇结构式如图,其分子中含a、b、c三种化学键。 ①甲醇的官能团名称为____。 ②甲醇分子中较易断裂的化学键是____(填字母)。从原子结构的视角分析得出此结论的依据是____。③写出甲醇与钠反应的化学方程式____。 ④在铜催化加热条件下,甲醇发生反应的化学方程式为____。 (3)甲醇燃料电池装置示意图如图所示: 它可将化学能转变为电能,可作为笔记本电脑等能量的来源。在催化剂作用下甲醇转化为HO和CO。写 2 2 出该电池工作时负极电极反应式:____。 【答案】(1) 高很多 乙醇分子间存在氢键,而丙烷分子间不存在氢键 (2) 羟基 bc 氧原子的吸引电子的能力比氢原子和碳原子的强 2CHOH+2Na→2CH ONa+H ↑ 2CHOH+O 2HCHO+2H O 3 3 2 3 2 2 (3)2CH OH+2H O-12e-=2CO ↑+12H+ 3 2 2 【详解】(1)乙醇、丙烷均为分子晶体,乙醇分子间存在氢键,而丙烷分子间不存在氢键,氢键的形成 导致其沸点升高,故推测乙醇比丙烷沸点高很多; (2)①由图可知,甲醇的官能团名称为羟基。 ②同周期从左到右,金属性减弱,非金属性变强,元素的电负性变强;同主族由上而下,金属性增强,非 金属性逐渐减弱,元素电负性减弱;氧的电负性强,其原子的吸引电子的能力比氢原子和碳原子的强,导 致甲醇分子中较易断裂的化学键是碳氧键、氢氧键。 ③甲醇与钠反应生成甲醇钠和氢气,2CHOH+2Na→2CH ONa+H ↑。 3 3 2 ④在铜催化加热条件下,甲醇中羟基被氧化为醛基生成甲醛,发生反应的化学方程式为2CHOH+O 3 2 2HCHO+2H O; 2 (3)反应中氧气生成水,反应还原反应,为正极;甲醇发生氧化生成二氧化碳和水,为负极;在催化剂 作用下甲醇失去电子发生氧化反应转化为HO和CO,反应为2CHOH+2H O-12e-=2CO ↑+12H+。 2 2 3 2 2【变式练习】 1.炼油、石化等工业会产生含硫(-2价)废水,处理的方法有沉淀法、氧化法。 (1)沉淀法。用如图1装置可以将废水中的硫转化为FeS沉淀。控制其他条件一定,测得出口处硫转化为 FeS的沉淀率与溶液pH的关系如图2所示。 ①该装置沉淀废水中的硫的原理可描述为_____。 ②pH>10时,pH越大,硫的沉淀率越低,原因是_____。 (2)氧化法。HO 氧化法、催化氧化法等可以将含硫废水中硫元素氧化。 2 2 ①HO 氧化法:向含S2-的废水中,加入HO 溶液,其他条件一定,测得硫(-2价)的去除率、S(单质)的生 2 2 2 2 成率与所加HO 溶液体积的关系如图3所示。当所加HO 溶液体积大于9mL时,所加HO 溶液越多,S 2 2 2 2 2 2 的生成率越低,用离子方程式表示其原因_____。 ②催化氧化法:MnO —聚苯胺(MnO 为催化剂、聚苯胺为催化剂载体)可用作空气氧化含硫(-2价)废水的催 2 2 化剂。碱性条件下,催化氧化废水的机理如图4所示。 a.转化I中化合价发生变化的元素有_____。 b.催化剂使用一段时间后催化效率会下降,处理的方法是用物质A浸取催化剂,再将催化剂干燥即可。催化剂使用一段时间后催化效率降低的原因是_____;物质A可选用_____(填序号)。 A.水 B.乙醇 C.CS D.浓盐酸 2 c.从物质转化与资源综合利用角度分析,催化氧化法的优点是_____。 【答案】(1) 电解时阳极Fe失去电子生成Fe2+,Fe2+可与废水中S2-反应生成FeS沉淀 pH>10 时,pH越大,Fe2+转化为Fe(OH) 沉淀,生成FeS沉淀的硫的量越少 2 (2) S2-+4H O=SO +4H O S、O、Mn 生成的S覆盖在催化剂表面或进入催化剂内空隙处,减少了 2 2 2 催化剂与废水反应的接触面积 C 催化氧化速率更快,除硫效率更高;以空气做氧化剂比HO 2 2 更经济 【解析】(1)①由图可知,图1装置为电解池,电极材料均为Fe,电解时阳极Fe失去电子发生氧化反应 生成Fe2+,Fe2+与废水中的S2-结合生成FeS沉淀,从而达到净化废水的目的; ②当pH>10时,pH越大,OH-浓度越大,废水中Fe2+与OH-结合生成Fe(OH) 沉淀,导致转化成FeS沉淀 2 的量减少,使得硫的沉淀率越低; (2)①HO 具有强氧化性,HO 溶液体积大于9mL时,所加HO 溶液越多,S生成率越低,可能是因为 2 2 2 2 2 2 硫元素被氧化成更高价态的 而滞留在溶液中,导致硫的生成率降低,反应为S2-+4H O=SO +4H O; 2 2 2 ②a.由图可知,转化Ⅰ中硫离子转化为硫单质,催化剂表面锰化合价由+1变为0,氧原子变为负二氧,故S 元素、O元素和Mn元素的化合价均发生变化; b. 由图可知,反应过程中生成了单质S,生成的S覆盖在催化剂表面或进入催化剂内空隙处,减少了催化 剂与废水反应的接触面积,从而导致催化效率下降;硫单质不和水、乙醇、浓盐酸反应且不溶于三者,硫 单质能溶于二硫化碳溶液,从而除去催化剂表面的硫单质,故选C; c.催化氧化可用空气氧化含硫(-2价)废水,催化剂使得反应速率更快,除硫效率更高且以空气做氧化剂比 HO 更经济。 2 2 2.工业上常用微生物法、吸收法、电解法、还原法等消除硫、氮等引起的污染。 (1)微生物法脱硫 富含有机物的弱酸性废水在SBR细菌作用下产生 、 等物质,可将废水中 还原为 , 同时用 或 将 从水中吹出,再用碱液吸收。 ① 的空间构型为_______。② 与 在SBR细菌作用下生成 和 的离子方程式为_______。 ③将 从水中吹出时,用 比 效果更好,其原因是_______。 (2)吸收法脱硫 烟气中的 可以用“亚硫酸铵吸收法”处理,发生的反应为 ,测得 25℃时溶液pH与各组分物质的量分数的变化关系如图-1所示。b点时溶液 ,则 _______。 (3)电解法脱硫 用NaOH吸收后 ,所得 溶液经电解后可制取 溶液,反应装置如图-2所示。电解时每 有1 mol 生成有_______ mol 透过质子交换膜。 (4)还原法脱氮用催化剂协同纳米零价铁去除水体中 。其催化还原反应的过程如图-3所示。 ①该反应机理中生成 的过程可描述为_______。 ②过程中 去除率及 生成率如图-4所示,为有效降低水体中氮元素的含量,宜调整水体pH为4.2, 当 时,随pH减小, 生成率逐渐降低的原因是_______。 【答案】(1) 正四面体形 二 氧化碳吹出时可增强溶液的酸性,抑制硫化氢的溶解,有利于将硫化氢吹出 (2)3:1 (3)2 (4) 纳米零价铁在催化剂表面失去电子变为亚铁离子,在催化剂层中氢离子得到电子变为氢原子,在酸 性条件下氢原子还原硝酸根变为NH,NH失去氢原子变为氮气 pH越小,氢离子浓度越大,会生成更多的氢原子,使硝酸根生成的中间产物NH更多的与氢原子反应生成铵根离子,从而减少氮气的生成 【解析】(1)① 中S原子价层电子对数为 ,其空间构型为正四面体形; 故答案为:正四面体形。 ② 与 在SBR细菌作用下生成 和 ,该反应在弱酸性条件下反应,根据氧化还原反 应得失电子守恒配平得到,其的离子方程式为 ;故 答案为: 。 ③将 从水中吹出时,用 比 效果更好,二氧化碳溶于水生成碳酸,增强溶液的酸性,抑制硫化氢 溶解,因此其原因是二氧化碳吹出时可增强溶液的酸性,抑制硫化氢的溶解,有利于将硫化氢吹出;故答 案为:二氧化碳吹出时可增强溶液的酸性,抑制硫化氢的溶解,有利于将硫化氢吹出。 (2)根据亚硫酸氢铵溶液的电荷守恒得到 ,b点时溶液 ,得到 ,测得25℃时溶液pH与各组分物质的量分数的变化关系如图-1所示, 则b点是 ,得到 ,则 ;故答案为:3:1。 (3)根据图中信息左边为阳极,右边为阴极,阴极电极反应式为 ,因 此电解时每有1 mol 生成有2mol 透过质子交换膜;故答案为:2。 (4)①根据图中信息,该反应机理中生成 的过程可描述为纳米零价铁在催化剂表面失去电子变为亚铁 离子,在催化剂层中氢离子得到电子变为氢原子,在酸性条件下氢原子还原硝酸根变为NH,NH失去氢原 子变为氮气;故答案为:纳米零价铁在催化剂表面失去电子变为亚铁离子,在催化剂层中氢离子得到电子 变为氢原子,在酸性条件下氢原子还原硝酸根变为NH,NH失去氢原子变为氮气。②过程中 去除率及 生成率如图-4所示,为有效降低水体中氮元素的含量,宜调整水体pH为4.2, 当 时,随pH减小, 生成率逐渐降低,根据图中信息氢离子浓度越大,会生成更多的氢原子,使 硝酸根生成的中间产物NH更多的与氢原子反应生成铵根离子,从而减少氮气的生成;故答案为:pH越 小,氢离子浓度越大,会生成更多的氢原子,使硝酸根生成的中间产物NH更多的与氢原子反应生成铵根 离子,从而减少氮气的生成。 3.(2022·北京房山·二模)氨对人类的生存和发展有着重要意义,1909年哈伯在实验室中首次利用氮气与 氢气反应合成氨,实现了人工固氮。 (1)反应N(g)+3H(g) 2NH (g)的化学平衡常数表达式为____。 2 2 3 (2)在一定条件下氨的平衡含量如表。 温度/℃ 压强/MPa 氨的平衡含量 200 10 81.5% 550 10 8.25% ①该反应为____(填“吸热”或“放热”)反应。 ②哈伯选用的条件是550℃、10MPa,而非200℃、10MPa,可能的原因是____。 (3)实验室研究是工业生产的基石。如图中的实验数据是在其它条件不变时,不同温度(200℃、400℃、 600℃)、压强下,平衡混合物中NH 的物质的量分数的变化情况。 3 ①曲线a对应的温度是____。 ②M、N、Q点平衡常数K的大小关系是____。 (4)尽管哈伯的合成氨法被评为“20世纪科学领域中最辉煌的成就”之一,但仍存在耗能高、产率低等问题。因此,科学家在持续探索,寻求合成氨的新路径。如图为电解法合成氨的原理示意图,阴极的电极反 应式为____。 (5)NH 转化为NO是工业制取硝酸的重要一步。已知:100kPa、298K时: 3 4NH (g)+3O(g) 2N(g)+6HO(g)ΔH=-1268kJ·mol-1 3 2 2 2 2NO(g) N(g)+O(g)ΔH=-180.5kJ·mol-1 2 2 请写出NH 转化为NO的热化学方程式____。 3 【答案】(1)K= (2) 放热 温度过低反应速率太慢;温度过高不利于反应平衡正向移动 (3) 200℃ K =K >K Q M N (4)N +6e−+6H+=2NH 2 3 (5)4NH (g)+5O(g) 4NO(g)+6H O(g) ΔH=−907kJ·mol−1 3 2 2 【解析】(1)根据平衡常数的表达式可知,该反应的平衡常数K= ; (2)①根据表格数据可知,压强不变,升高温度氨的平衡含量降低,说明升高温度平衡逆向移动,所以 该反应为放热反应; ②温度过低反应速率太慢;温度过高不利于反应平衡正向移动,所以选用的条件是550℃、10MPa; (3)①该反应为放热反应,压强相同时,温度越低NH 的物质的量分数越大,所以曲线a对应的温度为 3 200℃; ②该反应为放热反应,温度越高,平衡常数越小,温度:Q=M<N,所以平衡常数:K =K >K ; Q M N (4)据图可知,阴极上N 被还原为NH ,环境为酸性环境,所以阴极的电极反应式为N+6e− 2 3 2 +6H+=2NH; 3 (5)NH 转化为NO的化学方程式为4NH (g)+5O(g) 4NO(g)+6H O(g),依次将所给两个热化学方程式 3 3 2 2 标号为①、②,根据盖斯定律,①-②×2可得4NH (g)+5O(g) 4NO(g)+6H O(g)的ΔH=-1268kJ·mol-1- 3 2 2 (-180.5kJ·mol-1)×2=−907kJ·mol−1。1.(2022·山东·胜利一中模拟)1,6−己二醇是一种重要的化工原料,与乙二醇相比,用1,6−己二醇为原料 制备的聚酯具有更为优异的柔韧性和抗腐蚀性。工业上利用己二酸二甲酯加氢制备1,6−己二醇,该反应的 化学方程式如图: (g)+4H(g)→ (g)+2CH OH(g) ΔH。 2 3 (1)已知: 化学键 C=O C−O C−H C−C O−H H−H 键能/ kJ∙mol−1 745 358 413 347 467 436 计算上述反应的△H=___;此反应自发进行的条件是____(填“高温易自发”“低温易自发”或“任何温度 都能自发”)。 (2)将组成(物质的量分数)为4n%H (g)、n% (g)的气体通入刚性密闭反应器中, 2 在温度一定、压强为pMPa条件下只进行上述反应。平衡时,若压强为qMPa,平衡时 (g)的转化率为=____ (用p、q的代数式表示,下同),平衡常数K=____(以 p 分压表示,分压=总压×物质的量分数)。 (3)科研小组在高压反应釜中进行催化加氢反应,对己二酸二甲酯制备1,6−己二醇的工艺条件进行了研究。 图甲和图乙为此反应在相同时间时,反应压力、反应温度与反应物的转化率和1,6−己二醇选择性的变化关 系。已知,选择性= ×100%。 ①由图可知,在压强为27MPa时,己二酸二甲酯制备1,6−己二醇应选择的合适温度为____;选择此温度的 理由是____;当260℃时,转化率随着压强增大而不断增大的原因是____。 ②图丙为反应时间与加氢反应时反应物的转化率和选择性的关系。 综合考虑,反应时间控制在5h左右较为合适。此时1,6−己二醇的产率为____。 【答案】(1) −286 kJ∙mol−1 低温易自发 (2) ×100%或 % (3) 290℃ 290℃时反应物的转化率较高,且此温度下的产物选择性较高 相同温度时压强大,反应速率加快,且达到平衡后,增大压强利于平衡正向移动,使反应物转化率增大 50.05% 【解析】(1)根据方程式分析得到酯基中碳氧单键断裂,形成氧氢键和碳氢键,碳氧双键断裂又形成碳 氢键、碳氧单键和氧氢键,因此可简化计算上述反应的△H=2E(C=O)+2E(C−O)+4E(H−H) −4E(O−H) −4E(C−H) −2E(C−O) =745 kJ∙mol−1×2+436 kJ∙mol−1×4−467kJ∙mol−1×4−413 kJ∙mol−1×4= −286 kJ∙mol−1;该反 应是气体体积减小的反应即△H<0、△S<0,根据△G=△H−T△S判断温度低的时候△G<0,因此得到低 温易自发;故答案为:−286 kJ∙mol−1;低温易自发。 (2)根据题意建立三段式 0.2p−x+0.8p−4x+x+2x=q,解得2x=p−q,x= ,则a(已二酸二甲酯)= ×100%或 %;K= p ;故答案为: ×100%或 %; 。 (3)①由图可知,在27MPa时,290°C己二酸二甲酯的转化率和1,6−己二醇的选择性均高于280°C,因此 温度选择290°C;相同温度时压强大,反应速率快,且达平衡时,增大压强有利于平衡正向移动,使反应 物转化率增大;故答案为:290°C ;290℃时反应物的转化率较高,且此温度下的产物选择性较高;相同 温度时压强大,反应速率加快,且达到平衡后,增大压强利于平衡正向移动,使反应物转化率增大。 ②反应时间控制在5h时,产物的产率为92%×54.4%≈50.05%;故答案为:50.05%。 2.(2022·湖南娄底·模拟)丙烯是合成多种高分子材料的原料,工业上常采用裂解丁烷获得丙烯。化学原 理如下: 反应1:C H (g) C H(g)+CH (g) ΔH 4 10 3 6 4 1反应2:C H (g) C H(g)+C H(g) ΔH 4 10 2 4 2 6 2 (1)已知在101kPa和一定温度下,由最稳定单质生成1mol纯物质的热效应,称为该物质的标准生成热( )。化学规定,稳定单质的生成热为0。 几种相关物质的标准生成热数据如下表所示: 物质 C H (g) C H(g) C H(g) CH(g) C H(g) 4 10 3 6 2 4 4 2 6 /(kJ·mol-1) −124.7 20.4 52.3 −74.9 −84.7 反应1的能量变化如图1所示,逆反应活化能E=_______ kJ∙mol−1。 2 (2)在刚性密闭容器中充入一定量丁烷,在甲、乙两种不同催化剂作用下,相同时间内丙烯的产率与温度关 系如图2所示。工业上宜选择催化剂_______(填“甲”或“乙”)。温度高于500℃时,乙催化剂作用下丙 烯产率降低的主要原因可能是________(答一条)。 (3)在刚性密闭容器中充入适量丁烷,在一定温度下发生反应1和2,达到平衡后,再充入少量丁烷。下列 推断正确的是_______(填标号)。A.平衡向正反应方向移动,丁烷的转化率增大 B.平衡向正反应方向移动,丁烷的转化率减小C.平衡向逆反应方向移动,丁烷的转化率增大 D.平衡向逆反应方向移动,丁烷的转化率减小 (4)在一定条件下,C H (g) C H(g)+CH (g)生成丙烯的速率方程为υ (C H)=k c(C H ) −k 4 10 3 6 4 净 3 6 正 4 10 逆 c(C H)·c(CH)(k 、k 为正、逆反应速率常数,与温度、催化剂有关,与浓度无关),测得速率常数k(包 3 6 4 正 逆 括k 、k )的负对数pk(pk=−lgk)与温度关系如图3所示。其中,能代表pk 与T关系的直线为_______(填 正 逆 正 标号)。 (5)在一定温度T℃,总压强恒定为14.8kPa的条件下,向密闭容器充入C H 和N 的混合气体(N 不参与反 4 10 2 2 应)。在T℃下,发生反应1和2,C H 的平衡转化率与通入气体中C H 的物质的量分数的关系如图4所 4 10 4 10 示。 ①其他条件不变时,C H 的平衡转化率随着C H 的物质的量分数增大而减小,其原因是_______。 4 10 4 10 ②T℃时,C H 的物质的量分数为0.8对应的平衡体系中,C H 的选择性为 。该温度下,反应1的平衡 4 10 3 6 常数K=_______kPa[以分压计算的平衡常数为K,分压=总压×物质的量分数:C H 的选择性= p p 2 4]。 (6)己二睛是合成尼龙66的原料。工业上,采用丙烯氨氧化法制备丙烯腈(CH=CH−CN),又采用电有机合 2 成法制备己二睛[NC(CH )CN],装置如图所示。 2 4 阴极反应式为_______。 【答案】(1)3774.8 (2) 甲 催化剂乙的活性降低、选择性降低或副产物增多 (3)B (4)d (5) 平衡体系分压增大,平衡向逆反应方向移动 5 (6)2CH =CHCN+2H++2e-=NC(CH)CN 2 2 4 【解析】(1)根据生成热定义,物质的生成热可以表示其相对能量高低,反应热等于产物总能量与反应物总 能量之差,ΔH=(20.4+124.7−74.9) kJ∙mol−1=+70.2 kJ∙mol−1。同理可得: 1 △H=(52.3+124.7−84.7)kJ∙mol−1=+92.3 kJ∙mol−1。反应热等于正反应活化能与递反应活化能之差, 2 E=(3845−70.2) kJ∙mol−1=3774.8 kJ∙mol−1;故答案为:3774.8。 2 (2)根据图中曲线得到工业上选择催化效率高的催化剂甲;温度高于500°C,催化剂乙的活性降低、选择性 降低或副产物增多等导致丙烯产率降低;故答案为:甲;催化剂乙的活性降低、选择性降低或副产物增 多。 (3)在恒温恒容条件下,平衡常数不变,平衡后充入丁烷,平衡向正反应方向移动。可以用模拟法判断丁烷 转化率变化,充入丁烷后相当于将原平衡体系加压,丁烷的平衡转化率减小;故答案为:B。 (4)正反应是吸热反应,升高温度,平衡常数增大。平衡时净反应速率为0,有K= ,升高温度,速率常 数均增大,且k 增大的倍数大于k 增大的倍数。k越大,pk越小;故答案为:d。 正 逆(5)①总压强不变的条件下,增大混合气体中丁烷的物质的量分数,平衡体系的分压增大,平衡向逆反应方 向移动,故丁烷的平衡转化率减小;故答案为:平衡体系分压增大,平衡向逆反应方向移动。 ②取混合气体中n(C H )=0.8mol,n(N )=0.2mol。 4 10 2 反应1: ,反应2: , , 解得:x=0.4,y=0.08;平衡体系中气体的总物质的量为 0.32mol+0.08mol+0.08mol+0.4mol+0.4mol+0.2mol=1.48mol。p(C H )=14.8kPa× =3.2kPa, 4 10 p(C H)=p(CH )=4.0kPa, =5kPa;故答案为:5。 3 6 4 (6)根据图中信息,水中氢氧根得到电子变为氧气,因此阴极上丙烯睛发生还原反应,电极反应式为 2CH=CHCN+2H++2e-=NC(CH)CN;故答案为:2CH=CHCN+2H++2e-=NC(CH)CN。 2 2 4 2 2 4 3.(2022·江苏江苏·二模)我国学者分别使用Fe O 和Fe O 作催化剂对燃煤烟气脱硝脱硫进行了研究。 2 3 3 4 (1)催化剂制备。在60~100℃条件下,向足量NaOH溶液中通入N 一段时间,再加入适量新制FeSO 溶 2 4 液,充分反应后得到混合物X;向混合物X中加入NaNO 溶液,充分反应后经磁铁吸附、洗涤、真空干 3 燥,制得Fe O 催化剂。 3 4 ①通入N 的目的是___。 2 ②混合物X与NaNO 反应生成Fe O 和NH ,该反应的化学方程式为___。 3 3 4 3 (2)催化剂性能研究。如图1所示,当其他条件一定时,分别在无催化剂、Fe O 作催化剂、Fe O 作催化剂 2 3 3 4 的条件下,测定HO 浓度对模拟烟气(含一定比例的NO、SO 、O、N)中NO和SO 脱除率的影响,NO 2 2 2 2 2 2 脱除率与HO 浓度的关系如图2所示。 2 2已知•OH能将NO、SO 氧化。•OH产生机理如下。 2 反应Ⅰ:Fe3++H O=Fe2++•OOH+H+(慢反应) 2 2 反应Ⅱ:Fe2++H O=Fe3++•OH+OH-(快反应) 2 2 ①与Fe O 作催化剂相比,相同条件下Fe O 作催化剂时NO脱除率更高,其原因是___。 2 3 3 4 ②NO部分被氧化成NO 。NO 被NaOH溶液吸收生成两种含氧酸钠盐,该反应的离子方程式为___。 2 2 ③实验表明•OH氧化SO 的速率比氧化NO速率慢。但在无催化剂、Fe O 作催化剂、Fe O 作催化剂的条 2 2 3 3 4 件下,测得SO 脱除率几乎均为100%的原因是___。 2 【答案】(1) 排除NaOH溶液中的O,防止Fe2+被氧化为Fe3+ 12Fe(OH) +NaNO 2 2 3 4Fe O+NH↑+NaOH+10HO 3 4 3 2 (2) Fe O 催化剂表面同时存在Fe2+和Fe3+,Fe2+直接通过反应Ⅱ快速产生•OH,c(•OH)更大:Fe O 催化 3 4 2 3 剂表面仅存在Fe3+,Fe3+需先通过慢反应Ⅰ产生Fe2+再通过快反应Ⅱ产生•OH,总反应速率由慢反应Ⅰ决 定,c(•OH)小于前者;故Fe O 作催化剂比Fe2O 作催化剂时NO脱除率更大 2NO +2OH-=NO 3 4 3 2 +NO +H O SO 几乎完全被NaOH溶液吸收 2 2 【详解】(1)①氢氧化钠溶液中会溶解有少量空气中的氧气,氧气能氧化亚铁离子生成铁离子,通入N 2 的目的是排除NaOH溶液中的O,防止Fe2+被氧化为Fe3+; 2 ②氢氧化钠和硫酸亚铁生成氢氧化亚铁沉淀,混合物X中含有氢氧化亚铁,根据质量守恒可知,氢氧化亚 铁会与NaNO 反应生成Fe O 和NH 、氢氧化钠、水,该反应的化学方程式为12Fe(OH) +NaNO 3 3 4 3 2 34Fe O+NH↑+NaOH+10HO; 3 4 3 2 (2)①由已知反应机理反应Ⅰ、反应Ⅱ可知:Fe O 催化剂表面同时存在Fe2+和Fe3+,Fe2+直接通过反应Ⅱ 3 4 快速产生•OH,c(•OH)更大:Fe O 催化剂表面仅存在Fe3+,Fe3+需先通过慢反应Ⅰ产生Fe2+再通过快反应 2 3 Ⅱ产生•OH,总反应速率由慢反应Ⅰ决定,c(•OH)小于前者;故Fe O 作催化剂比Fe2O 作催化剂时NO脱 3 4 3 除率更大 ②NO 被NaOH溶液吸收生成两种含氧酸钠盐,根据质量守恒可知为含氮元素的盐,二氧化氮中部分氮元 2 素化合价升高、部分氮元素化合价降低,反应得到亚硝酸盐和硝酸盐,该反应的离子方程式为2NO +2OH- 2 =NO +NO +H O 2 ③二氧化硫能溶于水会和氢氧化钠反应被吸收,测得SO 脱除率几乎均为100%的原因是SO 几乎完全被 2 2 NaOH溶液吸收。 4.(2022·湖北·模拟)氢气在实验室和工业上有着广泛的用途。请回答: (1)氢气可以与煤在催化剂作用下制备乙炔,已知部分反应如下: Ⅰ. Ⅱ. Ⅲ. Ⅳ. 通过计算说明反应Ⅳ自发进行的条件_______。 (2)利用氢气与二氧化碳催化反应合成乙烯,是实现低碳转型的一条途径。在0.1MPa、120℃条件下,以 的投料比充入体积固定的密闭容器中,发生反应: ,平衡时水蒸气的物质的量百分数为50.0%。请回答: ①反应的平衡常数表达式为_______。 ②达到平衡时, 的转化率为_______。 (3)氢气可合成氨气,氨气与二氧化碳可以合成尿素,反应为:,分为两步: 反应步骤 反应方程式 Ⅰ 快速放热 Ⅱ 慢速吸热 已知投料的组成为 、 和水蒸气(有助于分离尿素),一定条件下,氨基甲酸铵( )物质 的量与时间的关系图(图甲,t 后物质的量不再改变),以及不同氨碳比( )与水碳比( )投料时 1 平衡转化率图象(图乙,a、b代表水碳比): 回答下列问题: ①已知反应I又可以分成两步:_______、 ,请写出第一步的 化学方程式_______。 ②下列叙述正确的是_______。 A.反应Ⅰ的活化能大于反应Ⅱ, B.增大氨碳比有利于提高尿素产率,原因之一是过量氨气与反应Ⅱ生成的水反应,促进平衡正移 C.实际生产中若选择曲线a,则氨碳比应控制在4.0左右 D.曲线a的水碳比大于曲线b,减小水碳比有利于尿素生成 ③如果某催化剂可以同等程度地加速反应Ⅰ和Ⅱ,请在图甲中画出保持其他条件不变,加入该催化剂后从0h到t 时的氨基甲酸铵物质的量变化曲线_______。 1 【答案】(1) ,且反 应可逆符号右侧气体物质的量比左侧多,△S>0,故反应在高温下自发 (2) 或 68.2% (3) BC 【详解】(1)将反应Ⅰ的二倍加上反应Ⅱ,再加反应Ⅲ的2倍得到反应Ⅳ. ,且反 应可逆符号右侧气体物质的量比左侧多,△S>0,故反应在高温下自发;故答案为: ,且反 应可逆符号右侧气体物质的量比左侧多,△S>0,故反应在高温下自发。 (2)利用氢气与二氧化碳催化反应合成乙烯,是实现低碳转型的一条途径。在0.1MPa、120℃条件下,以 的投料比充入体积固定的密闭容器中,发生反应: ,平衡时水蒸气的物质的量百分数为50.0%。请回答: ①反应的平衡常数表达式为 或 ;故答案为:或 。 ②以 的投料比充入体积固定的密闭容器中,假设分解加入4mol氢气和1mol二氧化碳, 达到平衡时,建立三段式 , ,解得x= , 的转化率为 ;故答案为:68.2%。 (3)①根据总反应和第二步反应得到第一步反应为 ;故答案为: 。 ②A.反应Ⅰ是快速放热,反应Ⅱ是慢速吸热,说明反应Ⅰ的活化能小于反应Ⅱ,且 ,故A错 误;B.增大氨碳比有利于提高尿素产率,过量氨气与反应Ⅱ生成的水反应,促进平衡正移,会生成更多 的尿素,故B正确;C.实际生产中若选择曲线a,氨碳比在4.0时二氧化碳转化率已经很大,再提高氨碳 比,虽然二氧化碳转化率增大,但氨气经济价值比二氧化碳经济价值大,因此增大氨碳比不划算,因此氨 碳比应控制在4.0左右,故C正确;D.根据总反应增加水碳比,可以理解为二氧化碳量不变,水的量增 大,平衡逆向移动,二氧化碳转化率减小,因此根据图象得到曲线a的水碳比小于曲线b,减小水碳比, 水蒸气量减少,有利于平衡正向移动,利于尿素生成,故D错误;综上所述,答案为:BC。 ③如果某催化剂可以同等程度地加速反应Ⅰ和Ⅱ,反应速率加快,生成氨基甲酸铵达到最高值时间缩短, 短时间放出的热量大,使得温度较高,平衡正向移动,因此生成氨基甲酸铵的量比原来增加,因此加入该催化剂后从0h到t 时的氨基甲酸铵物质的量变化曲线 ;故答案 1 为: 。 5.(2022·河北·模拟)将CO 还原成甲烷,是实现CO 资源化利用的有效途径之一。 2 2 I.CO 甲烷化 2 CO 甲烷化过程可能发生反应: 2 ⅰ.CO(g) + 4H(g) CH(g) + 2HO(g) ΔH 2 2 4 2 1 ⅱ.CO(g) + H(g) CO(g) + HO(g) ΔH=+41.2 kJ∙mol−1 2 2 2 2 ⅲ.CO(g) + 3H g) CH(g) + HO(g) ΔH=-206.1 kJ∙mol−1 2( 4 2 3 …… (1)ΔH=______ kJ∙mol−1。 1 (2)不同条件下,按照n(CO):n(H )=1:4投料,CO 的平衡转化率如图所示。 2 2 2①压强p、p、p 由大到小的顺序是______。 1 2 3 ②压强为p 时,随着温度升高,CO 的平衡转化率先减小后增大。解释温度高于600℃之后,随着温度升 1 2 高CO 转化率增大的原因______。 2 Ⅱ.微生物电化学法 微生物电化学产甲烷法是将电化学法和生物还原法有机结合,装置如上图所示。 (3)阴极的电极反应式是______。 (4)若生成1 mol CH ,理论上阳极室生成CO 的体积是______L(标准状况,忽略气体的溶解)。 4 2 【答案】(1) −164.9 (2)p >p>p 3 2 1 CO 平衡转化率为反应ⅰ和反应ⅱ的CO 平衡转化率之和。反应ⅰ为放热反应,随温度升高CO 平衡转化 2 2 2 率降低,反应ⅱ为吸热反应,随温度升高CO 平衡转化率升高。温度较高时,CO 平衡转化率主要取决于 2 2 反应ⅱ。(或:ⅰ为放热反应;ⅱ为吸热反应。600℃之后,CO 转化率主要取决于反应ⅱ) CO + 8e− 2 2+ 8H+ = CH + 2HO 44.8 4 2 【详解】(1)将反应ⅱ加反应ⅲ得到反应ⅰ,因此ΔH=+41.2 kJ∙mol−1+(-206.1 kJ∙mol−1) = 1 −164.9kJ∙mol−1;故答案为:−164.9。 (2)①该反应是体积减小的反应,画一条与y轴相平的平行线,从下到上,转化率变大,说明平衡正向移 动,压强不断增大,因此压强p、p、p 由大到小的顺序是p>p>p;故答案为:p>p>p。 1 2 3 3 2 1 3 2 1 ②压强为p 时,随着温度升高,CO 的平衡转化率先减小后增大。解释温度高于600℃之后,随着温度升 1 2 高CO 转化率增大的原因CO 平衡转化率为反应ⅰ和反应ⅱ的CO 平衡转化率之和。反应ⅰ为放热反应, 2 2 2 随温度升高CO 平衡转化率降低,反应ⅱ为吸热反应,随温度升高CO 平衡转化率升高。温度较高时, 2 2 CO 平衡转化率主要取决于反应ⅱ。(或:ⅰ为放热反应;ⅱ为吸热反应。600℃之后,CO 转化率主要取决 2 2 于反应ⅱ);故答案为:CO 平衡转化率为反应ⅰ和反应ⅱ的CO 平衡转化率之和。反应ⅰ为放热反应,随 2 2 温度升高CO 平衡转化率降低,反应ⅱ为吸热反应,随温度升高CO 平衡转化率升高。温度较高时,CO 2 2 2 平衡转化率主要取决于反应ⅱ。(或:ⅰ为放热反应;ⅱ为吸热反应。600℃之后,CO 转化率主要取决于 2 反应ⅱ)。 (3)根据图中信息CO 化合价降低变为CH,在阴极发生反应,因此阴极的电极反应式是CO + 8e− + 8H 2 4 2 + = CH + 2HO;故答案为:CO + 8e− + 8H+ = CH + 2HO。 4 2 2 4 2 (4)根据CO + 8e− + 8H+ = CH + 2HO,若生成1 mol CH ,转移8mol电子,有根据CHCOO− - 2 4 2 4 3 8e−+ 2HO=2CO +7H+,因此理论上阳极室生成2molCO ,其体积是44.8L;故答案为:44.8。 2 2 2 1.(2022·浙江·模拟)氮元素在工业应用上具有重要地位。 请回答: (1)某实验兴趣小组对F.Daniels的NO 气体分解实验学习后,探究相关类似实验。在T℃下,将NO 气体 2 4 1 2 4 通入1 L容器内,容器内存在如下反应: 反应Ⅰ 主反应: K 1 反应Ⅱ 副反应: K 2 ①向该容器内通入4 mol N O 和2 mol NO ,等到反应Ⅰ、Ⅱ均达到平衡后,测得c(NO )=5 mol/L, 2 5 2 2 c(N O)=0.5 mol/L,,则此温度下NO 的转化率=_______。 2 4 2 5 ②通过控制条件,使该容器内只进行反应Ⅰ,下列说法正确的是_______。A.当4v ( N O 消耗)=2v(NO 消耗)时,该化学反应达到平衡 2 5 2 B.反应达到平衡时,缩小容器体积,平衡常数K 变小,NO 的转化率下降 1 2 5 C.恒压状态下,反应达到平衡时,通入大量稀有气体,NO 的转化率将提高 2 5 D.恒容状态下,通入NO、NO 、O 各5 mol,反应达到平衡后,c(O )<5 mol/L 2 5 2 2 2 (2)已知:反应Ⅲ 反应Ⅳ ①写出NO与H 反应生成NH 和O 的热化学方程式,判断该反应自发进行的条件并说明理由:_______。 2 3 2 ②反应Ⅲ为工业制氨的化学方程式。如图1为工业制氨反应中逆反应速率与时间(t)的关系图。已知t 时, 1 该反应恰好达到化学平衡。t 时,将该化学反应体系升温到T℃(t 时恰好达到化学平衡)。t 时,向该化学 1 2 2 反应体系加入正催化剂,用曲线画出t ~t 时间段中逆反应速率。_______。 1 3 ③关于反应Ⅳ,恒容状态下N 进气速度对O 的转化率影响如图2。请解释曲线中A点到B点变化的原 2 2 因:_______。 【答案】(1) 50% AC (2) 2NO(g)+3H (H ) 2NH (g)+O(g) △H=-272 kJ/mol;由联立得到的反应方程式可知△H<0,△S< 2 2 3 20,故反应自发进行的条件为低温 随着N 的进气速率持续不断增大,反应器内的气体流速增大,反应热能被及时移走,等效于降低温度;该 2 反应为吸热反应,降低温度则反应逆向移动,故O 转化速率会一定程度的降低 2 【详解】(1)①反应容器的容积是1 L,向该容器内通入4 mol N O 和2 mol NO ,则反应开始时 2 5 2 c(N O)=4 mol/L,c(NO )=2 mol/L。等到反应Ⅰ、Ⅱ均达到平衡后,c(N O)=0.5 mol/L,则反应消耗 2 5 2 2 4 △c(NO )=1 mol/L,测得此时c(NO )=5 mol/L,若未发生反应Ⅱ,则NO 的浓度应该为c(NO )=5 mol/L+1 2 2 2 4 2 mol/L=6 mol/L,因此发生反应Ⅰ产生的NO 的浓度为c(NO )=(6-2)mol/L=4 mol/L,根据反应Ⅰ中物质反应 2 4 2 转化关系可知反应消耗NO 的浓度△c(NO )=2 mol/L,故此温度下NO 的转化率= ; 2 5 2 2 5 ②A.对于反应Ⅰ,在任何时刻都存在4v (N O 消耗)=2v(NO 生成),若4v (N O 消耗)=2v(NO 消耗)时, 2 5 2 2 5 2 v(NO 生成)= v(NO 消耗),反应达到平衡状态,A符合题意; 2 2 B.反应达到平衡时,缩小容器体积,化学平衡向气体体积减小的逆反应方向移动,导致NO 的转化率下 2 5 降,但温度不变,因此化学平衡常数K 不变,B错误; 1 C.恒压状态下,反应达到平衡时,通入大量稀有气体,反应容器的容积扩大,导致体系的压强减小,化 学平衡向气体体积扩大的正反应方向移动,从而使NO 的转化率提高,C正确; 2 5 D.根据①计算可知:在容器的容积是1 L,开始向容器中加入4 mol N O 和2 mol NO ,反应达到平衡 2 5 2 时,NO 的转化率是50%,此时容器中c(N O)=2 mol/L,c(NO )=5 mol/L,c(O )=1 mol/L,反应Ⅰ的化学 2 5 2 5 2 2 平衡常数K= 。在恒容状态下,通入NO、NO 、O 各5 mol,此时浓度商 2 5 2 2 Q= <K,反应正向进行,至反应达到平衡后,c(O )>5 mol/L,D错误; c 2 故合理选项是AC; (2)①已知:反应Ⅲ反应Ⅳ 根据盖斯定律,将反应Ⅲ-反应Ⅳ,整理可得热化学方程式2NO(g)+3H (H ) 2NH (g)+O(g) △H=-272 2 2 3 2 kJ/mol; 要使反应自发进行,体系的自由能△G=△H-T△S<0,由联立得到的总反应方程式2NO(g)+3H (H ) 2 2 2NH (g)+O(g) △H=-272 kJ/mol可知△H<0,△S<0,故反应自发进行的条件为低温条件; 3 2 ②合成NH 的正反应是放热反应,在t 时刻最高温度,v 、v 都增大,由于温度对吸热反应影响更大,因 3 1 正 逆 此v 增大的倍数大于v ,化学平衡逆向移动,随着反应的进行,v 逐渐减小,v 逐渐增大,在t 时刻反 逆 正 逆 正 2 应达到平衡状态,此时v =v ;然后在t 时刻向该化学反应体系加入正催化剂,v 、v 都增大,且增大 正 逆 2 正 逆 有的速率关系为v =v ,用曲线画出t ~t 时间段中逆反应速率为: 正 逆 1 3 ; ③反应Ⅳ是反应前后气体体积不变的吸热反应,在开始后,随着N 通入速率的增大,N 投入量的增大, 2 2 c(N )增大使化学反应正向进行,导致O 的转化率增大,但当N 通入速率过大时,随着N 的进气速率持续 2 2 2 2 不断增大,反应器内的气体流速增大,反应热能被及时移走,等效于降低温度;该反应为吸热反应,降低 温度,会使化学平衡逆向移动,故O 转化速率会一定程度的降低。 2 2.(2022·四川绵阳·一模)我国的能源以煤炭为主,燃煤烟气中 等有害气体的排放会污染环 境,用CO还原脱除SO 将其转化为单质硫,对工业生产具有重要的意义。 2 (1)已知常温常压下, 的燃烧热为 ,CO(g)的燃烧热为 ,则CO还原脱除 : _______。 (2)在某温度时,进行CO还原脱除 : 。 ①若在刚性容器中进行,下列说法一定能确定反应达到平衡状态的是_______。A. B.CO与SO 的浓度之比不再改变 2 C.容器内的压强不再改变 D. 的值不再改变 ②若控制 进料比(物质的量)为4∶1,反应达平衡时,混合气体中 的体积分数为5%,则该反应在 此温度下的平衡常数为_______。 (3)在600℃时,发生如下系列反应,测得不同 进料比(物质的量)下平衡体系各物质分布如图所示 (图中 起始投料固定为 )。 反应I: 反应II: 反应III: ①该条件下,为减少有毒物质COS的产生,同时脱除 ,实际生产中应控制 进料比为_______, 在进料比大于2.5之后,COS的含量会明显增大,试分析原因_______。 ②根据图中曲线,可判断 _______ (填“>”“=”或“<”)。 (4)SO —空气质子交换膜燃料电池也可用于处理SO ,其原理如图。若用该电池处理标准状况下SO 含量为 2 2 2 20%的燃煤烟气3.36L,则理论上电路中转移电子数为_______。【答案】(1)-268.8kJ/mol (2) AD 1.08 (3) 2.0 ,CO的含量较多,此时反应II的反应程度比反应III的程度大的多 > (4)0.06N A 【详解】(1)根据题意得出 的热化学方程式为 +O (g) SO (g) △H=- ,CO(g)的热化 2 2 学方程式为CO(g)+ O(g)=CO (g) △H=- ,将两个方程式依次编号为①②,由2×②-①得 2 2 ,所以△H=2×(-283.0)-(-297.2)=-268.8 kJ/mol。 (2)①正向反应速率等于逆向反应速率,且速率之比等于系数之比,即 时,可以判定反应 达到平衡状态,A正确;CO与SO 的浓度之比不再改变不能判断反应达到平衡状态,跟反应得投料比和反 2 应程度有关,B错误;根据方程式可以看出,反应前后的系数之和相等,压强一直保持不变,因此容器内 的压强不再改变无法判定反应达到平衡状态,C错误;反应达到平衡状态时,各成分的浓度不再发生改 变, 的值不再改变,可以判定反应达到平衡状态,D正确; ②控制 进料比(物质的量)为4∶1,设起始投料n(CO)=4mol,n(SO )=1mol,平衡时SO 反应xmol,列出 2 2三段式: ,根据反应达平衡时,混合气体中 的体 积分数为5%,可得 =5%,解出:x=0.75,反应前后系数相同,体积不影响平衡常 数,则平衡常数K= =1.08。 (3)①当进料比为2时,图中n(CO)比较大,同时n(SO )很少,n(COS)几乎为0,故实际生产中应控制 2 2 进料比为2.0;在进料比大于2.5之后,CO的含量较多,此时反应II的反应程度比反应III的程度 大的多,故 COS的含量会明显增大; ②投料比为2.0时,反应I中的产物n(S)、n(CO)很大,而n(CO)、n(SO )很小,则K 较大,反应II中产 2 2 1 物:n(COS)很小,n(CO)、 n(S)中n(S)很大,则K 较小,所以K > K 2 1 2 (4)标准状况下SO 的物质的量为 =0.03mol,在电极a上SO 转化为HSO ,一个SO 2 2 2 4 2 失去2个电子,则0.03molSO 失去0.03×2=0.06mol电子即0.06N 。 2 A 3.(2022·四川雅安·模拟)为早日实现“碳达峰”、“碳中和”,我国科学家利用 作为催化剂,实 现了常温下 加氢制 ,主反应为 ,伴随发生副 反应 (1)已知 ,则 _______ 。 (2)在恒温恒容的密闭容器中,加入 和 ,同时发生主、副反应。体系中 的选择性 (指转化为 的 占发生反应的 的百分比)随温度、压强的变化曲线如图所示:① _______ 。 ② 的选择性随温度升高而降低的原因可能是_______。 ③下列说法正确的是_______。 A.增大压强,体系中副反应平衡逆向移动 B.体系中 不再变化,代表反应达到平衡 C.及时分离出 可以加快主反应的反应速率 D.更换合适的催化剂可提高 的选择性 ④某温度下,若容器体积为1L,40min后,2个反应均达到平衡,此时 , ,则 _______ ,主反应的平衡常数的计算式为_______,此时 的选择性为_______(保留3位有效数字)。 (3)我国某研究团队发现,当选用某种Cu作催化剂时,主反应的中间体为 。此时反应分为两步: 第一步: 第二步: 其中第一步的反应历程如下图所示(*表示吸附态,即该物种吸附在催化剂表面)历程①: 历程②:_______(写方程式); 历程③: 我国科学家发现利用太阳能驱动 转化也可以实现上述第一步反应,原理如图所示: a的电极反应式为_______,该装置能量转化的主要形式是_______。 【答案】(1)-52.7 (2) > 主反应为放热反应,副反应为吸热反应,升高温度,平衡向吸热方向移动,故温度升高时不利 于主反应、有利于副反应的发生,所以 的选择性降低 ABD 0.01 53.8% (3) (或 ) 电能和太阳能转化为化 学能 【详解】(1)已知② ③根据盖斯定律,由②+③得反应 ,则 -52.7 ; (2)主反应为气体体积缩小的反应,副反应为气体体积不变的反应,故压强越大,主反应正向移动, 的选择性越大,故可知 > ; ②主反应为放热反应,副反应为吸热反应,升高温度,平衡向吸热方向移动,故温度升高时不利于主反 应、有利于副反应的发生,所以 的选择性降低; ③A.增大压强,主反应 正向移动,CO 的浓度降低,副反应 2 逆向移动,选项A正确; B.根据主反应和副反应中CO 与H 的比例不同,可知 为变量,根据“变量不变达平衡”可知,体 2 2 系中 不再变化,代表反应达到平衡,选项B正确; C.及时分离出 ,则反应物浓度降低,反应速率减小,选项C错误; D.更换合适的催化剂可调整主副反应的比例,从而提高 的选择性,选项D正确; 答案选ABD; ④某温度下,若容器体积为1L,40min后,2个反应均达到平衡,此时 , ,根据三段式可知:则 =0.01 ,主反应的平衡常数的计算式为 = , 此时 的选择性为 ; (3)已知:第一步: ,历程①: ,历程③: , 由第一步-历程③-历程①得历程②: (或 ); A上的Cat得电子产生Cat-,电极反应式为 ,根据装置中的信息可知,该装置能量转化的主 要形式是电能和太阳能转化为化学能。 4.(2022·江西·赣州市赣县第三中学模拟)碳化学是以分子中只含一个碳原子的化合物为原料生产化工产 品的方法。合成气(CO和 的混合气体)是一碳化学的重要原料,焦炭与水蒸气在刚性密闭容器中会发生 如下两个反应: Ⅰ: Ⅱ: 下表是几种物质的标准生成热(由对应稳定单质生成1mol某种物质的焓变叫做该物质的标准生成热)。 物质 标准生成热 0.0 0.0(1)反应Ⅰ的焓变 _______ (2)若在绝热恒容容器中仅发生反应Ⅱ,则下列事实能说明反应达到平衡状态的是_______。A.容器内气体 的压强不变 B.容器内温度不变 C.容器内气体的密度不再改变 D.容器内气体的平均相对分子质量不变 (3)已知反应Ⅱ的正反应速率 ,逆反应速率 , 、 分 别为正、逆反应速率常数, (k表示 或 )与温度 的关系如图所示,其中直线a、b分别表示 、 随温度的变化。升高温度,反应Ⅱ的平衡常数K_______(填“变大”或“变小”或“不变”)。 (4)在上图A点对应的温度下,向某刚性密闭容器中加入足量焦炭和一定量水蒸气,同时发生反应Ⅰ和反应 Ⅱ,已知起始时容器内压强为80kPa,10分钟后体系达到平衡状态,容器内压强变为100kPa。 ①平衡时CO的分压 _______kPa,平衡时水蒸气的转化率为_______%。 ②进一步提高水蒸气平衡转化率的方法有_______、_______(写两种不同的方法)。 【答案】(1)+131.3 (2)AB (3)变小 (4) 8 40 增大容器体积 及时分离出 或 【解析】(1) 生成物标准生成热总和-反应物标准生成热总和=( )-( )=+131.3 ,故答案为:+131.3; (2)A.该反应中气体体积不变,气体总物质的量为定值,且在绝热条件下,结合PV=nRT可知,混合气 体的压强为变量,当容器内气体的压强不变,表明正逆反应速率相等,达到平衡状态,故A正确; B.在绝热容器内,容器内温度为变量,当容器内温度不变,表明正逆反应速率相等,达到平衡状态,故B正确; C.混合气体的质量是定值,容器容积不变,则混合气体的密度为定值,当容器内气体的密度不再改变 时,不能说明反应达到平衡状态,故C错误; D.混合气体的质量是定值,混合气体的物质的量不变,则平均相对分子质量不变为定值,当容器内气体 的平均相对分子质量不变时,不能说明反应达到平衡状态,故D错误; 故选AB; (3) (k表示 或 )与温度 的关系如图所示,其中直线a、b分别表示 、 随温度的变化,由图 可知,随着温度的升高 减小,正逆反应速率均增大,但升高相同温度时,lg 增加的更多,说明平衡逆 向移动,K值变小,故答案为:变小; (4)①已知起始时容器内压强为80kPa,10分钟后体系达到平衡状态,容器内压强变为100kPa,列化学 平衡三段式, 则x-y+80-x-y+y+x+y=100,解得x=20kPa,A点对应的温度下平衡时, = , = ,A点 = ,则 = ,则(20-y) (80-20-y)=y(20+y),解得y=12 kPa,平衡时CO的分压 ,平衡时水蒸气的转化率为 100%=40%,故答案为:8;40; ②反应Ⅰ为气体体积增大的反应,增大容器体积,平衡正向移动,可以提高水蒸气平衡转化率,或者及时分离出 或 ,也会促进平衡正向移动,提高水蒸气平衡转化率,故答案为:增大容器体积;及时分 离出 或 。 5.(2022·广东·东莞市东华高级中学模拟)含氮化合物(NO 、NO 等)是主要的污染物之一,消除含氮化 x 合物的污染倍受关注。 (1)下列过程属于氮的固定过程的是_______(填选项字母)。 A.工业合成氨 B.工业利用氨气合成硝酸 C.雷雨天中氮气与氧气生成氮氧化合物 D.通过碱性试剂将气态的氮氧化合物转化为固态含氮化合物 (2)已知反应2NO (g)+4CO(g)=N(g)+4CO (g) = -1169kJ·mol-1,该反应的逆反应活化能为akJ·mol-1,则 2 2 2 其正反应活化能为_______kJ·mol-1 (用含a的代数式表示)。 (3)某种含二价铜微粒 的催化剂可用于汽车尾气脱氮。催化机理如图1,反应历程如图2。 ①Cu的基态核外电子排布式为_______,基态Cu+比Cu2+稳定的原因是_______,从化学键的角度解释 能结合NH 的原因:_______。 3 ②该脱氮过程的总反应方程式为_______。该反应历程的决速步骤是_______。(填选项) a.状态①→状态② b.状态②→状态③ c.状态③→状态④ d.状态④→状态 ⑤ (4)实验室用NaOH溶液对氮氧化合物进行尾气吸收,例如NaOH溶液可将NO 转化为NaNO 和NaNO 。 2 3 2该吸收过程中发生反应的离子方程式为_______。 【答案】(1)AC (2)(a-1169) (3) 或 Cu+的价电子式为 ,为全充满状态,较稳定, Cu2+的价电子式为 ,较不稳定 NH 中的N有孤电子对, 中的CuII有空轨道能 3 接受孤电子对,形成配位键 4NO+4NH +O 4N+6H O c 3 2 2 2 (4)2NO +2OH- =NO +NO +H O 2 2 【解析】(1)A.工业合成氨,氮气和氢气反应生成氨气,氮元素由游离态变为化合态,属于氮的固定, 故选A; B.工业利用氨气合成硝酸,氮元素不是游离态变为化合态,不属于氮的固定,故不选B; C.雷雨天中氮气与氧气生成氮氧化合物,氮元素由游离态变为化合态,属于氮的固定,故选C; D.通过碱性试剂将气态的氮氧化合物转化为固态含氮化合物,氮元素不是游离态变为化合态,不属于氮 的固定,故不选D; 选AC。 (2)已知反应2NO (g)+4CO(g)=N(g)+4CO (g) = -1169kJ·mol-1,该反应的逆反应活化能为akJ·mol-1, 2 2 2 焓变=正反应活化能-逆反应活化能,则其正反应活化能为akJ·mol-1+(-1169kJ·mol-1)= (a-1169)kJ·mol-1。 (3)①Cu是29号元素,基态Cu原子核外电子排布式为 ;Cu+的价电子式为 , 为全充满状态,较稳定,Cu2+的价电子式为 ,较不稳定,属于基态Cu+比Cu2+稳定;NH 中的N有孤电 3 子对, 中的CuII有空轨道能接受孤电子对,形成配位键,所以 能结合 NH 。 3 ②根据图示,该脱氮过程中氨气和一氧化氮、氧气在催化剂作用下反应生成氮气和水,总反应方程式为4NO+4NH +O 4N+6H O。活化能越大,反应速率越慢,慢反应决定总反应速率,属于该反应历程 3 2 2 2 的决速步骤是状态③→状态④,选c。 (4)NaOH溶液将NO 转化为NaNO 和NaNO ,根据得失电子守恒,发生反应的离子方程式为 2 3 2 2NO +2OH- =NO +NO +H O。 2 2 11.(2022·吉林·长春十一高模拟)煤炭燃烧时产生大量SO 、NO对环境造成很大污染,将煤进行气化和 2 液化是减少污染的有效手段。 (1)煤的液化是现代能源工业中重点推广的能源综合利用方案,最常见的液化方法为用煤生产CHOH。已 3 知制备甲醇的有关化学反应及平衡常数如下: i:CO(g)+3H(g) CHOH(g)+H O(g) △H 2 2 3 2 1 ii:CO(g)+H(g) CO(g)+HO(g) △H=41.2kJ/mol 2 2 2 2 iii:CO(g)+2H(g) CHOH(g) △H=-132.0kJ/mol 2 3 3 850℃时,三个反应的平衡常数分别为K=160、K=243、K=160。 1 2 3 ①△H=____,该反应在____(填“高温”或“低温”)能自发进行。 1 ②850℃时,在密闭容器中进行反应i,开始时只加入CO、H,反应10min后测得各组分的浓度如表。比 2 2 较正、逆反应的速率的大小:v ____v (填“>”“<”或“=”)。 正 逆 物质 H CO CHOH HO 2 2 3 2 浓度/ 0.2 0.5 0.8 0.8 mol/L (2)在CO 利用的科研中,中科院天津工业生物所将H 与CO 反应合成甲醇,再由甲醇经若干酶促反应合 2 2 2 成淀粉,首次在实验室实现二氧化碳到淀粉的从头合成。该研究成果在碳中和、碳排放、温室效应、粮食 危机等方面有着重大意义。 回答下列问题: 保持温度T不变,在一刚性密闭容器中,充入一定量的CO 和H,同时发生反应i和ii,起始及达平衡 2 2 时,容器内各气体的物质的量如表所示。 CO H CHOH CO HO 2 2 3 2起始量/mol 4.0 8.0 0 0 0 平衡量/mol n 3.0 1 已知起始时总压强为1.5pkPa,平衡时体系总压强为pkPa,则表中n=____,反应i的平衡常数K=____。 1 p (含p的式子表示) (3)取物质的量浓度为amol•L-1的甲醇,选择不同的工程酶组块作为催化剂反应10h,测得实验数据如表所 示。 实验序号 温度/K 不同工程酶的组块 淀粉/(g•L-1) 1 T agp-M 0.21 1 1 2 T agp-M 0.38 1 2 3 T agp-M 1.82 2 2 4 T agp-M 1.24 2 3 ①根据表中数据选取最佳的反应条件____(填实验序号)。 ②已知温度升高,反应生成的淀粉量先增加后急剧减少,其可能原因是____。 ③实验4可用淀粉的质量浓度表示反应速率为____g•L-1•h-1。 【答案】(1) -90.8kJ/mo1 低温 = (2) 2.0 (3) 3 随温度升高,催化剂活性增强反应速率加快,生成的淀粉量增加;续升高温度,催化剂失活, 反应速率减慢,生成的淀粉量减少 0.124 【解析】(1)①由盖斯定律可知,ii+iii得到反应i,△H=(41.2kJ/mol)+( -132.0kJ/mol)= -90.8kJ/mol,反应 1 为放热的熵减反应,根据△H-T△S<0反应可自发进行,则该反应在低温能自发进行。 ②由图表可知,Q= = K ,反应达到平衡状态,则v =v ; 1 正 逆 (2)已知,充入二氧化碳、氢气的总量为12mol,起始时总压强为1.5pkPa,平衡时体系总压强为pkPa, 则根据阿伏伽德罗定律可知,反应后总的物质的量为 ,反应ii为气体分子数不变的 反应,减少的物质的量为12mol-8mol=4mol为反应i进行导致的,根据反应CO(g)+3H(g) CHOH(g) 2 2 3 +H O(g)可知气体系数变化∆n=2; 2则反应反应平衡时甲醇为n=2.0mol; 1 由图表可知,反应后水的物质的量为3.0mol,则: 则反应后二氧化碳、氢气、甲醇、水的物质的量分别为1.0mol、1.0mol、2.0mol、3.0mol;反应后总的物 质的量为8mol,则二氧化碳、氢气、甲醇、水的分压分别为0.125pkPa、0.125pkPa、0.25pkPa、 0.375pkPa,则K= ; p (3)①根据表中数据选取最佳的反应条件:3,此时淀粉的产率最高; ②随温度升高,催化剂活性增强反应速率加快,生成的淀粉量增加;继续升高温度,催化剂失活,反应速 率减慢,生成的淀粉量减少,故温度升高,反应生成的淀粉量先增加后急剧减少; ③实验4可用淀粉的质量浓度表示反应速率为1.24g•L-1÷10h=0.124g•L-1•h-1。 1.(2022·辽宁·高考真题)工业合成氨是人类科学技术的一项重大突破,目前已有三位科学家因其获得诺 贝尔奖,其反应为: 。回答下列问题: (1)合成氨反应在常温下_______(填“能”或“不能”)自发。 (2)_______温(填“高”或“低”,下同)有利于提高反应速率,_______温有利于提高平衡转化率,综合考 虑催化剂(铁触媒)活性等因素,工业常采用 。 针对反应速率与平衡产率的矛盾,我国科学家提出了两种解决方案。 (3)方案一:双温-双控-双催化剂。使用 双催化剂,通过光辐射产生温差(如体系温度为 时, 的温度为 ,而 的温度为 )。下列说法正确的是_______。 a.氨气在“冷Ti”表面生成,有利于提高氨的平衡产率 b. 在“热Fe”表面断裂,有利于提高合成氨反应速率 c.“热Fe”高于体系温度,有利于提高氨的平衡产率 d.“冷Ti”低于体系温度,有利于提高合成氨反应速率 (4)方案二: 复合催化剂。 下列说法正确的是_______。 a. 时,复合催化剂比单一催化剂效率更高 b.同温同压下,复合催化剂有利于提高氨的平衡产率 c.温度越高,复合催化剂活性一定越高 (5)某合成氨速率方程为: ,根据表中数据, _______; 实验1 m n p q 2 2m n p 2q 3 m n 0.1p 10q 4 m 2n p 2.828q 在合成氨过程中,需要不断分离出氨的原因为_______。 a.有利于平衡正向移动 b.防止催化剂中毒 c.提高正反应速率 (6)某种新型储氢材料的晶胞如图,八面体中心为M金属离子,顶点均为 配体;四面体中心为硼原 子,顶点均为氢原子。若其摩尔质量为 ,则M元素为_______(填元素符号);在该化合物中,M 离子的价电子排布式为_______。 【答案】(1)能 (2) 高 低 (3)ab (4)a (5) -1 a (6) Fe 3d6 【详解】(1) ,则∆G=∆H- T∆S=(-92.4+0.2×273) kJ∙mol-1=-37.8 kJ∙mol-1<0,所以合成氨反应在常温下能自发进行。答案为:能; (2)温度越高,反应速率越快,所以高温有利于提高反应速率;因为正反应为放热反应,所以低温有利 于提高平衡转化率。答案为:高;低; (3)a.因为正反应为放热反应,所以低温有利于平衡正向移动,氨气在“冷Ti”表面生成,有利于提高 氨的平衡产率,a正确; b.温度升高,反应速率加快,所以 在“热Fe”表面断裂,有利于提高合成氨反应速率,b正确; c.合成氨反应的正反应为放热反应,“热Fe”高于体系温度,不利于提高氨的平衡产率,c不正确;d.温度升高,可提高合成氨反应的速率,所以“冷Ti”低于体系温度,不利于提高合成氨反应速率,d不 正确; 故选ab。答案为:ab; (4)a.从图中可以看出, 时,复合催化剂比单一催化剂的反应速率快,催化效率更高,a正确; b.催化剂只能改变反应速率,不能改变平衡产率,所以同温同压下,复合催化剂不能提高氨的平衡产 率,b不正确; c.虽然图中显示温度高反应速率快,但温度高到一定程度后,复合催化剂活性就可能不变或变低,c不正 确; 故选a。答案为:a; (5)选择实验1和3进行分析,此时 ,则γ=-1; a.在合成氨过程中,需要不断分离出氨,有利于平衡正向移动,a正确; b.氨是在该催化剂的催化作用下生成,不会使催化剂中毒,b不正确; c.分离出氨,并没有增大反应物的浓度,所以不会提高正反应速率,c不正确; 故选a。答案为:-1;a; (6)从图中信息可以进行以下计算:含黑球的数目为 =4,含白球的数目为8,则黑球与白球的 个数比为1:2。黑球的化学式为 ,白球的化学式为 。从而得出M+17×6+15×2=188, M=56,则M元素为Fe;在该化合物中,Fe2+的价电子排布式为3d6。答案为:Fe;3d6。 2.(2022·江苏·高考真题)氢气是一种清洁能源,绿色环保制氢技术研究具有重要意义。 (1)“ 热电循环制氢”经过溶解、电解、热水解和热分解4个步骤,其过程如图所示。 ①电解在质子交换膜电解池中进行。阳极区为酸性 溶液,阴极区为盐酸,电解过程中 转化为。电解时阳极发生的主要电极反应为_______(用电极反应式表示)。 ②电解后,经热水解和热分解的物质可循环使用。在热水解和热分解过程中,发生化合价变化的元素有 _______(填元素符号)。 (2)“ 热循环制氢和甲酸”的原理为:在密闭容器中,铁粉与吸收 制得的 溶液反 应,生成 、 和 ; 再经生物柴油副产品转化为Fe。 ①实验中发现,在 时,密闭容器中 溶液与铁粉反应,反应初期有 生成并放出 ,该 反应的离子方程式为_______。 ②随着反应进行, 迅速转化为活性 ,活性 是 转化为 的催化剂,其可能 反应机理如图所示。根据元素电负性的变化规律。如图所示的反应步骤Ⅰ可描述为_______。 ③在其他条件相同时,测得Fe的转化率、 的产率随 变化如题图所示。 的产率随 增加而增大的可能原因是_______。(3)从物质转化与资源综合利用角度分析,“ 热循环制氢和甲酸”的优点是_______。 【答案】(1) Cu、O (2) 吸附在催化剂的Fe2+上的H与 中碳原子作用,吸附在 O2-的H与 中的羟基氧作用生成的HO和 均吸附在上Fe2+ 随 增加,催化剂的量增 2 多,增大了接触面积, H 的产量增大, 的产率增大 2 (3)制得H,CO 转化为甲酸,生物柴油副产品的利用 2 2 【详解】(1)①电解在质子交换膜电解池中进行,H+可自由通过,阳极区为酸性 溶液,电解过程中 转化为 ,电解时阳极发生的主要电极反应为: ; ②电解后,经热水解得到的HCl和热分解得到的CuCl等物质可循环使用,从图中可知,热分解产物还有 O,从详解①中得知,进入热水解的物质有 ,故发生化合价变化的元素有Cu、O。 2 (2)①在 时,密闭容器中 溶液与铁粉反应,反应初期有 生成并放出 ,离子方程 式为: ; ②H的电负性大于Fe,小于O,在活性 表面,部分H吸附在催化剂的亚铁离子上,略带负电;另一部分H吸附在催化剂的氧离子上,略带正电;前者与 中略带正电的碳结合,后者与 中略带负 电的羟基氧结合生成HO, 转化为 ;故答案为:吸附在催化剂的Fe2+上的H与 中碳原 2 子作用,吸附在O2-的H与 中的羟基氧作用生成的HO和 均吸附在上Fe2+; 2 ③在其他条件相同时,随 增加,其与铁粉反应加快,从图中得知Fe的转化率也增大,即生成 和H 的速率更快,量更大,则得到活性 的速度更快,量也更多,生成 的速率更快, 2 产率也更大。故答案为:随 增加,催化剂的量增多,增大了接触面积, H 的产量增大, 2 的产率增大; (3)“ 热循环制氢和甲酸”系统将 转化为 和生成H 的速率快,原子利用率 2 高,不产生污染物,Fe初期生成 后迅速转化为活性 , 氧化为 再经生物柴油副产 品转化为Fe,得到循环利用,故该原理的优点是:制得H,CO 转化为甲酸,生物柴油副产品的利用。 2 2 13.(2022·海南·高考真题)某空间站的生命保障系统功能之一是实现氧循环,其中涉及反应: 回答问题: (1)已知:电解液态水制备 ,电解反应的 。由此计算 的燃烧热(焓) _______ 。 (2)已知: 的平衡常数(K)与反应温度(t)之间的关系如图1所示。①若反应为基元反应,且反应的 与活化能(Ea)的关系为 。补充完成该反应过程的能量变化示意 图(图2)_______。 ②某研究小组模拟该反应,温度t下,向容积为10L的抽空的密闭容器中通入 和 ,反 应平衡后测得容器中 。则 的转化率为_______,反应温度t约为_______℃。 (3)在相同条件下, 与 还会发生不利于氧循环的副反应: ,在反应器中按 通入反应物,在不同温度、不同催化剂条件下,反应进行到2min时,测得反应器中 、 浓度( )如下表所示。 t=350℃ t=400℃ 催化剂 催化剂 10.8 12722 345.2 42780 Ⅰ 催化剂 9.2 10775 34 38932 Ⅱ 在选择使用催化剂Ⅰ和350℃条件下反应, 生成 的平均反应速率为_______ ;若某空间站的生命保障系统实际选择使用催化剂Ⅱ和400℃的反应条件,原因是_______。 【答案】(1)-286 (2) 50%或0.5 660.2(或660.1或660.3,其他答案酌情给 分) (3) 5.4 相同催化剂,400℃的反应速率更快,相同温度,催化剂Ⅱ副产物浓度低,甲烷与甲醇比例高 【详解】(1)电解液态水制备 ,电解反应的 ,由此可以判断,2mol 完 全燃烧消耗 ,生成液态水的同时放出的热量为572kJ ,故1mol 完全燃烧生成液态水放出 的热量为286kJ,因此, 的燃烧热(焓) -286 。 (2)①由 的平衡常数(K)与反应温度(t)之间的关系图可知,K随着温度升高而减小,故该反应为放热反应。若反应为基元反应,则反应为一步完成,由于反应的 与活 化能(Ea)的关系为 ,由图2信息可知 =a ,则 a ,该反应为放热反应, 生成物的总能量小于反应物的,因此该反应过程的能量变化示意图为: 。 ②温度t下,向容积为10L的抽空的密闭容器中通入 和 ,反应平衡后测得容器中 ,则 的转化率为 ,根据C元素守恒可知, 的平衡量为 , 和 是按化学计量数之比投料的,则 的平衡量为 , 的平衡量是 的2倍,则 , 的平衡浓度分别为 、 、 、 ,则该反应的平衡常数K= ,根据图1中的信息可知,反应 温度t约为660.2℃。 (3)在选择使用催化剂Ⅰ和350℃条件下反应,由表中信息可知, 的浓度由0增加到10.8 ,因此, 生成 的平均反应速率为 ;由表中信 息可知,在选择使用催化剂Ⅰ和350℃条件下反应, 的浓度由0增加到10.8 ,, : =12722:10.8 1178;在选择使用催化剂Ⅱ和350℃的反应条件下, 的浓度由0增加到9.2 , : =10775:9.2 1171;在选择使用催化剂Ⅰ和 400℃条件下反应, 的浓度由0增加到345.2 , : =42780:345.2 124;在选择使用催化剂Ⅱ和400℃的反应条件下, 的浓度由0增加到34 , : =38932:34 1145。因此,若某空间站的生命保障系统实际选择使用催化剂Ⅱ和400℃ 的反应条件的原因是:相同催化剂,400℃的反应速率更快,相同温度,催化剂Ⅱ副产物浓度低,甲烷与 甲醇比例高。 4.(2022·河北·高考真题)氢能是极具发展潜力的清洁能源,以氢燃料为代表的燃料电池有良好的应用前 景。 (1) 时, 燃烧生成 )放热 , 蒸发吸热 ,表示 燃烧热的热化学方程 式为_______。 (2)工业上常用甲烷水蒸气重整制备氢气,体系中发生如下反应。 Ⅰ. Ⅱ. ①下列操作中,能提高 平衡转化率的是_______ (填标号)。 A.增加 用量 B.恒温恒压下通入惰性气体 C.移除 D.加入催化剂②恒温恒压条件下, 和 反应达平衡时, 的转化率为 , 的物质的量 为 ,则反应Ⅰ的平衡常数 _______ (写出含有a、b的计算式;对于反应 , ,x为物质的量分数)。其他条件不变, 起始量 增加到 ,达平衡时, ,平衡体系中 的物质的量分数为_______(结果保留两位有效 数字)。 (3)氢氧燃料电池中氢气在_______(填“正”或“负”)极发生反应。 (4)在允许 自由迁移的固体电解质燃料电池中, 放电的电极反应式为_______。 (5)甲醇燃料电池中,吸附在催化剂表面的甲醇分子逐步脱氢得到CO,四步可能脱氢产物及其相对能量如 图,则最可行途径为a→_______(用 等代号表示)。 【答案】(1)H (g)+ O (g)=HO(1) H= -286 kJ•mol-1 2 2 2 (2) BC 43% (3)负 (4)C H -(6n+2)e-+ (3n+1) O2-=n CO+(n+1) HO n 2n+2 2 2(5)a b e h j 【详解】(1)298K时,1gH 燃烧生成HO(g)放热121 kJ,则1molH 燃烧生成HO(g)放热 =242kJ, 2 2 2 2 用热化学方程式表示为:H(g)+ O(g)=HO(g) H= -242 kJ•mol-1①,又因为1 mol H O(1)蒸发吸热 2 2 2 1 2 44kJ,则HO(g)= H O(l) H= -44 kJ•mol-1②,根据盖斯定律可知,表示H 燃烧热的反应热为 H= H+ 2 2 2 2 1 H= -286 kJ•mol-1,故答案为:H(g)+ O (g)=HO(1) H= -286 kJ•mol-1; 2 2 2 2 (2)①A.增加CH (g)用量可以提高HO(g)的转化率,但是CH(g)平衡转化率减小,A不符合题意; 4 2 4 B.恒温恒压下通入惰性气体,相当于减小体系压强,反应混合物中各组分的浓度减小,反应Ⅰ的化学平 衡正向移动,能提高CH(g)平衡转化率,B符合题意; 4 C.移除CO(g),减小了反应混合物中CO(g)的浓度,反应Ⅰ的化学平衡正向移动,能提高CH(g)平衡转化 4 率,C符合题意; D.加入催化剂不能改变平衡状态,故不能提高CH(g)平衡转化率,D不符合题意; 4 综上所述,上述操作中,能提高CH(g)平衡转化率的是BC; 4 ②恒温恒压条件下,1 mol CH (g)和1 mol H O(g)反应达平衡时,CH (g)的转化率为α,CO (g)的物质的 4 2 4 2 量为b mol,则转化的CH (g)为α mol,剩余的CH (g)为(1-α)mol,根据C元素守恒可知,CO(g)的物质的 4 4 量为(α-b)mol,根据H和O守恒可知,HO(g)的物质的量为(1-α-b)mol,H(g)的物质的量为(3α+b)mol,则 2 2 反应混合物的总物质的量为(2α+2)mol,平衡混合物中,CH(g)、HO(g)、 CO(g) 、H(g)的物质的量分数 4 2 2 分别为 、 、 、 ,因此,反应I的平衡常数K= x ;其他条件不变,HO(g)起始量增加到5mol,达平衡时, 2 α=0.90,b =0.65,则平衡时,CH (g)为0.1mol,根据C元素守恒可知,CO(g)的物质的量为0.25mol,,根 4 据H和O守恒可知,HO(g)的物质的量为(5-0.90-0.65 )mol=3.45mol,H(g)的物质的量为 2 2 (3α+b )mol=3.35mol,平衡混合物的总物质的量为(2α+6 )mol=7.8mol,平衡体系中H(g)的物质的量分数为 2 ;(3)燃料电池中的燃料在负极发生氧化反应,因此,氢氧燃料电池中氢气在负极发生反应; (4)在允许O2-自由迁移的固体电解质燃料电池中,C H 在负极发生氧化反应生成CO 和HO,电极反 n 2n+2 2 2 应式为C H -(6n+2)e-+ (3n+1) O2-=nCO +(n+1) HO; n 2n+2 2 2 (5)由图示可知,吸附在催化剂表面的甲醇分子逐步脱氢得到CO,且能垒越低,活化能越小,越容易进 行,根据图示可知,其可行的途径为:a b e h j。 5.(2022·广东·高考真题)铬及其化合物在催化、金属防腐等方面具有重要应用。 (1)催化剂 可由 加热分解制备,反应同时生成无污染气体。 ①完成化学方程式: _______ _______。 ② 催化丙烷脱氢过程中,部分反应历程如图, 过程的焓变为_______(列式表示)。 ③ 可用于 的催化氧化。设计从 出发经过3步反应制备 的路线_______(用“→”表示含 氮物质间的转化);其中一个有颜色变化的反应的化学方程式为_______。 (2) 溶液中存在多个平衡。本题条件下仅需考虑如下平衡: (ⅰ) (ⅱ) ①下列有关 溶液的说法正确的有_______。 A.加入少量硫酸,溶液的pH不变 B.加入少量水稀释,溶液中离子总数增加C.加入少量 溶液,反应(ⅰ)的平衡逆向移动 D.加入少量 固体,平衡时 与 的比值保持不变 ②25℃时, 溶液中 随pH的变化关系如图。当 时,设 、 与 的平衡浓度分别为x、y、 ,则x、y、z之间的关系式为_______ ;计算溶液 中 的平衡浓度_____(写出计算过程,结果保留两位有效数字)。 ③在稀溶液中,一种物质对光的吸收程度(A)与其所吸收光的波长( )有关;在一定波长范围内,最大A对 应的波长( )取决于物质的结构特征;浓度越高,A越大。混合溶液在某一波长的A是各组分吸收程度 之和。为研究对反应(ⅰ)和(ⅱ)平衡的影响,配制浓度相同、 不同的 稀溶液,测得其A随 的 变化曲线如图,波长 、 和 中,与 的 最接近的是_______;溶液 从a变到b的过程中, 的值_______(填“增大”“减小”或“不变”)。【答案】(1) N↑ 4HO (E-E)+ΔH+(E-E) 2 2 1 2 3 4 2NO+O =2NO 2 2 (2) BD 当溶液pH=9时, ,因此可忽略溶液中 即 =0.20 反应(ii)的平衡常数K = = =3.3×10-7 2 联立两个方程可得 =6.0×10-4mol/L λ 增大 3 【解析】(1)① 分解过程中,生成Cr O 和无污染气体,根据元素守恒可知,其余生成物为 2 3 N、HO,根据原子守恒可知反应方程式为 ,故答案为:N↑;4HO。 2 2 2 2 ②设反应过程中第一步的产物为M,第二步的产物为N,则X→M ΔH=(E-E),M→N ΔH=ΔH,N→Y 1 1 2 2 ΔH=(E-E),根据盖斯定律可知,X(g)→Y(g)的焓变为ΔH+ΔH+ΔH=(E-E)+ΔH+(E-E),故答案为: 3 3 4 1 1 2 3 1 2 3 4 (E-E)+ΔH+(E-E)。 1 2 3 4 ③NH 在Cr O 作催化剂条件下,能与O 反应生成NO,NO与O 反应生成红棕色气体NO ,NO 与HO反 3 2 3 2 2 2 2 2 应生成HNO 和NO,若同时通入O,可将氮元素全部氧化为HNO,因此从NH 出发经过3步反应制备 3 2 3 3 HNO 的路线为 ;其中NO反应生成NO 过程中,气体颜色发生 3 2变化,其反应方程式为2NO+O =2NO,故答案为: ; 2 2 2NO+O =2NO。 2 2 (2)①KCr O 溶液中存在平衡:(i) 、(ii) 2 2 7 。 A.向溶液中加入少量硫酸,溶液中c(H+)增大,(ii)平衡逆向移动,根据勒夏特列原理可知,平衡移动只是 减弱改变量,平衡后,溶液中c(H+)依然增大,因此溶液的pH将减小,故A错误; B.加水稀释过程中,根据“越稀越水解”、“越稀越电离”可知,(i)和(ii)的平衡都正向移动,两个平衡 正向都是离子数增大的反应,因此稀释后,溶液中离子总数将增大,故B正确; C.加入少量NaOH溶液,(ii)正向移动,溶液中 将减小,(i)将正向移动,故C错误; D.平衡(i)的平衡常数K = ,平衡常数只与温度和反应本身有关,因此加入少量KCr O 溶液, 1 2 2 7 不变,故D正确; 综上所述,答案为:BD。 ②0.10mol/L K Cr O 溶液中,Cr原子的总浓度为0.20mol/L,当溶液pH=9.00时,溶液中Cr原子总浓度为 2 2 7 =0.20mol/L, 、 与 的平衡浓度分别为x、y、z mol/L,因此 =0.10;由图8可知,当溶液pH=9时, ,因此可忽略溶液中 ,即 =0.20,反应(ii)的平衡常数K = = =3.3×10-7,联 2 立两个方程可得 =6.0×10-4mol/L。③根据反应(i)、(ii)是离子浓度增大的平衡可知,溶液pH越大,溶液中 越 大,混合溶液在某一波长的A越大,溶液的pH越大,溶液中 越大,因此与 的λ 最接近的 max 是λ;反应(i)的平衡常数K = ,反应(ii)的平衡常数K = , = 3 1 2 = ,因此 = ,由上述分 析逆推可知,b>a,即溶液pH从a变到b的过程中,溶液中c(H+)减小,所以 的值将增 大,故答案为:λ;增大。 3 6.(2022·湖南·高考真题)2021年我国制氢量位居世界第一,煤的气化是一种重要的制氢途径。回答下列 问题: (1)在一定温度下,向体积固定的密闭容器中加入足量的 和 ,起始压强为 时,发生 下列反应生成水煤气: Ⅰ. Ⅱ. ①下列说法正确的是_______; A.平衡时向容器中充入惰性气体,反应Ⅰ的平衡逆向移动 B.混合气体的密度保持不变时,说明反应体系已达到平衡 C.平衡时 的体积分数可能大于 D.将炭块粉碎,可加快反应速率 ②反应平衡时, 的转化率为 ,CO的物质的量为 。此时,整个体系_______(填“吸收”或“放出”)热量_______kJ,反应Ⅰ的平衡常数 _______(以分压表示,分压=总压×物质的量分数)。 (2)一种脱除和利用水煤气中 方法的示意图如下: ①某温度下,吸收塔中 溶液吸收一定量的 后, ,则该溶液的 _______(该温度下 的 ); ②再生塔中产生 的离子方程式为_______; ③利用电化学原理,将 电催化还原为 ,阴极反应式为_______。 【答案】(1) BD 吸收 31.2 (2) 10 2 CO↑+ +H O 2CO+12e-+12H+=C H+4H O、AgCl+e-=Ag+Cl- 2 2 2 2 4 2 【解析】(1)①A.在恒温恒容条件下,平衡时向容器中充入情性气体不能改变反应混合物的浓度,因 此反应Ⅰ的平衡不移动,A说法不正确; B.在反应中有固体C转化为气体,气体的质量增加,而容器的体积不变,因此气体的密度在反应过程中 不断增大,当混合气体的密度保持不变时,说明反应体系已达到平衡,B说法正确; C.若C(s)和HO(g)完全反应全部转化为CO(g)和H(g),由C(s)+ 2H O(g) = CO (g)+ 2H (g)可知,H 的体 2 2 2 2 2 2 2 积分数的极值为 ,由于可逆反应只有一定的限度,反应物不可能全部转化为生成物,因此,平衡时H 的 2 体积分数不可能大于 ,C说法不正确; D.将炭块粉碎可以增大其与HO(g)的接触面积,因此可加快反应速率,D说法正确; 2综上所述,相关说法正确的是BD。 ②反应平衡时,HO(g)的转化率为50%,则水的变化量为0.5mol,水的平衡量也是0.5mol,由于CO的物 2 质的量为0.1mol,则根据O原子守恒可知CO 的物质的量为0.2mol,生成0.2mol CO 时消耗了0.2mol 2 2 CO,故在反应Ⅰ实际生成了0.3molCO。根据相关反应的热化学方程式可知,生成0.3mol CO要吸收热量 39.42kJ ,生成0.2mol CO 要放出热量8.22kJ此时,因此整个体系吸收热量39.42kJ-8.22kJ=31.2kJ;由H原 2 子守恒可知,平衡时H 的物质的量为0.5mol,CO的物质的量为0.1mol,CO 的物质的量为0.2mol,水的 2 2 物质的量为0.5mol,则平衡时气体的总物质的量为0.5mol+0.1mol+0.2mol+0.5mol=1.3mol,在同温同体积 条件下,气体的总压之比等于气体的总物质的量之比,则平衡体系的总压为0.2MPa 1.3=0.26MPa,反应I (C(s)+HO(g) CO(g)+H(g))的平衡常数K = 。 2 2 p (2)①某温度下,吸收塔中KCO 溶液吸收一定量的CO 后,c( ):c( )=1:2,由 2 3 2 可知, = ,则该溶液的 pH=10; ②再生塔中KHCO 受热分解生成KCO、HO和CO,该反应的离子方程式为2 CO↑+ 3 2 3 2 2 2 +H O; 2 ③利用电化学原理,将CO 电催化还原为C H,阴极上发生还原反应,阳极上水放电生成氧气和H+, 2 2 4 H+通过质子交换膜迁移到阴极区参与反应生成乙烯,铂电极和Ag/AgCl电极均为阴极,在电解过程中 AgCl可以转化为Ag,则阴极的电极反应式为2CO+12e-+12H+=C H+4H O、AgCl+e-=Ag+Cl-。 2 2 4 2