文档内容
专题十二 化学反应原理
必备知识 解读
1
必备知识 化学能、热焓
1.盖斯定律的应用和书写热化学方程式
(1).盖斯定律
① 概念:不管化学反应是一步完成,还是分几步完成,其反应热是相同的。即反应热只与反
应体系的始态和终态有关,而与反应途径无关。
② (2)应用:间接计算某些反应的反应热。如: ,则ΔH=ΔH+ΔH。
1 2
(2).利用盖斯定律计算反应热
运用盖斯定律的技巧——“三调一加”
一调:根据目标热化学方程式,调整已知热化学方程式中反应物和生成物的左右位置,改写已
知的热化学方程式。
二调:根据改写的热化学方程式调整相应ΔH的符号。
三调:调整中间物质的化学计量数。
一加:将调整好的热化学方程式及其ΔH相加。
运用盖斯定律的三个注意事项
a.热化学方程式乘以某一个数时,反应热的数值必须也乘上该数。
b.热化学方程式相加减时,物质之间相加减,反应热也必须相加减。
c.将一个热化学方程式颠倒时,ΔH的“+”“-”随之改变,但数值不变。
(2)热化学方程式及其书写
热化学方程式不仅表明了化学反应中的物质变化,也表明了化学反应中的能量变化,系数代
表物质的量。
书写如:(2019年全国统一高考化学试卷(新课标Ⅲ))近年来,随着聚酯工业的快速发展,
氯气的需求量和氯化氢的产出量也随之迅速增长。因此,将氯化氢转化为氯气的技术
成为科学研究的热点。回答下列问题:
(2)Deacon直接氧化法可按下列催化过程进行:
CuCl(s)═CuCl(s)+ Cl(g)△H=83kJ•mol﹣1
2 2 1
CuCl(s)+ O(g)═CuO(s)+ Cl(g)△H=﹣20kJ•mol﹣1
2 2 2
CuO(s)+2HCl(g)═CuCl(s)+HO(g)△H=﹣121kJ•mol﹣1
2 2 3
则4HCl(g)+O(g)═2Cl(g)+2HO(g)的△H= kJ•mol﹣1。
2 2 2
【答案】﹣116
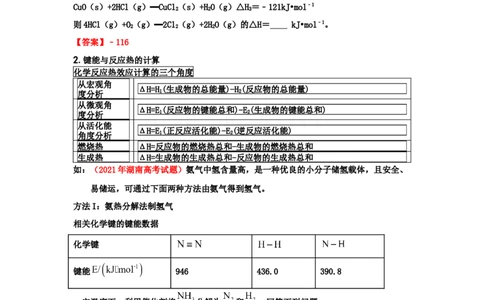
2.键能与反应热的计算
化学反应热效应计算的三个角度
从宏观角
ΔH=H(生成物的总能量)-H(反应物的总能量)
度分析 1 2
从微观角
ΔH=E(反应物的键能总和)-E(生成物的键能总和)
度分析 1 2
从活化能
ΔH=E(正反应活化能)-E(逆反应活化能)
角度分析 1 2
燃烧热 ΔH=反应物的燃烧热总和-生成物的燃烧热总和
生成热 ΔH=生成物的生成热总和-反应物的生成热总和
如:(2021年湖南高考试题)氨气中氢含量高,是一种优良的小分子储氢载体,且安全、
易储运,可通过下面两种方法由氨气得到氢气。
方法I:氨热分解法制氢气
相关化学键的键能数据
化学键
键能 946 436.0 390.8
一定温度下,利用催化剂将 分解为 和 。回答下列问题:
(1)反应 _______ ;
【答案】+90.8
2
必备知识 化学反应速率
一.概念与表示
1.概念:化学反应速率是用来衡量化学反应进行快慢程度的物理量。2.表示:通常用单位时间内反应物浓度的减少或生成物浓度的增加来表示。
3.表达式:v=。
4.单位:一般为mol·L-1·s-1、mol·L-1·min-1。
二.与化学方程式中各物质化学计量数的关系
某一反应中,以各物质表示的化学反应速率之比等于化学方程式中相应物质的化学计量数
之比。
如对于反应:mA(g)+nB(g) pC(g)+qD(g);则有v(A)∶v(B)∶v(C)∶v(D)=
m ∶ n ∶ p ∶ q 或v(A)=v(B)=v(C)=v(D)。
3
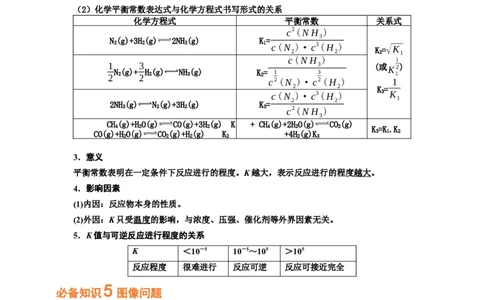
必备知识 化学平衡的移动和影响因素
1.平衡原理(勒夏特列原理)的应用
如果改变影响化学平衡的条件(浓度、压强、温度等)之一,平衡将向着减弱这种改变的方
向移动。
[注意] “减弱”不等于“消除”,更不是“扭转”,即平衡移动不能将外界影响完全消
除,而只能减弱。
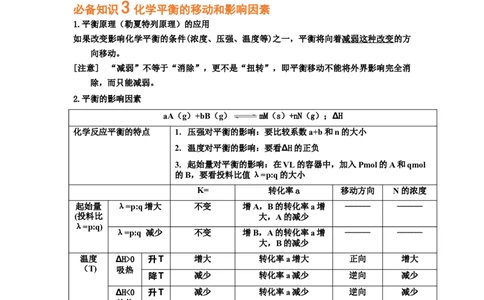
2.平衡的影响因素
aA(g)+bB(g) mM(s)+nN(g);∆H
化学反应平衡的特点 1. 压强对平衡的影响:要比较系数a+b和n的大小
2. 温度对平衡的影响:要看∆H的正负
3. 起始量对平衡的影响:在VL的容器中,加入Pmol的A和qmol
的B,要看投料比值λ=p:q的大小
K= 转化率a 移动方向 N的浓度
起始量 λ=p:q增大 不变 增A,B的转化率a增 ——— ———
(投料比 大,A的减少
λ=p:q)
λ=p:q 减少 不变 增B,A的转化率a增 ——— ———
大,B的减少
温度 ∆H>0 升T 增大 转化率a增大 正向 增大
(T) 吸热
降T 减少 转化率a减少 逆向 减少
∆H<0 升T 减少 转化率a减少 逆向 减少
放热
降T 增大 转化率a增大 正向 增大
压强(P) a+b=n 加 不变 不变 不变 增大
不变 P、
减P 不变 不变 不变 减少
a+b>n 加P 不变 转化率a增大 正向 增大
减少
减P 转化率a减少 逆向 减少
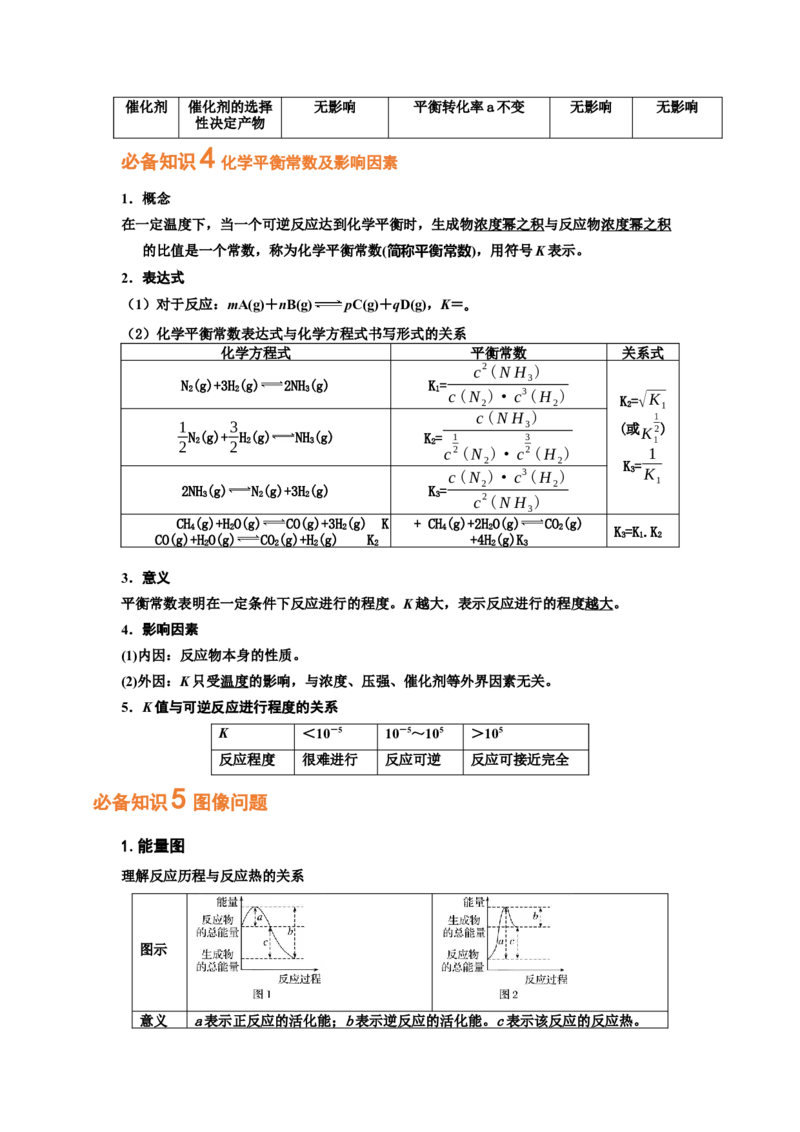
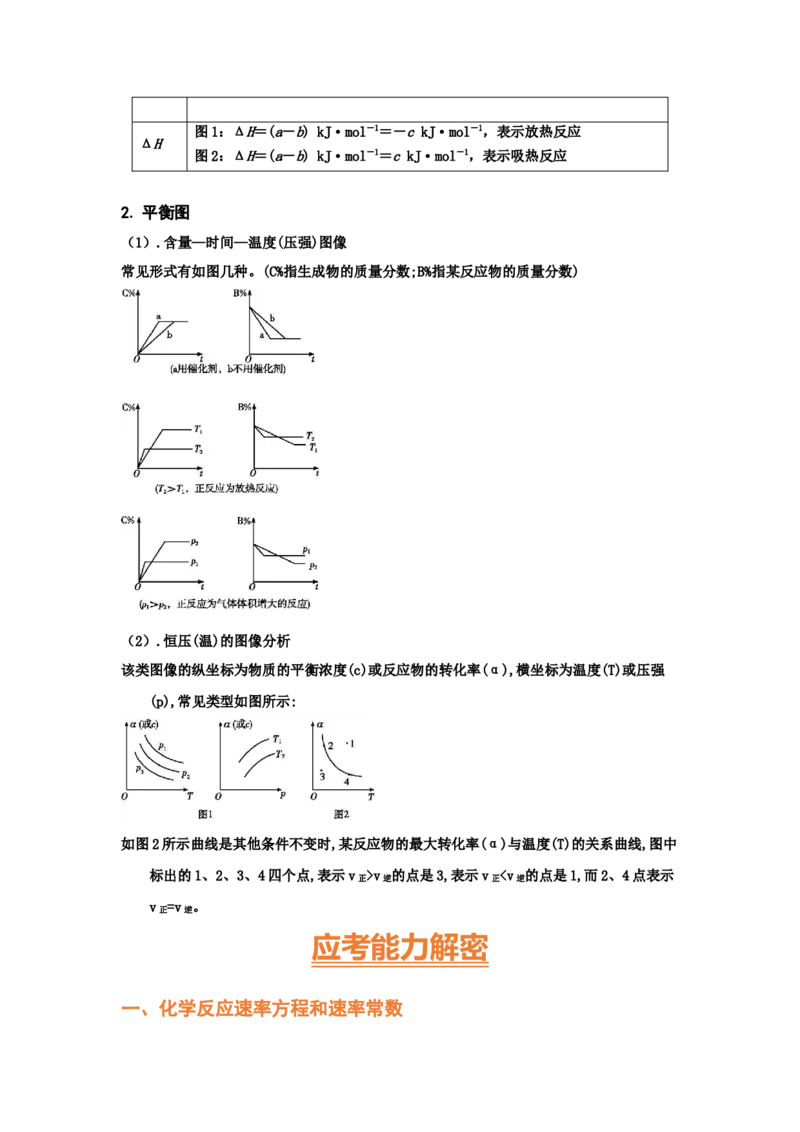
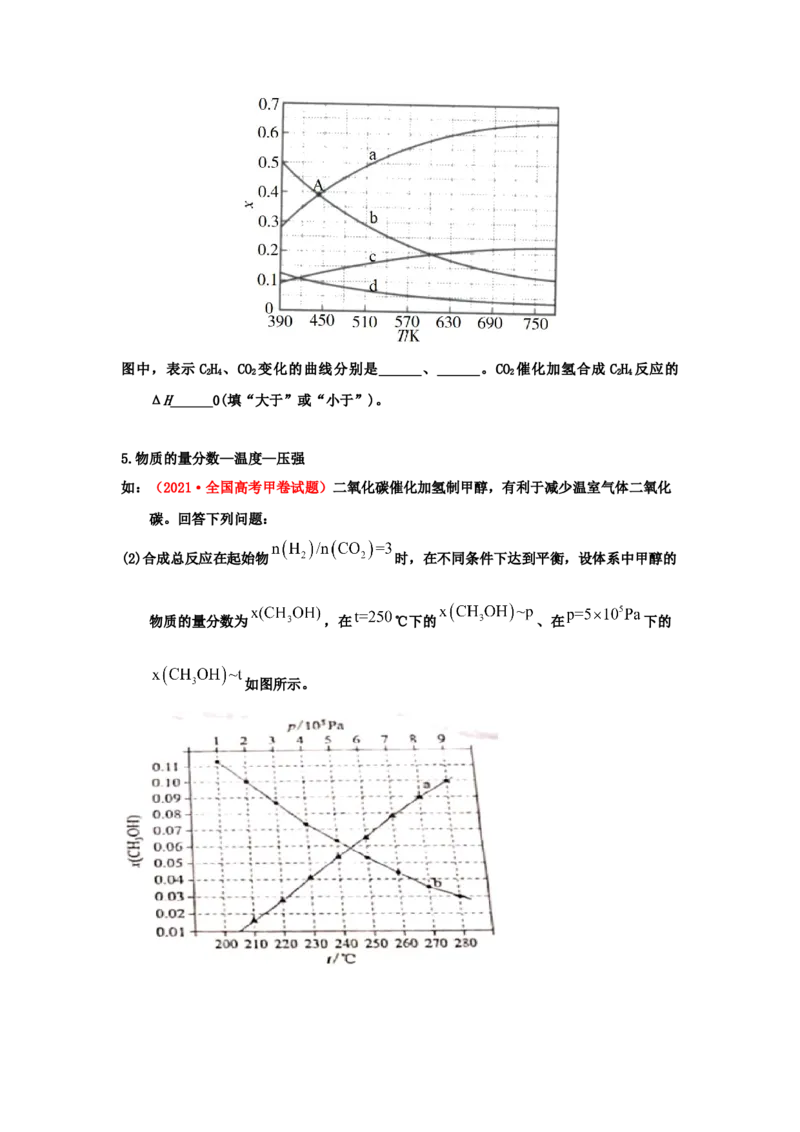
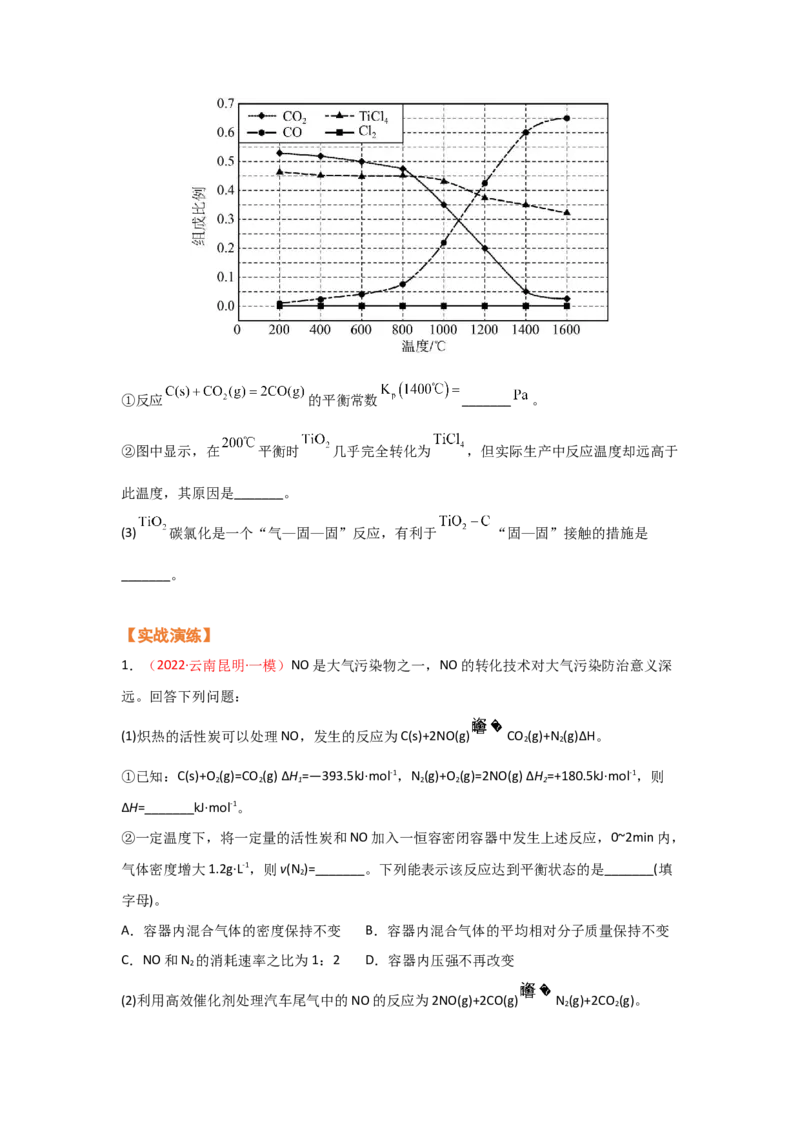
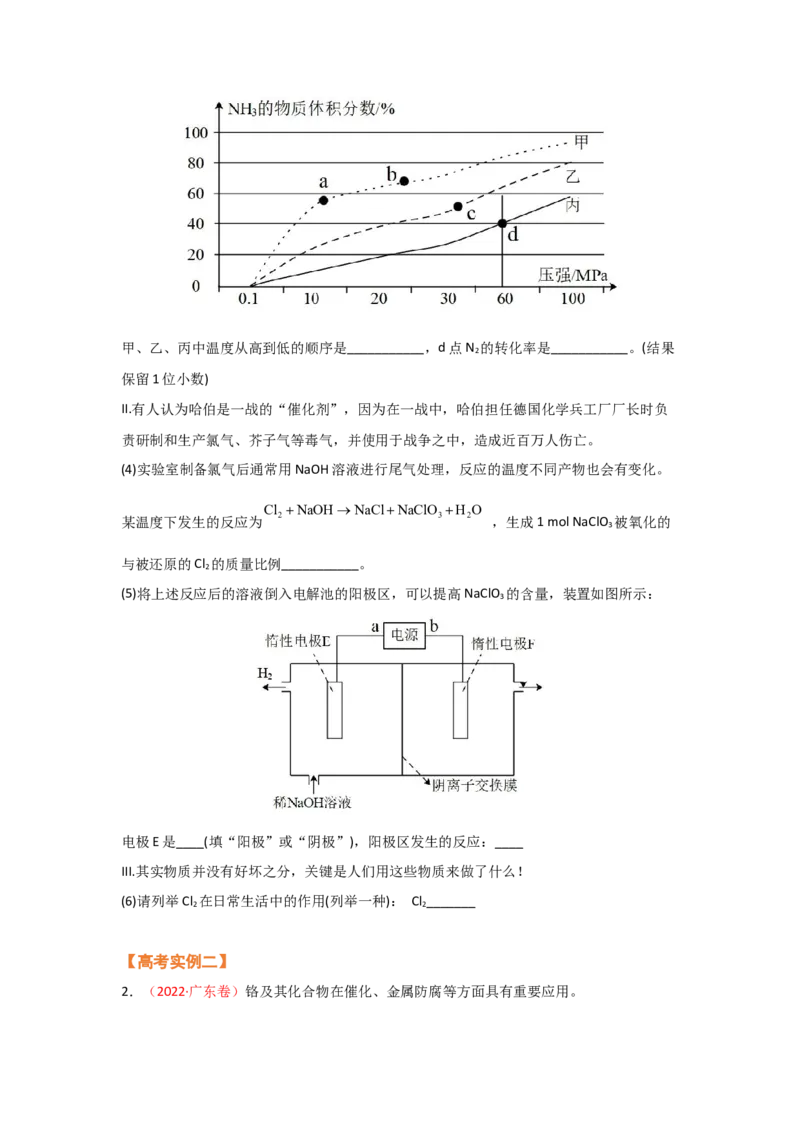
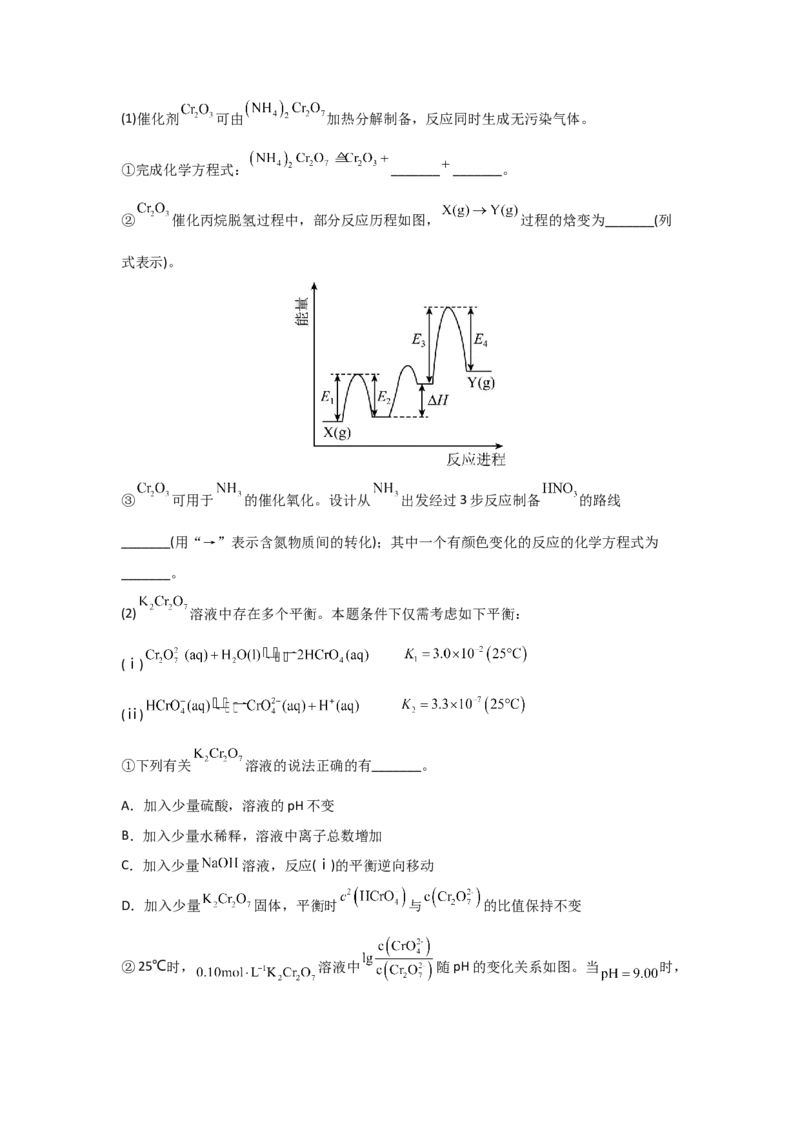
a+bv 的点是3,表示v 0,在恒温
2 2 2 2
密闭容器中,维持压强和投料比不变,将CO 和H 按一定流速⇌通过反应器,CO 转化率和
2 2 2
n(生成CH OH)100%
3
甲醇选择性[x(CH OH)%= n(消耗CO ) ]随温度变化关系如下图所示:
3 2
CO 转化率和甲醇选择性随温度的变化曲线
2
①若233-251℃时催化剂的活性受温度影响不大,分析235℃后图中曲线下降的原因
_______。
②在压强为P的恒温恒压密闭容器中,加入1molCO 和3molH 反应并达到平衡状态,CO
2 2 2
平衡转化率为20%,甲醇的选择性为50%,计算CO (g)+3H (g) CH OH(g)+H O(g)在该温度下
2 2 3 2
的平衡常数K=_______。(列出计算式) ⇌
p