文档内容
专题突破卷 08 化学反应速率与化学平衡
(考试时间:75分钟 试卷满分:100分)
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一项是符合题目要求的)
1.下列措施对增大反应速率明显有效的是
A.温度容积不变时向C(s)+HO(g) CO(g)+H(g)反应体系中增加C的量
2 2
B.Fe与稀硫酸反应制取H 时,改用浓硫酸
2
C.过氧化氢分解时加入适量的MnO
2
D.合成氨反应中在恒温、恒容条件下充入氩气使体系压强增大
2.对于化学反应 ,下列反应速率关系正确的是
A. (W)=3 (Z) B.2 (X)=3 (Z)
C.2 (X)= (Y) D.2 (W)=3 (X)
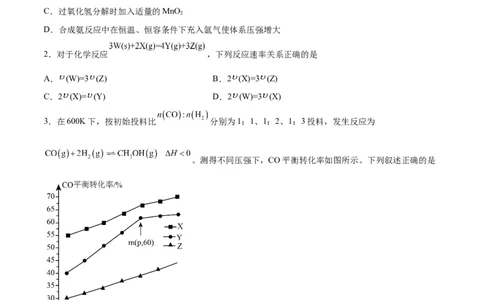
3.在600K下,按初始投料比 分别为1:1、1:2、1:3投料,发生反应为
。测得不同压强下,CO平衡转化率如图所示。下列叙述正确的是
A.曲线X代表起始投料比为1:1
B. ,该反应达到平衡状态
C.若其他条件不变,升高温度会使对应的曲线上移
D.m点对应的 的平衡转化率为60%
资料收集整理【淘宝店铺:向阳百分百】4.向一容积可变密闭容器中充入等物质的量的A、B,发生反应:2A(g)+2B(g) 3C(s)+4D(g)在不同压
强下,该反应平衡常数随温度变化如表所示。下列判断正确的是
压强Mpa
平衡常数 1.0 1.5 2.0
温度/℃
300 a b 16
516 c 64 d
800 160 f g
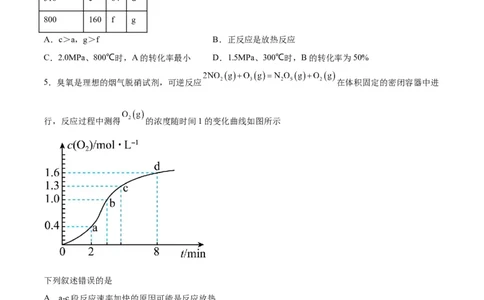
A.c>a,g>f B.正反应是放热反应
C.2.0MPa、800℃时,A的转化率最小 D.1.5MPa、300℃时,B的转化率为50%
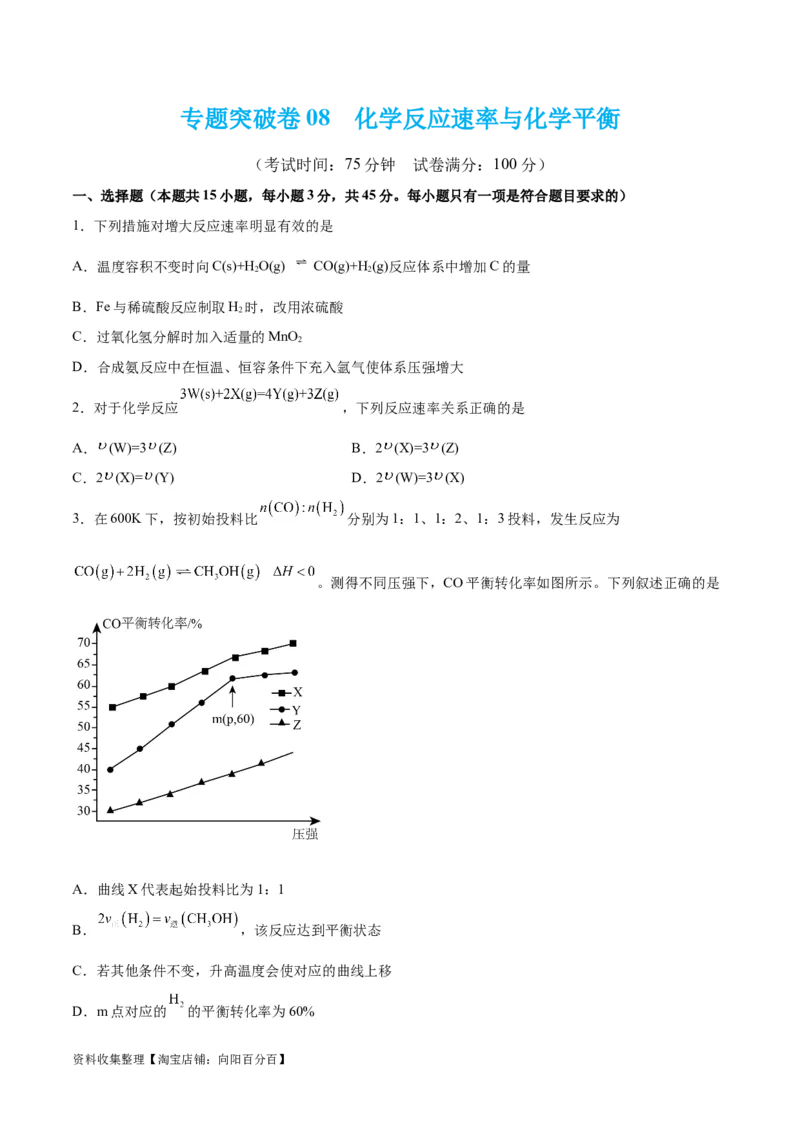
5.臭氧是理想的烟气脱硝试剂,可逆反应 在体积固定的密闭容器中进
行,反应过程中测得 的浓度随时间1的变化曲线如图所示
下列叙述错误的是
A.a-c段反应速率加快的原因可能是反应放热
B.若向容器内充入一定体积的 ,化学反应速率加快
C.向反应体系中通入氢气,反应速率降低
D.2~8min的化学反应速率
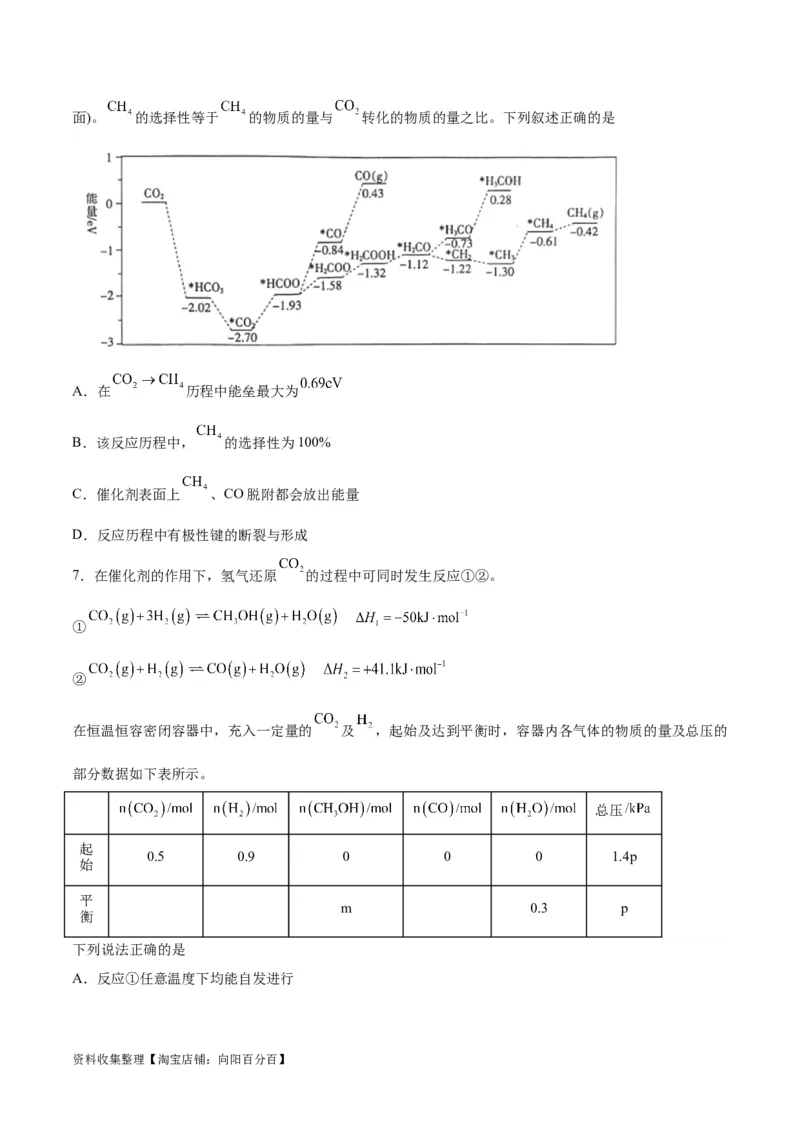
6.我国某科研团队开发催化剂用于光热催化 加氢制 。其反应历程如图所示(*表示吸附在催化剂表
资料收集整理【淘宝店铺:向阳百分百】面)。 的选择性等于 的物质的量与 转化的物质的量之比。下列叙述正确的是
A.在 历程中能垒最大为
B.该反应历程中, 的选择性为100%
C.催化剂表面上 、CO脱附都会放出能量
D.反应历程中有极性键的断裂与形成
7.在催化剂的作用下,氢气还原 的过程中可同时发生反应①②。
①
②
在恒温恒容密闭容器中,充入一定量的 及 ,起始及达到平衡时,容器内各气体的物质的量及总压的
部分数据如下表所示。
总压
起
0.5 0.9 0 0 0 1.4p
始
平
m 0.3 p
衡
下列说法正确的是
A.反应①任意温度下均能自发进行
资料收集整理【淘宝店铺:向阳百分百】B.恒温恒容下,再充入 和 ,反应①平衡右移,反应②平衡不移动
C.
D.反应②的平衡常数
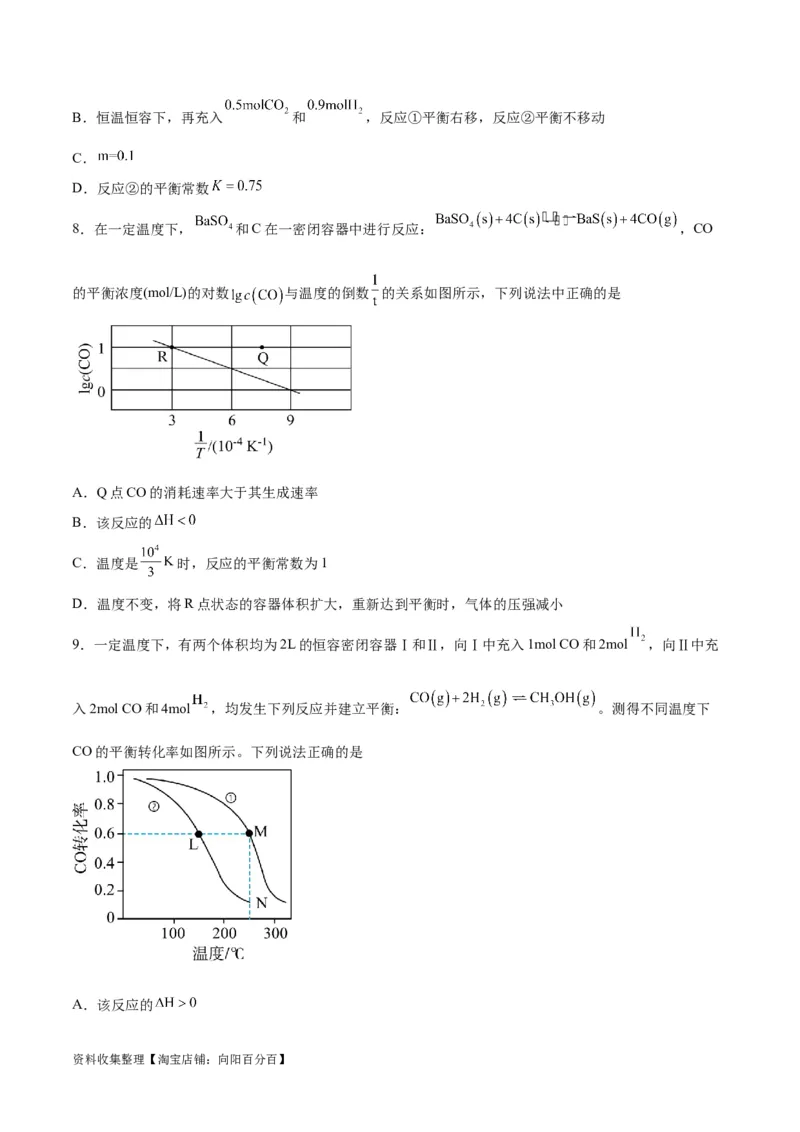
8.在一定温度下, 和C在一密闭容器中进行反应: ,CO
的平衡浓度(mol/L)的对数 与温度的倒数 的关系如图所示,下列说法中正确的是
A.Q点CO的消耗速率大于其生成速率
B.该反应的
C.温度是 时,反应的平衡常数为1
D.温度不变,将R点状态的容器体积扩大,重新达到平衡时,气体的压强减小
9.一定温度下,有两个体积均为2L的恒容密闭容器Ⅰ和Ⅱ,向Ⅰ中充入1mol CO和2mol ,向Ⅱ中充
入2mol CO和4mol ,均发生下列反应并建立平衡: 。测得不同温度下
CO的平衡转化率如图所示。下列说法正确的是
A.该反应的
资料收集整理【淘宝店铺:向阳百分百】B.L、M两点容器内正反应速率:
C.曲线①表示容器Ⅱ的变化过程
D.N点对应温度下该反应的平衡常数
10.在密闭容器中发生反应: ,往密闭容器中以 的比例通入两种反应物,
其中15 min后A在四温度下的转化率如下表所示,且 ,则下列说法正确的是
温度
转化率 10% 70% 70% 60%
A.该反应是吸热反应
B.T温度时( ),A的转化率是70%
C. 温度下,在15 min后继续进行反应,A的转化率变大
D. 温度反应15 min后,若 mol·L ,则 温度时的平衡常数是4.5
11.一定条件下,向1L恒容密闭容器中充入0.1mol A和0.3mol B发生反应: ,当
反应达平衡时,不可能存在的数据是
A. B.
C. D.
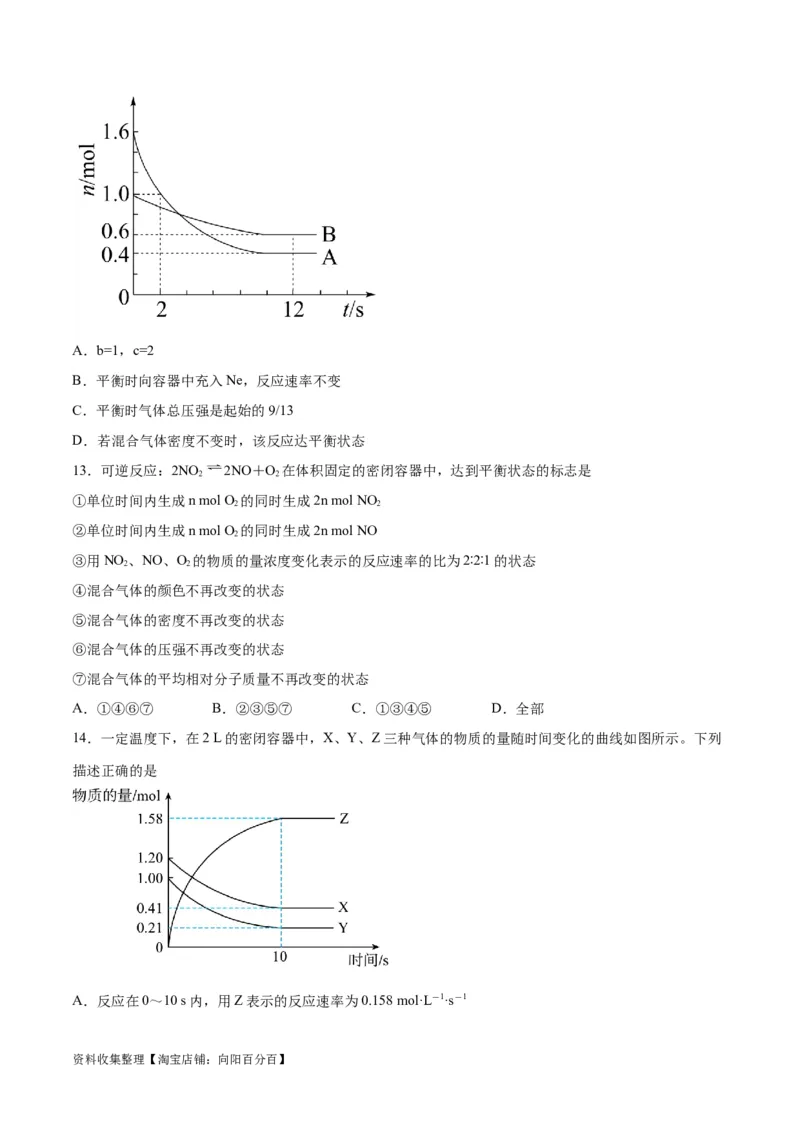
12.一定温度下,在2L恒容密闭容器中投入一定量A、B,发生反应: ,12s时生
成0.8molC,A、B物质的量变化如下图。下列说法不正确的是:
资料收集整理【淘宝店铺:向阳百分百】A.b=1,c=2
B.平衡时向容器中充入Ne,反应速率不变
C.平衡时气体总压强是起始的9/13
D.若混合气体密度不变时,该反应达平衡状态
13.可逆反应:2NO 2NO+O 在体积固定的密闭容器中,达到平衡状态的标志是
2 2
①单位时间内生成n mol O 的同时生成2n mol NO
2 2
②单位时间内生成n mol O 的同时生成2n mol NO
2
③用NO 、NO、O 的物质的量浓度变化表示的反应速率的比为2∶2∶1的状态
2 2
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的压强不再改变的状态
⑦混合气体的平均相对分子质量不再改变的状态
A.①④⑥⑦ B.②③⑤⑦ C.①③④⑤ D.全部
14.一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示。下列
描述正确的是
A.反应在0~10 s内,用Z表示的反应速率为0.158 mol·L-1·s-1
资料收集整理【淘宝店铺:向阳百分百】B.反应在0~10 s内,X的物质的量浓度减少了0.79 mol·L-1
C.反应进行到10 s时,Y的转化率为79.0%
D.反应的化学方程式为X(g)+Y(g)=Z(g)
15.已知 的速率方程为 (k为速率常数,只与温度、催化剂有关)。
实验测得, 在催化剂X表面反应的变化数据如下:
t/min 0 10 20 30 40 50 60 70
0.100 0.080 0.040 0.020 0
下列说法正确的是
A. ,
B. min时,
C.相同条件下,增大 的浓度或催化剂X的表面积,都能加快反应速率
D.保持其他条件不变,若 起始浓度为0.200 mol·L ,当浓度减至一半时共耗时50 min
二、填空题(本题包括4小题,共55分)
16.(16分)甲醇是一种重要的化工原料,具有开发和应用的广阔前景。工业上使用水煤气(CO与H 的混
2
合气体)转化成甲醇,反应为CO(g)+2H
2
(g)⇌CH
3
OH(g)。
(1)CO的平衡转化率与温度、压强的关系如图所示。
①p、p 的大小关系是p p(填“>”“<"或"=”)。
1 2 1 2
②A、B、C三点的平衡常数K 、K 、Kc的大小关系是 。
A B
③下列叙述能说明上述反应能达到化学平衡状态的是 (填字母)。
a.2v (H )=v (CHOH)
正 2 逆 3
资料收集整理【淘宝店铺:向阳百分百】b.CH OH的体积分数不再改变
3
c.混合气体的平均摩尔质量不再改变
d.同一时间内,消耗0.04molH,生成0.02molCO
2
(2)在T℃、p 压强时,往一容积为2L的密团容器内,充入0.3molCO与0.4molH 发生反应。
2 2 2
①平衡时H 的体积分数是 ;平衡后再加入1.0molCO后重新到达平衡,则CO的转化率 (填“增
2
大""不变”成“减小”),CO与CHOH的浓度比 (填"增大”“不变"或“减小")。
3
②若以不同比例投料,测得某时刻各物质的物质的量如下,CO:0.1mol、H:0.2mol、CHOH:0.2mol,
2 3
此时v(正) v(逆)(填“”“<"或“=”)。
③若p 压强恒定为p,则平衡常数K= (K 用气体平衡分压代替气体平衡浓度计算,分压=总压×气
2 p p
体的物质的量分数,整理出含p的最简表达式)。
17.(10分)用NH 催化还原NO 可以消除氮氧化物的污染。
3 x y
已知:反应I:4NH
3
(g)+6NO(g)⇌5N
2
(g)+6H
2
O(l) ΔH
1
反应II:2NO(g)+O
2
(g)⇌2NO
2
(g) ΔH
2
(且|ΔH
1
|=2|ΔH
2
|)
反应III:4NH
3
(g)+6NO
2
(g)⇌5N
2
(g)+3O
2
(g)+6H
2
O(l) ΔH
3
反应I和反应II在不同温度时的平衡常数及其大小关系如下表
温度/K 反应I 反应II
298 K 1 K 2 已知:K 1 >K 2 > >
398
(1)ΔH = (用ΔH、ΔH 的代数式表示);推测反应III是 反应(填“吸热”或“放热”)
3 1 2
(2)相同条件下,反应I在2L密闭容器内,选用不同的催化剂,反应产生N 的量随时间变化如图所示。
2
资料收集整理【淘宝店铺:向阳百分百】①计算0~4分钟在A催化剂作用下,反应速率v(NO)= 。
②下列说法不正确的是 。
A.单位时间内H—O键与N—H键断裂的数目相等时,说明反应已经达到平衡
B.若在恒容绝热的密闭容器中发生反应,当K值不变时,说明反应已经达到平衡
C.该反应的活化能大小顺序是:E(A)>E(B)>E(C)
a a a
D.增大压强能使反应速率加快,是因为增加了活化分子百分数
(3)恒温、恒压下,反应II达到平衡时体系中n(NO)∶n(O )∶n(NO)=2∶1∶2。在其他条件不变时,再充入NO 气
2 2 2
体,NO 体积分数 (填“变大”、“变小”或“不变”)。
2
18.(14分)硫酸是一种重要的基本化工产品。接触法制硫酸生产中的关键工序是 的催化氧化:
。回答下列问题:
(1)当 、 和 起始的物质的量分数分别为7.5%、10.5%和82%时,在0.5 MPa、2.5 MPa和
5.0 MPa压强下, 平衡转化率 随温度的变化如图所示。反应在5.0 MPa,550℃时的 ,判断
的依据是 。影响 的因素有 。
(2)将组成(物质的量分数)为 、 和 的气体通入反应器,在温度 、压强 条
件下进行反应。平衡时,若 转化率为 ,则 压强为 ,平衡常数 (以分压表示,分
压=总压×物质的量分数)。
(3)研究表明, 催化氧化的反应速率方程为: ,式中: 为反应速率常数,随温度
升高而增大; 为 平衡转化率, 为某时刻 转化率, 为常数。在 时,将一系列温度下的
资料收集整理【淘宝店铺:向阳百分百】、 值代入上述速率方程,得到 曲线,如图所示。
曲线上 最大值所对应温度称为该 下反应的最适宜温度 。 时,逐渐提高; 后, 逐渐下降。
原因是 。
19.(15分)氨气是重要的化工原料,在国民经济中占重要地位。工业合成氨的反应为
。回答下列问题:
(1)图甲表示合成氨反应在某段时间 中反应速率与时间的曲线图, 、 、 时刻分别改变某一外界
条件,则在下列达到化学平衡的时间段中, 的体积分数最小的一段时间是 (填字母)。
A. B. C. D.
时刻改变的条件是 。
(2)在773K时,分别将2mol 和6mol 充入一个固定容积为1L的密闭容器中,随着反应的进行,气体
混合物中 、 与反应时间t的关系如表所示:
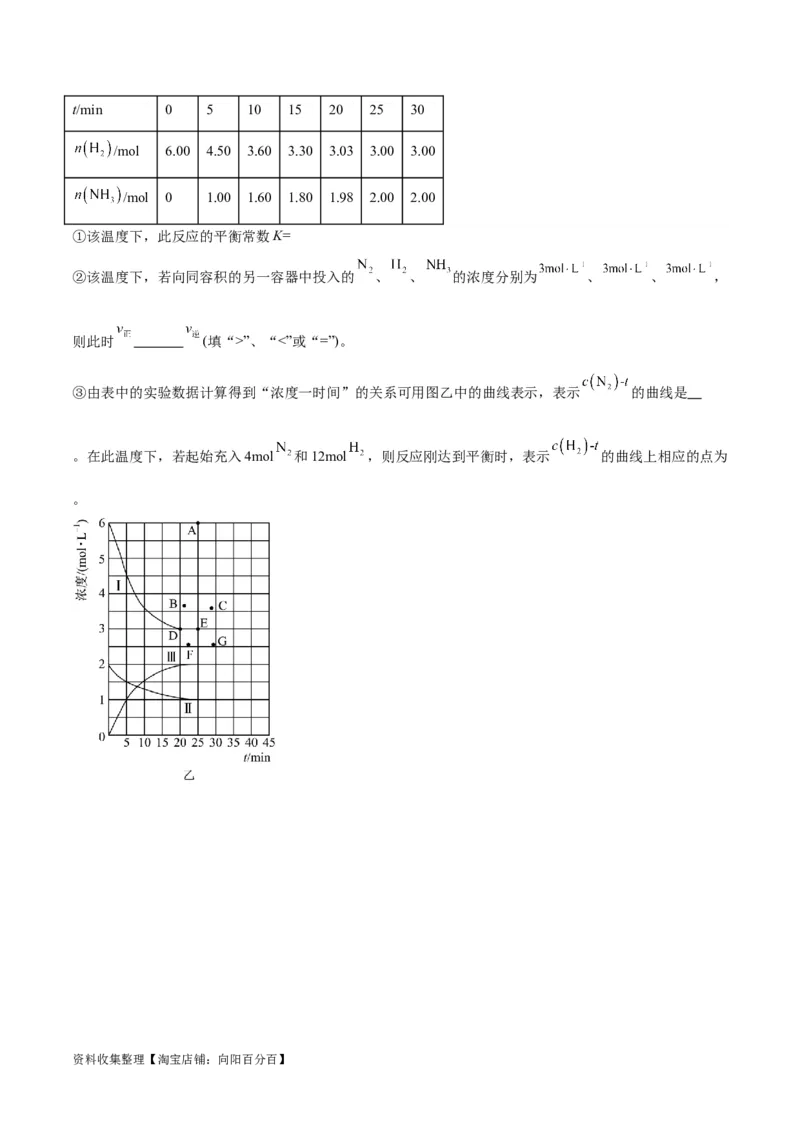
资料收集整理【淘宝店铺:向阳百分百】t/min 0 5 10 15 20 25 30
/mol 6.00 4.50 3.60 3.30 3.03 3.00 3.00
/mol 0 1.00 1.60 1.80 1.98 2.00 2.00
①该温度下,此反应的平衡常数K=
②该温度下,若向同容积的另一容器中投入的 、 、 的浓度分别为 、 、 ,
则此时 (填“>”、“<”或“=”)。
③由表中的实验数据计算得到“浓度一时间”的关系可用图乙中的曲线表示,表示 的曲线是
。在此温度下,若起始充入4mol 和12mol ,则反应刚达到平衡时,表示 的曲线上相应的点为
。
资料收集整理【淘宝店铺:向阳百分百】