文档内容
专题讲座(五) “位-构-性”综合推断题的解题方法
完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12*5分)
1.(2021·山东济宁市·高三二模)常温下,W、X、Y、Z四种短周期元素的最高价氧化物对应的水化物
溶液(浓度均为0.01mol·L-1)的pH和原子半径、原子序数的关系如图所示。下列说法错误的是
A.非金属性:W>Z>Y>X
B.简单离子的半径:Y>Z>W>X
C.W的氢化物空间构型不一定是三角锥形
D.Z的单质具有强氧化性和漂白性
2.(2021·浙江高三二模)A、B、C、D四种短周期元素,原子序数依次增大,其元素特征信息如下表所
示:
元素编
元素特征信息
号
A 单质常温下为气体,被人们看做理想的“绿色能源”
B 地壳范围内含量最多的元素
C 焰色反应显黄色
D C、D同周期,该周期中D的简单离子半径最小
下列说法不正确的是
A.113号元素与D同主族
B.原子半径D>C>B>AC.C单质与水反应所得的强碱性溶液中含有两种电子数相同的阴、阳离子
D.C、D的最高价氧化物水化物之间能发生反应,生成一种正四面体构型的离子
3.(2021·浙江高三三模)如图, 、 、 、 四种短周期元素的原子最外层电子数之和为 。下
列说法正确的是
A.原子半径( ):
B. 的氢化物一定比 的氢化物的沸点要低
C. 、 、 均有熔点高、硬度大的特性
D.某病毒 链中有 元素,可能是 取代了普通 链中的 元素
4.(2021·吉林松原市·高三其他模拟)短周期主族元素W、X、Y、Z的原子序数逐渐增大,四种元素形
成的化合物结构如图所示。在元素周期表中元素W是原子半径最小的元素,Z原子的最外层电子数是周期
数的3倍,且W与X、Y、Z均可形成电子数相等的分子。下列说法正确的是
A.简单气态氢化物稳定性:Z<X
B.由W、Y、Z三种元素组成的化合物均是共价化合物
C.YF 分子中的原子均是稳定的8电子结构
3
D.X元素的最高价氧化物对应的水化物为强酸
5.(2021·浙江金华市·高三二模)X、Y、Z、M、Q五种短周期主族元素,原子序数依次增大。元素X、
Y、Q的单质在常温下呈气态,元素Y的最高正价和最低负价之和为2,元素Z在同周期的主族元素中原子
半径最大,元素M是地壳中含最多的金属元素。下列说法不正确的是
A.元素X、Y可以形成YX、YX 等化合物
3 2 4
B.简单离子半径:Y<Z
C.元素Z、M的最高价氧化物对应的水化物能相互反应D.M、Q两种元素形成的化合物的水溶液呈酸性
6.(2021·山东滨州市·高三二模)短周期主族元素W、X、Y、Z的原子序数依次增大,W的一种核素没
有中子,Y原子中L层电子数与K层电子数三倍。a、b、c、d均是由以上四种元素中的两种组成的二元化
合物,且d是淡黄色固体;25℃时,0.1mol/L e的水溶液pH=13。上述物质的转化关系如图所示。
下列说法正确的是
A.沸点:a>c
B.元素的非金属性:X>W
C.f溶液中存在c(H+)+c(HCO-)+c(HCO)=c(OH-)
3 2 3
D.简单阴离子的还原性:Y>W
7.(2021·浙江高三一模)根据物质的组成、结构等信息可以预测其性质或用途。下列预测中,明显不
合理的是
A.根据化合价预测,高铜酸钠( )与 可生成硫酸盐
B.根据组成预测,铝酸三钙( )溶于足量盐酸,生成白色沉淀
C.根据在周期表中位置预测,单质砷(第ⅤA族)是重要的半导体材料
D.根据结构预测,葡萄糖[ ]溶液中加入新制氢氧化铜,溶液呈绛蓝色
8.(2020·浙江绍兴市·高三一模)氮化镓(GaN)是第三代半导体核心材料,镓(Ga) 与铝位于同一主族,
微量分散于铝土矿中,其熔点为29.8 ℃,沸点为2403℃。下列说法不正确的是
A.室温下合成氮化镓的普遍方法为:2Ga+N =2GaN
2
B.GaO 具有两性,既能与酸反应,又能与碱反应
2 3
C.从铝土矿提取Al的废液中电解提取Ga,阴极反应为: Ga(OH) +3e- =Ga +4OH-
D.由于液态镓的宽温度范围,故Ga可以用于制作高温温度计的材料
9.(2021·北京高三二模)下表是周期表中5种元素的相关信息,其中Q、W、X位于同一周期。
元素 信息 元素 信息
Q 位于周期表的第3周期第ⅢA族 Y 焰色反应为紫色
W 最高正化合价为+7价 ZX 本周期中原子半径最大 原子结构示意图为
下列说法正确的是
A.Q在地壳中含量最高
B.元素的金属性:
C.气态氢化物的稳定性:
D.Q的最高价氧化物对应的水化物既能与NaOH反应,又能与HCl反应
10.(2021·北京高三模拟)X、Y、Z、R、M为原子序数依次增大的短周期元素,其原子的最外层电子数
与原子半径的关系如图所示。
下列说法不正确的是
A.Y形成的化合物种类最多
B.同周期元素的简单阳离子中,R+的半径最大
C.同主族中,M的最高价氧化物对应水化物的酸性最强
D.X的原子与Y、Z、R、M的原子均可形成共价化合物
11.(2020·甘肃兰州市·高三一模)X、Y、Z、W为原子序数依次增大的四种短周期主族元素,W原子是
同周期元素中原子半径最小的主族元素。已知A、B、C、D、E为上述四种元素中的两种或三种所组成的5
种化合物间的转化关系如右图所示。A的相对分子质量为28,B分子中含有18个电子。下列有关说法错误
的是( )
A.由W、Z、X三种元素组成的化合物一定是强酸B.E能与金属钠反应产生气体
C.化合物D中含有极性键
D.最高价氧化物对应的水化物的酸性W最强
12.(2021·南昌市八一中学高三三模)阿散酸是一种饲料添加剂,其结构可表示为:
,其中As位于元素周期表中第四周期第ⅤA族。X、Y它们的单质均为
气体,Z原子半径最小,下列说法错误的是
A.X与Z可以形成原子个数比为1∶2的化合物
B.X、Y常见的氢化物分子之间可以形成氢键
C.X、Y、Z三元素可形成离子化合物
D.X的氢化物稳定性比Y的氢化物稳定性强
二、主观题(共3小题,共40分)
13.(2021·北京高三一模)(14分)有8种短周期主族元素x、y、z、d、e、f、g、h,其中x、y、d、
f随着原子序数的递增,其原子半径的相对大小、最高正价或最低负价的变化如图1所示,z、e、g、h的
最高价氧化物对应水化物溶液(浓度均为0.01mol/L)的pH与原子序数的关系如图2所示。
根据判断出的元素回答下列问题:
(1)f在周期表中的位置是___________;
(2)y、z、d的氢化物中最稳定的是(写化学式)___________;
(3)x与y形成的多种化合物中,最简单的化合物的空间构型是___________;
(4)描述e的单质在空气中燃烧的现象:___________;
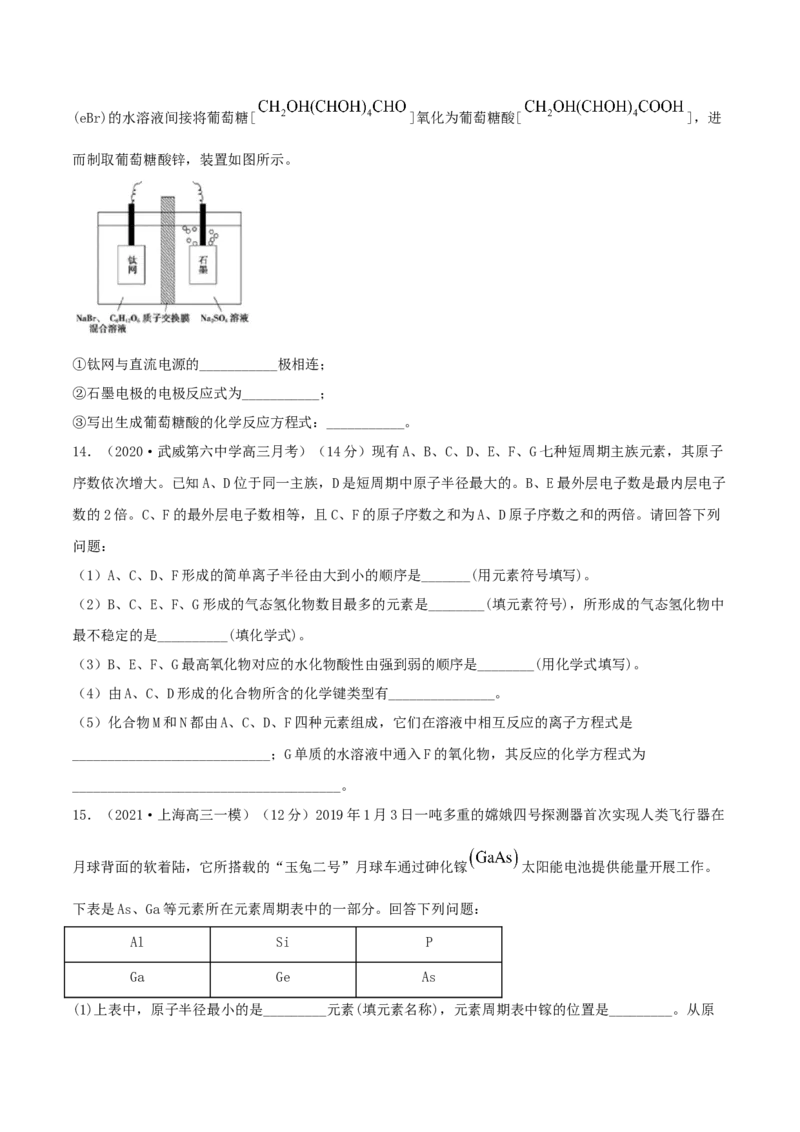
(5)锌元素对婴儿及青少年的智力和身体发育有重要的作用,被称为生命火花。利用恒电势电解e的溴化物(eBr)的水溶液间接将葡萄糖[ ]氧化为葡萄糖酸[ ],进
而制取葡萄糖酸锌,装置如图所示。
①钛网与直流电源的___________极相连;
②石墨电极的电极反应式为___________;
③写出生成葡萄糖酸的化学反应方程式:___________。
14.(2020·武威第六中学高三月考)(14分)现有A、B、C、D、E、F、G七种短周期主族元素,其原子
序数依次增大。已知A、D位于同一主族,D是短周期中原子半径最大的。B、E最外层电子数是最内层电子
数的2倍。C、F的最外层电子数相等,且C、F的原子序数之和为A、D原子序数之和的两倍。请回答下列
问题:
(1)A、C、D、F形成的简单离子半径由大到小的顺序是_______(用元素符号填写)。
(2)B、C、E、F、G形成的气态氢化物数目最多的元素是________(填元素符号),所形成的气态氢化物中
最不稳定的是__________(填化学式)。
(3)B、E、F、G最高氧化物对应的水化物酸性由强到弱的顺序是________(用化学式填写)。
(4)由A、C、D形成的化合物所含的化学键类型有_______________。
(5)化合物M和N都由A、C、D、F四种元素组成,它们在溶液中相互反应的离子方程式是
____________________________;G单质的水溶液中通入F的氧化物,其反应的化学方程式为
______________________________________。
15.(2021·上海高三一模)(12分)2019年1月3日一吨多重的嫦娥四号探测器首次实现人类飞行器在
月球背面的软着陆,它所搭载的“玉兔二号”月球车通过砷化镓 太阳能电池提供能量开展工作。
下表是As、Ga等元素所在元素周期表中的一部分。回答下列问题:
Al Si P
Ga Ge As
(1)上表中,原子半径最小的是_________元素(填元素名称),元素周期表中镓的位置是_________。从原子结构角度解释磷与砷的非金属性强弱:_______________。
(2)GaAs可以用浓硝酸溶解,生成HAsO 和Ga(NO)。配平反应的化学方程式,并标出电子转移方向和数目:
3 4 3 3
GaAs+HNO→Ga(NO)+NO↑+HAsO+HO,_________
3 3 3 2 3 4 2
(3)GaN、GaAs、GaP都是良好的半导体材料,晶体类型与晶体硅相同,它们的熔点如表。
晶体 GaN GaAs GaP
熔点/℃ 1700 1238 1480
解释它们熔点变化的原因______________。
(4)亚磷酸(HPO)与NaOH反应只能生成NaHPO 和NaHPO 两种盐,这两种盐溶液均呈碱性。根据以上信息
3 3 2 3 2 3
判断,亚磷酸应属于____________________酸,NaHPO 溶液中阴离子浓度由大到小的次序为_______。
2 3