文档内容
专题讲座(二)陌生化学方程式书写
【学科核心素养】
证据推理与模型认知:通过分析、推理等方法认识氧化还原反应的特征和实质,建立氧化还原反应书
写的思维模型。
科学探究与创新意识:认识科学探究是进行科学解释和发现。创造和应用的科学实践活动;能从氧化
还原反应的角度,进行陌生信息型离子方程式的书写和配平。
【核心素养发展目标】
1.了解物质的量及其单位摩尔质量、阿伏加德罗常数的含义与应用,利用物质的量将宏观的物理量与
微观粒子的个数联系起来,并能从宏观和微观结合的视角分析解决问题。
2.能从物质的量的角度认识物质的组成及变化,建立物质的量、物质的质量和微观粒子数之间计算的
思维模型。
3.能从宏观和微观相结合的角度理解影响物质体积大小的因素,知道气体摩尔体积的含义,能叙述阿
伏加德罗定律的内容。
4.能基于物质的量认识物质的组成及变化,建立n、m、V 之间计算的模型,熟悉阿伏加德罗定律的应
m
用。
【知识点解读】
信息型方程式的书写是高考的必考内容,考查频率高。试题往往与生产、生活实际相结合,以反应现
象、物质性质、元素价态变化、氧化剂(还原剂)得失电子数目等信息呈现出来,要求以此判断产物,从而
正确书写方程式。
1.题干中给出部分反应物和部分产物:
(1)信息提取:依题给信息找出已知的反应物和产物,确定反应类型。
(2)联想推理:根据原子个数守恒或物质的特征或元素价态变化特点及微粒存在形式填写出未知产物。
(3)配平:缺少的物质一般用HO、H+、OH-填补。
2
2.工艺流程、图像型化学方程式的书写:
(1)分析流程图中的反应物:包括原料、加入的物质及溶液酸碱环境。
(2)看生成物:包括目标产物和杂质。
(3)书写、配平:灵活运用元素守恒和得失电子守恒。
注意:有的方程式书写要求能从图表中提取有用的信息,看懂横坐标和纵坐标所表示的含义,看懂在
特定要求时,溶液中的粒子存在形式。
3.注意事项:(1)要注意溶液的酸碱性不同对产物的影响:如高锰酸钾在酸性条件下一般被还原为Mn2+,而在碱性条
件下则得到MnO2- ;酸性条件下,离子方程式中不能出现OH-;在碱性条件下,离子方程式中不能出现
4
H+。碱性条件下多氧配水,另一侧生成OH-(在反应物或生成物中配上水)。酸性条件下多氧配H+,另一侧
生成水(在反应物或生成物中配上H+);
(2)要注意反应物的量不同(或溶液的浓度不同)产物不同。如过量的铁与稀硝酸反应,生成硝酸亚铁;
浓硝酸和稀硝酸分别和铜反应的还原产物不同。
【典例剖析】
高频考点一 已知部分产物,写出完整的方程式
例1.某反应中反应物与生成物有AsH 、HSO 、KBrO 、KSO 、HAsO 、HO和一种未知物X。已知
3 2 4 3 2 4 3 4 2
0.2 mol KBrO 在反应中得到1 mol e-生成X,则X的化学式: ,试写出该反
3
应的化学方程式: 。
【答案】Br 4HSO +5AsH +8KBrO==5H AsO +4Br +4K SO +4H O
2 2 4 3 3 3 4 2 2 4 2
【解析】设X中Br的化合价为m,根据电子守恒得:0.2×(5-m)=1,m=0,所以KBrO 被还原成Br 。
3 2
在该氧化还原反应中,KBrO 是氧化剂,其还原产物为 Br ,AsH 为还原剂,其氧化产物为 HAsO ,
3 2 3 3 4
HSO 作为反应物提供酸性环境,根据化合价升降相等即可配平。
2 4
【方法技巧】遇到此类陌生度高的题目要能够把题目所给物质理清楚,是氧化还原反应的,可利用氧
化还原反应价态变化规律确定生成物中变价元素的价态,进而确定生成物,解答此类题的法宝是“守
恒”。
【变式探究】二硫化钨(WS,WS 中W的化合价为+4)可用作润滑剂及石油化工领域中的催化剂。由
2 2
钨铁矿(其主要成分是FeWO,还含少量Al O)制备二硫化钨的工艺流程如下:
4 2 3
(1)写出FeWO 在碱熔过程中发生反应的化学方程式:__________________________________。
4
(2)滤渣Ⅰ中主要成分的形成可用离子方程式表示为 __________________________________。
【答案】(1)4FeWO+O +8NaOH 2Fe O+4Na WO+4H O
4 2 2 3 2 4 2
(2)Al +CO +2H O=Al(OH) ↓+HC
O- 2 2 3 O-
2 3
【解析】(1)根据流程图,FeWO 在碱熔过程中,得到Fe O 和NaWO,反应物是NaOH、FeWO、
4 2 3 2 4 4O,生成物是NaWO、Fe O 等,FeWO 中Fe显+3价,W显+5价,NaWO 中W显+6价,FeWO 为还原
2 2 4 2 3 4 2 4 4
剂,O 为氧化剂,因此根据化合价升降法进行配平,得到化学反应方程式为4FeWO+O +8NaOH
2 4 2
2Fe O+4Na WO+4H O。(2)根据钨铁矿成分中有氧化铝,氧化铝为两性氧化物,碱熔过程中发生反应
2 3 2 4 2
Al
2
O
3
+2NaOH 2NaAlO
2
+H
2
O,粗钨酸钠溶液中通入过量的CO
2
,发生反应Al O-
2
+CO +2H O=Al(OH) ↓+HC ,滤渣Ⅰ为氢氧化铝。
2 2 3 O-
3
高频考点二 实验流程中化学方程式的书写
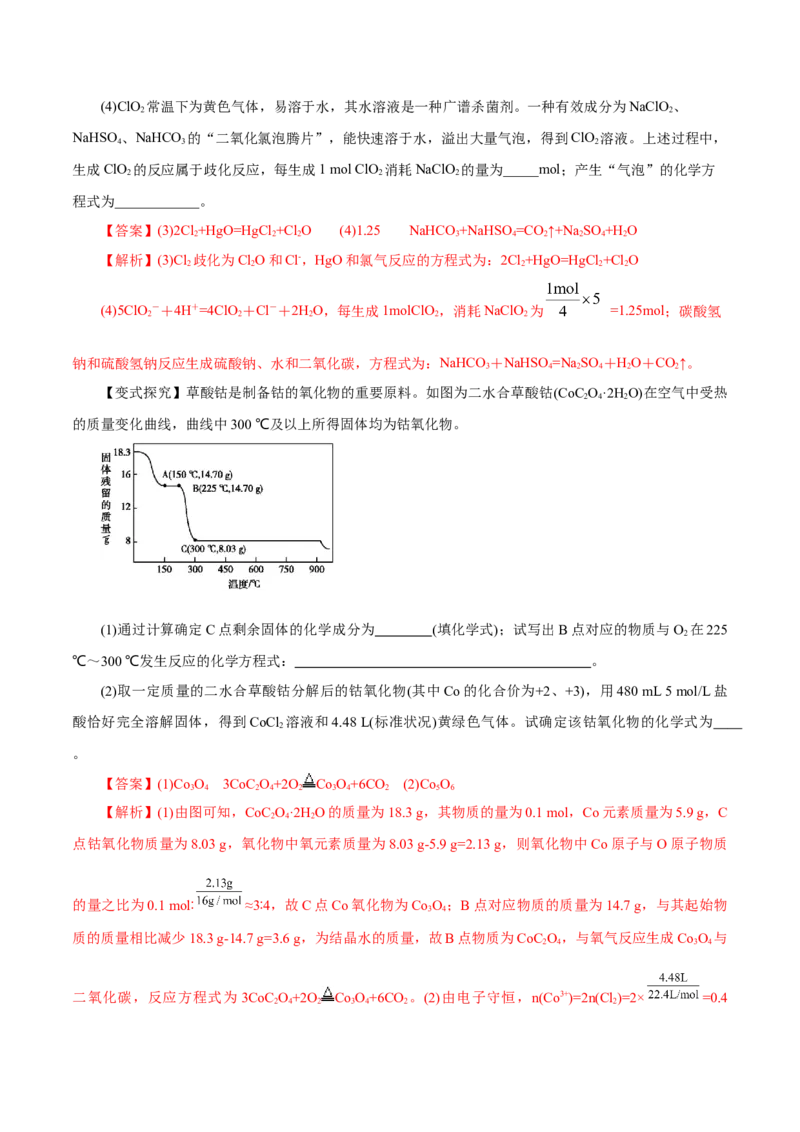
例2. 由于氯气会与自来水中的有机物发生反应,生成对人体有害的物质,人们尝试研究并使用新的
自来水消毒剂,如ClO 气体就是一种新型高效含氯消毒剂。某兴趣小组通过下图所示装置(夹持装置略)对
2
其进行制备、收集、吸收并制取 NaClO。
2
(1)图中装置有一明显错误,请指出并纠正:__________________________________________。
(2)打开B的活塞,A中有ClO 生成,写出其反应的离子方程式:__________________________。
2
(3)D中吸收ClO 后生成NaClO 和NaHCO ,写出D中所发生反应的离子方程式:
2 2 3
________________________________________________。
(4)E中溶液出现黄色能否说明ClO 未被HO 和NaCO 的混合溶液充分吸收,判断并说明理由:
2 2 2 2 3
______________________________________________________________。
(5)另一种制备ClO 的方法是用NaClO 与盐酸反应,同时有Cl 生成,产物中Cl 体积约占总气体体
2 3 2 2
积。则每生成0.5 mol ClO ,转移________ mol e-。
2
【答案】(1)C装置中导气管应该长进短出
(2)SO+2H++2ClO===2ClO ↑+HO+SO
2 2
(3)2CO+HO+2ClO ===2ClO+O+2HCO
2 2 2 2
(4)不能 因为D装置中有O 产生,O 也可能将I-氧化为I (5)0.5
2 2 2
【解析】(1)ClO 气体的密度比空气大,应该选用向上排空气法收集,所以图中装置C中导气管应该
2
“长进短出”。(2)依题意,稀硫酸、NaClO 和NaSO 混合能产生ClO ,氯元素化合价由+5价降低到+4
3 2 3 2价,表明ClO表现氧化性,而SO具有较强的还原性,所以其离子方程式为SO+2H++2ClO===2ClO ↑+
2
HO+SO。(3)由题意知ClO 与HO、NaCO 接触生成NaClO 和NaHCO ,氯元素化合价由ClO 的+4价
2 2 2 2 2 3 2 3 2
变化到NaClO 的+3价,ClO 作氧化剂,碳元素化合价没变,只能是HO 中-1价的氧被氧化为O,HO
2 2 2 2 2 2 2
作还原剂,所以D中发生反应的离子方程式为2CO+HO+2ClO ===2ClO+O↑+2HCO。(4)KI溶液变黄
2 2 2 2
说明有I 生成,即I-被氧化成I,除ClO 能氧化I-外,混合气体中的O 也能氧化I-,所以E中溶液出现
2 2 2 2
黄色不能说明ClO 未被HO 和NaCO 的混合溶液充分吸收。(5)NaClO 与盐酸反应有ClO 和Cl 生成,根
2 2 2 2 3 3 2 2
据“互不交叉原理”,NaClO 转化为ClO ,HCl转化为Cl,且ClO 与Cl 化学计量数之比为2∶1,其反应
3 2 2 2 2
方程式及转移的电子数为2NaClO+4HCl===2ClO ↑+Cl↑+2NaCl+2HO,转移2e-。根据方程式计量关
3 2 2 2
系可知每生成0.5 mol ClO 时转移0.5 mol e-。
2
【变式探究】(2019·江苏卷)实验室以工业废渣(主要含CaSO·2H O,还含少量SiO、Al O、Fe O)为
4 2 2 2 3 2 3
原料制取轻质CaCO 和(NH )SO 晶体,其实验流程如下:
3 4 2 4
将氨水和NH HCO 溶液混合,可制得(NH )CO 溶液,其离子方程式为
4 3 4 2 3
______________________________________________________________________;
浸取废渣时,向(NH )CO 溶液中加入适量浓氨水的目的是
4 2 3
________________________________________________________________________。
【解析】HCO与NH ·H O反应生成CO、NH和HO。CO水解显碱性,加入NH ·H O可以抑制CO水
3 2 2 3 2
解,增加溶液中c(CO),促进CaSO 转化为CaCO 。
4 3
【答案】HCO+NH ·H O===NH+CO+HO(或HCO+NH ·H O NH+CO+HO)
3 2 2 3 2 2
增加溶液中CO的浓度,促进CaSO 的转化
4
【方法技巧】 涉及实验流程题有关的陌生方程式书写模式总结如下:先写出“反应物(原料+加入的物
质+溶液酸碱环境)→生成物(目标产物+杂质)”,再进行配平。一定要学会灵活运用三大守恒(元素守恒、得
失电子守恒、电荷守恒),正确预测合理产物。
【变式探究】(2018·浙江卷)某同学用含结晶水的正盐X(四种短周期元素组成的纯净物)进行了如下实
验:实验中观测到:混合气甲呈无色并被蒸馏水全部吸收;固体乙为纯净物;步骤③中,取 溶液丙,恰
好中和需消耗0.002 00 mol NaOH,另取一定量溶液丙,加入少量KFeO 固体,产生黄绿色气体。
2 4
请回答:
(1)X的化学式是 ,步骤①的化学方程式是 。
(2)溶液丙与KFeO 固体反应的化学方程式是 。
2 4
【解析】含结晶水的正盐,共四种元素,可知混合气体甲中含有HO,另外最后加入酸化的硝酸银溶
2
液有白色沉淀生成,可判断甲中有氯元素,甲可以被水完全吸收,且丙可以消耗氢氧化钠,可知甲中含有
气体HCl,元素一共为四种,已推知三种(H、O、Cl),若盐X为铵盐,会完全分解,无固体剩余,可以排
除,则盐X中至少有一种金属元素,可知甲中无其他气体。n(HCl)=0.02 mol,n(H O)=
2
mol=0.05 mol,盐X为正盐,并且所含元素均为短周期元素,可知阴离子为氯离子,而阳离子可能为
Na+、Mg2+、Al3+,若是钠离子,无法产生HCl气体(不水解),而氯化镁与氯化铝灼烧后得到的分别是氧化
镁和氧化铝,根据质量计算可知阳离子为Mg2+,固体乙为MgO,n(MgO)=0.1 mol,故X为MgCl ·6H O。
2 2
【答案】(1)MgCl ·6H O MgCl ·6H O MgO+2HCl+5HO
2 2 2 2 2
(2)2K FeO+16HCl==4KCl+3Cl ↑+2FeCl +8H O
2 4 2 3 2
高频考点三 需要预测产物的方程式的书写
例3.铬及其化合物常被应用于冶金、化工、电镀、制药、纺织等行业,但使用后的废水因其中含高价
铬的化合物而毒性很强,必须进行处理。工业上往往采取下列循环工艺防止铬的污染:
(1)上述各步反应中属于氧化还原反应的是____________________(填序号)。
(2)第①步,含Cr O的废水在酸性条件下用绿矾FeSO ·7H O处理,写出并配平反应的离子方程式:
2 4 2
_______________________________________________________。
(3)第②步,向上述反应后的溶液中加入适量的碱石灰,使铬离子转变为Cr(OH) 沉淀。处理后,沉淀
3
物中除了 Cr(OH) 外,还有________________、________________(写化学式)。已知 Cr(OH) 性质类似
3 3
Al(OH) ,是既能与强酸反应又能与强碱反应的两性物质,写出从该沉淀物中分离出Cr(OH) 的离子方程
3 3
式:_____________________________________________。
(4)回收所得的 Cr(OH) ,经③④⑤步处理后又可转变成 KCr O 。纯净的KCr O 常用于准确测定
3 2 2 7 2 2 7NaSO 溶液的物质的量浓度,方法如下:
2 2 3
①Cr O+6I-+14H+===3I +2Cr3++7HO
2 2 2
②2S O+I===S O+2I-
2 2 4
准确称取纯净的KCr O 0.122 5 g,配成溶液,用上述方法滴定,消耗 NaSO 溶液25.00 mL。则
2 2 7 2 2 3
NaSO 溶液的物质的量浓度为________(保留四位有效数字)。
2 2 3
【答案】(1)①④ (2)Cr O+6Fe2++14H+===2Cr3++6Fe3++7HO
2 2
(3)Fe(OH) CaSO Cr(OH) +OH-==CrO+2H O CrO+CO +2H O==Cr(OH) ↓+HCO
3 4 3 2 2 2 3
(4)0.100 0 mol·L-1
【解析】(1)①中铬元素由+6价降至+3价,④中铬元素由+3价升至+6价。(2)亚铁离子具有还原
性,与重铬酸根离子反应生成铬离子和铁离子。(3)加入绿矾反应后,溶液中有铁离子和硫酸根离子,再加
入碱石灰,除生成Cr(OH) 外,还会生成氢氧化铁和硫酸钙。氢氧化铬类似氢氧化铝,具有两性,能与氢
3
氧化钠反应生成NaCrO :Cr(OH) +NaOH===NaCrO +2HO,NaCrO 类似偏铝酸钠,通入过量的CO 生
2 3 2 2 2 2
成氢氧化铬、碳酸氢钠:NaCrO +CO +2HO===Cr(OH) ↓+NaHCO 。(4)根据反应得关系式KCr O ~3I
2 2 2 3 3 2 2 7 2
~6NaSO,n(Na SO)=6n(K Cr O),c(Na SO)==0.100 0 mol·L-1。
2 2 3 2 2 3 2 2 7 2 2 3
【变式探究】NaClO 是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
2
回答下列问题:
(1)NaClO 中Cl的化合价为________________________。
2
(2)写出“反应”步骤中生成ClO 的化学方程式:
2
。
【解析】(1)根据化合物中元素正负化合价代数和为0知,NaClO 中Cl显+3价。(2)由流程图可
2
知,NaClO 与HSO 、SO 反应生成NaHSO 和ClO ,根据电子守恒、元素守恒可写出并配平反应方程式
3 2 4 2 4 2
为2NaClO+H SO +SO===2ClO +2NaHSO 。
3 2 4 2 2 4
【答案】(1)+3 (2)2NaClO+SO+H SO ===2ClO +2NaHSO
3 2 2 4 2 4
高频考点四 需要计算确定反应物或生成物的方程式的书写
例4.(2020·全国新课标Ⅱ卷节选)(3)Cl O为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl 反
2 2
应来制备,该反应为歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制备ClO的化学方程式为
2
______。(4)ClO 常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO、
2 2
NaHSO、NaHCO 的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO 溶液。上述过程中,
4 3 2
生成ClO 的反应属于歧化反应,每生成1 mol ClO 消耗NaClO 的量为_____mol;产生“气泡”的化学方
2 2 2
程式为____________。
【答案】(3)2Cl +HgO=HgCl +ClO (4)1.25 NaHCO +NaHSO =CO ↑+Na SO +H O
2 2 2 3 4 2 2 4 2
【解析】(3)Cl 歧化为ClO和Cl-,HgO和氯气反应的方程式为:2Cl+HgO=HgCl +ClO
2 2 2 2 2
(4)5ClO-+4H+=4ClO +Cl-+2HO,每生成1molClO,消耗NaClO 为 =1.25mol;碳酸氢
2 2 2 2 2
钠和硫酸氢钠反应生成硫酸钠、水和二氧化碳,方程式为:NaHCO +NaHSO=Na SO +HO+CO↑。
3 4 2 4 2 2
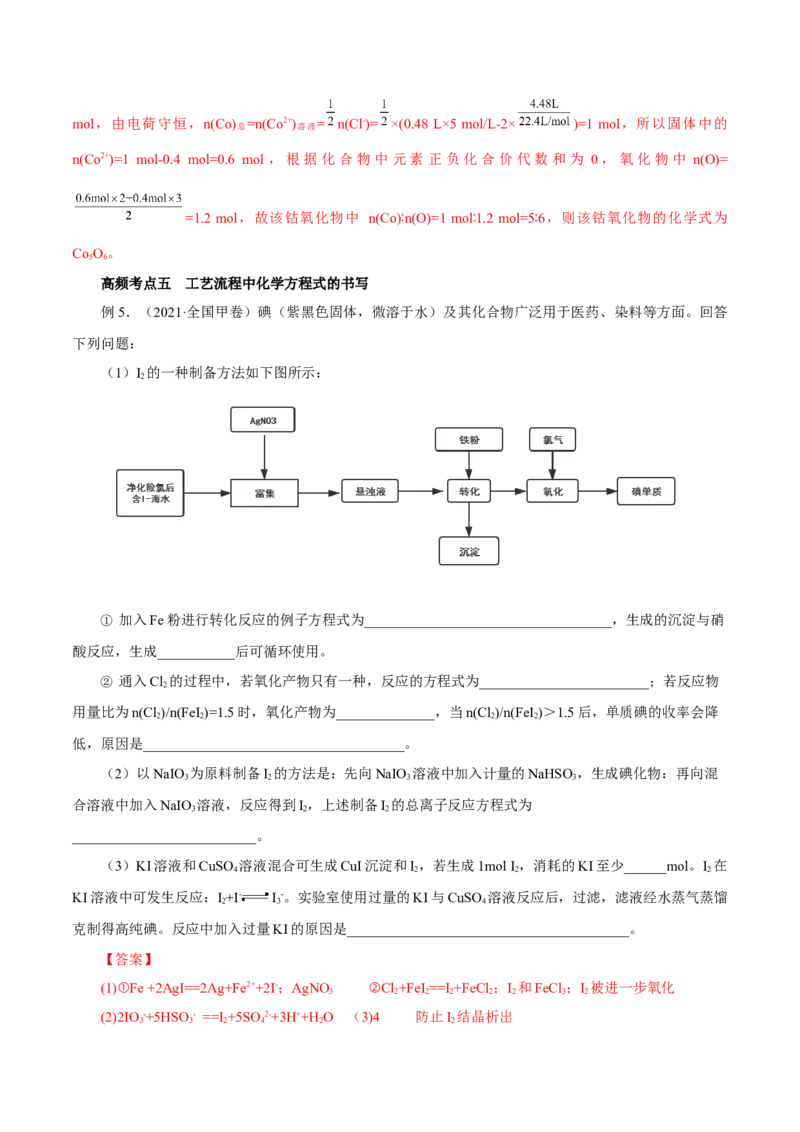
【变式探究】草酸钴是制备钴的氧化物的重要原料。如图为二水合草酸钴(CoC O·2H O)在空气中受热
2 4 2
的质量变化曲线,曲线中300 ℃及以上所得固体均为钴氧化物。
(1)通过计算确定C点剩余固体的化学成分为 (填化学式);试写出B点对应的物质与O 在225
2
℃~300 ℃发生反应的化学方程式: 。
(2)取一定质量的二水合草酸钴分解后的钴氧化物(其中Co的化合价为+2、+3),用480 mL 5 mol/L盐
酸恰好完全溶解固体,得到CoCl 溶液和4.48 L(标准状况)黄绿色气体。试确定该钴氧化物的化学式为
2
。
【答案】(1)Co O 3CoC O+2O Co O+6CO (2)Co O
3 4 2 4 2 3 4 2 5 6
【解析】(1)由图可知,CoC O·2H O的质量为18.3 g,其物质的量为0.1 mol,Co元素质量为5.9 g,C
2 4 2
点钴氧化物质量为8.03 g,氧化物中氧元素质量为8.03 g-5.9 g=2.13 g,则氧化物中Co原子与O原子物质
的量之比为0.1 mol∶ ≈3∶4,故C点Co氧化物为Co O ;B点对应物质的质量为14.7 g,与其起始物
3 4
质的质量相比减少18.3 g-14.7 g=3.6 g,为结晶水的质量,故B点物质为CoC O ,与氧气反应生成Co O 与
2 4 3 4
二氧化碳,反应方程式为3CoC O+2O Co O+6CO 。(2)由电子守恒,n(Co3+)=2n(Cl )=2× =0.4
2 4 2 3 4 2 2mol,由电荷守恒,n(Co) =n(Co2+) = n(Cl-)= ×(0.48 L×5 mol/L-2× )=1 mol,所以固体中的
总 溶液
n(Co2+)=1 mol-0.4 mol=0.6 mol,根据化合物中元素正负化合价代数和为 0,氧化物中 n(O)=
=1.2 mol,故该钴氧化物中 n(Co)∶n(O)=1 mol∶1.2 mol=5∶6,则该钴氧化物的化学式为
Co O。
5 6
高频考点五 工艺流程中化学方程式的书写
例5.(2021·全国甲卷)碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方面。回答
下列问题:
(1)I 的一种制备方法如下图所示:
2
① 加入Fe粉进行转化反应的例子方程式为___________________________________,生成的沉淀与硝
酸反应,生成___________后可循环使用。
② 通入Cl 的过程中,若氧化产物只有一种,反应的方程式为________________________;若反应物
2
用量比为n(Cl )/n(FeI )=1.5时,氧化产物为______________,当n(Cl )/n(FeI )>1.5后,单质碘的收率会降
2 2 2 2
低,原因是_____________________________________。
(2)以NaIO 为原料制备I 的方法是:先向NaIO 溶液中加入计量的NaHSO,生成碘化物:再向混
3 2 3 3
合溶液中加入NaIO 溶液,反应得到I,上述制备I 的总离子反应方程式为
3 2 2
__________________________。
(3)KI溶液和CuSO 溶液混合可生成CuI沉淀和I,若生成1mol I ,消耗的KI至少______mol。I 在
4 2 2 2
KI溶液中可发生反应:I+ I- I-。实验室使用过量的KI与CuSO 溶液反应后,过滤,滤液经水蒸气蒸馏
2 3 4
克制得高纯碘。反应中加入过量KI的原因是________________________________________。
【答案】
(1)①Fe +2AgI==2Ag+Fe2++2I-;AgNO ②Cl +FeI ==I +FeCl ;I 和FeCl ;I 被进一步氧化
3 2 2 2 2 2 3 2
(2)2IO -+5HSO - ==I +5SO2-+3H++H O (3)4 防止I 结晶析出
3 3 2 4 2 2【解析】在净化除氯后的含I海水中加入AgNO 富集后生成AgI悬浊液,再加入Fe粉后,Fe粉与AgI
3
发生置换反应生成Ag单质和FeI;通入C1 使之与I反应即可生成I。
2 2 2
(1)①由分析可知,Fe粉的转化反应为Fe+2AgI==2Ag+Fe2++2I-;生成的沉淀为Ag单质,与HNO
3
反应生成的AgNO 可重复循环利用。
3
②通入Cl 后,溶液中存在I-和Fe2+两种还原剂,但还原性I->Fe2+,I-先参与反应,所以当只有一种氧
2
化产物时,该氧化产物应为 I ,反应方程式为 Cl+FeI ==I +FeCl ;Cl 与FeI 中的I-刚好完全反应时,
2 2 2 2 2 2 2
n(Cl )/n(FeI )=1,I-完全反应后,Cl 与Fe2+反应生成Fe3+,此时n(Cl )/n(FeI )=0.5,所以n(Cl )/n(FeI )=1.5
2 2 2 2 2 2 2
时,FeI 刚好完全反应,此时的氧化产物有两种,分别为I 和FeCl ;当n(Cl )/n(FeI )>1.5时,生成的I 会
2 2 3 2 2 2
被Cl 继续氧化生成IO -,造成I 的收率降低。
2 3 2
(2)IO -加入NaHSO 后生成的碘化物为I-,再加入NaIO 后生成I ,所以总反应为IO -与NaHSO 反
3 3 3 2 3 3
应生成I、SO 2-、H+和HO,反应方程式为2IO -+5HSO -==I+5SO2-+3H++H O。
2 4 2 3 3 2 4 2
(3)KI溶液与CuSO 溶液反应生成CuI沉淀和 I ,反应方程式为2CuSO +4KI==I +2CuI↓,所以生成
4 2 4 2
1molI 时消耗的KI至少为4mol;反应中加入过量的KI可使生成的I 转化成I-,以防止I 结晶析出。
2 2 3 2
【变式探究】(2020·山东卷)用软锰矿(主要成分为MnO ,含少量Fe O、Al O)和BaS制备高纯
2 3 4 2 3
MnCO 的工艺流程如下:
3
已知:MnO 是一种两性氧化物;25℃时相关物质的K 见下表。
2 sp
物质 Fe(OH) Fe(OH) Al(OH) Mn(OH)
2 3 3 2
K
sp
回答下列问题:
(1)软锰矿预先粉碎的目的是____________________________,MnO 与BaS溶液反应转化为MnO的化
2
学方程式为________________________________________________________________。
(2)保持BaS投料量不变,随MnO 与BaS投料比增大,S的量达到最大值后无明显变化,而Ba(OH)
2 2
的量达到最大值后会减小,减小的原因是________________________。(3)滤液I可循环使用,应当将其导入到________________________操作中(填操作单元的名称)。
(4)净化时需先加入的试剂X为________________(填化学式)。再使用氨水调溶液的pH,则pH的理论
最小值为_______________(当溶液中某离子浓度 时,可认为该离子沉淀完全)。
(5)碳化过程中发生反应的离子方程式为______________________。
【答案】(1)增大接触面积,充分反应,提高反应速率
(2)过量的MnO 消耗了产生的Ba(OH) (3) 蒸发 (4).H O 4.9
2 2 2 2
(5)Mn2++HCO-+NH·H O=MnCO ↓+NH++H O
3 3 2 3 4 2
【解析】软锰矿粉(主要成分为MnO ,含少量Fe O、Al O)加入硫化钡溶液进行反应,主要发生
2 3 4 2 3
MnO +BaS+H O=Ba(OH) +MnO+S,过滤得到Ba(OH) 溶液,经蒸发结晶、过滤、干燥得到氢氧化钡;滤
2 2 2 2
渣用硫酸溶解,得到的滤液中主要金属阳离子有Mn2+、Fe2+、Fe3+、Al3+,得到的滤渣为不溶于稀硫酸的硫
磺;之后向滤液中加入合适的氧化剂将Fe2+转化为Fe3+,然后加入氨水调节pH,使Fe3+、Al3+转化为沉淀
除去,压滤得到的废渣为Fe(OH) 和Al(OH) ,此时滤液中的金属阳离子只有Mn2+,向滤液中加入碳酸氢
3 3
铵、氨水,Mn2+和碳酸氢根电离出的碳酸根结合生成碳酸锰沉淀,过滤、洗涤、干燥得到高纯碳酸锰。
(1)软锰矿预先粉碎可以增大反应物的接触面积,使反应更充分,提高反应速率;MnO 与BaS反应转
2
化为MnO,Mn元素的化合价由+4价降低为+2价,根据元素价态规律可知-2价的S元素应被氧化得到S单
质,则MnO 与BaS的系数比应为1:1,根据后续流程可知产物还有Ba(OH) ,结合元素守恒可得化学方
2 2
程式为:MnO +BaS+H O=Ba(OH) +MnO+S;
2 2 2
(2)根据题目信息可知MnO 为两性氧化物,所以当MnO 过量时,会消耗反应产生的Ba(OH) ,从而使
2 2 2
Ba(OH) 的量达到最大值或会减小;
2
(3)滤液I为结晶后剩余的Ba(OH) 饱和溶液,所以可以导入到蒸发操作中循环使用;
2
(4)净化时更好的除去Fe元素需要将Fe2+氧化为Fe3+,为了不引入新的杂质,且不将Mn元素氧化,加
入的试剂X可以是HO;根据表格数据可知,Fe(OH) 和Al(OH) 为同种沉淀,而Al(OH) 的K 稍大,所
2 2 3 3 3 sp
以当Al3+完全沉淀时,Fe3+也一定完全沉淀,当c(Al3+)=1.0×10-5mol/L时,c(OHˉ)=
=10-9.1mol/L,所以c(H+)=10-4.9mol/L,pH=4.9,即pH的理论最小值
为4.9;
(5)碳化过程Mn2+和碳酸氢根电离出的碳酸根结合生成碳酸锰沉淀,促进碳酸氢根的电离,产生的氢离子和一水合氨反应生成铵根和水,所以离子方程式为Mn2++HCO-+NH·H O=MnCO ↓+NH++H O。
3 3 2 3 4 2
【举一反三】(2019·全国卷Ⅰ)硼酸(H BO)是一种重要的化工原料,广泛应用于玻璃、医药、肥料
3 3
等工业。一种以硼镁矿(含MgB O·H O、SiO 及少量Fe O、Al O)为原料生产硼酸及轻质氧化镁的工艺流
2 2 5 2 2 2 3 2 3
程如下:
在“沉镁”中生成Mg(OH) ·MgCO 沉淀的离子方程式为
2 3
_______________________________________。
【解析】“沉镁”中,碳酸铵溶液与硫酸镁溶液发生相互促进水解反应生成碱式碳酸镁:2MgSO +
4
2(NH )CO+HO===Mg(OH) ·MgCO ↓+2(NH )SO +CO↑,或者反应生成碱式碳酸镁和碳酸氢盐。母液
4 2 3 2 2 3 4 2 4 2
含硫酸铵,可以将母液返回“溶浸”工序循环使用,体现绿色化学理念和环境保护思想。碱式碳酸镁转化
成轻质氧化镁,联系碳酸镁、氢氧化镁受热都能分解生成氧化镁,也可以联系碱式碳酸铜分解生成氧化
铜、水和二氧化碳,可知采用的方法是高温焙烧法,MgCO ·Mg(OH) =====2MgO+HO+CO↑。
3 2 2 2
【答案】2Mg2++3CO+2HO===Mg(OH) ·MgCO ↓+2HCO[或2Mg2++2CO+HO===
2 2 3 2
Mg(OH) ·MgCO ↓+CO↑]
2 3 2
【变式探究】(2019·全国卷Ⅱ)以重晶石(BaSO)为原料,可按如下工艺生产立德粉:
4
①在回转炉中重晶石被过量焦炭还原为可溶性硫化钡,该过程的化学方程式为
________________________________________________________________________。
回转炉尾气中含有有毒气体,生产上可通过水蒸气变换反应将其转化为CO 和一种清洁能源气体,该
2
反应的化学方程式为______________________________。
②在潮湿空气中长期放置的“还原料”,会逸出臭鸡蛋气味的气体,且水溶性变差,其原因是“还原
料”表面生成了难溶于水的________(填化学式)。
③沉淀器中反应的离子方程式为____________________________________。
【解析】①由流程图中经浸出槽后得到净化的BaS溶液以及回转炉尾气中含有有毒气体可知,在回转
炉中BaSO 与过量的焦炭粉反应生成可溶性的BaS和CO;生产上可通过水蒸气变换反应除去回转炉中的
4
有毒气体CO,即CO与HO反应生成CO 和H。②所得“还原料”的主要成分是BaS,BaS在潮湿空气中
2 2 2
长期放置能与空气中的HO反应生成具有臭鸡蛋气味的HS气体,“还原料”的水溶性变差,表明其表面
2 2生成了难溶性的BaCO 。③结合立德粉的成分可写出沉淀器中S2-、Ba2+、Zn2+、SO反应生成ZnS·BaSO
3 4
的离子方程式。
【答案】①BaSO+4C=============BaS+4CO↑ CO+HO===CO +H ②BaCO
4 2 2 2 3
③S2-+Ba2++Zn2++SO===ZnS·BaSO ↓
4