文档内容
主题二 元素及其化合物
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Cl-35.5 Na-23 K-39 Cr-52 Mn-55
Fe 56 Cu 64
第Ⅰ卷(选择题 共42分)
一、选择题(本题共14个小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合
题目要求的)
1.下列关于物质制备原理说法错误的是( )
A.工业制备金属钠:2NaCl(熔融)=====2Na+Cl↑
2
B.工业生产铁:Fe O+3CO=====2Fe+3CO
2 3 2
C.湿法炼铜:Fe+CuSO ===Cu+FeSO
4 4
D.以S为原料,工业生产硫酸在沸腾炉中的反应:2S+3O2SO
2 3
2.在给定的条件下,下列选项所示的物质间转化均能一步实现的是
A.
B.
C.
D.
3.实验室常用KSCN溶液检验Fe3+,可用K[Fe(CN) ]溶液检验Fe2+,现象为产生深蓝色沉淀。下列说
3 6
法正确的是( )
A.KSCN与K[Fe(CN) ]中C的化合价均为+4
3 6
B.上述元素中,金属性最强和非金属性最强的分别是K、N
C.若溶液中含有Fe3+,滴加KSCN溶液后会产生血红色沉淀
D.HS的相对分子质量大于HO的,因此熔沸点:HS>HO
2 2 2 2
4.NaCO 和NaHCO 是常见的两种钠盐,它们广泛应用于生产和生活中。下列有关碳酸钠和碳酸氢
2 3 3
钠的说法中,不正确的是( )
A.小苏打能中和胃酸,对胃壁不产生强烈的刺激或腐蚀作用,可用于治疗胃酸过多症B.NaHCO 能中和面粉发酵后产生的酸,并且产生二氧化碳气体,可用于做馒头
3
C.可以用澄清石灰水来鉴别NaCO 溶液和NaHCO 溶液
2 3 3
D.往NaCO 饱和溶液中通入CO 气体,可获得NaHCO 沉淀
2 3 2 3
5.利用自然资源制备相关化学物质,下列化学工艺不可行的是( )
A.提取食盐后母液――→含Br 的液体――→――→粗溴――→纯溴
2
B.石英砂――→粗硅――→粗四氯化硅――→――→高纯硅
C.FeS――→SO ――→HSO ――→HSO
2 2 2 3 2 4
D.铝土矿――→NaAlO 溶液――→Al(OH) ――→Al O――→铝
2 3 2 3
6.下列关系图中,A是一种正盐,B是气态氢化物,C是单质,F是强酸。当X无论是强酸还是强碱
时都有如下转化关系(其他反应产物及反应所需条件均已略去)。当X是强碱时, B能使湿润的红色石蕊试
纸变蓝。下列说法中不正确的是( )
O
2
A.当X是强酸时,A、B、C、D、E、F中均含同一种元素,F可能是HSO
2 4
B.当X是强碱时,A、B、C、D、E、F中均含同一种元素,F是HNO
3
C.B和Cl 的反应是氧化还原反应
2
D.当X是强酸时,C在常温下是气态单质
7.甲、乙、丙、丁均为中学化学常见的物质,它们之间的转化关系如图(反应条件及其他产物已略去)。
下列说法不正确的是( )
A.若甲是AlCl 溶液,则丁可能是NaOH溶液 B.若甲是Fe,则丁可能是Cl
3 2
C.若丁是CO,则甲可能为Mg D.若丁是O,则乙、丙的相对分子质量可能相差16
2 2
8.无氧条件下,锌还原亚硫酸氢钠可以得到连二亚硫酸钠(Na SO)。造纸工业中NaSO 用作漂白剂,
2 2 4 2 2 4
可将部分有色物质还原为无色物质,提高纸浆白度。下列关于NaSO 的性质推测不合理的是( )
2 2 4
A.NaSO 具有较强的还原性
2 2 4
B.NaSO 与盐酸反应可能生成S和SO
2 2 4 2
C.NaSO 的漂白原理与NaClO不相同
2 2 4
D.NaSO 的水溶液久置于空气中,溶液呈碱性
2 2 4
9.关于化合物(NH )Cr O 的性质,下列推测合理的是( )
4 2 2 7
A.(NH )Cr O 固体受热分解产物可能为CrO、NH 、N 和HO
4 2 2 7 3 3 2 2
B.在(NH )Cr O 溶液中滴加足量浓KOH溶液时只发生离子反应:NH ++OH-=NH↑+H O
4 2 2 7 4 3 2C.若一定条件下(NH )Cr O 溶液与HO 反应生成CrO(Cr为+6价),推测CrO 可能具有分子稳定性
4 2 2 7 2 2 5 5
差,易分解的性质
D.用浓盐酸酸化(NH )Cr O 溶液,会使平衡Cr O2-+H O 2CrO2-+2H+逆向移动,溶液由黄色
4 2 2 7 2 7 2 4
(或橙黄色)变为橙色
10.下列“类比”合理的是( )
A.由O+2H S=S+2H O,说明非金属性O>S,推测:高温下2C+ SiO = Si+2CO,非金属性C>Si
2 2 2 2
B.由CO+Ca(ClO) +H O=CaCO ↓+2HClO推测:SO +Ca(ClO) +H O=CaSO↓+2HClO
2 2 2 3 2 2 2 3
C.Fe与S在加热条件下反应生成FeS,推测:Cu与S在加热条件下生成CuS
D.由NaSO +2HCl=2NaCl+H O+SO ↑,推测:NaSO +H SO =Na SO +H O+SO ↑
2 3 2 2 2 3 2 4 2 4 2 2
11.已知氯磺酸(ClSOH)是极易水解的一元强酸,下列推测不合理的是( )
3
A.ClSOH与足量氢氧化钠溶液反应能生成两种盐
3
B.相同条件下,ClSOH比FSO H更容易水解
3 3
C.ClSOH的制备可以用HCl与SO 反应,也可用浓盐酸和浓HSO 反应制得
3 3 2 4
D.相同条件下,等物质的量的ClSOH和HCl分别溶于水制成1L溶液,两者pH不同
3
12.中学常见的某反应的化学方程式为a+b→c+d+H O(未配平,条件略去)。下列叙述不正确的是( )
2
A.若a是铁,b是稀硝酸(过量),且a可溶于c溶液中。则a与b反应的离子方程式为Fe+4H++NO-
3
=Fe3++NO↑+2HO
2
B.若c、d均为气体,且都能使澄清石灰水变浑浊,则将混合气体通入溴水中,橙色褪去,其褪色过
程的离子方程式为SO +Br +2H O=4H++SO2-+2Br-
2 2 2 4
C.若a是造成温室效应的主要气体之一,c、d均为钠盐,参加反应的a、b物质的量之比为4:5,则
上述反应的离子方程式为4CO+5OH-=CO 2-+3HCO-+H O
2 3 3 2
D.若c是无色有刺激性气味的气体,其水溶液呈弱碱性。在标准状况下用排空气法收集c气体得平均
摩尔质量为20g•mol-1的混合气体进行喷泉实验。假设溶质不扩散,实验完成后所得溶液的物质的量浓度约
为0.056mol•L-1
13.某兴趣小组将过量Cu与FeCl 溶液充分及应,静置后取上层清液于试管中,将KSCN溶液滴加到
3
清液中,观察到瞬间产生白色沉淀,局部出现红色;振荡试管,红色又迅速褪去。已知:
①CuCl +Cu=2CuCl↓(白色)——该反应速率很慢
2
②2CuCl +4KSCN=2CuSCN↓(白色)+(SCN) +4KCl——该反应速率很快
2 2
③(SCN) 是拟卤素,化学性质和氯气相似
2
下列说法正确的是( )
A.用KSCN溶液检验Fe3+时,Cu2+的存在不会对检验产生干扰B.局部出现红色主要是因为溶液中的Fe2+被空气中的O 氧化成Fe3+,Fe3+与KSCN反应生成Fe(SCN)
2 3
C.白色沉淀是CuCl,是溶液中CuCl 与Cu反应生成的
2
D.红色迅速褪去的原因是振荡试管时Cu2+与SCN-发生反应,从而使Fe3++3SCN- ⇌Fe(SCN)
3
平衡逆移
14.在探究FeSO 和Cu(NO ) 的混合物中各组分含量的过程中,进行了如下实验,下列说法错误的是(
4 3 2
)
A.反应②中铁粉过量,V=2240
B.固体中有铁粉和铜粉,m=0.68
C.原混合物中FeSO 和Cu(NO ) 的物质的量之比为5:1
4 3 2
D.①发生的反应为Cl+2Fe2+=2Cl-+2Fe3+,n=0.02
2
第II卷(非选择题 共58分)
二、填空题(本题共4小题,共58分)
15.(14分)氮、氧、硫、氯是四种重要的非金属元素,研究它们的性质及用途对生产,生活、科研具
有重要意义。
(1)一氯胺(NH Cl)是一种长效缓释水消毒剂,工业上可利用反应NHI (g)+Cl (g)=NH Cl(g)+HCl(g)制备。
2 3 2 2
①一氯胺(NH Cl)在中性或酸性环境中会发生水解反应,生成一种具有强烈杀菌作用的物质,该物质的
2
电子式为___________。
②氨气也是工业上制备硝酸的主要原料,制备硝酸的过程中涉及NO 与水的反应。该反应中氧化剂与
2
还原剂的物质的量之比为___________。
(2)SO 、NO 两种气体都能对大气造成污染,需要对其进行吸收处理。用氨水吸收SO 能得到含
2 2 2
(NH )SO 和NH HSO 的吸收液,写出生成(NH )SO 的离子方程式:___________。若向吸收液中通入过
4 2 3 4 3 4 2 3
量NO ,NH HSO 能与NO 发生反应生成N 和(NH )SO ,写出该反应的离子方程式:___________。
2 4 3 2 2 4 2 4
(3)Cl 与NaOH溶液反应可制取“84”消毒液。用过量的冷NaOH溶液吸收氯气,制得NaClO溶液(不
2
含NaClO,),此时ClO-的浓度为c mol/L;加热时NaClO能转化为NaClO,测得t时刻溶液中ClO-的浓
3 0 3
度为c mol/L (不考虑加热前后溶液体积的变化)。
1
①写出溶液中NaClO分解生成NaClO 的化学方程式:___________。
3
②t时刻溶液中c(Cl-)=___________mol/L(用含c、c 的代数式表示)。
0 1
(4)S N(S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质NH 通入
4 4 3SCl 的CCl 浓液中,可制得该物质:6 S Cl+16NH=S N+S +12NHCl (已知S 是硫单质中最稳定的)。
2 2 4 2 2 3 4 4 8 4 8
①上述制备反应中被氧化的元素是_______(填元素符号),物质NH 体现的性质有_______。
3
②S N 在常温下较稳定,但撞击或加热时会引起爆炸,生成非常稳定的单质产物,该爆炸反应的化学
4 4
方程式是_______。
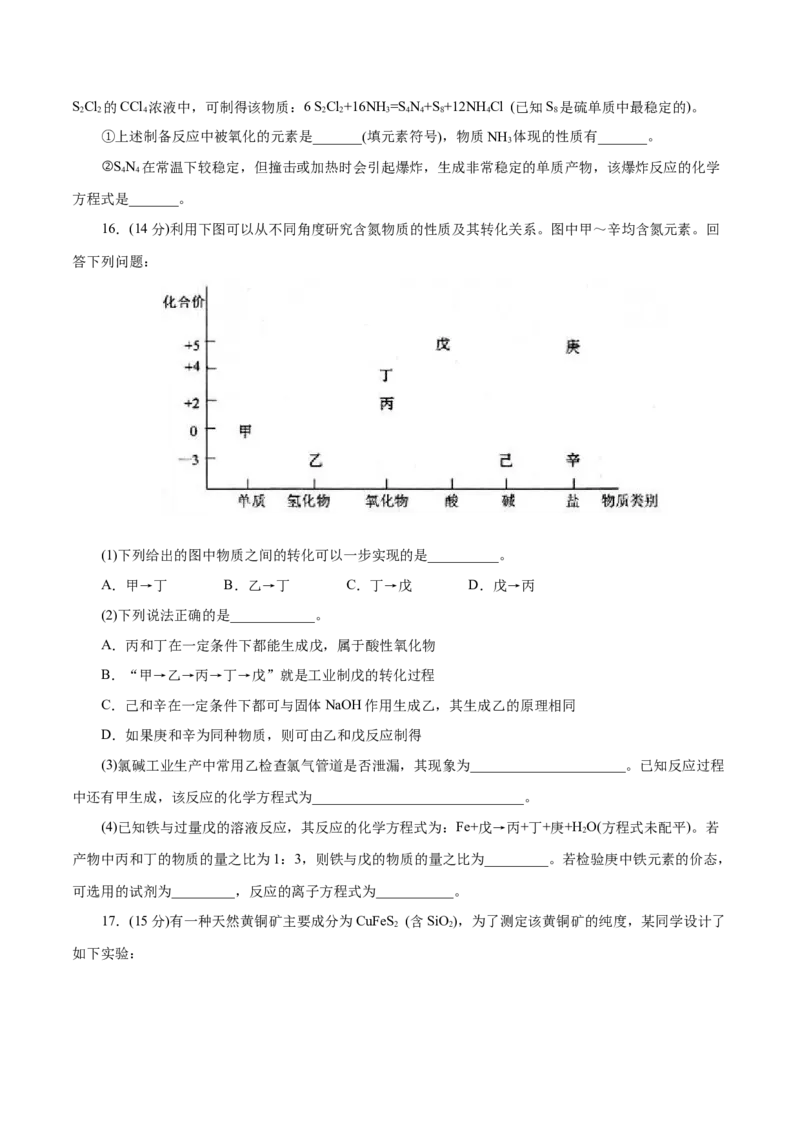
16.(14分)利用下图可以从不同角度研究含氮物质的性质及其转化关系。图中甲~辛均含氮元素。回
答下列问题:
(1)下列给出的图中物质之间的转化可以一步实现的是__________。
A.甲→丁 B.乙→丁 C.丁→戊 D.戊→丙
(2)下列说法正确的是____________。
A.丙和丁在一定条件下都能生成戊,属于酸性氧化物
B.“甲→乙→丙→丁→戊”就是工业制戊的转化过程
C.己和辛在一定条件下都可与固体NaOH作用生成乙,其生成乙的原理相同
D.如果庚和辛为同种物质,则可由乙和戊反应制得
(3)氯碱工业生产中常用乙检查氯气管道是否泄漏,其现象为______________________。已知反应过程
中还有甲生成,该反应的化学方程式为______________________________。
(4)已知铁与过量戊的溶液反应,其反应的化学方程式为:Fe+戊→丙+丁+庚+H O(方程式未配平)。若
2
产物中丙和丁的物质的量之比为1:3,则铁与戊的物质的量之比为_________。若检验庚中铁元素的价态,
可选用的试剂为_________,反应的离子方程式为___________。
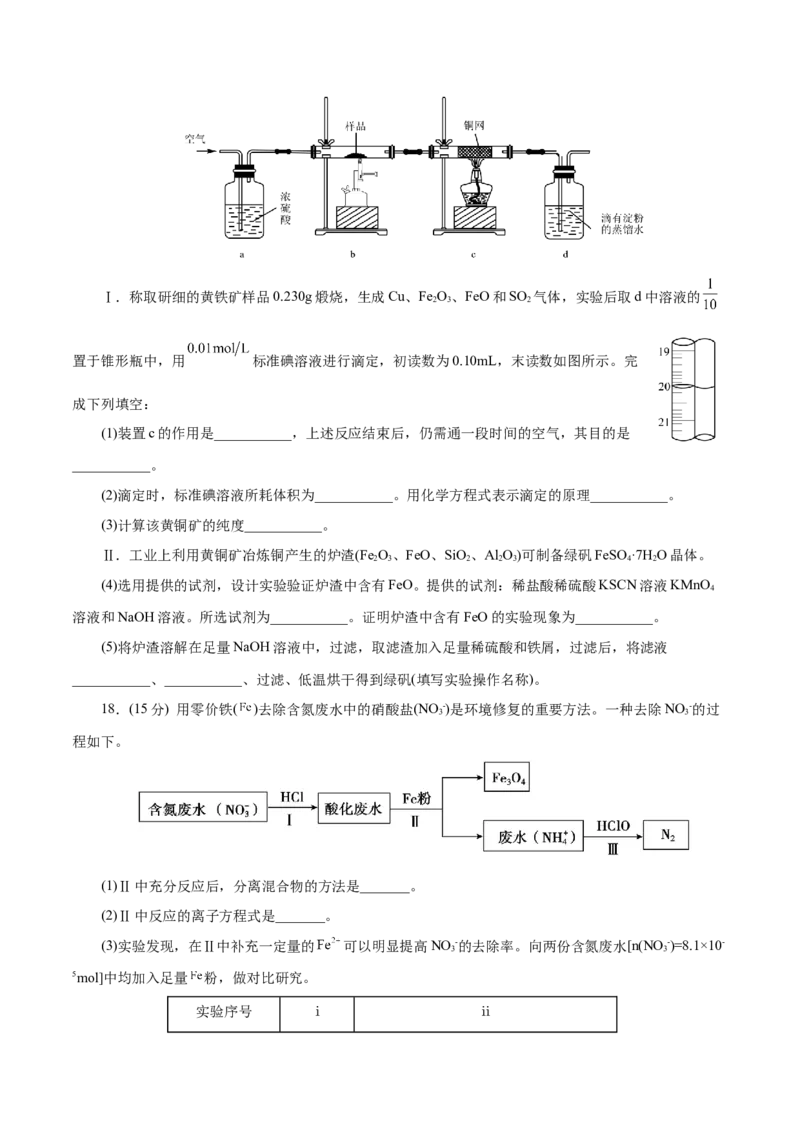
17.(15分)有一种天然黄铜矿主要成分为CuFeS (含SiO),为了测定该黄铜矿的纯度,某同学设计了
2 2
如下实验:Ⅰ.称取研细的黄铁矿样品0.230g煅烧,生成Cu、Fe O、FeO和SO 气体,实验后取d中溶液的
2 3 2
置于锥形瓶中,用 标准碘溶液进行滴定,初读数为0.10mL,末读数如图所示。完
成下列填空:
(1)装置c的作用是___________,上述反应结束后,仍需通一段时间的空气,其目的是
___________。
(2)滴定时,标准碘溶液所耗体积为___________。用化学方程式表示滴定的原理___________。
(3)计算该黄铜矿的纯度___________。
Ⅱ.工业上利用黄铜矿冶炼铜产生的炉渣(Fe O、FeO、SiO、Al O)可制备绿矾FeSO ·7H O晶体。
2 3 2 2 3 4 2
(4)选用提供的试剂,设计实验验证炉渣中含有FeO。提供的试剂:稀盐酸稀硫酸KSCN溶液KMnO
4
溶液和NaOH溶液。所选试剂为___________。证明炉渣中含有FeO的实验现象为___________。
(5)将炉渣溶解在足量NaOH溶液中,过滤,取滤渣加入足量稀硫酸和铁屑,过滤后,将滤液
___________、___________、过滤、低温烘干得到绿矾(填写实验操作名称)。
18.(15分) 用零价铁( )去除含氮废水中的硝酸盐(NO -)是环境修复的重要方法。一种去除NO -的过
3 3
程如下。
(1)Ⅱ中充分反应后,分离混合物的方法是_______。
(2)Ⅱ中反应的离子方程式是_______。
(3)实验发现,在Ⅱ中补充一定量的 可以明显提高NO -的去除率。向两份含氮废水[n(NO -)=8.1×10-
3 3
5mol]中均加入足量 粉,做对比研究。
实验序号 ⅰ ⅱ所加试剂 Fe粉 Fe粉、FeCl (3.6×10-5mol)
2
NO -的去除率 ≈50% ≈100%
3
分析ⅱ中NO -的去除率提高的原因:
3
A. 直接还原NO -了。
3
通过计算说明电子得、失数量关系:_______,证明该原因不合理。
B.研究发现:Fe O (导电)覆盖在铁粉表面;随着反应的进行,产生 (不导电),它覆盖在
3 4
Fe O 表面,形成钝化层,阻碍电子传输。
3 4
C. Fe2+能与FeO(OH)反应生成Fe O。
3 4
用57FeCl 做同位素示踪实验,证明该原因合理。
2
D. Cl-破坏钝化层。
将ⅱ中的FeCl 替换为_______,NO -的去除率约为50%,证明该原因不合理。
2 3
(4)ⅰ、ⅱ中均能发生Fe+2H+=Fe2++H ↑。该反应明显有助于ⅰ中NO -的去除,结合方程式解释原因:
2 3
_______。
(5)测定NO -含量
3
步骤1.取vmL含氮(NO -)水样,加入催化剂、v mLcmol·L-1FeSO 标准溶液(过量),再加入稀HSO 。
3 1 1 4 2 4
步骤2.用cmol·L-1KCrO 标准溶液滴定剩余的Fe2+ ( CrO2-被还原为Cr3+),终点时消耗v mL。
2 2 2 7 2 7 2
已知:3Fe2++NO-+4H+=3Fe2++NO↑+2HO
3 2
①水样中NO -的含量为_______ 。
3
②溶液中O 影响测定。向步骤1中加入适量NaHCO ,产生CO 驱赶O,否则会使测定结果
2 3 2 2
_______(填“偏大”或“偏小”)。