文档内容
主题四 化学工艺流程测试(一)
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Cl-35.5 Na-23 K-39 Cr-52 Mn-55
第Ⅰ卷(选择题 共45分)
一、选择题(本题共15个小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合
题目要求的)
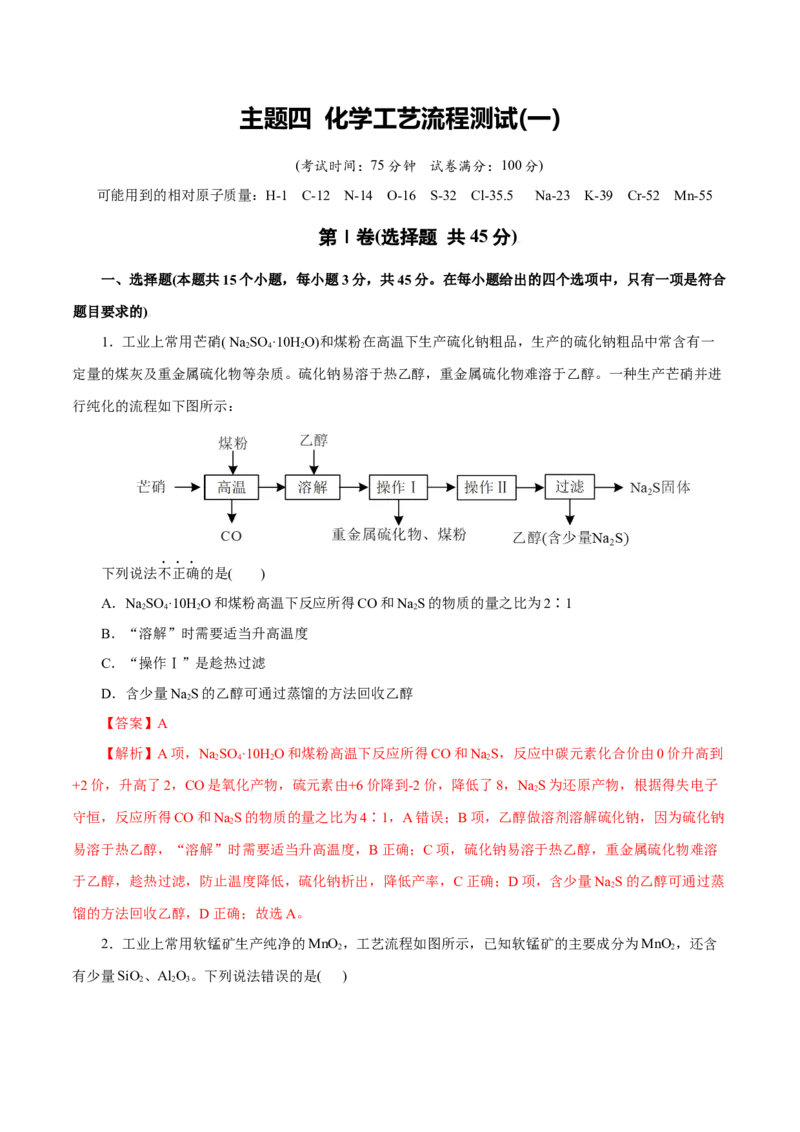
1.工业上常用芒硝( Na SO ·10H O)和煤粉在高温下生产硫化钠粗品,生产的硫化钠粗品中常含有一
2 4 2
定量的煤灰及重金属硫化物等杂质。硫化钠易溶于热乙醇,重金属硫化物难溶于乙醇。一种生产芒硝并进
行纯化的流程如下图所示:
下列说法不正确的是( )
A.NaSO ·10H O和煤粉高温下反应所得CO和NaS的物质的量之比为2∶1
2 4 2 2
B.“溶解”时需要适当升高温度
C.“操作Ⅰ”是趁热过滤
D.含少量NaS的乙醇可通过蒸馏的方法回收乙醇
2
【答案】A
【解析】A项,NaSO ·10H O和煤粉高温下反应所得CO和NaS,反应中碳元素化合价由0价升高到
2 4 2 2
+2价,升高了2,CO是氧化产物,硫元素由+6价降到-2价,降低了8,NaS为还原产物,根据得失电子
2
守恒,反应所得CO和NaS的物质的量之比为4∶1,A错误;B项,乙醇做溶剂溶解硫化钠,因为硫化钠
2
易溶于热乙醇,“溶解”时需要适当升高温度,B正确;C项,硫化钠易溶于热乙醇,重金属硫化物难溶
于乙醇,趁热过滤,防止温度降低,硫化钠析出,降低产率,C正确;D项,含少量NaS的乙醇可通过蒸
2
馏的方法回收乙醇,D正确;故选A。
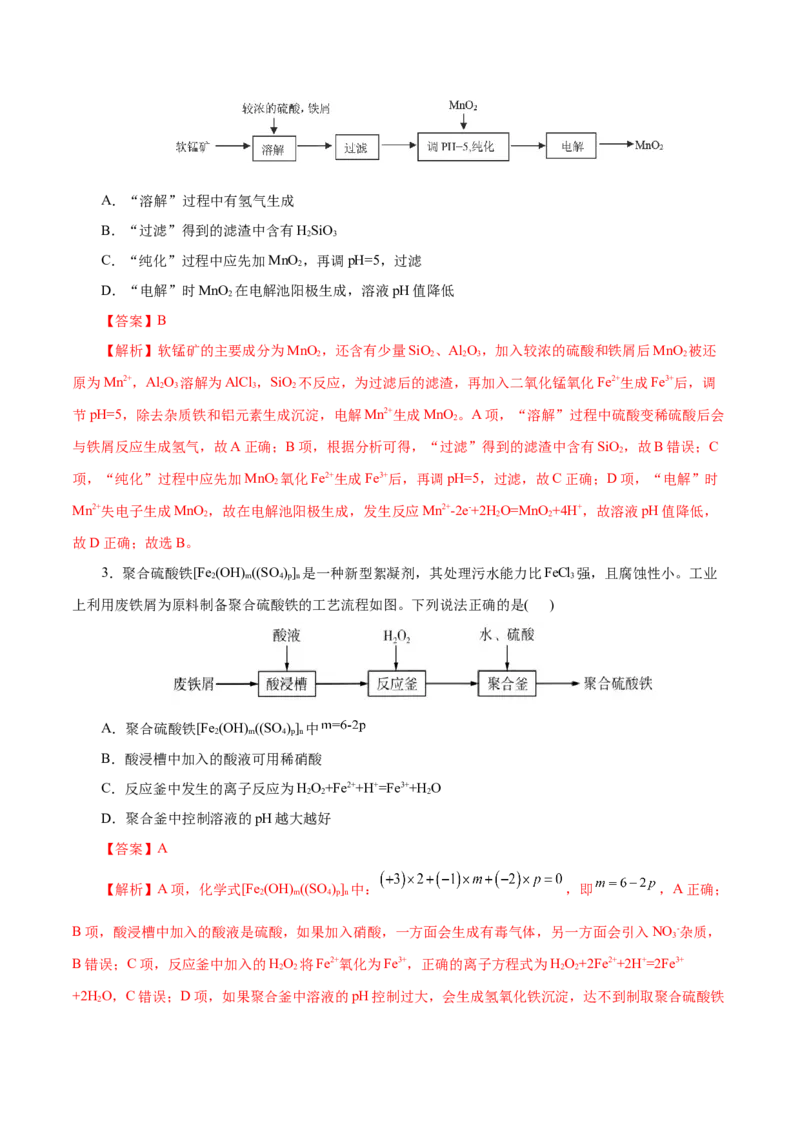
2.工业上常用软锰矿生产纯净的MnO ,工艺流程如图所示,已知软锰矿的主要成分为MnO ,还含
2 2
有少量SiO、Al O。下列说法错误的是( )
2 2 3A.“溶解”过程中有氢气生成
B.“过滤”得到的滤渣中含有HSiO
2 3
C.“纯化”过程中应先加MnO ,再调pH=5,过滤
2
D.“电解”时MnO 在电解池阳极生成,溶液pH值降低
2
【答案】B
【解析】软锰矿的主要成分为MnO ,还含有少量SiO、Al O,加入较浓的硫酸和铁屑后MnO 被还
2 2 2 3 2
原为Mn2+,Al O 溶解为AlCl ,SiO 不反应,为过滤后的滤渣,再加入二氧化锰氧化Fe2+生成Fe3+后,调
2 3 3 2
节pH=5,除去杂质铁和铝元素生成沉淀,电解Mn2+生成MnO 。A项,“溶解”过程中硫酸变稀硫酸后会
2
与铁屑反应生成氢气,故A正确;B项,根据分析可得,“过滤”得到的滤渣中含有SiO,故B错误;C
2
项,“纯化”过程中应先加MnO 氧化Fe2+生成Fe3+后,再调pH=5,过滤,故C正确;D项,“电解”时
2
Mn2+失电子生成MnO ,故在电解池阳极生成,发生反应Mn2+-2e-+2H O=MnO +4H+,故溶液pH值降低,
2 2 2
故D正确;故选B。
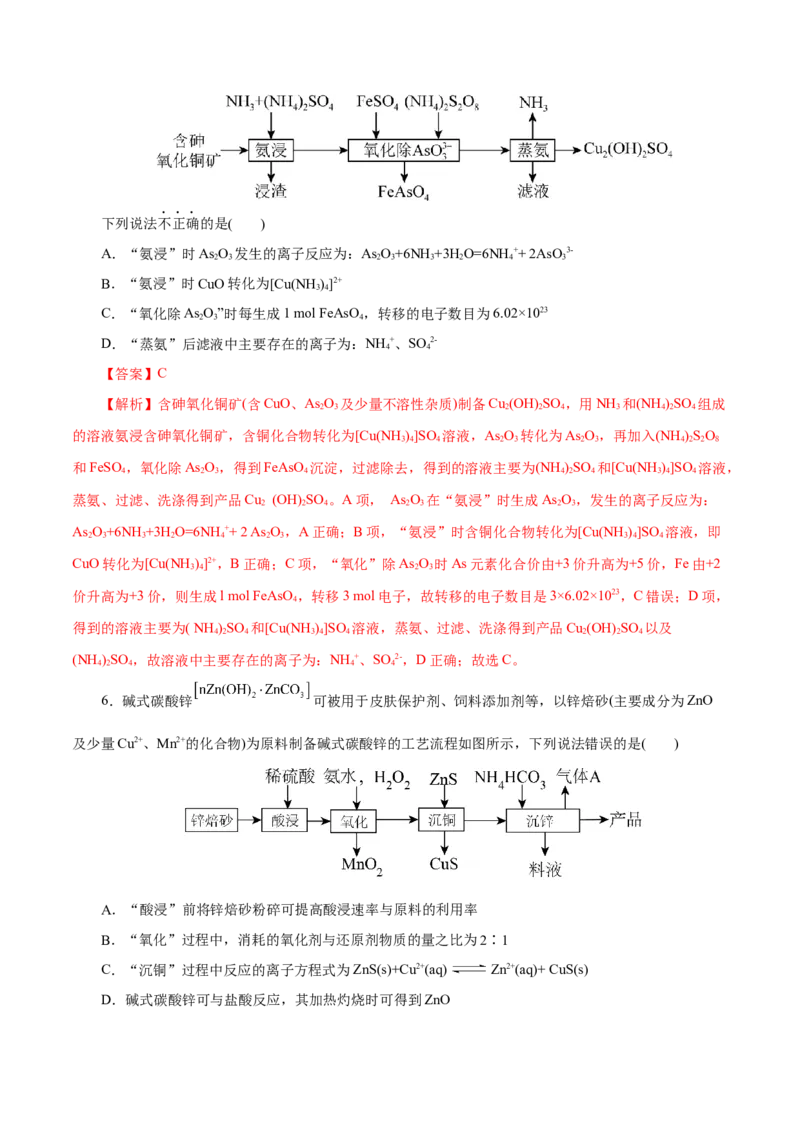
3.聚合硫酸铁[Fe (OH) ((SO )] 是一种新型絮凝剂,其处理污水能力比FeCl 强,且腐蚀性小。工业
2 m 4 p n 3
上利用废铁屑为原料制备聚合硫酸铁的工艺流程如图。下列说法正确的是( )
A.聚合硫酸铁[Fe (OH) ((SO )] 中
2 m 4 p n
B.酸浸槽中加入的酸液可用稀硝酸
C.反应釜中发生的离子反应为HO+Fe2++H+=Fe3++H O
2 2 2
D.聚合釜中控制溶液的pH越大越好
【答案】A
【解析】A项,化学式[Fe (OH) ((SO )] 中: ,即 ,A正确;
2 m 4 p n
B项,酸浸槽中加入的酸液是硫酸,如果加入硝酸,一方面会生成有毒气体,另一方面会引入NO -杂质,
3
B错误;C项,反应釜中加入的HO 将Fe2+氧化为Fe3+,正确的离子方程式为HO+2Fe2++2H+=2Fe3+
2 2 2 2
+2H O,C错误;D项,如果聚合釜中溶液的pH控制过大,会生成氢氧化铁沉淀,达不到制取聚合硫酸铁
2的目的,D错误;故选A。
4.一种以辉钼矿(主要成分是MoS ,还含有NiS、PbS、SiO 和Fe的氧化物等杂质)为原料生产四钼酸
2 2
铵晶体[(NH )MoO •2H O]的工艺流程如图所示。
4 2 4 13 2
已知:“酸浸”时,MoO 转化为MoO 2+;“除杂”后钼元素以MoO 2-存在;Ni3+可将水氧化。
3 2 4
下列说法错误的是( )
A.“焙烧”时产生的尾气可用石灰乳吸收
B.滤渣I的主要成分是SiO,PbSO
2 4
C.“酸浸”时,HO 将Fe2+、Ni2+氧化为Fe3+和Ni3+
2 2
D.“结晶”时,发生的反应为2NH ++4MoO2-+6H+=(NH)MoO •2H O↓+HO
4 4 4 2 4 13 2 2
【答案】C
【解析】辉钼矿(主要成分是MoS ,还含有NiS、PbS、SiO 和Fe的氧化物等杂质)在空气中焙烧,
2 2
MoS 转化为MoO ,PbS转化为PbO,NiS转化为Ni O,加稀硫酸和过氧化氢酸浸,MoO 转化为
2 3 2 3 3
MoO 2+,PbO转化为PbSO ,HO 的作用是将Fe2+转化为Fe3+,Ni O 转化为硫酸镍,过滤得到滤渣I的主
2 4 2 2 2 3
要成分为二氧化硅和硫酸铅;滤液中含有MoO 2+、Ni2+和Fe3+,加入过量浓氨水MoO 2+转化为(NH )MoO
2 2 4 2 4
溶液,Ni2+和Fe3+形成沉淀,过滤得到滤渣II的成分是氢氧化镍和氢氧化铁;滤液中加入稀硫酸调pH=
5.5,结晶析出四钼酸铵晶体,经一系列操作得到四钼酸铵晶体。A项,“焙烧”时生成二氧化硫气体,石
灰乳为氢氧化钙,可用石灰乳吸收二氧化硫,故A正确;B项,滤渣I的主要成分是SiO,PbSO ,故B正
2 4
确;C项,“酸浸”时,HO 将Fe2+氧化为Fe3+,故C错误;D项,“结晶”时,滴加稀硫酸与过量的浓
2 2
氨水反应,将(NH )MoO 溶液转化为四钼酸铵晶体,发生的反应为2NH ++4MoO2-
4 2 4 4 4
+6H+=(NH)MoO •2H O↓+HO,故D正确;故选C。
4 2 4 13 2 2
5.弱碱性条件下,利用含砷氧化铜矿(含CuO、As O 及少量不溶性杂质)制备Cu (OH) SO 的工艺流
2 3 2 2 4
程如图:下列说法不正确的是( )
A.“氨浸”时As O 发生的离子反应为:As O+6NH+3H O=6NH ++ 2AsO3-
2 3 2 3 3 2 4 3
B.“氨浸”时CuO转化为[Cu(NH )]2+
3 4
C.“氧化除As O”时每生成1 mol FeAsO ,转移的电子数目为6.02×1023
2 3 4
D.“蒸氨”后滤液中主要存在的离子为:NH +、SO 2-
4 4
【答案】C
【解析】含砷氧化铜矿(含CuO、As O 及少量不溶性杂质)制备Cu (OH) SO ,用NH 和(NH )SO 组成
2 3 2 2 4 3 4 2 4
的溶液氨浸含砷氧化铜矿,含铜化合物转化为[Cu(NH )]SO 溶液,As O 转化为As O,再加入(NH )SO
3 4 4 2 3 2 3 4 2 2 8
和FeSO ,氧化除As O,得到FeAsO 沉淀,过滤除去,得到的溶液主要为(NH )SO 和[Cu(NH )]SO 溶液,
4 2 3 4 4 2 4 3 4 4
蒸氨、过滤、洗涤得到产品Cu (OH) SO 。A项, As O 在“氨浸”时生成As O,发生的离子反应为:
2 2 4 2 3 2 3
As O+6NH+3H O=6NH ++ 2 As O,A正确;B项,“氨浸”时含铜化合物转化为[Cu(NH )]SO 溶液,即
2 3 3 2 4 2 3 3 4 4
CuO转化为[Cu(NH )]2+,B正确;C项,“氧化”除As O 时As元素化合价由+3价升高为+5价,Fe由+2
3 4 2 3
价升高为+3价,则生成l mol FeAsO ,转移3 mol电子,故转移的电子数目是3×6.02×1023,C错误;D项,
4
得到的溶液主要为( NH)SO 和[Cu(NH )]SO 溶液,蒸氨、过滤、洗涤得到产品Cu (OH) SO 以及
4 2 4 3 4 4 2 2 4
(NH )SO ,故溶液中主要存在的离子为:NH +、SO 2-,D正确;故选C。
4 2 4 4 4
6.碱式碳酸锌 可被用于皮肤保护剂、饲料添加剂等,以锌焙砂(主要成分为ZnO
及少量Cu2+、Mn2+的化合物)为原料制备碱式碳酸锌的工艺流程如图所示,下列说法错误的是( )
A.“酸浸”前将锌焙砂粉碎可提高酸浸速率与原料的利用率
B.“氧化”过程中,消耗的氧化剂与还原剂物质的量之比为2∶1
C.“沉铜”过程中反应的离子方程式为ZnS(s)+Cu2+(aq) Zn2+(aq)+ CuS(s)
D.碱式碳酸锌可与盐酸反应,其加热灼烧时可得到ZnO【答案】B
【解析】锌焙砂加入稀硫酸酸浸将锌、铜、锰转化为相应的盐溶液,加入氨水和过氧化氢生成二氧化
锰沉淀,过滤滤液加入硫化锌将铜离子转化为锌离子和硫化铜,过滤滤液加入碳酸氢铵生成碱式碳酸锌。
A项,“酸浸”前将锌焙砂粉碎可增加反应物接触面积,提高酸浸速率与原料的利用率,A正确;B项,
“氧化”过程中,过氧化氢将二价锰离子氧化为二氧化锰,根据电子守恒可知,HO~2e-~Mn2+,则消耗的
2 2
氧化剂与还原剂物质的量之比为1∶1,B错误;C项,“沉铜”过程中加入硫化锌将铜离子转化为锌离子
和硫化铜,反应的离子方程式为ZnS(s)+Cu2+(aq) Zn2+(aq)+ CuS(s),C正确;D.碱式碳酸锌含有碳
酸根离子和氢氧根离子可与盐酸反应,其加热灼烧时可得到氧化锌、二氧化碳、水,D正确;故选B。
7.重铬酸钠在工业生产上具有广泛用途。一种以铬铁矿(含FeCr O 及少量Al O、SiO 等)为原料制备
2 4 2 3 2
NaCr O 的工艺流程如下:
2 2 7
已知滤渣1为Fe O。下列说法错误的是( )
2 3
A.流程中可循环使用的物质有CO
2
B.滤渣2的成分是Al(OH) 和HSiO
3 2 3
C.“调pH”是向溶液中加NaOH使pH增大,促进氧化还原反应进行
D.“高温焙烧"发生的主要反应为4FeCr O+7O +8Na CO 2Fe O+8Na CrO+CO
2 4 2 2 3 2 3 2 4 2
【答案】C
【解析】铬铁矿在空气中与纯碱高温煅烧,得到含有NaAlO 、NaSiO、NaCrO、Fe O 的固体产物,
2 2 3 2 4 2 3
水浸,Fe O 不溶,滤渣1为Fe O,滤液含有NaAlO 、NaSiO、NaCrO,通入CO 调节pH值使
2 3 2 3 2 2 3 2 4 2
NaAlO 、NaSiO 转化为Al(OH) 和HSiO,则滤渣2为Al(OH) 和HSiO,滤液主要含有NaCrO,再次
2 2 3 3 2 3 3 2 3 2 4
调节pH将CrO2-转化为Cr O2-,得到NaCr O。A项,根据流程可知高温焙烧时产生的CO 可以在除杂过
4 2 7 2 2 7 2
程中再次使用,A正确;B项,根据分析可知通入CO 调节pH值使NaAlO 、NaSiO 转化为Al(OH) 和
2 2 2 3 3
HSiO,滤渣2为Al(OH) 和HSiO,B正确;C项,调节pH的目的是将CrO2-转化为Cr O2-,该过程并
2 3 3 2 3 4 2 7
不是氧化还原反应,C错误;D项,铬铁矿主要成分为FeCr O,而滤渣1为Fe O,说明焙烧过程中
2 4 2 3
Fe(Ⅱ)被氧化为Fe(Ⅲ),同时还有CO 生成,根据电子守恒、元素守恒可得发生的反应为
2
4FeCr O+7O +8Na CO 2Fe O+8Na CrO+CO ,D正确;故选C。
2 4 2 2 3 2 3 2 4 2
8.工业利用含镍废料(以镍铁钙合金为主)制取NiC O(草酸镍),再经高温煅烧NiC O 制取Ni O 的流
2 4 2 4 2 3程如图所示。已知:NiC O、CaC O 均难溶于水;Fe3+完全沉淀的pH约为3.7。下列说法正确的是( )
2 4 2 4
A.酸溶时,可加入大量硫酸来提高“酸溶”效率
B.调pH时,加入NaCO 溶液,目的是使Fe3+转化为Fe (CO) 沉淀
2 3 2 3 3
C.沉镍时,发生反应的离子方程式为:Ni2++C O2-=NiC O↓
2 4 2 4
D.煅烧时,反应的化学方程式为:2NiC O Ni O+3CO↑+CO ↑
2 4 2 3 2
【答案】D
【解析】含镍废料中以镍铁钙合金为主,加入硫酸溶解,得到Ni2+、Fe2+、Ca2+,加入HO 将Fe2+氧化
2 2
成Fe3+,加入碳酸钠调节pH,使Fe3+以氢氧化铁形式除去,加入氟化铵,以氟化钙形式除去,加入草酸,
以NiC O 进行沉镍。A项,加入硫酸不能大量,否则在调pH时消耗较多的碳酸钠,难以调节pH,故A错
2 4
误;B项,调节pH,Fe3+以氢氧化铁形式沉降出来,而除去,故B错误;C项,草酸为弱酸,书写离子方
程式时,以化学式的形式书写,故C错误;D项,煅烧是NiC O 转化成Ni O,Ni的化合价由+2价升高为
2 4 2 3
+3价,因此C的化合价应降低,即化学方程式为2NiC O Ni O+3CO↑+CO ↑,故D正确;故选D。
2 4 2 3 2
9.钪(Sc)可用于制备铝钪合金、燃料电池、钪钠卤灯、示踪剂、激光晶体等产品。以钛白酸性废水
(主要含 、Fe2+、Sc3+)为原料制备氧化钪(ScO)的工艺流程如下。下列说法正确的是( )
2 3
A.酸洗时加入HO 的目的是将Ti 4+还原为Ti2+
2 2
B.“操作Ⅰ”需要的玻璃仪器有分液漏斗
C.“滤渣Ⅰ”的主要成分是Ti (OH)、Fe(OH)
4 3
D.草酸钪焙烧时反应的化学方程式:2Sc(C O)+3O 2ScO+12CO
2 2 4 3 2 2 3 2
【答案】D
【解析】钛白酸性废水(主要含Ti 4+、Fe2+,Sc3+),酸洗时加入HO 的目的是将Fe2+氧化为Fe3+,“滤
2 2
渣Ⅰ”的主要成分是Ti (OH) 、Fe(OH) 、Sc(OH) ,加入10%的盐酸调pH的目的是将Sc(OH) 转化为含,
4 3 3 3Sc3+的溶液,再加入草酸溶液得到草酸钪,草酸钪与氧气焙烧时生成ScO 和CO 。A项,“有机相”中主
2 3 2
要含有Ti 4+、Fe2+,Sc3+,酸洗时加入HO 的目的是将Fe2+氧化为Fe3+,有利于后面沉淀除去Fe3+,A项错
2 2
误;B项,“操作Ⅰ”是过滤,过滤操作需要的玻璃仪器有烧杯、玻璃棒、漏斗,B项错误;C项,“滤
渣Ⅰ”的主要成分是Ti (OH) 、Fe(OH) 、Sc(OH) ,C项错误;D项,草酸钪与氧气焙烧时生成ScO 和
4 3 3 2 3
CO,D项正确;故选D。
2
10.高铁酸钾(K FeO)具有杀菌消毒及净水作用,某实验小组在碱性条件下制备KFeO 流程如图所示:
2 4 2 4
下列说法错误的是( )
A.1molK FeO 消毒能力相当于1.5mol HClO
2 4
B.氧化反应:3NaClO+2Fe(NO )+10 NaOH=2Na FeO+3NaCl+6 NaNO +5H O
3 3 2 4 3 2
C.同温度时高铁酸钠溶解度大于高铁酸钾
D.提纯时,应用到的玻璃仪器有蒸发皿、玻璃棒、烧杯、酒精灯
【答案】D
【解析】A项,1mol次氯酸得2mol电子生成氯离子,1molK FeO 得3mol电子转化为三价铁,故
2 4
1molK FeO 消毒能力相当于1.5mol HClO,A正确;B项,根据得失电子守恒和元素守恒配平方程:
2 4
3NaClO+2Fe(NO )+10 NaOH=2Na FeO+3NaCl+6 NaNO +5H O,B正确;C项,流程图中高铁酸钠加入饱
3 3 2 4 3 2
和氢氧化钾溶液利用同温度时高铁酸钠溶解度大于高铁酸钾可生成高铁酸钾,C正确;D项,提纯时需过
滤,应用到的玻璃仪器有漏斗、玻璃棒、烧杯,D错误;故选D。
11.硫代硫酸钠晶体(NaSO·5H O)不溶于乙醇,可用作纸浆漂白时的脱氯剂等。用工业硫化钠(主要
2 2 3 2
成分NaS,含少量NaSO )及纯碱等为原料制备NaSO·5H O的流程如下:
2 2 4 2 2 3 2
下列说法正确的是( )
A.NaSO 作脱氯剂时主要利用其氧化性
2 2 3
B.“净化”时加入的试剂X可选用BaCl 溶液
2
C.“反应”过程中体系pH大小对产品产率无影响
D.提纯NaSO·5H O时,应先用水洗,再用乙醇洗涤
2 2 3 2【答案】D
【解析】由题给流程可知,向工业硫化钠溶于热水得到的溶液中加入氢氧化钡或硫化钡除去溶液中的
硫酸钠和碳酸钠,趁热过滤得到硫化钠溶液,向溶液中加入碳酸钠溶液后,通入二氧化硫反应得到硫代硫
酸钠,硫代硫酸钠溶液经蒸发浓缩、冷却结晶、过滤、洗涤得到硫代硫酸钠晶体。A项,硫代硫酸钠具有
还原性,作脱氯剂时表现还原性,故A错误;B项,加入X的目的是除去溶液中的硫酸钠和碳酸钠,若加
入氯化钡溶液会引入新杂质氯离子,故B错误;C项,若溶液pH过小,硫代硫酸根离子会与氢离子反应,
使产率降低,故C错误;D项,提纯硫代硫酸钠晶体时应先用水洗涤除去晶体表面吸附的可溶性杂质,然
后用乙醇洗涤除去水,故D正确;故选D。
12.工业上以黄铁矿(主要成分为FeS,含有少量NiS、CuS、SiO 等杂质)为原料制备
2 2
K[Fe(CN) ]•3H O,工艺流程如图:
4 6 2
下列说法错误的是( )
A.“焙烧”时氧化产物有Fe O 和SO
2 3 2
B.“调pH”分离Fe3+与Cu2+、Ni2+是利用了它们氢氧化物K 的不同
sp
C.“溶液Ⅰ”中主要反应的离子方程式为6OH-+6HCN+Fe2+=[Fe(CN)]4-+6H O
6 2
D.“一系列操作”为过滤、洗涤、干燥
【答案】C
【解析】A项,由工艺流程图可知,黄铁矿焙烧的主要化学方程式为:4FeS(s)+11O(g) = 2Fe O(s)
2 2 2 3
+4SO(g),“焙烧”时氧化产物有Fe O 和SO ,故A正确;B项,Fe(OH) 的Ksp远小于Cu (OH) 、Ni
2 2 3 2 3 2
(OH) 的Ksp,所以当pH达到一定值时Fe3+产生沉淀,而Cu2+、Ni2+不沉淀,从而将其分离,故B正确;C
2
项,写离子方程式时石灰乳不能拆开,故C错误;D项,由工艺流程图可知,由溶液得到晶体的操作为:
过滤、洗涤、干燥,故D正确。故选C。
13.工业上可用克劳斯工艺处理含HS的尾气获得硫黄,工艺流程如下:
2已知反应炉中部分HS发生反应:2HS+3O 2SO +2H O。下列说法错误的是( )
2 2 2 2 2
A.可用品红溶液检验排放的气体中是否含有二氧化硫
B.每回收32g单质硫,理论上消耗氧气的体积为33.6l(标准状况)
C.催化转化器中发生的反应为SO +2H S 3S+2HO
2 2 2
D.为提高HS转化为S的比例,理论上应控制反应炉中HS的转化率约为
2 2
【答案】B
【解析】由题干已知信息可知,反应炉中部分HS发生反应:2HS+3O 2SO +2H O,催化转化
2 2 2 2 2
器中发生反应为:SO +2H S 3S+2HO,生成的硫蒸气经硫冷凝器可将硫冷凝下来,变为固体和气体
2 2 2
分离。A项,利用SO 可使品红溶液褪色的特性,故可用品红溶液检验排放的气体中是否含有二氧化硫,
2
A正确;B项,每回收32g单质硫的物质的量为: =1mol,根据分析可知,生成1molS需SO 的物
2
质的量为 mol,生成 molSO 需要O 的物质的量为:0.5mol,故理论上消耗氧气的体积为
2 2
0.5mol×22.4L/mol=11.2L,B错误;C项,催化转化器中发生的反应为SO +2H S 3S+2HO,C正确;
2 2 2
D项,根据反应方程式2HS+3O 2SO +2H O、SO +2H S 3S+2HO可知,为提高HS转化为S的
2 2 2 2 2 2 2 2
比例,理论上应控制反应炉中HS的转化率约为33.3%,D正确;故选B。
2
14.以黄铁矿(主要成分是FeS,含少量SiO)和软锰矿(主要成分是MnO ,含少量Fe O、Al O)为原
2 2 2 2 3 2 3
料制备MnSO ·H O的工艺流程如下。下列说法错误的是( )
4 2
A.酸浸过程得到的滤液中含有Mn2+、Fe3+,则该过程中主要反应的离子方程式是
3MnO +2FeS +12H+=3Mn 2++2Fe3++4S+6H O
2 2 2
B.滤渣1的成分中含有S和SiO
2
C.酸浸和沉锰操作均应在较高温度下进行
D.调pH的目的是除去Fe3+、Al3+
【答案】C【解析】软锰矿(主要成分MnO ,含少量Al O 和SiO)和黄铁矿(FeS )混合粉碎后用稀硫酸溶解,待完
2 2 3 2 2
全反应后过滤,除去不溶于酸的SiO 和其它杂质,所得滤液1中主要含有Mn2+、Al3+、Fe3+、H+、SO 2-,
2 4
然后加入NaOH溶液,调节溶液pH,使Al3+、Fe3+完全转化为Al(OH) 、Fe(OH) 沉淀,并过滤除去,再加
3 3
入氨水、NH HCO ,Mn2+反应产生MnCO ,过滤,除去不溶性杂质,用HSO 溶解MnCO ,得到MnSO
4 3 3 2 4 3 4
溶液,将滤液蒸发结晶、趁热过滤、用热水洗涤、干燥即可得到MnSO ·H O。A项,MnO 具有强氧化性,
4 2 2
能够将FeS 氧化为Fe3+、S,MnO 被还原为Mn2+,根据电子守恒、电荷守恒、原子守恒,可得反应的离子
2 2
方程式为3MnO +2FeS +12H+=3Mn 2++2Fe3++4S+6H O,A正确;B项,酸性氧化物SiO 不能溶于水,S也
2 2 2 2
不能溶于水,也不溶于酸,因此用稀硫酸溶解后的滤渣1的成分中含有S和SiO,B正确;C项,酸浸时
2
采用高温可以使反应速率加快,而沉锰时如果温度过高,MnCO 溶解度增大,导致沉锰效率降低,因此应
3
该在低温下进行沉锰,C错误;D项,调pH的目的是使溶液中的Fe3+、Al3+转化为Fe(OH) 、Al(OH) 沉淀,
3 3
从而达到除去Fe3+、Al3+的目的,D正确;故选C。
15.某废矿渣的主要成分有FeO、NiO、Al O、SiO,为节约和充分利用资源,通过如图工艺流程回
2 3 2
收铁、镍。下列说法错误的是( )
已知:ⅰ.常温下,K (NiCO)=1.4×10-7;K [Ni(OH) ]=1.0×10-15。
sp 3 sp 2
ⅱ.“萃取”可将金属离子进行富集与分离,原理如下:X2+(水相)+2RH(有机相) XR (有机相)
2
+2H+(水相)。
A.滤液①中,主要存在的钠盐有NaAlO 、NaSiO
2 2 3
B.“反萃取”应控制在酸性环境进行
C.“沉镍”过程中反应方程式为:Ni2++2HCO-=NiCO ↓+CO ↑+H O,“沉镍”时若溶液pH越大,越
3 3 2 2
能充分吸收二氧化碳,NiCO 的产率越高
3
D.已知“水相”中c(Ni2+)=2×10-2mol•L-1,加NaHCO “沉镍”,当沉镍率达到99%时,溶液中
3
c(CO2-)=7×10-4mol•L-1
3
【答案】C
【解析】废矿渣的主要成分有FeO、NiO、Al O、SiO 加入氢氧化钠溶液,Al O、SiO 分别与氢氧化
2 3 2 2 3 2钠溶液反应生成偏铝酸钠和水、硅酸钠和水,滤液①中偏铝酸钠、硅酸钠和剩余氢氧化钠,过滤得到滤渣
为FeO、NiO,硫酸酸浸溶液中为Fe2+、Ni2+,加入萃取剂,Ni2+进入水相中,沉镍,加入碳酸氢钠,生成
碳酸镍,Fe2+进入有机相,再反萃取,进入水相,再加氧化剂氧为Fe3+,再加入碳酸钠沉铁得到黄钠铁矾。
A项,Al O、SiO 分别与氢氧化钠溶液反应生成偏铝酸钠和水、硅酸钠和水,滤液①中偏铝酸钠、硅酸钠,
2 3 2
A正确;B项,萃取原理为:X2+(水相)+2RH(有机相) XR (有机相)+2H+(水相),进行反萃取,需要
2
使反应逆向进行,在此条件下,酸性有利于反萃取,B正确;C项,“沉镍”过程产生一种气体为二氧化
碳和碳酸镍,根据电荷守恒和原子守恒,离子方程式为:Ni2++2HCO-=NiCO ↓+CO ↑+H O;由于
3 3 2 2
K (NiCO)=1.4×10-7>K [Ni(OH) ]=1.0×10-15,所以pH过大,OH-浓度偏高,容易生成Ni(OH) 沉淀,C错误;
sp 3 sp 2 2
D项,①沉镍率达到99%时,溶液中根据c(Ni2+)=2×10-2mol•L-1×(1-99%)=2×10-4mol•L-1,根据
K (NiCO)=1.4×10-7=c(CO 2-)c(Ni2+),可知c(CO2-)= = =7×10-4mol•L-1,D正确;故选
sp 3 3 3
C。
第II卷(非选择题 共55分)
二、填空题(本题共4小题,共55分)
16.(12分)某研究小组用铝土矿(主要成分为Al O,含少量FeO 和FeO)为原料制备絮凝剂聚合氯化
2 3 2 3 2 3
铝( )。按如下流程开展实验:
已知:①用NaOH溶液溶解铝土矿过程中FeO 转变为难溶性的铝硅酸盐。
2 3
② 的絮凝效果可用盐基度衡量,盐基度 。当盐基度为 时,絮凝效果较
好。
③酸性条件下,Cr O2-能氧化Cl-。
2 7
请回答:
(1)步骤I所得滤渣为 ;步骤II所发生反应的离子方程式为 。(2)下列说法不正确的是___________。
A.步骤I,反应须在密闭耐高压容器中进行,以实现所需反应温度
B.步骤II,滤液浓度较大时通入过量CO 有利于减少Al(OH) 沉淀中的杂质
2 3
C.步骤III,为减少Al(OH) 吸附的杂质,洗涤时需对漏斗中的沉淀充分搅拌
3
D.步骤IV中控制Al(OH) 和AlCl 的投料比可控制产品盐基度
3 3
(3)测定产品的盐基度。
Cl-的定量测定:称取一定量样品,配成溶液,移取25.00mL溶液于锥形瓶中,调pH=6.5~10.5,滴加
指示剂KCrO 溶液。在不断摇动下,用0.1000mol·L-1AgNO 标准溶液滴定至浅红色(Ag CrO 沉淀),30秒
2 4 3 2 4
内不褪色。平行测试3次,平均消耗AgNO 标准溶液22.50mL。另测得上述样品溶液中c(Al3
3
+)=0.1000mol·L-1。
①产品的盐基度为 。
②盐基度在0.60~0.85时絮凝效果较好的原因是 。
③测定Cl-过程中溶液pH过低或过高均会影响测定结果,原因是 。
【答案】(1) FeO、铝硅酸盐(2分) [Al(OH) ]- +CO =Al(OH) ↓+HCO-(2分)
2 3 4 2 3 3
(2)BC(2分)
(3) 0.7(2分) 铝离子水解更快(2分) pH过低,指示剂会与氢离子反应生成重铬酸跟,会氧化
氯离子,导致消耗的硝酸银偏少,而pH过高,氢氧根会与银离子反应,导致消耗的硝酸银偏多(2分)
【解析】铝土矿主要成分为Al O,含少量FeO 和FeO。铝土矿加氢氧化钠溶液“碱溶”,Al O 生
2 3 2 3 2 3 2 3
成Na[Al(OH) ] ,FeO 转变为难溶性的铝硅酸盐,FeO 和氢氧化钠溶液不反应,过滤,滤液中通入二氧
4 2 3 2 3
化碳生成生成氢氧化铝沉淀,过滤、洗涤得氢氧化铝,一部分氢氧化铝用盐酸溶解得氯化铝溶液,氯化铝
溶液和另一部分氢氧化铝混合得聚合氯化铝溶液,加热得聚合氯化铝固体。(1)FeO 和氢氧化钠溶液不反
2 3
应、FeO 转变为难溶性的铝硅酸盐,步骤I所得滤渣为FeO、铝硅酸盐;步骤II中Na[Al(OH) ]和过量二
2 3 2 3 4
氧化碳反应生成氢氧化铝沉淀和碳酸氢钠,所发生反应的离子方程式为[Al(OH) ]-
4
+CO =Al(OH) ↓+HCO-。(2)A项,步骤I,反应温度高于100℃,因此反应须在密闭耐高压容器中进行,以
2 3 3
实现所需反应温度,故A正确;B项,步骤Ⅱ,滤液浓度较大时通二氧化碳转化为碳酸氢钠沉淀(溶解度较
小),不利于除杂,故B错误;C项,步骤Ⅲ,洗涤时不能对漏斗中的沉淀进行搅拌,故C错误;D项,
中a、b可通过控制Al(OH) 和AlCl 的投料比控制,所以控制Al(OH) 和AlCl 的投料比可
3 3 3 3
控制产品盐基度,故D正确;选BC。(3)①平均消耗0.1mol/L的AgNO 标准溶液22.50mL,
3n(Cl-)=n(Ag+)=0.0225L×0.1mol/L=0.00225mol,c(Cl-)= ,c(Al3+)=0.1000mol·L-1,根
据电荷守恒,c(OH-)=0.21mol,所以产品的化学式为 ,产品的盐基度为 。②
盐基度在0.60~0.85时,铝离子水解更快,所以絮凝效果较好。③pH过低,指示剂会与氢离子反应生成重
铬酸跟,会氧化氯离子,导致消耗的硝酸银偏少,而pH过高,氢氧根会与银离子反应,导致消耗的硝酸
银偏多,所以测定Cl-过程中溶液pH过低或过高均会影响测定结果。
17.(14分)过硫酸铵[(NH )SO]是一种重要的氧化剂、漂白剂。工业上用粗硫酸铵(杂质主要为含铁化
4 2 2 8
合物)生产过硫酸铵的一种工艺流程如图所示。
已知:(NH )SO 具有强氧化性和腐蚀性,0℃时在水中的溶解度为58.2g,微溶于乙醇,不溶于丙酮。
4 2 2 8
回答下列问题:
(1) (NH )SO 中S元素的化合价为 该物质中N、O、S元素的第一电离能由大到小的顺序
4 2 2 8
是 。
(2)用离子方程式表示(NH )SO 溶液呈酸性的原因: 。
4 2 4
(3)若将等体积、等浓度的氨水和稀硫酸混合后,混合溶液的主要溶质为 (填化学式),混合
溶液中各离子的浓度由大到小的顺序为 。
(4)FeOOH可用于脱除HS,其产物为FeSSH,常温下,FeSSH经空气氧化可再生出FeOOH,从而循
2
环使用。写出FeOOH再生的化学方程式: 。
(5)降温结晶后所得(NH )SO 晶体经过滤、 (填试剂名称)洗涤、干燥可得纯净的
4 2 2 8
(NH )SO 晶体,写出在实验室中洗涤(NH )SO 晶体的操作: 。
4 2 2 8 4 2 2 8
【答案】(1) +6(1分) N>O>S(2分)
(2)NH ++H O NH ·H O +H+(2分)
4 2 3 2
(3) NH HSO (1分) c(H+)>c(SO 2-)>c(NH +)>c(OH―) (2分)
4 4 4 4
(4) FeSSH+O =FeOOH+2S(2分)
2
(5) 无水乙醇(2分) 过滤后,用玻璃棒引流,将无水乙醇注入漏斗中,直至没过晶体,然后等待
液体从漏斗底部流走 ,重复操作两到三次(2分)
【解析】(1)①过硫酸铵中铵根离子为+1价,8个氧原子中有2个氧原子存在过氧键,为-1价,其余6个氧原子化合价为-2价,根据化合价计算规则,可求得S元素的化合价为+6价;②由于N元素的2p轨道
处于半满状态,较稳定,所以第一电离能N>O,同主族元素,原子序数越大,第一电离能越小,所以第
一电离能O>S,所以该物质中N、O、S元素的第一电离能由大到小的顺序是N>O>S;(2)硫酸铵是强酸
弱碱盐,铵根离子水解显酸性,离子方程式为:NH ++H O NH ·H O +H+;(3)等体积、等浓度的氨
4 2 3 2
水和稀硫酸混合,稀硫酸过量,混合溶液的主要溶质为NH HSO ;NH HSO 是强电解质,会完全电离成等
4 4 4 4
量的NH +、H+和SO 2-,由于水也会电离出H+,而NH +会发生水解,所以浓度大小:H+>SO 2->NH +;
4 4 4 4 4
NH +水解产生NH ·H O和OH-,水解是微弱的,综上所述,混合溶液中各离子的浓度由大到小的顺序为:
4 3 2
c(H+)>c(SO 2-)>c(NH +)>c(OH―);(4)FeSSH经空气氧化可再生出FeOOH,根据氧化还原规律及元素守恒,
4 4
可得其反应方程式为:FeSSH+O =FeOOH+2S。(5)①由于过硫酸铵0℃时在水中的溶解度较大,但微溶于
2
乙醇,所以过硫酸铵晶体可用无水乙醇洗涤,不仅可以洗除杂志,同时乙醇易挥发,便于晶体干燥;②过
滤后,用玻璃棒引流,将无水乙醇注入漏斗中,直至没过晶体,然后等待液体从漏斗底部流走 ,重复操
作两到三次 。
18.(14分)钒钛系SCR催化剂主要包含TiO 、VO、WO。从废SCR催化剂中回收TiO 、VO、WO
2 2 5 3 2 2 5 3
的某种工艺部分流程如下:
(1)“碱浸”选择高温的目的是_________。Ti元素可以形成多种配合物,在配合物Ti(CN) 中,提供孤
4
电子对的是_________原子,原因是_________。
(2)钛酸钠_________(填“难”或“易”)溶于水。钛酸钠有多种存在形态,其中较为常见的一种是
NaTiO ,则将其化学式写成氧化物的形式为_________。在酸洗过程中NaTiO 转化为HTiO 的化学方程
2 3 7 2 3 7 2 3
式为_________。
(3)钒钨溶液中钨元素以WO2-的形式存在,调节pH为2~3,溶液中的WO2-会转化为HW O 6-,再经
4 4 2 12 40
萃取、反萃取等过程可制得WO。写出WO2-转化为HW O 6-的离子方程式_________。
3 4 2 12 40
(4)为测定废催化剂中VO 的含量,现进行如下实验:准确称取5.000 g废催化剂样品于烧杯中,加入
2 5
足量质量分数为50%的硫酸,加热,冷却后将溶液移入 容量瓶中,加水定容。准确量取 溶
液于锥形瓶中,滴加2~3滴指示剂,用浓度为 的NH ) Fe(SO ) 标准溶液进行滴定,恰好完全
4 2 4 2
反应时消耗标准溶液的体积为 。实验过程中,V元素最终转化为V3+,计算废催化剂中VO 的含
2 5
量为_________(以百分数表示,废催化剂中其他成分对测定无影响)。【答案】(1)加快反应速率或加快碱浸速率(1分)
C(或碳)(1分) C的电负性比N弱,更容易提供孤电子对形成配位键(2分)
(2)难(2分) NaO·3TiO (2分) NaTiO+H SO +2H O=3HTiO +NaSO(2分)
2 2 2 3 7 2 4 2 2 3 2 4
(3)12WO2-+18H+=H W O 6-+8H O(2分)
4 2 12 40 2
(4)18.2%(2分)
【解析】废催化剂中加入氢氧化钠进行高温碱浸,生成可溶性的含钒、钨的盐,经过滤得到沉淀钛酸
钠,用稀硫酸进行酸洗,水洗、焙烧得到二氧化钛。(1)为了加快反应速率或加快碱浸速率,“碱浸”选择
高温。在配合物Ti(CN) 中,因为C的电负性比N弱,更容易提供孤电子对形成配位键,故分子提供孤电
4
子对的是 C(或碳)。(2)经过过滤得到钒钨溶液和钛酸钠,推知钛酸钠难溶于水。根据 NaTiO 的原子组成,
2 3 7
其化学式写成氧化物的形式为NaO·3TiO ;在酸洗过程中NaTiO 与稀硫酸反应生成HTiO 和硫酸钠,其
2 2 2 3 7 2 3
化学方程式为NaTiO+H SO +2H O=3HTiO +NaSO 。(3)钒钨溶液中钨元素以WO2-的形式存在,调节pH
2 3 7 2 4 2 2 3 2 4 4
为2~3,溶液中的WO2-会转化为HW O 6-,即WO2-在酸性条件反应生成HW O 6-和水,则离子方程式
4 2 12 40 4 2 12 40
为12WO2-+18H+=H W O 6-+8H O。(4)为测定废催化剂中VO 的含量,现进行如下实验:准确称取5.000
4 2 12 40 2 2 5
g废催化剂样品于烧杯中,加入足量质量分数为50%的硫酸,加热,冷却后将溶液移入250mL容量瓶中,
加水定容。准确量取 25.00mL 溶液于锥形瓶中,滴加 2~3 滴指示剂,用浓度为 0.1000mol·L-1的NH )
4 2
Fe(SO ) 标准溶液进行滴定,恰好完全反应时消耗标准溶液的体积为20.00mL。实验过程中,V元素最终转
4 2
化为V3+,滴定过程中发生氧化还原反应,亚铁离子转化为铁离子,V元素由+5价转化为V3+,设废催化剂
中 VO 的质量为 m, ,解得 m=0.91g,则 VO 含量为
2 5 2 5
18.2%。
19.(15分)分铜液净化渣主要含铜、碲(Te)、锑(Sb)、砷(As)等元素的化合物,一种回收工艺流程如图:
已知:①“碱浸”时,铜、锑转化为难溶氢氧化物或氧化物,碱浸液含有NaTeO 、NaAsO 。
2 3 3 4
②“酸浸”时,锑元素发生反应生成难溶的Sb O(SO ) 浸渣。
2 4 4
回答下列问题:(1)As位于第四周期VA族,基态As的价层电子排布式为 。
(2)“碱浸”时,TeO 与NaOH反应的离子方程式为 。
2
(3)向碱浸液中加入盐酸调节pH=4,有TeO 析出,分离出TeO 的操作是 。滤液中As元素最主
2 2
要的存在形式为 。(填标号)(25℃,HAsO 的各级电离常数为K =6.3×10-3,K =1.0×10-7,
3 4 a1 a2
K =3.2×10-12)
a3
A.HAsO B.HAsO - C.HAsO 2- D.AsO 3-
3 4 2 4 4 4
(4)①Sb O(SO ) 中,Sb的化合价为 。
2 4 4
②“氯盐酸浸”时,通入SO 的目的是 。
2
(5)“水解”时,生成SbOCl的化学方程式为 。
(6)TeO 可用作电子元件材料,熔点为733℃,TeO 晶胞是长方体结构如图。碲的配位数为 。
2 2
已知N 为阿伏加德罗常数的值,则该晶体的密度为 g/cm3。
A
【答案】(1) 4s24p3(1分) (2) TeO +2OH-=TeO 2-+H O(2分)
2 3 2
(3) 过滤(1分) B(2分)
(4) +5(1分) 将Sb O(SO ) 还原为SbCl (2分)
2 4 4 3
(5)SbCl +H O=SbOCl+2HCl(2分)
3 2
(6) 6(2分) (2分)
【解析】结合题干信息,分铜液加入氢氧化钠溶液进行碱浸,铜、锑转化为难溶氢氧化物或氧化物,
碱浸液含有NaTeO 、NaAsO ;过滤后向滤渣中加入硫酸进行酸浸,铜的氢氧化物或氧化物均溶解,锑元
2 3 3 4
素反应生成难溶的Sb O(SO ) 浸渣,过滤后向浸渣中加入盐酸、氯化钠和二氧化硫,反应生成三氯化锑,
2 4 4
三氯化锑水解生成转化为SbOCl;碱浸液中加入酸调节PH=4,NaTeO 转化生成亚碲酸,亚碲酸不稳定分
2 3
解生成二氧化碲。(1)As为33号元素,基态As的价层电子排布式为:4s24p3。(2)TeO 属于酸性氧化物,与
2
NaOH反应的离子方程式为:TeO +2OH-=TeO 2-+H O。(3)向碱浸液加入盐酸调节pH=4,TeO 以沉淀析出,
2 3 2 2
分离出TeO 的操作是过滤;由题干信息可知,HAsO 的各级电离常数为:K =6.3×10-3,K =1.0×10-7,
2 3 4 a1 a2K =3.2×10-12,pH=4,则c(H+)=10-4mol/L,HAsO H++ H AsO - ,Ka= ,
a3 3 4 2 4 1
,故As主要以HAsO - 形式存在,故选B。(4)①结合化合物的化合价为0,
2 4
Sb O(SO ) 中,Sb 的化合价为+5 价;② SO 具有还原性,“氯盐酸浸”时,通入 SO 的目的是将
2 4 4 2 2
Sb O(SO ) 还 原 为 SbCl 。 (5)“ 水 解 ” 时 , SbCl 水 解 生 成 SbOCl , 化 学 方 程 式 为 :
2 4 4 3 3
SbCl +H O=SbOCl+2HCl。(6)结合图示晶胞结构,离碲离子最近的氧负离子有6个,故碲的配位数为6;根
3 2
据 均 摊 , 该 晶 胞 含 有 2+4× =4 个 O 原 子 , 含 有 1+8× =2 个 Te , 则 该 晶 体 的 密 度 =
g· cm-3。