文档内容
主题四 化学工艺流程测试(一)
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Cl-35.5 Na-23 K-39 Cr-52 Mn-55
第Ⅰ卷(选择题 共45分)
一、选择题(本题共15个小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合
题目要求的)
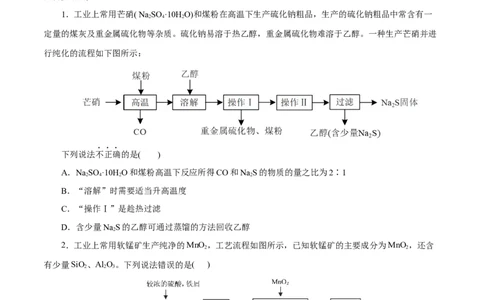
1.工业上常用芒硝( Na SO ·10H O)和煤粉在高温下生产硫化钠粗品,生产的硫化钠粗品中常含有一
2 4 2
定量的煤灰及重金属硫化物等杂质。硫化钠易溶于热乙醇,重金属硫化物难溶于乙醇。一种生产芒硝并进
行纯化的流程如下图所示:
下列说法不正确的是( )
A.NaSO ·10H O和煤粉高温下反应所得CO和NaS的物质的量之比为2∶1
2 4 2 2
B.“溶解”时需要适当升高温度
C.“操作Ⅰ”是趁热过滤
D.含少量NaS的乙醇可通过蒸馏的方法回收乙醇
2
2.工业上常用软锰矿生产纯净的MnO ,工艺流程如图所示,已知软锰矿的主要成分为MnO ,还含
2 2
有少量SiO、Al O。下列说法错误的是( )
2 2 3
A.“溶解”过程中有氢气生成
B.“过滤”得到的滤渣中含有HSiO
2 3
C.“纯化”过程中应先加MnO ,再调pH=5,过滤
2
D.“电解”时MnO 在电解池阳极生成,溶液pH值降低
2
3.聚合硫酸铁[Fe (OH) ((SO )] 是一种新型絮凝剂,其处理污水能力比FeCl 强,且腐蚀性小。工业
2 m 4 p n 3上利用废铁屑为原料制备聚合硫酸铁的工艺流程如图。下列说法正确的是( )
A.聚合硫酸铁[Fe (OH) ((SO )] 中
2 m 4 p n
B.酸浸槽中加入的酸液可用稀硝酸
C.反应釜中发生的离子反应为HO+Fe2++H+=Fe3++H O
2 2 2
D.聚合釜中控制溶液的pH越大越好
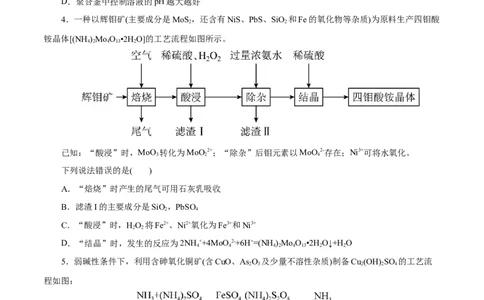
4.一种以辉钼矿(主要成分是MoS ,还含有NiS、PbS、SiO 和Fe的氧化物等杂质)为原料生产四钼酸
2 2
铵晶体[(NH )MoO •2H O]的工艺流程如图所示。
4 2 4 13 2
已知:“酸浸”时,MoO 转化为MoO 2+;“除杂”后钼元素以MoO 2-存在;Ni3+可将水氧化。
3 2 4
下列说法错误的是( )
A.“焙烧”时产生的尾气可用石灰乳吸收
B.滤渣I的主要成分是SiO,PbSO
2 4
C.“酸浸”时,HO 将Fe2+、Ni2+氧化为Fe3+和Ni3+
2 2
D.“结晶”时,发生的反应为2NH ++4MoO2-+6H+=(NH)MoO •2H O↓+HO
4 4 4 2 4 13 2 2
5.弱碱性条件下,利用含砷氧化铜矿(含CuO、As O 及少量不溶性杂质)制备Cu (OH) SO 的工艺流
2 3 2 2 4
程如图:
下列说法不正确的是( )
A.“氨浸”时As O 发生的离子反应为:As O+6NH+3H O=6NH ++ 2AsO3-
2 3 2 3 3 2 4 3
B.“氨浸”时CuO转化为[Cu(NH )]2+
3 4
C.“氧化除As O”时每生成1 mol FeAsO ,转移的电子数目为6.02×1023
2 3 4D.“蒸氨”后滤液中主要存在的离子为:NH +、SO 2-
4 4
6.碱式碳酸锌 可被用于皮肤保护剂、饲料添加剂等,以锌焙砂(主要成分为ZnO
及少量Cu2+、Mn2+的化合物)为原料制备碱式碳酸锌的工艺流程如图所示,下列说法错误的是( )
A.“酸浸”前将锌焙砂粉碎可提高酸浸速率与原料的利用率
B.“氧化”过程中,消耗的氧化剂与还原剂物质的量之比为2∶1
C.“沉铜”过程中反应的离子方程式为ZnS(s)+Cu2+(aq) Zn2+(aq)+ CuS(s)
D.碱式碳酸锌可与盐酸反应,其加热灼烧时可得到ZnO
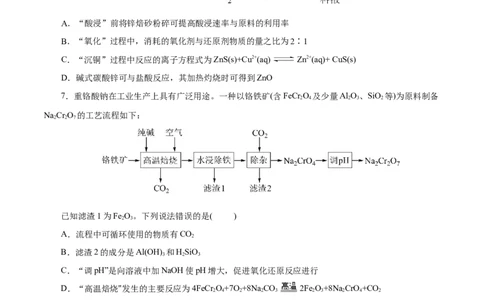
7.重铬酸钠在工业生产上具有广泛用途。一种以铬铁矿(含FeCr O 及少量Al O、SiO 等)为原料制备
2 4 2 3 2
NaCr O 的工艺流程如下:
2 2 7
已知滤渣1为Fe O。下列说法错误的是( )
2 3
A.流程中可循环使用的物质有CO
2
B.滤渣2的成分是Al(OH) 和HSiO
3 2 3
C.“调pH”是向溶液中加NaOH使pH增大,促进氧化还原反应进行
D.“高温焙烧"发生的主要反应为4FeCr O+7O +8Na CO 2Fe O+8Na CrO+CO
2 4 2 2 3 2 3 2 4 2
8.工业利用含镍废料(以镍铁钙合金为主)制取NiC O(草酸镍),再经高温煅烧NiC O 制取Ni O 的流
2 4 2 4 2 3
程如图所示。已知:NiC O、CaC O 均难溶于水;Fe3+完全沉淀的pH约为3.7。下列说法正确的是( )
2 4 2 4
A.酸溶时,可加入大量硫酸来提高“酸溶”效率B.调pH时,加入NaCO 溶液,目的是使Fe3+转化为Fe (CO) 沉淀
2 3 2 3 3
C.沉镍时,发生反应的离子方程式为:Ni2++C O2-=NiC O↓
2 4 2 4
D.煅烧时,反应的化学方程式为:2NiC O Ni O+3CO↑+CO ↑
2 4 2 3 2
9.钪(Sc)可用于制备铝钪合金、燃料电池、钪钠卤灯、示踪剂、激光晶体等产品。以钛白酸性废水
(主要含 、Fe2+、Sc3+)为原料制备氧化钪(ScO)的工艺流程如下。下列说法正确的是( )
2 3
A.酸洗时加入HO 的目的是将Ti 4+还原为Ti2+
2 2
B.“操作Ⅰ”需要的玻璃仪器有分液漏斗
C.“滤渣Ⅰ”的主要成分是Ti (OH)、Fe(OH)
4 3
D.草酸钪焙烧时反应的化学方程式:2Sc(C O)+3O 2ScO+12CO
2 2 4 3 2 2 3 2
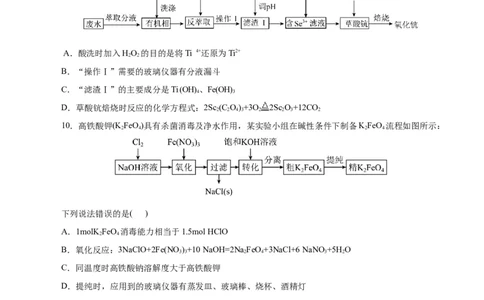
10.高铁酸钾(K FeO)具有杀菌消毒及净水作用,某实验小组在碱性条件下制备KFeO 流程如图所示:
2 4 2 4
下列说法错误的是( )
A.1molK FeO 消毒能力相当于1.5mol HClO
2 4
B.氧化反应:3NaClO+2Fe(NO )+10 NaOH=2Na FeO+3NaCl+6 NaNO +5H O
3 3 2 4 3 2
C.同温度时高铁酸钠溶解度大于高铁酸钾
D.提纯时,应用到的玻璃仪器有蒸发皿、玻璃棒、烧杯、酒精灯
11.硫代硫酸钠晶体(NaSO·5H O)不溶于乙醇,可用作纸浆漂白时的脱氯剂等。用工业硫化钠(主要
2 2 3 2
成分NaS,含少量NaSO )及纯碱等为原料制备NaSO·5H O的流程如下:
2 2 4 2 2 3 2
下列说法正确的是( )
A.NaSO 作脱氯剂时主要利用其氧化性
2 2 3B.“净化”时加入的试剂X可选用BaCl 溶液
2
C.“反应”过程中体系pH大小对产品产率无影响
D.提纯NaSO·5H O时,应先用水洗,再用乙醇洗涤
2 2 3 2
12.工业上以黄铁矿(主要成分为FeS,含有少量NiS、CuS、SiO 等杂质)为原料制备
2 2
K[Fe(CN) ]•3H O,工艺流程如图:
4 6 2
下列说法错误的是( )
A.“焙烧”时氧化产物有Fe O 和SO
2 3 2
B.“调pH”分离Fe3+与Cu2+、Ni2+是利用了它们氢氧化物K 的不同
sp
C.“溶液Ⅰ”中主要反应的离子方程式为6OH-+6HCN+Fe2+=[Fe(CN)]4-+6H O
6 2
D.“一系列操作”为过滤、洗涤、干燥
13.工业上可用克劳斯工艺处理含HS的尾气获得硫黄,工艺流程如下:
2
已知反应炉中部分HS发生反应:2HS+3O 2SO +2H O。下列说法错误的是( )
2 2 2 2 2
A.可用品红溶液检验排放的气体中是否含有二氧化硫
B.每回收32g单质硫,理论上消耗氧气的体积为33.6l(标准状况)
C.催化转化器中发生的反应为SO +2H S 3S+2HO
2 2 2
D.为提高HS转化为S的比例,理论上应控制反应炉中HS的转化率约为
2 2
14.以黄铁矿(主要成分是FeS,含少量SiO)和软锰矿(主要成分是MnO ,含少量Fe O、Al O)为原
2 2 2 2 3 2 3
料制备MnSO ·H O的工艺流程如下。下列说法错误的是( )
4 2A.酸浸过程得到的滤液中含有Mn2+、Fe3+,则该过程中主要反应的离子方程式是
3MnO +2FeS +12H+=3Mn 2++2Fe3++4S+6H O
2 2 2
B.滤渣1的成分中含有S和SiO
2
C.酸浸和沉锰操作均应在较高温度下进行
D.调pH的目的是除去Fe3+、Al3+
15.某废矿渣的主要成分有FeO、NiO、Al O、SiO,为节约和充分利用资源,通过如图工艺流程回
2 3 2
收铁、镍。下列说法错误的是( )
已知:ⅰ.常温下,K (NiCO)=1.4×10-7;K [Ni(OH) ]=1.0×10-15。
sp 3 sp 2
ⅱ.“萃取”可将金属离子进行富集与分离,原理如下:X2+(水相)+2RH(有机相) XR (有机相)
2
+2H+(水相)。
A.滤液①中,主要存在的钠盐有NaAlO 、NaSiO
2 2 3
B.“反萃取”应控制在酸性环境进行
C.“沉镍”过程中反应方程式为:Ni2++2HCO-=NiCO ↓+CO ↑+H O,“沉镍”时若溶液pH越大,越
3 3 2 2
能充分吸收二氧化碳,NiCO 的产率越高
3
D.已知“水相”中c(Ni2+)=2×10-2mol•L-1,加NaHCO “沉镍”,当沉镍率达到99%时,溶液中
3
c(CO2-)=7×10-4mol•L-1
3
第II卷(非选择题 共55分)
二、填空题(本题共4小题,共55分)
16.(12分)某研究小组用铝土矿(主要成分为Al O,含少量FeO 和FeO)为原料制备絮凝剂聚合氯化
2 3 2 3 2 3铝( )。按如下流程开展实验:
已知:①用NaOH溶液溶解铝土矿过程中FeO 转变为难溶性的铝硅酸盐。
2 3
② 的絮凝效果可用盐基度衡量,盐基度 。当盐基度为 时,絮凝效果较
好。
③酸性条件下,Cr O2-能氧化Cl-。
2 7
请回答:
(1)步骤I所得滤渣为 ;步骤II所发生反应的离子方程式为 。
(2)下列说法不正确的是___________。
A.步骤I,反应须在密闭耐高压容器中进行,以实现所需反应温度
B.步骤II,滤液浓度较大时通入过量CO 有利于减少Al(OH) 沉淀中的杂质
2 3
C.步骤III,为减少Al(OH) 吸附的杂质,洗涤时需对漏斗中的沉淀充分搅拌
3
D.步骤IV中控制Al(OH) 和AlCl 的投料比可控制产品盐基度
3 3
(3)测定产品的盐基度。
Cl-的定量测定:称取一定量样品,配成溶液,移取25.00mL溶液于锥形瓶中,调pH=6.5~10.5,滴加
指示剂KCrO 溶液。在不断摇动下,用0.1000mol·L-1AgNO 标准溶液滴定至浅红色(Ag CrO 沉淀),30秒
2 4 3 2 4
内不褪色。平行测试3次,平均消耗AgNO 标准溶液22.50mL。另测得上述样品溶液中c(Al3
3
+)=0.1000mol·L-1。
①产品的盐基度为 。
②盐基度在0.60~0.85时絮凝效果较好的原因是 。
③测定Cl-过程中溶液pH过低或过高均会影响测定结果,原因是 。
17.(14分)过硫酸铵[(NH )SO]是一种重要的氧化剂、漂白剂。工业上用粗硫酸铵(杂质主要为含铁化
4 2 2 8
合物)生产过硫酸铵的一种工艺流程如图所示。已知:(NH )SO 具有强氧化性和腐蚀性,0℃时在水中的溶解度为58.2g,微溶于乙醇,不溶于丙酮。
4 2 2 8
回答下列问题:
(1) (NH )SO 中S元素的化合价为 该物质中N、O、S元素的第一电离能由大到小的顺序
4 2 2 8
是 。
(2)用离子方程式表示(NH )SO 溶液呈酸性的原因: 。
4 2 4
(3)若将等体积、等浓度的氨水和稀硫酸混合后,混合溶液的主要溶质为 (填化学式),混合
溶液中各离子的浓度由大到小的顺序为 。
(4)FeOOH可用于脱除HS,其产物为FeSSH,常温下,FeSSH经空气氧化可再生出FeOOH,从而循
2
环使用。写出FeOOH再生的化学方程式: 。
(5)降温结晶后所得(NH )SO 晶体经过滤、 (填试剂名称)洗涤、干燥可得纯净的
4 2 2 8
(NH )SO 晶体,写出在实验室中洗涤(NH )SO 晶体的操作: 。
4 2 2 8 4 2 2 8
18.(14分)钒钛系SCR催化剂主要包含TiO 、VO、WO。从废SCR催化剂中回收TiO 、VO、WO
2 2 5 3 2 2 5 3
的某种工艺部分流程如下:
(1)“碱浸”选择高温的目的是_________。Ti元素可以形成多种配合物,在配合物Ti(CN) 中,提供孤
4
电子对的是_________原子,原因是_________。
(2)钛酸钠_________(填“难”或“易”)溶于水。钛酸钠有多种存在形态,其中较为常见的一种是
NaTiO ,则将其化学式写成氧化物的形式为_________。在酸洗过程中NaTiO 转化为HTiO 的化学方程
2 3 7 2 3 7 2 3
式为_________。
(3)钒钨溶液中钨元素以WO2-的形式存在,调节pH为2~3,溶液中的WO2-会转化为HW O 6-,再经
4 4 2 12 40
萃取、反萃取等过程可制得WO。写出WO2-转化为HW O 6-的离子方程式_________。
3 4 2 12 40
(4)为测定废催化剂中VO 的含量,现进行如下实验:准确称取5.000 g废催化剂样品于烧杯中,加入
2 5
足量质量分数为50%的硫酸,加热,冷却后将溶液移入 容量瓶中,加水定容。准确量取 溶
液于锥形瓶中,滴加2~3滴指示剂,用浓度为 的NH ) Fe(SO ) 标准溶液进行滴定,恰好完全
4 2 4 2
反应时消耗标准溶液的体积为 。实验过程中,V元素最终转化为V3+,计算废催化剂中VO 的含
2 5
量为_________(以百分数表示,废催化剂中其他成分对测定无影响)。
19.(15分)分铜液净化渣主要含铜、碲(Te)、锑(Sb)、砷(As)等元素的化合物,一种回收工艺流程如图:已知:①“碱浸”时,铜、锑转化为难溶氢氧化物或氧化物,碱浸液含有NaTeO 、NaAsO 。
2 3 3 4
②“酸浸”时,锑元素发生反应生成难溶的Sb O(SO ) 浸渣。
2 4 4
回答下列问题:
(1)As位于第四周期VA族,基态As的价层电子排布式为 。
(2)“碱浸”时,TeO 与NaOH反应的离子方程式为 。
2
(3)向碱浸液中加入盐酸调节pH=4,有TeO 析出,分离出TeO 的操作是 。滤液中As元素最主
2 2
要的存在形式为 。(填标号)(25℃,HAsO 的各级电离常数为K =6.3×10-3,K =1.0×10-7,
3 4 a1 a2
K =3.2×10-12)
a3
A.HAsO B.HAsO - C.HAsO 2- D.AsO 3-
3 4 2 4 4 4
(4)①Sb O(SO ) 中,Sb的化合价为 。
2 4 4
②“氯盐酸浸”时,通入SO 的目的是 。
2
(5)“水解”时,生成SbOCl的化学方程式为 。
(6)TeO 可用作电子元件材料,熔点为733℃,TeO 晶胞是长方体结构如图。碲的配位数为 。
2 2
已知N 为阿伏加德罗常数的值,则该晶体的密度为 g/cm3。
A