文档内容
专题 16 溶液的配制与滴定法的应用
1.二氯异氰尿酸钠[(CNO) ClNa]是常用的杀菌消毒剂,常温下为白色固体,难溶于冷水。
3 2
某同学利用高浓度的NaClO溶液和(CNO) H 固体,在10 ℃时反应制备二氯异氰尿酸钠。
3 3
某实验小组通过下列实验测定二氯异氰尿酸钠样品中有效氯的含量。
反应原理:[(CNO) Cl]-+H++2HO===(CNO) H +2HClO,HClO+2I-+H+===I +Cl-+
3 2 2 3 3 2
HO,I+2SO===SO+2I-
2 2 2 4
实验步骤:准确称取m g样品,用容量瓶配制成250 mL溶液;取25.00 mL上述溶液于碘量
瓶中,加入适量稀硫酸和过量KI溶液,充分反应后,用c mol·L-1 Na SO 标准溶液滴定至
2 2 3
溶液呈微黄色。加入淀粉指示剂继续滴定至终点,消耗NaSO 溶液平均为V mL。
2 2 3
(1)滴定终点的颜色变化为_______________________________。
(2)该样品的有效氯含量表达式为____________________________________________(化为最
简式)。(该样品的有效氯=×100%)
2.摩尔盐[(NH ) Fe(SO ) ·6H O]是一种常见的复盐。某实验小组用下列方法测定摩尔盐中
4 2 4 2 2
Fe2+的含量,取30.00 g固体于小烧杯中,加入适量稀硫酸,溶解后在250 mL容量瓶中定容。
取25.00 mL上述溶液于锥形瓶中,用0.1 mol·L-1的KMnO 溶液滴定至终点。平行操作三次,
4
消耗KMnO 溶液的平均体积为16.00 mL。此样品中Fe2+的含量为________%(结果保留小数
4
点后1位)。导致该测定结果与理论值有偏差的可能原因是____________(填字母)。
A.配制溶液定容时俯视刻度线
B.取摩尔盐溶液的滴定管没有润洗
C.取待测液的锥形瓶洗净后未干燥
D.摩尔盐的结晶水数量不足
3.硫代硫酸钠(Na SO)广泛用于电镀、鞣制皮革、棉织品漂白后的脱氯剂等。某实验小组
2 2 3
的同学用下列方法测定NaSO·5H O的质量分数,准确称取5.00 g硫代硫酸钠样品,溶于
2 2 3 2
蒸馏水配制成100 mL溶液,取25.00 mL注入锥形瓶中,以淀粉作指示剂,用0.100 0 mol·
L-1标准碘溶液滴定。已知:2SO(aq)+I(aq)===SO(aq)(无色)+2I-(aq)。
2 2 4
(1)滴定终点的现象是_______________________________________________________。
(2)第一次滴定开始和结束时,滴定管中的液面如图,则消耗标准碘溶液的体积为
________mL。
(3)重复上述操作三次,记录另两次数据如表中所示,则产品中 NaSO·5H O的质量分数为
2 2 3 2
________%(结果保留两位小数)。滴定次数 初读数/mL 末读数/mL
第二次 1.24 23.36
第三次 0.24 24.45
4.草酸(HOOC—COOH,弱酸)及其化合物在工业中有重要作用。草酸具有较强的还原性,
与氧化剂作用易被氧化成二氧化碳和水,故实验室可利用草酸测定次氯酸钠溶液的浓度。实
验步骤如下:取20.00 mL 0.5 mol·L-1草酸溶液于锥形瓶中,用次氯酸钠溶液滴定,至终点
时消耗次氯酸钠溶液为25.00 mL。
(1)次氯酸钠与草酸反应的离子方程式为__________________________________________。
(2)次氯酸钠溶液物质的量浓度为____mol·L-1。
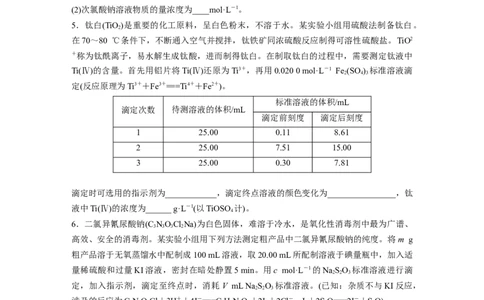
5.钛白(TiO)是重要的化工原料,呈白色粉末,不溶于水。某实验小组用硫酸法制备钛白。
2
在70~80 ℃条件下,不断通入空气并搅拌,钛铁矿同浓硫酸反应制得可溶性硫酸盐。TiO2
+称为钛酰离子,易水解生成钛酸,进而制得钛白。在制取钛白的过程中,需要测定钛液中
Ti(Ⅳ)的含量。首先用铝片将Ti(Ⅳ)还原为Ti3+,再用0.020 0 mol·L-1 Fe (SO ) 标准溶液滴
2 4 3
定(反应原理为Ti3++Fe3+===Ti4++Fe2+)。
标准溶液的体积/mL
滴定次数 待测溶液的体积/mL
滴定前刻度 滴定后刻度
1 25.00 0.11 8.61
2 25.00 7.51 15.00
3 25.00 0.30 7.81
滴定时可选用的指示剂为____________,滴定终点溶液的颜色变化为________________,钛
液中Ti(Ⅳ)的浓度为______ g·L-1(以TiOSO 计)。
4
6.二氯异氰尿酸钠(C NOClNa)为白色固体,难溶于冷水,是氧化性消毒剂中最为广谱、
3 3 3 2
高效、安全的消毒剂。某实验小组用下列方法测定粗产品中二氯异氰尿酸钠的纯度。将m g
粗产品溶于无氧蒸馏水中配制成100 mL溶液,取20.00 mL所配制溶液于碘量瓶中,加入适
量稀硫酸和过量KI溶液,密封在暗处静置5 min。用c mol·L-1的NaSO 标准溶液进行滴
2 2 3
定,加入指示剂,滴定至终点时,消耗V mL Na SO 标准溶液。(已知:杂质不与KI反应,
2 2 3
涉及的反应为C NOCl+3H++4I-===C HNO+2I+2Cl-、I+2SO===2I-+SO)
3 3 3 3 3 3 3 2 2 2 4
(1)加入的指示剂是__________(填名称)。
(2)C NOClNa的百分含量为________%(用含m、c、V的代数式表示)。
3 3 3 2
(3)下列操作会导致粗产品中二氯异氰尿酸钠的纯度偏低的是________(填字母)。
a.盛装NaSO 标准溶液的滴定管未润洗
2 2 3
b.滴定管在滴定前有气泡,滴定后无气泡
c.碘量瓶中加入的稀硫酸偏少
7.叠氮化钠(NaN )是易溶于水的白色晶体,微溶于乙醇,不溶于乙醚,常用作汽车安全气
3
囊中的药剂。实验室用滴定法测定叠氮化钠样品中NaN 的质量分数:
3①将2.500 g试样配成500 mL溶液。
②取50.00 mL上述溶液置于锥形瓶中,加入50.00 mL 0.100 0 mol·L-1(NH )Ce(NO ) 溶液。
4 2 3 6
发生反应:2(NH )Ce(NO )+2NaN ===4NH NO +2Ce(NO )+2NaNO +3N↑。
4 2 3 6 3 4 3 3 3 3 2
③充分反应后,将溶液稀释,向溶液中加入 8 mL浓硫酸,滴入3滴邻菲罗琳指示液,用
0.050 0 mol·L-1(NH )Fe(SO ) 标准溶液滴定过量的Ce4+,消耗溶液体积为34.00 mL。发生
4 2 4 2
反应:Ce4++Fe2+===Ce3++Fe3+。
试样中NaN 的质量分数为__________(结果保留四位有效数字)。
3
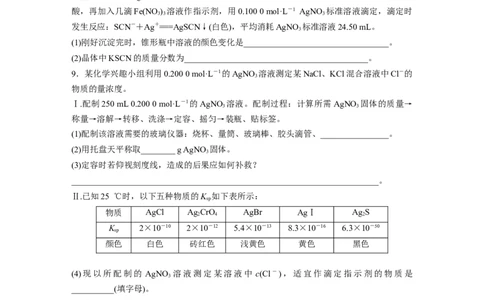
8.硫氰化钾(KSCN)是中学化学实验室的常见药品。某实验小组测定制备的晶体中KSCN的
含量:称取10.00 g样品,配成1 000 mL溶液,取25.00 mL溶液于锥形瓶中,加入适量稀硝
酸,再加入几滴Fe(NO ) 溶液作指示剂,用0.100 0 mol·L-1 AgNO 标准溶液滴定,滴定时
3 3 3
发生反应:SCN-+Ag+===AgSCN↓(白色),平均消耗AgNO 标准溶液24.50 mL。
3
(1)刚好沉淀完时,锥形瓶中溶液的颜色变化是__________________________________。
(2)晶体中KSCN的质量分数为___________________________________________。
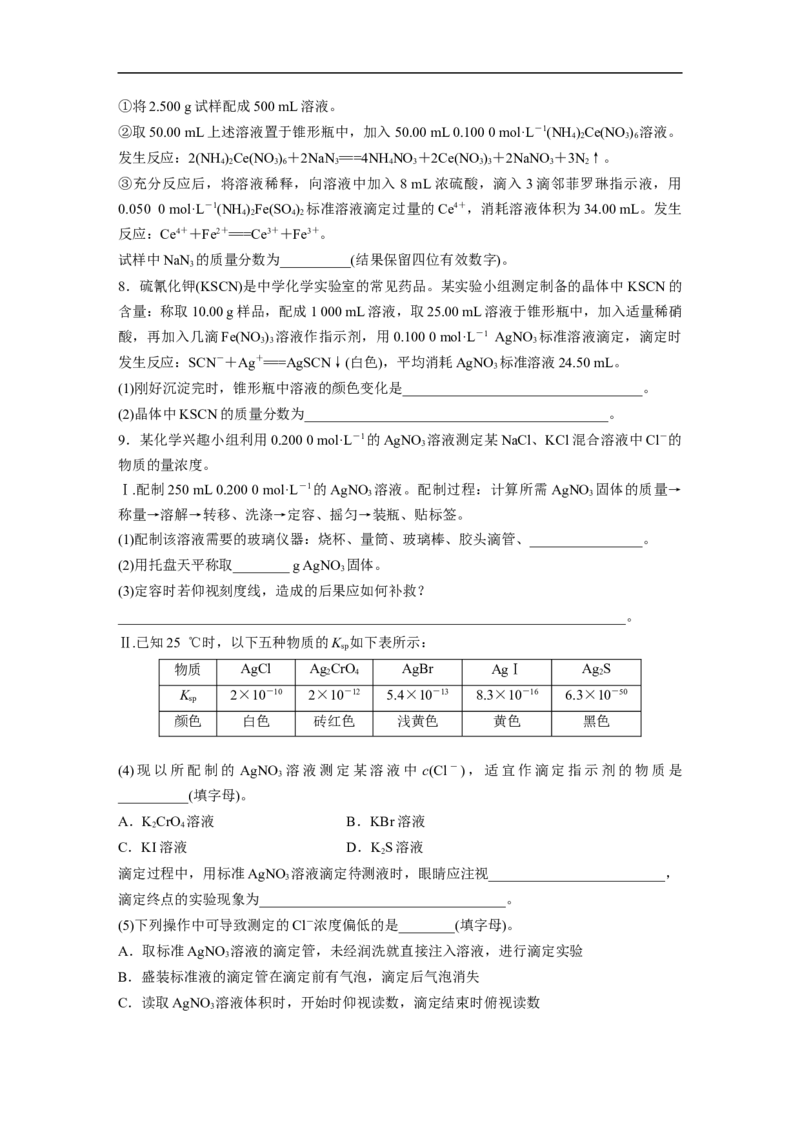
9.某化学兴趣小组利用0.200 0 mol·L-1的AgNO 溶液测定某NaCl、KCl混合溶液中Cl-的
3
物质的量浓度。
Ⅰ.配制250 mL 0.200 0 mol·L-1的AgNO 溶液。配制过程:计算所需AgNO 固体的质量→
3 3
称量→溶解→转移、洗涤→定容、摇匀→装瓶、贴标签。
(1)配制该溶液需要的玻璃仪器:烧杯、量筒、玻璃棒、胶头滴管、________________。
(2)用托盘天平称取________ g AgNO 固体。
3
(3)定容时若仰视刻度线,造成的后果应如何补救?
________________________________________________________________________。
Ⅱ.已知25 ℃时,以下五种物质的K 如下表所示:
sp
物质 AgCl Ag CrO AgBr AgⅠ Ag S
2 4 2
K 2×10-10 2×10-12 5.4×10-13 8.3×10-16 6.3×10-50
sp
颜色 白色 砖红色 浅黄色 黄色 黑色
(4)现以所配制的 AgNO 溶液测定某溶液中 c(Cl-),适宜作滴定指示剂的物质是
3
__________(填字母)。
A.KCrO 溶液 B.KBr溶液
2 4
C.KI溶液 D.KS溶液
2
滴定过程中,用标准AgNO 溶液滴定待测液时,眼睛应注视_________________________,
3
滴定终点的实验现象为___________________________________。
(5)下列操作中可导致测定的Cl-浓度偏低的是________(填字母)。
A.取标准AgNO 溶液的滴定管,未经润洗就直接注入溶液,进行滴定实验
3
B.盛装标准液的滴定管在滴定前有气泡,滴定后气泡消失
C.读取AgNO 溶液体积时,开始时仰视读数,滴定结束时俯视读数
3D.锥形瓶内有少量蒸馏水
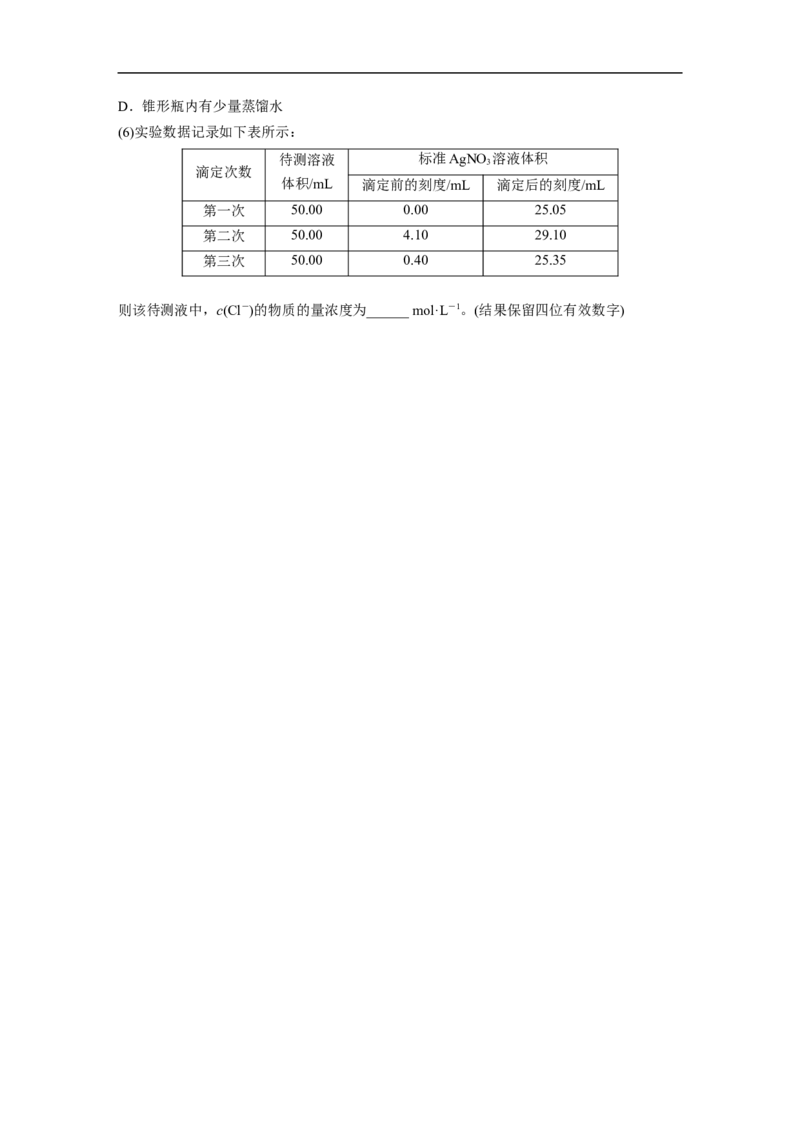
(6)实验数据记录如下表所示:
待测溶液 标准AgNO 溶液体积
3
滴定次数
体积/mL 滴定前的刻度/mL 滴定后的刻度/mL
第一次 50.00 0.00 25.05
第二次 50.00 4.10 29.10
第三次 50.00 0.40 25.35
则该待测液中,c(Cl-)的物质的量浓度为______ mol·L-1。(结果保留四位有效数字)