文档内容
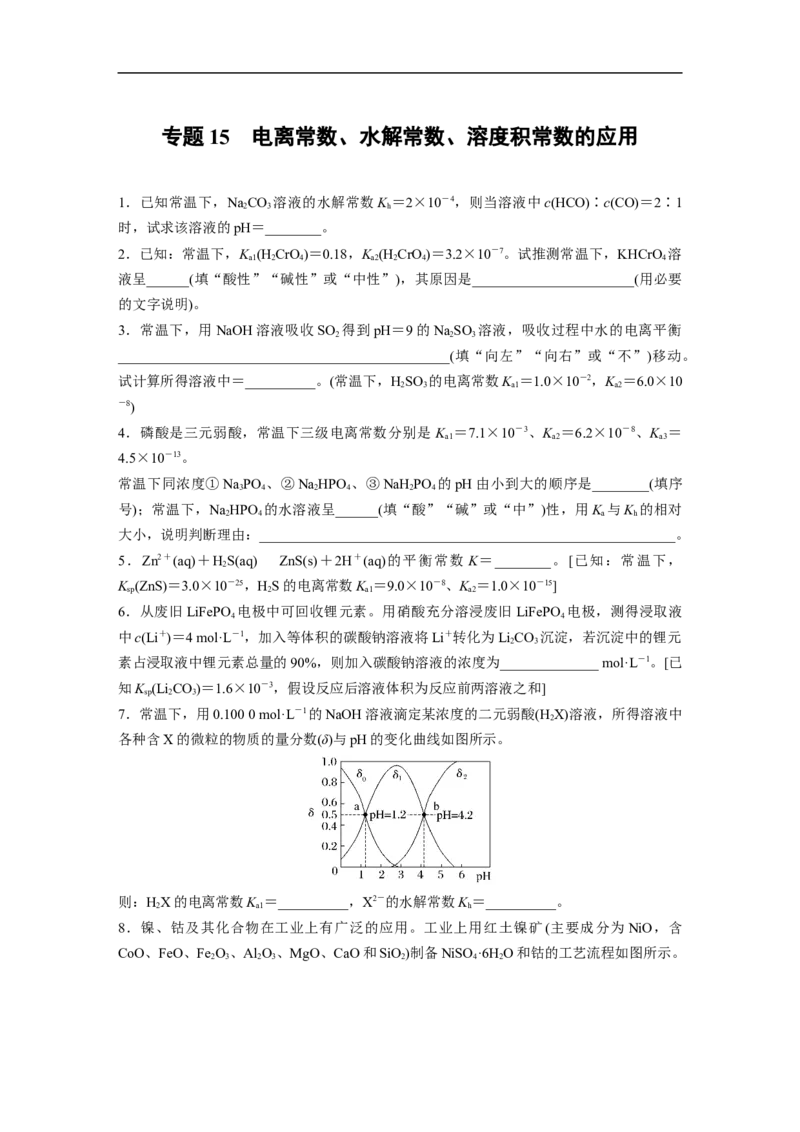
专题 15 电离常数、水解常数、溶度积常数的应用
1.已知常温下,NaCO 溶液的水解常数K =2×10-4,则当溶液中c(HCO)∶c(CO)=2∶1
2 3 h
时,试求该溶液的pH=________。
2.已知:常温下,K (H CrO)=0.18,K (H CrO)=3.2×10-7。试推测常温下,KHCrO 溶
a1 2 4 a2 2 4 4
液呈______(填“酸性”“碱性”或“中性”),其原因是_______________________(用必要
的文字说明)。
3.常温下,用NaOH溶液吸收SO 得到pH=9的NaSO 溶液,吸收过程中水的电离平衡
2 2 3
_______________________________________________(填“向左”“向右”或“不”)移动。
试计算所得溶液中=__________。(常温下,HSO 的电离常数K =1.0×10-2,K =6.0×10
2 3 a1 a2
-8)
4.磷酸是三元弱酸,常温下三级电离常数分别是 K =7.1×10-3、K =6.2×10-8、K =
a1 a2 a3
4.5×10-13。
常温下同浓度①NaPO 、②NaHPO 、③NaH PO 的pH由小到大的顺序是________(填序
3 4 2 4 2 4
号);常温下,NaHPO 的水溶液呈______(填“酸”“碱”或“中”)性,用K 与K 的相对
2 4 a h
大小,说明判断理由:___________________________________________________________。
5.Zn2+(aq)+HS(aq)ZnS(s)+2H+(aq)的平衡常数 K=________。[已知:常温下,
2
K (ZnS)=3.0×10-25,HS的电离常数K =9.0×10-8、K =1.0×10-15]
sp 2 a1 a2
6.从废旧LiFePO 电极中可回收锂元素。用硝酸充分溶浸废旧LiFePO 电极,测得浸取液
4 4
中c(Li+)=4 mol·L-1,加入等体积的碳酸钠溶液将Li+转化为LiCO 沉淀,若沉淀中的锂元
2 3
素占浸取液中锂元素总量的90%,则加入碳酸钠溶液的浓度为______________ mol·L-1。[已
知K (Li CO)=1.6×10-3,假设反应后溶液体积为反应前两溶液之和]
sp 2 3
7.常温下,用0.100 0 mol·L-1的NaOH溶液滴定某浓度的二元弱酸(H X)溶液,所得溶液中
2
各种含X的微粒的物质的量分数(δ)与pH的变化曲线如图所示。
则:HX的电离常数K =__________,X2-的水解常数K =__________。
2 a1 h
8.镍、钴及其化合物在工业上有广泛的应用。工业上用红土镍矿(主要成分为NiO,含
CoO、FeO、Fe O、Al O、MgO、CaO和SiO)制备NiSO ·6H O和钴的工艺流程如图所示。
2 3 2 3 2 4 2滤渣3的成分为MgF 和CaF 。若滤液1中c(Ca2+)=1.0×10-3 mol·L-1,当滤液2中c(Mg2+)
2 2
=1.5×10-6 mol·L-1时,除钙率为________(忽略沉淀前后溶液体积变化)。[已知:K (CaF )
sp 2
=1.5×10-10、K (MgF )=7.5×10-11]
sp 2
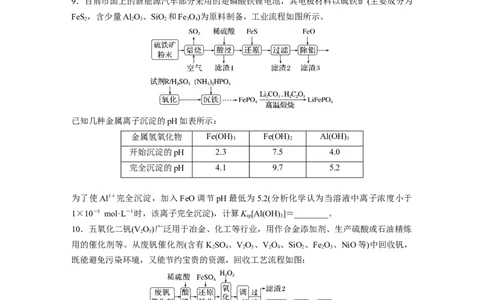
9.目前市面上的新能源汽车部分采用的是磷酸铁锂电池,其电极材料以硫铁矿(主要成分为
FeS,含少量Al O、SiO 和Fe O)为原料制备,工业流程如图所示。
2 2 3 2 3 4
已知几种金属离子沉淀的pH如表所示:
金属氢氧化物 Fe(OH) Fe(OH) Al(OH)
3 2 3
开始沉淀的pH 2.3 7.5 4.0
完全沉淀的pH 4.1 9.7 5.2
为了使Al3+完全沉淀,加入FeO调节pH最低为5.2(分析化学认为当溶液中离子浓度小于
1×10-5 mol·L-1时,该离子完全沉淀),计算K [Al(OH) ]=________。
sp 3
10.五氧化二钒(V O)广泛用于冶金、化工等行业,用作合金添加剂、生产硫酸或石油精炼
2 5
用的催化剂等。从废钒催化剂(含有KSO 、VO 、VO 、SiO 、Fe O 、NiO等)中回收钒,
2 4 2 5 2 4 2 2 3
既能避免污染环境,又能节约宝贵的资源,回收工艺流程如图:
加入HO 的目的是将过量的Fe2+转化为Fe3+。“氧化1”后,溶液中的金属阳离子主要有
2 2
Fe3+、Ni2+、VO2+,调节pH使离子沉淀,若溶液中c(Ni2+)=0.2 mol·L-1,则调节溶液的
pH最小值为__________可使Fe3+沉淀完全(离子浓度≤1.0×10-5 mol·L-1时沉淀完全),此
时________(填“有”或“无”)Ni(OH) 沉淀生成。{假设溶液体积不变,lg 6≈0.8,
2
K [Fe(OH) ]=2.16×10-39,K [Ni(OH) ]=2×10-15}
sp 3 sp 2