文档内容
绝密★启用前
2025 年高考考前信息必刷卷 01(江西专用)
化 学
考情速递
高考·新动向:考试内容可能会有所调整,强调核心知识点和实际应用能力,减少偏题和怪题;化学实
验操作可能成为考查重点,要求学生具备实验设计、操作和数据分析的能力;化学与物理、生物等学
科的交叉内容可能增加,考查学生的综合运用能力;题型可能更加灵活,增加开放性、探究性题目,
考查学生的创新思维和问题解决能力;试题可能更多涉及绿色化学、环境保护和可持续发展等热点话
题;可能引入数字化实验工具和模拟软件,考查学生在虚拟环境中的实验设计和分析能力,如2024年
江西高考17题温度传感的数字化;试题设计可能更注重考查学生的化学核心素养,如科学探究、证据
推理、模型认知等。
高考·新考法:新考法可能会对考纲进行调整,强调对基础知识的理解和应用能力,减少单纯记忆的内
容。 试题形式可能更加多样化,包括选择题、填空题、实验题和开放性问题等,旨在考查学生的综合
素质和创新能力,如2024年江西高考17题第(6)问设计一种实用温度传感装置。可能会更加重视学
生的实验能力,要求学生能够理解实验原理、设计实验方案、分析实验结果等,如2024年江西高考17
题。试题内容可能会与实际生活紧密结合,考查学生将化学知识应用于日常生活中的能力,如2024年
江西高考选择题3、7题。可能会鼓励跨学科知识的运用,考查学生在化学与物理、生物、环境等学科
之间的联系,如2024年江西高考15题。
高考·新情境:试题通常会结合新情境来考查学生的综合素养和实际应用能力。新情境题目往往涉及
生活中的实际问题、科学实验设计、数据分析等内容,旨在培养学生的创新思维和解决问题的能力。
在准备高考化学复习时,建议关注以下几个方面:
(1)实验设计与分析:理解实验原理,能够根据给定的情境设计实验,并分析实验结果。
(2)生活中的化学:关注化学在日常生活中的应用,如食品添加剂、环境保护、能源利用等。
(3)化学反应与方程式:熟练掌握常见化学反应及其方程式,能够根据情境推导反应过程。
(4)数据处理与计算:能够处理实验数据,进行简单的计算和推理。
(5)新材料与新技术:了解一些新材料、新技术的基本概念及其应用,例如纳米材料、绿色化学等。
命题·大预测:本套试卷有以下特点:
1.核心素养导向:如第2题通过三和中物质结构分析(比较键角大小),考查“宏观辨识与微观探析”素养,
预测类似题目将更注重物质结构与性质的深度关联。
2.实验创新特色:第3题仪器的创新使用,考查学生的创新能力。第17题中数字化的应用。
3.科技成果为背景:第4题以药物吲哚美辛结构和第10题以(杂)芳基磺酰氯( )为引发剂的有机催
化光调控活性聚合考查有机反应类型、有机物的性质、碳原子的杂化方式等有机化学基础知识。
4.强调实际应用和环境保护:第8题以废渣——分银渣的分离提纯和第15题失活催化剂回收镍为背景考
查化学实验知识和沉淀溶解平衡知识,第16题以温室气体CH 和CO 获得合成气(CO与H)为背景考查
4 2 2化学原理,体现了环境保护思想。
5.综合性与开放性:第18题有机推断,需要根据设定条件写出一种有机物的结构简式,体现了发散和收敛
的思维品质。
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡皮擦
干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 O 16
一、选择题:本题共14小题,每小题3分,共42分。每小题只有一个选项符合题目要求。
1.江西——一个被网友戏称为“阿卡林省”的地方,其省会城市——南昌正逐渐在网络上出圈,成为新
晋网红城市。下列说法错误的是
A.2024年春节江西各地烟花燃放涉及氧化还原反应
B.秋水广场的水幕灯光秀与丁达尔效应有关
C.南昌著名小吃——白糖糕含有的蔗糖属于纯净物
D.南昌瓷板画所使用的蓝色颜料主要成分是氧化铁
【答案】D
【解析】A.烟花燃烧有元素化合价的升降,涉及氧化还原反应,A正确;B.水幕灯光秀的一道道光
束利用了胶体的丁达尔效应,B正确;C.蔗糖的分子式为C H O ,属于纯净物,C正确;D.氧化
11 22 11
铁为三氧化二铁,显红棕色,所以蓝色颜料主要成分不是氧化铁,D错误;故选D。
2.根据以下三种物质的结构,下列说法正确的是
A.三种物质的沸点:
B.水中的溶解性:
C.与金属Na反应的剧烈程度:
D.键角:Y中的 中的
【答案】C
【解析】A. X中含有三个羟基,可以形成分子间氢键,沸点比Y大,Z属于盐,沸点最大,则三种
物质的沸点: ,A错误;B. Z属于钠盐,易溶于水,则水中的溶解性: ,B错误;
C. S的非金属性较弱,则S—H键更容易断裂,更容易和钠反应,C正确;D. 两个分子中,S和O
的价层电子对相同,孤电子对也相同,但O的电负性比S大,则X中电子对之间的斥力更大,键角更大,D错误;故选C。
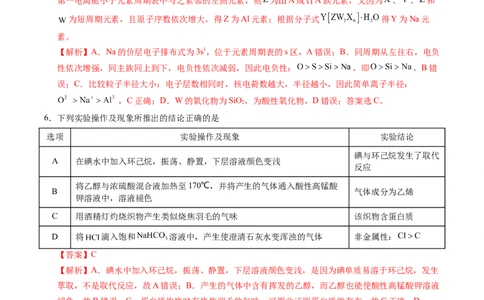
3.实验室可通过如图所示装置浓缩双氧水(夹持装置略,常压下 的沸点为150℃),下列叙述错误的是
A.仪器A能用蒸馏烧瓶代替 B.实验时可撤去减压系统
C.毛细管的主要作用是防暴沸 D.通空气能起到搅拌、加速水挥发的作用
【答案】B
【分析】常压下 的沸点为150℃, 易分解,则需在减压下浓缩 ,空气流入毛细管对烧
瓶中的溶液进行搅拌,同时还能加速水逸出。
【解析】A.蒸馏烧瓶的上口可通空气、支管可接冷凝和减压系统,则仪器A能用蒸馏烧瓶代替,A正
确;B.常压下 的沸点为150℃, 易分解,则需在减压下浓缩 ,实验时不可撤去减压
系统,B不正确;C.空气流入毛细管可以对烧瓶中的溶液防止暴沸,C正确;D.通入的空气从毛细
管逸出,能起到搅拌作用,同时加速水挥发,D正确;答案选B。
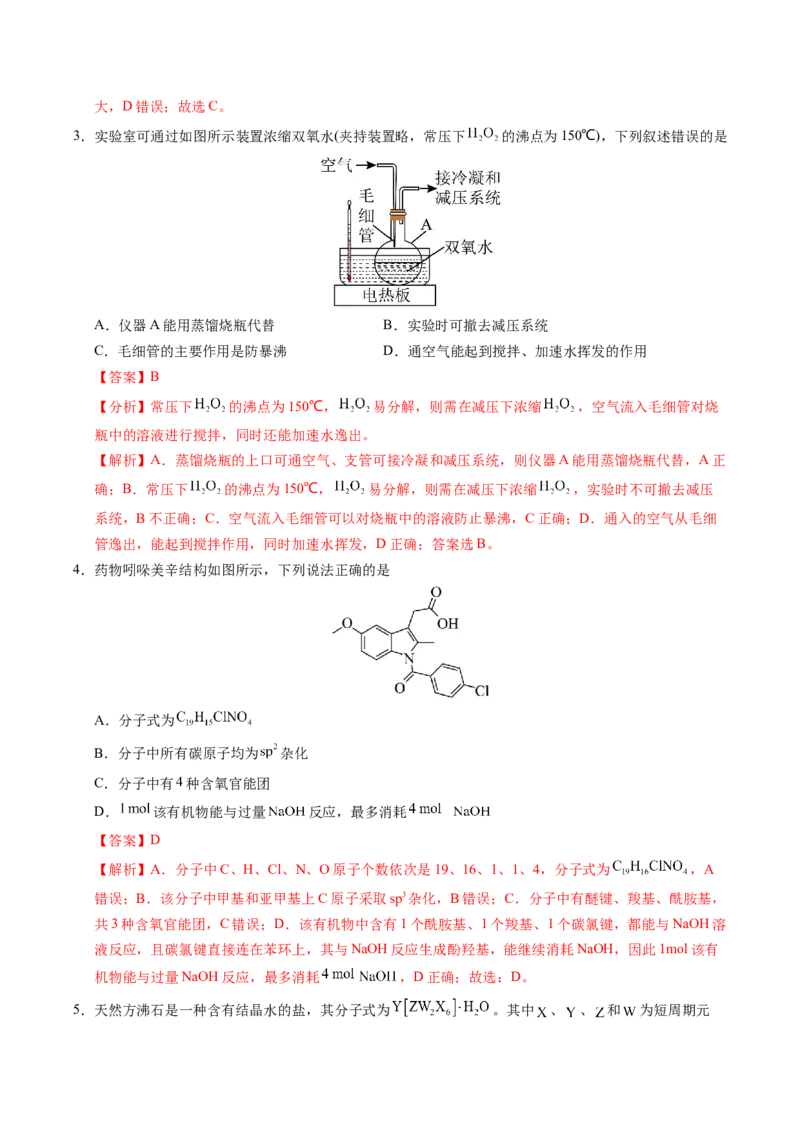
4.药物吲哚美辛结构如图所示,下列说法正确的是
A.分子式为
B.分子中所有碳原子均为 杂化
C.分子中有 种含氧官能团
D. 该有机物能与过量 反应,最多消耗
【答案】D
【解析】A.分子中C、H、Cl、N、O原子个数依次是19、16、1、1、4,分子式为 ,A
错误;B.该分子中甲基和亚甲基上C原子采取sp3杂化,B错误;C.分子中有醚键、羧基、酰胺基,
共3种含氧官能团,C错误;D.该有机物中含有1个酰胺基、1个羧基、1个碳氯键,都能与NaOH溶
液反应,且碳氯键直接连在苯环上,其与NaOH反应生成酚羟基,能继续消耗NaOH,因此1mol该有
机物能与过量NaOH反应,最多消耗 ,D正确;故选:D。
5.天然方沸石是一种含有结晶水的盐,其分子式为 。其中 、 、 和 为短周期元素,且原子序数依次增大。 的某种单质可滤除大气中的大量紫外线,保护地球生物, 的第一电离
能小于元素周期表中与之紧邻的左侧元素,基态 原子未成对电子数为2个,其单质及氧化物均为常
见的共价晶体。下列说法正确的是
A. 位于元素周期表的 区 B.电负性:
C.简单离子半径: D.W的氧化物具有两性
【答案】C
【分析】 的某种单质可滤除大气中的大量紫外线,保护地球生物,此单质应为臭氧,因此 为O元
素;基态 原子未成对电子数为2个,其单质及氧化物均为常见的共价晶体,因此 为Si元素; 的
第一电离能小于元素周期表中与之紧邻的左侧元素,则 为ⅢA或ⅥA族元素,又因为 、 、 和
为短周期元素,且原子序数依次增大,得Z为Al元素;根据分子式 得Y为Na元
素。
【解析】A.Na的价层电子排布式为3s1,位于元素周期表的s区,A错误;B.同周期从左往右,电负
性依次增强,同主族同上到下,电负性依次减弱,因此电负性: ,即 ,B错
误;C.比较粒子半径大小:电子层数相同时,核电荷数越大,半径越小,因此简单离子半径:
,C正确;D.W的氧化物为SiO,为酸性氧化物,D错误;答案选C。
2
6.下列实验操作及现象所推出的结论正确的是
选项 实验操作及现象 实验结论
碘与环己烷发生了取代
A 在碘水中加入环己烷,振荡、静置,下层溶液颜色变浅
反应
将乙醇与浓硫酸混合液加热至170℃,并将产生的气体通入酸性高锰酸
B 气体成分为乙烯
钾溶液中,溶液褪色
C 用酒精灯灼烧织物产生类似烧焦羽毛的气味 该织物含蛋白质
D 将 滴入饱和 溶液中,产生使澄清石灰水变浑浊的气体 非金属性:
【答案】C
【解析】A.碘水中加入环己烷,振荡、静置,下层溶液颜色变浅,是因为碘单质易溶于环己烷,发生
萃取,不是取代反应,故A错误;B.产生的气体中含有挥发的乙醇,而乙醇也能使酸性高锰酸钾溶液
褪色,故B错误;C.蛋白质灼烧时有烧焦羽毛的气味,可据此证明蛋白质的存在,故C正确;D.
HCl不是最高价氧化物的水化物,不能根据盐酸酸性强于碳酸得出非金属性: ,故D错误;故
选:C。
7. 能与 反应生成一系列高附加值的化学品,其碳元素转化关系如下图所示。设 为阿伏加德罗
常数的值,下列说法正确的是A.反应①每生成 ,消耗 分子数目为
B.标准状况下, 中含中子数目为
C.反应③每生成 ,转移电子数目为
D. 溶液中含H原子数目为
【答案】A
【解析】A.反应①为CO+4H =CH +2H O,每生成 ,消耗 分子数目为 ,A正确;B.
2 2 4 2
标准状况下, 物质的量为0.1mol,HCHO中中子数为6+8=14个,故 中含中子
数目为 ,B错误;C.反应③中CO→ 从+4价到-2价,每生成 即0.1mol,转
2
移电子数目为 ,C错误;D. 溶液中HCOOH和HO中都含H原子,故H原子数目大于
2
,D错误;答案选A。
8.分银渣是从阳极泥中提取贵金属后的尾渣,有 、 、 及Au、Ag等,具有较高的综合
利用价值。一种从分银渣中提取有用产品流程的如下:
已知: ;v中生成 和 ; 、 、
、 的 依次为 、 、 、 。
下列说法不正确的是
A.步骤ⅰ中一定发生反应:
B.步骤ⅰ、ⅲ后需先过滤再加盐酸
C.步骤ⅱ、ⅳ提取Pb(Ⅱ)、 时,均有 和 参加反应
D.试剂a可为NaCl,促进Au、Ag的浸出
【答案】C
【分析】已知 、 的 分别为 、 ,分银渣中有 、 、
及Au、Ag等,向分银渣中加入 溶液,发生沉淀转化反应:
, 会转化为 ,过滤,弃去含有 的滤
液,然后向滤渣中加入盐酸,发生反应 、、 ;然后过滤,得到含有Pb(Ⅱ)的
溶液,向固体A中加入 溶液,发生反应 ,过滤,
弃去含有 的滤液,然后向滤渣中加入盐酸,发生反应 ,得到
含有Ba2+的溶液;再过滤,向固体B中加入NaClO、HCl,在酸性条件下NaClO 可以将Au、Ag氧化
3 3
为金属阳离子,并与溶液中的Cl-结合形成络离子 和 ; 不反应,仍以固体形式
存在。
【解析】A.步骤ⅰ中加入 溶液, 固体会转化为 ,故步骤ⅰ中一定发生反应:
,A正确;B.根据分析可知,步骤ⅰ、ⅲ后需先过滤再
加盐酸,B正确;C.步骤ⅳ发生的反应是 ,故 没有参加反
应,C错误;D.试剂a可为NaCl,促进Pb(Ⅱ)的浸出,NaCl的加入,增大了溶液中c(Cl-),促进
Au、Ag形成配合物,使Au、Ag变成络离子 和 进入溶液,有利于Au、Ag的浸出,
D正确;故选C。
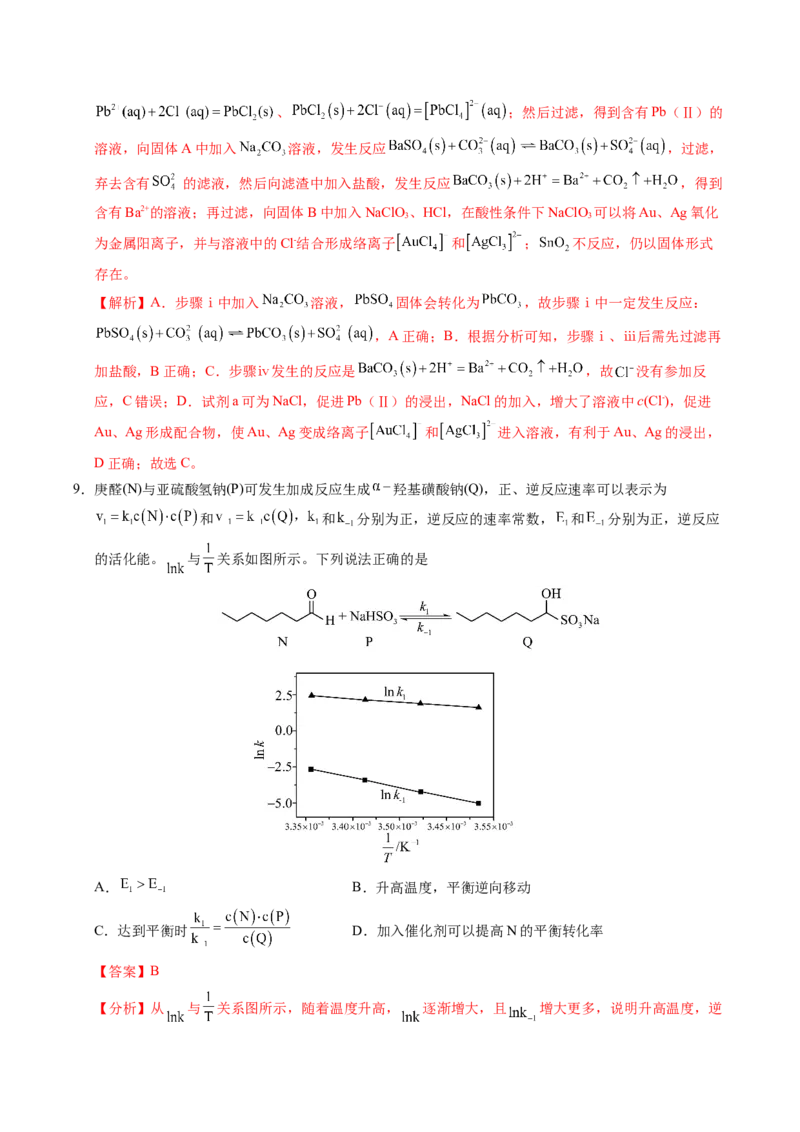
9.庚醛(N)与亚硫酸氢钠(P)可发生加成反应生成 羟基磺酸钠(Q),正、逆反应速率可以表示为
和 和 分别为正,逆反应的速率常数, 和 分别为正,逆反应
的活化能。 与 关系如图所示。下列说法正确的是
A. B.升高温度,平衡逆向移动
C.达到平衡时 D.加入催化剂可以提高N的平衡转化率
【答案】B
【分析】从 与 关系图所示,随着温度升高, 逐渐增大,且 增大更多,说明升高温度,逆反应速率增加更多,平衡应逆向移动,则该反应正向应为放热反应。
【解析】A.该反应为放热反应,所以正反应活化能更小,即 ,A错误;B.该反应正向为放热
反应,升高温度,平衡逆向移动,B正确;C.达到平衡时正逆反应速率相等,则有 ,所以
,C错误;D.加入催化剂可加快反应速率,但不影响平衡移动,不会提高N的平衡
转化率,D错误;故选B。
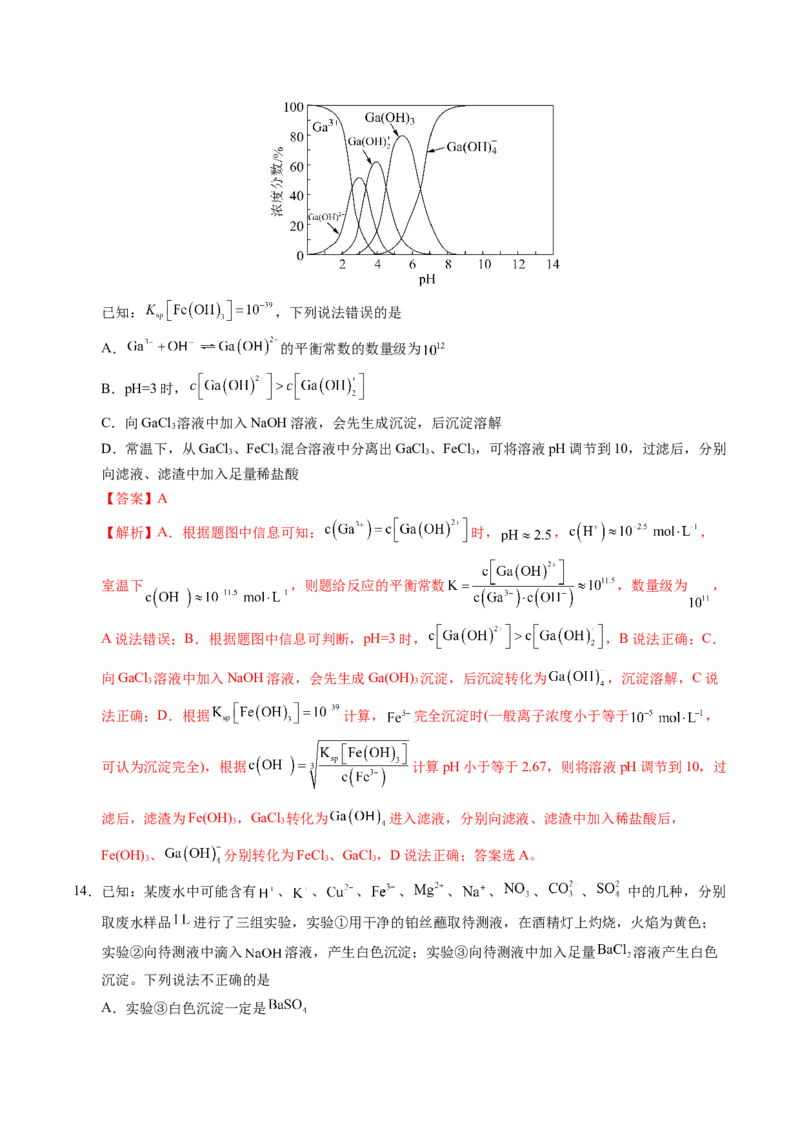
10.复旦大学一课题组首次实现了以(杂)芳基磺酰氯( )为引发剂的有机催化光调控活性聚合(如
图)。图中R、R'为烷基,Ar为芳基。下列说法错误的是
A.X能发生氧化反应、还原反应和加聚反应 B.Y遇水能发生取代反应生成
C.M分子中C、N均只采用 杂化 D.Z是线型高分子材料,具有热塑性
【答案】C
【解析】A.X含有碳碳双键,能与酸性高锰酸钾溶液发生氧化反应,在一定条件下发生加聚反应,
与氢气发生加成反应也属于还原反应,故A正确;B.Y中S-Cl遇水能发生取代反应得到S-OH,可
生成ArSO H,故B正确;C.M分子中R'为烷基,碳原子的价层电子对数是4,所以碳原子的杂化方
3
式都sp3杂化,故C错误;D.Z是线型高分子材料,可以重复加热融化,具有热塑性,可以反复加
工,多次使用,故D正确;故选C。
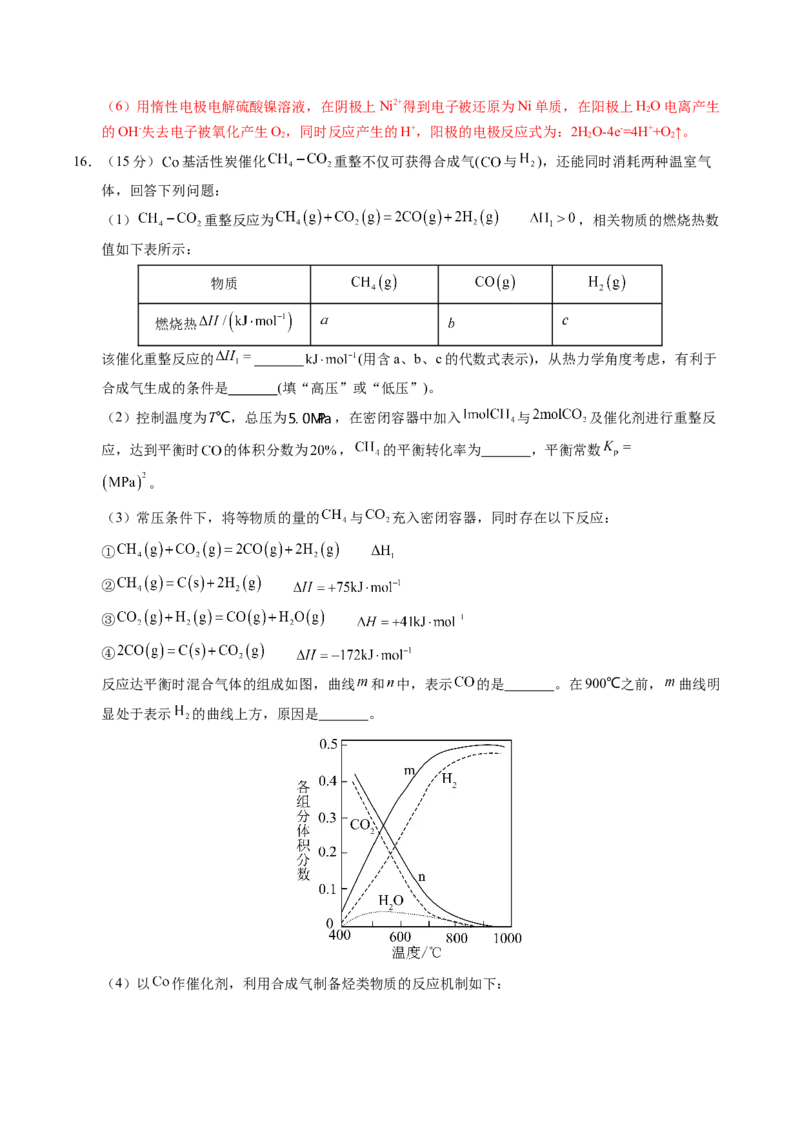
11.低空经济为新能源电池拓宽了应用场景。一种新型光伏电池工作原理如图所示,其中 为电解
质溶液。太阳光照下,敏化后的 产生电子 和空穴 ,驱动电流产生和离子移动。下列说法
错误的是
A.电池工作时,涉及光能转化为电能
B.敏化 电极是负极
C. 电极反应为:D.光敏化剂结构中,中心离子 的配位数是6
【答案】C
【分析】太阳光照射TiO 电极上,敏化后的TiO 失去电子为原电池的负极,Pt电极为正极;【解析】
2 2
A.该装置是光伏电池,太阳光照下敏化后的 产生电子 和空穴 ,驱动电流产生和离子移
动,所以电池工作时,涉及光能转化为电能,A正确;B.太阳光照下,敏化后的 产生电子
和空穴 ,即敏化 电极失电子为负极,B正确;C. 电极为正极,发生得电子还原反应,
电极电极反应为: ,C错误;D.由图可知,光敏化剂结构中,中心离子 与6个N
原子成键,配位数是6,D正确;答案选C。
12.已知合金 的立方晶胞结构如图1所示, 原子以金刚石方式堆积,八面体空隙和半数的四
面体空隙中填入 四面体:沿 轴投影晶胞中所有 原子的分布图如图2所示, 点的分数坐标
为 。设晶胞参数为 , 的摩尔质量为 , 为阿伏加德罗常数的值。
下列说法错误的是
A.电负性: B.B点的分数坐标为
C.A、C两原子间的距离为 D.该晶体的密度为
【答案】C
【解析】A.Na与Al同周期,同周期主族元素的电负性从左至右逐渐增大,故电负性: ,A
正确;B.A点的分数坐标为 ,可得B点的分数坐标为 ,B正确;C.由图2可知,
A、C两点之间的距离为体对角线的 ,故A、C两原子间的距离为 ,C错误;D.根据均摊
法可知该晶胞中含有Na原子的数量为 ,则每个晶胞中含有4个 ,故晶胞的
密度为 ,D正确;答案选C。
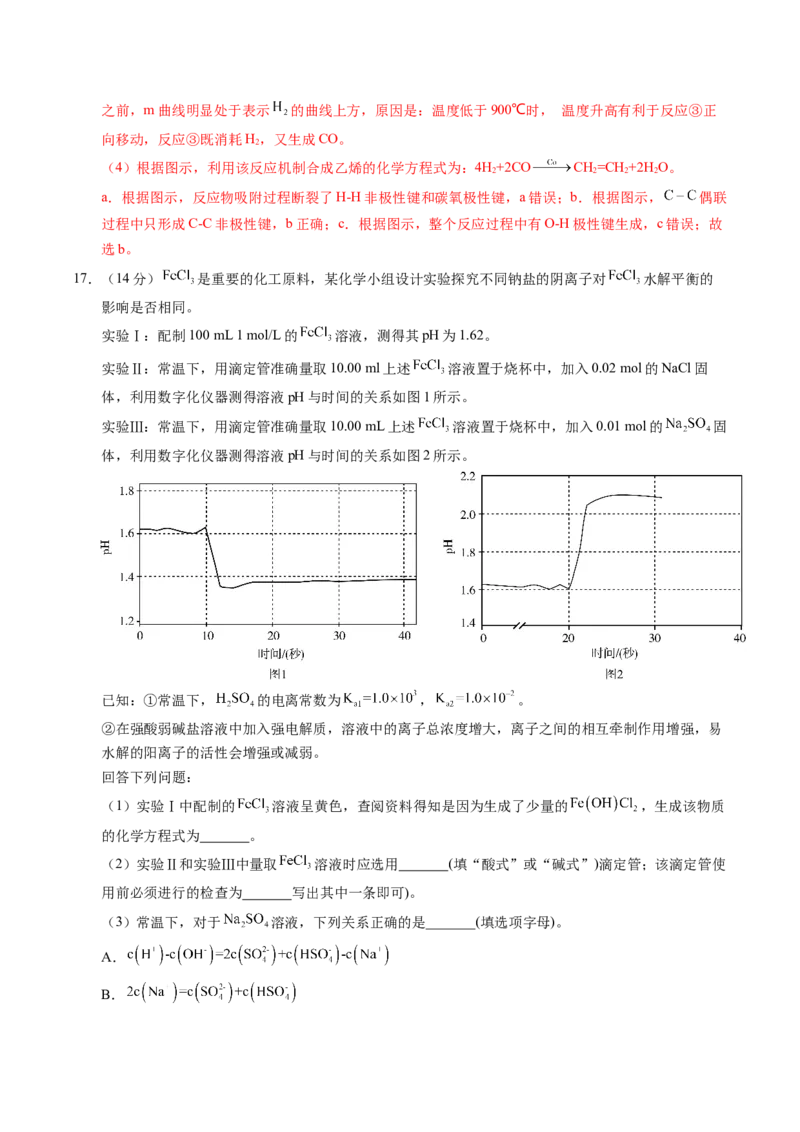
13.室温下,调节GaCl 溶液的pH,测定含Ga微粒的浓度分数随pH的变化情况如图所示:
3已知: ,下列说法错误的是
A. 的平衡常数的数量级为
B.pH=3时,
C.向GaCl 溶液中加入NaOH溶液,会先生成沉淀,后沉淀溶解
3
D.常温下,从GaCl 、FeCl 混合溶液中分离出GaCl 、FeCl ,可将溶液pH调节到10,过滤后,分别
3 3 3 3
向滤液、滤渣中加入足量稀盐酸
【答案】A
【解析】A.根据题图中信息可知: 时, , ,
室温下 ,则题给反应的平衡常数 ,数量级为 ,
A说法错误;B.根据题图中信息可判断,pH=3时, ,B说法正确;C.
向GaCl 溶液中加入NaOH溶液,会先生成Ga(OH) 沉淀,后沉淀转化为 ,沉淀溶解,C说
3 3
法正确;D.根据 计算, 完全沉淀时(一般离子浓度小于等于 ,
可认为沉淀完全),根据 计算pH小于等于2.67,则将溶液pH调节到10,过
滤后,滤渣为Fe(OH) ,GaCl 转化为 进入滤液,分别向滤液、滤渣中加入稀盐酸后,
3 3
Fe(OH) 、 分别转化为FeCl 、GaCl ,D说法正确;答案选A。
3 3 3
14.已知:某废水中可能含有 、 、 、 、 、 、 、 、 中的几种,分别
取废水样品 进行了三组实验,实验①用干净的铂丝蘸取待测液,在酒精灯上灼烧,火焰为黄色;
实验②向待测液中滴入 溶液,产生白色沉淀;实验③向待测液中加入足量 溶液产生白色
沉淀。下列说法不正确的是
A.实验③白色沉淀一定是B.废水中一定存在的阴离子为 ,一定不存在的阴离子为
C.废水中一定存在的阳离子为 、 ,一定不存在的阳离子为 、 、
D.若实验②和实验③沉淀的物质的量均为 ,则废水中一定含有
【答案】C
【分析】①用干净的铂丝蘸取待测液,在酒精灯上灼烧,火焰为黄色,说明废水中含Na+;实验②向
待测液中滴入NaOH溶液,产生白色沉淀,说明废水中含Mg2+,由于生成的是白色沉淀,所以不含
Cu2+、Fe3+,MgCO 是微溶物,所以不存在 ;实验③向待测液中加入足量BaCl 溶液产生白色沉
3 2
淀说明废水中含 。据此分析解答。
【解析】A.根据分析可知原溶液不含有 ,则和BaCl 生成的白色沉淀为BaSO,故A正确;
2 4
B.根据分析可知废水中一定存在的阴离子为 ,一定不存在的阴离子为 ,故B正确;C.根
据分析可知废水中一定存在的阳离子为Na+和Mg2+,一定不存在的阳离子为Cu2+和Fe3+,不能确定
K+存在与否,故C错误;D.实验②得到沉淀Mg(OH) 的物质的量为1mol,则Mg2+为1mol,实验③
2
得到的沉淀BaSO,物质的量为1mol,则含1mol ,阳离子还有Na+,根据电荷守恒,废水中一定
4
还有 ,故D正确;故选:C。
二、选择题:本题共4小题,共58分。
15.(14分)从失活催化剂(主要成分为Al O、Fe O、SiO、NiO、VO)中回收镍的一种工艺流程如下图
2 3 2 3 2 2 5
所示。
已知:常温时,该工艺条件下金属离子形成沉淀时lgc(M)与溶液pH的关系如下图所示:
回答下列问题:
(1)基态Ni原子的价电子轨道表示式为 。
(2)工业上用焦炭还原“滤渣1”可以制备某单质,该反应的化学方程式为 。
(3)常温下,五价钒在酸浸液中以 形式存在,在6.0≤pH≤8.0时以 形式存在。“调节pH”
时,五价钒发生变化的离子方程式为 ,“调节pH”的范围是 。(4)常温下,Fe(OH) 的K = 。
3 sp
(5)实验室中萃取分液操作需要用到的玻璃仪器有 。
(6)若采用惰性电极电解硫酸镍溶液制镍,阳极的电极反应式为 。
【答案】(1) (2分)
(2) (2分)
(3) (2分) 6.0≤pH<7.6(或6.0~7.6)(2分)
(4)10-37.4(2分)
(5)分液漏斗、烧杯(2分)
(6)2HO-4e-=4H++O ↑(2分)
2 2
【分析】失活催化剂中主要成分为Al O、Fe O、SiO、NiO、VO,向其中加入稀硫酸,金属氧化物
2 3 2 3 2 2 5
反应变为可溶性硫酸盐进入溶液中,只有酸性氧化物SiO 不与稀硫酸反应,仍以固体形式存在,因此
2
得到滤渣1中含有SiO,同时在产生含有可溶性硫酸盐的滤液,主要含有Al3+、Fe3+、Ni2+、 ;向
2
滤液中加入NaOH溶液,调整溶液pH至6.0-7.6,Al3+转化为Al(OH) 沉淀,Fe3+形成Fe(OH) 沉淀,
3 3
变为 ,Ni2+不反应仍然存在于溶液中;再加入萃取剂萃取溶液中的镍元素,分液得到含有
Ni2+的有机相和含有 水相;向水相中加入硫酸溶液,将镍离子反萃取入水相,电解硫酸镍溶液可
得金属镍。
【解析】(1)Ni是28号元素,根据构造原理可知:基态Ni原子的价电子排布式为3d84s2,故其价电
子轨道表示式为 ;
(2)根据上述分析可知: “滤渣1”是SiO,工业上用焦炭还原二氧化硅可以制备硅单质,同时生成
2
CO气体,该反应的化学方程式为: ;
(3)在酸性溶液中钒元素以 的形式存在,根据图示可知Ni2+开始形成Ni(OH) 沉淀的pH=7.6,
2
故当加入NaOH“调节pH”在6.0≤pH≤7.6时,钒元素以 形式存在,而Ni2+不能反应,仍以Ni2+的形
式存在于溶液中“调节pH”时,五价钒发生变化的离子方程式为将 转化为 的离子方程式为:
;
(4)室温下,当溶液中c(Fe3+)=1.0×10-5mol/L时,认为Fe3+沉淀完全,此时溶液的pH=3.2,c(H+)=10-
3.2mol/L,则此时溶液中c(OH-)= ,故常温下Fe(OH) 的溶度积
3
常数 ;
(5)在实验室中进行萃取、分液操作需要用到的玻璃仪器为分液漏斗、烧杯;(6)用惰性电极电解硫酸镍溶液,在阴极上Ni2+得到电子被还原为Ni单质,在阳极上HO电离产生
2
的OH-失去电子被氧化产生O,同时反应产生的H+,阳极的电极反应式为:2HO-4e-=4H++O ↑。
2 2 2
16.(15分) 基活性炭催化 重整不仅可获得合成气( 与 ),还能同时消耗两种温室气
体,回答下列问题:
(1) 重整反应为 ,相关物质的燃烧热数
值如下表所示:
物质
燃烧热
该催化重整反应的 (用含a、b、c的代数式表示),从热力学角度考虑,有利于
合成气生成的条件是 (填“高压”或“低压”)。
(2)控制温度为 ,总压为 ,在密闭容器中加入 与 及催化剂进行重整反
应,达到平衡时 的体积分数为 , 的平衡转化率为 ,平衡常数
。
(3)常压条件下,将等物质的量的 与 充入密闭容器,同时存在以下反应:
①
②
③
④
反应达平衡时混合气体的组成如图,曲线 和 中,表示 的是 。在900℃之前, 曲线明
显处于表示 的曲线上方,原因是 。
(4)以 作催化剂,利用合成气制备烃类物质的反应机制如下:根据图示,利用该反应机制合成乙烯的化学方程式为 。下列说法正确的是 (填序号)。
a.反应物吸附过程只断裂极性键
b. 偶联过程中只形成非极性键
c.整个反应过程中无极性键生成
【答案】(1)(a-2b-2c)(2分) 低压(1分)
(2)37.5%(2分) 0.55(2分)
(3)m(2分) 温度低于900℃时, 温度升高有利于反应③正向移动,反应③既消耗H,又生
2
成CO(2分)
(4)4H+2CO CH=CH +2H O (2分) b(2分)
2 2 2 2
【解析】(1)由 、 、 的燃烧热数值可知①
;② ;③
;由盖斯定律①-2×②-2×③可得 (a-2b-2c)
;该反应是气体体积增大的反应,从热力学角度考虑,有利于合成气生成的条件是低压。
(2)根据已知条件列出“三段式”
达到平衡时CO的体积分数为 20%,解得x=0.375mol, 的平衡转化率为
=37.5%,因控制总压为5.0 ,则平衡常数 =0.55 。
(3)由盖斯定律可知,反应②-反应④可得反应①
,反应①和反应③是吸热反应,反应④是放热反应,升
高温度反应①和反应③正向移动,反应④逆向移动,CO的体积分数增大,则表示CO的是m,900℃之前,m曲线明显处于表示 的曲线上方,原因是:温度低于900℃时, 温度升高有利于反应③正
向移动,反应③既消耗H,又生成CO。
2
(4)根据图示,利用该反应机制合成乙烯的化学方程式为:4H+2CO CH=CH +2H O。
2 2 2 2
a.根据图示,反应物吸附过程断裂了H-H非极性键和碳氧极性键,a错误;b.根据图示, 偶联
过程中只形成C-C非极性键,b正确;c.根据图示,整个反应过程中有O-H极性键生成,c错误;故
选b。
17.(14分) 是重要的化工原料,某化学小组设计实验探究不同钠盐的阴离子对 水解平衡的
影响是否相同。
实验Ⅰ:配制100 mL 1 mol/L的 溶液,测得其pH为1.62。
实验Ⅱ:常温下,用滴定管准确量取10.00 ml上述 溶液置于烧杯中,加入0.02 mol的NaCl固
体,利用数字化仪器测得溶液pH与时间的关系如图1所示。
实验Ⅲ:常温下,用滴定管准确量取10.00 mL上述 溶液置于烧杯中,加入0.01 mol的 固
体,利用数字化仪器测得溶液pH与时间的关系如图2所示。
已知:①常温下, 的电离常数为 , 。
②在强酸弱碱盐溶液中加入强电解质,溶液中的离子总浓度增大,离子之间的相互牵制作用增强,易
水解的阳离子的活性会增强或减弱。
回答下列问题:
(1)实验Ⅰ中配制的 溶液呈黄色,查阅资料得知是因为生成了少量的 ,生成该物质
的化学方程式为 。
(2)实验Ⅱ和实验Ⅲ中量取 溶液时应选用 (填“酸式”或“碱式”)滴定管;该滴定管使
用前必须进行的检查为 写出其中一条即可)。
(3)常温下,对于 溶液,下列关系正确的是_______(填选项字母)。
A.
B.C. 的平衡常数
D.
(4)图1中10s后溶液的pH下降的主要原因为 。
(5)实验Ⅱ和实验Ⅰ中,加入NaCl固体和 固体的物质的量之比为2∶1的原因为 。
(6)图2中20s后溶液pH增大的主要原因为 。结合图1和图2得出的实验结论:不同的钠盐
对 溶液水解平衡的影响是不同的。
【答案】(1) (2分)
(2)酸式(2分) 检漏(2分)
(3)AC(2分)
(4)加入NaCl固体后,离子总浓度增大,离子之间的相互牵制作用增强,导致 的活性增强,水
解程度增大(2分)
(5)控制溶液中的 相同,排除由于 不同对实验结果的影响(2分)
(6)加入 固体后,硫酸根离子浓度变大, ,平衡正向移动导致溶液中
减小(2分)
【分析】控制变量法研究不同因素对实验的影响要注意控制变量,使变量以外的其它量均相同;
【解析】(1)根据质量守恒可知,氯化铁和水生成 ,化学方程式为
;(2)氯化铁溶液中铁离子水解使溶液显酸性,故量取 溶液
时应选用酸式滴定管;该滴定管使用前必须进行的检查为检漏,防止漏液;(3)A.由电荷守恒可知
,则 ,A
项正确;B.由物料守恒可知 ,B项错误;C.由 的电离常数为
可知 的平衡常数 ,C项正确;D.由质子守恒
可知 ,D项错误;故选AC;(4)已知②原理可知,加入NaCl固体后,离
子总浓度增大,离子之间的相互牵制作用增强,导致 的活性增强,水解程度增大;(5)由控制
变量法可知,加入NaCl固体和 固体的物质的量之比为2:1的原因是排除由于 不同对
实验结果的影响;故答案为:控制溶液中的 相同,排除由于 不同对实验结果的影响;
(6)已知:常温下, 的电离常数为 , 。则加入 固体后,硫
酸根离子浓度变大, ,平衡正向移动导致溶液中 减小,溶液的pH增大;
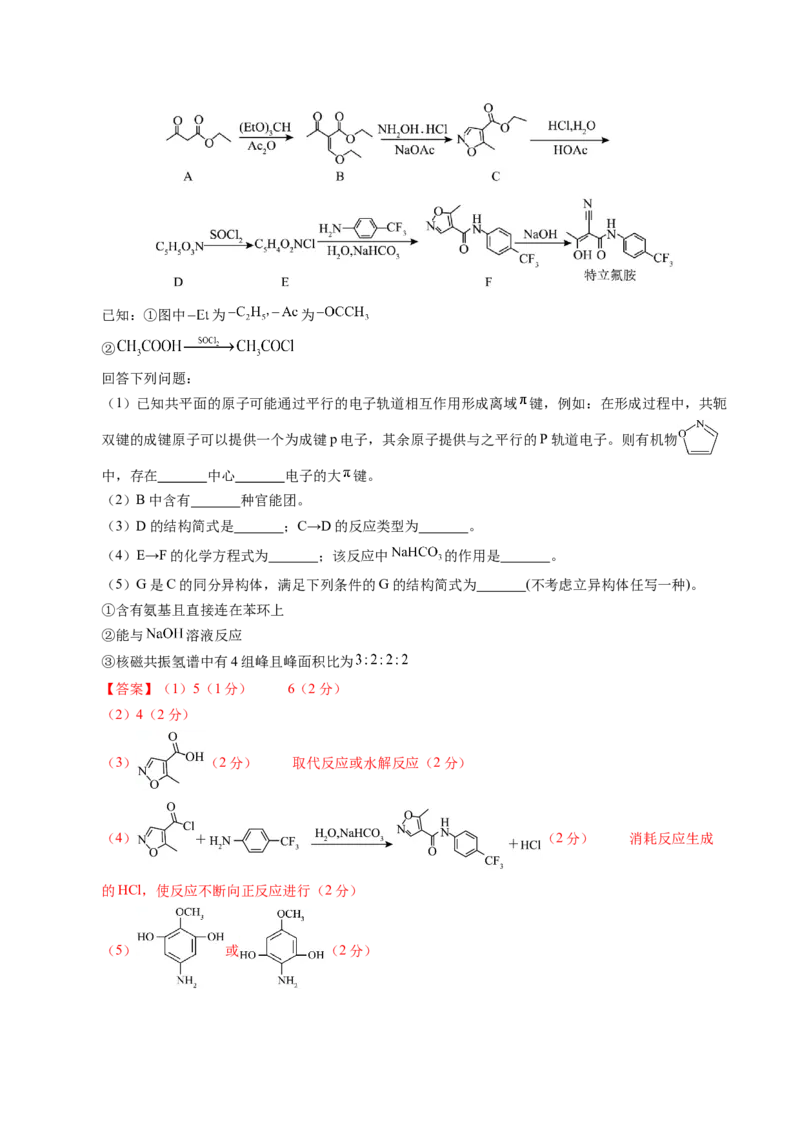
18.(15分)特立氟胺是一种口服嘧啶合成酶抑制剂和免疫调节剂,其合成路线如下:已知:①图中 为 为
②
回答下列问题:
(1)已知共平面的原子可能通过平行的电子轨道相互作用形成离域 键,例如:在形成过程中,共轭
双键的成键原子可以提供一个为成键p电子,其余原子提供与之平行的P轨道电子。则有机物
中,存在 中心 电子的大 键。
(2)B中含有 种官能团。
(3)D的结构简式是 ;C→D的反应类型为 。
(4)E→F的化学方程式为 ;该反应中 的作用是 。
(5)G是C的同分异构体,满足下列条件的G的结构简式为 (不考虑立异构体任写一种)。
①含有氨基且直接连在苯环上
②能与 溶液反应
③核磁共振氢谱中有4组峰且峰面积比为
【答案】(1)5(1分) 6(2分)
(2)4(2分)
(3) (2分) 取代反应或水解反应(2分)
(4) (2分) 消耗反应生成
的HCl,使反应不断向正反应进行(2分)
(5) 或 (2分)【解析】(1)有机物 中,形成大π键的原子为5个,碳碳双键中每个碳原子提供一个电子参与
形成大π键,碳氮双键的N原子和C原子也提供一个电子参与形成大π键,O原子提供2个电子参与
形成大π键,存在5中心6电子的大π键;
(2)根据B的结构简式可知,所含官能团有:酮羰基、碳碳双键、醚键、酯基,共有4种官能团;
(3)根据分析可知,D的结构简式为 ;C→D的反应类型为:取代反应或水解反应;
(4)根据分析可知,E的结构简式为 ,E与 发生取代反应生成F,反应
的化学方程式为 ;该反应中
NaHCO 的作用是:消耗反应生成的HCl,使反应不断向正反应进行;
3
(5)C为 ,分子式为:C HNO ,不饱和度为4,G是C的同分异构体,满足①含有氨
7 9 3
基且直接连在苯环上,②能与 溶液反应,③核磁共振氢谱中有4组峰且峰面积比为 ,
说明含有一个甲基和两个酚羟基,因此满足下列条件的G的结构简式为 或
。