文档内容
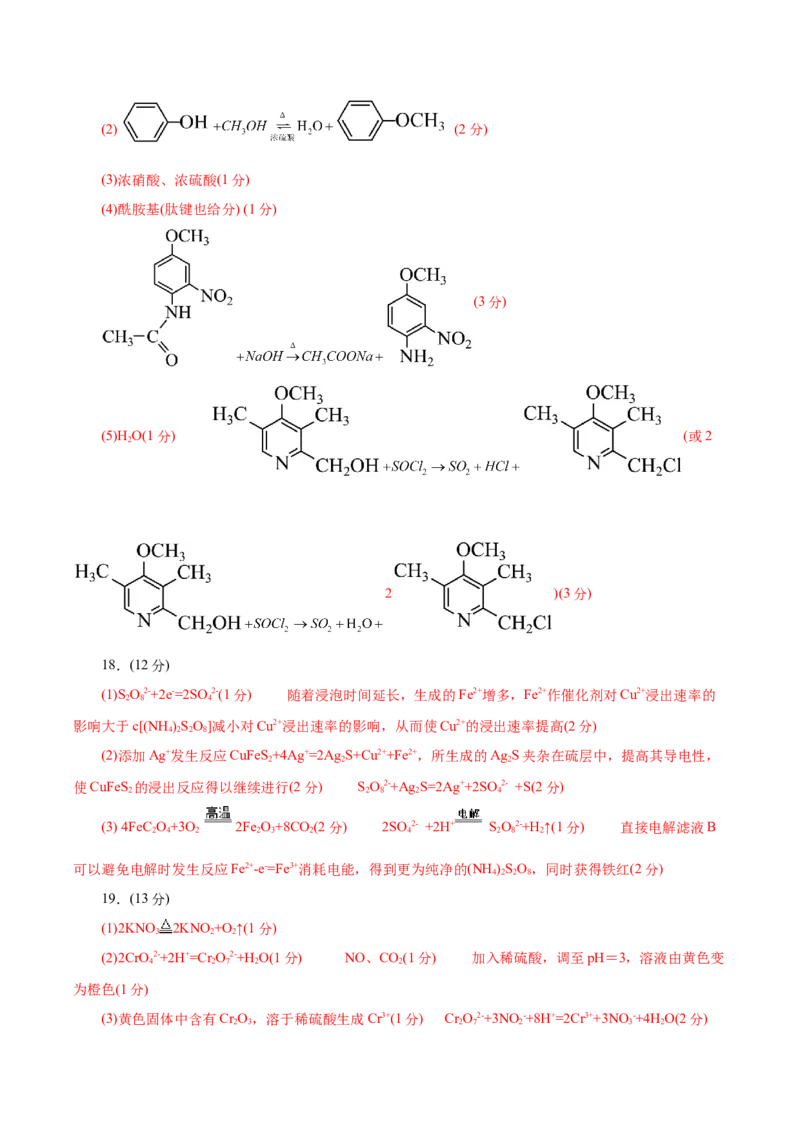
2025 年高考考前信息必刷卷 04(北京专用)
化 学·参考答案
第一部分
一、选择题(本部分共14题,每题3分,共42分。在每题列出的四个选项中,选出最符合题目要求的
一项。)
1 2 3 4 5 6 7 8 9 10 11 12 13 14
A A B B A C D A B B A A D B
第二部分
二、非选择题(本部分共5题,共58分。)
15.(9分)
(1)3(1分) (1分)
(2) (2分)
(3)AC(2分) (4)6(1分) (5) sp2(1分) 弱(1分)
16.(12分)
(1)升高温度(1分) 减小压强(1分)
(2)正向(1分) 110(2分) 15(2分)
(3) ΔH-2ΔH(1分)
3 4
(4)a(1分)
(5)体系未达到平衡,温度升高,生成CO的反应速率增大的程度大于生成C H 的速率(1分)
2 4
AB(2分)
17.(12分)
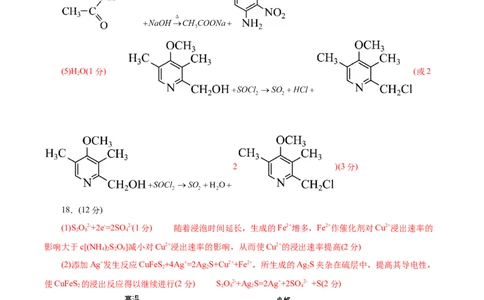
(1)苯酚(1分)(2) (2分)
(3)浓硝酸、浓硫酸(1分)
(4)酰胺基(肽键也给分) (1分)
(3分)
(5)H O(1分) (或2
2
2 )(3分)
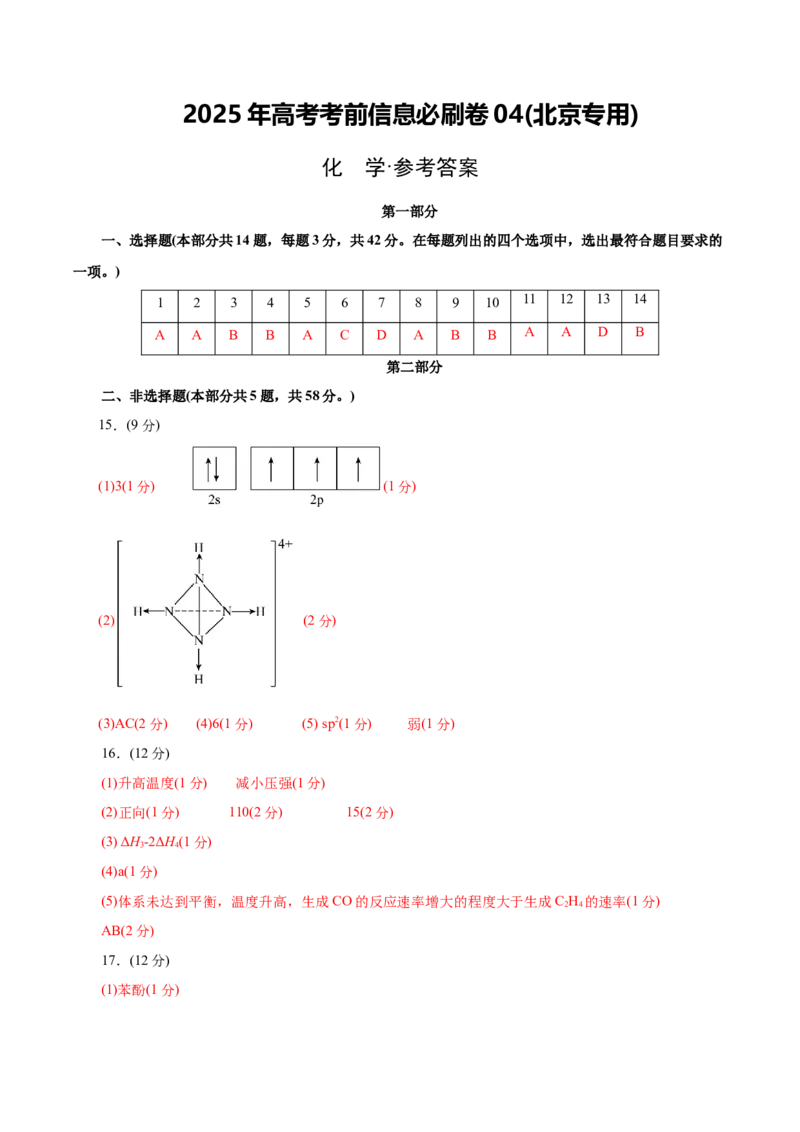
18.(12分)
(1)S O2-+2e-=2SO2-(1分) 随着浸泡时间延长,生成的Fe2+增多,Fe2+作催化剂对Cu2+浸出速率的
2 8 4
影响大于c[(NH )SO]减小对Cu2+浸出速率的影响,从而使Cu2+的浸出速率提高(2分)
4 2 2 8
(2)添加Ag+发生反应CuFeS+4Ag+=2Ag S+Cu2++Fe2+,所生成的Ag S夹杂在硫层中,提高其导电性,
2 2 2
使CuFeS 的浸出反应得以继续进行(2分) S O2-+Ag S=2Ag++2SO2- +S(2分)
2 2 8 2 4
(3) 4FeC O+3O 2Fe O+8CO (2分) 2SO 2- +2H+ SO2-+H ↑(1分) 直接电解滤液B
2 4 2 2 3 2 4 2 8 2
可以避免电解时发生反应Fe2+-e-=Fe3+消耗电能,得到更为纯净的(NH )SO,同时获得铁红(2分)
4 2 2 8
19.(13分)
(1)2KNO 2KNO+O ↑(1分)
3 2 2
(2)2CrO 2-+2H+=Cr O2-+H O(1分) NO、CO(1分) 加入稀硫酸,调至pH=3,溶液由黄色变
4 2 7 2 2
为橙色(1分)
(3)黄色固体中含有Cr O,溶于稀硫酸生成Cr3+(1分) CrO2-+3NO-+8H+=2Cr3++3NO-+4H O(2分)
2 3 2 7 2 3 2Cr3++6NO-=[Cr(NO) ]3- (2分) [Cr(NO) ]3- Cr3++6NO-,加入HSO 溶液,NO -+H+=HNO ,且
2 6 6 2 2 4 2 2
HNO 易分解,c(NO -)减小,平衡正向移动,[Cr(NO) ]3-转化为Cr3+,溶液由玫瑰红色变为绿色(2分)
2 2 6
(4)实验Ⅱ中,过滤除去了Cr O,溶液中的c(H+)比实验Ⅰ中的小,Cr O2-的氧化性减弱的程度大于
2 3 2 7
HNO 的还原性增强的程度,使Cr O2-与HNO 不能反应生成Cr3+,溶液仍为橙色(2分)
2 2 7 2