文档内容
2024 年高考临考押题卷 01
化 学
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用
橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Cl 35.5 Ca 40 Mn 55 Cu 64 I 127
第Ⅰ卷(选择题 共 39 分)
一、选择题:本题共13小题,每小题3分,共39分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1.第19届亚运会秉持“绿色、智能、节俭、文明”办会理念。下列说法不正确的是( )
A. 亚运村餐厅“竹餐具”中含有丰富的多糖
B. 火炬燃料“零碳甲醇”燃烧不产生二氧化碳
C. 吉祥物“江南忆”机器人所用芯片的主要成分为硅
D. 火炬使用的“1070”铝合金具有硬度高、耐高温的特点
2.氮化镓是新型半导体材料。工业制备氮化镓的常用方法是 。下列叙述正确
的是
A.基态 原子电子排布式:
B. 的VSEPR模型:
C.基态 原子价层电子的轨道表示式:
D. 的电子式:
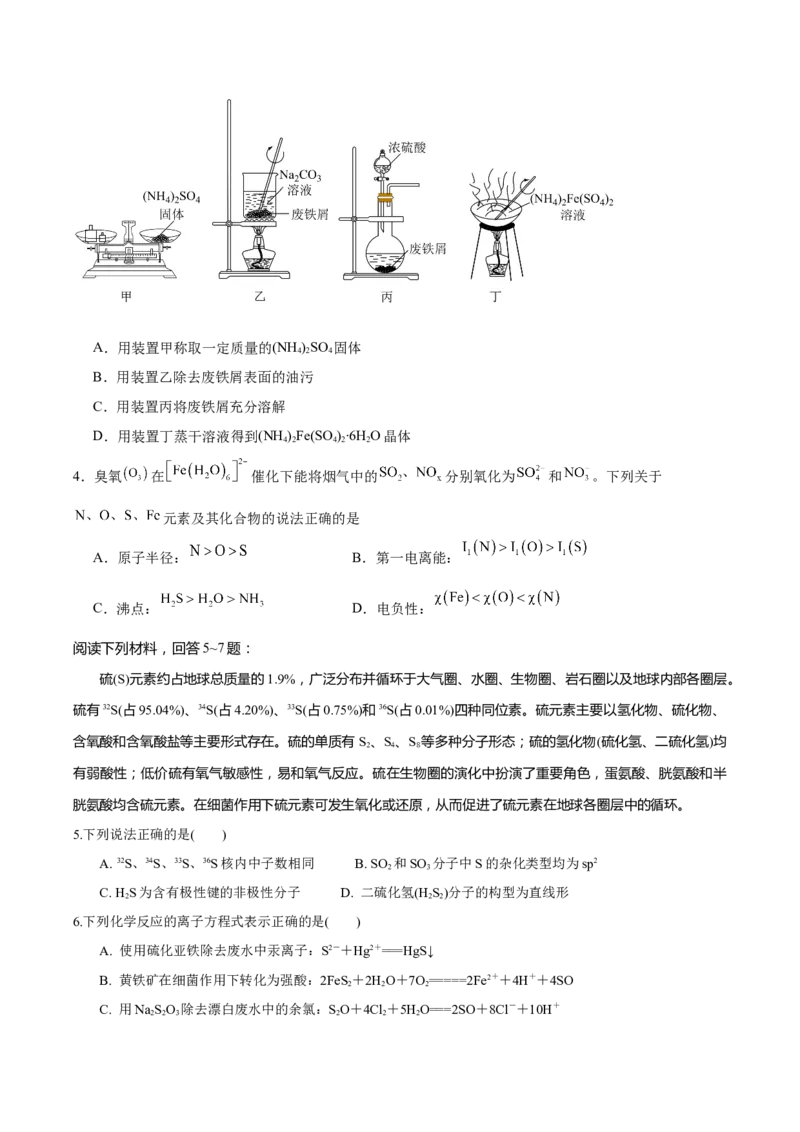
3.下列由废铁屑制取(NH )Fe(SO )∙6H O的实验装置与操作能达到实验目的的是
4 2 4 2 2A.用装置甲称取一定质量的(NH )SO 固体
4 2 4
B.用装置乙除去废铁屑表面的油污
C.用装置丙将废铁屑充分溶解
D.用装置丁蒸干溶液得到(NH )Fe(SO )∙6H O晶体
4 2 4 2 2
4.臭氧 在 催化下能将烟气中的 分别氧化为 和 。下列关于
元素及其化合物的说法正确的是
A.原子半径: B.第一电离能:
C.沸点: D.电负性:
阅读下列材料,回答5~7题:
硫(S)元素约占地球总质量的1.9%,广泛分布并循环于大气圈、水圈、生物圈、岩石圈以及地球内部各圈层。
硫有32S(占95.04%)、34S(占4.20%)、33S(占0.75%)和36S(占0.01%)四种同位素。硫元素主要以氢化物、硫化物、
含氧酸和含氧酸盐等主要形式存在。硫的单质有S、S、S 等多种分子形态;硫的氢化物(硫化氢、二硫化氢)均
2 4 8
有弱酸性;低价硫有氧气敏感性,易和氧气反应。硫在生物圈的演化中扮演了重要角色,蛋氨酸、胱氨酸和半
胱氨酸均含硫元素。在细菌作用下硫元素可发生氧化或还原,从而促进了硫元素在地球各圈层中的循环。
5.下列说法正确的是( )
A. 32S、34S、33S、36S核内中子数相同 B. SO 和SO 分子中S的杂化类型均为sp2
2 3
C. HS为含有极性键的非极性分子 D. 二硫化氢(HS)分子的构型为直线形
2 2 2
6.下列化学反应的离子方程式表示正确的是( )
A. 使用硫化亚铁除去废水中汞离子:S2-+Hg2+===HgS↓
B. 黄铁矿在细菌作用下转化为强酸:2FeS+2HO+7O=====2Fe2++4H++4SO
2 2 2
C. 用NaSO 除去漂白废水中的余氯:SO+4Cl+5HO===2SO+8Cl-+10H+
2 2 3 2 2 2D. 半 胱 氨 酸 [HOOCCH(NH)CHSH] 和 足 量 烧 碱 溶 液 反 应 : HSCH(NH)CHCOOH + OH -
2 2 2 2
===HSCH(NH)CHCOO-+HO
2 2 2
7.硫及其化合物的转化有着重要的应用。下列含硫物质的转化不正确的是( )
A. 实验室探究SO 的制备与性质:NaSO(s)――→SO(g)――→BaSO(s)
2 2 3 2 4
B. 工业上制备HSO 的部分流程:FeS(s)――→SO(g)――→SO(g)
2 4 2 2 3
C. 用NaCO 溶液吸收SO 制备NaSO:
2 3 2 2 3
SO(g)――→NaHSO(aq)――→NaSO(aq)
2 3 2 3
D. 实验室探究浓硫酸的性质:HSO(浓)――→SO(g)――→HSO(aq)
2 4 2 2 4
8.化学离不开生活,下列有关物质的性质或用途正确的是
A.漂白粉和明矾都常用于自来水的处理,二者的作用原理相同
B.铁分别与氯气、碘反应生成的产物中,铁的化合价不同
C.将红热的木炭投入浓HNO 中,有红棕色气体产生,证明木炭有还原性
3
D.在火焰上灼烧搅拌过某无色溶液的玻璃棒,火焰出现黄色,溶液中含Na元素
9.工业上用 催化还原 可以消除氮氧化物的污染,反应原理为:
。不同的催化剂催化该反应的最佳
活性温度不同。下列说法正确的是
A.上述反应平衡常数
B.其他条件不变时,反应单位时间, 去除率随温度升高而增大的原因可能是平衡常数变大
C.其他条件不变,在低温下使用高效催化剂可提高 的平衡转化率
D.反应中若采用高分子分离膜及时分离出水蒸气,可以使反应的平衡常数增大
10.一种重要有机中间体的合成路线如下,下列说法中正确的是
A.物质丙的分子式为B.物质甲可以发生氧化、取代、水解和消去反应
C.图示反应类型为加成反应
D.物质乙中的原子不可能处于同一平面
11.下列实验方案能达到探究目的的是
选
探究目的 实验方案
项
CO还原Fe O 实验中,Fe O 向CO还原Fe O 所得到的产物中加入稀盐酸,再滴加KSCN溶液,
A 2 3 2 3 2 3
是否全部被还原 观察颜色变化
比较CHCOO-和ClO-结合 室温下,用pH计分别测定等物质的量浓度的CHCOONa溶液和
B 3 3
H+的能力大小 NaClO溶液的pH
比较Ksp(BaSO )和 将BaSO 粉末和NaCO 饱和溶液混合,充分振荡,静置,取少量上
C 4 4 2 3
Ksp(BaCO )的相对大小 层清液,滴加盐酸和BaCl 溶液,观察是否有沉淀产生
3 2
蔗糖水解产物是否具有还原 向蔗糖溶液中加入少量稀硫酸,加热煮沸,冷却后加入银氨溶液,
D
性 水浴加热,观察现象
12.室温下,用含少量 杂质的 溶液制备 的过程如下图所示。下列说法正确的
是
已知:
A.“除锌”后所得上层清液中, 一定小于
B. 溶液中存在:
C.氨水、 溶液中存在:
D.“沉锰”后的滤液中存在:
13.在某催化剂作用下CO 和H 合成甲酸仅涉及以下反应:
2 2I.CO(g)+H(g) HCOOH(g) △H<0
2 2 1
II.CO(g)+H(g) CO(g)+HO(g) △H
2 2 2 2
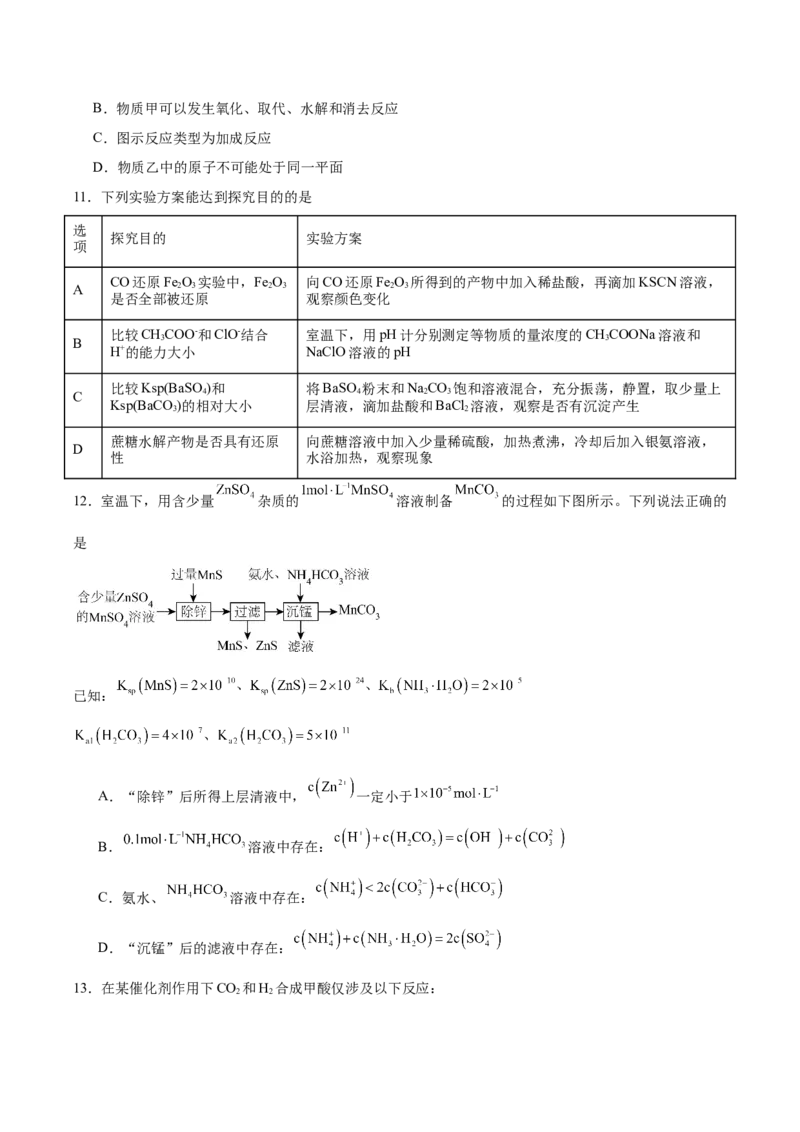
在2L刚性容器中,CO(g)和H(g)各投lmol发生反应,平衡时CO 的转化率及HCOOH和CO的选择性(产
2 2 2
物的选择性:生成的HCOOH或CO与转化的CO 的比值)随温度变化如图所示。下列说法正确的是
2
A. H<0
2
B.曲△线b表示平衡时HCOOH的选择性
C.240℃时,反应I的平衡常数K=
D.在200℃~360℃之间,温度对反应I的影响要小于反应II
二、非选择题:本题共4小题,共61分。
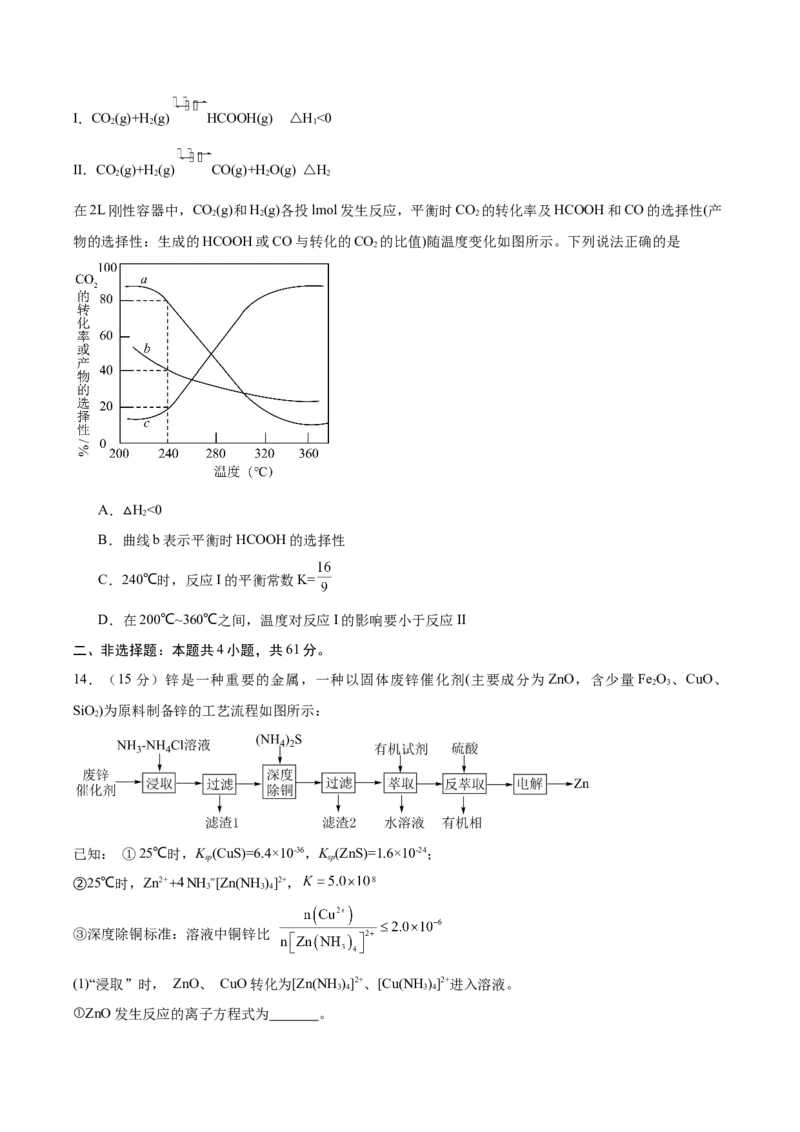
14.(15分)锌是一种重要的金属,一种以固体废锌催化剂(主要成分为ZnO,含少量Fe O 、CuO、
2 3
SiO)为原料制备锌的工艺流程如图所示:
2
已知: ①25℃时,K (CuS)=6.4×10-36,K (ZnS)=1.6×10-24;
sp sp
②25℃时,Zn2+ NH =[Zn(NH )]2+, 8
3 3 4
③深度除铜标准:溶液中铜锌比
(1)“浸取”时, ZnO、 CuO转化为[Zn(NH )]2+、[Cu(NH )]2+进入溶液。
3 4 3 4
①ZnO发生反应的离子方程式为 。②浸取温度应控制在 30℃左右, 其原因为 。
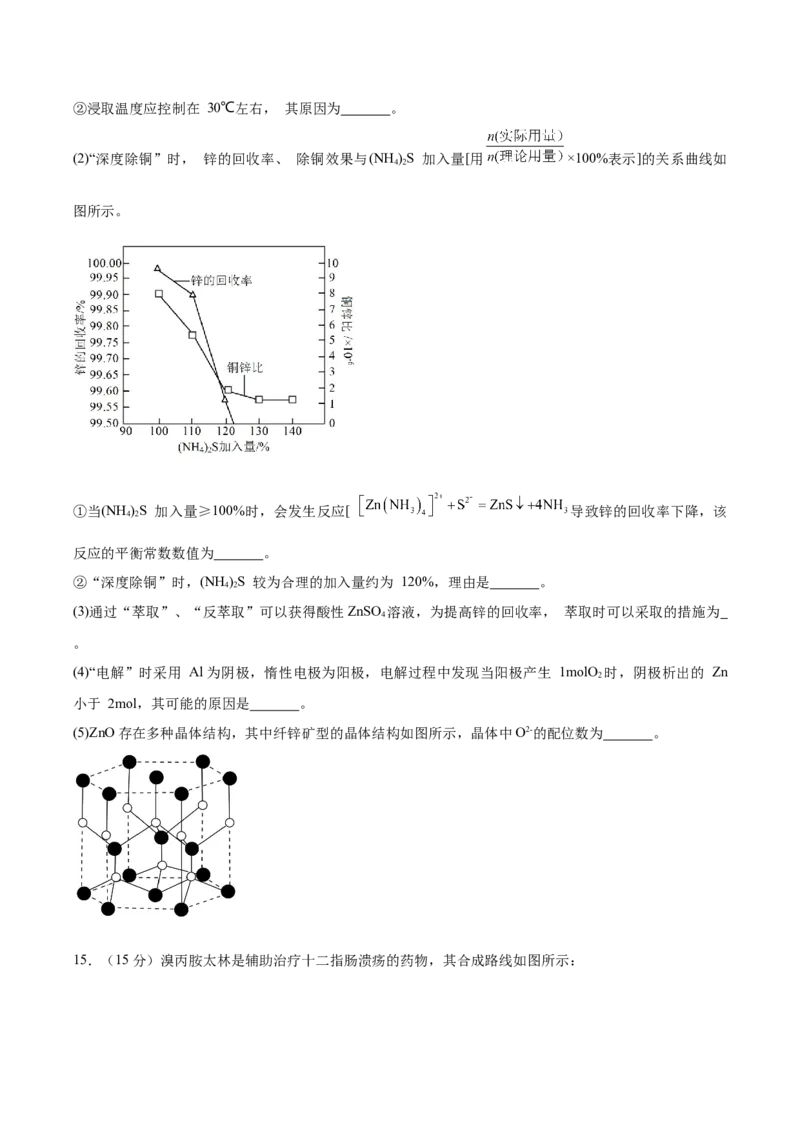
(2)“深度除铜”时, 锌的回收率、 除铜效果与(NH )S 加入量[用 ×100%表示]的关系曲线如
4 2
图所示。
①当(NH )S 加入量≥100%时,会发生反应[ 导致锌的回收率下降,该
4 2
反应的平衡常数数值为 。
②“深度除铜”时,(NH )S 较为合理的加入量约为 120%,理由是 。
4 2
(3)通过“萃取”、“反萃取”可以获得酸性ZnSO 溶液,为提高锌的回收率, 萃取时可以采取的措施为
4
。
(4)“电解”时采用 Al为阴极,惰性电极为阳极,电解过程中发现当阳极产生 1molO 时,阴极析出的 Zn
2
小于 2mol,其可能的原因是 。
(5)ZnO存在多种晶体结构,其中纤锌矿型的晶体结构如图所示,晶体中O2-的配位数为 。
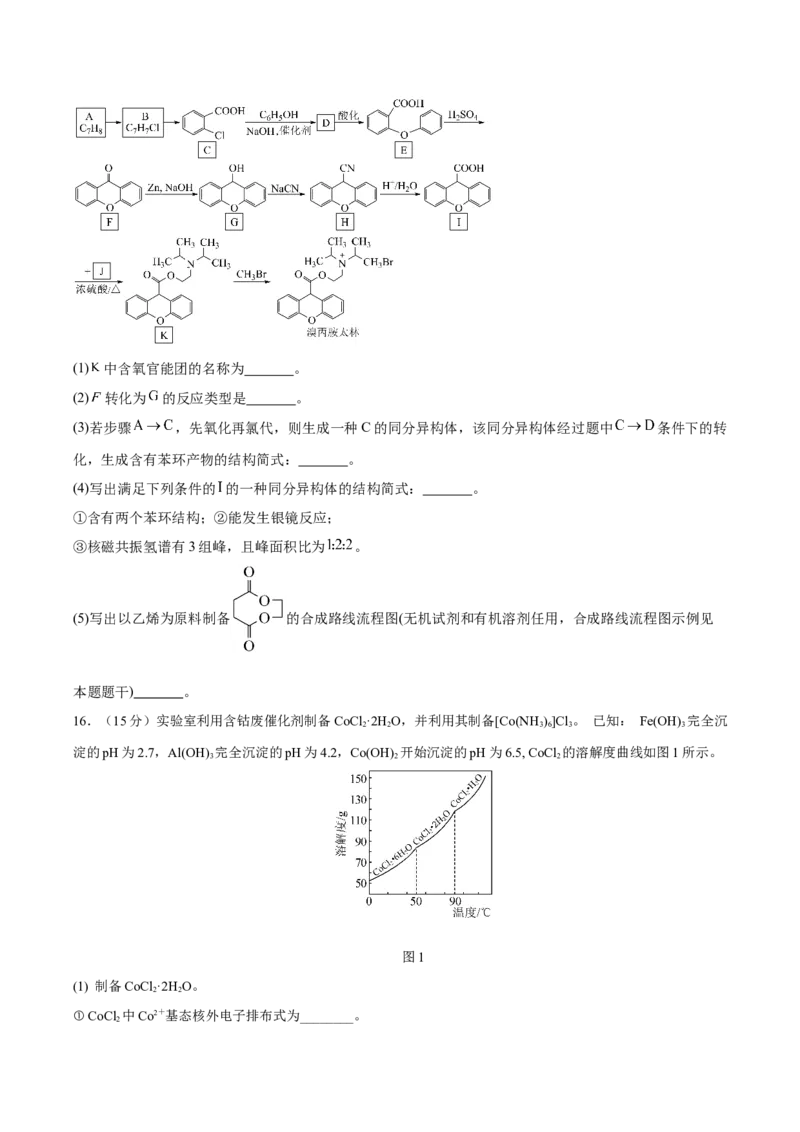
15.(15分)溴丙胺太林是辅助治疗十二指肠溃疡的药物,其合成路线如图所示:(1) 中含氧官能团的名称为 。
(2) 转化为 的反应类型是 。
(3)若步骤 ,先氧化再氯代,则生成一种C的同分异构体,该同分异构体经过题中 条件下的转
化,生成含有苯环产物的结构简式: 。
(4)写出满足下列条件的 的一种同分异构体的结构简式: 。
①含有两个苯环结构;②能发生银镜反应;
③核磁共振氢谱有3组峰,且峰面积比为 。
(5)写出以乙烯为原料制备 的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见
本题题干) 。
16.(15分)实验室利用含钴废催化剂制备CoCl·2HO,并利用其制备[Co(NH)]Cl。 已知: Fe(OH) 完全沉
2 2 3 6 3 3
淀的pH为2.7,Al(OH) 完全沉淀的pH为4.2,Co(OH) 开始沉淀的pH为6.5, CoCl 的溶解度曲线如图1所示。
3 2 2
图1
(1) 制备CoCl·2HO。
2 2
① CoCl 中Co2+基态核外电子排布式为________。
2② 补充完整以含钴废催化剂(主要成分为CoO,少量FeO 和AlO)为原料制备CoCl·2HO的实验方案:
2 3 2 3 2 2
_________________________________________________________________,洗涤 2~3次,低温干燥,得到产
品CoCl·2HO。(实验中须使用的仪器和试剂: pH计、1 mol·L-1 HCl溶液、CoCO 固体)
2 2 3
(2) 制备[Co(NH)]Cl 并测定Co含量。将CoCl·2HO和活性炭(催化剂)加入三颈瓶中(装置如图2),然后再依次
3 6 3 2 2
通过滴液漏斗缓慢滴加NHCl和浓氨水混合溶液、HO 溶液,控制温度不超过60 ℃充分反应,冷却后过滤。
4 2 2
图2
① 三颈瓶中制得[Co(NH)]3+的离子方程式为____________________________________。
3 6
② 加入NHCl的作用是________。
4
③ 在没有活性炭存在时,能得到一种化学式为Co(NH)Cl 的纯净物。测得1 mol Co(NH )Cl 与足量的硝酸银
3 5 3 3 5 3
溶液反应生成2 mol AgCl,该配合物内界的化学式为________。
④ 准确称取7.080 0 g样品于烧杯中,加入足量NaOH溶液充分反应,微沸加热至无NH 放出。冷却至室温后,
3
加入过量的KI固体和盐酸,充分摇荡。将所得溶液定容至250 mL,然后取出25.00 mL溶液放入锥形瓶中,滴
加少量淀粉溶液,用0.1 mol·L-1 NaSO 溶液滴定至终点,消耗NaSO 溶液的体积为24.00 mL。计算样品中钴
2 2 3 2 2 3
元素的质量分数(写出计算过程)。
已知:[Co(NH)]3++3OH-===Co(OH)↓+6NH↑;2Co(OH) +2I-+6H+===2Co2++I +6HO;I +2SO===2I-
3 6 3 3 3 2 2 2 2
+SO。
4
17.(16分)捕集并转化 可以有效实现碳达峰、碳中和。
Ⅰ.工业上利用两种温室气体 和 催化重整制取 和CO,主要反应为
反应①:
过程中还发生三个副反应:
反应②:反应③:
反应④:
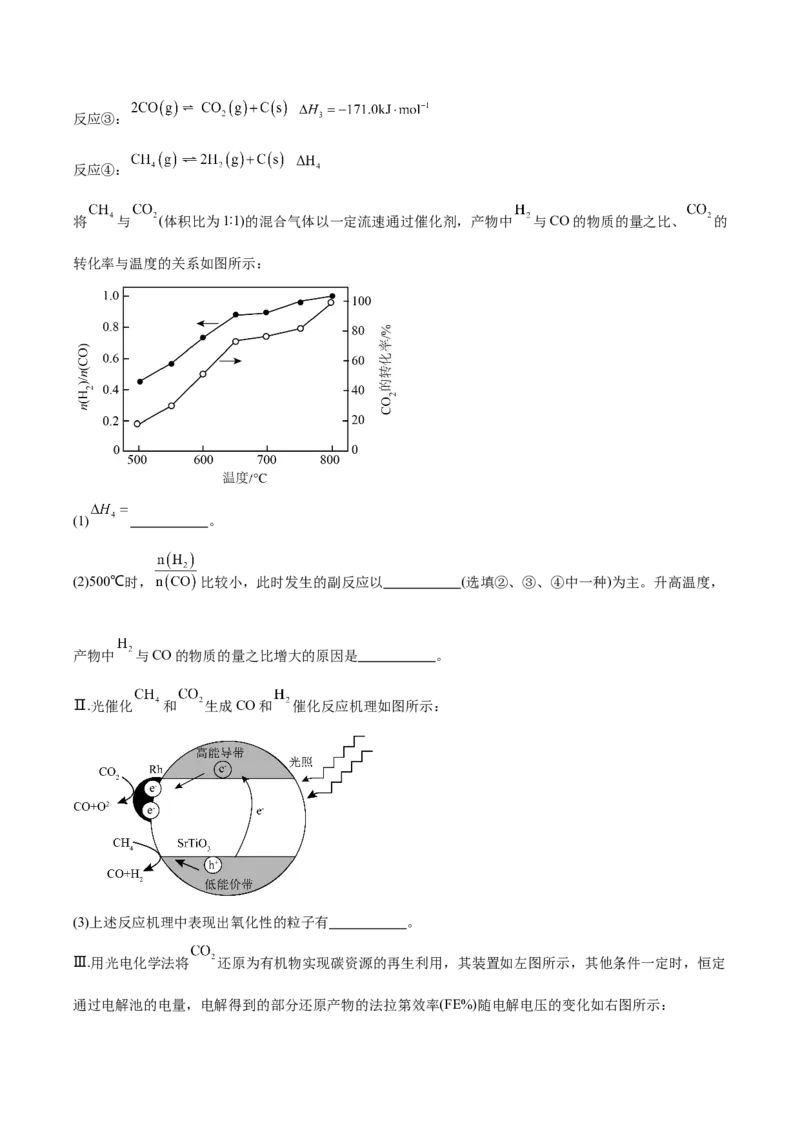
将 与 (体积比为1∶1)的混合气体以一定流速通过催化剂,产物中 与CO的物质的量之比、 的
转化率与温度的关系如图所示:
(1) 。
(2)500℃时, 比较小,此时发生的副反应以 (选填②、③、④中一种)为主。升高温度,
产物中 与CO的物质的量之比增大的原因是 。
Ⅱ.光催化 和 生成CO和 催化反应机理如图所示:
(3)上述反应机理中表现出氧化性的粒子有 。
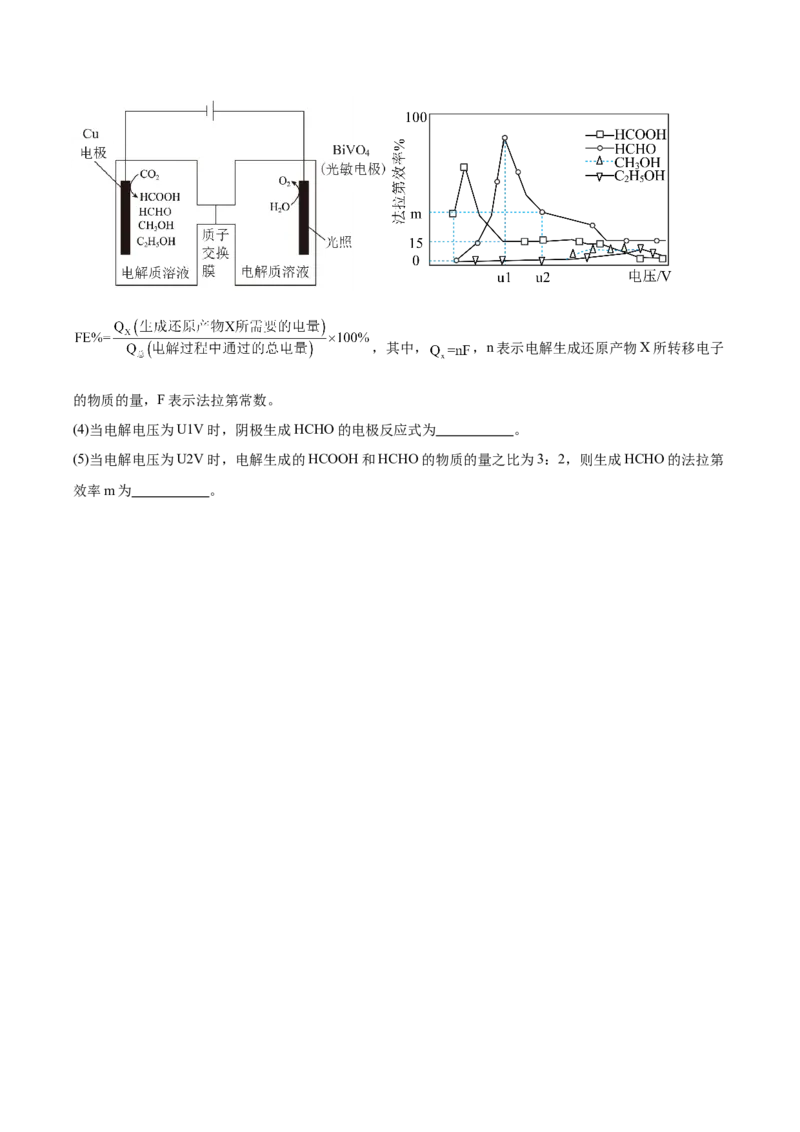
Ⅲ.用光电化学法将 还原为有机物实现碳资源的再生利用,其装置如左图所示,其他条件一定时,恒定
通过电解池的电量,电解得到的部分还原产物的法拉第效率(FE%)随电解电压的变化如右图所示:,其中, ,n表示电解生成还原产物X所转移电子
的物质的量,F表示法拉第常数。
(4)当电解电压为U1V时,阴极生成HCHO的电极反应式为 。
(5)当电解电压为U2V时,电解生成的HCOOH和HCHO的物质的量之比为3:2,则生成HCHO的法拉第
效率m为 。