文档内容
微专题23 金属与硝酸反应的规律与计算
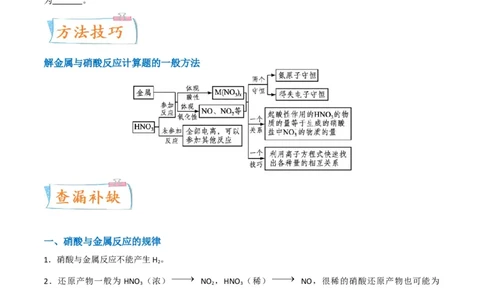
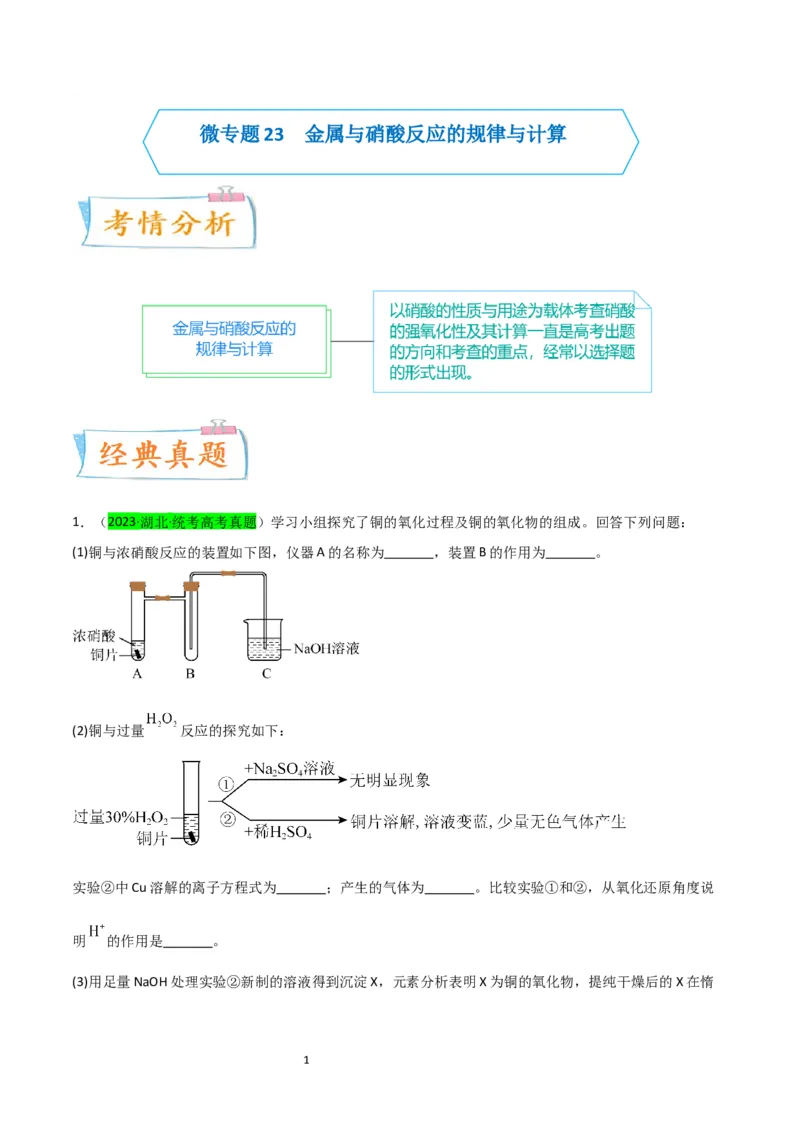
1.(2023·湖北·统考高考真题)学习小组探究了铜的氧化过程及铜的氧化物的组成。回答下列问题:
(1)铜与浓硝酸反应的装置如下图,仪器A的名称为 ,装置B的作用为 。
(2)铜与过量 反应的探究如下:
实验②中Cu溶解的离子方程式为 ;产生的气体为 。比较实验①和②,从氧化还原角度说
明 的作用是 。
(3)用足量NaOH处理实验②新制的溶液得到沉淀X,元素分析表明X为铜的氧化物,提纯干燥后的X在惰
1性氛围下加热,mgX完全分解为ng黑色氧化物Y, 。X的化学式为 。
(4)取含X粗品0.0500g(杂质不参加反应)与过量的酸性KI完全反应后,调节溶液至弱酸性。以淀粉为指示剂,
用 标准溶液滴定,滴定终点时消耗 标准溶液15.00mL。(已知:
, )标志滴定终点的现象是 ,粗品中X的相对含量
为 。
解金属与硝酸反应计算题的一般方法
一、硝酸与金属反应的规律
1.硝酸与金属反应不能产生H 。
2
2.还原产物一般为 HNO (浓) NO ,HNO (稀) NO,很稀的硝酸还原产物也可能为
3 2 3
N O,N ,或NH NO 。
2 2 4 3
3.硝酸与金属反应时既表现出氧化性,又表现出酸性。
4.硝酸与Cu反应:
(1)Cu与浓硝酸反应时,浓硝酸被还原为NO ,氮元素的化合价变化由+5 +4;
2
(2)Cu与稀硝酸反应时,稀硝酸被还原为NO,氮元素的化合价变化由+5 +2。
(3)一般情况下,硝酸的浓度越小,其还原产物的价态越低。
25.硝酸与Zn反应:
(1)锌与浓硝酸:Zn+4HNO₃=Zn(NO₃)₂+2NO₂↑+2H₂O
(2)锌与中等浓度的硝酸:3Zn+8HNO₃=3Zn(NO₃)₂+2NO↑+4H₂O
(3)与一般稀硝酸4Zn+10HNO₃=4Zn(NO₃)₂+N₂O↑+5H₂O
(4)与较稀硝酸反应:5Zn+12HNO₃=5Zn(NO₃)₂+N₂↑+6H₂O
(5)与极稀硝酸反应:4Zn+10HNO₃=4ZN(NO₃)₂+NH₄NO₃+3H₂O
二、硝酸与金属反应的计算方法
1.原子守恒法
HNO₃与金属反应时,一部分HNO₃起酸的作用,以NO 的形式存在于溶液中;一部分作为氧化剂,转化为
还原产物。这两部分中氮原子的总物质的量等于反应消耗的HNO₃中氮原子的物质的量。
2.得失电子法
HNO₃与金属的反应属于氧化还原反应,HNO₃中氮原子得电子的物质的量等于金属失电子的物质的量。
3.电荷守恒法
HNO₃过量时反应后溶液中(不考虑OH-)有:
( 代表金属离子)。
4.离子方程式计算法
金属与H SO ,HNO₃的混合酸反应时,由于硝酸盐中NO 在H SO 提供的H+的条件下能继续与金属反应,
2 4 2 4
因此此类题目应用离子方程式来计算,先作过量判断,然后根据完全反应的金属或H+或NO 进行相关计算,
且溶液中要符合电荷守恒。
1.(2022·北京·高考真题)下列方程式与所给事实不相符的是
A.加热 固体,产生无色气体:
B.过量铁粉与稀硝酸反应,产生无色气体:
3C.苯酚钠溶液中通入 ,出现白色浑浊:
D.乙醇、乙酸和浓硫酸混合加热,产生有香味的油状液体:
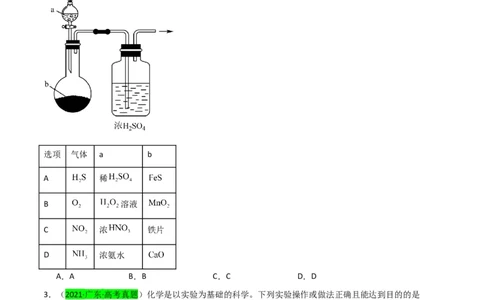
2.(2021·海南·统考高考真题)用如图装置制取干燥的气体(a、b表示加入的试剂),能实现的是
选项 气体 a b
A 稀
B 溶液
C 浓 铁片
D 浓氨水
A.A B.B C.C D.D
3.(2021·广东·高考真题)化学是以实验为基础的科学。下列实验操作或做法正确且能达到目的的是
选
操作或做法 目的
项
A 将铜丝插入浓硝酸中 制备
B 将密闭烧瓶中的 降温 探究温度对平衡移动的影响
C 将溴水滴入 溶液中,加入乙醇并振荡 萃取溶液中生成的碘
D 实验结束,将剩余 固体放回原试剂瓶 节约试剂
4A.A B.B C.C D.D
1.(2023春·福建福州·高一校联考期中)关于硝酸的说法正确的是
A.敞口放置的浓硝酸,浓度会变低是因为浓硝酸有吸水性
B.稀硝酸与Cu反应生成NO和硝酸铜时,硝酸既表现强氧化性又表现酸性
C.硝酸电离出的H+,能被Zn、Fe等金属还原成H
D.常温下,向浓硝酸中投入Fe片,不会产生大量₂的红棕色气体,没有反应发生
2.(2023春·江西宜春·高一上高中学校考期末)将7.6g铁、铜合金加入100mL某浓度的稀硝酸中,完全
反应后,溶液仍呈强酸性,且共收集到NO气体2.24L(标准状况下)。若反应前后溶液的体积变化忽略不计,
则下列说法不正确的是
A.上述反应中金属共失去电子0.3mol B.原硝酸的浓度:c(HNO )=3mol•L-1
3
C.合金中,铜的质量为4.8g D.反应后,铁的化合价为+3
3.(2023春·江苏常州·高一常州高级中学校考阶段练习)为了测定铁铜合金的组成,将7.6g铁、铜合金加
入100mL某浓度的稀硝酸中,将合金完全溶解后,共收集到NO气体2.24L(标准状况下),并测得溶液中
H+的浓度为0.5mol•L-1,若反应前后溶液的体积变化忽略不计,则下列判断不正确的是
A.上述反应中金属共失去电子0.3mol
B.合金中,铜的质量为4.8g
C.原硝酸的浓度:c(HNO )=3mol•L-1
3
D.要使溶液中的金属离子完全沉淀,需加5mol•L-1的NaOH溶液70mL
4.(2023春·四川成都·高一校考期中)我国清代《本草纲目拾遗》中记叙无机药物335种,其中“强水”
条目下写道:“性最烈,能蚀五金……其水甚强,五金八石皆能穿第,惟玻璃可盛。”这里的“强水”是
指硝酸,下列有关硝酸的相关描述中正确的是
A.王水指浓硝酸与浓盐酸按3:1的体积比混合所得的混合物
B.向装有Fe(NO ) 溶液的试管中加入稀硫酸,可在试管口观察到红棕色气体
3 2
C.常温下,浓硝酸可以用铝制容器储存,说明浓硝酸与铝不反应
D.稀HNO 与金属反应时,可被还原为更低价态,说明稀HNO 氧化性强于浓HNO
3 3 3
5.(2023春·黑龙江鹤岗·高一鹤岗一中校考期中)将铁粉和铜粉的均匀混合物平均分成四等份,分别加入
同浓度的稀硝酸,充分反应,在标准状况下生成 的体积和剩余金属的质量如下表(设硝酸的还原产物只
有 )。下列说法正确的是
5编号 ① ② ③ ④
硝酸体积/mL 100 200 300 400
剩余金属/g 18.6 9.6 0 0
NO体积/L 2.24 4.48 6.72 V
A.①中溶液存在 B.
C.硝酸的浓度为 D.④中
6.(2023春·福建福州·高一福建省福州第一中学校考期中)某金属单质跟一定浓度的硝酸反应,假定只产
生单一的还原产物。当参加反应的单质与被还原硝酸的物质的量之比为2:1时,还原产物是 ( )
A.NO B.NO C.N O D.N
2 2 2
7.(2022·山东德州·统考二模)下列有关计算正确的是
A.Na O 作供氧剂时,每生成5.6 L O (标况),转移电子数为0. 25N
2 2 2 A
B.1.92 g Cu与足量稀硝酸反应,被还原硝酸的物质的量为0.02 mol
C.利用铝热反应制备金属时,每得到1 mol Fe,一定消耗0.5 mol氧化剂
D.已知NH 的燃烧热为316.25 kJ/mol,则NH 燃烧的热化学方程式为:4NH (g)+5O (g)=4NO(g)
3 3 3 2
+6H O(g) H=-1265 kJ/mol
2
8.(2022秋·新△疆和田·高三统考期中)向mg由铁粉和铜粉组成的混合物中,加入某浓度的稀硝酸,充分
反应后测得生成NO的体积[V(NO)](已换算成标准状况下)、m(固体剩余质量)随加入的稀硝酸的体积的变化
如图所示(设硝酸的还原产物只有NO)。下列说法中正确的是
A.稀硝酸的浓度为0.4mol·L-1
B.a点时,100mL稀硝酸中溶解了Fe和Cu共8.4g
C.b点对应的溶液中可能含有的金属阳离子为Fe2+、Fe3+、Cu2+
6D.加入稀硝酸至400mL时,收集到的V(NO)约为6.91L
1.(2022秋·山东聊城·高三聊城二中校考期中)某兴趣小组探究金属与硝酸的还原产物,进行了下列三组
实验,下列说法正确的是
实验操作(室温)及实验现象
① 将足量的铜粉加入 中,溶液呈绿色,产生红棕色气体
② 将足量的铜粉加入 中,溶液呈蓝色,产生无色气体
③ 将足量的铁粉加入 中,溶液呈浅绿色,无气体生成
A.实验①②反应后溶液颜色不同,说明氧化产物不同
B.实验②中产生的气体不能和血红蛋白结合
C.实验③中铁发生了钝化
D.以上实验说明硝酸的还原产物与硝酸的浓度及金属的活泼性有关
2.(2022秋·山东青岛·高三统考期末)浓硝酸和稀硝酸均具有强氧化性,浓硝酸还原产物为NO ,稀硝酸
2
还原产物为NO。同温同压下,0.1mol金属单质M与足量浓硝酸反应,生成NO 体积为V ;0.1mol金属单
2 1
质N与足量稀硝酸反应,生成NO体积为V 。下列说法错误的是
2
A.M和N反应中,被还原硝酸的物质的量之比一定为
B.M和N反应中,消耗硝酸的物质的量之比一定为
C.产物中M和N化合价之比一定为
D.将生成的气体恰好溶于水生成硝酸,需要通入氧气的体积之比一定为
3.(2023·全国·高三专题练习)硝酸与金属反应后所得还原产物与硝酸的浓度和金属的活泼性有关。10
mL 0.5 mol·L-1HNO 与0.048 g Mg恰好完全反应。若氮元素只被还原到一种价态,下列说法不正确的是
3
7A.HNO 作还原剂
3
B.HNO 浓度越低,N元素还原价态越低
3
C.反应中转移电子数为0.004 mol
D.还原产物可能为NH NO
4 3
4.(2023·山东淄博·校联考二模)探究铜与硝酸反应的生成 时的硝酸浓度。如图所示,先通 一段时
间后关闭活塞K,将铜丝伸入溶液中,当A中气体变为无色时,上提铜丝,再将B中溶液稀释至 ,
取 ,用 的 溶液滴定至终点时消耗 (忽略硝酸的挥发、分解及溶液体积变
化)。下列说法正确的是
A.可用盛有 溶液的洗气瓶进行尾气吸收
B.铜与硝酸反应主要生成 时的硝酸浓度不大于
C.若不通 ,可能导致所得实验结果偏高
D.若通过直接滴定A中剩余酸的量(掩蔽掉 的干扰)进行求算,所得实验结果偏低
5.(2023·全国·高三专题练习)将1.92g铜粉与一定量的浓硝酸反应,硝酸的还原产物为NO和NO ,当铜
2
粉完全反应时收集到混合气体1.12L(气体体积折算为标准状况)。则所消耗硝酸的物质的量是
A.0.08mol B.0.09mol C.0.11mol D.0.12mol
6.(2023·全国·高三专题练习)用图所示装置进行实验,探究硝酸与铁反应的产物。
8主要实验操作 实验现象
①A 中有红棕色气体产生,一段时间后,气体颜
打开弹簧夹,通入一段时间CO 2 后,滴入浓硝酸后无 色逐渐变浅;反应停止后,A 中无固体剩余。
明显现象,加热烧瓶,反应开始后停止加热。
②B 中溶液变棕色。
取少量A 中溶液,加几滴氯水,再滴入硫氰化钾溶
③溶液变为红色
液
④B中棕色溶液变浅,有无色气体逸出,且在空气
取少量 B 中溶液,加热
中变为红棕色
已知:FeSO +NO=Fe(NO)SO (棕色) ∆H<0 。
4 4
下列说法正确的是
A.滴入浓硝酸加热前没有明显现象的原因是:温度低,反应速率太慢
B.实验现象③说明反应后A 中溶液含有 Fe2+
C.实验现象④说明 A 中有 NO 生成
D.可用浓 NaOH 溶液和湿润的红色石蕊试纸检验硝酸的还原产物中是否有 NH
7.(2023·全国·高三专题练习)将质量为32g的铜与150mL的一定浓度的硝酸反应,铜完全溶解,产生标
准状况下11.2L的NO和NO 的混合气体,将生成的混合气体与一定体积的氧气一起通入足量NaOH溶液中,
2
气体恰好被吸收生成NaNO 。下列说法不正确的是
3
A.标准状况下,通入的O 体积为5.6L
2
B.向反应后的溶液加NaOH,使铜沉淀完全,需要NaOH的物质的量至少为1.0mol
C.标准状况下,混合气体构成是5.6L的NO和5.6L的NO
2
D.硝酸的物质的量浓度为10.0mol·L−1
8.(2023春·重庆万州·高三重庆市万州第二高级中学校考阶段练习)将一定质量的镁铜合金加入到稀硝酸
中,两者恰好完全反应,假设反应过程中还原产物全是NO,向所得溶液中加入物质的量浓度为3 mol·L-1
NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1 g,则下列有关叙述中正确的是
9( )
A.加入合金的质量不可能为6.4 g
B.参加反应的硝酸的物质的量为0.1 mol
C.沉淀完全时消耗NaOH溶液的体积为150 mL
D.溶解合金时收集到NO气体的体积在标准状况下为2.24 L
9.(2023·高一课时练习)关于硝酸的说法正确的是
A.硝酸电离出的H+离子,能被Zn、Fe等金属还原成H
2
B.浓HNO 与浓HCl按3∶1的体积比所得的混合物叫王水
3
C.硝酸与金属反应时,主要是+5价的氮元素得电子
D.常温下,向浓HNO 中投入Fe片,会产生大量的红棕色气体
3
10.(2023春·甘肃张掖·高一高台县第一中学校考阶段练习)在某100mL混酸中,硝酸的物质的量浓度为
0.4mol/L,硫酸的物质的量浓度为0.2mol/L,加入2.56g铜粉,微热,待充分反应后,溶液中Cu2+的物质的
量浓度为
A.0.15mol/L B.0.3mol/L C.0.225mol/L D.无法计算
11.(2022秋·湖南岳阳·高三校考阶段练习)实验研究发现,金属与硝酸发生氧化还原反应时,硝酸的浓
度越稀,对应还原产物中氮元素的化合价越低。现有一定量的铝粉和铁粉的混合物与足量很稀的硝酸充分
反应,反应过程中无气体放出,在反应结束后的溶液中逐滴加入5mol/LNaOH溶液,所加NaOH溶液的体
积 与产生沉淀的物质的量 关系如图所示,下列说法正确的是
A. 点到 点的反应为:
B.样品中铝粉和铁粉的质量之比为 :
C. 点对应 溶液的体积为
D.原硝酸溶液中硝酸的物质的量为
12.(2023·全国·高三专题练习)铁粉与硝酸反应可制备硝酸铁,硝酸铁溶液可用于刻蚀银器。铁粉用量
和硝酸浓度都会影响反应产物。
10I.常温下过量铁粉与不同浓度硝酸反应的还原产物的探究。利用如图装置进行实验,其中装置A为氮气氛
围。
(1)实验一:硝酸初始浓度为12.0mol•L-1时,硝酸的还原产物主要是NO 。装置B中NO 发生反应的化学方
2 2
程式为 。
(2)实验二:硝酸浓度为6.0mol•L-1时,硝酸的还原产物主要是NO。利用上述装置进行实验时,证明还原产
物主要是NO的现象是 。
(3)实验三:硝酸浓度为0.5mol•L-1时,过量铁粉与硝酸反应产生H ,充分反应后所得溶液几乎无色。取装
2
置A中上层清液,加入过量NaOH溶液并煮沸,产生的气体能使湿润的红色石蕊试纸变蓝。过量铁粉与
0.5mol•L-1硝酸混合发生反应的离子方程式有:①Fe+2H+=Fe2++H ↑;② 。
2
II.硝酸铁溶液刻蚀银器的原理探究。
(4)已知:①0.1mol•L-1硝酸铁溶液pH的为1.6。
②将5mL0.1mol•L-1硝酸铁溶液滴加到有银镜的试管中,1min银镜完全溶解。
提出猜想猜想a:Fe3+具有氧化性,能氧化Ag。
猜想b:酸性条件下NO ,能氧化Ag。
设计实验,验证猜想
序号 实验方案 实验现象 结论
①将5mLpH约为1.6的0.05mol•L-1 溶液滴加到有银镜
猜想
的试管甲中
猜想a成
a 立
②将5mLpH约为1.6的硫酸溶液滴加到有银镜的试管乙中
猜想 1.2min试管丙中银镜完全 猜想b成
将5mL 溶液滴加到有银镜的试管丙中
b 溶解 立
实验结论:硝酸铁溶液刻蚀银器原理是0.1mol•L-1硝酸铁溶液中的Fe3+和NO 均能氧化Ag。
11