文档内容
微专题26 化学工艺流程题-----核心反应与条件控制
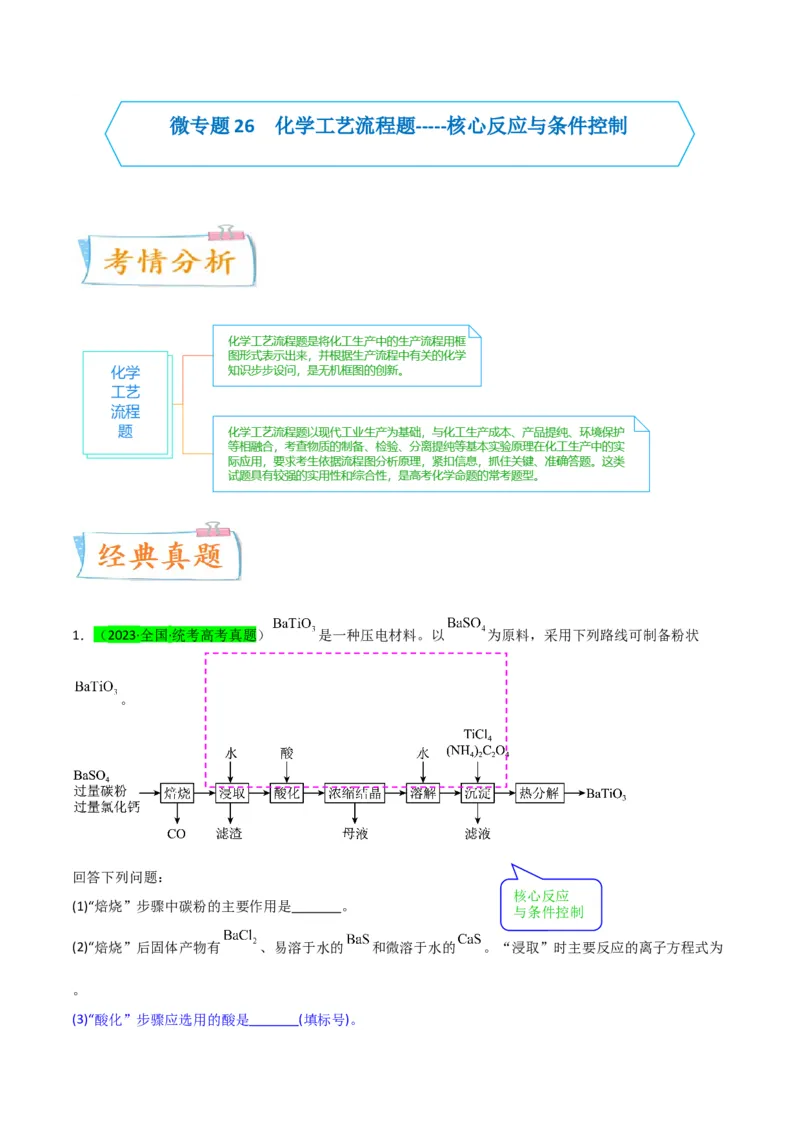
1.(2023·全国·统考高考真题) 是一种压电材料。以 为原料,采用下列路线可制备粉状
。
回答下列问题:
核心反应
(1)“焙烧”步骤中碳粉的主要作用是 。
与条件控制
(2)“焙烧”后固体产物有 、易溶于水的 和微溶于水的 。“浸取”时主要反应的离子方程式为
。
(3)“酸化”步骤应选用的酸是 (填标号)。a.稀硫酸 b.浓硫酸 c.盐酸 d.磷酸
(4)如果焙烧后的产物直接用酸浸取,是否可行? ,其原因是 。
(5)“沉淀”步骤中生成 的化学方程式为 。
(6)“热分解”生成粉状钛酸钡,产生的 。
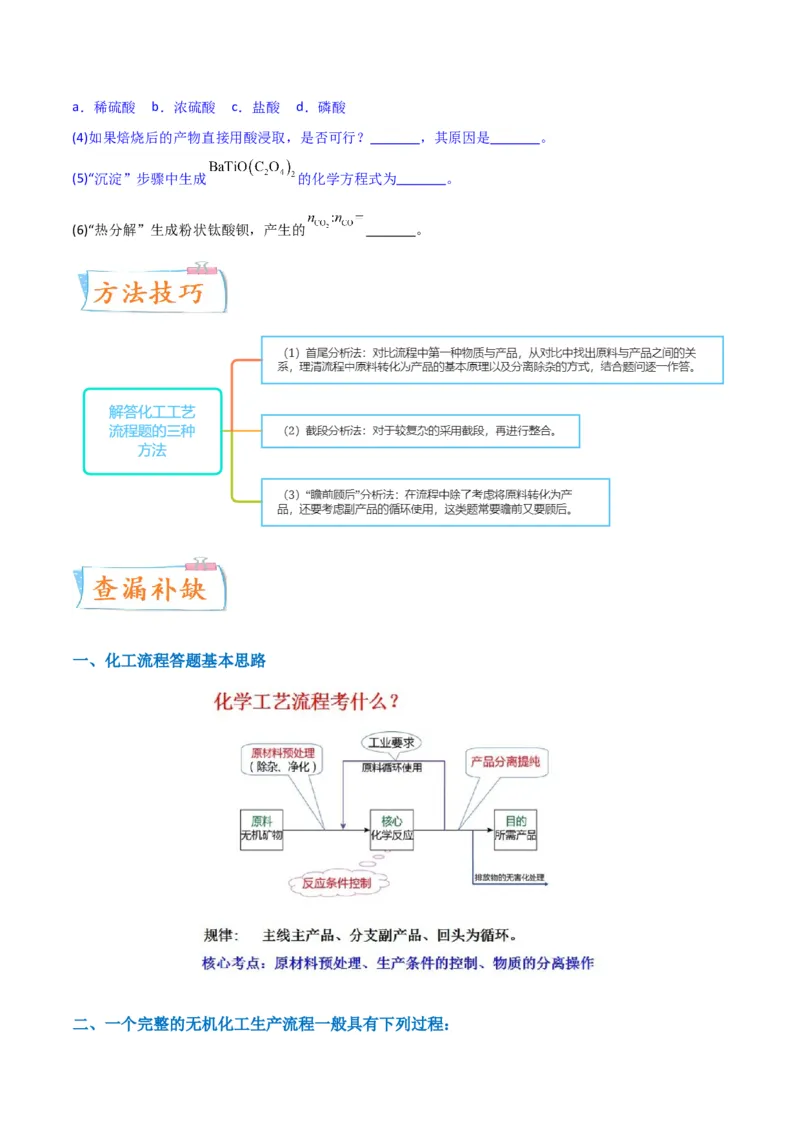
一、化工流程答题基本思路
二、一个完整的无机化工生产流程一般具有下列过程:原料 对原料的预处理 核心化学反应 产品的提纯和分离 目标产物
三、核心反应与条件控制:
1.溶液的PH:
提供酸碱性环境反应、抑制或促进离子水解等产生沉淀便于分离等。调节PH的方法:调节pH所需的物质
一般应满足两点:一是能与H+反应,使溶液pH增大;二是不引入新杂质。(一般酸、碱、氧化物、水解
的盐等)如:要除去Cu2+中混有的Fe3+,可加入CuO、Cu(OH)、Cu(OH)CO 等物质来调节溶液的pH,
2 2 2 3
不可加入NaOH溶液、氨水等。
①调节溶液的酸碱性,使某些金属离子形成氢氧化物沉淀析出(或抑制水解)。
②加入酸或调节溶液至酸性还可除去氧化物(膜)。
③加入碱或调节溶液至碱性还可除去油污,除去铝片氧化膜,溶解铝、二氧化硅等。
④特定的氧化还原反应需要的酸性条件(或碱性条件)。
2.温度:
(1)升温----加快反应(溶解)速率;促进平衡向吸热方向移动;去除热稳定性差的物质或易升华的物质。
(2)降温----防止物质分解,挥发;使平衡向放热方向移动;使高沸点的物质液化,使其与其他物质分离;
降低溶解度,减少损失。
(3)控温-----水浴、沙浴、油浴-----受热均匀,便于控制温度。温度太高---速率太快;物质可能分解、
挥发、水解;催化剂可能中毒;发生副反应等。温度太低----速率可能太慢;催化剂活性不高;物质转化率、
产率不高等。
主要从物质性质(热稳定性、水解、氧化性或还原性、溶解度、熔沸点、挥发性、胶体聚沉等)和反应原理
(反应速率、平衡移动、催化剂活性、副反应)两个角度思考。
3.控制压强:改变速率,影响平衡。
4.使用合适的催化剂:加快反应速率,缩短达到平衡所需要的时间。
5.趁热过滤:防止某物质降温时析出。
6.洗涤:常见的洗涤方式有“水洗”和“乙醇洗”。“水洗”的目的是除去沉淀或晶体表面残留的杂质,
当沉淀物的溶解度随温度升高而增大时一般可用冰水洗;“乙醇洗”既可以除去沉淀或晶体表面残留的杂
质,又可以降低晶体的溶解度,减少损失,还可以利用乙醇易挥发的性质,加快除去沉淀或晶体表面的水
分。
7.氧化:氧化剂的选择要依据试题设置的情境,常见的氧化剂有氯气、过氧化氢、氧气和次氯酸钠等,
为了避免引入新的杂质,通常选择的氧化剂有过氧化氢和氧气。
1.(2023·全国·统考高考真题)铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、铝、硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如下图所示:
核心反应
与条件控制
已知:最高价铬酸根在酸性介质中以Cr O 存在,在碱性介质中以CrO 存在。
2
回答下列问题:
(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为 (填化学式)。
(2)水浸渣中主要有SiO 和 。
2
(3)“沉淀”步骤调pH到弱碱性,主要除去的杂质是 。
(4)“除硅磷”步骤中,使硅、磷分别以MgSiO 和MgNH PO 的形式沉淀,该步需要控制溶液的pH≈9以达到
3 4 4
最好的除杂效果,若pH<9时,会导致 ;pH>9时,会导致 。
(5)“分离钒”步骤中,将溶液pH调到1.8左右得到V O 沉淀,V O 在pH<1时,溶解为VO 或VO3+在碱性条
2 5 2 5
件下,溶解为VO 或VO ,上述性质说明V O 具有 (填标号)。
2 5
A.酸性 B.碱性 C.两性
(6)“还原”步骤中加入焦亚硫酸钠(Na S O )溶液,反应的离子方程式为 。
2 2 5
2.(2023·辽宁·统考高考真题)某工厂采用如下工艺处理镍钴矿硫酸浸取液含(
和 )。实现镍、钴、镁元素的回收。
已知:
核心反应
与条件控制
物质回答下列问题:
(1)用硫酸浸取镍钴矿时,提高浸取速率的方法为 (答出一条即可)。
(2)“氧化”中,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸 , 中过氧
键的数目为 。
(3)“氧化”中,用石灰乳调节 , 被 氧化为 ,该反应的离子方程式为 (
的电离第一步完全,第二步微弱);滤渣的成分为 、 (填化学式)。
(4)“氧化”中保持空气通入速率不变, (Ⅱ)氧化率与时间的关系如下。 体积分数为 时,
(Ⅱ)氧化速率最大;继续增大 体积分数时, (Ⅱ)氧化速率减小的原因是 。
(5)“沉钴镍”中得到的 (Ⅱ)在空气中可被氧化成 ,该反应的化学方程式为 。
(6)“沉镁”中为使 沉淀完全 ,需控制 不低于 (精确至0.1)。
3.(2021·福建·高考真题)四钼酸铵是钼深加工的重要中间产品具有广泛的用途。一种以钼精矿(主要含
,还有 、 的化合物及 等)为原料制备四钼酸铵的工艺流程如下图所示。核心反应
回答下列问题: 与条件控制
(1)“焙烧”产生的气体用_______吸收后可制取氮肥。
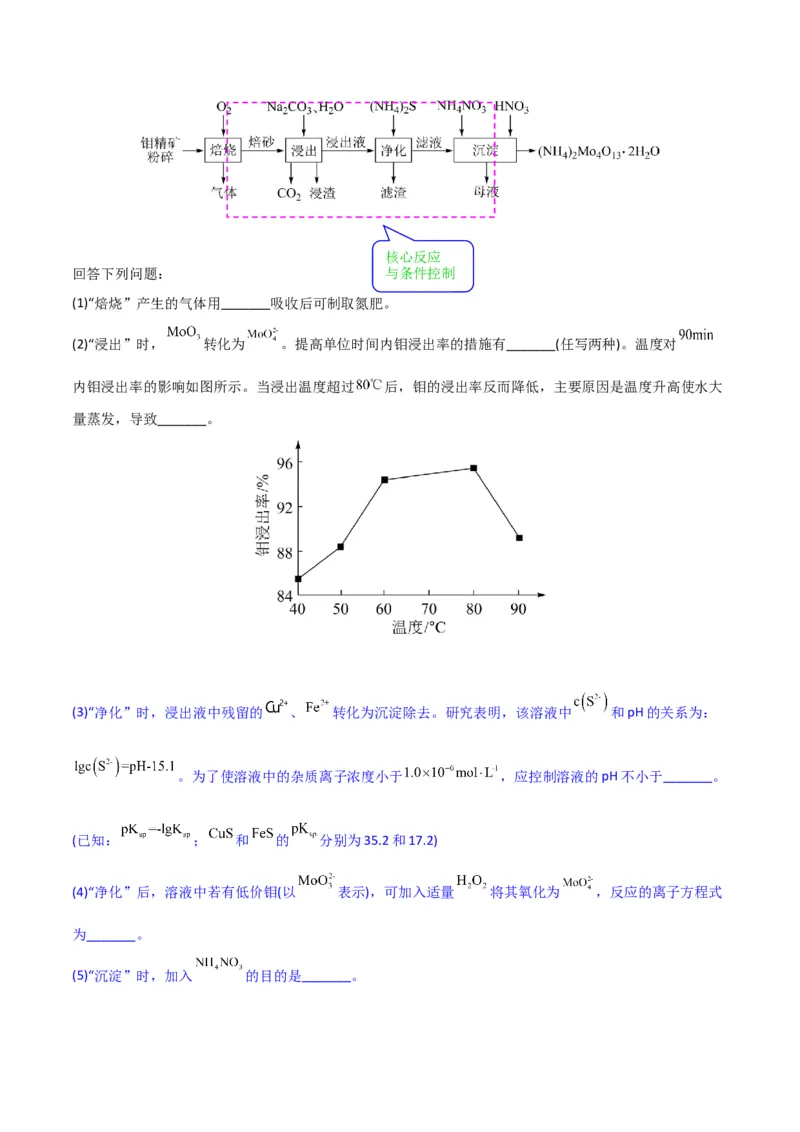
(2)“浸出”时, 转化为 。提高单位时间内钼浸出率的措施有_______(任写两种)。温度对
内钼浸出率的影响如图所示。当浸出温度超过 后,钼的浸出率反而降低,主要原因是温度升高使水大
量蒸发,导致_______。
(3)“净化”时,浸出液中残留的 、 转化为沉淀除去。研究表明,该溶液中 和pH的关系为:
。为了使溶液中的杂质离子浓度小于 ,应控制溶液的pH不小于_______。
(已知: ; 和 的 分别为35.2和17.2)
(4)“净化”后,溶液中若有低价钼(以 表示),可加入适量 将其氧化为 ,反应的离子方程式
为_______。
(5)“沉淀”时,加入 的目的是_______。(6)高温下用 还原(NH ) Mo O 可制得金属钼,反应的化学方程式为_______。【已知:(NH ) Mo O 受热
4 2 4 13 4 2 4 13
分解生成 】
1.(2023·山东·统考高考真题)盐湖卤水(主要含 、 和硼酸根等)是锂盐的重要来
核心反应
与条件控制
源。一种以高镁卤水为原料经两段除镁制备 的工艺流程如下:
已知:常温下, 。相关化合物的溶解度与温度的关系如图所示。
回答下列问题:
(1)含硼固体中的 在水中存在平衡: (常温下, );
与 溶液反应可制备硼砂 。常温下,在 硼砂溶液中,
水解生成等物质的量浓度的 和 ,该水解反应的离子方程式为 ,该溶
液 。(2)滤渣Ⅰ的主要成分是 (填化学式);精制Ⅰ后溶液中 的浓度为 ,则常温下精制Ⅱ过程中
浓度应控制在 以下。若脱硼后直接进行精制Ⅰ,除无法回收 外,还将增加 的
用量(填化学式)。
(3)精制Ⅱ的目的是 ;进行操作 时应选择的试剂是 ,若不进行该操作而直接浓缩,将导致
。
2.(2023·海南海口·海南华侨中学校考二模)穿甲弹的弹芯用钨合金制造。工业上以黑钨矿(主要成分是
FeWO 、MnWO ,含少量的Fe O 、SiO )为原料冶炼钨的流程如图所示。
4 4 2 3 2
已知:钨酸H WO 难溶于水。
2 4
核心反应
回答下列问题: 与条件控制
(1)浸取在加热、通空气条件下进行,FeWO 转化为Na WO 的化学方程式为 。
4 2 4
(2)“滤渣1”的成分为 。除硅时,加入稀盐酸调节pH时,如果pH太低,钨的产率会降低,其原因
是 。
(3)“系列操作X”的目的是去除部分氨,使(NH ) WO 转化为仲钨酸铵 析出并分离,则该系
4 2 4
列操作是 。
(4)已知:含大量钨酸钙固体的溶液中存在 。 时,
,当温度升高至 时, ,则 (填“ ”“ ”或“ ”)0。
3.(2023·陕西商洛·统考三模)固体电解质LATP的化学式为Li Al Ti (PO ) ,某研究人员以钛铁矿精粉
1.4 0.4 1.6 4 3
(主要成分为FeTiO ,含少量Al O ,SiO )为原料合成LATP的工艺流程如图所示。
3 2 3 2核心反应
与条件控制
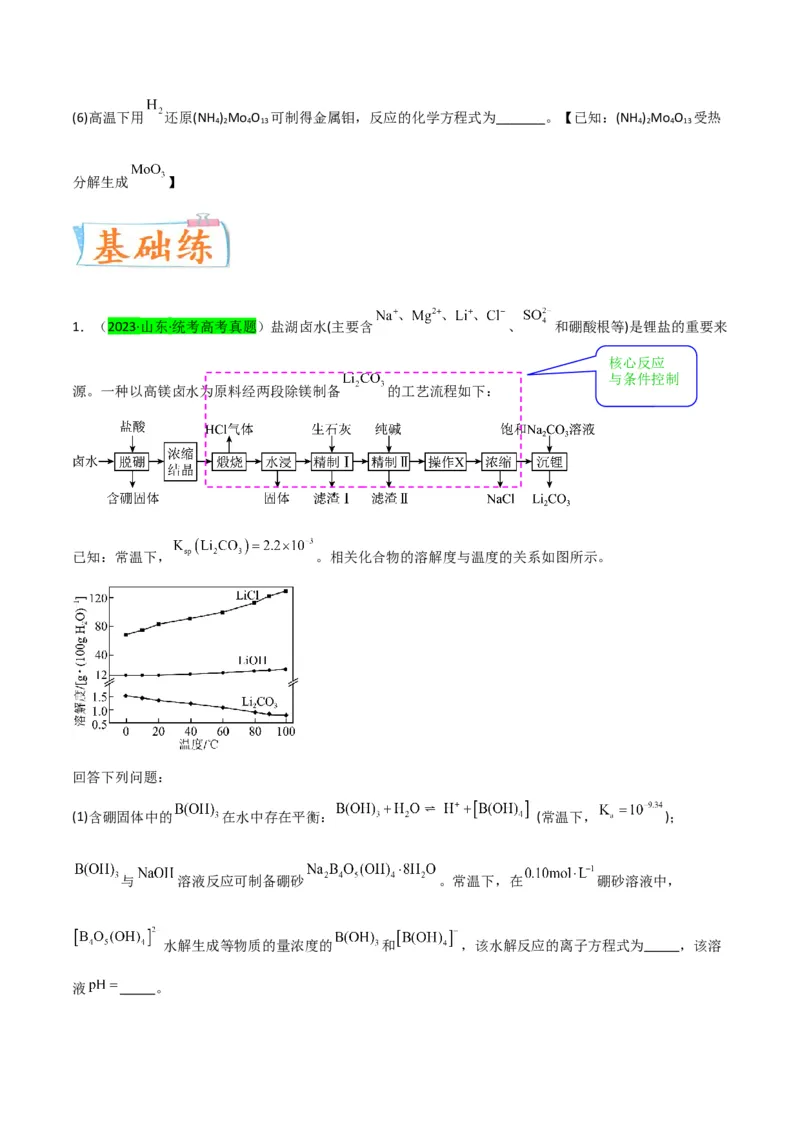
请回答下列问题:
(1)LATP中钛的化合价为 价。
(2)“粉碎”的目的是 ,为了达到这一目的,还可以采用的措施有 (答一条即可)。
(3)“碱浸”的目的是除去 (填化学式)。
(4)“碱浸”时加入适当过量的NaOH溶液,“酸浸”时加入适当过量的稀硫酸,且NaOH溶液和稀硫酸均不
宜过量太多,其主要原因是 。
(5)“沉钛”时生成Ti (PO ) 的化学方程式为 。
3 4 4
(6)本实验洗涤Ti (PO ) 时采用如图所示装置,该装置为抽滤装置,其原理是用抽气泵使吸滤瓶中的压强降
3 4 4
低,达到快速固液分离的目的。其中“安全瓶”的作用是 。
(7)常温下,Ti (PO ) 的K =a,当溶液中c(Ti4+)≤1.0×10-5mol·L-1时可认为Ti4+沉淀完全,则“沉钛”时,溶液
3 4 4 sp
中c( )最低为 mol·L-1。
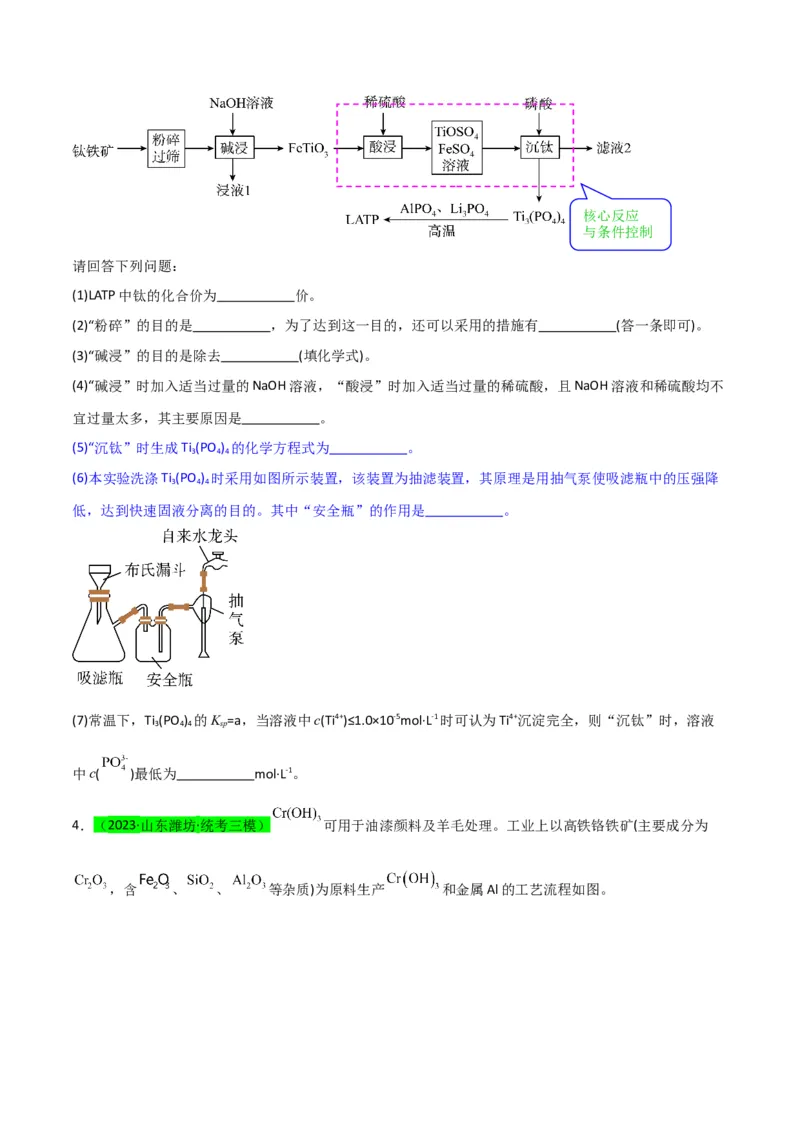
4.(2023·山东潍坊·统考三模) 可用于油漆颜料及羊毛处理。工业上以高铁铬铁矿(主要成分为
,含 、 、 等杂质)为原料生产 和金属Al的工艺流程如图。核心反应
与条件控制
已知:
I.“焙烧”过程中, 反应转化为
Ⅱ.若溶液中相关离子的物质的量浓度为c,则常温时,lgc与溶液pH的关系如图所示。
Ⅲ. (黄色) (橙色) 。
回答下列问题:
(1)“焙烧”时, 发生反应的化学方程式为 。
(2)“水浸”后滤渣主要成分为 (填化学式);“调pH”时通入的“气体X”是 。
(3)常温下,图像上M点对应的溶液 。
(4)用稀硫酸进行“酸浸”,调节溶液pH的最大值为 。“沉铝”后
的母液Ⅱ的主要成分为 。
(5)加入 “析铬”时, 被还原的离子方程式为 。
5.(2023·湖南邵阳·统考三模)金属钒主要用于冶炼特种钢,被誉为“合金的维生素”。人们在化工实践
中,以富钒炉渣(其中的钒以FeO•V O 、V O 等形式存在,还有少量的SiO 、Al O 等)为原料提取金属钒的
2 3 2 5 2 2 3
工艺流程如图所示:核心反应
提示:①钒有多种价态,其中+5价最稳定; 与条件控制
②V O 在碱性条件下可转化为VO 。
2 5
(1)可加快“高温氧化”速率的措施有 (填一条)。
(2)“气体X”和“气体Y”的化学式分别为 、 。
(3)“沉硅、沉铝”中得到含铝沉淀的离子方程式为 。
(4)写出“高温氧化”过程中发生反应的化学方程式 。
(5)写出“热解”时的化学方程式 。
(6)在“高温还原”反应中,氧化钙最终转化为 (写化学式)。
(7)已知:25℃时,NH •H O的电离平衡常数K =1.8×10-5,H CO 的电离平衡常数K =4.3×10-7,K =5.6×10-11,
3 2 b 2 3 a1 a2
判断NH HCO 溶液呈 (填“酸性”“碱性”或“中性”)。
4 3
1.(2023·浙江·统考高考真题)某研究小组用铝土矿为原料制备絮凝剂聚合氯化铝( )
按如下流程开展实验。
核心反应
与条件控制
已知:①铝土矿主要成分为 ,含少量 和 。用 溶液溶解铝土矿过程中 转变为难
溶性的铝硅酸盐。
② 的絮凝效果可用盐基度衡量,盐基度
当盐基度为0.60~0.85时,絮凝效果较好。
请回答:
(1)步骤Ⅰ所得滤液中主要溶质的化学式是 。(2)下列说法不正确的是___________。
A.步骤I,反应须在密闭耐高压容器中进行,以实现所需反应温度
B.步骤Ⅱ,滤液浓度较大时通入过量 有利于减少 沉淀中的杂质
C.步骤Ⅲ,为减少 吸附的杂质,洗涤时需对漏斗中的沉淀充分搅拌
D.步骤Ⅳ中控制 和 的投料比可控制产品盐基度
(3)步骤V采用如图所示的蒸汽浴加热,仪器A的名称是 ;步骤V不宜用酒精灯直接加热的原
因是 。
(4)测定产品的盐基度。
的定量测定:称取一定量样品,配成溶液,移取 溶液于锥形瓶中,调 ,滴加指示
剂 溶液。在不断摇动下,用 标准溶液滴定至浅红色(有 沉淀),30秒
内不褪色。平行测试3次,平均消耗 标准溶液 。另测得上述样品溶液中
。
①产品的盐基度为 。
②测定 过程中溶液 过低或过高均会影响测定结果,原因是 。
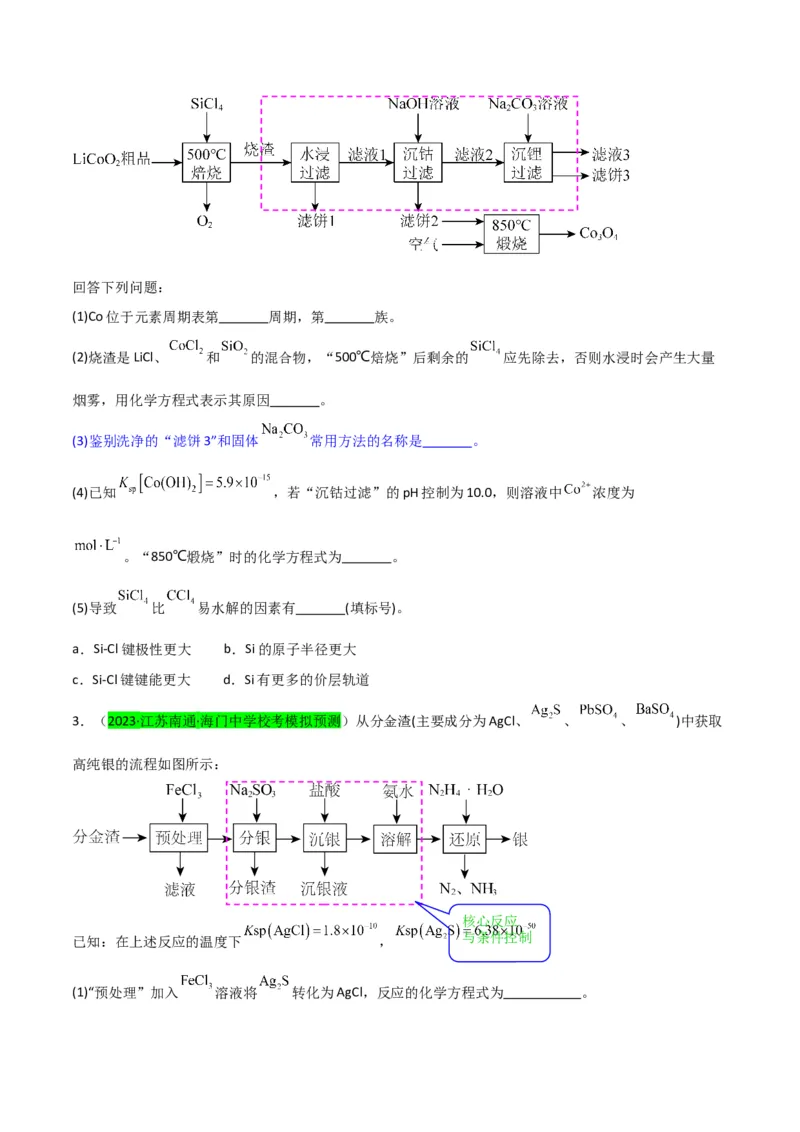
2.(2023·湖北·统考高考真题) 是生产多晶硅的副产物。利用 对废弃的锂电池正极材料
核心反应
进行氯化处理以回收Li、Co等金属,工艺路线如下:
与条件控制回答下列问题:
(1)Co位于元素周期表第 周期,第 族。
(2)烧渣是LiCl、 和 的混合物,“500℃焙烧”后剩余的 应先除去,否则水浸时会产生大量
烟雾,用化学方程式表示其原因 。
(3)鉴别洗净的“滤饼3”和固体 常用方法的名称是 。
(4)已知 ,若“沉钴过滤”的pH控制为10.0,则溶液中 浓度为
。“850℃煅烧”时的化学方程式为 。
(5)导致 比 易水解的因素有 (填标号)。
a.Si-Cl键极性更大 b.Si的原子半径更大
c.Si-Cl键键能更大 d.Si有更多的价层轨道
3.(2023·江苏南通·海门中学校考模拟预测)从分金渣(主要成分为AgCl、 、 、 )中获取
高纯银的流程如图所示:
核心反应
与条件控制
已知:在上述反应的温度下 ,
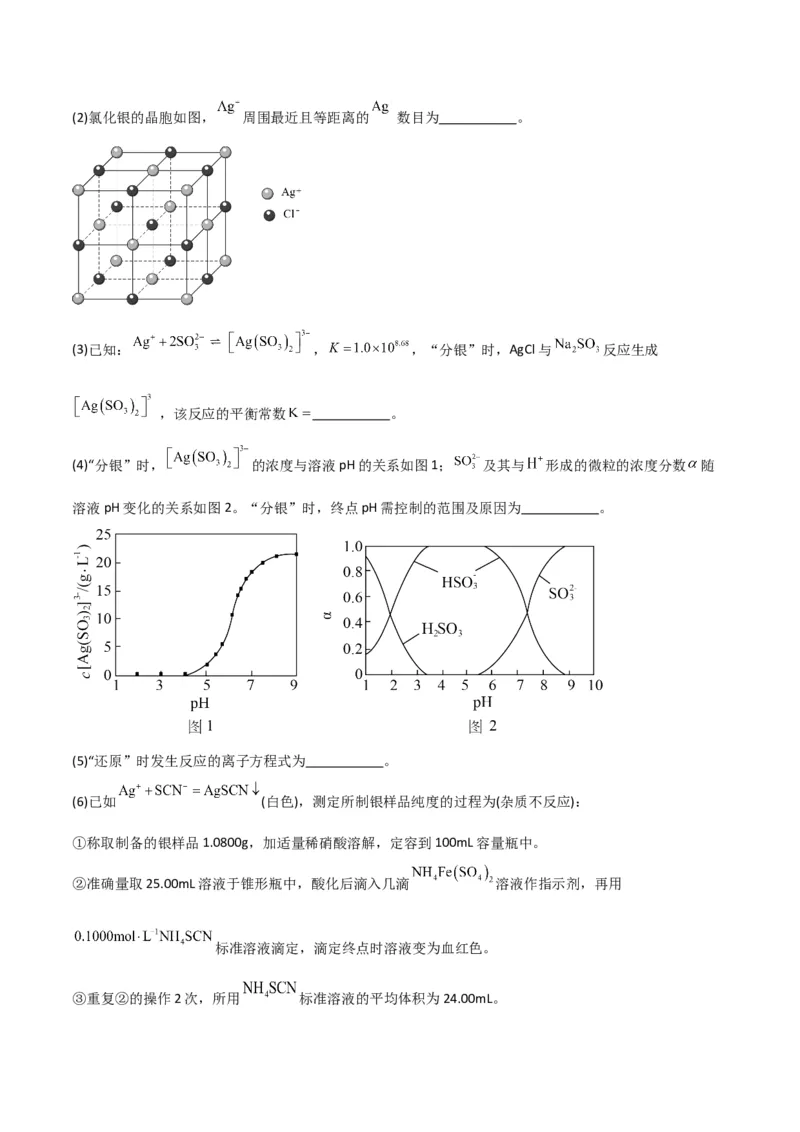
(1)“预处理”加入 溶液将 转化为AgCl,反应的化学方程式为 。(2)氯化银的晶胞如图, 周围最近且等距离的 数目为 。
(3)已知: , ,“分银”时,AgCl与 反应生成
,该反应的平衡常数 。
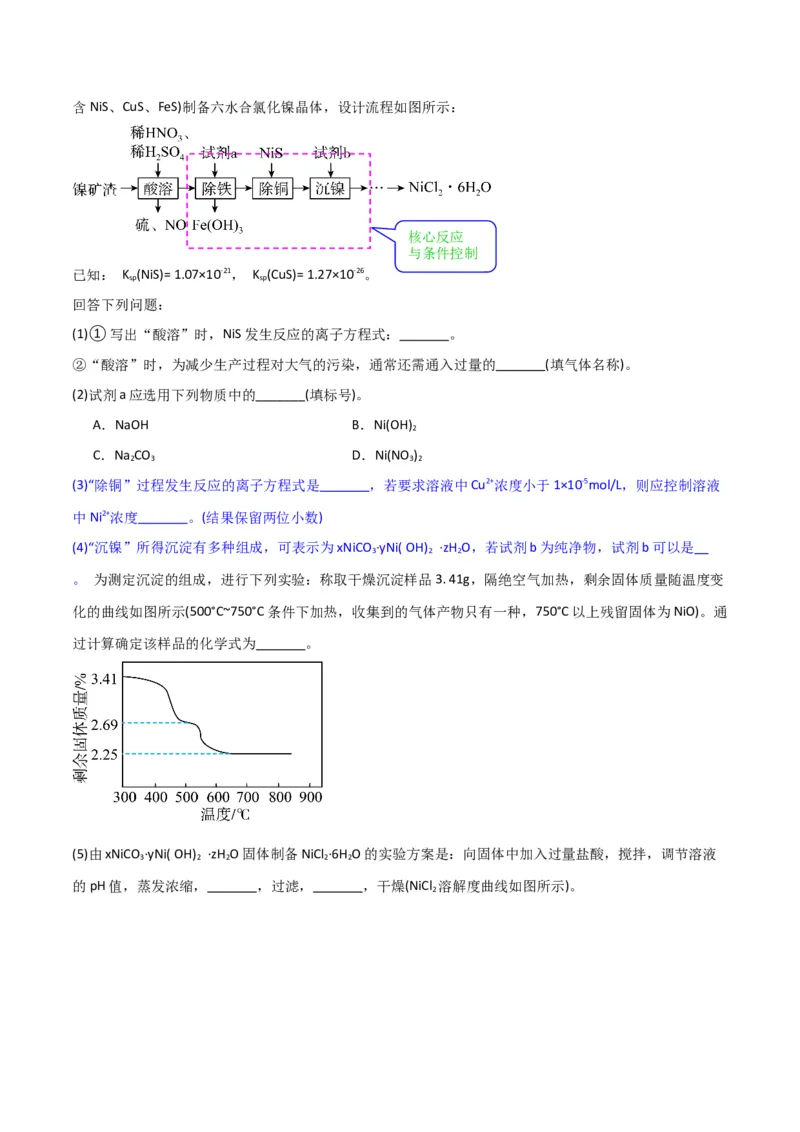
(4)“分银”时, 的浓度与溶液pH的关系如图1; 及其与 形成的微粒的浓度分数 随
溶液pH变化的关系如图2。“分银”时,终点pH需控制的范围及原因为 。
(5)“还原”时发生反应的离子方程式为 。
(6)已如 (白色),测定所制银样品纯度的过程为(杂质不反应):
①称取制备的银样品1.0800g,加适量稀硝酸溶解,定容到100mL容量瓶中。
②准确量取25.00mL溶液于锥形瓶中,酸化后滴入几滴 溶液作指示剂,再用
标准溶液滴定,滴定终点时溶液变为血红色。
③重复②的操作2次,所用 标准溶液的平均体积为24.00mL。计算样品中银的质量分数(写出计算过程) 。
4.(2023·江西·校联考二模)钯(Pd)是一种贵金属,活性炭载钯催化剂广泛应用于石油化工、制药等工业,
但使用过程中因生成难溶于酸的PdO而失活。一种从废钯催化剂(杂质主要含有机物、活性炭、 及
少量Fe、Cu等元素)中回收海绵钯的工艺流程如图:
核心反应
与条件控制
已知:I.阴、阳离子交换树脂的基本工作原理分别为 、
( 表示树脂的有机成分)。
Ⅱ.“沉钯”时得到氯钯酸铵 固体,不溶于冷水,可溶于稀盐酸。
请回答下列问题:
(1)进行“焙烧”的目的是 。
(2)“浸取”时,加入 有利于Pd的溶解,生成的四氯合钯(Ⅱ)酸( )为二元强酸。加入浓盐酸
和 后主要反应的离子方程式: 。
(3)“离子交换除杂”应使用 (填“阳离子”或“阴离子”)树脂。
(4)“还原”过程 转化为 ,在反应器出口处器壁内侧有白色晶体生成,该过程发生的化学方程式为
,且该反应的副产物可循环利用至 环节(填环节名称)。
(5)研究表明有些过渡金属型氢化物能高效的储存和输送氢能源,如LaH 、TiH ,已知标准状况下,1体
2.76 1.73
积的钯粉大约可吸附896体积的氢气(钯粉的密度为10.64g·cm-3,相对原子质量为106.4),试写出钯(Pd)的
氢化物的化学式 。在第二步还原过程中,也可用 代替N H 进行热还原,但消耗的H 质量比理论
2 4 2
值略高,其原因是 。
5.(2023·云南·校联考二模)六水合氯化镍(NiCl ·6H O)常用于电镀、陶瓷等工业。某实验室以镍矿渣(主要
2 2含NiS、CuS、FeS)制备六水合氯化镍晶体,设计流程如图所示:
核心反应
与条件控制
已知: K (NiS)= 1.07×10-21, K (CuS)= 1.27×10-26。
sp sp
回答下列问题:
(1)①写出“酸溶”时,NiS发生反应的离子方程式: 。
②“酸溶”时,为减少生产过程对大气的污染,通常还需通入过量的 (填气体名称)。
(2)试剂a应选用下列物质中的_______(填标号)。
A.NaOH B.Ni(OH)
2
C.Na CO D.Ni(NO )
2 3 3 2
(3)“除铜”过程发生反应的离子方程式是 ,若要求溶液中Cu2+浓度小于1×10-5mol/L,则应控制溶液
中Ni2+浓度 。(结果保留两位小数)
(4)“沉镍”所得沉淀有多种组成,可表示为xNiCO ·yNi( OH) ·zH O,若试剂b为纯净物,试剂b可以是
3 2 2
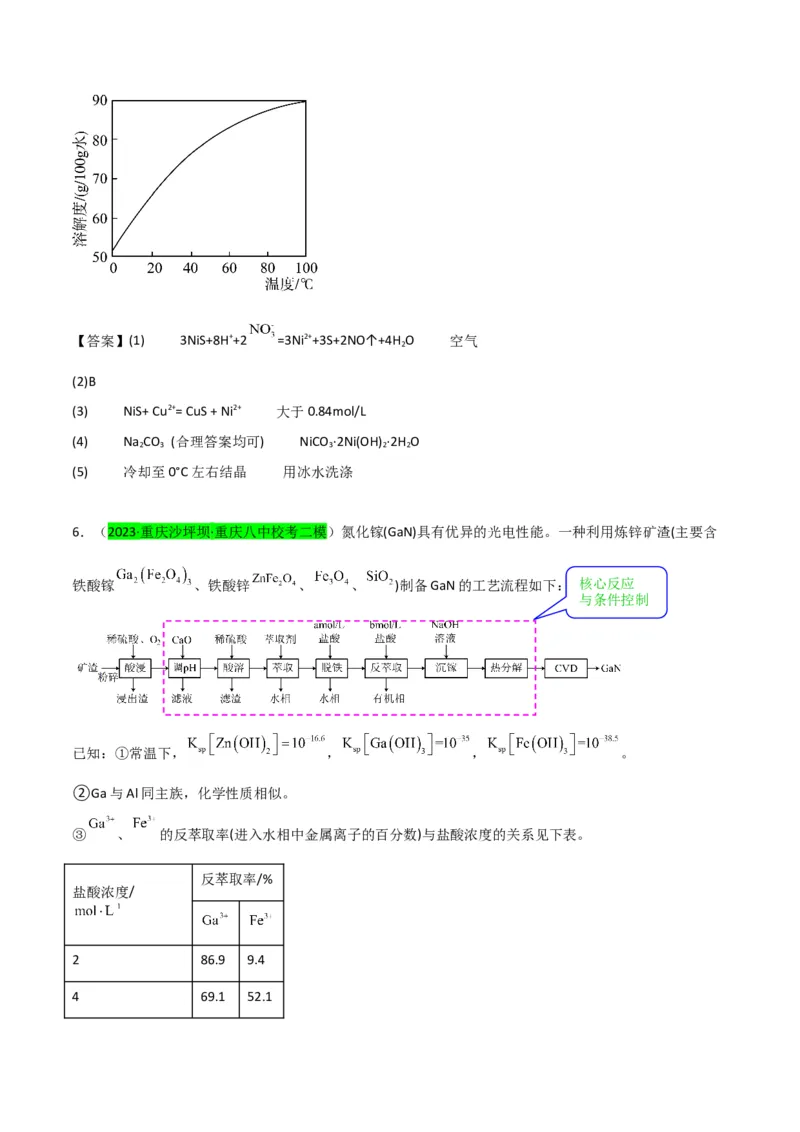
。 为测定沉淀的组成,进行下列实验:称取干燥沉淀样品3. 41g,隔绝空气加热,剩余固体质量随温度变
化的曲线如图所示(500°C~750°C条件下加热,收集到的气体产物只有一种,750°C以上残留固体为NiO)。通
过计算确定该样品的化学式为 。
(5)由xNiCO ·yNi( OH) ·zH O固体制备NiCl ·6H O的实验方案是:向固体中加入过量盐酸,搅拌,调节溶液
3 2 2 2 2
的pH值,蒸发浓缩, ,过滤, ,干燥(NiCl 溶解度曲线如图所示)。
2【答案】(1) 3NiS+8H++2 =3Ni2++3S+2NO↑+4H O 空气
2
(2)B
(3) NiS+ Cu2+= CuS + Ni2+ 大于0.84mol/L
(4) Na CO (合理答案均可) NiCO ·2Ni(OH) ·2H O
2 3 3 2 2
(5) 冷却至0°C左右结晶 用冰水洗涤
6.(2023·重庆沙坪坝·重庆八中校考二模)氮化镓(GaN)具有优异的光电性能。一种利用炼锌矿渣(主要含
铁酸镓 、铁酸锌 、 、 )制备GaN的工艺流程如下: 核心反应
与条件控制
已知:①常温下, , , 。
②Ga与Al同主族,化学性质相似。
③ 、 的反萃取率(进入水相中金属离子的百分数)与盐酸浓度的关系见下表。
反萃取率/%
盐酸浓度/
2 86.9 9.4
4 69.1 52.16 17.5 71.3
回答下列问题:
(1)基态镓的电子排布式为 ,GaN晶胞结构与金刚石类似,其中N原子的轨道杂化类型为 。
(2)提高“酸溶”时溶出率的方法有 (任写2种)。
(3)酸浸时 发生反应的化学方程式为 。
(4)“酸浸”所得浸出液中 、 浓度分别为 、 。常温下,为尽可能多地提取 并
确保不混入 ,“调pH”时需用CaO调节pH的范围为 (假设调pH时溶液体积不变);“酸
溶”所得滤渣的主要成分是 (填化学式)。
(5)“脱铁”和“反萃取”时,所用盐酸的浓度 , (选填上表中盐酸的浓度)。
(6)“沉镓”时,若加入NaOH的量过多,会导致 的沉淀率降低,原因是 (用离子方程式表示)。