文档内容
微专题38 强弱电解质的判断与比较
1.(2023·浙江·统考高考真题)草酸( )是二元弱酸。某小组做如下两组实验:
实验I:往 溶液中滴加 溶液。
实验Ⅱ:往 溶液中滴加 溶液。
[已知: 的电离常数 ,溶液混合后体积变化忽略不
计],下列说法正确的是
A.实验I可选用甲基橙作指示剂,指示反应终点
B.实验I中 时,存在
C.实验Ⅱ中发生反应
D.实验Ⅱ中 时,溶液中
【答案】D
【解析】A. 溶液被氢氧化钠溶液滴定到终点时生成显碱性的草酸钠溶液,为了减小实验误差要
资料整理【淘宝店铺:向阳百分百】选用变色范围在碱性范围的指示剂,因此,实验I可选用酚酞作指示剂,指示反应终点,故A错误;
B.实验I中 时,溶质是 、 且两者物质的量浓度相等,
,,则草酸氢根的电离程度大于草酸根的水解程度,因此存在
,故B错误;
C.实验Ⅱ中,由于开始滴加的氯化钙量较少而 过量,因此该反应在初始阶段发生的是
,该反应的平衡常数为
,因为平衡常数很大,说明反应能够完全进行,当
完全消耗后, 再和 发生反应,故C错误;
D.实验Ⅱ中 时,溶液中的钙离子浓度为
,溶液中
,故D正确。
综上所述,答案为D。
2.(2022·北京·高考真题)2022年3月神舟十三号航天员在中国空间站进行了“天宫课堂”授课活动。其
中太空“冰雪实验”演示了过饱和醋酸钠溶液的结晶现象。下列说法不正确的是
A.醋酸钠是强电解质
B.醋酸钠晶体与冰都是离子晶体
C.常温下,醋酸钠溶液的
资料整理【淘宝店铺:向阳百分百】D.该溶液中加入少量醋酸钠固体可以促进醋酸钠晶体析出
【答案】B
【解析】A.醋酸钠在水溶液中能完全电离,醋酸钠是强电解质,故A正确;
B.醋酸钠晶体是离子晶体,冰是分子晶体,故B错误;
C.醋酸钠是强碱弱酸盐,常温下,醋酸钠溶液的 ,故C正确;
D.过饱和醋酸钠溶液处于亚稳态,加入少量醋酸钠固体可以促进醋酸钠晶体析出,形成饱和溶液,故D
正确;
选B。
一、判断弱电解质的三个思维角度
1.弱电解质的定义,即弱电解质不能完全电离,如测0.1 mol·L-1的CHCOOH溶液的pH>1。
3
2.弱电解质溶液中存在电离平衡,条件改变,平衡移动,如 pH=1的CHCOOH加水稀释10倍后,
3
17。
二、弱电解质的判断方法
(1)在相同浓度、相同温度下,与强电解质溶液做导电性对比实验。
(2)浓度与pH的关系。如0.1 mol·L-1 CH COOH溶液的pH>1,则可证明CH COOH是弱电解质。
3 3
(3)测定对应盐溶液的酸碱性。如CH COONa溶液呈碱性,则可证明CH COOH是弱酸。
3 3
(4)稀释前后溶液的pH与稀释倍数的关系。例如,将pH=2的酸溶液稀释至原体积的1 000倍,若pH小
于5,则证明该酸为弱酸;若pH为5,则证明该酸为强酸。
(5)通过电离常数比较,电离常数越大,弱酸(或弱碱)酸性(或碱性)相对较强。
一、定义与物质类别
完全电离 强 电解质:包括强酸、强碱、大多数盐等。
电解质 在水溶液中
弱部 电分电解离质
:包括弱酸、弱碱、极少数盐[如(CH3COO)2Pb]、水等
资料整理【淘宝店铺:向阳百分百】1.弱电解质:包括弱酸、弱碱、极少数盐(如醋酸铅)、两性氢氧化物、水等。
2.弱电解质的电离平衡
(1)电离平衡的建立
在一定条件下(如温度、压强等),当弱电解质电离产生离子的速率和离子结合成分子的速率相等时,电离
过程达到了平衡。
(2)电离平衡的特征(也适用于勒夏特列原理)
3.判断强弱电解质的核心依据
电解质在水溶液中的电离程度,若不完全电离则为弱电解质。
4.弱电解质判断的注意事项
①酸碱的强弱和溶液酸碱性的强弱不是等同关系,前者看电离程度,后者看溶液中c(H+)和c(OH-)的相对
大小。强酸溶液的酸性不一定比弱酸溶液的酸性强。
②弱酸、弱碱是弱电解质,但它们对应的盐一般为强电解质,如醋酸铵:CHCOONH===NH+CHCOO
3 4 3
-。
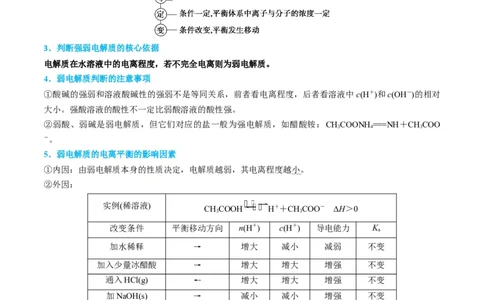
5.弱电解质的电离平衡的影响因素
①内因:由弱电解质本身的性质决定,电解质越弱,其电离程度越小。
②外因:
实例(稀溶液)
CHCOOH H++CHCOO- ΔH>0
3 3
改变条件 平衡移动方向 n(H+) c(H+) 导电能力 K
a
加水稀释 → 增大 减小 减弱 不变
加入少量冰醋酸 → 增大 增大 增强 不变
通入HCl(g) ← 增大 增大 增强 不变
加NaOH(s) → 减小 减小 增强 不变
加入镁粉 → 减小 减小 增强 不变
升高温度 → 增大 增大 增强 增大
加CHCOONa(s) ← 减小 减小 增强 不变
3
6.强、弱电解质的比较
(1)一元强酸(HCl)与一元弱酸(CH COOH)的比较
3
①相同物质的量浓度、相同体积的盐酸与醋酸溶液的比较
c(H+) pH 中和碱的 与足量活泼金属反应产 开始与金
资料整理【淘宝店铺:向阳百分百】属反应的
酸 能力 生H 的量
2
速率
盐酸 大 小 大
相同 相同
醋酸溶液 小 大 小
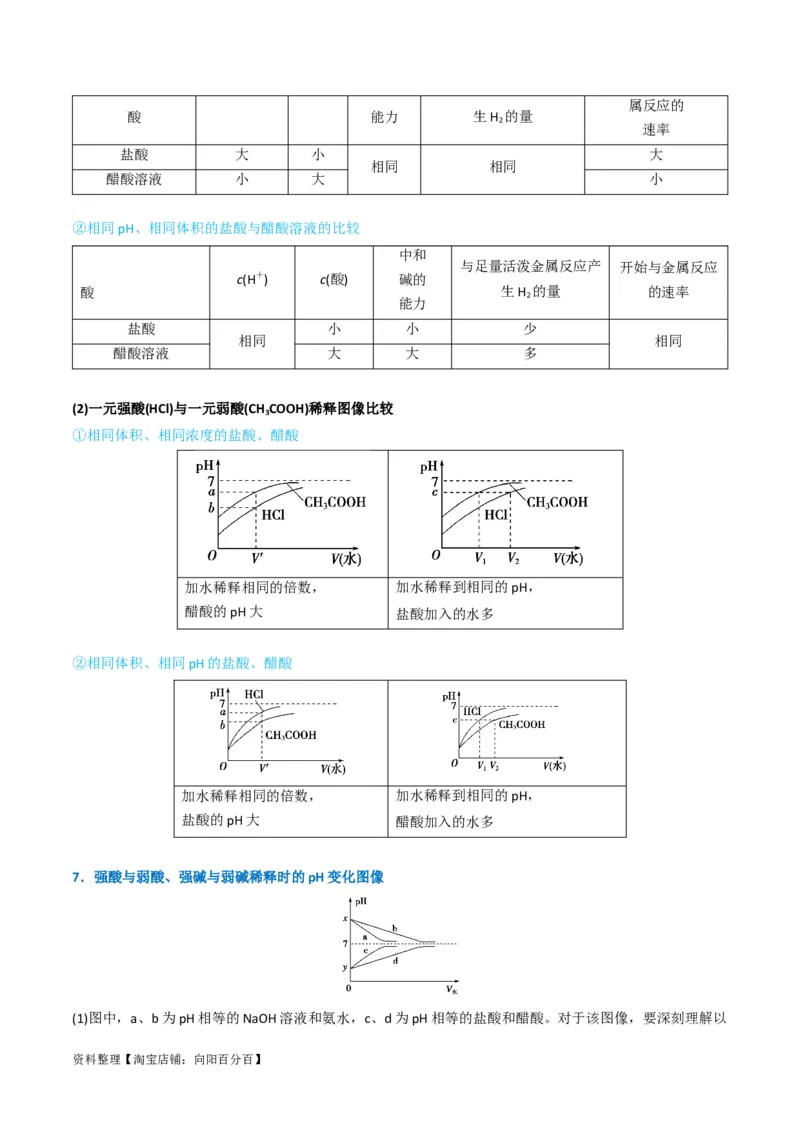
②相同pH、相同体积的盐酸与醋酸溶液的比较
中和
与足量活泼金属反应产 开始与金属反应
c(H+) c(酸) 碱的
酸 生H 的量 的速率
2
能力
盐酸 小 小 少
相同 相同
醋酸溶液 大 大 多
(2)一元强酸(HCl)与一元弱酸(CH COOH)稀释图像比较
3
①相同体积、相同浓度的盐酸、醋酸
加水稀释相同的倍数, 加水稀释到相同的pH,
醋酸的pH大 盐酸加入的水多
②相同体积、相同pH的盐酸、醋酸
加水稀释相同的倍数, 加水稀释到相同的pH,
盐酸的pH大 醋酸加入的水多
7.强酸与弱酸、强碱与弱碱稀释时的pH变化图像
(1)图中,a、b为pH相等的NaOH溶液和氨水,c、d为pH相等的盐酸和醋酸。对于该图像,要深刻理解以
资料整理【淘宝店铺:向阳百分百】下4点:
①对于pH=y的强酸溶液稀释时,体积每增大10n倍,pH就增大n个单位,即pH=y+n;对于pH=y的弱
酸溶液来说,体积每增大10n倍,pH增大不足n个单位,即pH<y+n;无论怎样稀释,酸溶液的pH不能
等于或大于7,只能趋近于7。
②对于pH=x的强碱溶液稀释时,体积每增大10n倍,pH就减小n个单位,即pH=x-n;对于pH=x的弱
碱溶液来说,体积每增大10n倍,pH减小不足n个单位,即pH>x-n;无论怎样稀释,碱溶液的pH不能
等于或小于7,只能趋近于7。
③加水稀释相同倍数后的pH大小;氨水>NaOH溶液,盐酸>醋酸。
④稀释后的pH仍然相等,则加水量的多少:氨水>NaOH溶液,醋酸>盐酸。
(2)体积相同、浓度相同的盐酸与醋酸加水稀释图像如图。
若稀释相同倍数,二者浓度仍相同,仍然是盐酸的pH小,但差变小。
1.(2023·全国·高三专题练习)下列说法正确的是
A.Na CO 是强电解质,故Na CO 的电离方程式为Na CO =Na +CO
2 3 2 3 2 3
B.室温下,0.1 mol·L-1的BOH溶液的pH=11,则BOH的电离方程式为BOH B++OH-
C.25 ℃ NaA溶液的pH>7,则HA的电离方程式为HA=H++A-
D.CaCO 的饱和水溶液导电性很弱,故CaCO 的电离方程式为CaCO Ca2++CO
3 3 3
【答案】B
【解析】A.Na CO 的电离方程式为Na CO =2Na++CO ,故A错误;
2 3 2 3
B.室温下,0.1 mol·L-1的BOH溶液的pH=11,说明BOH为弱碱,电离过程可逆,电离方程式为:BOH
B++OH-,故B正确;
C.25 ℃ NaA溶液的pH>7,说明NaA是强碱弱酸盐,HA为弱酸,电离过程可逆,电离方程式为:HA H
++A-,故C错误;
资料整理【淘宝店铺:向阳百分百】D.CaCO 难溶,但属于强电解质,全部电离,电离方程式为:CaCO =Ca2++CO ,故D错误;
3 3
故选B。
2.(2023·重庆渝中·重庆巴蜀中学校考模拟预测)下列实验操作能达到实验目的的是
实验操作 实验目的
A 将充满 的试管倒扣在水槽中,试管内液面高于水槽 证明 与水发生反应
比较还原性:
B 向 、KI的混合溶液中加入少量溴水和 ,振荡
C 用pH计分别测量 盐酸和 醋酸的pH 验证 为弱酸
向含琼脂和食盐水的混合物中滴加酚酞、 溶液,混合均匀后
D 验证锌对铁的保护
再放入裹有锌皮的铁钉
A.A B.B C.C D.D
【答案】C
【解析】A.二氧化硫溶于水也会导致液面上升,不能达到实验目的,A不符合题意;
B.少量的溴水和碘离子反应也不完全,不能证明其不和氯离子反应,不能达到实验目的,B不符合题意;
C.分别测量 盐酸和 醋酸的pH,等浓度的醋酸pH较大,说明气部分电离,为弱酸,
C符合题意;
D. 能检验亚铁离子,但是其中的配离子铁离子会和锌生成亚铁离子,故不能达到实验目的,
D不符合题意;
故选C。
1.(2023·上海·统考模拟预测)常温常压下,下列物质的物理量种前者是后者两倍的是
A.28 g 和28g 中所含的中子数
B.2.24 L 和2.24 L 原子数
C.1mol 和2mol 的密度
资料整理【淘宝店铺:向阳百分百】D.0.1mol·L 和0.1 mol·L 的
【答案】C
【解析】A.28 g28Si是1mol28Si,质子数为14N ,中子数14N ,28g14N是2mol14N,质子数为2×7N =14N ,
A A A A
中子数为2×7N =14N ,A不符合;
A A
B.常温常压下2.24 LSO 和2.24 LN 分子数为1:1,原子数之比为3:2,B不符合;
2 2
C.1molSO 和2molO 的密度之比等于分子的摩尔质量之比,与物质的量无关,密度之比等于64:32=2:1,C
2 2
符合;
D.硫酸为强电解质,能完全电离,醋酸为弱电解质,不能完全电离,故0.1mol·L−1H SO 和0.1 mol·L−1
2 4
CH COOH的c(H+)之比大于2:1,D不符合;
3
故答案为:C。
2.(2022·广东·统考模拟预测)根据下列实验操作与现象能得出相应结论的是
选
实验操作与现象 结论
项
A 将少量氯气缓慢通入到 溶液中,得到黄色溶液 氧化性:
向 溶液中滴加NaOH溶液,测得溶液的导电性在滴加NaOH
B HX是弱酸
溶液过程中开始时增强
溶液中 、 至少含
C 向某溶液中加入几滴 溶液及足量稀硝酸,最终得到白色沉淀
有一种
D 将 通入酸性 溶液中, 溶液褪色 具有漂白性
A.A B.B C.C D.D
【答案】B
【解析】A. 也可被 氧化生成碘单质,且得到的溶液也可显黄色,所以不能证明氧化性: ,
故A错误;
B.由导电性增大可知弱电解质变为强电解质,则HX是弱电解质,HX是弱酸,故B正确;
C.若溶液中含有 ,最终也可得到硫酸钡沉淀,故C错误;
D. 使 溶液褪色表现出的是 的还原性,故D错误;
选B。
资料整理【淘宝店铺:向阳百分百】3.(2023·辽宁沈阳·沈阳二中校考模拟预测)下列操作能实现相应的实验目的的是
选
实验目的 操作步骤及现象
项
加入酚酞做指示剂,用同浓度的烧碱溶液滴定,终点消耗烧碱溶液体
A 证明HA是强酸
积与HA相同
证明H 与I (g)的反应为可 将物质的量之比为2:1的H 与I (g)混合气体在一定条件下充分反应,
B 2 2 2 2
逆反应 混合气体呈紫色
向麦芽糖溶液中加稀硫酸并加热,冷却后加入烧碱中和过量硫酸再加
C 证明麦芽糖能水解
入银氨溶液加热,析出银镜
D 证明氧化性: 将硫酸酸化的H O 滴入Fe(NO ) 溶液中,再滴入KSCN溶液,溶液变红
2 2 3 2
A.A B.B C.C D.D
【答案】B
【解析】A.证明HA是强酸,加入酚酞做指示剂,用同浓度的烧碱溶液滴定消耗等体积的烧碱溶液,由于达
到滴定终点时溶液呈碱性,无法说明HA为强酸,故A错误;
B.将物质的量之比为2:1的H 与I (g)混合气体在一定条件下充分反应,混合气体呈紫色,说明I (g)未完
2 2 2
全反应,证明H 与I (g)的反应为可逆反应,故B正确;
2 2
C.麦芽糖、葡萄糖中都有-CHO,向麦芽糖溶液中加稀硫酸并加热,冷却后加入烧碱中和过量硫酸,再加
入银氨溶液加热,析出银镜,不能说明麦芽糖水解产物具有还原性,故C错误;
D.酸性条件下硝酸根离子氧化亚铁离子生成铁离子,由现象不能判断H O 、Fe3+的氧化性,故D错误;
2 2
故选B。
4.(2023·湖南·校联考模拟预测)常温下,用 的 溶液滴定 浓度分别为 、
的一元酸(HA)、二元酸 溶液,得到如图滴定曲线,其中c、d为两种酸恰好完全中和的化学计量点。
忽略溶液混合时体积变化,下列叙述正确的是
资料整理【淘宝店铺:向阳百分百】A.X曲线代表 ,Y曲线代表HA,
B.两种酸恰好完全中和时,均可用酚酞或甲基橙作指示剂
C.若a点 ,则a点
D. 溶液中,
【答案】D
【解析】A.比较图中c、d点数值可知,HA消耗的 小于 消耗 的二倍,则 ,
A错误;
B. 、HA恰好完全中和时,产物为强碱弱酸盐,均呈碱性,可使用酚酞作指示剂,不可使用甲基橙作
指示剂,B错误;
C. 完全中和时消耗 ,a点 时, %=75%,占消
耗氢氧化钠总体积的四分之三,则溶质为 与 ,且二者的浓度比为 ,则a点物料守恒和电荷
守恒有关系式: ①,
②,用②-①,得 ;由于a点溶液呈酸性,
,故 ,C错误;
D.由图可知, 被完全中和时需消耗 ,则加入 溶液时, 恰
好转化为 ,因为 ,所以 溶液呈酸性,故可推断 的电离程度大于 的水解程度,
即 ,故 ,D正确;
故答案为:D。
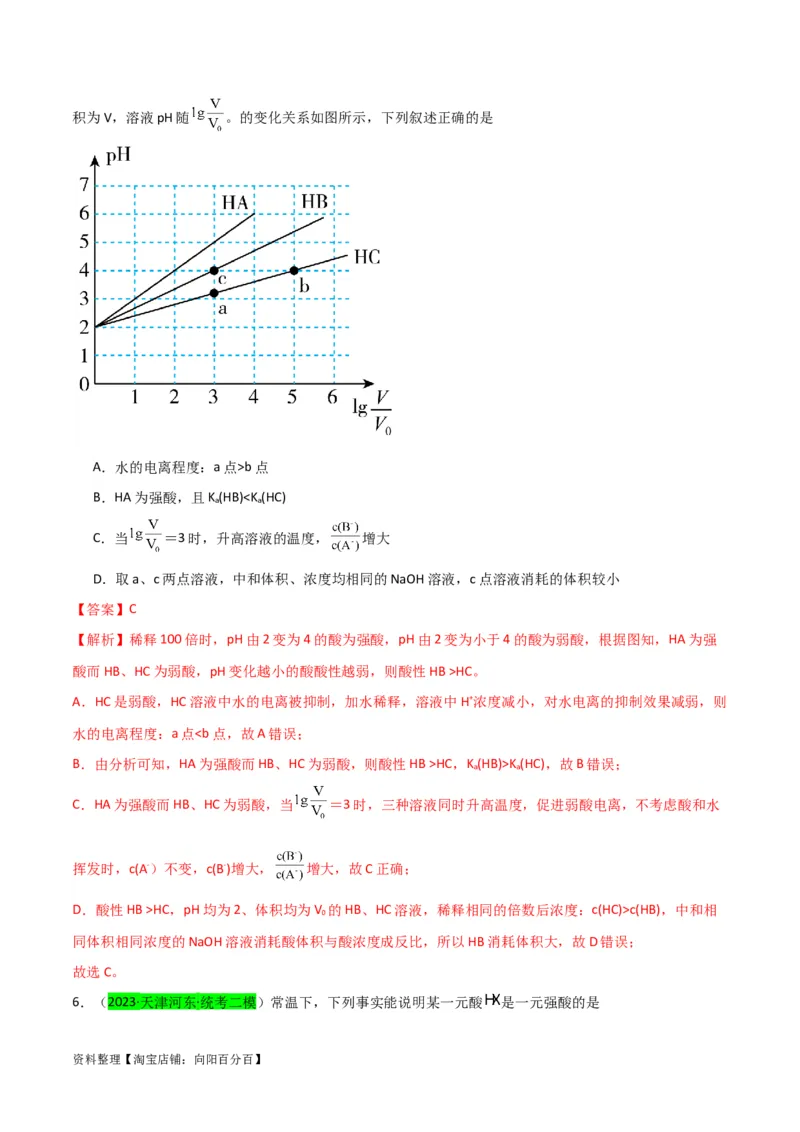
5.(2023·贵州贵阳·统考二模)常温下,pH均为2、体积均为V 的HA、HB、HC溶液,分别加水稀释至体
0
资料整理【淘宝店铺:向阳百分百】积为V,溶液pH随 。的变化关系如图所示,下列叙述正确的是
A.水的电离程度:a点>b点
B.HA为强酸,且K(HB)HC。
A.HC是弱酸,HC溶液中水的电离被抑制,加水稀释,溶液中H+浓度减小,对水电离的抑制效果减弱,则
水的电离程度:a点HC,K(HB)>K(HC),故B错误;
a a
C.HA为强酸而HB、HC为弱酸,当 =3时,三种溶液同时升高温度,促进弱酸电离,不考虑酸和水
挥发时,c(A-)不变,c(B-)增大, 增大,故C正确;
D.酸性HB >HC,pH均为2、体积均为V 的HB、HC溶液,稀释相同的倍数后浓度:c(HC)>c(HB),中和相
0
同体积相同浓度的NaOH溶液消耗酸体积与酸浓度成反比,所以HB消耗体积大,故D错误;
故选C。
6.(2023·天津河东·统考二模)常温下,下列事实能说明某一元酸 是一元强酸的是
资料整理【淘宝店铺:向阳百分百】A. 溶液的
B. 溶液
C. 溶液比 硝酸导电能力弱
D. 溶液与 溶液混合
【答案】D
【解析】A. 溶液的 ,说明HX在水溶液中只能部分电离,属于一元弱酸,A不合题意;
B. 溶液 ,说明NaX是强碱弱酸盐,因为X-水解呈碱性,即HX为一元弱酸,B不合
题意;
C. 溶液比 硝酸导电能力弱说明HX只能部分电离,属于一元弱酸,C不合题意;
D. 溶液与 溶液,二者前后完全反应生成NaX,混合后溶液
即说明NaX为强酸强碱盐,即说明HX为一元强酸,D符合题意;
故答案为:D。
7.(2023·吉林长春·统考模拟预测) 时,向浓度均为 、体积均为 的两种一元酸
溶液中分别加入 固体,溶液中 随 的变化如图所示。下列说法正确的是
A.a点时溶液中水电离出的
资料整理【淘宝店铺:向阳百分百】B.c点时溶液中:
C.水的电离程度:
D.中和等体积、等浓度的两种酸所需的 的物质的量:
【答案】B
【解析】A.a点 , ,则溶液中 mol/L,HX抑制水电离,所以水电离
出的 mol/L,A错误;
B.c点表示向浓度为 、体积为100 mL的HY溶液中加入0.005 mol NaOH固体,溶质为等物质的
量浓度的HY、NaY,溶液呈酸性,HY电离大于NaY水解,所以 ,B正确;
C.d点酸电离出的氢离子浓度大于c点,水的电离程度dHY。
Y
下列判断正确的是
A.V>V
x Y
B.M点:c(X-)= c(Y-)
C.b表示盐酸滴定NaX溶液的曲线
D.常温下,K (HX) = 9.0×10-12
a
【答案】A
【解析】A.NaY溶液水解程度更大,初始碱性更强,氢氧根离子浓度更大;加入等量V 体积盐酸后,
M
NaX、NaY溶液的pH相等,那么两者消耗氢氧根离子的量相同,则NaY溶液的体积更小,故V>V,A正确;
x Y
B.根据物料守恒可知,NaX溶液中 ,NaY溶液中 ,且初始钠
资料整理【淘宝店铺:向阳百分百】离子浓度相同,若M点:c(X-)= c(Y-),则 ,M点pH相同,则
;已知:酸性HX>HY,则 ;两者相互矛
盾,B错误;
C.由分析可知,b表示盐酸滴定NaY溶液的曲线,C错误;
D. ,由0.1 mol·L-1的NaX溶液的初始pH=11可知,pOH=3,
、 ,则 ,
,D错误;
故选A。
1.(2023春·福建福州·高三统考阶段练习)利用如图装置和试剂,能达到实验目的的是
A B C D
探究蔗糖在酸
探究温度对化学反应
电解饱和食盐水并收集某种产物 性条件下的水 证明醋酸是一种弱电解质
速率的影响
解反应
A.A B.B C.C D.D
【答案】A
【解析】A.电解饱和食盐水,铁棒是阴极,阴极生成氢气,用向下排空气法收集氢气,石墨是阳极,阳
极生成氯气,用氢氧化钠吸收氯气,故选A;
资料整理【淘宝店铺:向阳百分百】B.蔗糖在稀硫酸中发生水解反应生成葡萄糖和果糖,蔗糖和浓硫酸混合发生脱水反应,故不选B;
C.用1mol/L的盐酸和1mol/L的醋酸溶液组成串联电路,串联电路中的电流一样大,灯泡亮度相同,不能
证明醋酸是弱电解质,故不选C;
D.图示装置可探究温度对化学平衡的影响,不能探究温度对反应速率的影响,故不选D;
选A。
2.(2023秋·辽宁朝阳·高三校联考期末)硼酸微溶于冷水,在水溶液中发生电离:
,使溶液显酸性,通常可通过乙硼烷(B H )水解制得硼酸:
2 6
。下列说法错误的是
A.硼酸属于弱电解质
B. 中存在极性键和配位键
C.乙硼烷中硼元素的化合价为+3价
D.硼酸与过量NaOH溶液反应生成 和
【答案】D
【解析】A.由硼酸的电离方程式知,硼酸是一元弱酸,A项正确;
B. 中B与O之间存在配位键,O和H之间存在极性键,B项正确;
C.电负性: ,所以乙硼烷中硼元素显 价,C项正确;
D.硼酸是一元酸,根据电离方程式可知硼酸与过量NaOH溶液反应生成 ,D项错误;
故选D。
3.(2023·广东深圳·统考二模)下列实验操作能达到相应实验目的的是
选
实验目的 实验操作
项
A 除去氨气中的水蒸气 将混合气体通入盛有浓 的洗气瓶
验证 是弱电解 分别取相同体积、 溶液和盐酸,测定两者pH,并
B
质 比较大小
检验1-溴丁烷中含有溴元
C 取适量样品于试管中,加入适量 溶液后加热,再滴加 溶液
素
资料整理【淘宝店铺:向阳百分百】验证 向 溶液中滴加几滴 溶液,产生白
D
色沉淀后,再滴加几滴 溶液
A.A B.B C.C D.D
【答案】B
【解析】A.由于H SO 能与NH 反应生成NH HSO 或者(NH ) SO ,故NH 不能用浓H SO 干燥,A不合题意;
2 4 3 4 4 4 2 4 3 2 4
B.分别取相同体积0.1mol/L的CH COOH溶液和盐酸,测定两者pH,测得前者pH大于1,后者等于1,即
3
说明CH COOH是弱酸,属于弱电解质,B符合题意;
3
C.由于NaOH能与AgNO 反应生成黑色沉淀Ag O,故取适量样品于试管中,加入适量NaOH溶液后加热,
3 2
再滴加足量的HNO 酸化后滴加AgNO 溶液,若生成淡黄色沉淀,即可检验为溴代烃,C不合题意;
3 3
D.向 溶液中滴加几滴 溶液,产生白色沉淀后,再滴加几滴
溶液,由于AgNO 溶液过量,生成黄色沉淀AgI,可能是Ag+与I-直接反应,也可能是AgCl转
3
化为AgI,D不合题意;
故答案为:B。
4.(2023·天津·校联考一模)已知常温时 的 的 ,现将 和体积都相
同的次氯酸和氢氟酸溶液分别加蒸馏水稀释, 随溶液体积的变化如图所示,下列叙述正确的是
A.曲线Ⅱ为氢氟酸稀释时 的变化曲线
B.取相同体积a点的两种酸溶液,中和相同浓度的 溶液,消耗 溶液体积较小
C.b点溶液中水的电离程度比c点溶液中水的电离程度小
D.从b点到d点,溶液中 的值变小( 代表 或 )
【答案】D
资料整理【淘宝店铺:向阳百分百】【解析】A.酸性越强,加水稀释时溶液pH变化越大,HF酸性强于HClO,加水稀释时pH变化大,所以曲
线Ⅰ代表HF稀释时pH变化曲线,选项A错误;
B.pH相同的两种酸,越弱的酸其浓度越大,消耗的NaOH溶液体积更多,HF酸性强于HClO,所以中和相
同体积、相同浓度的NaOH溶液, 浓度小,消耗溶液体积较大,选项B错误;
C.酸越弱,电离出H+趋势越小,对水的电离抑制程度越低,所以b点溶液中水的电离程度比c点溶液中
水的电离程度大,选项C错误;
D.溶液中 = = ,K 和K 只随温度的改变而改变,所以从b点到d点,溶
a w
液中 保持不变,选项D正确;
答案选D。
5.(2023·全国·高三统考专题练习)根据实验目的,下列实验操作及现象、实验结论都正确的是
选
实验目的 实验操作及现象 实验结论
项
检验硫酸厂周边空气 用注射器多次抽取空气,慢慢注入盛有酸性KMnO 稀溶液的 空气中不含
A 4
是否含有SO 同一试管中,溶液不变色 SO
2 2
证明CH COOH是弱 CH COOH是
B 3 用pH计分别测量醋酸溶液和盐酸的pH,醋酸溶液的pH大 3
电解质 弱电解质
向淀粉水解液中加入NaOH溶液调节溶液至碱性,并分成两
淀粉部分水
C 探究淀粉的水解程度 份,向第一份中加入银氨溶液并水浴加热出现银镜;向第二
解
份中滴加少量碘水,溶液变蓝色
探究卤素单质Cl 、
2 向NaBr溶液中通入过量氯气,溶液变橙色,再滴加淀粉KI 氧化性:
D Br 和I 的氧化性强
2 2 溶液,溶液变蓝色 Cl >Br >I
弱 2 2 2
A.A B.B C.C D.D
【答案】A
【解析】A.具有还原性的二氧化硫能与酸性高锰酸钾溶液反应使溶液褪色,溶液不变色说明空气中不含
有二氧化硫,故A正确;
B.没有明确醋酸和盐酸的浓度是否相同,则醋酸溶液的pH大不能证明醋酸是弱电解质,故B错误;
C.碘水会与氢氧化钠溶液反应,则向碱性淀粉水解液中加入碘水,溶液不会变蓝色,故C错误;
D.向溴化钠溶液中通入过量氯气后,再滴加淀粉碘化钾溶液,过量氯气会优先与碘化钾溶液反应使溶液
资料整理【淘宝店铺:向阳百分百】变蓝色,无法比较溴和碘的氧化性强弱,故D错误;
故选A。
6.(2023·浙江·校联考模拟预测)下列说法不正确的是
A.相同温度下, 相等的氨水、 溶液中, 相等
B. 的醋酸溶液的物质的量浓度大于 的醋酸溶液的10倍
C. 均为4的盐酸和氯化铵溶液等体积混合后,所得溶液的
D.用同浓度的 溶液分别与等体积、等 的盐酸和醋酸溶液恰好完全反应,盐酸消耗 溶
液的体积更大
【答案】D
【解析】A.相同温度下,水的离子积相等, 相等的氨水、 溶液中, 相等,则溶液中
相等,A正确;
B.醋酸为弱酸,不能完全电离,浓度越大,电离程度越小, 的醋酸溶液的物质的量浓度为
( 为电离度), 的醋酸溶液的物质的量浓度为 ( 为电离度),故前者比后者
的10倍还大,B正确;
C. 均为4的盐酸和氯化铵溶液等体积混合的瞬间, ,不发生变化,铵根离子
和一水合氨的浓度瞬间变为原来的二分之一,则二者的比值不变,故所得溶液中水的电离平衡没有移动,
氯化铵的水解平衡没有移动,混合溶液中 , ,C正确;
D.醋酸是弱酸,等体积、等 的盐酸和醋酸溶液中醋酸的物质的量大于盐酸的物质的量,则用同浓度的
溶液分别与等体积、等 的盐酸和醋酸溶液恰好完全反应,醋酸消耗 溶液的体积更大,D
资料整理【淘宝店铺:向阳百分百】错误。
故选D。
7.(2023春·上海宝山·高三上海市行知中学校考阶段练习)常温常压下c(H+)=0.1 mol·L−1的两种一元酸HX
和HY的溶液,分别取50mL,加足量的镁粉,充分反应后,收集H 的体积为V(HX)和V(HY),若
2
V(HX)>V(HY),下列说法正确的是
A.HX一定是弱酸 B.HY一定是强酸
C.HX的酸性强于HY的酸性 D.反应过程中二者生成H 的速率相同
2
【答案】A
【解析】常温常压下c(H+)=0.1 mol·L−1的两种一元酸HX和HY的溶液,分别取50mL,加足量的镁粉,充分
反应后,收集H 的体积为V(HX)和V(HY),若V(HX)>V(HY),说明HX的物质的量大于HY的物质的量。
2
A.HX的物质的量大于HY的物质的量,体积相同,说明HX物质的量浓度大于HY物质的量浓度,则说明
HX一定是弱酸,故A正确;
B.根据A选项分析HX一定是弱酸,而HY可能是强酸,也可能是比HX强的弱酸,故B错误;
C.根据B选项分析HX的酸性弱于HY的酸性,故C错误;
D.开始两者氢离子浓度相等,产生氢气的速率相等,后来HX会发生电离或则HX电离出的氢离子浓度比
HY电离出的氢离子浓度大,因此后来产生氢气的速率是HX大于HY,故D错误;
答案为A。
8.(2023·全国·高三专题练习)常温下,为证明NH •H O是弱电解质。下列方法不正确的是
3 2
A.测定0.01mol•L-1氨水的pH
B.测定0.01mol•L-1NH Cl溶液的酸碱性
4
C.测定pH为10的氨水稀释十倍后的pH
D.比较0.01mol•L-1的氨水和1mol•L-1NaOH溶液的导电能力
【答案】D
【解析】A.通过测定 氨水的 ,可证明 是弱电解质,A正确;
B.若 溶液呈酸性,则说明 是强酸弱碱盐,从而说明 是弱电解质,B正确;
C. 的氨水稀释10倍后 ,可以证明氨水稀释过程中有 电离出来,从而说明
是弱电解质,C正确;
资料整理【淘宝店铺:向阳百分百】D.氨水浓度小于 溶液的浓度,无法用导电能力证明 是弱电解质,D错误;
故选D。
9.(2023·全国·高三专题练习)常温下,下列用来判断CH COOH是一种弱酸的说法正确的是
3
①向pH=3的HCl溶液中加入CH COONa固体,溶液pH增大
3
②pH相同的盐酸和CH COOH溶液,取相同体积分别用标准NaOH溶液滴定测其浓度,CH COOH溶液消耗
3 3
的NaOH溶液的体积较大
③0.1mol•L-1CH COOH溶液的pH>1
3
④0.1mol•L-1的盐酸与过量的Mg反应,当加入CH COONa固体后,反应速率减慢,但生成氢气的总量不变
3
⑤相同物质的量浓度、相同体积的CH COOH溶液和盐酸分别与足量的活泼金属反应,消耗金属的量相同
3
⑥pH=4的CH COOH溶液与pH=10的NaOH溶液等体积混合后溶液呈酸性
3
⑦CH COOH溶液中有两种分子存在
3
⑧醋酸钠溶液的pH大于7
A.②③④⑤⑥⑦ B.①②③④⑥⑦⑧ C.②③⑤⑥⑧ D.全部
【答案】B
【解析】
序
解释 正误
号
加入 固体,溶液pH增大,说明 溶液呈碱性,故可知 为弱
① 正确
酸
pH相同的盐酸和 溶液, 溶液消耗的 溶液的体积较大,说明
② 正确
溶液的浓度大,则 为弱酸
溶液的 ,说明 溶液中 小于 ,故可知
③ 正确
为弱酸
盐酸与Mg反应,加入 固体,反应速率减慢,说明溶液中 减小,则可知
④ 正确
与 反应生成了弱酸,故可知 为弱酸
同浓度、同体积的 溶液和盐酸分别与足量的活泼金属反应,消耗金属的量相同, 不正
⑤
不能说明 是弱酸 确
pH之和为14的强酸与 溶液中和后,溶液呈中性,而pH之和为14的弱酸与 溶
⑥ 正确
液中和后,溶液呈酸性
资料整理【淘宝店铺:向阳百分百】水溶液中有水分子存在,则另一种分子必为醋酸分子,故可知醋酸不完全电离,则
⑦ 正确
是弱酸
⑧ 醋酸钠溶液的pH大于7,说明醋酸钠溶液呈碱性,故可知 是弱酸 正确
故选B。
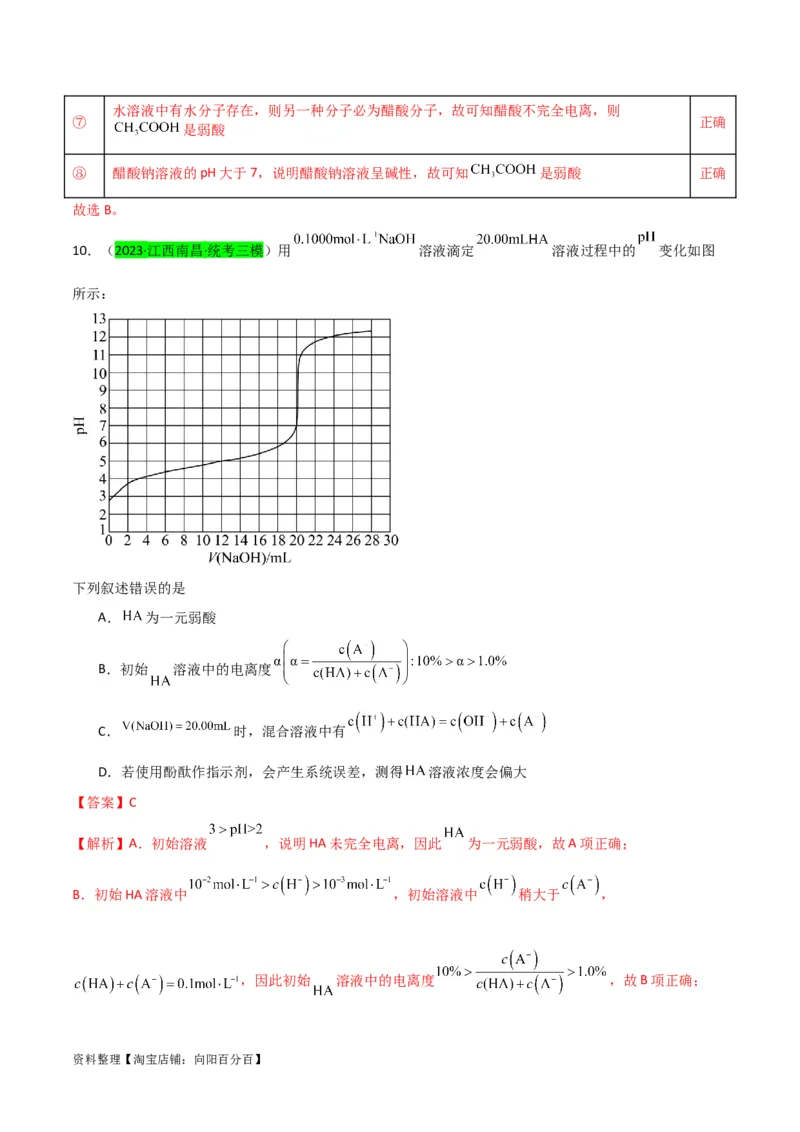
10.(2023·江西南昌·统考三模)用 溶液滴定 溶液过程中的 变化如图
所示:
下列叙述错误的是
A. 为一元弱酸
B.初始 溶液中的电离度
C. 时,混合溶液中有
D.若使用酚酞作指示剂,会产生系统误差,测得 溶液浓度会偏大
【答案】C
【解析】A.初始溶液 ,说明HA未完全电离,因此 为一元弱酸,故A项正确;
B.初始HA溶液中 ,初始溶液中 稍大于 ,
,因此初始 溶液中的电离度 ,故B项正确;
资料整理【淘宝店铺:向阳百分百】C. 时,溶液中溶质为NaA,溶液中存在电荷守恒: ,
物料守恒: ,因此 ,故C项错误;
D.酚酞试液在溶液pH>10时变红,由图可知当溶液pH>10时,所加NaOH溶液体积大于20mL,因此测得
溶液浓度会偏大,故D项正确;
综上所述,错误的是C项。
11.(2023·全国·高三专题练习)下列说法正确的是
A.测得 的一元酸 溶液的 ,则 一定是一种弱电解质
B. 时,可溶性正盐 溶液的 ,升温至 后溶液的 仍为 ,则 不可能为强碱弱
酸盐
C. 时,测得 的一元酸 溶液的 ,将该溶液加水稀释100倍,所得溶液的
,则 为弱酸
D. 时, 的 溶液与 的 溶液等体积混合,所得溶液的 一定等于7
【答案】A
【解析】A.无论溶液处于什么温度, 的一元酸 溶液的 都说明 没有完全电离,
一定是一种弱电解质,A正确;
B.25℃时,若假设 为强碱弱酸盐,且 ,则此溶液中 ,此时升高温度,
增大, 的水解程度也增大,即溶液中的 增大,假设此时 增大到 ,而 增大
到 ,溶液中的 , 保持不变,说明上述假设合理,B错误;
C.25℃时,酸溶液稀释100倍,而溶液的 正好增大2个单位,说明原溶液中 完全电离, 为强
酸,C错误;
D.25℃时,若 的 溶液为弱酸溶液,此时溶液中酸的浓度远大于 ,该溶液与等体积浓
资料整理【淘宝店铺:向阳百分百】度为 的 溶液反应,则酸过量,溶液呈酸性,D错误;
故选A。
12.(2023·全国·高三专题练习)相同温度下,关于盐酸和醋酸两种溶液的比较,下列说法正确的是
A.pH相等的两溶液中:c(CH COO-)=c(Cl-)
3
B.分别中和pH相等、体积相等的两溶液,所需NaOH的物质的量相同
C.相同浓度的两溶液,分别与金属镁反应,反应速率相同
D.相同浓度的两溶液,分别与NaOH固体反应后呈中性的溶液中(忽略溶液体积变化):
c(CH COO-)=c(Cl-)
3
【答案】A
【解析】A. 为强电解质、 为弱电解质,根据电荷守恒得:醋酸溶液中
,盐酸中 ,又因两溶液的 相等,故
,A项正确;
B. 相等的两种溶液,溶质的酸性越弱,溶液的浓度越大,体积相同时所含溶质的物质的量就越多,
的酸性小于 ,所以分别中和 相等、体积相等的两溶液时醋酸溶液所消耗的氢氧化钠更
多,B项错误;
C.溶液与金属镁反应, 越大反应速率越快,相同浓度的两溶液, 完全电离而醋酸部分电离,盐
酸溶液中氢离子浓度始终大于醋酸溶液,因此反应速率:盐酸大于醋酸,C项错误;
D.醋酸恰好和氢氧化钠反应生成醋酸钠溶液中醋酸根离子水解溶液显碱性,中性溶液应为醋酸和醋酸钠,
盐酸恰好反应溶液显中性,设 溶液和盐酸的浓度均为 ,则醋酸反应后呈中性的溶液中,
、结合电荷守恒可知有 ,盐酸反应后呈中性的溶液中, 且
,故二者分别与 固体反应后呈中性的溶液中: ,D项错误;
资料整理【淘宝店铺:向阳百分百】答案选A。
13.(2023·全国·高三专题练习) 时,改变 甲酸 与丙酸 溶液的
,溶液中 分子的物质的量分数 随之改变[已知
], 与 的关系如图所示。下列说法正确的是
A.若弱酸 增大是通过向弱酸中加入 固体实现的,则图中M、N两点对应溶液中的 相
等
B.对于甲酸和丙酸,当 时,溶液都为酸性
C.等浓度的 和 两种溶液的 :前者>后者
D.将 的 溶液与 的 溶液等体积混合,所得溶液中:
【答案】B
【解析】A.两溶液的起始浓度均为 ,M、N两点 相等,则
,根据电荷守恒,M点 ,
,同理,N点 ,
资料整理【淘宝店铺:向阳百分百】,M点和N点, ,但两点
不同, 不同, 不同,故 不相同,A错误;
B.当 时, , ,根据图示可知,此时两溶液均为酸性,
B正确;
C.根据M点知, 时, ,则 ,根据N点知,
时, ,则 ,等浓度的
和 两种溶液中, 的水解程度大于 ,故溶液 :
,C错误;
D. 的电离常数为 , 的水解常数 ,则 的电离程
度大于 的水解程度,溶液呈酸性,故溶液中 ,
D错误;
故答案为:B。
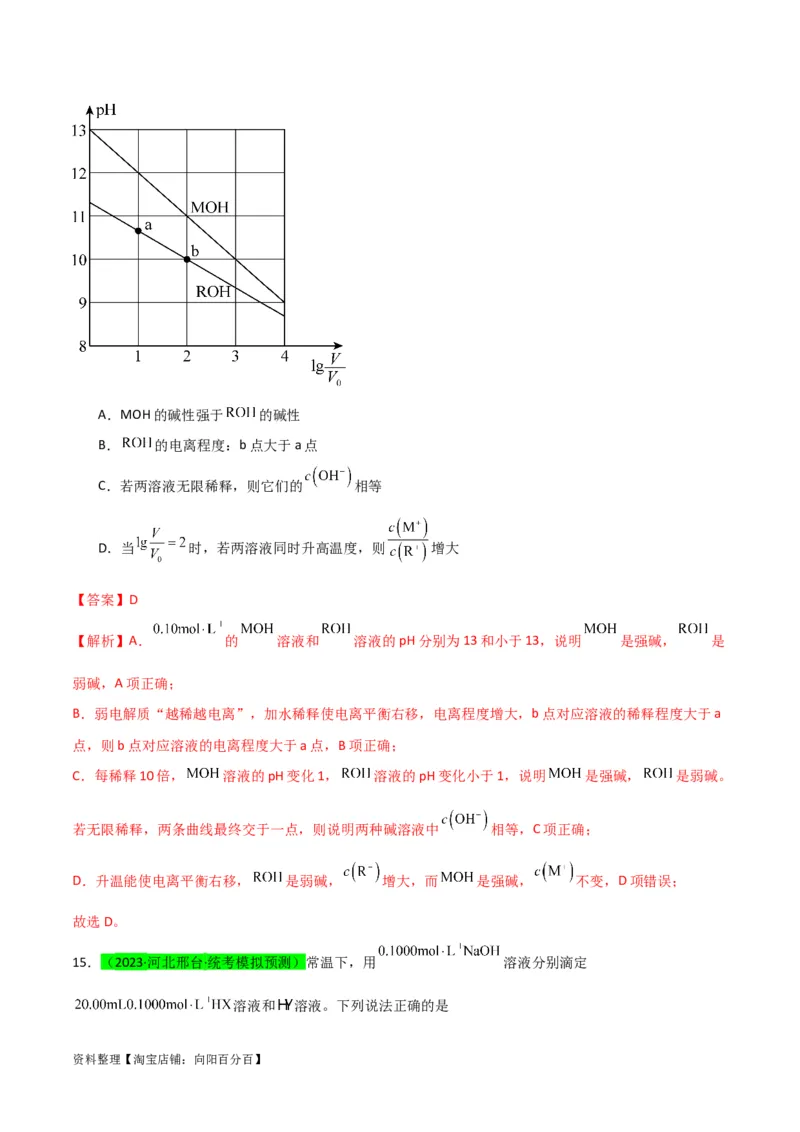
14.(2023·全国·高三专题练习)浓度均为 、体积均为 的 和 溶液,分别加水稀释
至体积 , 随 的变化如图所示。下列叙述错误的是
资料整理【淘宝店铺:向阳百分百】A.MOH的碱性强于 的碱性
B. 的电离程度:b点大于a点
C.若两溶液无限稀释,则它们的 相等
D.当 时,若两溶液同时升高温度,则 增大
【答案】D
【解析】A. 的 溶液和 溶液的pH分别为13和小于13,说明 是强碱, 是
弱碱,A项正确;
B.弱电解质“越稀越电离”,加水稀释使电离平衡右移,电离程度增大,b点对应溶液的稀释程度大于a
点,则b点对应溶液的电离程度大于a点,B项正确;
C.每稀释10倍, 溶液的pH变化1, 溶液的pH变化小于1,说明 是强碱, 是弱碱。
若无限稀释,两条曲线最终交于一点,则说明两种碱溶液中 相等,C项正确;
D.升温能使电离平衡右移, 是弱碱, 增大,而 是强碱, 不变,D项错误;
故选D。
15.(2023·河北邢台·统考模拟预测)常温下,用 溶液分别滴定
溶液和 溶液。下列说法正确的是
资料整理【淘宝店铺:向阳百分百】A.
B.①点溶液中存在
C.③点溶液中存在
D.①点和④点溶液中的 相等
【答案】B
【解析】A.根据等浓度的酸溶液的 可知 ,A项错误;
B.根据加入 溶液的体积可知①点溶液中溶质为 和 ,且物质的量相等,此时溶液呈碱性说明
的水解程度大于 的电离程度,则此时溶液中存在 ,B项正
确;
C.③点溶液中溶质为 和 ,则 ,C项错误;
D.①点溶液比④点溶液的 小,溶液中 ,则 ,则④点溶
液中 大,D项错误;
故选B。
资料整理【淘宝店铺:向阳百分百】