文档内容
选择题标准练(二)
1.(2024·甘肃二模)物质的性质决定物质的用途。下列叙述中两者对应关系不正确的是( )
A.SO 有还原性,可用作食品抗氧化剂
2
B.ClO 有还原性,可用于自来水消毒
2
C.Al O 熔点高,可用于制作耐火材料
2 3
D.Na O 能与CO 反应生成O,可作潜水艇中的供氧剂
2 2 2 2
2.设N 为阿伏加德罗常数的值。下列叙述中正确的是( )
A
A.28 g C H 的烃分子中含有C—C σ键的数目一定为1.6N
5 10 A
B.在标准状况下,22.4 L由SO 和SO 组成的混合物中含有硫原子的数目为N
2 3 A
C.2.00 L 0.5 mol·L-1的稀硫酸和足量金属钠反应,消耗钠原子的数目为2N
A
D.在2CuH+2HCl Cu+CuCl +2H ↑反应中,每生成4.48 L(标准状况)H ,反应转移的电子数目为
2 2 2
0.3N
A
3.(2024·江苏泰州一模调研)在指定条件下,下列选项所示的物质间转化能实现的是( )
A.Na CO(aq) CO NaHCO (aq)
2 3 2 3
B.FeS SO SO
2 2 3
C.NH NO HNO
3 3
D.Cu Cu(NO )(aq) Cu(NO )(s)
3 2 3 2
4.(2024·陕西渭南质检)文化自信是一个国家、一个民族发展中更基本、更深沉、更持久的力量。下
列文化内容中蕴含的化学知识描述不正确的是( )
选项 文化类别 文化内容 化学知识
A 饮食文化 渭南早餐文化的时辰包子 面团发酵过程中常用到小苏打
使用84消毒液对室内环境消毒,建议用凉水
B 劳动文化 84消毒液见光或受热易变质
稀释、早晚进行消杀
在厚重的历史文化氛围的滋养下,唐装汉服
鉴别纯棉、真丝可以用灼烧的
C 服饰文化 轻舞,传统文化与时尚潮流在大唐不夜城深
方法
度碰撞,“变装穿越”火出圈
烟花利用了“焰色试验”原理,
D 节日文化 蒲城杆火技艺被称为中华一绝
该原理属于化学变化
5.(2024·浙江6月选考)下列化学用语不正确的是 ( )
·· ·· ··
A.CO 的电子式为 · O · C · O ·
2 · · · ·
·· ·· ··B.Cl 中共价键的电子云轮廓图为
2
C.NH 的空间填充模型为
3
D.3,3-二甲基戊烷的键线式为
6.(2024·甘肃张掖第三次诊断)某抗失眠药物的结构简式如图所示。下列有关该化合物的说法错误的
是 ( )
A.该分子的分子式为C H ONBr
17 14 2 2 2
B.该化合物中碳原子的杂化轨道类型有两种
C.1 mol该化合物与氢氧化钠溶液反应最多消耗3 mol NaOH
D.该物质一个分子含有1个手性碳原子
7.(2024·甘肃张掖第三次诊断)宏观辨识与微观探析是化学学科核心素养之一。常温下,下列各组粒
子在指定溶液中能大量共存的是( )
A.0.1 mol·L-1碳酸钠溶液(pH=11)中:[Al(OH) ]-、Cl-、CN-
4
B.加入苯酚显紫色的溶液中能大量共存的离子:K+、NH+
、CHCOO-、S2-
4 3
C.0.1 mol·L-1酸性KMnO
溶液中:CO2- 、Fe2+、SO2-
、Br-
4 2 4 4
K
D.常温下
W
=10-13
mol·L-1的溶液中:Cl-、Fe2+、NO- 、NH+
c(H+) 3 4
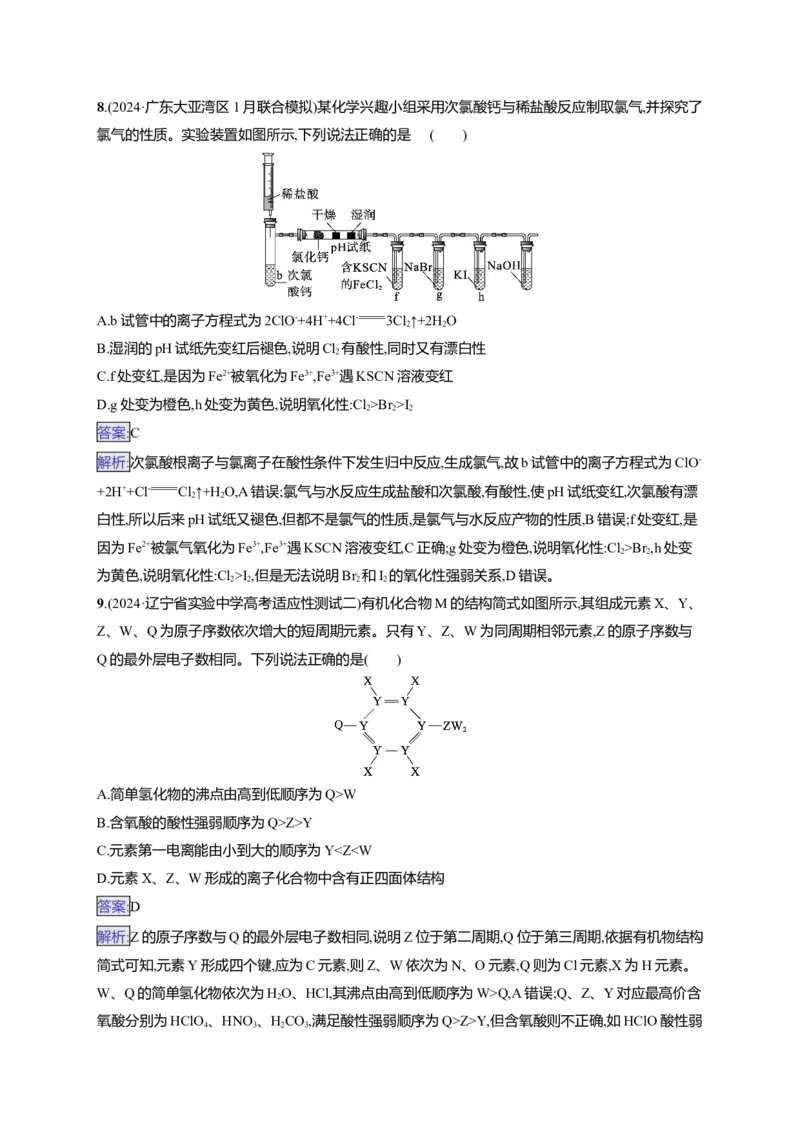
8.(2024·广东大亚湾区1月联合模拟)某化学兴趣小组采用次氯酸钙与稀盐酸反应制取氯气,并探究了
氯气的性质。实验装置如图所示,下列说法正确的是 ( )
A.b试管中的离子方程式为2ClO-+4H++4Cl- 3Cl↑+2H O
2 2
B.湿润的pH试纸先变红后褪色,说明Cl 有酸性,同时又有漂白性
2
C.f处变红,是因为Fe2+被氧化为Fe3+,Fe3+遇KSCN溶液变红
D.g处变为橙色,h处变为黄色,说明氧化性:Cl >Br >I
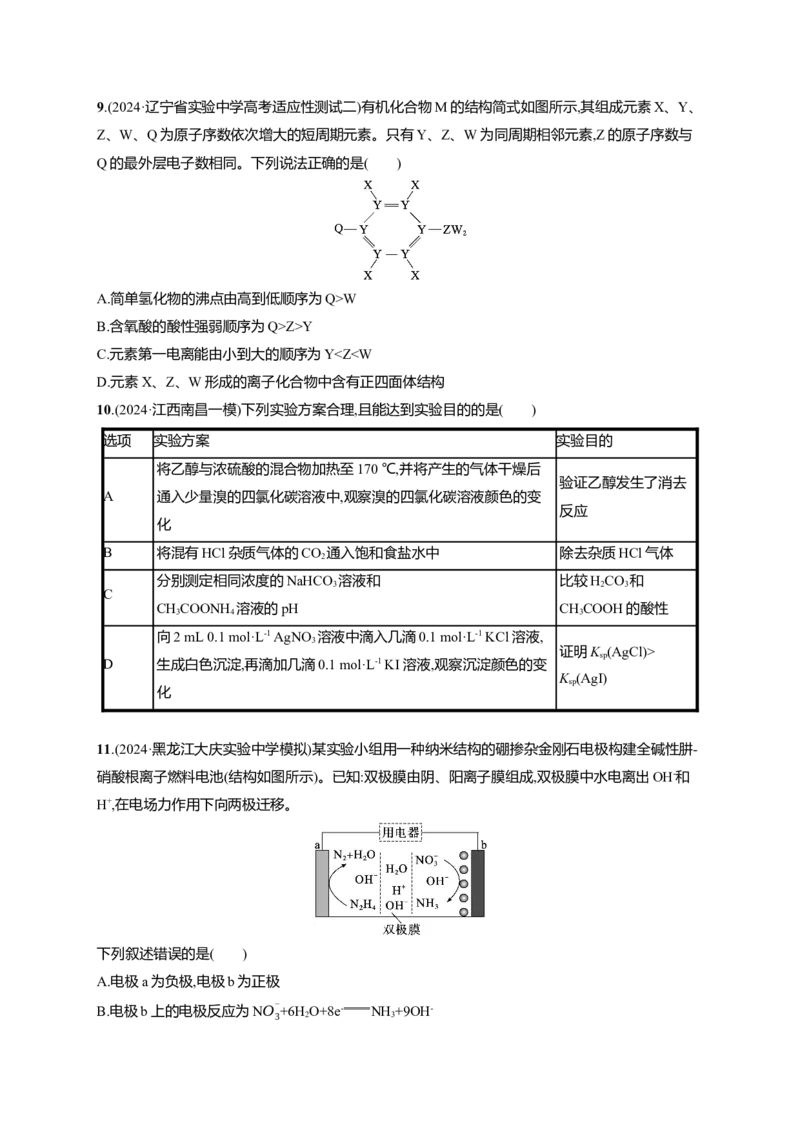
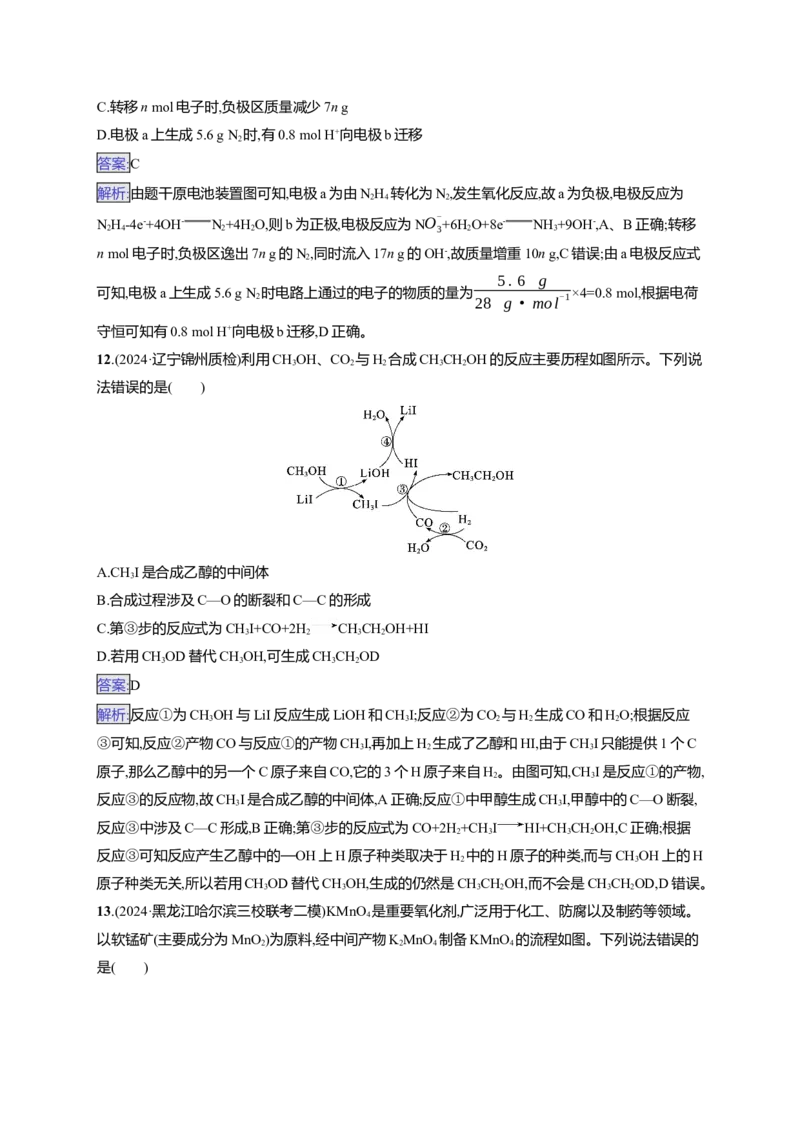
2 2 29.(2024·辽宁省实验中学高考适应性测试二)有机化合物M的结构简式如图所示,其组成元素X、Y、
Z、W、Q为原子序数依次增大的短周期元素。只有Y、Z、W为同周期相邻元素,Z的原子序数与
Q的最外层电子数相同。下列说法正确的是( )
A.简单氢化物的沸点由高到低顺序为Q>W
B.含氧酸的酸性强弱顺序为Q>Z>Y
C.元素第一电离能由小到大的顺序为Y
sp
D 生成白色沉淀,再滴加几滴0.1 mol·L-1 KI溶液,观察沉淀颜色的变
K (AgI)
sp
化
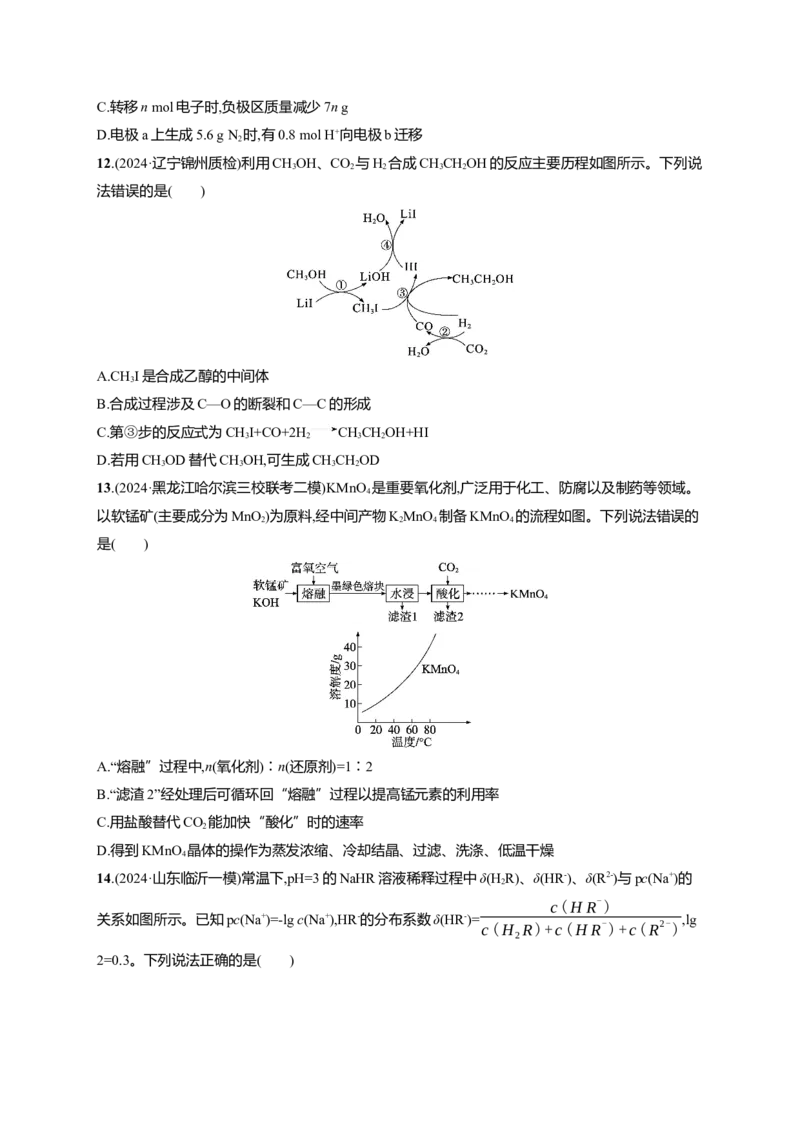
11.(2024·黑龙江大庆实验中学模拟)某实验小组用一种纳米结构的硼掺杂金刚石电极构建全碱性肼-
硝酸根离子燃料电池(结构如图所示)。已知:双极膜由阴、阳离子膜组成,双极膜中水电离出OH-和
H+,在电场力作用下向两极迁移。
下列叙述错误的是( )
A.电极a为负极,电极b为正极
B.电极b上的电极反应为NO-
+6H O+8e- NH +9OH-
3 2 3C.转移n mol电子时,负极区质量减少7n g
D.电极a上生成5.6 g N 时,有0.8 mol H+向电极b迁移
2
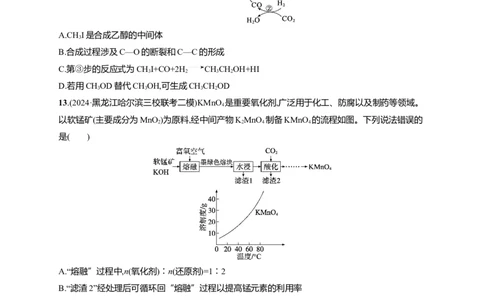
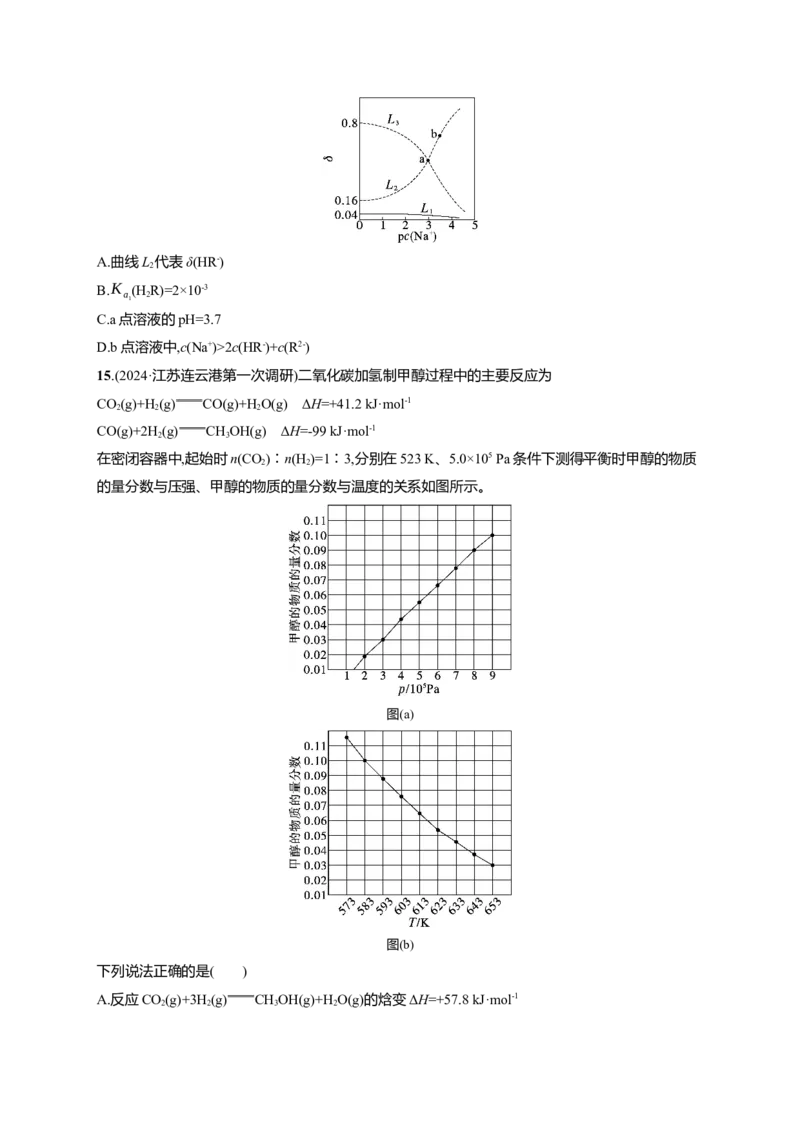
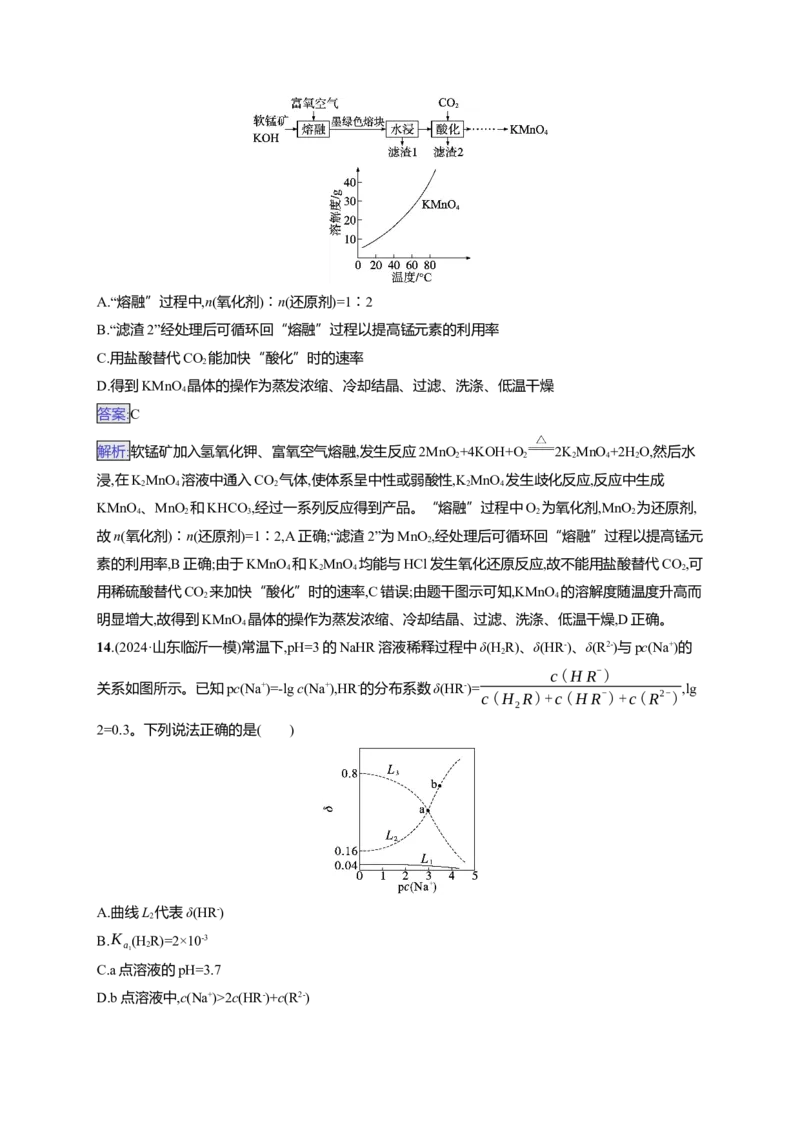
12.(2024·辽宁锦州质检)利用CHOH、CO 与H 合成CHCHOH的反应主要历程如图所示。下列说
3 2 2 3 2
法错误的是( )
A.CHI是合成乙醇的中间体
3
B.合成过程涉及C—O的断裂和C—C的形成
C.第③步的反应式为CHI+CO+2H CHCHOH+HI
3 2 3 2
D.若用CHOD替代CHOH,可生成CHCHOD
3 3 3 2
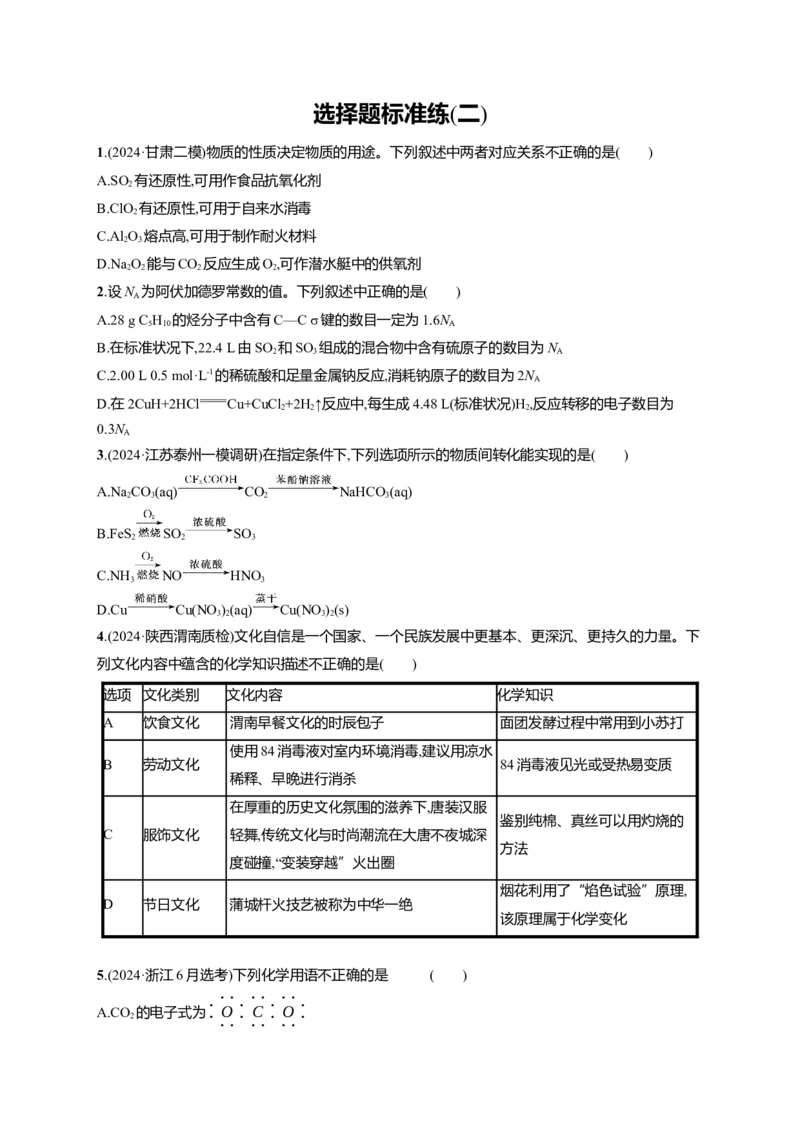
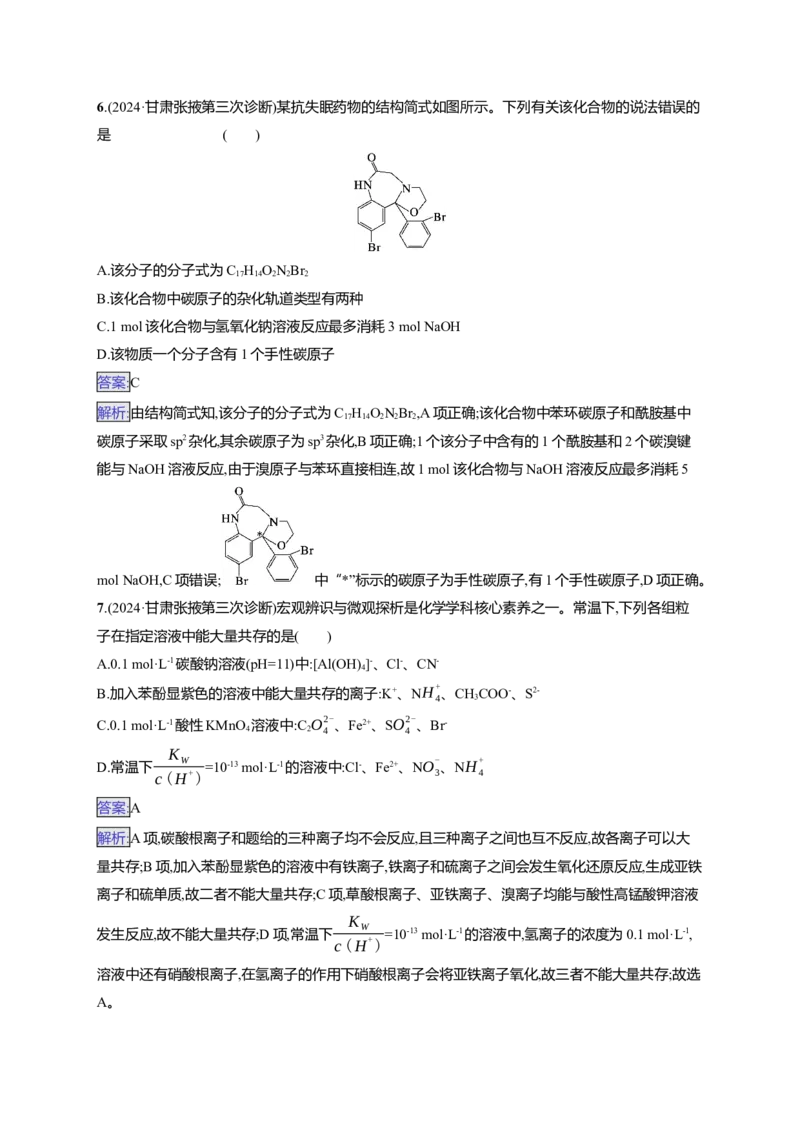
13.(2024·黑龙江哈尔滨三校联考二模)KMnO 是重要氧化剂,广泛用于化工、防腐以及制药等领域。
4
以软锰矿(主要成分为MnO )为原料,经中间产物KMnO 制备KMnO 的流程如图。下列说法错误的
2 2 4 4
是( )
A.“熔融”过程中,n(氧化剂)∶n(还原剂)=1∶2
B.“滤渣2”经处理后可循环回“熔融”过程以提高锰元素的利用率
C.用盐酸替代CO 能加快“酸化”时的速率
2
D.得到KMnO 晶体的操作为蒸发浓缩、冷却结晶、过滤、洗涤、低温干燥
4
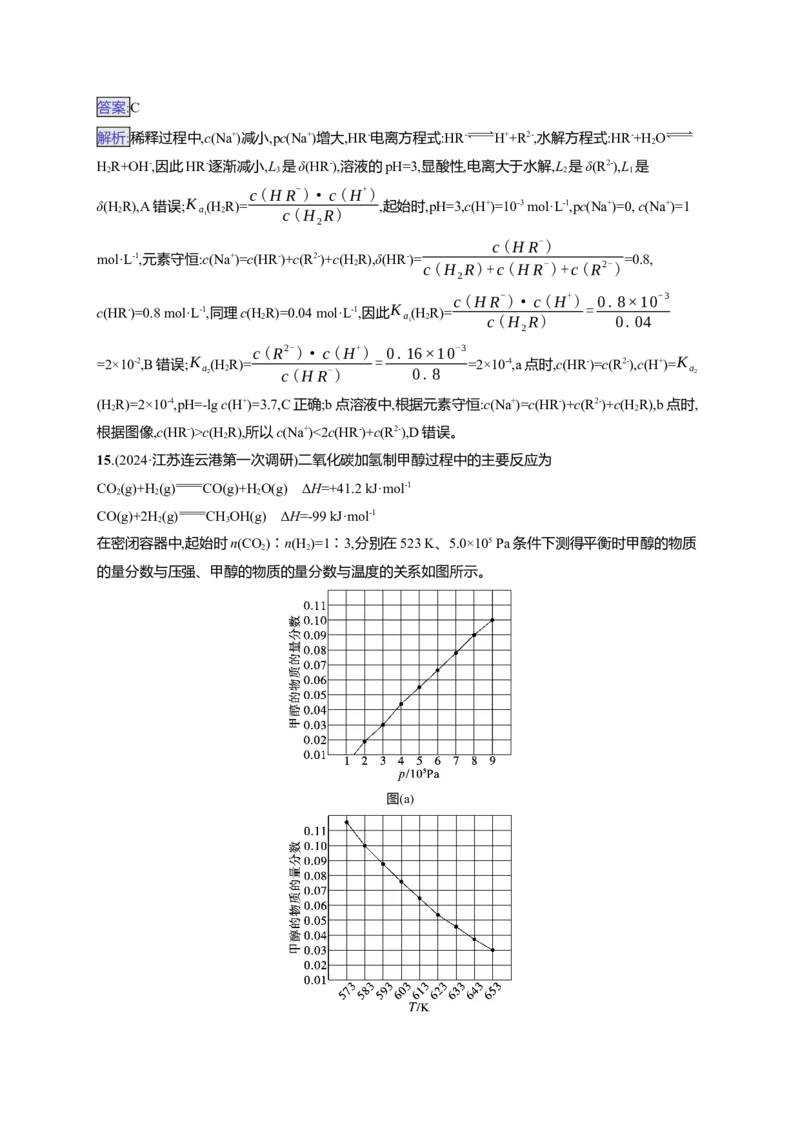
14.(2024·山东临沂一模)常温下,pH=3的NaHR溶液稀释过程中δ(H R)、δ(HR-)、δ(R2-)与pc(Na+)的
2
c(H R-)
关系如图所示。已知pc(Na+)=-lg c(Na+),HR-的分布系数δ(HR-)= ,lg
c(H R)+c(H R-)+c(R2-)
2
2=0.3。下列说法正确的是( )A.曲线L 代表δ(HR-)
2
B.K (H R)=2×10-3
a 2
1
C.a点溶液的pH=3.7
D.b点溶液中,c(Na+)>2c(HR-)+c(R2-)
15.(2024·江苏连云港第一次调研)二氧化碳加氢制甲醇过程中的主要反应为
CO(g)+H(g) CO(g)+HO(g) ΔH=+41.2 kJ·mol-1
2 2 2
CO(g)+2H(g) CHOH(g) ΔH=-99 kJ·mol-1
2 3
在密闭容器中,起始时n(CO)∶n(H )=1∶3,分别在523 K、5.0×105 Pa条件下测得平衡时甲醇的物质
2 2
的量分数与压强、甲醇的物质的量分数与温度的关系如图所示。
图(a)
图(b)
下列说法正确的是( )
A.反应CO(g)+3H(g) CHOH(g)+H O(g)的焓变ΔH=+57.8 kJ·mol-1
2 2 3 2B.在583 K、9×105 Pa条件下,平衡时甲醇的物质的量分数为0.10
C.当甲醇的物质的量分数为0.03时,CO 的平衡转化率为11.3%
2
D.其他条件相同,高压和低温可以提高CHOH的平衡产率
3
选择题标准练(二)
1.(2024·甘肃二模)物质的性质决定物质的用途。下列叙述中两者对应关系不正确的是( )
A.SO 有还原性,可用作食品抗氧化剂
2
B.ClO 有还原性,可用于自来水消毒
2
C.Al O 熔点高,可用于制作耐火材料
2 3
D.Na O 能与CO 反应生成O,可作潜水艇中的供氧剂
2 2 2 2
答案:B
解析:SO 具有还原性,可用作食品抗氧化剂,防止食品被氧化,A正确;ClO 有氧化性,可用于自来水消
2 2
毒,B错误;氧化铝熔点高,因此可用于制作耐火材料,C正确;Na O 能与CO 反应生成O,可作供氧
2 2 2 2
剂,D正确。
2.设N 为阿伏加德罗常数的值。下列叙述中正确的是( )
A
A.28 g C H 的烃分子中含有C—C σ键的数目一定为1.6N
5 10 A
B.在标准状况下,22.4 L由SO 和SO 组成的混合物中含有硫原子的数目为N
2 3 A
C.2.00 L 0.5 mol·L-1的稀硫酸和足量金属钠反应,消耗钠原子的数目为2N
A
D.在2CuH+2HCl Cu+CuCl +2H ↑反应中,每生成4.48 L(标准状况)H ,反应转移的电子数目为
2 2 2
0.3N
A
答案:D
解析:C H 可能为环烷烃,可能为烯烃,若为环烷烃时,28 g C H 的烃分子中含有C—C σ键的数目为
5 10 5 10
2.0N ,A错误;在标准状况下,SO 不是气体,无法计算,B错误;钠除了能与酸反应以外,还能与水反应,由
A 3
于钠是足量的,无法计算消耗的钠的原子数,C错误;2CuH+2HCl Cu+CuCl +2H ↑中,铜的化合价由
2 2
+1降到0和升高到+2,H的化合价由-1和+1升高和降低到0,故每生成4.48 L(标准状况)H (0.2 mol),
2
反应转移的电子数目为0.3N ,D正确。
A
3.(2024·江苏泰州一模调研)在指定条件下,下列选项所示的物质间转化能实现的是( )
A.Na CO(aq) CO NaHCO (aq)
2 3 2 3
B.FeS SO SO
2 2 3
C.NH NO HNO
3 3D.Cu Cu(NO )(aq) Cu(NO )(s)
3 2 3 2
答案:A
解析:碳酸钠与CFCOOH反应生成CFCOONa、CO 和HO,CO、HO和苯酚钠反应生成苯酚和碳
3 3 2 2 2 2
酸氢钠;FeS 与O 反应生成氧化铁和二氧化硫,二氧化硫和硫酸不反应;氨气催化氧化生成NO,NO和
2 2
浓硫酸不能反应生成硝酸;由于硝酸是易挥发性酸,铜离子发生水解,因此硝酸铜溶液蒸干得不到硝酸
铜。
4.(2024·陕西渭南质检)文化自信是一个国家、一个民族发展中更基本、更深沉、更持久的力量。下
列文化内容中蕴含的化学知识描述不正确的是( )
选项 文化类别 文化内容 化学知识
A 饮食文化 渭南早餐文化的时辰包子 面团发酵过程中常用到小苏打
使用84消毒液对室内环境消毒,建议用凉水
B 劳动文化 84消毒液见光或受热易变质
稀释、早晚进行消杀
在厚重的历史文化氛围的滋养下,唐装汉服
鉴别纯棉、真丝可以用灼烧的
C 服饰文化 轻舞,传统文化与时尚潮流在大唐不夜城深
方法
度碰撞,“变装穿越”火出圈
烟花利用了“焰色试验”原理,
D 节日文化 蒲城杆火技艺被称为中华一绝
该原理属于化学变化
答案:D
解析:小苏打是碳酸氢钠,面团发酵利用碳酸氢钠受热易分解产生二氧化碳而使得面团疏松多孔,A正
确;84消毒液中有效成分为次氯酸钠,杀菌消毒的原理是二氧化碳、水将次氯酸钠转化为次氯酸,次氯
酸见光或受热易分解,因此使用84消毒液对室内环境消毒,建议用凉水稀释、早晚进行消杀,B正确;
棉花的主要成分是纤维素、真丝的主要成分是蛋白质,灼烧真丝有烧焦羽毛气味而纯棉没有,可以用
灼烧的方法鉴别真丝和纯棉,C正确;“焰色试验”是物理变化,D错误。
5.(2024·浙江6月选考)下列化学用语不正确的是 ( )
·· ·· ··
A.CO 的电子式为 · O · C · O ·
2 · · · ·
·· ·· ··
B.Cl 中共价键的电子云轮廓图为
2
C.NH 的空间填充模型为
3
D.3,3-二甲基戊烷的键线式为
答案:A
·· ··
解析:CO 2 的电子式为O · · · ·C · · · · O (或· · O · ··C·· · O · ·),A项错误;B、C、D项正确。
· ·· ·· ·
·· ··6.(2024·甘肃张掖第三次诊断)某抗失眠药物的结构简式如图所示。下列有关该化合物的说法错误的
是 ( )
A.该分子的分子式为C H ONBr
17 14 2 2 2
B.该化合物中碳原子的杂化轨道类型有两种
C.1 mol该化合物与氢氧化钠溶液反应最多消耗3 mol NaOH
D.该物质一个分子含有1个手性碳原子
答案:C
解析:由结构简式知,该分子的分子式为C H ONBr ,A项正确;该化合物中苯环碳原子和酰胺基中
17 14 2 2 2
碳原子采取sp2杂化,其余碳原子为sp3杂化,B项正确;1个该分子中含有的1个酰胺基和2个碳溴键
能与NaOH溶液反应,由于溴原子与苯环直接相连,故1 mol该化合物与NaOH溶液反应最多消耗5
mol NaOH,C项错误; 中“*”标示的碳原子为手性碳原子,有1个手性碳原子,D项正确。
7.(2024·甘肃张掖第三次诊断)宏观辨识与微观探析是化学学科核心素养之一。常温下,下列各组粒
子在指定溶液中能大量共存的是( )
A.0.1 mol·L-1碳酸钠溶液(pH=11)中:[Al(OH) ]-、Cl-、CN-
4
B.加入苯酚显紫色的溶液中能大量共存的离子:K+、NH+
、CHCOO-、S2-
4 3
C.0.1 mol·L-1酸性KMnO
溶液中:CO2- 、Fe2+、SO2-
、Br-
4 2 4 4
K
D.常温下
W
=10-13
mol·L-1的溶液中:Cl-、Fe2+、NO- 、NH+
c(H+) 3 4
答案:A
解析:A项,碳酸根离子和题给的三种离子均不会反应,且三种离子之间也互不反应,故各离子可以大
量共存;B项,加入苯酚显紫色的溶液中有铁离子,铁离子和硫离子之间会发生氧化还原反应,生成亚铁
离子和硫单质,故二者不能大量共存;C项,草酸根离子、亚铁离子、溴离子均能与酸性高锰酸钾溶液
K
W
发生反应,故不能大量共存;D项,常温下 =10-13 mol·L-1的溶液中,氢离子的浓度为0.1 mol·L-1,
c(H+)
溶液中还有硝酸根离子,在氢离子的作用下硝酸根离子会将亚铁离子氧化,故三者不能大量共存;故选
A。8.(2024·广东大亚湾区1月联合模拟)某化学兴趣小组采用次氯酸钙与稀盐酸反应制取氯气,并探究了
氯气的性质。实验装置如图所示,下列说法正确的是 ( )
A.b试管中的离子方程式为2ClO-+4H++4Cl- 3Cl↑+2H O
2 2
B.湿润的pH试纸先变红后褪色,说明Cl 有酸性,同时又有漂白性
2
C.f处变红,是因为Fe2+被氧化为Fe3+,Fe3+遇KSCN溶液变红
D.g处变为橙色,h处变为黄色,说明氧化性:Cl >Br >I
2 2 2
答案:C
解析:次氯酸根离子与氯离子在酸性条件下发生归中反应,生成氯气,故b试管中的离子方程式为ClO-
+2H++Cl- Cl↑+H O,A错误;氯气与水反应生成盐酸和次氯酸,有酸性,使pH试纸变红,次氯酸有漂
2 2
白性,所以后来pH试纸又褪色,但都不是氯气的性质,是氯气与水反应产物的性质,B错误;f处变红,是
因为Fe2+被氯气氧化为Fe3+,Fe3+遇KSCN溶液变红,C正确;g处变为橙色,说明氧化性:Cl >Br ,h处变
2 2
为黄色,说明氧化性:Cl >I ,但是无法说明Br 和I 的氧化性强弱关系,D错误。
2 2 2 2
9.(2024·辽宁省实验中学高考适应性测试二)有机化合物M的结构简式如图所示,其组成元素X、Y、
Z、W、Q为原子序数依次增大的短周期元素。只有Y、Z、W为同周期相邻元素,Z的原子序数与
Q的最外层电子数相同。下列说法正确的是( )
A.简单氢化物的沸点由高到低顺序为Q>W
B.含氧酸的酸性强弱顺序为Q>Z>Y
C.元素第一电离能由小到大的顺序为YQ,A错误;Q、Z、Y对应最高价含
2
氧酸分别为HClO、HNO、HCO,满足酸性强弱顺序为Q>Z>Y,但含氧酸则不正确,如HClO酸性弱
4 3 2 3于HCO,B错误;N原子2p轨道半充满,较为稳定,元素第一电离能在C、N、O中最大,即顺序应为
2 3
Y
sp
D 生成白色沉淀,再滴加几滴0.1 mol·L-1 KI溶液,观察沉淀颜色的变
K (AgI)
sp
化
答案:A
解析:将乙醇与浓硫酸的混合物加热至170 ℃,产生乙烯,将乙烯干燥后通入少量溴的四氯化碳溶液中,
乙烯与溴发生加成反应,溴的四氯化碳溶液颜色变浅或褪色,A正确;将混有HCl杂质气体的CO 通入
2
饱和食盐水中,CO 也会溶解消耗,应当通入饱和NaHCO 溶液中,B错误;CH COONH 中铵根离子也
2 3 3 4
会水解,影响溶液的酸碱性,而NaHCO 中钠离子不水解,故无法比较HCO 和CHCOOH的酸性,C错
3 2 3 3
误;向2 mL 0.1 mol·L-1 AgNO 溶液中滴入几滴0.1 mol·L-1 KCl溶液,生成白色沉淀,再滴加几滴0.1
3
mol·L-1 KI溶液,会出现黄色沉淀,但是由于银离子过量,可能是过量的银离子直接和碘离子反应生成
碘化银黄色沉淀,无法证明K (AgCl)>K (AgI),D错误。
sp sp
11.(2024·黑龙江大庆实验中学模拟)某实验小组用一种纳米结构的硼掺杂金刚石电极构建全碱性肼-
硝酸根离子燃料电池(结构如图所示)。已知:双极膜由阴、阳离子膜组成,双极膜中水电离出OH-和
H+,在电场力作用下向两极迁移。
下列叙述错误的是( )
A.电极a为负极,电极b为正极
B.电极b上的电极反应为NO-
+6H O+8e- NH +9OH-
3 2 3C.转移n mol电子时,负极区质量减少7n g
D.电极a上生成5.6 g N 时,有0.8 mol H+向电极b迁移
2
答案:C
解析:由题干原电池装置图可知,电极a为由NH 转化为N,发生氧化反应,故a为负极,电极反应为
2 4 2
NH-4e-+4OH- N+4H
O,则b为正极,电极反应为NO-
+6H O+8e- NH +9OH-,A、B正确;转移
2 4 2 2 3 2 3
n mol电子时,负极区逸出7n g的N,同时流入17n g的OH-,故质量增重10n g,C错误;由a电极反应式
2
5.6 g
可知,电极a上生成5.6 g N 时电路上通过的电子的物质的量为 ×4=0.8 mol,根据电荷
2 28 g·mol-1
守恒可知有0.8 mol H+向电极b迁移,D正确。
12.(2024·辽宁锦州质检)利用CHOH、CO 与H 合成CHCHOH的反应主要历程如图所示。下列说
3 2 2 3 2
法错误的是( )
A.CHI是合成乙醇的中间体
3
B.合成过程涉及C—O的断裂和C—C的形成
C.第③步的反应式为CHI+CO+2H CHCHOH+HI
3 2 3 2
D.若用CHOD替代CHOH,可生成CHCHOD
3 3 3 2
答案:D
解析:反应①为CHOH与LiI反应生成LiOH和CHI;反应②为CO 与H 生成CO和HO;根据反应
3 3 2 2 2
③可知,反应②产物CO与反应①的产物CHI,再加上H 生成了乙醇和HI,由于CHI只能提供1个C
3 2 3
原子,那么乙醇中的另一个C原子来自CO,它的3个H原子来自H。由图可知,CH I是反应①的产物,
2 3
反应③的反应物,故CHI是合成乙醇的中间体,A正确;反应①中甲醇生成CHI,甲醇中的C—O断裂,
3 3
反应③中涉及C—C形成,B正确;第③步的反应式为CO+2H+CH I HI+CHCHOH,C正确;根据
2 3 3 2
反应③可知反应产生乙醇中的—OH上H原子种类取决于H 中的H原子的种类,而与CHOH上的H
2 3
原子种类无关,所以若用CHOD替代CHOH,生成的仍然是CHCHOH,而不会是CHCHOD,D错误。
3 3 3 2 3 2
13.(2024·黑龙江哈尔滨三校联考二模)KMnO 是重要氧化剂,广泛用于化工、防腐以及制药等领域。
4
以软锰矿(主要成分为MnO )为原料,经中间产物KMnO 制备KMnO 的流程如图。下列说法错误的
2 2 4 4
是( )A.“熔融”过程中,n(氧化剂)∶n(还原剂)=1∶2
B.“滤渣2”经处理后可循环回“熔融”过程以提高锰元素的利用率
C.用盐酸替代CO 能加快“酸化”时的速率
2
D.得到KMnO 晶体的操作为蒸发浓缩、冷却结晶、过滤、洗涤、低温干燥
4
答案:C
解析:软锰矿加入氢氧化钾、富氧空气熔融,发生反应2MnO +4KOH+O 2KMnO +2H O,然后水
2 2 2 4 2
浸,在KMnO 溶液中通入CO 气体,使体系呈中性或弱酸性,K MnO 发生歧化反应,反应中生成
2 4 2 2 4
KMnO 、MnO 和KHCO ,经过一系列反应得到产品。“熔融”过程中O 为氧化剂,MnO 为还原剂,
4 2 3 2 2
故n(氧化剂)∶n(还原剂)=1∶2,A正确;“滤渣2”为MnO ,经处理后可循环回“熔融”过程以提高锰元
2
素的利用率,B正确;由于KMnO 和KMnO 均能与HCl发生氧化还原反应,故不能用盐酸替代CO,可
4 2 4 2
用稀硫酸替代CO 来加快“酸化”时的速率,C错误;由题干图示可知,KMnO 的溶解度随温度升高而
2 4
明显增大,故得到KMnO 晶体的操作为蒸发浓缩、冷却结晶、过滤、洗涤、低温干燥,D正确。
4
14.(2024·山东临沂一模)常温下,pH=3的NaHR溶液稀释过程中δ(H R)、δ(HR-)、δ(R2-)与pc(Na+)的
2
c(H R-)
关系如图所示。已知pc(Na+)=-lg c(Na+),HR-的分布系数δ(HR-)= ,lg
c(H R)+c(H R-)+c(R2-)
2
2=0.3。下列说法正确的是( )
A.曲线L 代表δ(HR-)
2
B.K (H R)=2×10-3
a 2
1
C.a点溶液的pH=3.7
D.b点溶液中,c(Na+)>2c(HR-)+c(R2-)答案:C
解析:稀释过程中,c(Na+)减小,pc(Na+)增大,HR-电离方程式:HR- H++R2-,水解方程式:HR-+H O
2
HR+OH-,因此HR-逐渐减小,L 是δ(HR-),溶液的pH=3,显酸性,电离大于水解,L 是δ(R2-),L 是
2 3 2 1
c(H R-)·c(H+)
δ(H R),A错误;K (H R)= ,起始时,pH=3,c(H+)=10-3 mol·L-1,pc(Na+)=0, c(Na+)=1
2 a 1 2 c(H R)
2
c(H R-)
mol·L-1,元素守恒:c(Na+)=c(HR-)+c(R2-)+c(H R),δ(HR-)= =0.8,
2 c(H R)+c(H R-)+c(R2-)
2
c(H R-)·c(H+) 0.8×10-3
c(HR-)=0.8 mol·L-1,同理c(H R)=0.04 mol·L-1,因此 K (H R)= =
2 a 1 2 c(H R) 0.04
2
c(R2-)·c(H+) 0.16×10-3
=2×10-2,B错误;K (H R)= = =2×10-4,a点时,c(HR-)=c(R2-),c(H+)=K
a 2 2 c(H R-) 0.8 a 2
(H R)=2×10-4,pH=-lg c(H+)=3.7,C正确;b点溶液中,根据元素守恒:c(Na+)=c(HR-)+c(R2-)+c(H R),b点时,
2 2
根据图像,c(HR-)>c(H R),所以c(Na+)<2c(HR-)+c(R2-),D错误。
2
15.(2024·江苏连云港第一次调研)二氧化碳加氢制甲醇过程中的主要反应为
CO(g)+H(g) CO(g)+HO(g) ΔH=+41.2 kJ·mol-1
2 2 2
CO(g)+2H(g) CHOH(g) ΔH=-99 kJ·mol-1
2 3
在密闭容器中,起始时n(CO)∶n(H )=1∶3,分别在523 K、5.0×105 Pa条件下测得平衡时甲醇的物质
2 2
的量分数与压强、甲醇的物质的量分数与温度的关系如图所示。
图(a)图(b)
下列说法正确的是( )
A.反应CO(g)+3H(g) CHOH(g)+H O(g)的焓变ΔH=+57.8 kJ·mol-1
2 2 3 2
B.在583 K、9×105 Pa条件下,平衡时甲醇的物质的量分数为0.10
C.当甲醇的物质的量分数为0.03时,CO 的平衡转化率为11.3%
2
D.其他条件相同,高压和低温可以提高CHOH的平衡产率
3
答案:D
解析:根据盖斯定律,①CO(g)+H(g) CO(g)+HO(g) ΔH=+41.2 kJ·mol-1,②CO(g)+2H(g)
2 2 2 2
CHOH(g) ΔH=-99 kJ·mol-1,将反应①+②整理可得:CO (g)+3H(g) CHOH(g)+H O(g) ΔH=-57.8
3 2 2 3 2
kJ·mol-1,A错误;图(b)中为等压线,图(a)中为等温线,升高温度平衡逆向移动,在523 K、9×105 Pa条件
下平衡时甲醇的物质的量分数为0.10,那么在583 K、9×105 Pa条件下,平衡时甲醇的物质的量分数应
该小于0.10,B错误;没有给出指定的温度与压强,不能计算CO 的平衡转化率,C错误;根据A选项可
2
知CO(g)+3H(g) CHOH(g)+H O(g)为放热反应,要提高CHOH的产率,需要平衡正向移动,根据
2 2 3 2 3
平衡移动原理可知低温和高压可以提高CHOH的平衡产率,D正确。
3