文档内容
选择题标准练(五)
1.(2024·广东佛山质检一)杭州亚运会展示了我国科技力量。下列说法错误的是( )
A.会场使用的5G通信光纤的主要材料是Si
B.场馆能源来自风能和太阳能,二者都属于可再生能源
C.竞赛自行车车架采用碳纤维材料,它是一种无机非金属材料
D.体育场馆形状类似“莲花碗”,采用的钢材料韧性比生铁强
2.(2024·山东临沂一模)下列有关实验操作的描述正确的是( )
A.加热液体出现暴沸时,立即停止加热并加入沸石
B.配制NaSiO 溶液时,加入少量NaOH溶液
2 3
C.用热的氢氧化钠溶液清洗试管内壁残留的矿物油
D.滴定实验时,不能向锥形瓶中加入蒸馏水,以免溶液稀释产生误差
3.(2024·黑龙江大庆实验中学模拟)下列化学用语或图示表达正确的是( )
A.四水合铜离子[Cu(H O) ]2+的结构:
2 4
B.H—H形成的σ键:
C.基态碘原子简化电子排布式:[Kr]5s25p5
D.环氧乙烷的结构简式:
4.(2024·黑龙江齐齐哈尔一模)阿伏加德罗在化学上的主要贡献是提出了分子的概念,并创立了分子
学说。设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.1 mol硝基(—NO )与46 g NO 所含电子数均为23N
2 2 A
B.1 mol Na O 与足量的CO 反应转移的电子数为2N
2 2 2 A
C.标准状况下,22.4 L C H 含σ键数目一定为8N
3 6 A
D.10 L 0.1 mol·L-1 Na S溶液中,S2-和HS-的数目之和为N
2 A
5.(2024·江苏南通如皋市适应性考试二)反应Mn2++2HCO-
MnCO ↓+CO ↑+H O可用于制取
3 3 2 2
MnCO 。下列说法正确的是( )
3
A.基态Mn2+的电子排布式为[Ar]3d54s2
B.HCO- 中C的杂化方式为sp2杂化
3
C.CO2-
的空间结构为三角锥形
3
D.CO 是含非极性共价键的非极性分子
26.(2024·安徽合肥三模)下列各组离子在溶液中可以大量共存,且加入试剂后发生反应的离子方程式
书写也正确的是( )
选项 微粒组 加入试剂 发生反应的离子方程式
A K+、[Al(OH)
]-、SO2- 、CO2-
少量HCl溶液 [Al(OH) ]-+H+ Al(OH) ↓+H O
4 4 3 4 3 2
少量Ba(NO )
B H+、Fe2+、SO2- 、Na+ 3 2 3Fe2++4H++NO- 3Fe3++NO↑+2HO
4 3 2
溶液
C
Cl-、Na+、SiO2- 、HCO-
过量醋酸溶液
2H++SiO2-
HSiO↓
3 3 3 2 3
D
Fe3+、H+、MnO- 、SO2-
通入少量SO 2Fe3++SO+2H O
2Fe2++SO2-
+4H+
4 4 2 2 2 4
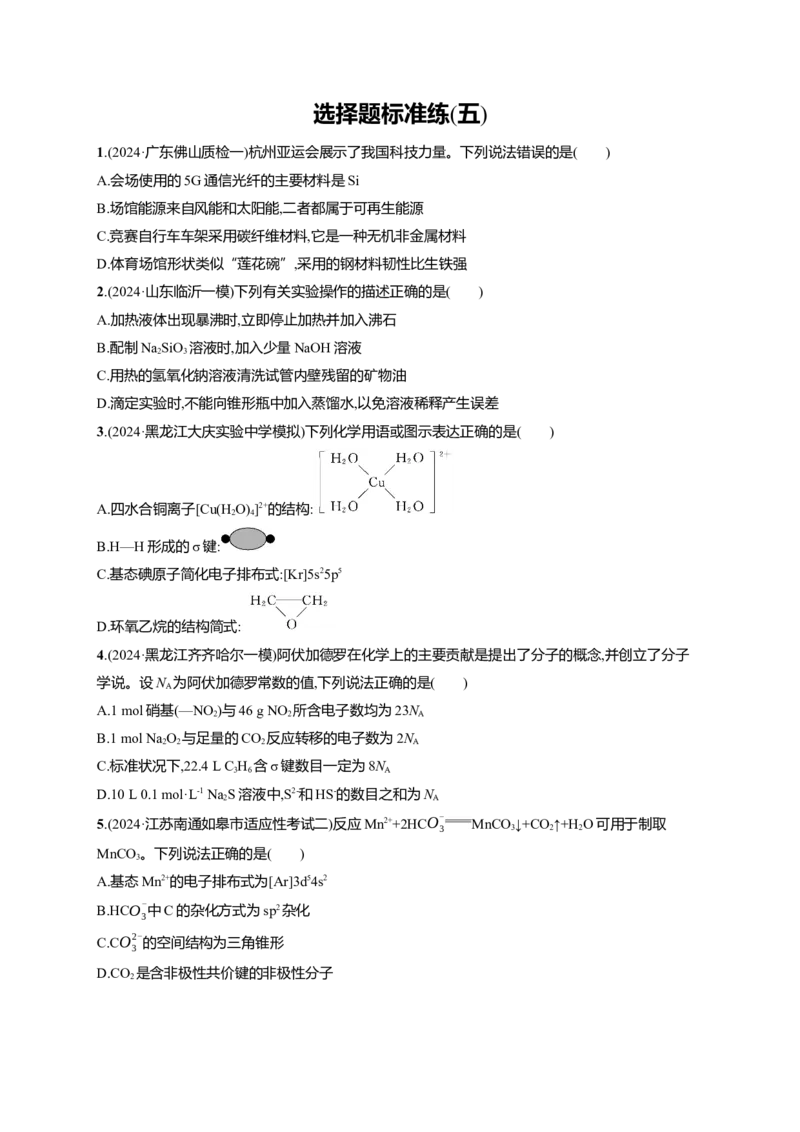
7.(2024·江西南昌一模)能用如图所示装置完成气体制备、尾气处理(加热和夹持等装置略去)的是(
)
选项 气体 制备试剂 烧杯中试剂
A. NH 碱石灰与浓氨水 HSO 溶液
3 2 4
B. CO 大理石和硫酸 石灰水
2
C. C H 电石与水 水
2 2
D. Cl MnO 与浓盐酸 NaOH溶液
2 2
8.(2024·安徽省第二次大联考)对下列事实的解释错误的是( )
选项 事实 解释
A 第一电离能:N>O N的2p轨道半充满,结构更稳定,能量更低
碳正离子稳定性:
B Br电负性比F小,电子云更偏向碳正离子
C 热稳定性:H O>HS HO分子间存在氢键,H S分子间不存在氢键
2 2 2 2
D C—H键长:CH >C H C的杂化轨道中s成分越多,形成的C—H化学键越强,键长越短
4 2 4
9.(2024·浙江丽水湖州衢州三地市4月质检)由不饱和烃A制备聚1,3-丁二烯的合成路线(部分反应条
件略去)如下4步反应所示:A D 聚1,3-丁二烯
下列说法不正确的是( )
A.第一步反应属于取代反应
B.A分子中的所有原子在同一直线上
C.聚1,3-丁二烯能使溴水褪色
D.B和C均属于醇类
10.(2024·广西柳州三模)Q、X、Y、Z为原子序数依次增大的短周期元素,X、Y、Z为同周期相邻元
素,且X、Y为金属元素,最外层电子数之和满足Q=X+Z,下列结论正确的是( )
A.原子半径:Q>X>Y>Z
B.四种元素中,电负性最大的是Z
C.Y的最高价氧化物对应水化物是强碱
D.Q和Z的最简单氢化物的沸点:Q>Z
11.(2024·甘肃张掖第三次诊断)根据实验操作、现象,能得出相应结论的是( )
选项 操作 现象 结论
将Fe(NO ) 样品溶于稀硫酸,滴加
3 2
A 观察到溶液变红 Fe(NO ) 样品已氧化变质
3 2
KSCN溶液
向盛有等体积、等浓度的HO 溶液的
2 2 加KMnO 溶液的试管 MnO- 比Cu2+的催化效果
4 4
B 两支试管中分别加入0.2 mL等浓度
中产生气泡速率更快 好
CuSO 溶液和KMnO 溶液
4 4
以KCrO 为指示剂,用AgNO 标准溶 先出现浅黄色沉淀,后
2 4 3
C K (AgBr)HCO-
2 3 3
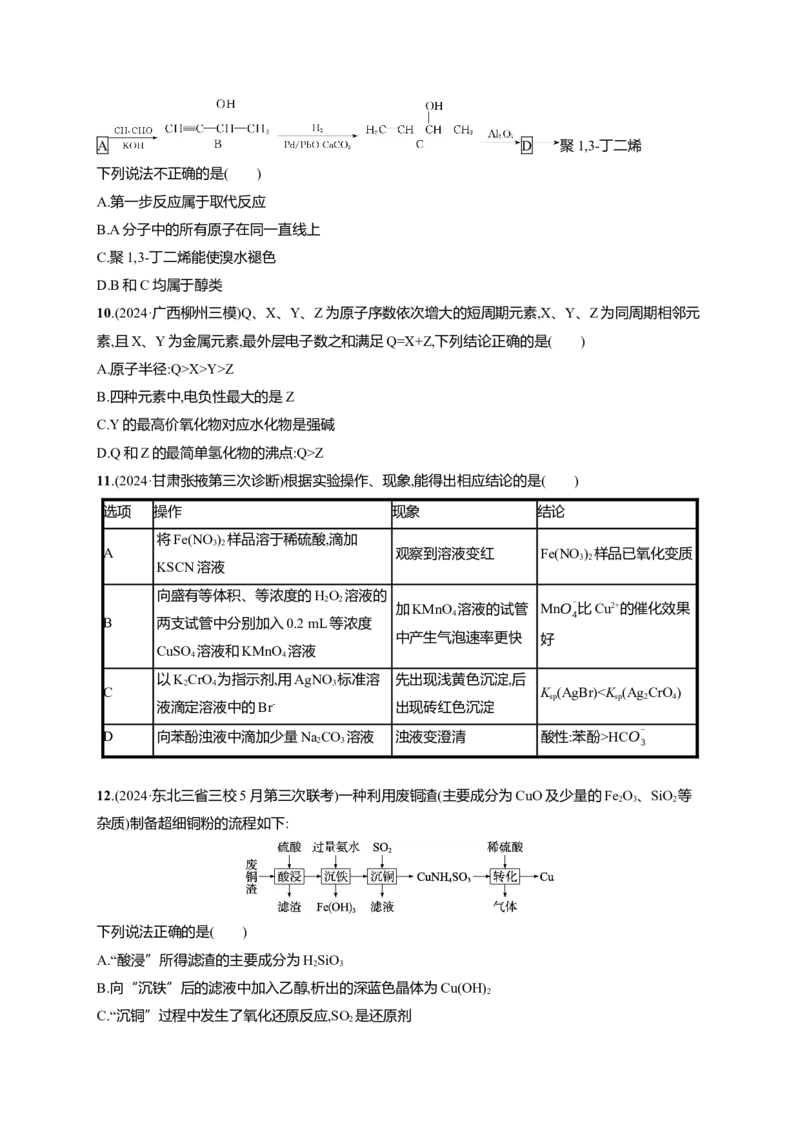
12.(2024·东北三省三校5月第三次联考)一种利用废铜渣(主要成分为CuO及少量的Fe O、SiO 等
2 3 2
杂质)制备超细铜粉的流程如下:
下列说法正确的是( )
A.“酸浸”所得滤渣的主要成分为HSiO
2 3
B.向“沉铁”后的滤液中加入乙醇,析出的深蓝色晶体为Cu(OH)
2
C.“沉铜”过程中发生了氧化还原反应,SO 是还原剂
2D.“转化”后的滤液中含有的阳离子为NH+
和H+
4
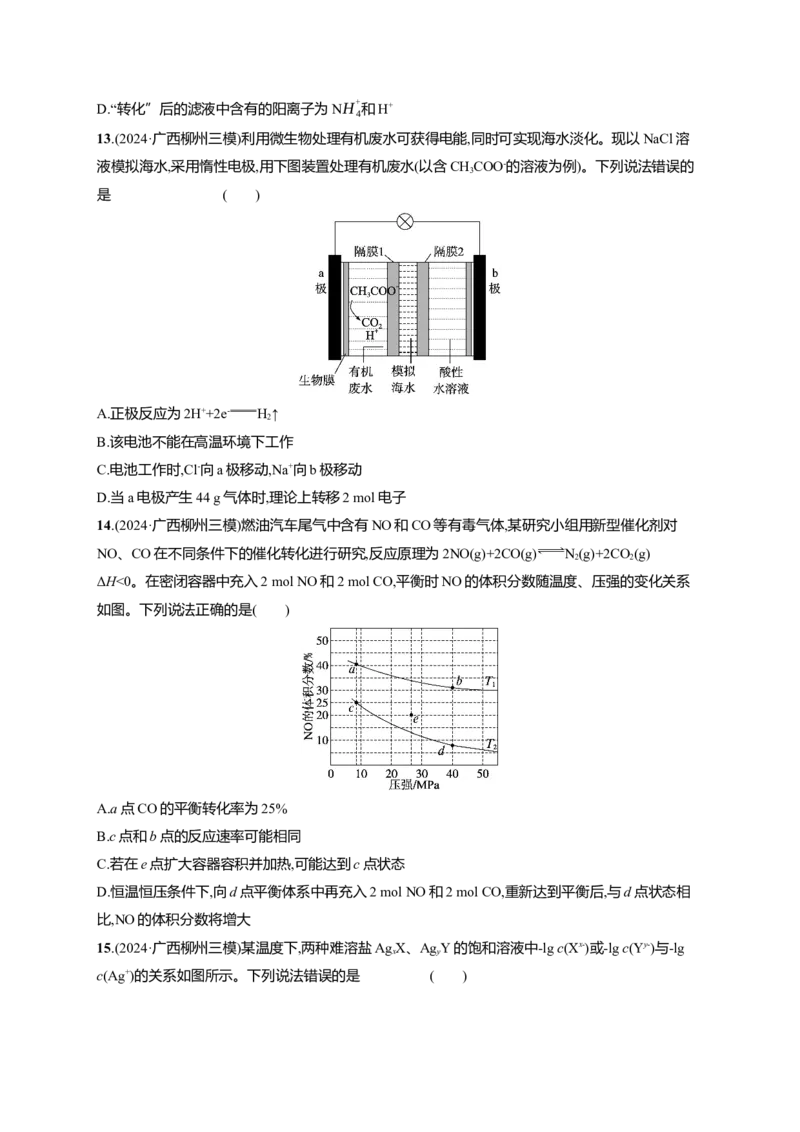
13.(2024·广西柳州三模)利用微生物处理有机废水可获得电能,同时可实现海水淡化。现以NaCl溶
液模拟海水,采用惰性电极,用下图装置处理有机废水(以含CHCOO-的溶液为例)。下列说法错误的
3
是 ( )
A.正极反应为2H++2e- H↑
2
B.该电池不能在高温环境下工作
C.电池工作时,Cl-向a极移动,Na+向b极移动
D.当a电极产生44 g气体时,理论上转移2 mol电子
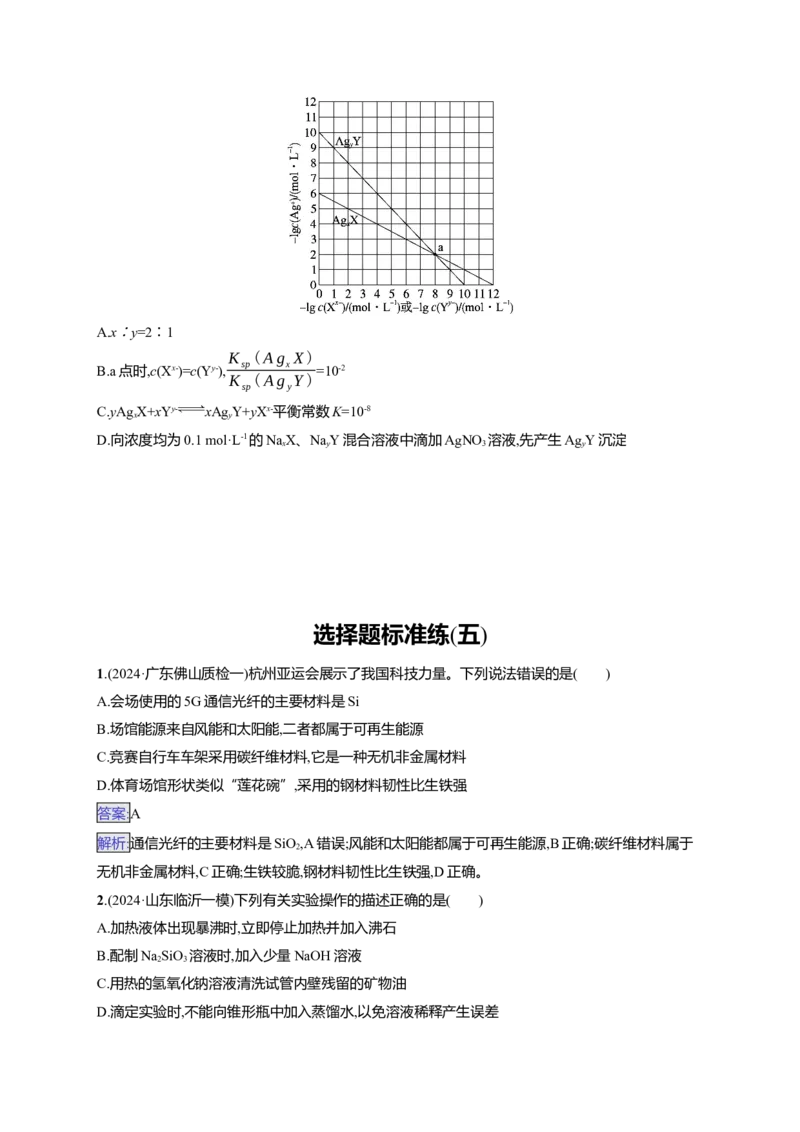
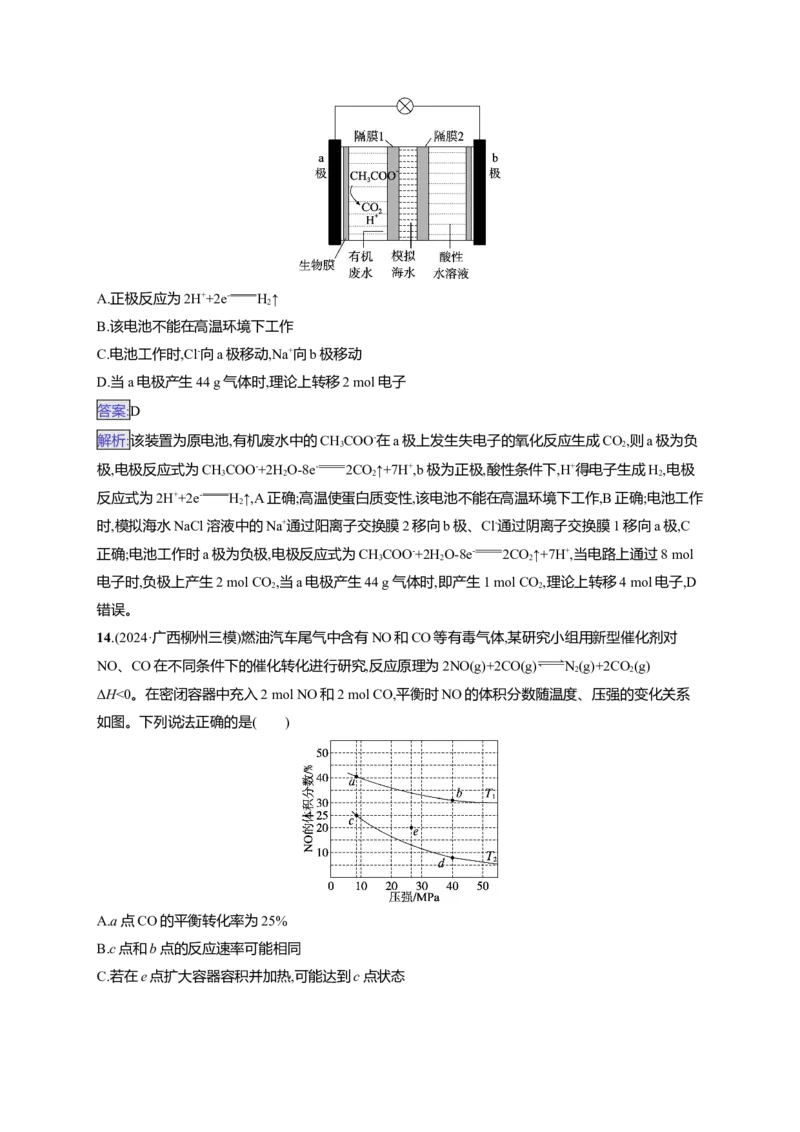
14.(2024·广西柳州三模)燃油汽车尾气中含有NO和CO等有毒气体,某研究小组用新型催化剂对
NO、CO在不同条件下的催化转化进行研究,反应原理为2NO(g)+2CO(g) N(g)+2CO (g)
2 2
ΔH<0。在密闭容器中充入2 mol NO和2 mol CO,平衡时NO的体积分数随温度、压强的变化关系
如图。下列说法正确的是( )
A.a点CO的平衡转化率为25%
B.c点和b点的反应速率可能相同
C.若在e点扩大容器容积并加热,可能达到c点状态
D.恒温恒压条件下,向d点平衡体系中再充入2 mol NO和2 mol CO,重新达到平衡后,与d点状态相
比,NO的体积分数将增大
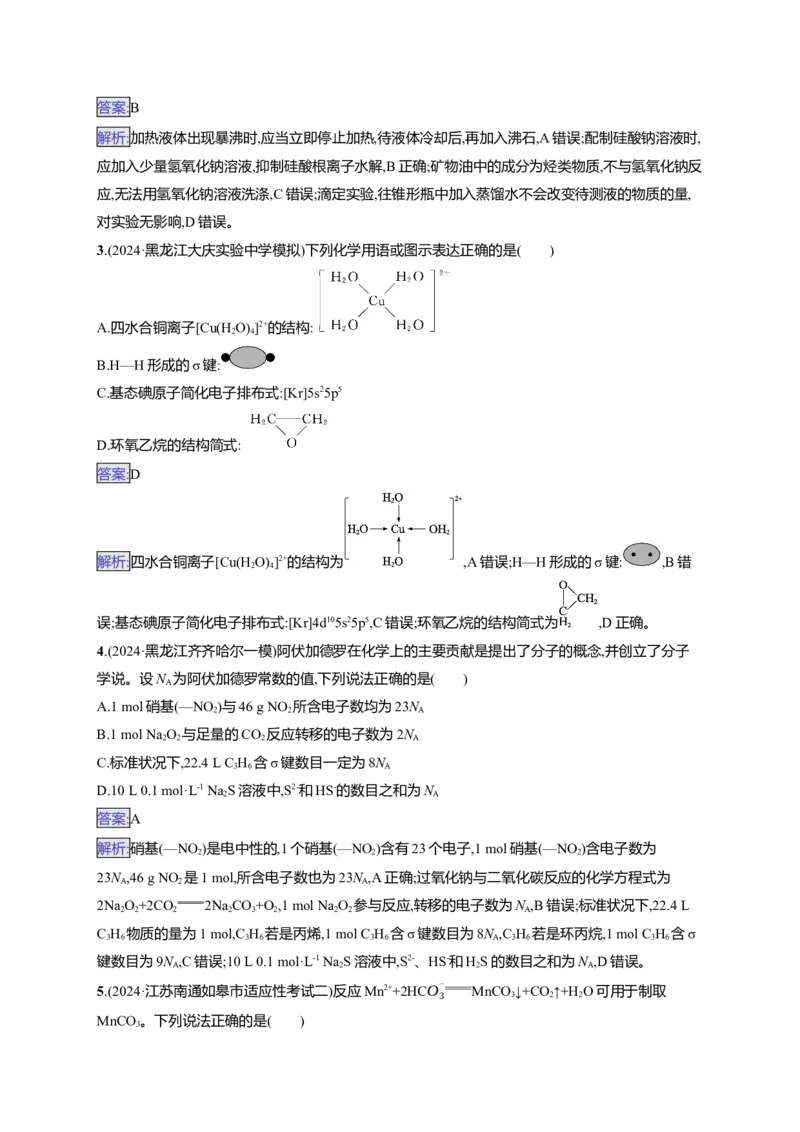
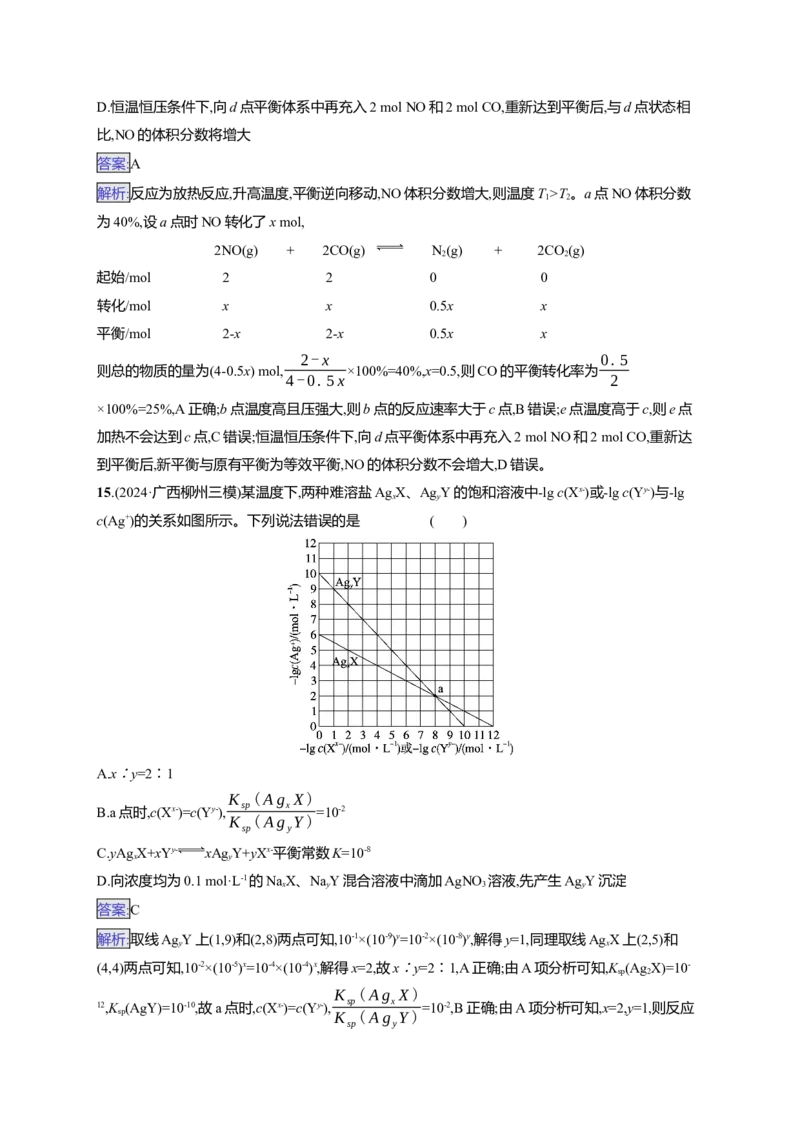
15.(2024·广西柳州三模)某温度下,两种难溶盐AgX、AgY的饱和溶液中-lg c(Xx-)或-lg c(Yy-)与-lg
x y
c(Ag+)的关系如图所示。下列说法错误的是 ( )A.x∶y=2∶1
K (Ag X)
sp x
B.a点时,c(Xx-)=c(Yy-), =10-2
K (Ag Y )
sp y
C.yAgX+xYy- xAgY+yXx-平衡常数K=10-8
x y
D.向浓度均为0.1 mol·L-1的NaX、NaY混合溶液中滴加AgNO 溶液,先产生AgY沉淀
x y 3 y
选择题标准练(五)
1.(2024·广东佛山质检一)杭州亚运会展示了我国科技力量。下列说法错误的是( )
A.会场使用的5G通信光纤的主要材料是Si
B.场馆能源来自风能和太阳能,二者都属于可再生能源
C.竞赛自行车车架采用碳纤维材料,它是一种无机非金属材料
D.体育场馆形状类似“莲花碗”,采用的钢材料韧性比生铁强
答案:A
解析:通信光纤的主要材料是SiO,A错误;风能和太阳能都属于可再生能源,B正确;碳纤维材料属于
2
无机非金属材料,C正确;生铁较脆,钢材料韧性比生铁强,D正确。
2.(2024·山东临沂一模)下列有关实验操作的描述正确的是( )
A.加热液体出现暴沸时,立即停止加热并加入沸石
B.配制NaSiO 溶液时,加入少量NaOH溶液
2 3
C.用热的氢氧化钠溶液清洗试管内壁残留的矿物油
D.滴定实验时,不能向锥形瓶中加入蒸馏水,以免溶液稀释产生误差答案:B
解析:加热液体出现暴沸时,应当立即停止加热,待液体冷却后,再加入沸石,A错误;配制硅酸钠溶液时,
应加入少量氢氧化钠溶液,抑制硅酸根离子水解,B正确;矿物油中的成分为烃类物质,不与氢氧化钠反
应,无法用氢氧化钠溶液洗涤,C错误;滴定实验,往锥形瓶中加入蒸馏水不会改变待测液的物质的量,
对实验无影响,D错误。
3.(2024·黑龙江大庆实验中学模拟)下列化学用语或图示表达正确的是( )
A.四水合铜离子[Cu(H O) ]2+的结构:
2 4
B.H—H形成的σ键:
C.基态碘原子简化电子排布式:[Kr]5s25p5
D.环氧乙烷的结构简式:
答案:D
解析:四水合铜离子[Cu(H O) ]2+的结构为 ,A错误;H—H形成的σ键: ,B错
2 4
误;基态碘原子简化电子排布式:[Kr]4d105s25p5,C错误;环氧乙烷的结构简式为 ,D正确。
4.(2024·黑龙江齐齐哈尔一模)阿伏加德罗在化学上的主要贡献是提出了分子的概念,并创立了分子
学说。设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.1 mol硝基(—NO )与46 g NO 所含电子数均为23N
2 2 A
B.1 mol Na O 与足量的CO 反应转移的电子数为2N
2 2 2 A
C.标准状况下,22.4 L C H 含σ键数目一定为8N
3 6 A
D.10 L 0.1 mol·L-1 Na S溶液中,S2-和HS-的数目之和为N
2 A
答案:A
解析:硝基(—NO )是电中性的,1个硝基(—NO )含有23个电子,1 mol硝基(—NO )含电子数为
2 2 2
23N ,46 g NO 是1 mol,所含电子数也为23N ,A正确;过氧化钠与二氧化碳反应的化学方程式为
A 2 A
2NaO+2CO 2NaCO+O ,1 mol Na O 参与反应,转移的电子数为N ,B错误;标准状况下,22.4 L
2 2 2 2 3 2 2 2 A
C H 物质的量为1 mol,C H 若是丙烯,1 mol C H 含σ键数目为8N ,C H 若是环丙烷,1 mol C H 含σ
3 6 3 6 3 6 A 3 6 3 6
键数目为9N ,C错误;10 L 0.1 mol·L-1 Na S溶液中,S2-、HS-和HS的数目之和为N ,D错误。
A 2 2 A
5.(2024·江苏南通如皋市适应性考试二)反应Mn2++2HCO-
MnCO ↓+CO ↑+H O可用于制取
3 3 2 2
MnCO 。下列说法正确的是( )
3A.基态Mn2+的电子排布式为[Ar]3d54s2
B.HCO-
中C的杂化方式为sp2杂化
3
C.CO2-
的空间结构为三角锥形
3
D.CO 是含非极性共价键的非极性分子
2
答案:B
解析:基态Mn2+的电子排布式为[Ar]3d5,A错误;HCO-
中C的价层电子对数为3,没有孤电子对,杂化方
3
式为sp2杂化,B正确;CO2-
中C的价层电子对数为3,没有孤电子对,其空间结构为平面三角形,C错
3
误;CO 是含极性共价键的非极性分子,D错误。
2
6.(2024·安徽合肥三模)下列各组离子在溶液中可以大量共存,且加入试剂后发生反应的离子方程式
书写也正确的是( )
选项 微粒组 加入试剂 发生反应的离子方程式
A K+、[Al(OH)
]-、SO2- 、CO2-
少量HCl溶液 [Al(OH) ]-+H+ Al(OH) ↓+H O
4 4 3 4 3 2
少量Ba(NO )
B H+、Fe2+、SO2- 、Na+ 3 2 3Fe2++4H++NO- 3Fe3++NO↑+2HO
4 3 2
溶液
C
Cl-、Na+、SiO2- 、HCO-
过量醋酸溶液
2H++SiO2-
HSiO↓
3 3 3 2 3
D
Fe3+、H+、MnO- 、SO2-
通入少量SO 2Fe3++SO+2H O
2Fe2++SO2-
+4H+
4 4 2 2 2 4
答案:A
解析:A项,该组离子间不发生反应,能大量共存,加入少量HCl溶液,H+优先与[Al(OH) ]-反应,其离子方
4
程式为[Al(OH) ]-+H+ Al(OH) ↓+H O,A正确;B项,原溶液中各离子间不反应,可大量共存,加入少
4 3 2
量Ba(NO )
溶液后,酸性条件下NO-
具有氧化性,与Fe2+发生氧化还原反应,离子方程式为3Fe2++4H+
3 2 3
+NO- +Ba2++SO2- 3Fe3++NO↑+2HO+BaSO↓,B错误;C项,SiO2- 与HCO-
不能大量共存,醋酸为弱
3 4 2 4 3 3
酸,不能拆开,加入过量醋酸溶液,反应的离子方程式为2CHCOOH+SiO2-
HSiO↓+2CH COO-,C
3 3 2 3 3
错误;D项,通入少量SO
后,MnO-
氧化性更强,优先与SO 发生氧化还原反应,反应的离子方程式为
2 4 2
2MnO- +5SO+2H O 2Mn2++5SO2- +4H+,D错误。
4 2 2 4
7.(2024·江西南昌一模)能用如图所示装置完成气体制备、尾气处理(加热和夹持等装置略去)的是(
)选项 气体 制备试剂 烧杯中试剂
A. NH 碱石灰与浓氨水 HSO 溶液
3 2 4
B. CO 大理石和硫酸 石灰水
2
C. C H 电石与水 水
2 2
D. Cl MnO 与浓盐酸 NaOH溶液
2 2
答案:D
解析:浓氨水滴入固体碱石灰上,生成NH ,氨气尾气吸收时不能将导管直接通入HSO 溶液中,会引起
3 2 4
倒吸,A错误;不能用硫酸与大理石制备CO,生成的硫酸钙会附着在大理石上,阻碍反应进行,B错误;
2
电石与饱和食盐水反应生成C H,尾气应用酸性高锰酸钾溶液或溴的四氯化碳溶液吸收,C错
2 2
误;MnO 与浓盐酸在加热条件下制取Cl,为了防止污染空气,过量的Cl 用NaOH溶液吸收,D正确。
2 2 2
8.(2024·安徽省第二次大联考)对下列事实的解释错误的是( )
选项 事实 解释
A 第一电离能:N>O N的2p轨道半充满,结构更稳定,能量更低
碳正离子稳定性:
B Br电负性比F小,电子云更偏向碳正离子
C 热稳定性:H O>HS HO分子间存在氢键,H S分子间不存在氢键
2 2 2 2
D C—H键长:CH >C H C的杂化轨道中s成分越多,形成的C—H化学键越强,键长越短
4 2 4
答案:C
解析:N的电子排布式为1s22s22p3,O的电子排布式为1s22s22p4,即N的2p轨道半充满,结构更稳定,所
以第一电离能N>O,A正确;Br电负性比F小,电子云更偏向碳正离子,所以碳正离子稳定性:
,B正确;分子间氢键只能影响物理性质,不能够影响化学性质,应该是元素
的非金属性越强,氢化物的稳定性越强,所以热稳定性HO>HS,C错误;CH 中C的杂化类型为
2 2 4
sp3,C H 中C的杂化类型为sp2,C的杂化轨道中s成分越多,形成的C—H化学键越强,键长越短,所以
2 4
C—H键长:CH >C H,D正确。
4 2 4
9.(2024·浙江丽水湖州衢州三地市4月质检)由不饱和烃A制备聚1,3-丁二烯的合成路线(部分反应条
件略去)如下4步反应所示:
A D 聚1,3-丁二烯
下列说法不正确的是( )
A.第一步反应属于取代反应B.A分子中的所有原子在同一直线上
C.聚1,3-丁二烯能使溴水褪色
D.B和C均属于醇类
答案:A
解析:第一步反应是H—C≡C—H和CHCHO发生加成反应生成 ,即反应类型
3
属于加成反应,A错误;A为H—C≡C—H,分子中碳原子采取sp杂化,空间结构为直线形,即所有原子在
同一直线上,B正确;聚1,3-丁二烯的结构简式为 ,其中含有碳碳双键,所以能
使溴水褪色,C正确;B和C的结构中均含有羟基,所以均属于醇类,D正确。
10.(2024·广西柳州三模)Q、X、Y、Z为原子序数依次增大的短周期元素,X、Y、Z为同周期相邻元
素,且X、Y为金属元素,最外层电子数之和满足Q=X+Z,下列结论正确的是( )
A.原子半径:Q>X>Y>Z
B.四种元素中,电负性最大的是Z
C.Y的最高价氧化物对应水化物是强碱
D.Q和Z的最简单氢化物的沸点:Q>Z
答案:D
解析:X、Y、Z为同周期相邻元素,且X、Y为金属元素,最外层电子数之和满足Q=X+Z,则X为
Mg,Y为Al,Z为Si,Q为O。原子半径:X>Y>Z>Q,A错误;电负性最大,则非金属性最强,则电负性最大
的为O,即为Q,B错误;Y的最高价氧化物对应水化物是Al(OH) ,是弱碱,C错误;Q的简单氢化物是
3
HO,Z的简单氢化物是SiH,水分子间形成氢键,熔、沸点高,所以Q和Z的最简单氢化物的沸
2 4
点:Q>Z,D正确。
11.(2024·甘肃张掖第三次诊断)根据实验操作、现象,能得出相应结论的是( )
选项 操作 现象 结论
将Fe(NO ) 样品溶于稀硫酸,滴加
3 2
A 观察到溶液变红 Fe(NO ) 样品已氧化变质
3 2
KSCN溶液
向盛有等体积、等浓度的HO 溶液的
2 2 加KMnO 溶液的试管 MnO- 比Cu2+的催化效果
4 4
B 两支试管中分别加入0.2 mL等浓度
中产生气泡速率更快 好
CuSO 溶液和KMnO 溶液
4 4
以KCrO 为指示剂,用AgNO 标准溶 先出现浅黄色沉淀,后
2 4 3
C K (AgBr)HCO-
2 3 3答案:D
解析:A项,NO-
在酸性条件下具有强氧化性,能将Fe2+氧化成Fe3+,对检验Fe(NO ) 是否变质产生干
3 3 2
扰;B项,KMnO 溶液可氧化过氧化氢,CuSO 溶液可催化过氧化氢分解,反应原理不同,不能探究催化
4 4
效果;C项,Br-与Ag+反应产生浅黄色的AgBr沉淀,CrO2-
与Ag+反应产生砖红色的Ag CrO 沉淀,Cr
4 2 4
O2- 和Br-浓度不同且AgBr与Ag CrO 沉淀类型不相似,故根据实验操作、现象,不能比较AgBr与
4 2 4
Ag CrO 的K 大小;D项,向苯酚浊液中滴加少量NaCO 溶液,生成苯酚钠、碳酸氢钠,则浊液变澄清,
2 4 sp 2 3
可知酸性:苯酚>HCO-
;故选D。
3
12.(2024·东北三省三校5月第三次联考)一种利用废铜渣(主要成分为CuO及少量的Fe O、SiO 等
2 3 2
杂质)制备超细铜粉的流程如下:
下列说法正确的是( )
A.“酸浸”所得滤渣的主要成分为HSiO
2 3
B.向“沉铁”后的滤液中加入乙醇,析出的深蓝色晶体为Cu(OH)
2
C.“沉铜”过程中发生了氧化还原反应,SO 是还原剂
2
D.“转化”后的滤液中含有的阳离子为NH+
和H+
4
答案:C
解析:废铜渣(主要成分为CuO及少量的Fe O、SiO 等杂质)“酸浸”时CuO、少量Fe O 与HSO 反
2 3 2 2 3 2 4
应生成硫酸铜、硫酸铁,SiO 不溶于HSO ,所以滤渣的成分是SiO,滤液中加过量氨水沉铁除去Fe3+,
2 2 4 2
铜离子转化为[Cu(NH )]2+,所得滤液通二氧化硫沉铜,过滤出产生的CuNH SO 沉淀,加稀硫酸转化,+1
3 4 4 3
价铜发生歧化反应,得到铜离子和Cu。据分析,“酸浸”所得滤渣的主要成分为SiO,A错误;若向“沉
2
铁”后所得滤液中加入乙醇,析出的深蓝色晶体为[Cu(NH )]SO ·H O,B错误;“沉铜”时向含有
3 4 4 2
[Cu(NH )]2+和过量氨水的混合溶液中通入二氧化硫生成CuNH SO 沉淀,铜元素化合价降低,则发生
3 4 4 3
氧化还原反应,SO 是还原剂,C正确;“转化”时,CuNHSO 在稀硫酸中发生歧化反应,得到铜离子和
2 4 3
Cu,结合元素守恒可知,“转化”后所得滤液中含有的主要阳离子:NH+
、H+、Cu2+,D错误。
4
13.(2024·广西柳州三模)利用微生物处理有机废水可获得电能,同时可实现海水淡化。现以NaCl溶
液模拟海水,采用惰性电极,用下图装置处理有机废水(以含CHCOO-的溶液为例)。下列说法错误的
3
是 ( )A.正极反应为2H++2e- H↑
2
B.该电池不能在高温环境下工作
C.电池工作时,Cl-向a极移动,Na+向b极移动
D.当a电极产生44 g气体时,理论上转移2 mol电子
答案:D
解析:该装置为原电池,有机废水中的CHCOO-在a极上发生失电子的氧化反应生成CO,则a极为负
3 2
极,电极反应式为CHCOO-+2H O-8e- 2CO↑+7H+,b极为正极,酸性条件下,H+得电子生成H,电极
3 2 2 2
反应式为2H++2e- H↑,A正确;高温使蛋白质变性,该电池不能在高温环境下工作,B正确;电池工作
2
时,模拟海水NaCl溶液中的Na+通过阳离子交换膜2移向b极、Cl-通过阴离子交换膜1移向a极,C
正确;电池工作时a极为负极,电极反应式为CHCOO-+2H O-8e- 2CO↑+7H+,当电路上通过8 mol
3 2 2
电子时,负极上产生2 mol CO ,当a电极产生44 g气体时,即产生1 mol CO ,理论上转移4 mol电子,D
2 2
错误。
14.(2024·广西柳州三模)燃油汽车尾气中含有NO和CO等有毒气体,某研究小组用新型催化剂对
NO、CO在不同条件下的催化转化进行研究,反应原理为2NO(g)+2CO(g) N(g)+2CO (g)
2 2
ΔH<0。在密闭容器中充入2 mol NO和2 mol CO,平衡时NO的体积分数随温度、压强的变化关系
如图。下列说法正确的是( )
A.a点CO的平衡转化率为25%
B.c点和b点的反应速率可能相同
C.若在e点扩大容器容积并加热,可能达到c点状态D.恒温恒压条件下,向d点平衡体系中再充入2 mol NO和2 mol CO,重新达到平衡后,与d点状态相
比,NO的体积分数将增大
答案:A
解析:反应为放热反应,升高温度,平衡逆向移动,NO体积分数增大,则温度T>T 。a点NO体积分数
1 2
为40%,设a点时NO转化了x mol,
2NO(g) + 2CO(g) N (g) + 2CO (g)
2 2
起始/mol 2 2 0 0
转化/mol x x 0.5x x
平衡/mol 2-x 2-x 0.5x x
2-x 0.5
则总的物质的量为(4-0.5x) mol, ×100%=40%,x=0.5,则CO的平衡转化率为
4-0.5x 2
×100%=25%,A正确;b点温度高且压强大,则b点的反应速率大于c点,B错误;e点温度高于c,则e点
加热不会达到c点,C错误;恒温恒压条件下,向d点平衡体系中再充入2 mol NO和2 mol CO,重新达
到平衡后,新平衡与原有平衡为等效平衡,NO的体积分数不会增大,D错误。
15.(2024·广西柳州三模)某温度下,两种难溶盐AgX、AgY的饱和溶液中-lg c(Xx-)或-lg c(Yy-)与-lg
x y
c(Ag+)的关系如图所示。下列说法错误的是 ( )
A.x∶y=2∶1
K (Ag X)
sp x
B.a点时,c(Xx-)=c(Yy-), =10-2
K (Ag Y )
sp y
C.yAgX+xYy- xAgY+yXx-平衡常数K=10-8
x y
D.向浓度均为0.1 mol·L-1的NaX、NaY混合溶液中滴加AgNO 溶液,先产生AgY沉淀
x y 3 y
答案:C
解析:取线AgY上(1,9)和(2,8)两点可知,10-1×(10-9)y=10-2×(10-8)y,解得y=1,同理取线AgX上(2,5)和
y x
(4,4)两点可知,10-2×(10-5)x=10-4×(10-4)x,解得x=2,故x∶y=2∶1,A正确;由A项分析可知,K (Ag X)=10-
sp 2
K (Ag X)
sp x
12,K (AgY)=10-10,故a点时,c(Xx-)=c(Yy-), =10-2,B正确;由A项分析可知,x=2,y=1,则反应
sp K (Ag Y )
sp yyAgX+xYy- xAgY+yXx-为Ag X(s)+2Y-(aq) 2AgY(s)+X2-(aq)平衡常数K=
x y 2
c(X2-) c2(Ag+)c(X2-) K (Ag X) 10-12
= = sp 2 = =108,C错误;由题干图示信息可知,当Xx-
c2(Y-) c2(Ag+)c2(Y-) K2 (AgY ) (10-10)2
sp
和Yy-浓度均为0.1 mol·L-1时,AgY对应的Ag+浓度更小,即析出沉淀AgY需要的Ag+浓度更小,先产
y y
生AgY沉淀,D正确。
y