文档内容
12.滴定过程图像及分析
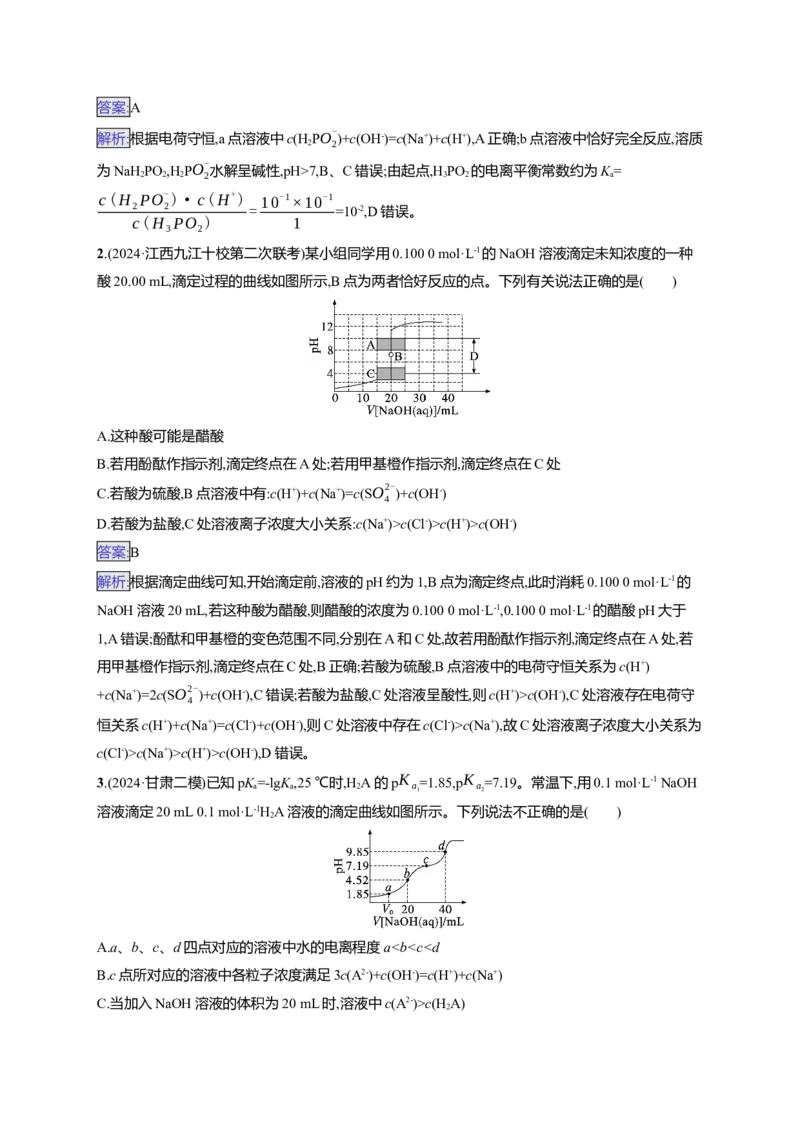
1.(2024·广东大亚湾区1月联合模拟)常温下,向20.00 mL 1 mol·L-1次磷酸HPO (一元酸)中,逐滴加入
3 2
1 mol·L-1 NaOH溶液,溶液的pH与所加NaOH溶液的体积关系如图所示。下列有关叙述正确的是(
)
A.a点溶液中c(H
PO-
)+c(OH-)=c(Na+)+c(H+)
2 2
B.b点溶液中pH=7
C.NaH PO 溶液显酸性
2 2
D.HPO 的电离平衡常数约为1×10-1
3 2
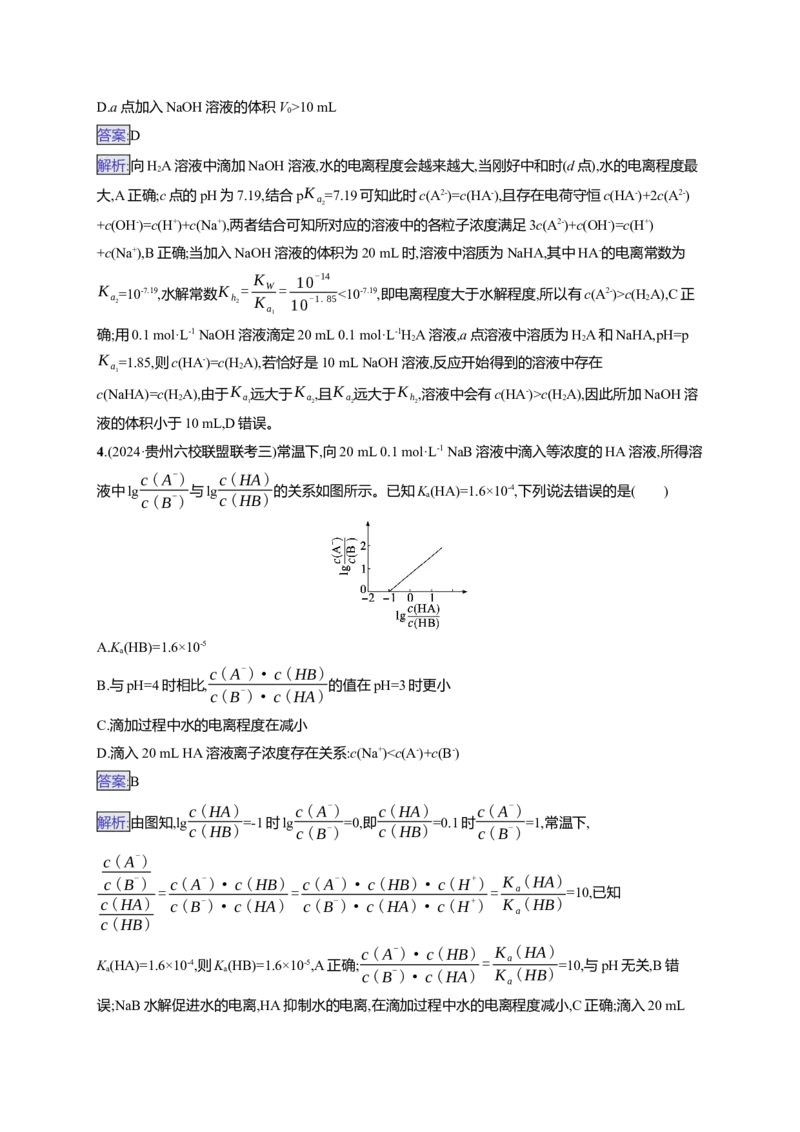
2.(2024·江西九江十校第二次联考)某小组同学用0.100 0 mol·L-1的NaOH溶液滴定未知浓度的一种
酸20.00 mL,滴定过程的曲线如图所示,B点为两者恰好反应的点。下列有关说法正确的是( )
A.这种酸可能是醋酸
B.若用酚酞作指示剂,滴定终点在A处;若用甲基橙作指示剂,滴定终点在C处
C.若酸为硫酸,B点溶液中有:c(H+)+c(Na+)=c(SO2-
)+c(OH-)
4
D.若酸为盐酸,C处溶液离子浓度大小关系:c(Na+)>c(Cl-)>c(H+)>c(OH-)
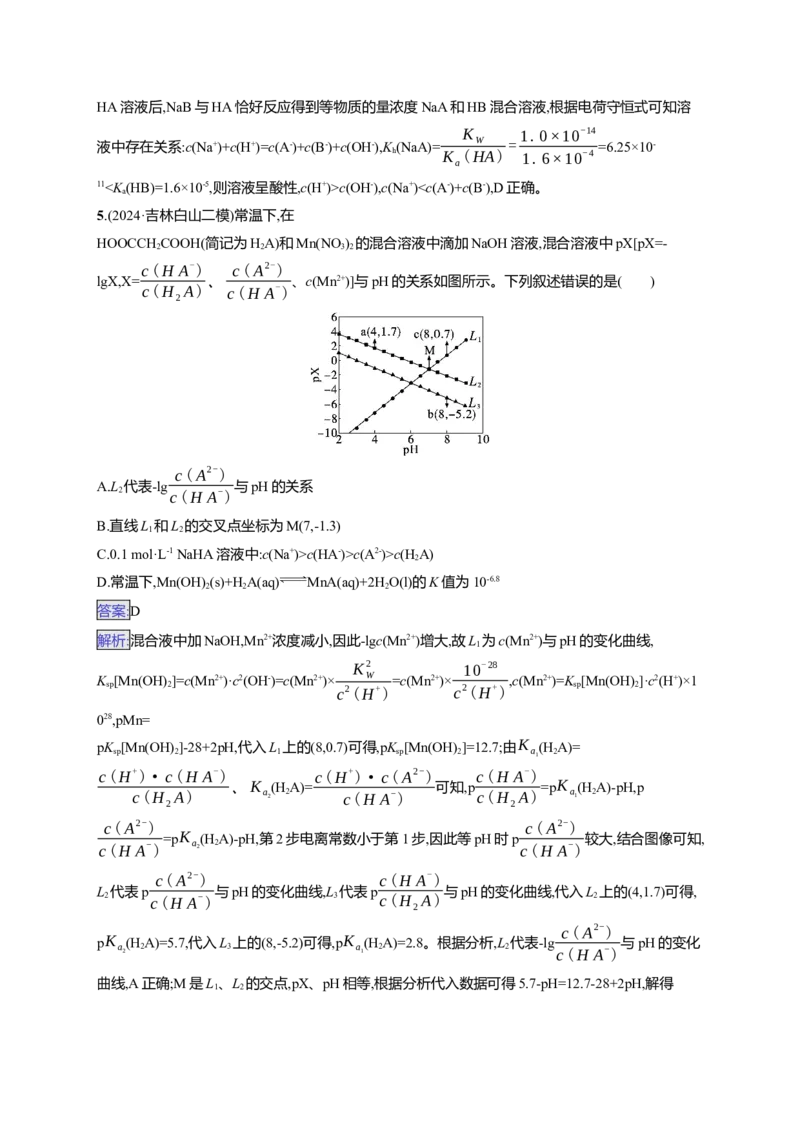
3.(2024·甘肃二模)已知pK=-lgK,25 ℃时,H A的pK =1.85,pK =7.19。常温下,用0.1 mol·L-1 NaOH
a a 2 a a
1 2
溶液滴定20 mL 0.1 mol·L-1HA溶液的滴定曲线如图所示。下列说法不正确的是( )
2
A.a、b、c、d四点对应的溶液中水的电离程度ac(H A)
2
D.a点加入NaOH溶液的体积V>10 mL
04.(2024·贵州六校联盟联考三)常温下,向20 mL 0.1 mol·L-1 NaB溶液中滴入等浓度的HA溶液,所得溶
c(A-) c(HA)
液中lg 与lg 的关系如图所示。已知K(HA)=1.6×10-4,下列说法错误的是( )
c(B-) c(HB) a
A.K(HB)=1.6×10-5
a
c(A-)·c(HB)
B.与pH=4时相比, 的值在pH=3时更小
c(B-)·c(HA)
C.滴加过程中水的电离程度在减小
D.滴入20 mL HA溶液离子浓度存在关系:c(Na+)c(HA-)>c(A2-)>c(H A)
2
D.常温下,Mn(OH) (s)+HA(aq) MnA(aq)+2H O(l)的K值为10-6.8
2 2 2
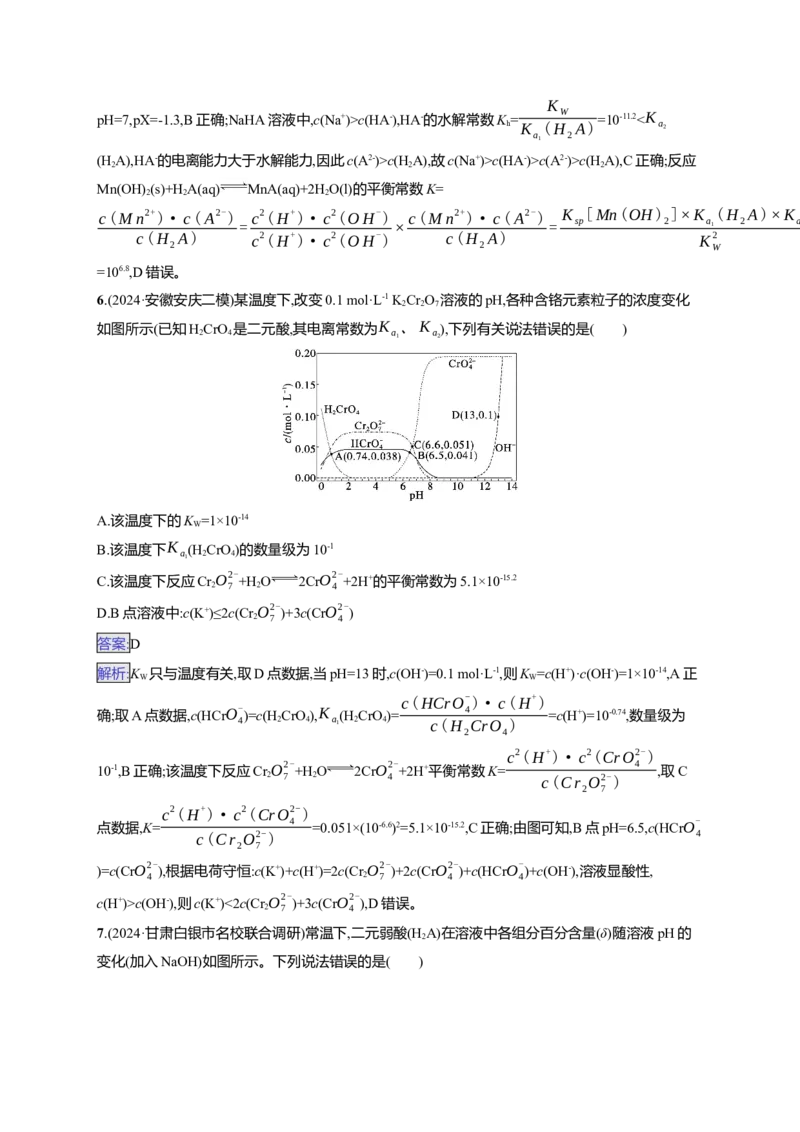
6.(2024·安徽安庆二模)某温度下,改变0.1 mol·L-1 K Cr O 溶液的pH,各种含铬元素粒子的浓度变化
2 2 7
如图所示(已知HCrO 是二元酸,其电离常数为 K 、K ),下列有关说法错误的是( )
2 4 a a
1 2A.该温度下的K =1×10-14
W
B.该温度下 K (H CrO)的数量级为10-1
a 2 4
1
C.该温度下反应CrO2-
+H O
2CrO2-
+2H+的平衡常数为5.1×10-15.2
2 7 2 4
D.B点溶液中:c(K+)≤2c(CrO2- )+3c(CrO2-
)
2 7 4
7.(2024·甘肃白银市名校联合调研)常温下,二元弱酸(H A)在溶液中各组分百分含量(δ)随溶液pH的
2
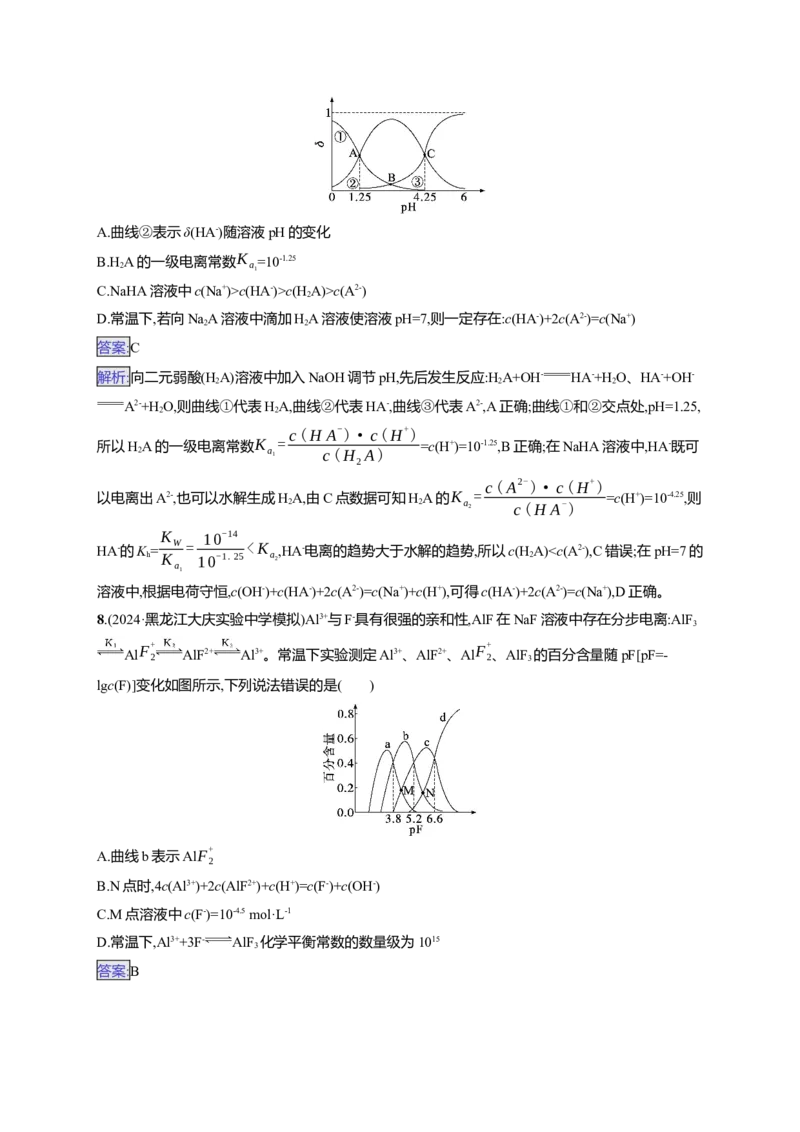
变化(加入NaOH)如图所示。下列说法错误的是( )
A.曲线②表示δ(HA-)随溶液pH的变化
B.H A的一级电离常数 K =10-1.25
2 a
1
C.NaHA溶液中c(Na+)>c(HA-)>c(H A)>c(A2-)
2
D.常温下,若向NaA溶液中滴加HA溶液使溶液pH=7,则一定存在:c(HA-)+2c(A2-)=c(Na+)
2 2
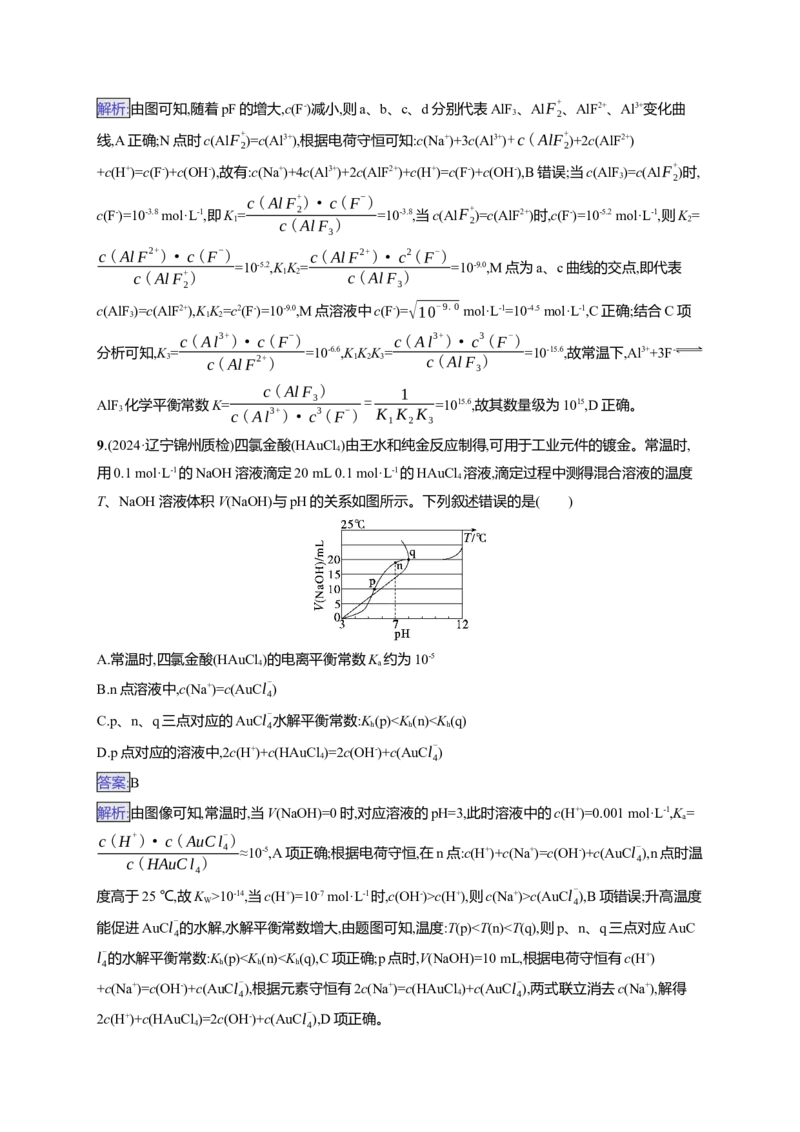
8.(2024·黑龙江大庆实验中学模拟)Al3+与F-具有很强的亲和性,AlF在NaF溶液中存在分步电离:AlF
3
Al F 2 + AlF2+ Al3+。常温下实验测定Al3+、AlF2+、Al F 2 + 、AlF 3 的百分含量随pF[pF=-
lgc(F)]变化如图所示,下列说法错误的是( )
A.曲线b表示AlF+
2
B.N点时,4c(Al3+)+2c(AlF2+)+c(H+)=c(F-)+c(OH-)
C.M点溶液中c(F-)=10-4.5 mol·L-1
D.常温下,Al3++3F- AlF 化学平衡常数的数量级为1015
3
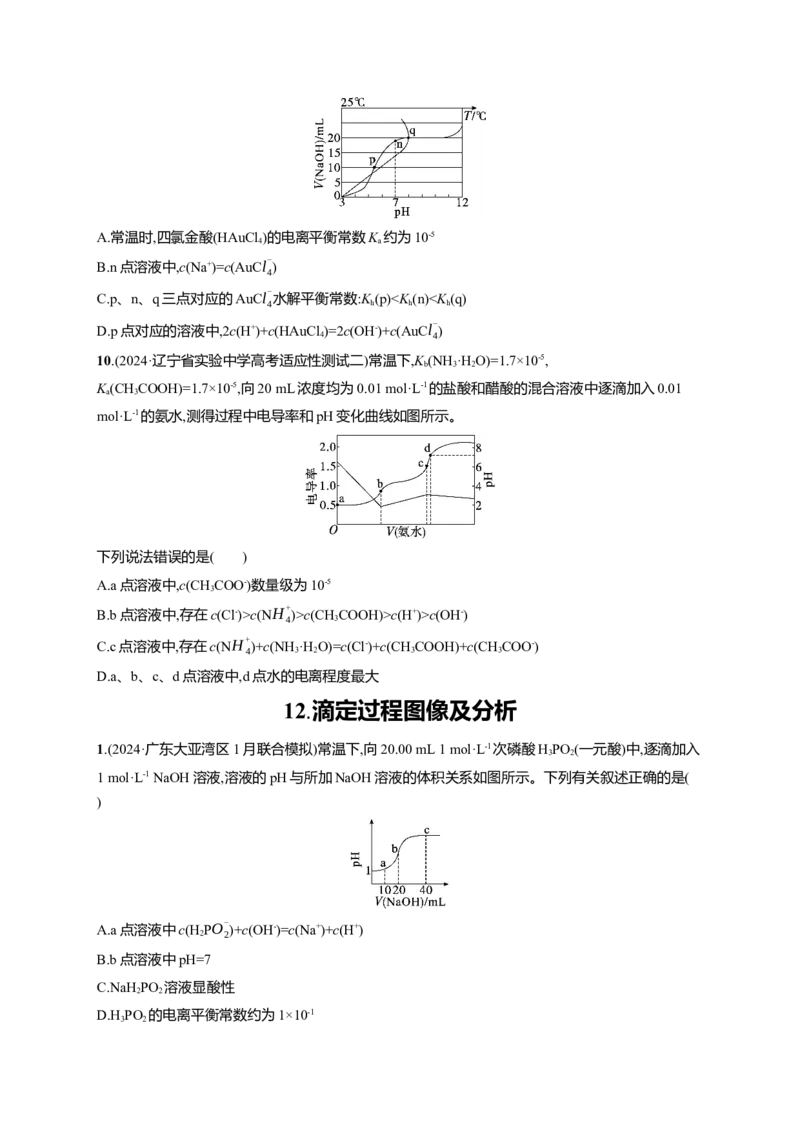
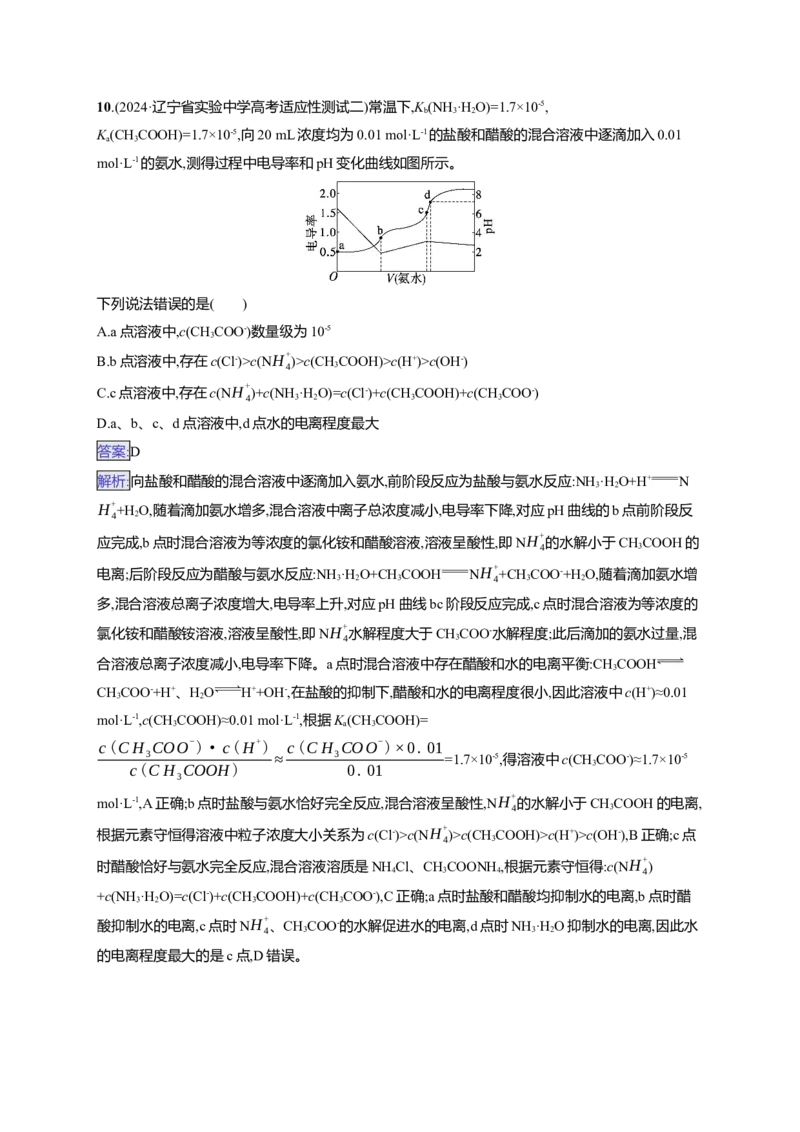
9.(2024·辽宁锦州质检)四氯金酸(HAuCl )由王水和纯金反应制得,可用于工业元件的镀金。常温时,
4
用0.1 mol·L-1的NaOH溶液滴定20 mL 0.1 mol·L-1的HAuCl 溶液,滴定过程中测得混合溶液的温度
4
T、NaOH溶液体积V(NaOH)与pH的关系如图所示。下列叙述错误的是( )A.常温时,四氯金酸(HAuCl )的电离平衡常数K 约为10-5
4 a
B.n点溶液中,c(Na+)=c(AuCl-
)
4
C.p、n、q三点对应的AuCl-
水解平衡常数:K (p)c(NH+
)>c(CHCOOH)>c(H+)>c(OH-)
4 3
C.c点溶液中,存在c(NH+
)+c(NH ·H O)=c(Cl-)+c(CHCOOH)+c(CHCOO-)
4 3 2 3 3
D.a、b、c、d点溶液中,d点水的电离程度最大
12.滴定过程图像及分析
1.(2024·广东大亚湾区1月联合模拟)常温下,向20.00 mL 1 mol·L-1次磷酸HPO (一元酸)中,逐滴加入
3 2
1 mol·L-1 NaOH溶液,溶液的pH与所加NaOH溶液的体积关系如图所示。下列有关叙述正确的是(
)
A.a点溶液中c(H
PO-
)+c(OH-)=c(Na+)+c(H+)
2 2
B.b点溶液中pH=7
C.NaH PO 溶液显酸性
2 2
D.HPO 的电离平衡常数约为1×10-1
3 2答案:A
解析:根据电荷守恒,a点溶液中c(H
PO-
)+c(OH-)=c(Na+)+c(H+),A正确;b点溶液中恰好完全反应,溶质
2 2
为NaH PO ,H
PO-
水解呈碱性,pH>7,B、C错误;由起点,H PO 的电离平衡常数约为K=
2 2 2 2 3 2 a
c(H PO-)·c(H+) 10-1×10-1
2 2 = =10-2,D错误。
c(H PO ) 1
3 2
2.(2024·江西九江十校第二次联考)某小组同学用0.100 0 mol·L-1的NaOH溶液滴定未知浓度的一种
酸20.00 mL,滴定过程的曲线如图所示,B点为两者恰好反应的点。下列有关说法正确的是( )
A.这种酸可能是醋酸
B.若用酚酞作指示剂,滴定终点在A处;若用甲基橙作指示剂,滴定终点在C处
C.若酸为硫酸,B点溶液中有:c(H+)+c(Na+)=c(SO2-
)+c(OH-)
4
D.若酸为盐酸,C处溶液离子浓度大小关系:c(Na+)>c(Cl-)>c(H+)>c(OH-)
答案:B
解析:根据滴定曲线可知,开始滴定前,溶液的pH约为1,B点为滴定终点,此时消耗0.100 0 mol·L-1的
NaOH溶液20 mL,若这种酸为醋酸,则醋酸的浓度为0.100 0 mol·L-1,0.100 0 mol·L-1的醋酸pH大于
1,A错误;酚酞和甲基橙的变色范围不同,分别在A和C处,故若用酚酞作指示剂,滴定终点在A处,若
用甲基橙作指示剂,滴定终点在C处,B正确;若酸为硫酸,B点溶液中的电荷守恒关系为c(H+)
+c(Na+)=2c(SO2- )+c(OH-),C错误;若酸为盐酸,C处溶液呈酸性,则c(H+)>c(OH-),C处溶液存在电荷守
4
恒关系c(H+)+c(Na+)=c(Cl-)+c(OH-),则C处溶液中存在c(Cl-)>c(Na+),故C处溶液离子浓度大小关系为
c(Cl-)>c(Na+)>c(H+)>c(OH-),D错误。
3.(2024·甘肃二模)已知pK=-lgK,25 ℃时,H A的pK =1.85,pK =7.19。常温下,用0.1 mol·L-1 NaOH
a a 2 a a
1 2
溶液滴定20 mL 0.1 mol·L-1HA溶液的滴定曲线如图所示。下列说法不正确的是( )
2
A.a、b、c、d四点对应的溶液中水的电离程度ac(H A)
2D.a点加入NaOH溶液的体积V>10 mL
0
答案:D
解析:向HA溶液中滴加NaOH溶液,水的电离程度会越来越大,当刚好中和时(d点),水的电离程度最
2
大,A正确;c点的pH为7.19,结合pK =7.19可知此时c(A2-)=c(HA-),且存在电荷守恒c(HA-)+2c(A2-)
a
2
+c(OH-)=c(H+)+c(Na+),两者结合可知所对应的溶液中的各粒子浓度满足3c(A2-)+c(OH-)=c(H+)
+c(Na+),B正确;当加入NaOH溶液的体积为20 mL时,溶液中溶质为NaHA,其中HA-的电离常数为
K 10-14
K =10-7.19,水解常数K = W = <10-7.19,即电离程度大于水解程度,所以有c(A2-)>c(H A),C正
a 2 h 2 K 10-1.85 2
a
1
确;用0.1 mol·L-1 NaOH溶液滴定20 mL 0.1 mol·L-1HA溶液,a点溶液中溶质为HA和NaHA,pH=p
2 2
K =1.85,则c(HA-)=c(H A),若恰好是10 mL NaOH溶液,反应开始得到的溶液中存在
a 2
1
c(NaHA)=c(H A),由于 K 远大于 K ,且 K 远大于 K ,溶液中会有c(HA-)>c(H A),因此所加NaOH溶
2 a a a h 2
1 2 2 2
液的体积小于10 mL,D错误。
4.(2024·贵州六校联盟联考三)常温下,向20 mL 0.1 mol·L-1 NaB溶液中滴入等浓度的HA溶液,所得溶
c(A-) c(HA)
液中lg 与lg 的关系如图所示。已知K(HA)=1.6×10-4,下列说法错误的是( )
c(B-) c(HB) a
A.K(HB)=1.6×10-5
a
c(A-)·c(HB)
B.与pH=4时相比, 的值在pH=3时更小
c(B-)·c(HA)
C.滴加过程中水的电离程度在减小
D.滴入20 mL HA溶液离子浓度存在关系:c(Na+)c(OH-),c(Na+)c(HA-)>c(A2-)>c(H A)
2
D.常温下,Mn(OH) (s)+HA(aq) MnA(aq)+2H O(l)的K值为10-6.8
2 2 2
答案:D
解析:混合液中加NaOH,Mn2+浓度减小,因此-lgc(Mn2+)增大,故L 为c(Mn2+)与pH的变化曲线,
1
K2 10-28
K [Mn(OH) ]=c(Mn2+)·c2(OH-)=c(Mn2+)× W =c(Mn2+)× ,c(Mn2+)=K [Mn(OH) ]·c2(H+)×1
sp 2 c2(H+) c2(H+) sp 2
028,pMn=
pK [Mn(OH) ]-28+2pH,代入L 上的(8,0.7)可得,pK [Mn(OH) ]=12.7;由 K (H A)=
sp 2 1 sp 2 a 2
1
c(H+)·c(H A-) c(H+)·c(A2-) c(H A-)
、K (H A)= 可知,p =pK (H A)-pH,p
c(H A) a 2 2 c(H A-) c(H A) a 1 2
2 2
c(A2-) c(A2-)
=pK (H A)-pH,第2步电离常数小于第1步,因此等pH时p 较大,结合图像可知,
c(H A-) a 2 2 c(H A-)
c(A2-) c(H A-)
L 代表p 与pH的变化曲线,L 代表p 与pH的变化曲线,代入L 上的(4,1.7)可得,
2 c(H A-) 3 c(H A) 2
2
c(A2-)
pK (H A)=5.7,代入L 上的(8,-5.2)可得,pK (H A)=2.8。根据分析,L 代表-lg 与pH的变化
a 2 2 3 a 1 2 2 c(H A-)
曲线,A正确;M是L、L 的交点,pX、pH相等,根据分析代入数据可得5.7-pH=12.7-28+2pH,解得
1 2K
pH=7,pX=-1.3,B正确;NaHA溶液中,c(Na+)>c(HA-),HA-的水解常数K = W =10-11.2c(H A),故c(Na+)>c(HA-)>c(A2-)>c(H A),C正确;反应
2 2 2
Mn(OH) (s)+HA(aq) MnA(aq)+2H O(l)的平衡常数K=
2 2 2
c(Mn2+)·c(A2-) c2(H+)·c2(OH-) c(Mn2+)·c(A2-) K [Mn(OH) ]×K (H A)×K (H A) 10-12.7×10-2.8×10-5.7
= × = sp 2 a 1 2 a 2 2 =
c(H A) c2(H+)·c2(OH-) c(H A) K2 (10-14)2
2 2 W
=106.8,D错误。
6.(2024·安徽安庆二模)某温度下,改变0.1 mol·L-1 K Cr O 溶液的pH,各种含铬元素粒子的浓度变化
2 2 7
如图所示(已知HCrO 是二元酸,其电离常数为 K 、K ),下列有关说法错误的是( )
2 4 a a
1 2
A.该温度下的K =1×10-14
W
B.该温度下 K (H CrO)的数量级为10-1
a 2 4
1
C.该温度下反应CrO2-
+H O
2CrO2-
+2H+的平衡常数为5.1×10-15.2
2 7 2 4
D.B点溶液中:c(K+)≤2c(CrO2- )+3c(CrO2-
)
2 7 4
答案:D
解析:K 只与温度有关,取D点数据,当pH=13时,c(OH-)=0.1 mol·L-1,则K =c(H+)·c(OH-)=1×10-14,A正
W W
c(HCrO-)·c(H+)
确;取A点数据,c(HCrO- )=c(H CrO),K (H CrO)= 4 =c(H+)=10-0.74,数量级为
4 2 4 a 1 2 4 c(H CrO )
2 4
c2(H+)·c2(CrO2-)
10-1,B正确;该温度下反应CrO2-
+H O
2CrO2-
+2H+平衡常数K=
4
,取C
2 7 2 4 c(Cr O2-)
2 7
c2(H+)·c2(CrO2-)
点数据,K=
4 =0.051×(10-6.6)2=5.1×10-15.2,C正确;由图可知,B点pH=6.5,c(HCrO-
c(Cr O2-) 4
2 7
)=c(CrO2- ),根据电荷守恒:c(K+)+c(H+)=2c(CrO2- )+2c(CrO2- )+c(HCrO- )+c(OH-),溶液显酸性,
4 2 7 4 4
c(H+)>c(OH-),则c(K+)<2c(CrO2- )+3c(CrO2-
),D错误。
2 7 4
7.(2024·甘肃白银市名校联合调研)常温下,二元弱酸(H A)在溶液中各组分百分含量(δ)随溶液pH的
2
变化(加入NaOH)如图所示。下列说法错误的是( )A.曲线②表示δ(HA-)随溶液pH的变化
B.H A的一级电离常数 K =10-1.25
2 a
1
C.NaHA溶液中c(Na+)>c(HA-)>c(H A)>c(A2-)
2
D.常温下,若向NaA溶液中滴加HA溶液使溶液pH=7,则一定存在:c(HA-)+2c(A2-)=c(Na+)
2 2
答案:C
解析:向二元弱酸(H A)溶液中加入NaOH调节pH,先后发生反应:H A+OH- HA-+H O、HA-+OH-
2 2 2
A2-+H O,则曲线①代表HA,曲线②代表HA-,曲线③代表A2-,A正确;曲线①和②交点处,pH=1.25,
2 2
c(H A-)·c(H+)
所以HA的一级电离常数K = =c(H+)=10-1.25,B正确;在NaHA溶液中,HA-既可
2 a
1
c(H A)
2
c(A2-)·c(H+)
以电离出A2-,也可以水解生成HA,由C点数据可知HA的K = =c(H+)=10-4.25,则
2 2 a 2 c(H A-)
K 10-14
HA-的K = W = 10-14,当c(H+)=10-7
mol·L-1时,c(OH-)>c(H+),则c(Na+)>c(AuCl-
),B项错误;升高温度
W 4
能促进AuCl-
的水解,水解平衡常数增大,由题图可知,温度:T(p)c(NH+
)>c(CHCOOH)>c(H+)>c(OH-)
4 3
C.c点溶液中,存在c(NH+
)+c(NH ·H O)=c(Cl-)+c(CHCOOH)+c(CHCOO-)
4 3 2 3 3
D.a、b、c、d点溶液中,d点水的电离程度最大
答案:D
解析:向盐酸和醋酸的混合溶液中逐滴加入氨水,前阶段反应为盐酸与氨水反应:NH·H O+H+ N
3 2
H+
+H O,随着滴加氨水增多,混合溶液中离子总浓度减小,电导率下降,对应pH曲线的b点前阶段反
4 2
应完成,b点时混合溶液为等浓度的氯化铵和醋酸溶液,溶液呈酸性,即NH+
的水解小于CHCOOH的
4 3
电离;后阶段反应为醋酸与氨水反应:NH·H O+CHCOOH
NH+
+CH COO-+H O,随着滴加氨水增
3 2 3 4 3 2
多,混合溶液总离子浓度增大,电导率上升,对应pH曲线bc阶段反应完成,c点时混合溶液为等浓度的
氯化铵和醋酸铵溶液,溶液呈酸性,即NH+
水解程度大于CHCOO-水解程度;此后滴加的氨水过量,混
4 3
合溶液总离子浓度减小,电导率下降。a点时混合溶液中存在醋酸和水的电离平衡:CH COOH
3
CHCOO-+H+、HO H++OH-,在盐酸的抑制下,醋酸和水的电离程度很小,因此溶液中c(H+)≈0.01
3 2
mol·L-1,c(CHCOOH)≈0.01 mol·L-1,根据K(CHCOOH)=
3 a 3
c(CH COO-)·c(H+) c(CH COO-)×0.01
3 ≈ 3 =1.7×10-5,得溶液中c(CHCOO-)≈1.7×10-5
c(CH COOH) 0.01 3
3
mol·L-1,A正确;b点时盐酸与氨水恰好完全反应,混合溶液呈酸性,NH+
的水解小于CHCOOH的电离,
4 3
根据元素守恒得溶液中粒子浓度大小关系为c(Cl-)>c(NH+
)>c(CHCOOH)>c(H+)>c(OH-),B正确;c点
4 3
时醋酸恰好与氨水完全反应,混合溶液溶质是NH
Cl、CHCOONH,根据元素守恒得:c(NH+
)
4 3 4 4
+c(NH ·H O)=c(Cl-)+c(CHCOOH)+c(CHCOO-),C正确;a点时盐酸和醋酸均抑制水的电离,b点时醋
3 2 3 3
酸抑制水的电离,c点时NH+
、CHCOO-的水解促进水的电离,d点时NH ·H O抑制水的电离,因此水
4 3 3 2
的电离程度最大的是c点,D错误。