文档内容
13.沉淀溶解平衡曲线及分析
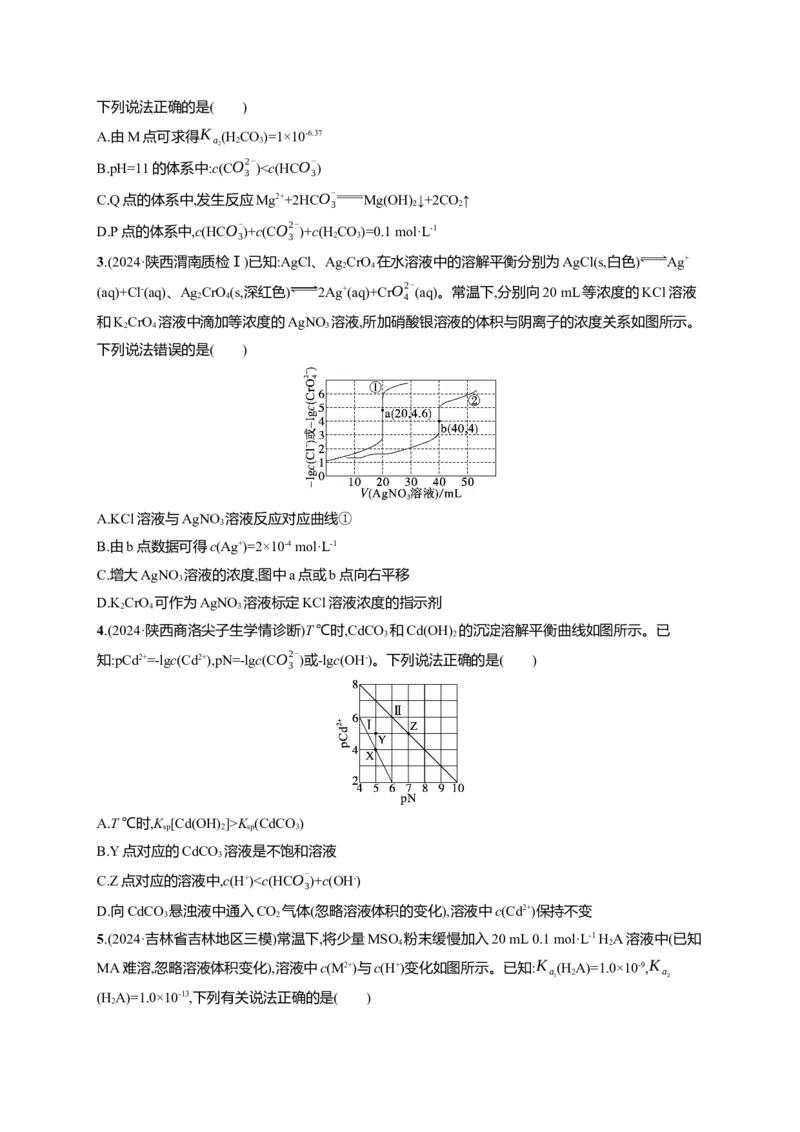
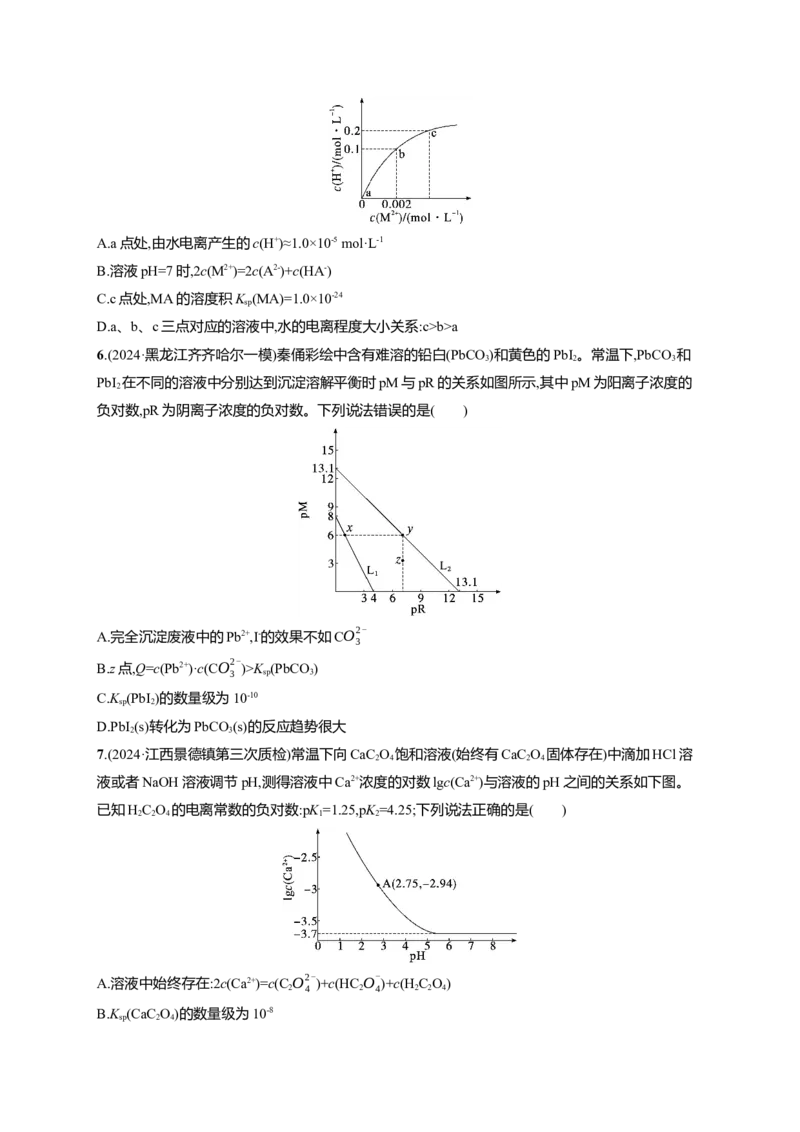
1.(2024·安徽黄山二模)室温下向含KSCN、KIO 和KCrO 的溶液中滴加AgNO 溶液,混合液中
3 2 4 3
pX{[pX=-lgc(X)],X=IO- 、SCN-、CrO2- }和pAg[pAg=-lgc(Ag+)]的关系如图所示,已知:
3 4
K (AgSCN)K (CdCO)
sp 2 sp 3
B.Y点对应的CdCO 溶液是不饱和溶液
3
C.Z点对应的溶液中,c(H+)b>a
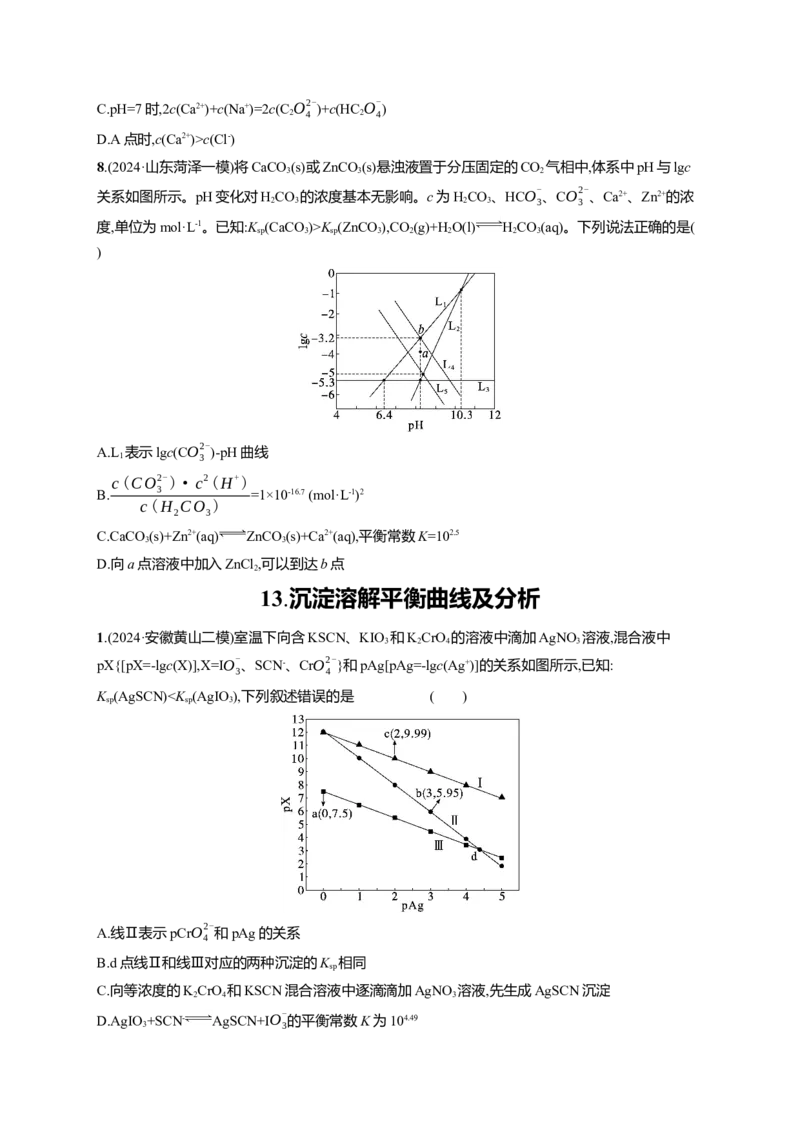
6.(2024·黑龙江齐齐哈尔一模)秦俑彩绘中含有难溶的铅白(PbCO )和黄色的PbI 。常温下,PbCO 和
3 2 3
PbI 在不同的溶液中分别达到沉淀溶解平衡时pM与pR的关系如图所示,其中pM为阳离子浓度的
2
负对数,pR为阴离子浓度的负对数。下列说法错误的是( )
A.完全沉淀废液中的Pb2+,I-的效果不如CO2-
3
B.z点,Q=c(Pb2+)·c(CO2-
)>K (PbCO )
3 sp 3
C.K (PbI )的数量级为10-10
sp 2
D.PbI (s)转化为PbCO (s)的反应趋势很大
2 3
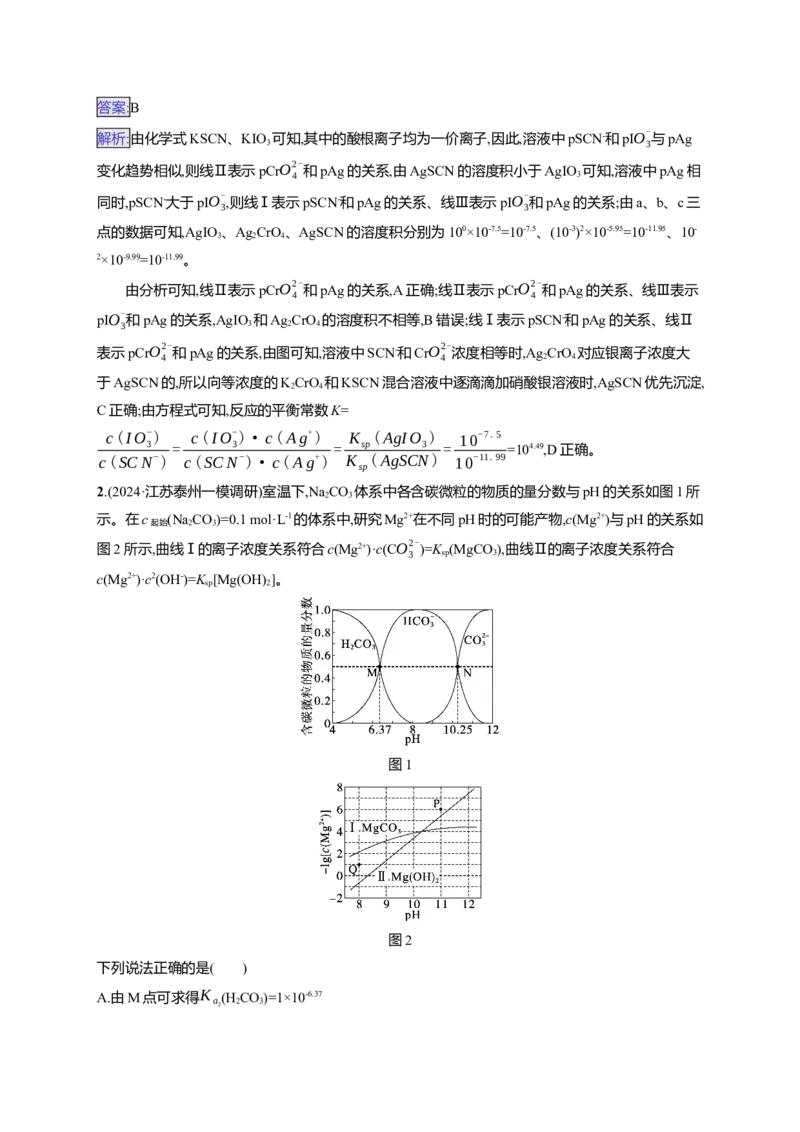
7.(2024·江西景德镇第三次质检)常温下向CaC O 饱和溶液(始终有CaC O 固体存在)中滴加HCl溶
2 4 2 4
液或者NaOH溶液调节pH,测得溶液中Ca2+浓度的对数lgc(Ca2+)与溶液的pH之间的关系如下图。
已知HC O 的电离常数的负对数:pK =1.25,pK =4.25;下列说法正确的是( )
2 2 4 1 2
A.溶液中始终存在:2c(Ca2+)=c(CO2- )+c(HCO-
)+c(H C O)
2 4 2 4 2 2 4
B.K (CaC O)的数量级为10-8
sp 2 4C.pH=7时,2c(Ca2+)+c(Na+)=2c(CO2- )+c(HCO-
)
2 4 2 4
D.A点时,c(Ca2+)>c(Cl-)
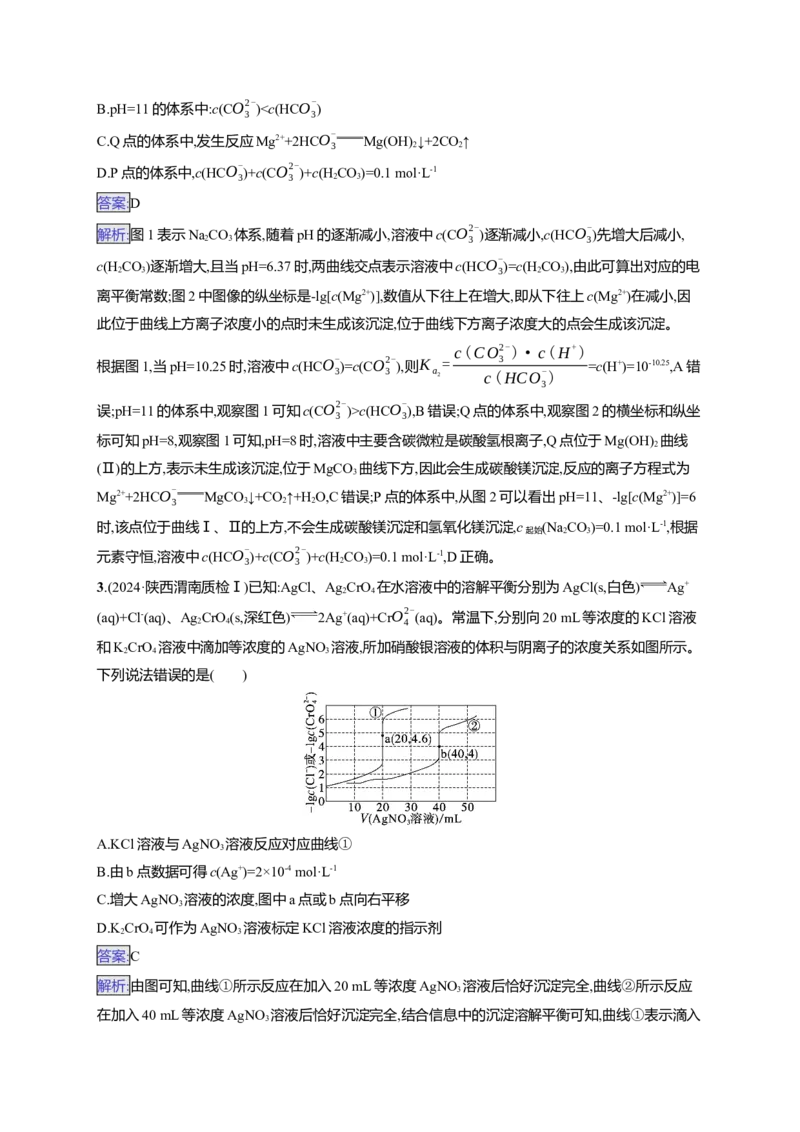
8.(2024·山东菏泽一模)将CaCO (s)或ZnCO (s)悬浊液置于分压固定的CO 气相中,体系中pH与lgc
3 3 2
关系如图所示。pH变化对HCO
的浓度基本无影响。c为HCO、HCO- 、CO2-
、Ca2+、Zn2+的浓
2 3 2 3 3 3
度,单位为mol·L-1。已知:K (CaCO)>K (ZnCO),CO (g)+HO(l) HCO(aq)。下列说法正确的是(
sp 3 sp 3 2 2 2 3
)
A.L
表示lgc(CO2-
)-pH曲线
1 3
c(CO2-)·c2(H+)
B. 3 =1×10-16.7 (mol·L-1)2
c(H CO )
2 3
C.CaCO (s)+Zn2+(aq) ZnCO (s)+Ca2+(aq),平衡常数K=102.5
3 3
D.向a点溶液中加入ZnCl,可以到达b点
2
13.沉淀溶解平衡曲线及分析
1.(2024·安徽黄山二模)室温下向含KSCN、KIO 和KCrO 的溶液中滴加AgNO 溶液,混合液中
3 2 4 3
pX{[pX=-lgc(X)],X=IO- 、SCN-、CrO2- }和pAg[pAg=-lgc(Ag+)]的关系如图所示,已知:
3 4
K (AgSCN)c(HCO-
),B错误;Q点的体系中,观察图2的横坐标和纵坐
3 3
标可知pH=8,观察图1可知,pH=8时,溶液中主要含碳微粒是碳酸氢根离子,Q点位于Mg(OH) 曲线
2
(Ⅱ)的上方,表示未生成该沉淀,位于MgCO 曲线下方,因此会生成碳酸镁沉淀,反应的离子方程式为
3
Mg2++2HCO-
MgCO ↓+CO ↑+H O,C错误;P点的体系中,从图2可以看出pH=11、-lg[c(Mg2+)]=6
3 3 2 2
时,该点位于曲线Ⅰ、Ⅱ的上方,不会生成碳酸镁沉淀和氢氧化镁沉淀,c (Na CO)=0.1 mol·L-1,根据
起始 2 3
元素守恒,溶液中c(HCO- )+c(CO2-
)+c(H CO)=0.1 mol·L-1,D正确。
3 3 2 3
3.(2024·陕西渭南质检Ⅰ)已知:AgCl、Ag CrO 在水溶液中的溶解平衡分别为AgCl(s,白色) Ag+
2 4
(aq)+Cl-(aq)、Ag CrO(s,深红色)
2Ag+(aq)+CrO2-
(aq)。常温下,分别向20 mL等浓度的KCl溶液
2 4 4
和KCrO 溶液中滴加等浓度的AgNO 溶液,所加硝酸银溶液的体积与阴离子的浓度关系如图所示。
2 4 3
下列说法错误的是( )
A.KCl溶液与AgNO 溶液反应对应曲线①
3
B.由b点数据可得c(Ag+)=2×10-4 mol·L-1
C.增大AgNO 溶液的浓度,图中a点或b点向右平移
3
D.KCrO 可作为AgNO 溶液标定KCl溶液浓度的指示剂
2 4 3
答案:C
解析:由图可知,曲线①所示反应在加入20 mL等浓度AgNO 溶液后恰好沉淀完全,曲线②所示反应
3
在加入40 mL等浓度AgNO 溶液后恰好沉淀完全,结合信息中的沉淀溶解平衡可知,曲线①表示滴入
3KCl溶液的变化曲线,曲线②表示滴入KCrO
溶液的变化曲线,根据b点计算:c(CrO2-
)=10-4 mol·L-1、
2 4 4
c(Ag+)=2×10-4 mol·L-1,K (Ag CrO)=(2×10-4)2×10-4=4×10-12,同理根据a点计算K (AgCl)=10-4.6×10-
sp 2 4 sp
4.6=10-9.2。由分析可知,KCl溶液与AgNO
溶液反应对应曲线①,A正确;b点c(CrO2-
)=10-4 mol·L-1,此
3 4
时恰好反应,结合沉淀溶解平衡可知,c(Ag+)=2×10-4 mol·L-1,B正确;增大AgNO 溶液的浓度,可使消耗
3
AgNO 溶液的体积减小,可实现图像中a点或b点向左平移,C错误;AgCl(s,白色)恰好沉淀时-
3
lgc(Cl-)=4.6,Ag
CrO(s,深红色)恰好沉淀时-lgc(CrO2-
)=4,Ag CrO 溶解能力稍大于AgCl,结合终点颜
2 4 4 2 4
色变化,可知KCrO 可作为AgNO 溶液标定KCl溶液浓度的指示剂,D正确。
2 4 3
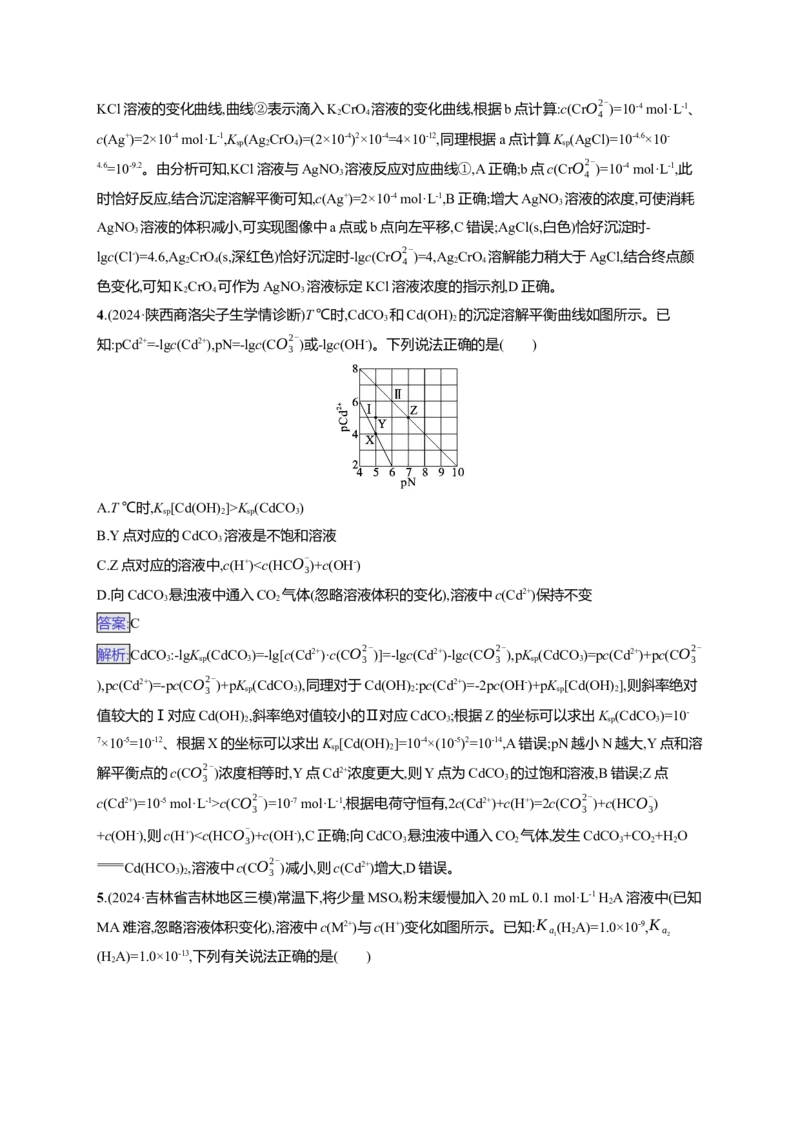
4.(2024·陕西商洛尖子生学情诊断)T ℃时,CdCO 和Cd(OH) 的沉淀溶解平衡曲线如图所示。已
3 2
知:pCd2+=-lgc(Cd2+),pN=-lgc(CO2-
)或-lgc(OH-)。下列说法正确的是( )
3
A.T ℃时,K [Cd(OH) ]>K (CdCO)
sp 2 sp 3
B.Y点对应的CdCO 溶液是不饱和溶液
3
C.Z点对应的溶液中,c(H+)c(CO2- )=10-7 mol·L-1,根据电荷守恒有,2c(Cd2+)+c(H+)=2c(CO2- )+c(HCO- )
3 3 3
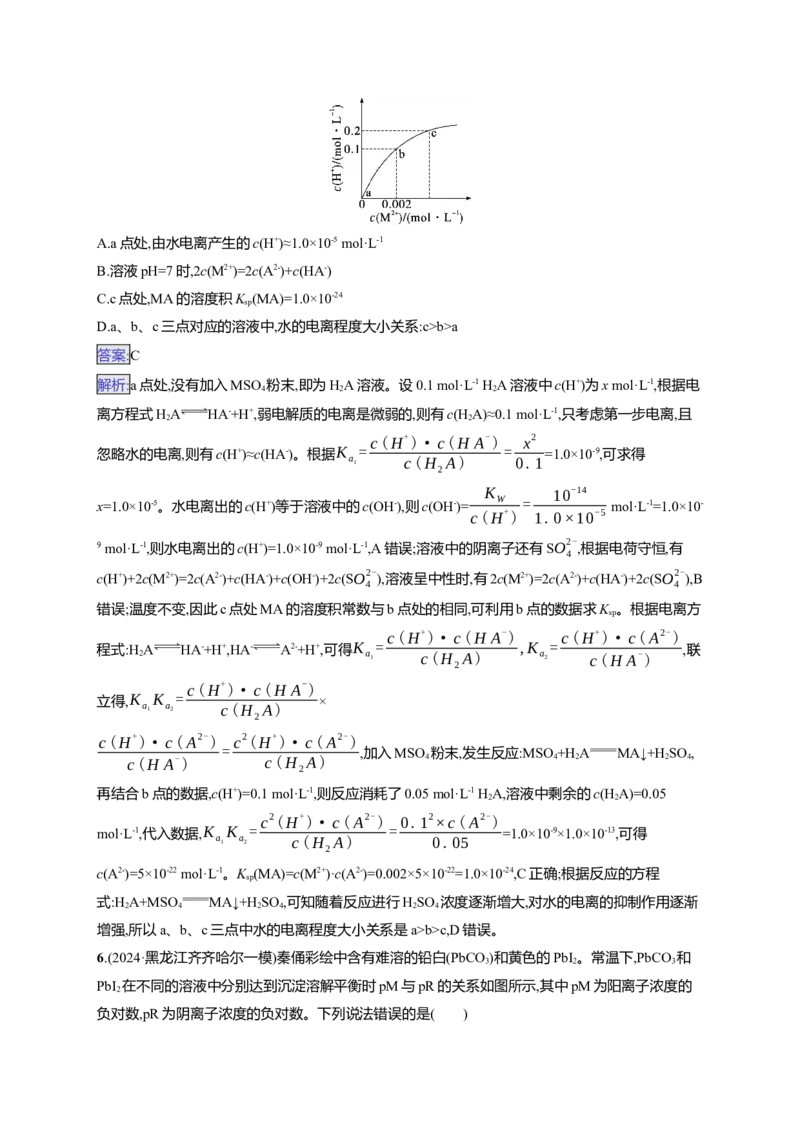
+c(OH-),则c(H+)b>a
答案:C
解析:a点处,没有加入MSO 粉末,即为HA溶液。设0.1 mol·L-1 H A溶液中c(H+)为x mol·L-1,根据电
4 2 2
离方程式HA HA-+H+,弱电解质的电离是微弱的,则有c(H A)≈0.1 mol·L-1,只考虑第一步电离,且
2 2
c(H+)·c(H A-) x2
忽略水的电离,则有c(H+)≈c(HA-)。根据K = = =1.0×10-9,可求得
a
1
c(H A) 0.1
2
K 10-14
x=1.0×10-5。水电离出的c(H+)等于溶液中的c(OH-),则c(OH-)= W = mol·L-1=1.0×10-
c(H+) 1.0×10-5
9 mol·L-1,则水电离出的c(H+)=1.0×10-9
mol·L-1,A错误;溶液中的阴离子还有SO2-
,根据电荷守恒,有
4
c(H+)+2c(M2+)=2c(A2-)+c(HA-)+c(OH-)+2c(SO2- ),溶液呈中性时,有2c(M2+)=2c(A2-)+c(HA-)+2c(SO2-
),B
4 4
错误;温度不变,因此c点处MA的溶度积常数与b点处的相同,可利用b点的数据求K 。根据电离方
sp
c(H+)·c(H A-) c(H+)·c(A2-)
程式:H A HA-+H+,HA- A2-+H+,可得K = ,K = ,联
2 a 1 c(H A) a 2 c(H A-)
2
c(H+)·c(H A-)
立得,K K = ×
a
1
a
2
c(H A)
2
c(H+)·c(A2-) c2(H+)·c(A2-)
= ,加入MSO 粉末,发生反应:MSO +H A MA↓+H SO ,
c(H A-) c(H A) 4 4 2 2 4
2
再结合b点的数据,c(H+)=0.1 mol·L-1,则反应消耗了0.05 mol·L-1 H A,溶液中剩余的c(H A)=0.05
2 2
c2(H+)·c(A2-) 0.12×c(A2-)
mol·L-1,代入数据,K K = = =1.0×10-9×1.0×10-13,可得
a
1
a
2
c(H A) 0.05
2
c(A2-)=5×10-22 mol·L-1。K (MA)=c(M2+)·c(A2-)=0.002×5×10-22=1.0×10-24,C正确;根据反应的方程
sp
式:H A+MSO MA↓+H SO ,可知随着反应进行HSO 浓度逐渐增大,对水的电离的抑制作用逐渐
2 4 2 4 2 4
增强,所以a、b、c三点中水的电离程度大小关系是a>b>c,D错误。
6.(2024·黑龙江齐齐哈尔一模)秦俑彩绘中含有难溶的铅白(PbCO )和黄色的PbI 。常温下,PbCO 和
3 2 3
PbI 在不同的溶液中分别达到沉淀溶解平衡时pM与pR的关系如图所示,其中pM为阳离子浓度的
2
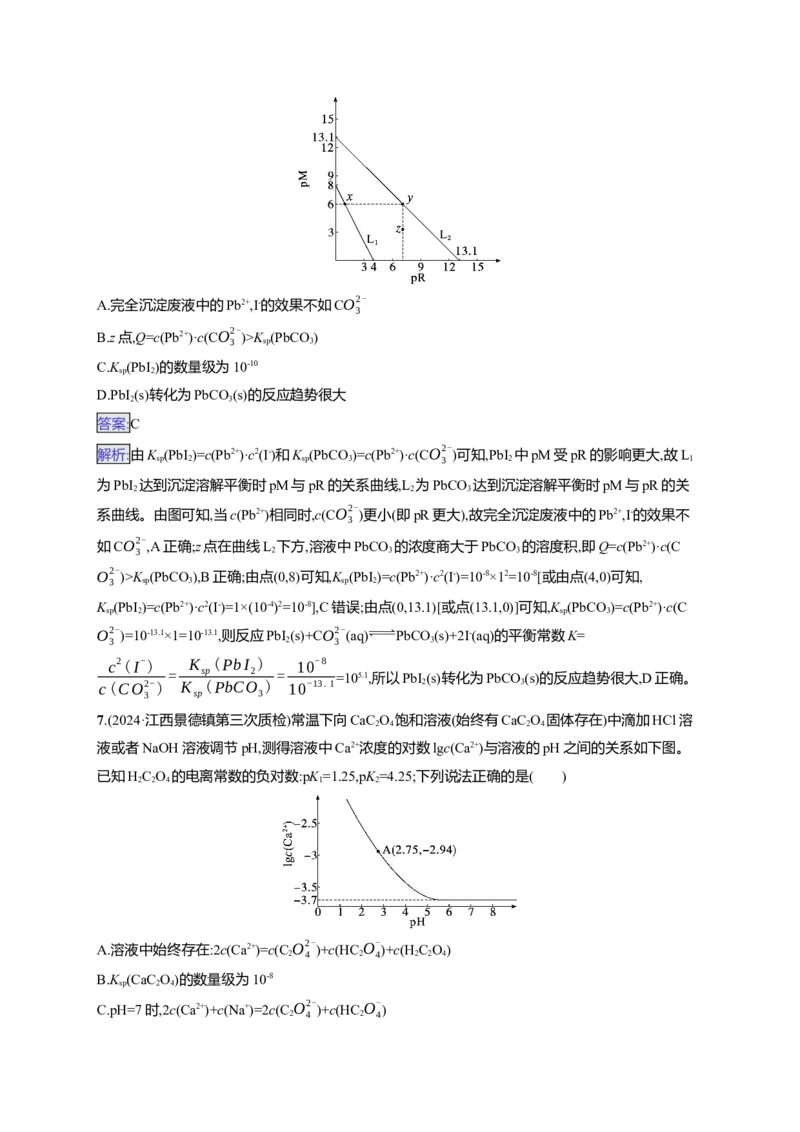
负对数,pR为阴离子浓度的负对数。下列说法错误的是( )A.完全沉淀废液中的Pb2+,I-的效果不如CO2-
3
B.z点,Q=c(Pb2+)·c(CO2-
)>K (PbCO )
3 sp 3
C.K (PbI )的数量级为10-10
sp 2
D.PbI (s)转化为PbCO (s)的反应趋势很大
2 3
答案:C
解析:由K (PbI )=c(Pb2+)·c2(I-)和K (PbCO
)=c(Pb2+)·c(CO2-
)可知,PbI 中pM受pR的影响更大,故L
sp 2 sp 3 3 2 1
为PbI 达到沉淀溶解平衡时pM与pR的关系曲线,L 为PbCO 达到沉淀溶解平衡时pM与pR的关
2 2 3
系曲线。由图可知,当c(Pb2+)相同时,c(CO2-
)更小(即pR更大),故完全沉淀废液中的Pb2+,I-的效果不
3
如CO2-
,A正确;z点在曲线L 下方,溶液中PbCO 的浓度商大于PbCO 的溶度积,即Q=c(Pb2+)·c(C
3 2 3 3
O2- )>K (PbCO ),B正确;由点(0,8)可知,K (PbI )=c(Pb2+)·c2(I-)=10-8×12=10-8[或由点(4,0)可知,
3 sp 3 sp 2
K (PbI )=c(Pb2+)·c2(I-)=1×(10-4)2=10-8],C错误;由点(0,13.1)[或点(13.1,0)]可知,K (PbCO )=c(Pb2+)·c(C
sp 2 sp 3
O2- )=10-13.1×1=10-13.1,则反应PbI (s)+CO2- (aq) PbCO (s)+2I-(aq)的平衡常数K=
3 2 3 3
c2(I-) K (PbI ) 10-8
= sp 2 = =105.1,所以PbI (s)转化为PbCO (s)的反应趋势很大,D正确。
c(CO2-) K (PbCO ) 10-13.1 2 3
3 sp 3
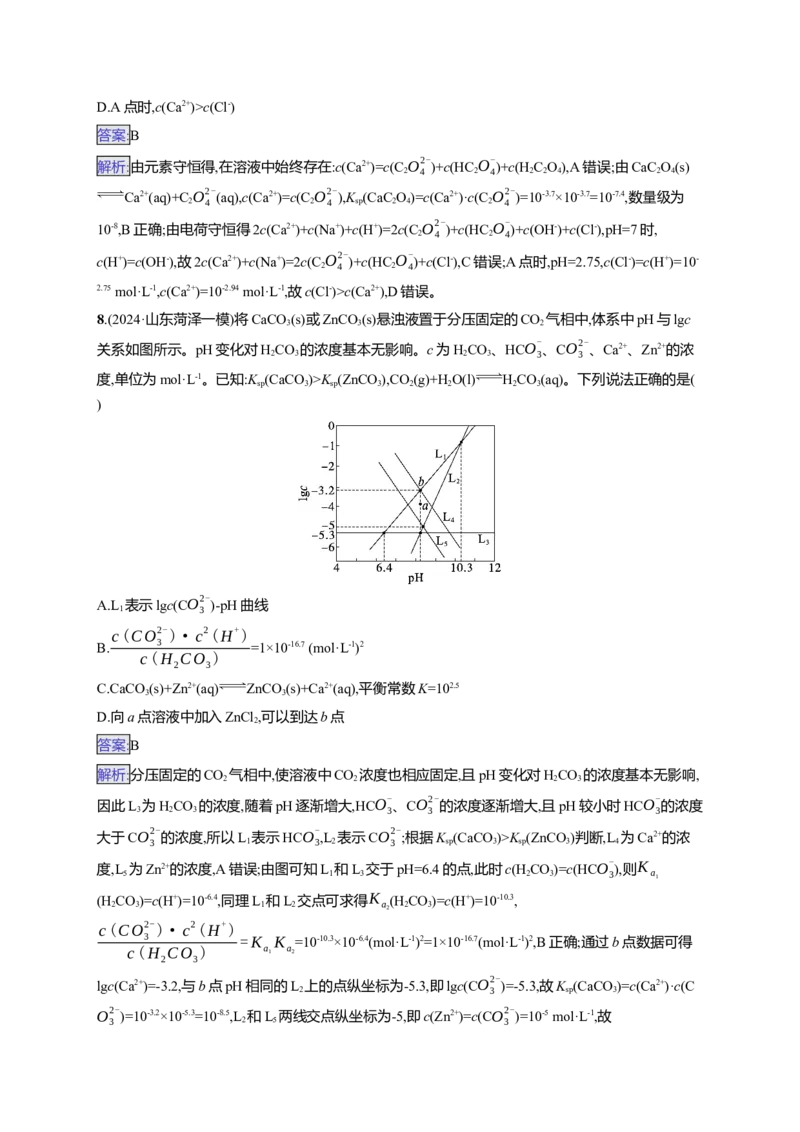
7.(2024·江西景德镇第三次质检)常温下向CaC O 饱和溶液(始终有CaC O 固体存在)中滴加HCl溶
2 4 2 4
液或者NaOH溶液调节pH,测得溶液中Ca2+浓度的对数lgc(Ca2+)与溶液的pH之间的关系如下图。
已知HC O 的电离常数的负对数:pK =1.25,pK =4.25;下列说法正确的是( )
2 2 4 1 2
A.溶液中始终存在:2c(Ca2+)=c(CO2- )+c(HCO-
)+c(H C O)
2 4 2 4 2 2 4
B.K (CaC O)的数量级为10-8
sp 2 4
C.pH=7时,2c(Ca2+)+c(Na+)=2c(CO2- )+c(HCO-
)
2 4 2 4D.A点时,c(Ca2+)>c(Cl-)
答案:B
解析:由元素守恒得,在溶液中始终存在:c(Ca2+)=c(CO2- )+c(HCO-
)+c(H C O),A错误;由CaC O(s)
2 4 2 4 2 2 4 2 4
Ca2+(aq)+CO2- (aq),c(Ca2+)=c(C O2- ),K (CaC O)=c(Ca2+)·c(CO2- )=10-3.7×10-3.7=10-7.4,数量级为
2 4 2 4 sp 2 4 2 4
10-8,B正确;由电荷守恒得2c(Ca2+)+c(Na+)+c(H+)=2c(CO2- )+c(HCO-
)+c(OH-)+c(Cl-),pH=7时,
2 4 2 4
c(H+)=c(OH-),故2c(Ca2+)+c(Na+)=2c(CO2- )+c(HCO-
)+c(Cl-),C错误;A点时,pH=2.75,c(Cl-)=c(H+)=10-
2 4 2 4
2.75 mol·L-1,c(Ca2+)=10-2.94 mol·L-1,故c(Cl-)>c(Ca2+),D错误。
8.(2024·山东菏泽一模)将CaCO (s)或ZnCO (s)悬浊液置于分压固定的CO 气相中,体系中pH与lgc
3 3 2
关系如图所示。pH变化对HCO
的浓度基本无影响。c为HCO、HCO- 、CO2-
、Ca2+、Zn2+的浓
2 3 2 3 3 3
度,单位为mol·L-1。已知:K (CaCO)>K (ZnCO),CO (g)+HO(l) HCO(aq)。下列说法正确的是(
sp 3 sp 3 2 2 2 3
)
A.L
表示lgc(CO2-
)-pH曲线
1 3
c(CO2-)·c2(H+)
B. 3 =1×10-16.7 (mol·L-1)2
c(H CO )
2 3
C.CaCO (s)+Zn2+(aq) ZnCO (s)+Ca2+(aq),平衡常数K=102.5
3 3
D.向a点溶液中加入ZnCl,可以到达b点
2
答案:B
解析:分压固定的CO 气相中,使溶液中CO 浓度也相应固定,且pH变化对HCO 的浓度基本无影响,
2 2 2 3
因此L 为HCO
的浓度,随着pH逐渐增大,HCO- 、CO2- 的浓度逐渐增大,且pH较小时HCO-
的浓度
3 2 3 3 3 3
大于CO2-
的浓度,所以L
表示HCO-
,L
表示CO2-
;根据K (CaCO)>K (ZnCO)判断,L 为Ca2+的浓
3 1 3 2 3 sp 3 sp 3 4
度,L 为Zn2+的浓度,A错误;由图可知L 和L 交于pH=6.4的点,此时c(H CO)=c(HCO- ),则 K
5 1 3 2 3 3 a 1
(H CO)=c(H+)=10-6.4,同理L 和L 交点可求得 K (H CO)=c(H+)=10-10.3,
2 3 1 2 a 2 3
2
c(CO2-)·c2(H+)
3 =K K =10-10.3×10-6.4(mol·L-1)2=1×10-16.7(mol·L-1)2,B正确;通过b点数据可得
c(H CO ) a 1 a 2
2 3
lgc(Ca2+)=-3.2,与b点pH相同的L
上的点纵坐标为-5.3,即lgc(CO2-
)=-5.3,故K (CaCO)=c(Ca2+)·c(C
2 3 sp 3
O2- )=10-3.2×10-5.3=10-8.5,L 和L 两线交点纵坐标为-5,即c(Zn2+)=c(CO2- )=10-5 mol·L-1,故
3 2 5 3K (ZnCO)=c(Zn2+)·c(CO2- )=10-10,根据CaCO (s)+Zn2+(aq) ZnCO (s)+Ca2+(aq),K=
sp 3 3 3 3
K (CaCO ) 10-8.5
sp 3 = =101.5,C错误;b为L 和L 交点,向a点溶液中加入CaCl 可以到达b点,D错
K (ZnCO ) 10-10 1 4 2
sp 3
误。