文档内容
第 18 讲 卤族元素 溴、碘单质的提取
[复习目标] 1.掌握卤素单质的性质及卤素离子的检验。2.掌握卤素单质的提取。
考点 卤素单质的性质及 X-的检验
1.卤族元素
卤族元素又称卤素,位于元素周期表的第ⅦA族,价层电子排布式为ns2np5。
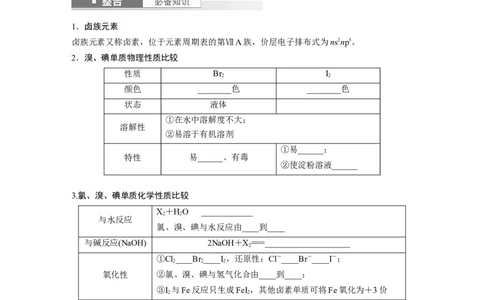
2.溴、碘单质物理性质比较
性质 Br I
2 2
颜色 ________色 ________色
状态 液体
①在水中溶解度不大;
溶解性
②易溶于有机溶剂
①易______;
特性 易______、有毒
②使淀粉溶液______
3.氯、溴、碘单质化学性质比较
X+HO____________
2 2
与水反应
氯、溴、碘与水反应由____到____
与碱反应(NaOH) 2NaOH+X===____________________
2
①Cl____Br ____I,还原性:Cl-____Br-____I-;
2 2 2
氧化性 ②氯、溴、碘与氢气化合由____到____;
③I 与Fe反应只生成FeI,其他卤素单质可将Fe氧化为+3价
2 2
4.氟的特殊性
(1)氟无正化合价。
(2)F 能与水反应放出O,化学方程式:____________________________________________
2 2
_______________________________________________________________________________
。
(3)在HX中,HF的熔、沸点最高,氢氟酸是弱酸,能腐蚀玻璃。
5.卤素离子的检验方法
(1)AgNO 溶液——沉淀法
3未知液―――――→生成
(2)置换——萃取法
未知液――――――――→ ―――――――――――→有机层呈
(3)氧化——淀粉法检验I-
未知液――――――――――――――→ ――――→____色溶液,表明有I-
[应用举例]
鉴别NaCl溶液、NaBr溶液、NaI溶液可以选用的试剂是________(填序号)。
①碘水、淀粉溶液 ②氯水、CCl
4
③溴水、苯 ④硝酸、AgNO 溶液
3
⑤氯水、苯 ⑥CCl 、淀粉溶液
4
1.卤素气态氢化物的水溶液都是强酸溶液( )
2.浓HSO 能干燥HCl,所以浓硫酸也能干燥HBr( )
2 4
3.加碘盐能使淀粉变蓝( )
4.清洗碘升华实验所用试管的操作是先用酒精清洗,再用水清洗( )
5.液溴易挥发,存放液溴的试剂瓶中应加水封( )
6.用加热的方法可将NaHCO 中混有的少量碘除去( )
3
7.可用F 与NaCl溶液反应产生Cl,验证F 的氧化性大于Cl( )
2 2 2 2
一、卤素性质的递变规律
1.下列有关卤素的说法错误的是( )
A.从HF、HCl、HBr、HI酸性递增的事实,可推出F、Cl、Br、I的非金属性递增的规律
B.HF、HCl、HBr、HI的热稳定性依次减弱,还原性依次增强
C.单质的颜色随核电荷数的增加而加深
D.碘在碘化钾溶液中的溶解度大于在纯水中的溶解度
2.(2024·合肥模拟)向KBr、KI混合溶液中依次加入少量氯水和CCl ,振荡后静置,可观察
4
到溶液分层,下层呈紫红色。下列有关说法正确的是( )
A.元素Br在周期表中位于第三周期第ⅦA族
B.简单阴离子的半径:r(Cl-)Br >I
2 2 2
二、拟卤素和卤素互化物的结构与性质
3.氰[(CN) ]的结构简式为N≡C—C≡N,其化学性质与卤素(X )很相似,化学上称之为拟
2 2卤素,其氧化性介于Br 和I 之间。
2 2
(1)写出(CN) 的电子式:_________________________________________________________。
2
(2)写出(CN) 在常温下与烧碱溶液反应的化学方程式:________________________________。
2
(3)在 KBr、KI、KCN 的混合溶液中通入少量氯气,发生反应的离子方程式为
_______________________________________________________________________________
________________________________________________________________________。
4.一氯化碘(ICl)、三氯化碘(ICl )是卤素互化物,它们的性质与卤素单质相似。
3
(1)ICl 与水反应的产物可能为___________________________________________________(填
3
化学式)。
(2)ICl在常温下与烧碱溶液反应的离子方程式为_____________________________________,
该反应是否是氧化还原反应?____________(填“是”或“否”)。
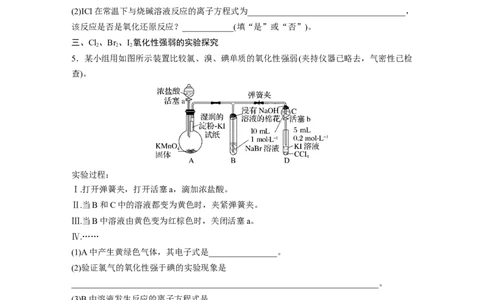
三、Cl、Br 、I 氧化性强弱的实验探究
2 2 2
5.某小组用如图所示装置比较氯、溴、碘单质的氧化性强弱(夹持仪器已略去,气密性已检
查)。
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为红棕色时,关闭活塞a。
Ⅳ.……
(1)A中产生黄绿色气体,其电子式是________________。
(2)验证氯气的氧化性强于碘的实验现象是
________________________________________________________________________。
(3)B中溶液发生反应的离子方程式是_______________________________________________
_______________________________________________________________________________
。
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是_________________________________
_______________________________________________________________________________
。
(5)过程Ⅲ实验的目的是___________________________________________________________
_______________________________________________________________________________
。(6) 氯 、 溴 、 碘 单 质 的 氧 化 性 逐 渐 减 弱 的 原 因 : 同 主 族 元 素 从 上 到 下 ,
_______________________________________________________________________________,
得电子能力逐渐减弱。
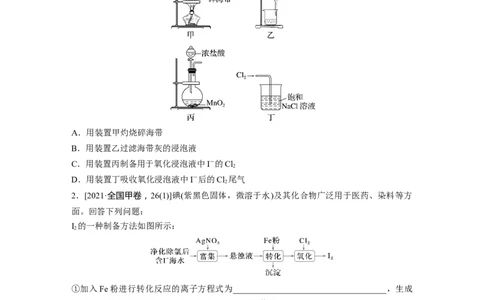
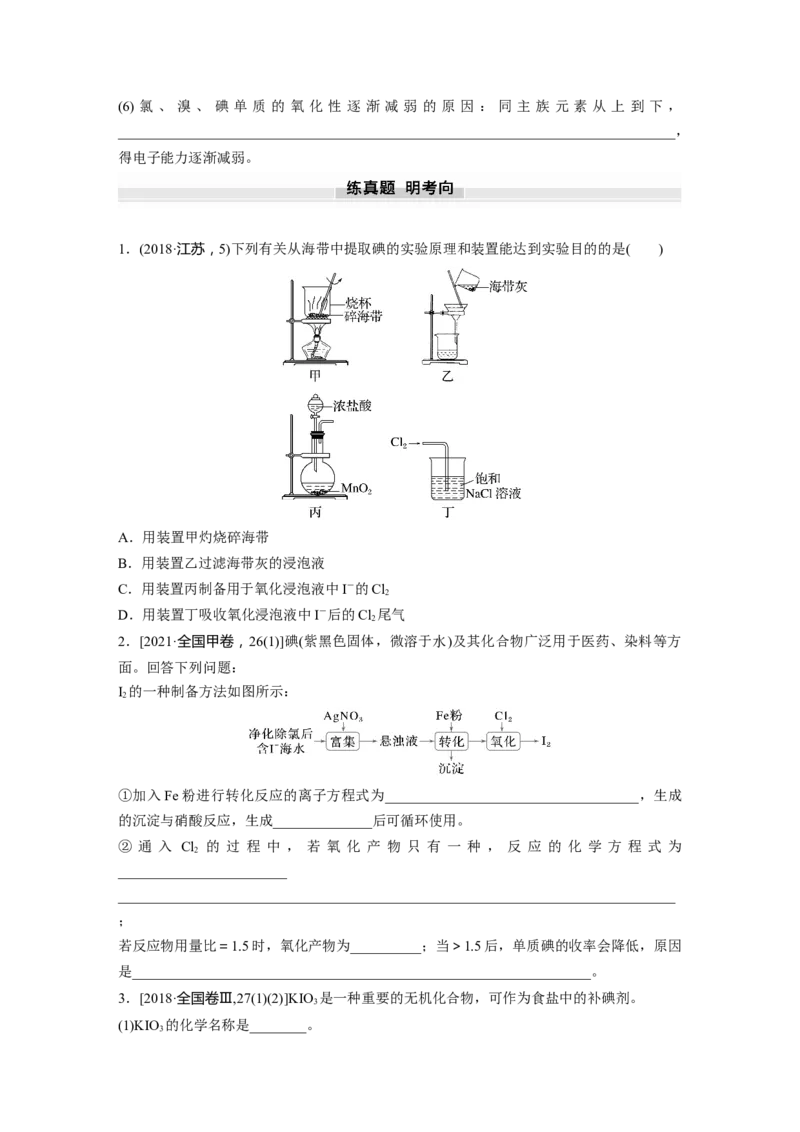
1.(2018·江苏,5)下列有关从海带中提取碘的实验原理和装置能达到实验目的的是( )
A.用装置甲灼烧碎海带
B.用装置乙过滤海带灰的浸泡液
C.用装置丙制备用于氧化浸泡液中I-的Cl
2
D.用装置丁吸收氧化浸泡液中I-后的Cl 尾气
2
2.[2021·全国甲卷,26(1)]碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方
面。回答下列问题:
I 的一种制备方法如图所示:
2
①加入Fe粉进行转化反应的离子方程式为____________________________________,生成
的沉淀与硝酸反应,生成______________后可循环使用。
② 通 入 Cl 的 过 程 中 , 若 氧 化 产 物 只 有 一 种 , 反 应 的 化 学 方 程 式 为
2
________________________
_______________________________________________________________________________
;
若反应物用量比=1.5时,氧化产物为__________;当>1.5后,单质碘的收率会降低,原因
是_________________________________________________________________。
3.[2018·全国卷Ⅲ,27(1)(2)]KIO 是一种重要的无机化合物,可作为食盐中的补碘剂。
3
(1)KIO 的化学名称是________。
3(2)利用“KClO 氧化法”制备KIO 工艺流程如下图所示:
3 3
“ 酸 化 反 应 ” 所 得 产 物 有 KH(IO) 、 Cl 和 KCl 。 “ 逐 Cl” 采 用 的 方 法 是
3 2 2 2
__________________。“滤液”中的溶质主要是__________。“调pH”中发生反应的化学
方程式为________________________________________________________________________
_______________________________________________________________________________
。