文档内容
第 17 讲 氯及其重要化合物的转化关系
[复习目标] 掌握氯及其化合物的转化关系及条件。
1.在氯及其化合物的“价—类”二维图中填充 Cl 、HCl、NaCl、HClO、NaClO、
2
Ca(ClO) 。
2
2.完成上述转化关系中①~⑧的化学方程式(合理即可)。
①MnO +4HCl(浓)=====MnCl +Cl↑+2HO;
2 2 2 2
②Cl+HOHCl+HClO;
2 2
③2Cl+2Ca(OH) ===CaCl +Ca(ClO) +2HO;
2 2 2 2 2
④NaClO+2HCl===NaCl+Cl↑+HO;
2 2
⑤2HClO=====2HCl+O↑;
2
⑥2NaCl+2HO=====2NaOH+H↑+Cl↑;
2 2 2
⑦2Fe+3Cl=====2FeCl ;
2 3
⑧2FeCl +Cl===2FeCl 。
2 2 3
一、制取Cl 并探究其与碱在不同温度下的反应产物
2
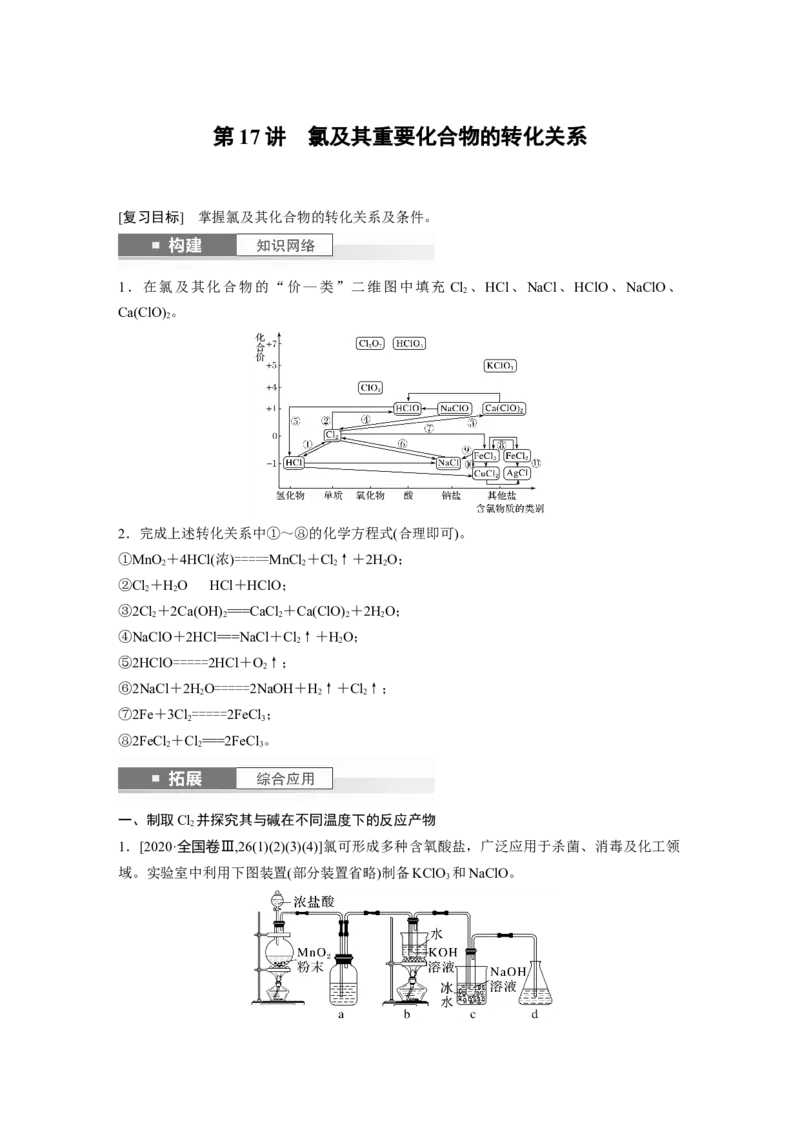
1.[2020·全国卷Ⅲ,26(1)(2)(3)(4)]氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领
域。实验室中利用下图装置(部分装置省略)制备KClO 和NaClO。
3回答下列问题:
(1)盛放MnO 粉末的仪器名称是__________,a中的试剂为__________。
2
(2)b 中 采 用 的 加 热 方 式 是 __________ , c 中 化 学 反 应 的 离 子 方 程 式 是
_____________________,
采用冰水浴冷却的目的是_________________________________________________________。
(3)d的作用是________________,可选用试剂________(填标号)。
A.NaS B.NaCl
2
C.Ca(OH) D.HSO
2 2 4
(4)反应结束后,取出b中试管,经冷却结晶,________,__________________,干燥,得
到KClO 晶体。
3
答案 (1)圆底烧瓶 饱和食盐水
(2)水浴加热 Cl+2OH-===ClO-+Cl-+HO 避免生成NaClO (3)吸收尾气(Cl ) AC
2 2 3 2
(4)过滤 少量(冷)水洗涤
解析 由题干信息及装置图分析各装置的作用,a装置用于除杂,b装置用于制备氯酸钾,c
装置用于制备次氯酸钠,d装置用于尾气处理。(2)b装置的加热方式为水浴加热。c装置中
氯气与氢氧化钠发生反应的离子方程式为Cl +2OH-===ClO-+Cl-+HO。根据b、c装置
2 2
水浴温度的不同推知,生成氯酸盐时需要酒精灯加热,生成次氯酸盐时需要冰水冷却,所以
c中冰水浴的目的是避免氯酸钠的生成。(3)d是尾气处理装置,吸收氯气可以用硫化钠溶液
或氢氧化钙浊液。(4)从溶液中获得纯净氯酸钾的操作是冷却结晶,过滤,少量冷水洗涤,
干燥,此处用少量冷水洗涤的目的是降低氯酸钾的损耗。
二、其他含氯化合物的制备
2.(2020·山东等级模拟考,10)亚氯酸钠(NaClO)是一种高效的漂白剂和氧化剂,可用于各
2
种纤维和某些食品的漂白。马蒂逊(Mathieson)法制备亚氯酸钠的流程如下:
下列说法错误的是( )
A.反应①阶段,参加反应的NaClO 和SO 的物质的量之比为2∶1
3 2
B.若反应①通过原电池来实现,则ClO 是正极产物
2
C.反应②中的HO 可用NaClO 代替
2 2 4
D.反应②条件下,ClO 的氧化性大于 HO
2 2 2
答案 C
解析 根据流程知,反应①中氧化剂是NaClO ,还原剂是SO ,还原产物是ClO ,氧化产
3 2 2
物是 NaHSO ,根据化合价升降相等可得参加反应的 NaClO 和 SO 的物质的量之比为
4 3 22∶1,A项正确;由反应①化合价变化情况,再根据原电池正极发生还原反应,所以 ClO
2
是正极产物,B项正确;据反应②,在ClO 与HO 的反应中,ClO 转化为NaClO ,氯元素
2 2 2 2 2
的化合价降低,作氧化剂,HO 只能作还原剂,氧元素的化合价升高,不能用 NaClO 代替
2 2 4
HO,且可以推出ClO 的氧化性大于HO,C项错误,D项正确。
2 2 2 2 2
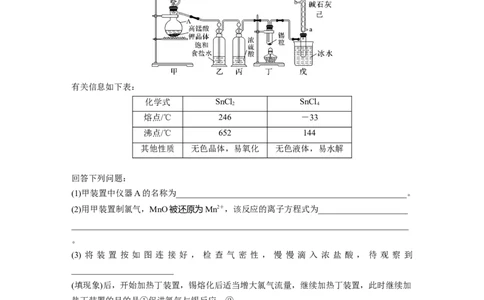
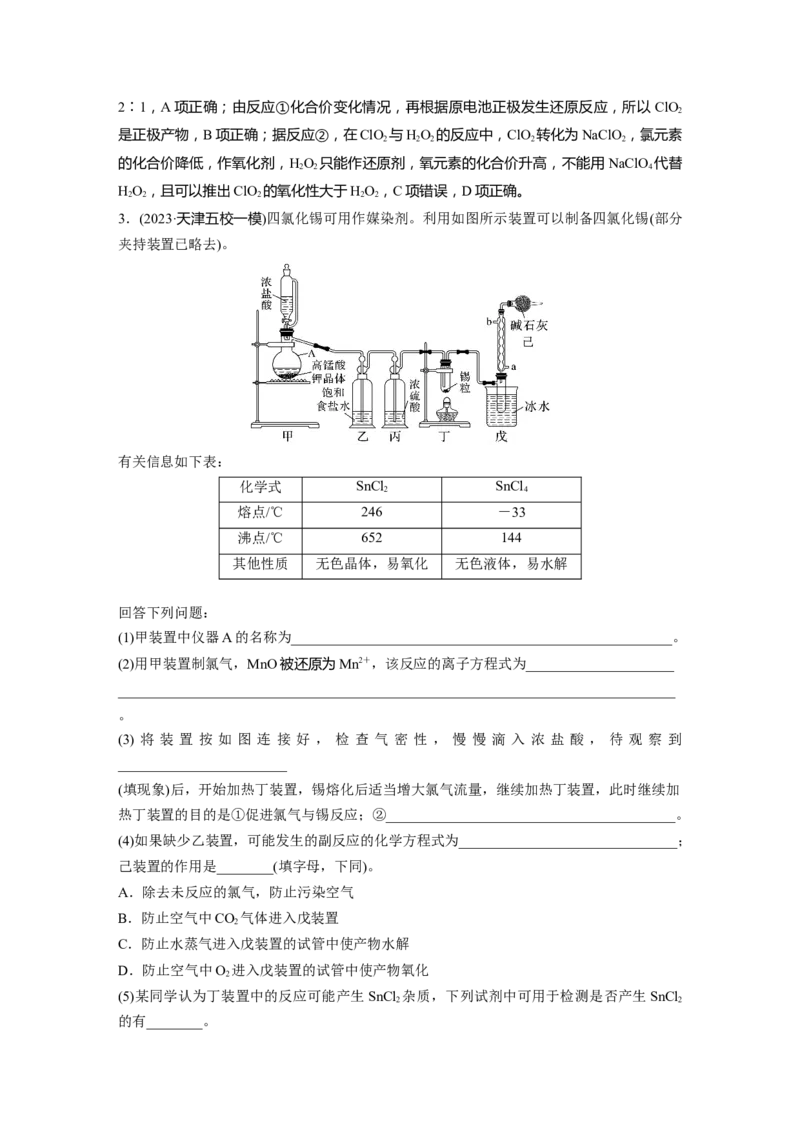
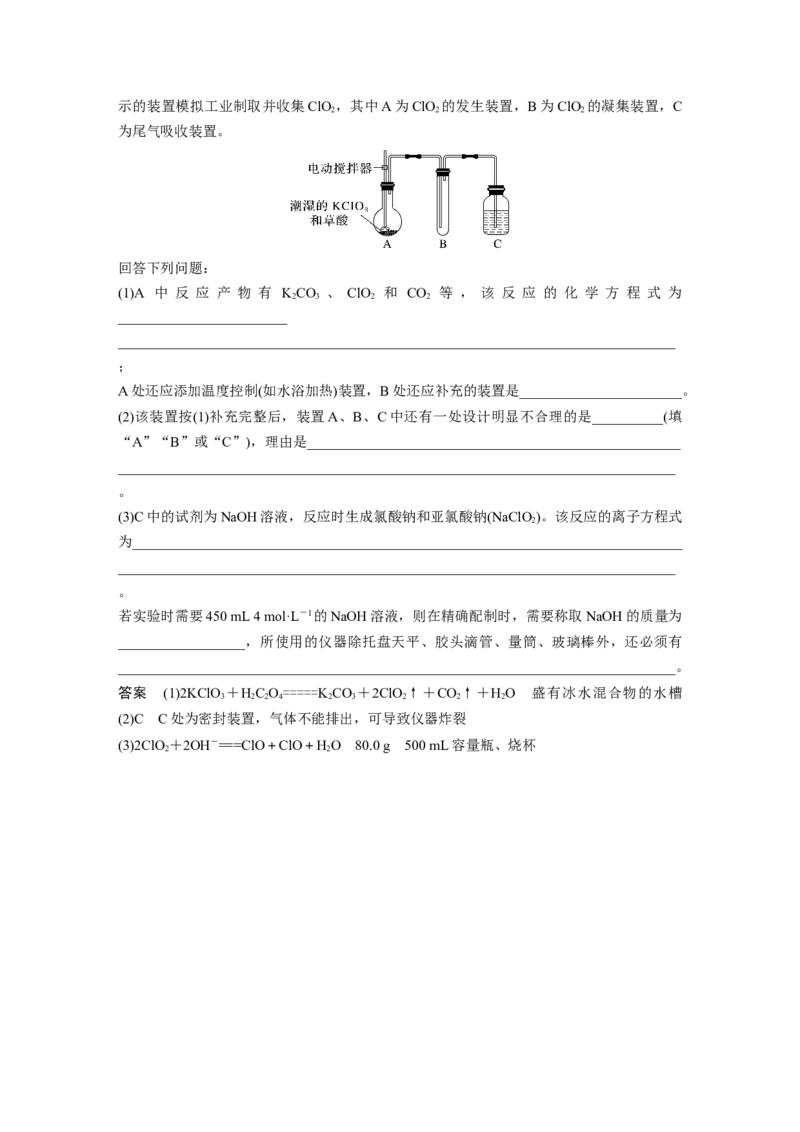
3.(2023·天津五校一模)四氯化锡可用作媒染剂。利用如图所示装置可以制备四氯化锡(部分
夹持装置已略去)。
有关信息如下表:
化学式 SnCl SnCl
2 4
熔点/℃ 246 -33
沸点/℃ 652 144
其他性质 无色晶体,易氧化 无色液体,易水解
回答下列问题:
(1)甲装置中仪器A的名称为______________________________________________________。
(2)用甲装置制氯气,MnO被还原为Mn2+,该反应的离子方程式为_____________________
_______________________________________________________________________________
。
(3) 将 装 置 按 如 图 连 接 好 , 检 查 气 密 性 , 慢 慢 滴 入 浓 盐 酸 , 待 观 察 到
________________________
(填现象)后,开始加热丁装置,锡熔化后适当增大氯气流量,继续加热丁装置,此时继续加
热丁装置的目的是①促进氯气与锡反应;②_________________________________________。
(4)如果缺少乙装置,可能发生的副反应的化学方程式为_______________________________;
己装置的作用是________(填字母,下同)。
A.除去未反应的氯气,防止污染空气
B.防止空气中CO 气体进入戊装置
2
C.防止水蒸气进入戊装置的试管中使产物水解
D.防止空气中O 进入戊装置的试管中使产物氧化
2
(5)某同学认为丁装置中的反应可能产生SnCl 杂质,下列试剂中可用于检测是否产生SnCl
2 2
的有________。A.HO 溶液
2 2
B.FeCl 溶液(滴有KSCN)
3
C.AgNO 溶液
3
D.溴水
(6)反应中用去锡粒1.19 g,反应后在戊装置的试管中收集到2.38 g SnCl ,则SnCl 的产率为
4 4
________(结果保留3位有效数字)。
答案 (1)蒸馏烧瓶 (2)2MnO+10Cl-+16H+===2Mn2++5Cl↑+8HO (3)丁装置内充满
2 2
黄绿色气体 使SnCl 汽化,利于从混合物中分离出来 (4)Sn+2HCl===SnCl +H↑ AC
4 2 2
(5)BD (6)91.2%
解析 (3)整个装置中充满氯气,即丁装置充满黄绿色气体时,再加热熔化锡粒生成SnCl ,
4
继续加热丁装置,促进氯气与锡反应,使生成的SnCl 汽化,有利于从混合物中分离出来,
4
便于在戊装置处冷却收集。(4)碱石灰能吸收二氧化碳,但二氧化碳对反应没有影响,故 B
不符合;即使有O 进入,O 能氧化丁中生成的副产物SnCl ,但不会氧化戊装置试管中的产
2 2 2
物SnCl ,故D不符合。(5)H O 溶液能氧化SnCl ,同时双氧水被还原生成水,但是没有明
4 2 2 2
显现象,无法检验,故A错误;FeCl 溶液(滴有KSCN)呈红色,氯化铁氧化SnCl ,铁离子
3 2
被还原生成亚铁离子,溶液褪色,可以检验,故B正确;AgNO 溶液能检验氯离子,但是
3
不能检验Sn2+,故C错误;溴水氧化SnCl ,溴被还原生成溴离子,溶液褪色,可以检验,
2
故D正确。(6)用去锡粒1.19 g,其物质的量为=0.01 mol,根据Sn原子守恒可知生成SnCl
4
0.01 mol,则SnCl 的产率为×100%≈91.2%。
4
课时精练
1.氯及含氯物质在生产、生活中具有广泛的应用。下列含氯物质的转化正确的是( )
A.漂白粉――→HClO(aq)――→Cl(g)
2
B.MgCl (aq)――→无水MgCl ――→Mg
2 2
C.Cu――→CuCl ――→CuCl
2
D.NaCl(aq)――→NaHCO (s)――→NaCO(s)
3 2 3
答案 C
解析 HClO见光分解生成O,2HClO=====2HCl+O↑,A错误;加热MgCl 溶液时,会促
2 2 2
进Mg2+水解生成Mg(OH) ,得不到无水MgCl ,B错误;发生反应2FeCl +Cu===CuCl +
2 2 3 2
2FeCl 、2CuCl +NaSO +HO===2CuCl↓+NaSO +2HCl,C正确;先将NH 通入饱和
2 2 2 3 2 2 4 3
NaCl溶液中,再通入CO 才可制得NaHCO 晶体,D错误。
2 3
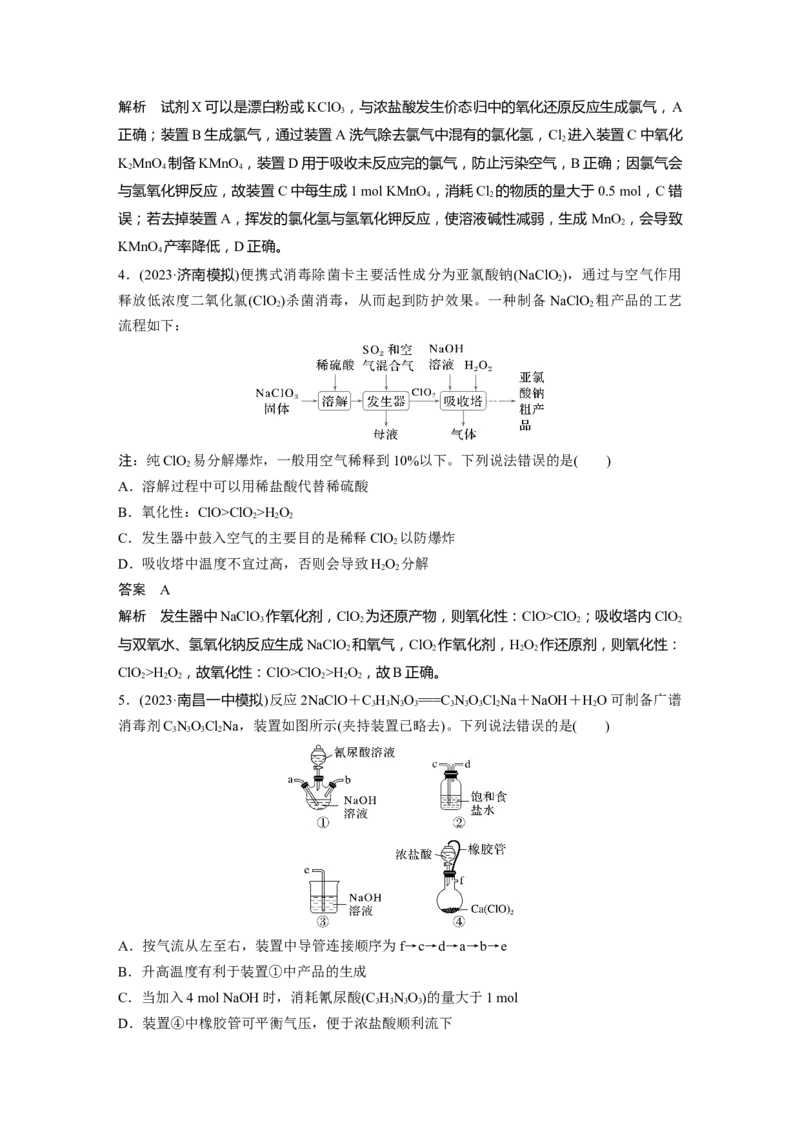
2.(2023·广东惠州模拟)部分含氯物质的分类与相应化合价关系如图所示。下列推断不合理
的是( )A.常温下,a、d水溶液的pH:aClO >H O
2 2 2
C.发生器中鼓入空气的主要目的是稀释ClO 以防爆炸
2
D.吸收塔中温度不宜过高,否则会导致HO 分解
2 2
答案 A
解析 发生器中NaClO 作氧化剂,ClO 为还原产物,则氧化性:ClO>ClO ;吸收塔内ClO
3 2 2 2
与双氧水、氢氧化钠反应生成NaClO 和氧气,ClO 作氧化剂,HO 作还原剂,则氧化性:
2 2 2 2
ClO >H O,故氧化性:ClO>ClO >H O,故B正确。
2 2 2 2 2 2
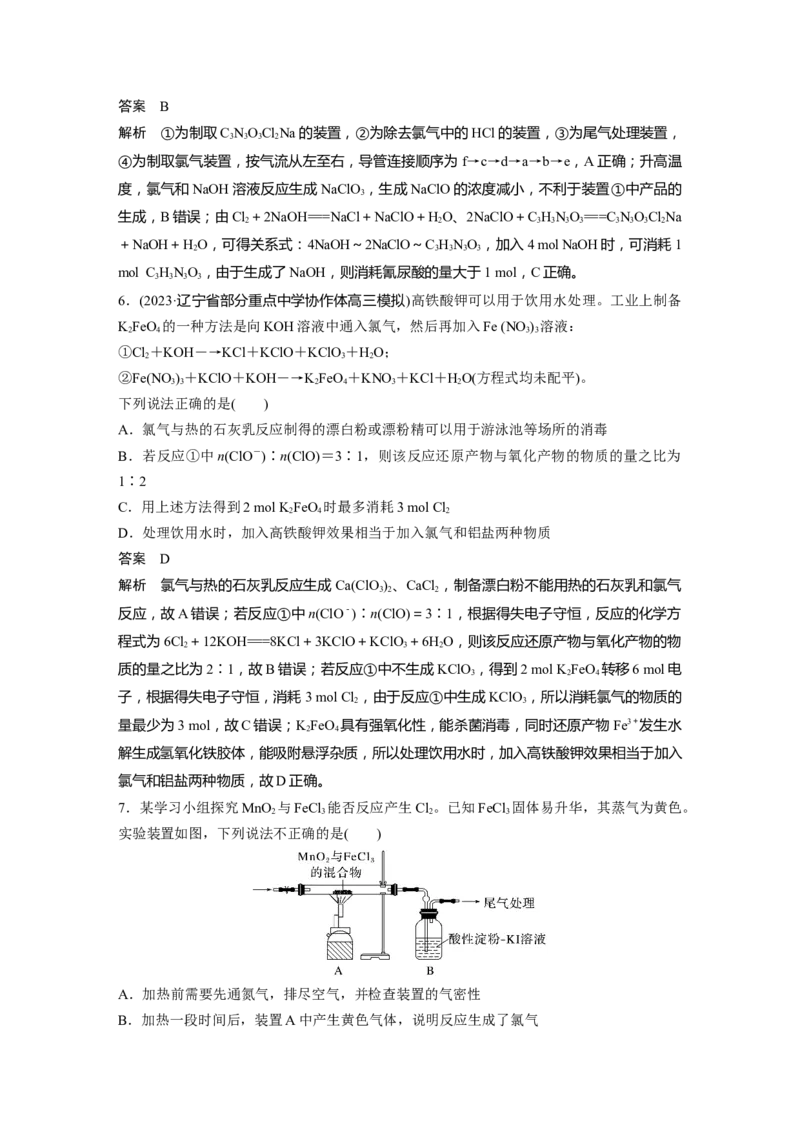
5.(2023·南昌一中模拟)反应2NaClO+C HNO===C NOClNa+NaOH+HO可制备广谱
3 3 3 3 3 3 3 2 2
消毒剂C NOClNa,装置如图所示(夹持装置已略去)。下列说法错误的是( )
3 3 3 2
A.按气流从左至右,装置中导管连接顺序为f→c→d→a→b→e
B.升高温度有利于装置①中产品的生成
C.当加入4 mol NaOH时,消耗氰尿酸(C HNO)的量大于1 mol
3 3 3 3
D.装置④中橡胶管可平衡气压,便于浓盐酸顺利流下答案 B
解析 ①为制取C NOClNa的装置,②为除去氯气中的HCl的装置,③为尾气处理装置,
3 3 3 2
④为制取氯气装置,按气流从左至右,导管连接顺序为f→c→d→a→b→e,A正确;升高温
度,氯气和NaOH溶液反应生成NaClO ,生成NaClO的浓度减小,不利于装置①中产品的
3
生成,B错误;由Cl+2NaOH===NaCl+NaClO+HO、2NaClO+C HNO===C NOClNa
2 2 3 3 3 3 3 3 3 2
+NaOH+HO,可得关系式:4NaOH~2NaClO~C HNO ,加入4 mol NaOH时,可消耗1
2 3 3 3 3
mol C HNO,由于生成了NaOH,则消耗氰尿酸的量大于1 mol,C正确。
3 3 3 3
6.(2023·辽宁省部分重点中学协作体高三模拟)高铁酸钾可以用于饮用水处理。工业上制备
KFeO 的一种方法是向KOH溶液中通入氯气,然后再加入Fe (NO) 溶液:
2 4 3 3
①Cl+KOH―→KCl+KClO+KClO+HO;
2 3 2
②Fe(NO )+KClO+KOH―→KFeO+KNO+KCl+HO(方程式均未配平)。
3 3 2 4 3 2
下列说法正确的是( )
A.氯气与热的石灰乳反应制得的漂白粉或漂粉精可以用于游泳池等场所的消毒
B.若反应①中n(ClO-)∶n(ClO)=3∶1,则该反应还原产物与氧化产物的物质的量之比为
1∶2
C.用上述方法得到2 mol K FeO 时最多消耗3 mol Cl
2 4 2
D.处理饮用水时,加入高铁酸钾效果相当于加入氯气和铝盐两种物质
答案 D
解析 氯气与热的石灰乳反应生成Ca(ClO ) 、CaCl ,制备漂白粉不能用热的石灰乳和氯气
3 2 2
反应,故A错误;若反应①中n(ClO-)∶n(ClO)=3∶1,根据得失电子守恒,反应的化学方
程式为6Cl +12KOH===8KCl+3KClO+KClO +6HO,则该反应还原产物与氧化产物的物
2 3 2
质的量之比为2∶1,故B错误;若反应①中不生成KClO ,得到2 mol K FeO 转移6 mol电
3 2 4
子,根据得失电子守恒,消耗3 mol Cl ,由于反应①中生成KClO,所以消耗氯气的物质的
2 3
量最少为3 mol,故C错误;KFeO 具有强氧化性,能杀菌消毒,同时还原产物Fe3+发生水
2 4
解生成氢氧化铁胶体,能吸附悬浮杂质,所以处理饮用水时,加入高铁酸钾效果相当于加入
氯气和铝盐两种物质,故D正确。
7.某学习小组探究MnO 与FeCl 能否反应产生Cl 。已知FeCl 固体易升华,其蒸气为黄色。
2 3 2 3
实验装置如图,下列说法不正确的是( )
A.加热前需要先通氮气,排尽空气,并检查装置的气密性
B.加热一段时间后,装置A中产生黄色气体,说明反应生成了氯气C.从安全角度出发,在装置A、B之间应添加冷凝装置,防止堵塞导管
D.除了氯气外,升华的FeCl 、未除尽的O 都可使B中溶液变蓝
3 2
答案 B
解析 FeCl 升华后产生的气体也为黄色,B错误;FeCl 固体易升华,对于易升华的物质要
3 3
注意采取安全措施,C正确;空气中的O 、Cl 、FeCl 都有氧化性,均可将KI氧化为I ,D
2 2 3 2
正确。
8.常温下,二氯化二硫(S Cl)为橙黄色液体,遇水易水解,工业上用于橡胶的硫化。某学
2 2
习小组用氯气和硫单质合成SCl 的实验装置如图所示,下列说法不正确的是( )
2 2
A.实验时需后点燃E处的酒精灯
B.C、D中所盛试剂分别为饱和氯化钠溶液、浓硫酸
C.二氯化二硫水解反应产物为S、HS、HCl
2
D.G、H之间应加上D装置
答案 C
解析 因为装置中有空气,所以实验时应先点燃最左边酒精灯,产生氯气排尽空气,再点燃
E处酒精灯,故A正确;因为SCl 遇水易水解,所以E中应为纯净干燥的氯气与S反应,C
2 2
瓶中盛饱和氯化钠溶液吸收挥发出的HCl气体,D瓶中盛浓硫酸吸水,故B正确;根据元
素守恒,二氯化二硫(S Cl)水解反应产物中一定有含氧元素的化合物,且元素的化合价必须
2 2
有升有降,故C错误;因为二氯化二硫遇水易水解,所以G、H之间应加上D装置,以防
止右侧水蒸气扩散进入G中,故D正确。
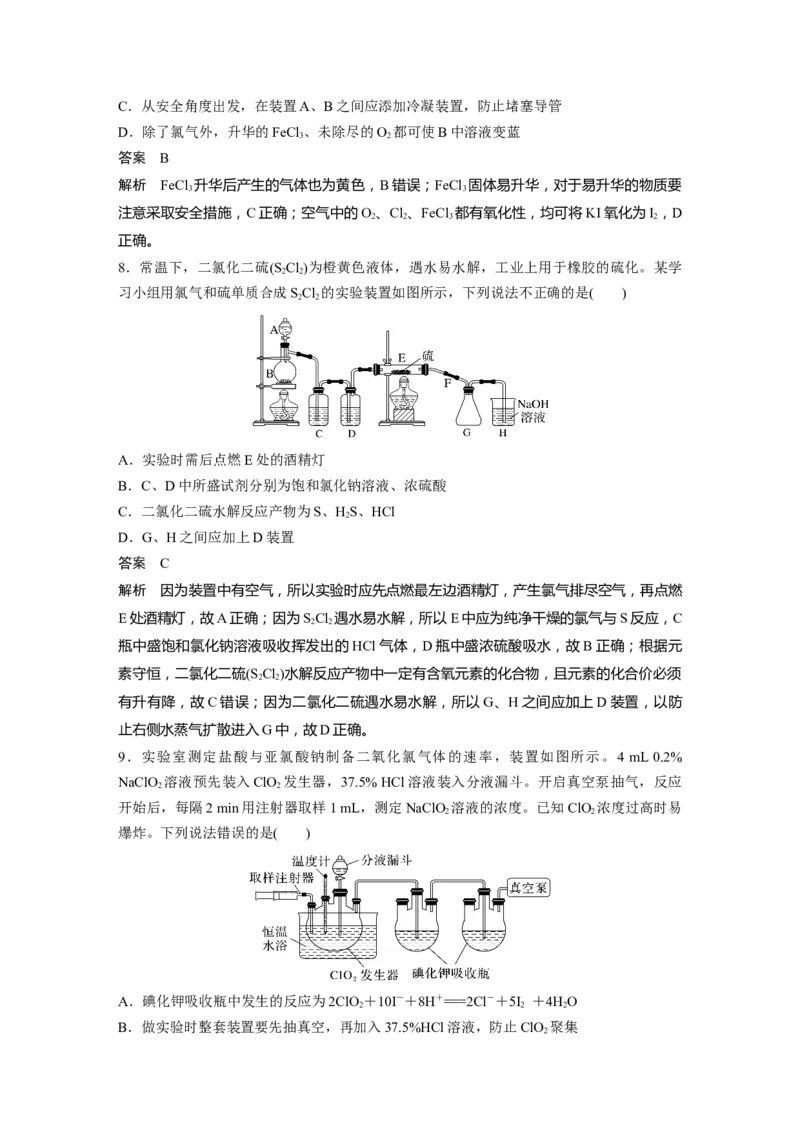
9.实验室测定盐酸与亚氯酸钠制备二氧化氯气体的速率,装置如图所示。4 mL 0.2%
NaClO 溶液预先装入ClO 发生器,37.5% HCl溶液装入分液漏斗。开启真空泵抽气,反应
2 2
开始后,每隔2 min用注射器取样1 mL,测定NaClO 溶液的浓度。已知ClO 浓度过高时易
2 2
爆炸。下列说法错误的是( )
A.碘化钾吸收瓶中发生的反应为2ClO +10I-+8H+===2Cl-+5I +4HO
2 2 2
B.做实验时整套装置要先抽真空,再加入37.5%HCl溶液,防止ClO 聚集
2C.分液漏斗作为空气入口,起到搅拌作用
D.实验过程中分液漏斗活塞保持关闭,防止ClO 逸出
2
答案 D
解析 ClO 污染空气,可用酸性KI溶液吸收,A项正确;实验前先打开真空泵,再打开分
2
液漏斗活塞,让盐酸一次性加入发生器,产生的 ClO 快速被抽走,防止聚集爆炸,B项正
2
确;实验过程中,为使真空泵工作顺畅,分液漏斗活塞应保持打开状态,空气从分液漏斗进
入发生器,起到搅拌的作用,C项正确、D项错误。
10.NaClO 是一种重要的杀菌消毒剂,也常用来漂白织物等,下列说法错误的是( )
2
已知:NaClO 饱和溶液在温度低于38 ℃时析出NaClO·3H O,高于38 ℃时析出NaClO。
2 2 2 2
A.“反应”步骤中生成ClO 的化学方程式为2NaClO+SO +HSO ===2ClO +2NaHSO
2 3 2 2 4 2 4
B.“尾气吸收”是吸收“电解”过程排出的少量ClO ,此反应的离子方程式为2OH-+
2
HO+2ClO ===2ClO+O↑+2HO
2 2 2 2 2
C.“电解”中阴极反应的主要产物是Cl
2
D.“一系列操作”为蒸发浓缩、趁热过滤、洗涤、干燥
答案 C
解析 电解装置中阴极上ClO 得电子生成ClO,阳极上Cl-失电子生成Cl ,C错误。
2 2
11.二氧化氯(ClO ,黄绿色、易溶于水的气体)是一种高效、低毒的消毒剂。其一种生产工
2
艺如图所示。下列说法正确的是( )
A.气体A为Cl
2
B.参加反应的NaClO 和NCl 的物质的量之比为3∶1
2 3
C.溶液B中含有大量的Na+、Cl-、OH-
D.可将混合气通过饱和食盐水除去ClO 中的NH
2 3
答案 C
解析 根据题意分析,气体A为H ,故A错误;在NCl 溶液中加入NaClO 溶液加热反应
2 3 2
生成ClO 、NH 和溶液B,由氢元素守恒可知,有水参加反应,结合得失电子守恒、原子守
2 3
恒和电荷守恒可知,反应还生成 NaCl 与 NaOH,化学方程式为 6NaClO +NCl +
2 3
3HO===3NaCl+6ClO ↑+NH ↑+3NaOH,参加反应的NaClO 和NCl 的物质的量之比为
2 2 3 2 36∶1,故B错误;根据上述分析可知,溶液B中含有NaCl与NaOH,则含有大量的Na+、
Cl-、OH-,故C正确;二氧化氯(ClO )是一种黄绿色、易溶于水的气体,不可用饱和食盐
2
水除去ClO 中的NH ,故D错误。
2 3
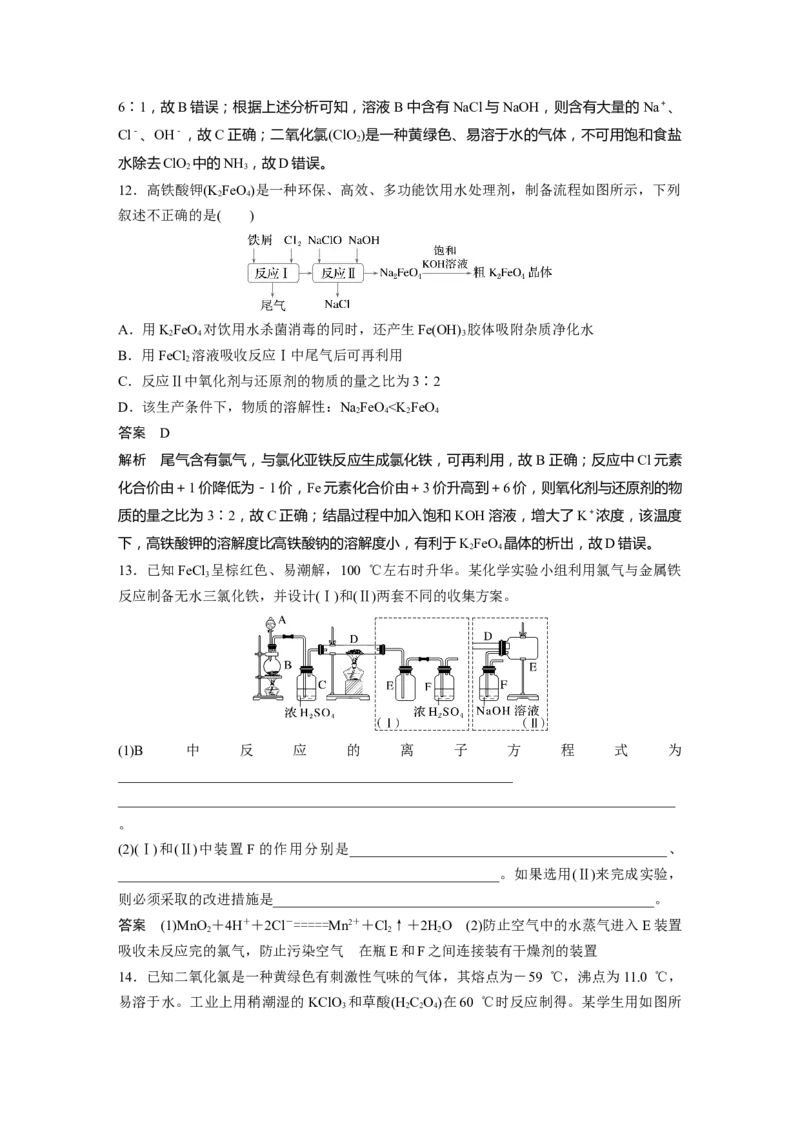
12.高铁酸钾(K FeO)是一种环保、高效、多功能饮用水处理剂,制备流程如图所示,下列
2 4
叙述不正确的是( )
A.用KFeO 对饮用水杀菌消毒的同时,还产生Fe(OH) 胶体吸附杂质净化水
2 4 3
B.用FeCl 溶液吸收反应Ⅰ中尾气后可再利用
2
C.反应Ⅱ中氧化剂与还原剂的物质的量之比为3∶2
D.该生产条件下,物质的溶解性:NaFeO