文档内容
第 23 讲 氨 铵盐
[复习目标] 1.能从结构的角度分析 NH 的性质。2.掌握氨的实验室制法及喷泉实验。3.知
3
道铵盐的性质与NH的检验方法。
考点一 氨
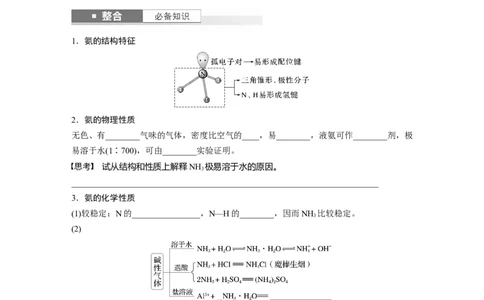
1.氨的结构特征
2.氨的物理性质
无色、有________气味的气体,密度比空气的____,易________,液氨可作________剂,极
易溶于水(1∶700),可由________实验证明。
思考 试从结构和性质上解释NH 极易溶于水的原因。
3
________________________________________________________________________
3.氨的化学性质
(1)较稳定:N的________________,N—H的________,因而NH 比较稳定。
3
(2)
(3)较强的配位能力
Cu(OH) 溶于氨水:_____________________________________________________________
2
______________________________________________________________________________。
(4)还原性
催化氧化:_____________________________________________________________________。
1.向AlCl 溶液中逐滴加入过量的氨水,先产生白色沉淀,最后白色沉淀溶解( )
32.氨溶于水显弱碱性是因为氨气分子能电离出OH-( )
3.氨极易溶于水,因此氨水比较稳定(不容易分解)( )
4.氨水和液氨不同,氨水是混合物,液氨是纯净物( )
5.氨水中物质的量浓度最大的粒子是NH ·H O(水除外)( )
3 2
6.氨水显弱碱性,是弱电解质( )
7.现有1 mol·L-1的氨水,则该溶液中NH ·H O的浓度是1 mol·L-1( )
3 2
一、氨的还原性
1.依据信息完成下列反应的化学方程式。
(1)在加热条件下,氨气容易被氧化铜氧化生成氮气:_________________________________。
(2)工业上常用浓氨水检验输送氯气的管道是否泄露,Cl 能将NH 氧化为N ,同时产生白烟。
2 3 2
用化学方程式解释检验原理:_____________________________________________________
_______________________________________________________________________________
。
(3)工业上制取硝酸的流程如下:
NH ――→NO――→NO ――→HNO
3 2 3
写出各步转化的化学方程式:
①________________________________________________________________________;
②________________________________________________________________________;
③________________________________________________________________________。
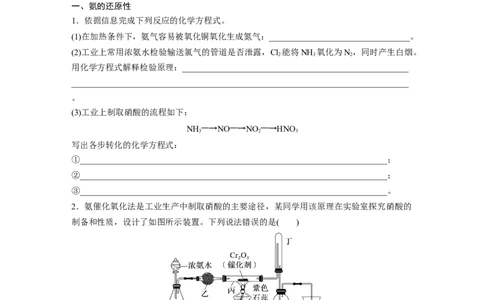
2.氨催化氧化法是工业生产中制取硝酸的主要途径,某同学用该原理在实验室探究硝酸的
制备和性质,设计了如图所示装置。下列说法错误的是( )
A.甲装置中的固体可以是NaOH或CaO
B.乙装置中的干燥剂可以是碱石灰
C.丙中发生的反应是4NH +5O=====4NO+6HO
3 2 2
D.若戊中观察到紫色石蕊溶液变红,则说明已制得HNO
3
二、肼(N H)的结构与性质
2 4
3.联氨(又称肼,NH,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。
2 4(1)联氨的电子式为_____________________________________________________________,
其中氮的化合价为________。
(2)联氨为二元弱碱,在水中的电离方程式与氨相似。写出联氨的第一步电离方程式:
______________________________,联氨与硫酸形成的酸式盐的化学式为____________。
(3)实验室可用NaClO溶液与NH 反应制备联氨,反应的化学方程式为__________________
3
_______________________________________________________________________________
。
已知2NH(l)+NO(l)===3N(g)+4HO(g)
2 4 2 4 2 2
ΔH=-1 048.9 kJ·mol-1,分析联氨和NO 可作为火箭推进剂的主要原因:______________
2 4
_______________________________________________________________________________
。
考点二 铵盐及氨的实验室制法
1.铵盐
(1)物理性质
铵盐大多数是____色固体,绝大多数易溶于水。
(2)化学性质
2.NH的检验步骤
未知液――――→产生使湿润的红色石蕊试纸变______的气体,则证明含NH。
3.氨的实验室制法
(1)加热NH Cl和Ca(OH) 的固体混合物制取氨气
4 2
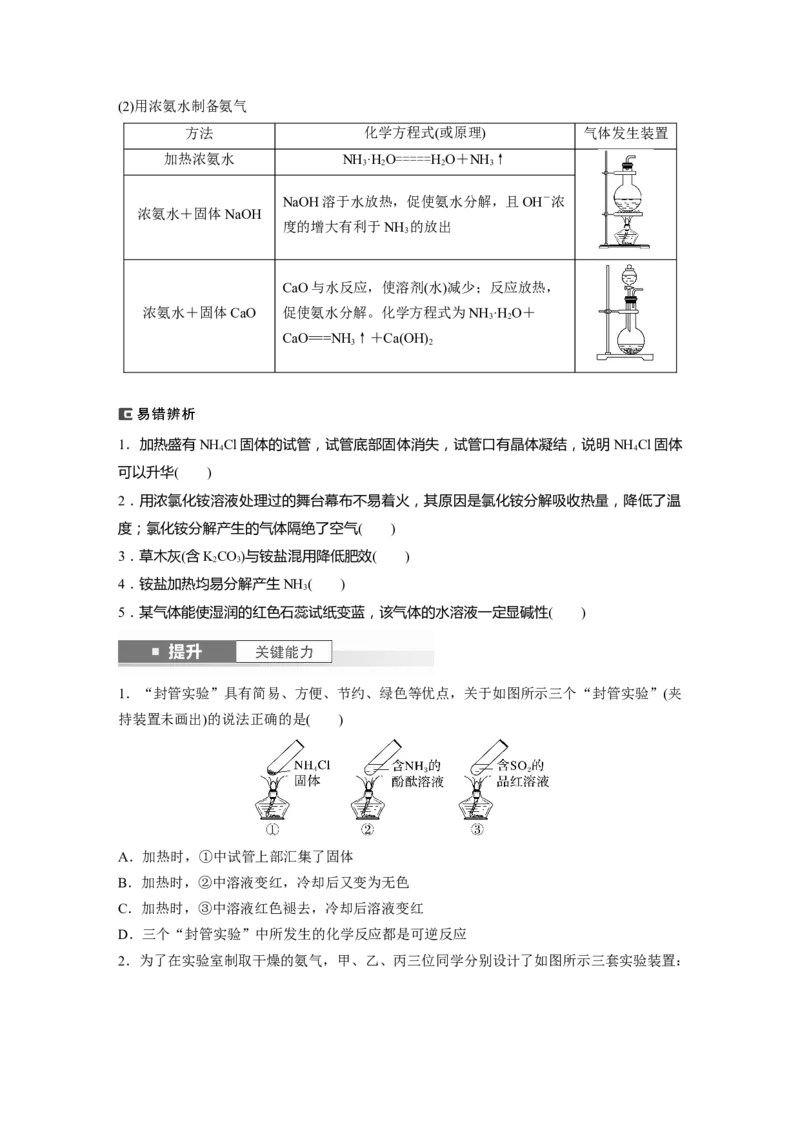
简易装置示意图如图。(2)用浓氨水制备氨气
方法 化学方程式(或原理) 气体发生装置
加热浓氨水 NH ·H O=====HO+NH ↑
3 2 2 3
NaOH溶于水放热,促使氨水分解,且OH-浓
浓氨水+固体NaOH
度的增大有利于NH 的放出
3
CaO与水反应,使溶剂(水)减少;反应放热,
浓氨水+固体CaO 促使氨水分解。化学方程式为NH ·H O+
3 2
CaO===NH ↑+Ca(OH)
3 2
1.加热盛有NH Cl固体的试管,试管底部固体消失,试管口有晶体凝结,说明NH Cl固体
4 4
可以升华( )
2.用浓氯化铵溶液处理过的舞台幕布不易着火,其原因是氯化铵分解吸收热量,降低了温
度;氯化铵分解产生的气体隔绝了空气( )
3.草木灰(含KCO)与铵盐混用降低肥效( )
2 3
4.铵盐加热均易分解产生NH ( )
3
5.某气体能使湿润的红色石蕊试纸变蓝,该气体的水溶液一定显碱性( )
1.“封管实验”具有简易、方便、节约、绿色等优点,关于如图所示三个“封管实验”(夹
持装置未画出)的说法正确的是( )
A.加热时,①中试管上部汇集了固体
B.加热时,②中溶液变红,冷却后又变为无色
C.加热时,③中溶液红色褪去,冷却后溶液变红
D.三个“封管实验”中所发生的化学反应都是可逆反应
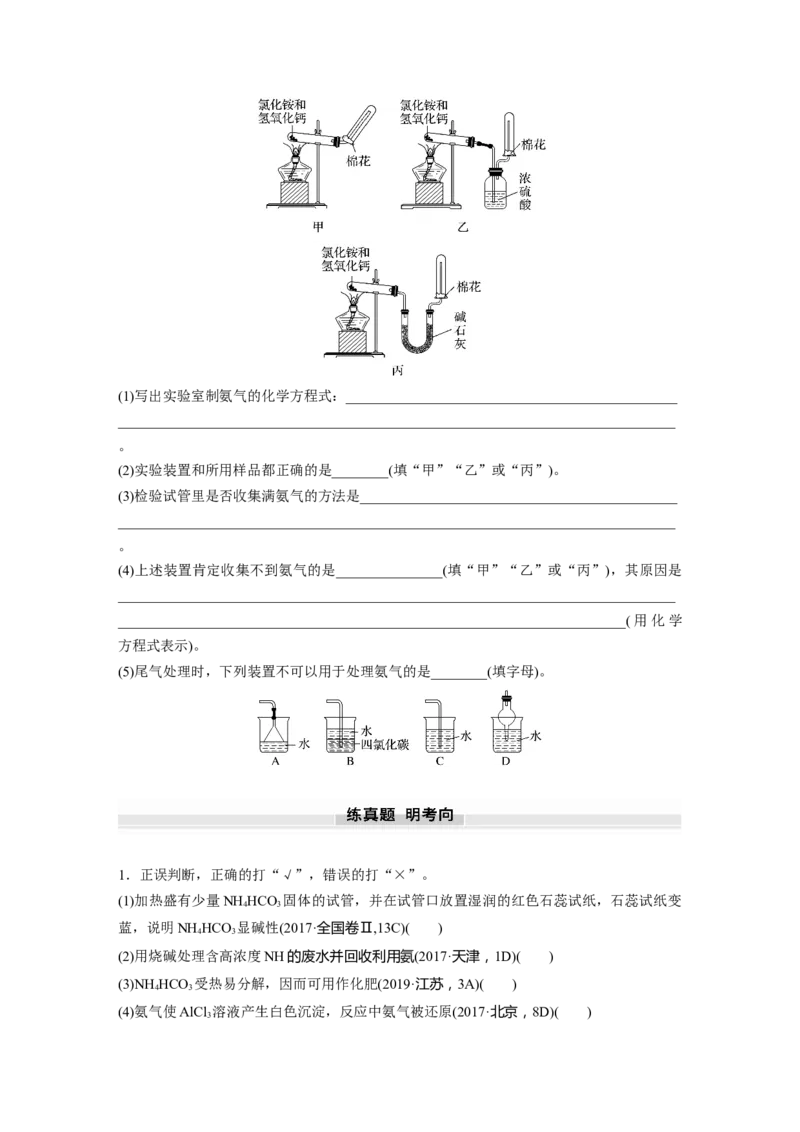
2.为了在实验室制取干燥的氨气,甲、乙、丙三位同学分别设计了如图所示三套实验装置:(1)写出实验室制氨气的化学方程式:_______________________________________________
_______________________________________________________________________________
。
(2)实验装置和所用样品都正确的是________(填“甲”“乙”或“丙”)。
(3)检验试管里是否收集满氨气的方法是_____________________________________________
_______________________________________________________________________________
。
(4)上述装置肯定收集不到氨气的是_______________(填“甲”“乙”或“丙”),其原因是
_______________________________________________________________________________
________________________________________________________________________(用化学
方程式表示)。
(5)尾气处理时,下列装置不可以用于处理氨气的是________(填字母)。
1.正误判断,正确的打“√”,错误的打“×”。
(1)加热盛有少量NH HCO 固体的试管,并在试管口放置湿润的红色石蕊试纸,石蕊试纸变
4 3
蓝,说明NH HCO 显碱性(2017·全国卷Ⅱ,13C)( )
4 3
(2)用烧碱处理含高浓度NH的废水并回收利用氨(2017·天津,1D)( )
(3)NH HCO 受热易分解,因而可用作化肥(2019·江苏,3A)( )
4 3
(4)氨气使AlCl 溶液产生白色沉淀,反应中氨气被还原(2017·北京,8D)( )
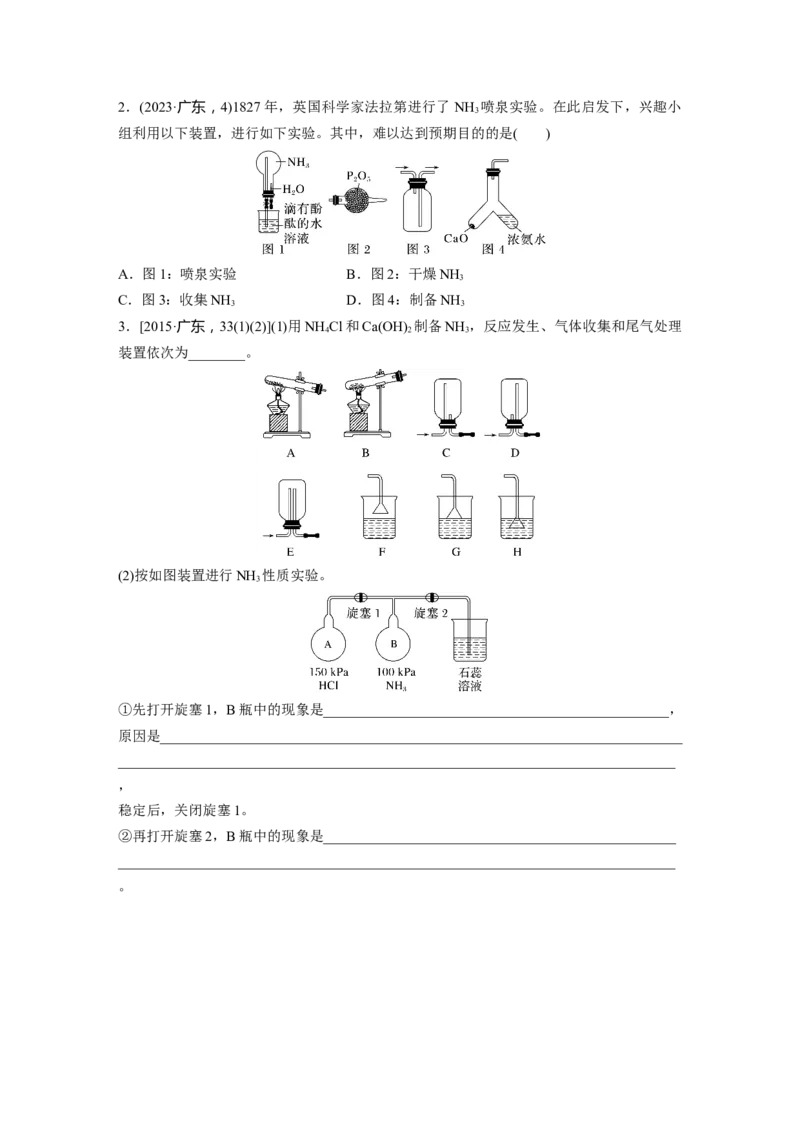
32.(2023·广东,4)1827年,英国科学家法拉第进行了NH 喷泉实验。在此启发下,兴趣小
3
组利用以下装置,进行如下实验。其中,难以达到预期目的的是( )
A.图1:喷泉实验 B.图2:干燥NH
3
C.图3:收集NH D.图4:制备NH
3 3
3.[2015·广东,33(1)(2)](1)用NH Cl和Ca(OH) 制备NH ,反应发生、气体收集和尾气处理
4 2 3
装置依次为________。
(2)按如图装置进行NH 性质实验。
3
①先打开旋塞1,B瓶中的现象是_________________________________________________,
原因是__________________________________________________________________________
_______________________________________________________________________________
,
稳定后,关闭旋塞1。
②再打开旋塞2,B瓶中的现象是__________________________________________________
_______________________________________________________________________________
。