文档内容
第 30 讲 陌生过渡金属及其化合物的制备流程分析
[复习目标] 1.了解常考过渡金属及其重要化合物。2.能依据信息及化合价解答陌生过渡金
属及其化合物制备流程中的有关问题。
1.过渡金属——多变价
(1)高价态金属通常形成含氧酸根离子的盐,具有较强的氧化性,如 KMnO 、KCr O 、
4 2 2 7
KFeO 等,均能将浓盐酸氧化成Cl。
2 4 2
(2)在空气中灼烧一些不稳定的低价金属的化合物,在分解的同时可能被氧化:
MnOOH――――→MnO ;Fe(OH) ――――→Fe O;CoC O――――→Co O。
2 2 2 3 2 4 3 4
(3)低价金属的氢氧化物,为难溶性的弱碱,且易分解成氧化物,如 Fe(OH) 、Mn(OH) 、
2 2
Cr(OH) 。
3
(4)低价硫化物,通常为有色难溶物,如HgS(黑或红)、FeS(黑)、Cu S(黑)、FeS(金黄)。
2 2
工业生产中,常通过转化价态、调节pH将过渡金属生成氢氧化物沉淀或生成难溶硫化物分
离除去。
2.过渡金属易形成配合物
(1)金属离子常易水解,其水合离子通常显色,如Cu2+(aq,蓝)、Fe2+(aq,浅绿)、Fe3+(aq,
黄)、Cr3+(aq,绿)。
(2)容易形成配合物的中心离子,如[Cu(NH )]2+、[Ag(NH)]+、[Fe(SCN) ]3-、
3 4 3 2 6
[Cr(NH )(H O) Cl]2+。
3 3 2 2
(3)向一些盐溶液中滴加氨水,先生成难溶性碱,继续滴加,生成含氨配合物,如
CuSO (aq)[或AgNO(aq)]――→Cu(OH) (s)[或AgOH(s)]――→[Cu(NH )]2+{或[Ag(NH)]+}。
4 3 2 3 4 3 2
3.锌及其化合物的转化
①Zn(OH) +2OH-===[Zn(OH) ]2-,
2 4
②Zn(OH) +2H+===Zn2++2HO,
2 2
③ZnO+2H+===Zn2++HO,
2
④ZnO+2OH-+HO===[Zn(OH) ]2-。
2 4
4.铬的重要化合物
(1)Cr O 和Cr(OH) 显两性,其转化关系如下:Cr3+Cr(OH) [Cr(OH) ]-。
2 3 3 3 4
反应的离子方程式:
①Cr3++3OH-===Cr(OH) ↓;
3
②Cr(OH) +OH-===[Cr(OH) ]-,Cr3++4OH-===[Cr(OH) ]-;
3 4 4③[Cr(OH) ]-+H+===Cr(OH) ↓+HO;
4 3 2
④Cr(OH) +3H+===Cr3++3HO,[Cr(OH) ]-+4H+===Cr3++4HO。
3 2 4 2
(2)铬(Ⅵ)最重要的化合物是KCr O,在水溶液中Cr O和CrO存在下列平衡:
2 2 7 2
2CrO(黄色)+2H+Cr O(橙红色)+HO。
2 2
5.钒的重要化合物
(1)五氧化二钒既能溶于强碱,又能溶于强酸,如:
VO+6NaOH===2NaVO +3HO;
2 5 3 4 2
VO+6HCl===2VOCl +Cl↑+3HO。
2 5 2 2 2
(2)VO2+、VO:在酸性介质中,VO具有强氧化性,如:
VO+Fe2++2H+===VO2++Fe3++HO,
2
2VO+HC O+2H+===2VO2++2CO↑+2HO。
2 2 4 2 2
6.钴的配合物
(1)Co(Ⅱ)与HO、Cl-配合的平衡转化
2
[Co(H O) ]2+[CoCl ]2-
2 6 4
粉红色 蓝色
(2)Co(Ⅱ)的配合物具有较强的还原性
Co2++6NH ―→[Co(NH )]2+――→[Co(NH )]3+
3 3 6 3 6
1.(2023·湖南衡阳校联考三模)锌是一种浅灰色的过渡金属。在现代工业中,是电池制造中
不可替代且相当重要的金属,以菱锌矿(主要成分为 ZnCO 、ZnO,含有少量 SiO 和
3 2
NaSiO)制备锌单质的流程如图所示:
2 3
下列说法错误的是( )
A.SO的空间结构为正四面体形
B.滤渣的主要成分为SiO 和HSiO
2 2 3
C.“沉淀”步骤中,消耗CO 的物质的量与消耗Na[Zn(OH) ]的物质的量之比为1∶1
2 2 4
D.“热还原”过程发生了置换反应
2.(2024·长沙模拟)以黄铁矿(主要成分是FeS ,含少量SiO)和软锰矿(主要成分是MnO ,
2 2 2
含少量Fe O、Al O)为原料制备MnSO ·H O的工艺流程如图。下列说法正确的是( )
2 3 2 3 4 2A.酸浸和沉锰操作均应在较高温度下进行
B.滤渣1的成分中含有S和SiO
2
C.调pH的目的只为除去溶液中的Fe3+
D.沉锰操作中主要反应的离子方程式是 2HCO+Mn2+===MnCO ↓ +CO ↑+HO
3 2 2
3.钒元素在酸性溶液中有多种存在形式,其中VO2+为蓝色,VO为淡黄色,VO具有较强
的氧化性,Fe2+、SO等能把VO还原为VO2+。向VOSO 溶液中滴加酸性KMnO 溶液,溶
4 4
液颜色由蓝色变为淡黄色。下列说法不正确的是( )
A.在酸性溶液中氧化性:MnO>VO
B.FeI 溶液与足量酸性(VO )SO 溶液发生反应的离子方程式:Fe2++VO+2H+===Fe3++
2 2 2 4
VO2++HO
2
C.向 VOSO 溶液中滴加酸性 KMnO 溶液反应的化学方程式为 10VOSO +2HO+
4 4 4 2
2KMnO ===5(VO )SO +2MnSO +2HSO +KSO
4 2 2 4 4 2 4 2 4
D.向含1 mol VO的酸性溶液中滴加1.25 mol FeSO 的溶液完全反应,转移电子为1 mol
4
4.[2019·全国卷Ⅲ,26(1)(2)(3)(4)(5)]高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工
业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如
图所示。回答下列问题:
相关金属离子[c(Mn+)=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下:
0
金属离子 Mn2+ Fe2+ Fe3+ Al3+ Mg2+ Zn2+ Ni2+
开始沉淀的pH 8.1 6.3 1.5 3.4 8.9 6.2 6.9
沉淀完全的pH 10.1 8.3 2.8 4.7 10.9 8.2 8.9
(1)“滤渣1”含有S和________;写出“溶浸”中二氧化锰与硫化锰反应的化学方程式:
______________________________________________________________________________________________________________________________________________________________
。
(2)“氧化”中添加适量的MnO 的作用是___________________________________________
2
_______________________________________________________________________________
。
(3)“调pH”除铁和铝,溶液的pH范围应调节为________~6之间。
(4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是________________。
(5)“除杂2”的目的是生成MgF 沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原
2
因 是
_____________________________________________________________________________
_______________________________________________________________________________
。
5.(2023·江西新余统考二模)铬(Cr)广泛应用于冶金、化工、航天等领域。工业上以铬铁矿
(主要成分为FeCr O,含有少量Al O)为原料制备金属铬的工艺流程如图所示:
2 4 2 3
回答下列问题:
(1)为提高焙烧效率,可以采取的措施为_____________________________________________
_______________________________________________________________________________
。
(2)亚铬酸亚铁(FeCrO)中Cr的化合价为________,“焙烧”中FeCr O 反应的化学方程式
2 4 2 4
为______________________________________________________________________________
_______________________________________________________________________________
。
(3)“酸化”中反应的离子方程式为_________________________________________________
_______________________________________________________________________________
,
已知:“酸化”后溶液中c(CrO)=1.6×10-3mol·L-1,c(CrO)=2×10-8mol·L-1。则该温度
2
下该反应的平衡常数为______。
(4)“沉铝”需控制pH=6~10的原因为____________________________________________
_______________________________________________________________________________
。
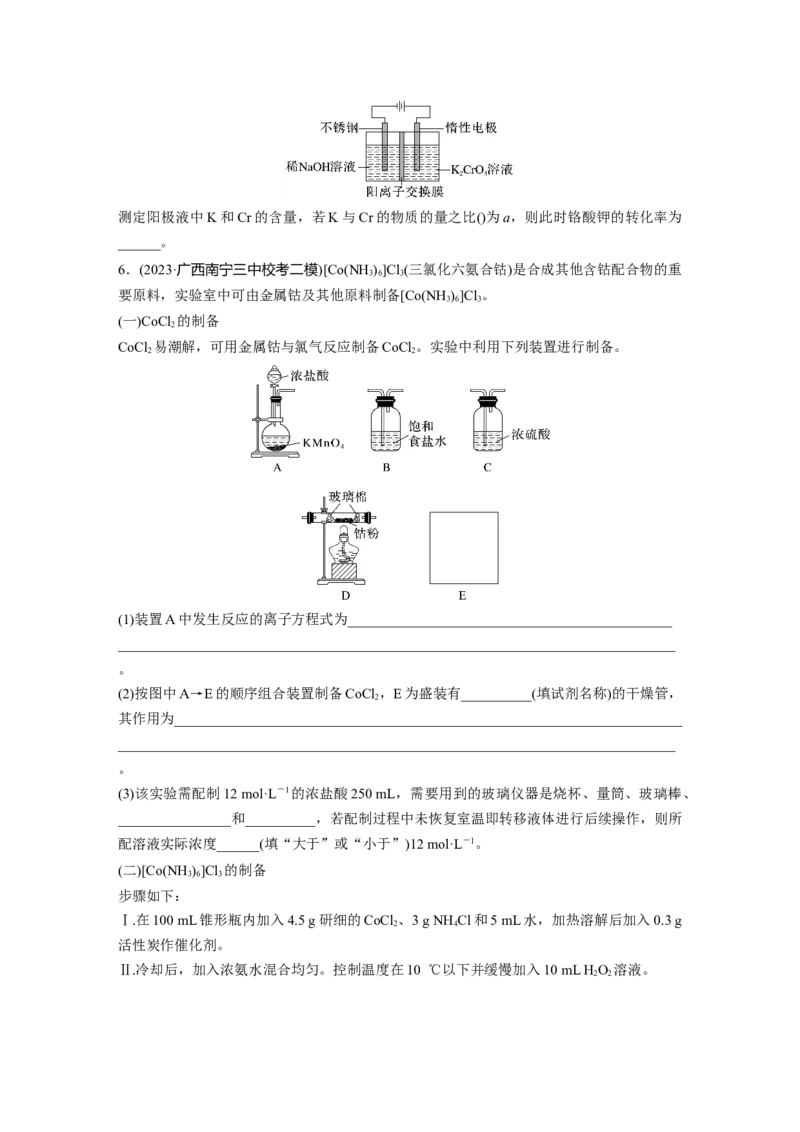
(5)以铬酸钾(K CrO)为原料,用电化学法制备重铬酸钾的实验装置如图。
2 4测定阳极液中K和Cr的含量,若K与Cr的物质的量之比()为a,则此时铬酸钾的转化率为
______。
6.(2023·广西南宁三中校考二模)[Co(NH )]Cl (三氯化六氨合钴)是合成其他含钴配合物的重
3 6 3
要原料,实验室中可由金属钴及其他原料制备[Co(NH )]Cl 。
3 6 3
(一)CoCl 的制备
2
CoCl 易潮解,可用金属钴与氯气反应制备CoCl 。实验中利用下列装置进行制备。
2 2
(1)装置A中发生反应的离子方程式为______________________________________________
_______________________________________________________________________________
。
(2)按图中A→E的顺序组合装置制备CoCl ,E为盛装有__________(填试剂名称)的干燥管,
2
其作用为________________________________________________________________________
_______________________________________________________________________________
。
(3)该实验需配制12 mol·L-1的浓盐酸250 mL,需要用到的玻璃仪器是烧杯、量筒、玻璃棒、
________________和__________,若配制过程中未恢复室温即转移液体进行后续操作,则所
配溶液实际浓度______(填“大于”或“小于”)12 mol·L-1。
(二)[Co(NH )]Cl 的制备
3 6 3
步骤如下:
Ⅰ.在100 mL锥形瓶内加入4.5 g研细的CoCl 、3 g NH Cl和5 mL水,加热溶解后加入0.3 g
2 4
活性炭作催化剂。
Ⅱ.冷却后,加入浓氨水混合均匀。控制温度在10 ℃以下并缓慢加入10 mL H O 溶液。
2 2Ⅲ.在60 ℃下反应一段时间后,经过一系列操作后,过滤、洗涤、干燥得到[Co(NH )]Cl 晶
3 6 3
体。
已知:不同温度下[Co(NH )]Cl 在水中的溶解度如图所示。
3 6 3
回答下列问题:
(4)步骤Ⅱ中在加入HO 溶液时,控制温度在10 ℃以下的目的是_______________________。
2 2
(5)制备[Co(NH )]Cl 的总反应的化学方程式为______________________________________
3 6 3
_______________________________________________________________________________
。
(6)Ⅲ中的“一系列操作”包括___________________________________________________、
________________________。