文档内容
第 30 讲 陌生过渡金属及其化合物的制备流程分析
[复习目标] 1.了解常考过渡金属及其重要化合物。2.能依据信息及化合价解答陌生过渡金
属及其化合物制备流程中的有关问题。
1.过渡金属——多变价
(1)高价态金属通常形成含氧酸根离子的盐,具有较强的氧化性,如 KMnO 、KCr O 、
4 2 2 7
KFeO 等,均能将浓盐酸氧化成Cl。
2 4 2
(2)在空气中灼烧一些不稳定的低价金属的化合物,在分解的同时可能被氧化:
MnOOH――――→MnO ;Fe(OH) ――――→Fe O;CoC O――――→Co O。
2 2 2 3 2 4 3 4
(3)低价金属的氢氧化物,为难溶性的弱碱,且易分解成氧化物,如 Fe(OH) 、Mn(OH) 、
2 2
Cr(OH) 。
3
(4)低价硫化物,通常为有色难溶物,如HgS(黑或红)、FeS(黑)、Cu S(黑)、FeS(金黄)。
2 2
工业生产中,常通过转化价态、调节pH将过渡金属生成氢氧化物沉淀或生成难溶硫化物分
离除去。
2.过渡金属易形成配合物
(1)金属离子常易水解,其水合离子通常显色,如Cu2+(aq,蓝)、Fe2+(aq,浅绿)、Fe3+(aq,
黄)、Cr3+(aq,绿)。
(2)容易形成配合物的中心离子,如[Cu(NH )]2+、[Ag(NH)]+、[Fe(SCN) ]3-、
3 4 3 2 6
[Cr(NH )(H O) Cl]2+。
3 3 2 2
(3)向一些盐溶液中滴加氨水,先生成难溶性碱,继续滴加,生成含氨配合物,如
CuSO (aq)[或AgNO(aq)]――→Cu(OH) (s)[或AgOH(s)]――→[Cu(NH )]2+{或[Ag(NH)]+}。
4 3 2 3 4 3 2
3.锌及其化合物的转化
①Zn(OH) +2OH-===[Zn(OH) ]2-,
2 4
②Zn(OH) +2H+===Zn2++2HO,
2 2
③ZnO+2H+===Zn2++HO,
2
④ZnO+2OH-+HO===[Zn(OH) ]2-。
2 4
4.铬的重要化合物
(1)Cr O 和Cr(OH) 显两性,其转化关系如下:Cr3+Cr(OH) [Cr(OH) ]-。
2 3 3 3 4
反应的离子方程式:
①Cr3++3OH-===Cr(OH) ↓;
3
②Cr(OH) +OH-===[Cr(OH) ]-,Cr3++4OH-===[Cr(OH) ]-;
3 4 4③[Cr(OH) ]-+H+===Cr(OH) ↓+HO;
4 3 2
④Cr(OH) +3H+===Cr3++3HO,[Cr(OH) ]-+4H+===Cr3++4HO。
3 2 4 2
(2)铬(Ⅵ)最重要的化合物是KCr O,在水溶液中Cr O和CrO存在下列平衡:
2 2 7 2
2CrO(黄色)+2H+Cr O(橙红色)+HO。
2 2
5.钒的重要化合物
(1)五氧化二钒既能溶于强碱,又能溶于强酸,如:
VO+6NaOH===2NaVO +3HO;
2 5 3 4 2
VO+6HCl===2VOCl +Cl↑+3HO。
2 5 2 2 2
(2)VO2+、VO:在酸性介质中,VO具有强氧化性,如:
VO+Fe2++2H+===VO2++Fe3++HO,
2
2VO+HC O+2H+===2VO2++2CO↑+2HO。
2 2 4 2 2
6.钴的配合物
(1)Co(Ⅱ)与HO、Cl-配合的平衡转化
2
[Co(H O) ]2+[CoCl ]2-
2 6 4
粉红色 蓝色
(2)Co(Ⅱ)的配合物具有较强的还原性
Co2++6NH ―→[Co(NH )]2+――→[Co(NH )]3+
3 3 6 3 6
1.(2023·湖南衡阳校联考三模)锌是一种浅灰色的过渡金属。在现代工业中,是电池制造中
不可替代且相当重要的金属,以菱锌矿(主要成分为 ZnCO 、ZnO,含有少量 SiO 和
3 2
NaSiO)制备锌单质的流程如图所示:
2 3
下列说法错误的是( )
A.SO的空间结构为正四面体形
B.滤渣的主要成分为SiO 和HSiO
2 2 3
C.“沉淀”步骤中,消耗CO 的物质的量与消耗Na[Zn(OH) ]的物质的量之比为1∶1
2 2 4
D.“热还原”过程发生了置换反应
答案 C
解析 菱锌矿(主要成分为ZnCO 、ZnO,含有少量SiO 和NaSiO)与硫酸反应生成硫酸锌、
3 2 2 3
硅酸、硫酸钠,二氧化硅不与硫酸反应,过滤,向滤液中加入过量氢氧化钠溶液,向溶液中通入二氧化碳得到氢氧化锌,过滤,将氢氧化锌煅烧得到氧化锌,再用过量焦炭还原得到锌。
“沉淀”时CO 会先与未反应完的NaOH反应,因此消耗的二氧化碳量比Na[Zn(OH) ]多,
2 2 4
故C错误;ZnO+C=====Zn+CO↑是置换反应,故D正确。
2.(2024·长沙模拟)以黄铁矿(主要成分是FeS ,含少量SiO)和软锰矿(主要成分是MnO ,
2 2 2
含少量Fe O、Al O)为原料制备MnSO ·H O的工艺流程如图。下列说法正确的是( )
2 3 2 3 4 2
A.酸浸和沉锰操作均应在较高温度下进行
B.滤渣1的成分中含有S和SiO
2
C.调pH的目的只为除去溶液中的Fe3+
D.沉锰操作中主要反应的离子方程式是 2HCO+Mn2+===MnCO ↓ +CO ↑+HO
3 2 2
答案 B
解析 酸浸时采用高温可以使反应速率加快,而沉锰时如果温度过高,氨水和 NH HCO 受
4 3
热分解,MnCO 溶解度增大,导致沉锰效率降低,因此应该在低温下进行沉锰,A错误;
3
SiO 、生成的S均不溶于稀硫酸,因此用稀硫酸溶解后的滤渣 1的成分中含有S和SiO ,B
2 2
正确;调pH的目的是使溶液中的Fe3+、Al3+转化为Fe(OH) 、Al(OH) 沉淀,从而达到除去
3 3
Fe3+、Al3+的目的,C错误;沉锰操作中加入NH ·H O和NH HCO ,反应的离子方程式为
3 2 4 3
2HCO+Mn2++2NH ·H O===MnCO ↓+CO+2NH+2HO,D错误。
3 2 3 2
3.钒元素在酸性溶液中有多种存在形式,其中VO2+为蓝色,VO为淡黄色,VO具有较强
的氧化性,Fe2+、SO等能把VO还原为VO2+。向VOSO 溶液中滴加酸性KMnO 溶液,溶
4 4
液颜色由蓝色变为淡黄色。下列说法不正确的是( )
A.在酸性溶液中氧化性:MnO>VO
B.FeI 溶液与足量酸性(VO )SO 溶液发生反应的离子方程式:Fe2++VO+2H+===Fe3++
2 2 2 4
VO2++HO
2
C.向 VOSO 溶液中滴加酸性 KMnO 溶液反应的化学方程式为 10VOSO +2HO+
4 4 4 2
2KMnO ===5(VO )SO +2MnSO +2HSO +KSO
4 2 2 4 4 2 4 2 4
D.向含1 mol VO的酸性溶液中滴加1.25 mol FeSO 的溶液完全反应,转移电子为1 mol
4
答案 B
解析 向VOSO 溶液中滴加酸性KMnO 溶液,溶液颜色由蓝色变为淡黄色,说明 MnO将
4 4
VO2+氧化为VO,从而得出氧化性:MnO>VO,故A正确;碘离子的还原性强于亚铁离子且加入足量酸性(VO )SO 溶液,碘离子应参与氧化还原反应,故B错误;向含1 mol VO的
2 2 4
酸性溶液中滴加含1.25 mol Fe2+的溶液发生反应:Fe2++VO+2H+===Fe3++VO2++HO,
2
则VO的量不足,所以转移电子为1 mol,故D正确。
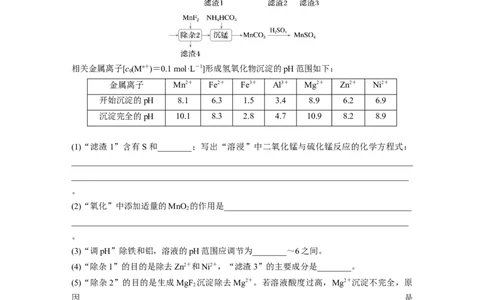
4.[2019·全国卷Ⅲ,26(1)(2)(3)(4)(5)]高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工
业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如
图所示。回答下列问题:
相关金属离子[c(Mn+)=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下:
0
金属离子 Mn2+ Fe2+ Fe3+ Al3+ Mg2+ Zn2+ Ni2+
开始沉淀的pH 8.1 6.3 1.5 3.4 8.9 6.2 6.9
沉淀完全的pH 10.1 8.3 2.8 4.7 10.9 8.2 8.9
(1)“滤渣1”含有S和________;写出“溶浸”中二氧化锰与硫化锰反应的化学方程式:
________________________________________________________________________________
_______________________________________________________________________________
。
(2)“氧化”中添加适量的MnO 的作用是____________________________________________
2
_______________________________________________________________________________
。
(3)“调pH”除铁和铝,溶液的pH范围应调节为________~6之间。
(4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是________。
(5)“除杂2”的目的是生成MgF 沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原
2
因 是
______________________________________________________________________________
______________________________________________________________________________。
答案 (1)SiO(或不溶性硅酸盐) MnO +MnS+2HSO ===2MnSO +S+2HO (2)将Fe2+
2 2 2 4 4 2
氧化为Fe3+ (3)4.7 (4)NiS和ZnS (5)F-与H+结合生成弱电解HF,导致MgF (s)Mg2+
2
(aq)+2F-(aq)平衡向右移动
解析 (1)硫化锰矿中硅元素主要以SiO 或不溶性硅酸盐形式存在,则“滤渣1”的主要成
2
分为S和SiO(或不溶性硅酸盐)。结合“滤渣1”中含S,可知“溶浸”时MnO 与MnS在
2 2
酸性条件下发生氧化还原反应生成MnSO 和S,根据化合价升降法可配平该反应。
45.(2023·江西新余统考二模)铬(Cr)广泛应用于冶金、化工、航天等领域。工业上以铬铁矿
(主要成分为FeCr O,含有少量Al O)为原料制备金属铬的工艺流程如图所示:
2 4 2 3
回答下列问题:
(1)为提高焙烧效率,可以采取的措施为____________________________________________。
(2)亚铬酸亚铁(FeCrO)中Cr的化合价为________,“焙烧”中FeCr O 反应的化学方程式
2 4 2 4
为_____________________________________________________________________________。
(3)“酸化”中反应的离子方程式为________,已知:“酸化”后溶液中c(Cr O)=1.6×10
2
-3mol·L-1,c(CrO)=2×10-8mol·L-1。则该温度下该反应的平衡常数为______。
(4)“沉铝”需控制pH=6~10的原因为____________________________________________。
(5)以铬酸钾(K CrO)为原料,用电化学法制备重铬酸钾的实验装置如图。
2 4
测定阳极液中K和Cr的含量,若K与Cr的物质的量之比()为a,则此时铬酸钾的转化率为
______。
答案 (1)将矿石粉碎或增大空气的量等(任选一条) (2)+3 4FeCr O +7O +
2 4 2
8NaCO=====2Fe O+8NaCrO+8CO
2 3 2 3 2 4 2
(3)2CrO+2H+Cr O+HO 4×1014 (4)pH高于10时,AlO不能完全转化为氢氧化铝,
2 2
pH低于6时,氢氧化铝会继续溶解转化为铝离子,故需控制pH在6~10的范围,让AlO中
铝以氢氧化铝形式存在而过滤除去 (5)2-a
解析 (3)酸化时发生的反应为铬酸钠溶液与稀硫酸反应生成重铬酸钠和硫酸钠,反应的离
子方程式为 2CrO+2H+Cr O+HO;由题给数据可知,该反应的平衡常数 K==
2 2
4×1014。(5)起始时=a,设KCrO 为1 mol,反应过程中有x mol K CrO 转化为KCr O ,
2 4 2 4 2 2 7
则阳极区剩余的KCrO 为(1-x) mol,对应的n =2(1-x) mol,n =(1-x) mol,生成的
2 4 K Cr
KCr O 为 mol,对应的n =x mol,n =x mol,则==a,解得x=2-a,则转化率为2-
2 2 7 K Cr
a。
6.(2023·广西南宁三中校考二模)[Co(NH )]Cl (三氯化六氨合钴)是合成其他含钴配合物的重
3 6 3
要原料,实验室中可由金属钴及其他原料制备[Co(NH )]Cl 。
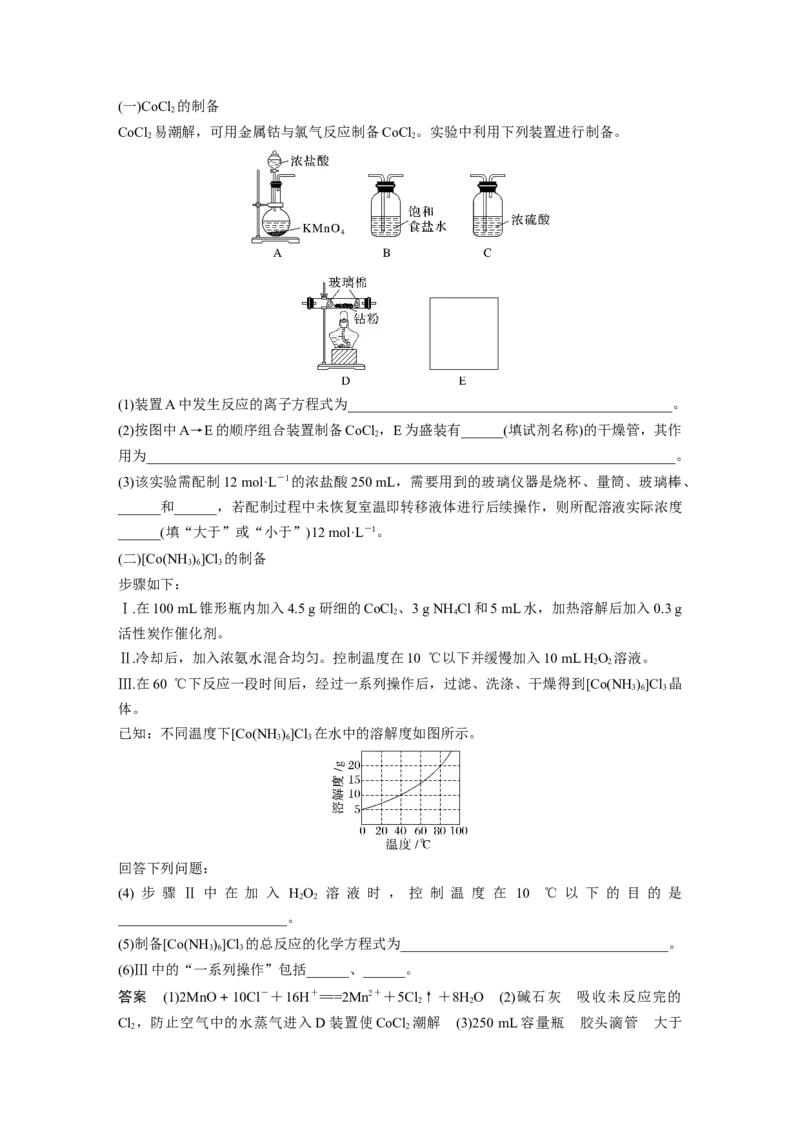
3 6 3(一)CoCl 的制备
2
CoCl 易潮解,可用金属钴与氯气反应制备CoCl 。实验中利用下列装置进行制备。
2 2
(1)装置A中发生反应的离子方程式为______________________________________________。
(2)按图中A→E的顺序组合装置制备CoCl ,E为盛装有______(填试剂名称)的干燥管,其作
2
用为___________________________________________________________________________。
(3)该实验需配制12 mol·L-1的浓盐酸250 mL,需要用到的玻璃仪器是烧杯、量筒、玻璃棒、
______和______,若配制过程中未恢复室温即转移液体进行后续操作,则所配溶液实际浓度
______(填“大于”或“小于”)12 mol·L-1。
(二)[Co(NH )]Cl 的制备
3 6 3
步骤如下:
Ⅰ.在100 mL锥形瓶内加入4.5 g研细的CoCl 、3 g NH Cl和5 mL水,加热溶解后加入0.3 g
2 4
活性炭作催化剂。
Ⅱ.冷却后,加入浓氨水混合均匀。控制温度在10 ℃以下并缓慢加入10 mL H O 溶液。
2 2
Ⅲ.在60 ℃下反应一段时间后,经过一系列操作后,过滤、洗涤、干燥得到[Co(NH )]Cl 晶
3 6 3
体。
已知:不同温度下[Co(NH )]Cl 在水中的溶解度如图所示。
3 6 3
回答下列问题:
(4) 步 骤 Ⅱ 中 在 加 入 HO 溶 液 时 , 控 制 温 度 在 10 ℃ 以 下 的 目 的 是
2 2
________________________。
(5)制备[Co(NH )]Cl 的总反应的化学方程式为______________________________________。
3 6 3
(6)Ⅲ中的“一系列操作”包括______、______。
答案 (1)2MnO+10Cl-+16H+===2Mn2++5Cl↑+8HO (2)碱石灰 吸收未反应完的
2 2
Cl ,防止空气中的水蒸气进入D装置使CoCl 潮解 (3)250 mL容量瓶 胶头滴管 大于
2 2(4)防止温度过高使HO 和NH ·H O分解
2 2 3 2
(5)2CoCl +2NH Cl+10NH ·H O+HO=====2[Co(NH )]Cl +12HO (6)趁热过滤 冷却结
2 4 3 2 2 2 3 6 3 2
晶
解析 (6)由[Co(NH ) ]Cl 在水中的溶解度曲线可知,[Co(NH )]Cl 的溶解度随温度变化较
3 6 3 3 6 3
大,降温时[Co(NH )]Cl 会结晶析出,所以在60 ℃下反应一段时间后,应该趁热过滤除去
3 6 3
活性炭,再冷却结晶使[Co( NH ) ]Cl 晶体析出,经过过滤、洗涤、干燥等操作得到
3 6 3
[Co(NH )]Cl 晶体。
3 6 3
课时精练
1.以含镍废料(主要成分为NiO,含少量FeO、Fe O 、CoO、BaO和SiO)为原料制备NiO
2 3 2 x y
和碳酸亚钴(CoCO)的工艺流程如图:
3
下列说法不正确的是( )
A.“滤渣Ⅰ”的主要成分是SiO、BaSO
2 4
B.“氧化”时的离子反应为6Fe2++6H++ClO===6Fe3++Cl-+3HO
2
C.“调pH”过程中形成黄钠铁矾渣,NaCO 必须过量
2 3
D.“沉钴”过程发生的反应为Co2++2HCO===CoCO↓+CO↑+HO
3 2 2
答案 C
解析 废料中加入硫酸,NiO、FeO、Fe O 、CoO、BaO均能与硫酸反应,生成的NiSO 、
2 3 4
FeSO 、Fe (SO ) 、CoSO 进入溶液,SiO 和硫酸钡为滤渣,A正确;“调pH”过程中形成
4 2 4 3 4 2
黄钠铁矾渣,NaCO 不能过量,防止Co2+、Ni2+形成沉淀而损失,C错误。
2 3
2.某铬贫矿主要成分为Fe(CrO ) ,还含有Fe O 、MgO、Al O ,采用次氯酸钠法处理矿石
2 2 2 3 2 3
并制备CrO 的工艺流程如图,已知“氧化浸出”时铁以最高价氧化物存在。下列说法错误
3
的是( )A.“氧化浸出”时煮沸的目的是加快氧化浸出速率
B.滤渣的主要成分是MgO、Fe O
2 3
C.化合物Ⅰ为NaOH,化合物Ⅱ为NaHCO
3
D.实验室进行“混合”时,将NaCr O 溶液缓慢倒入浓硫酸中,边倒边搅拌
2 2 7
答案 D
解析 温度升高,反应速率变快,A正确;Al O 与NaOH溶液反应,则“滤渣”的主要成
2 3
分为MgO、Fe O ,B正确;由于电解时产生氢气和氯气,故会产生 NaOH,“沉铝”时通
2 3
入过量的 CO ,产生 NaHCO ,C 正确;实验室进行“混合”时,将浓硫酸缓慢倒入
2 3
NaCr O 溶液中,边倒边搅拌,D错误。
2 2 7
3.(2023·山东省实验中学一模)以红土镍镉矿(NiS、CdO,含SiO 、CuO、PbO、Fe O 等杂
2 2 3
质)为原料回收部分金属单质,其工艺流程如图所示:
已知:电极电位是表示某种离子或原子获得电子而被还原的趋势。在 25 ℃下,部分电对的
电极电位如表:
电对 Cu2+/Cu Pb2+/Pb Cd2+/Cd Fe2+/Fe Ni2+/Ni
电极电位/V +0.337 -0.126 -0.402 -0.442 -0.257
下列说法错误的是( )
A.“浆化”的目的是增大接触面积,加快酸浸反应速率,提高某些金属元素浸取率
B.“物质A”可以是NiCO,“调pH”后,所得滤渣Ⅱ为Fe(OH)
3 3
C.“金属A”是Pb和Cu混合物,“金属B”是Cd
D.该工艺流程中可以循环利用的物质有CO、HSO 、Ni等
2 4答案 C
解析 由电极电位表可知金属活动性顺序为Fe>Cd>Ni>Pb>Cu。镍镉矿浆化后,在空气中加
入稀硫酸酸浸,硫化镍和金属氧化物溶于稀硫酸得到硫酸盐,二氧化硅不与稀硫酸反应,过
滤得到含有二氧化硅、硫酸铅的滤渣Ⅰ和滤液;向滤液中加入碳酸镍或氧化镍调节溶液
pH,将溶液中铁离子转化为氢氧化铁沉淀,过滤得到含有氢氧化铁的滤渣Ⅱ和滤液;由金
属活动性顺序可知,向滤液中只能加入镍,将溶液中铜离子转化为铜,过滤得到含有铜、镍
的金属A和硫酸镍、硫酸镉的滤液;滤液经电解、过滤得到含有镉和镍的固体和稀硫酸;
固体通入一氧化碳气化分离得到Ni(CO) 和镉;Ni(CO) 受热分解生成一氧化碳和镍,则该
4 4
工艺流程中可以循环利用的物质为一氧化碳、硫酸和镍等。
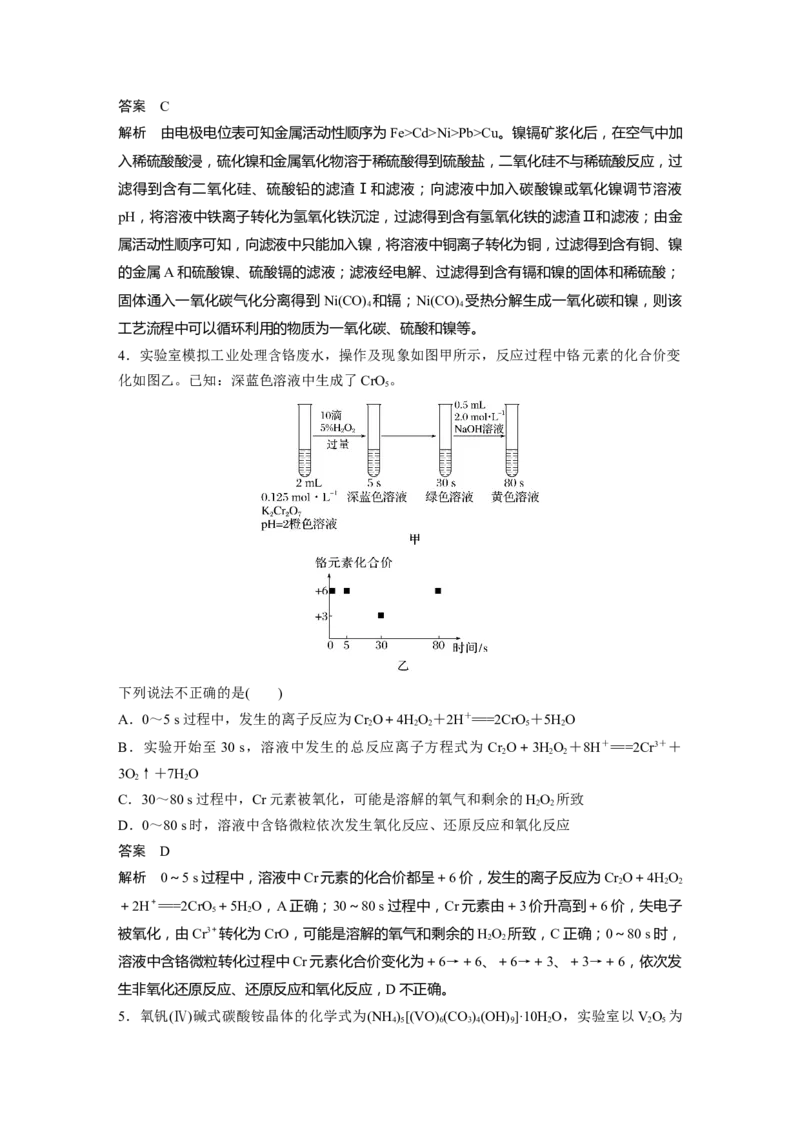
4.实验室模拟工业处理含铬废水,操作及现象如图甲所示,反应过程中铬元素的化合价变
化如图乙。已知:深蓝色溶液中生成了CrO。
5
下列说法不正确的是( )
A.0~5 s过程中,发生的离子反应为Cr O+4HO+2H+===2CrO+5HO
2 2 2 5 2
B.实验开始至30 s,溶液中发生的总反应离子方程式为 Cr O+3HO +8H+===2Cr3++
2 2 2
3O↑+7HO
2 2
C.30~80 s过程中,Cr元素被氧化,可能是溶解的氧气和剩余的HO 所致
2 2
D.0~80 s时,溶液中含铬微粒依次发生氧化反应、还原反应和氧化反应
答案 D
解析 0~5 s过程中,溶液中Cr元素的化合价都呈+6价,发生的离子反应为Cr O+4HO
2 2 2
+2H+===2CrO +5HO,A正确;30~80 s过程中,Cr元素由+3价升高到+6价,失电子
5 2
被氧化,由Cr3+转化为CrO,可能是溶解的氧气和剩余的HO 所致,C正确;0~80 s时,
2 2
溶液中含铬微粒转化过程中Cr元素化合价变化为+6→+6、+6→+3、+3→+6,依次发
生非氧化还原反应、还原反应和氧化反应,D不正确。
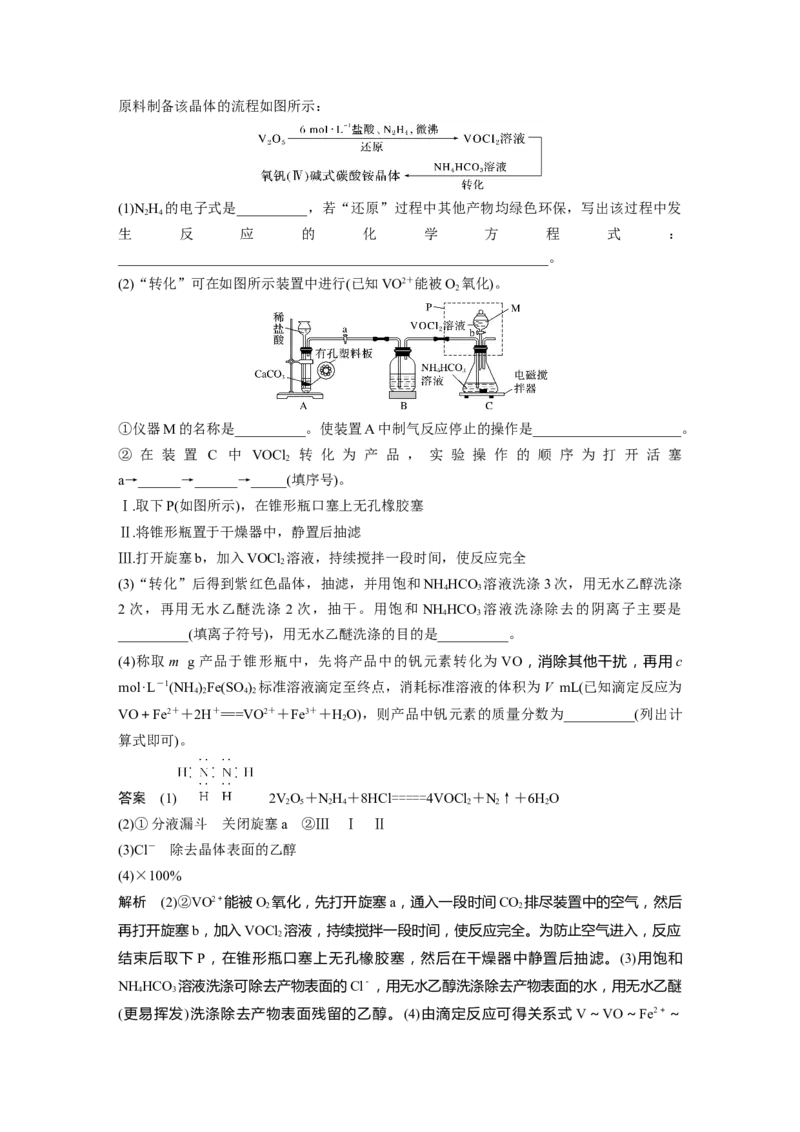
5.氧钒(Ⅳ)碱式碳酸铵晶体的化学式为(NH )[(VO) (CO)(OH) ]·10H O,实验室以VO 为
4 5 6 3 4 9 2 2 5原料制备该晶体的流程如图所示:
(1)N H 的电子式是__________,若“还原”过程中其他产物均绿色环保,写出该过程中发
2 4
生 反 应 的 化 学 方 程 式 :
_____________________________________________________________。
(2)“转化”可在如图所示装置中进行(已知VO2+能被O 氧化)。
2
①仪器M的名称是__________。使装置A中制气反应停止的操作是_____________________。
② 在 装 置 C 中 VOCl 转 化 为 产 品 , 实 验 操 作 的 顺 序 为 打 开 活 塞
2
a→______→______→_____(填序号)。
Ⅰ.取下P(如图所示),在锥形瓶口塞上无孔橡胶塞
Ⅱ.将锥形瓶置于干燥器中,静置后抽滤
Ⅲ.打开旋塞b,加入VOCl 溶液,持续搅拌一段时间,使反应完全
2
(3)“转化”后得到紫红色晶体,抽滤,并用饱和NH HCO 溶液洗涤3次,用无水乙醇洗涤
4 3
2次,再用无水乙醚洗涤 2次,抽干。用饱和 NH HCO 溶液洗涤除去的阴离子主要是
4 3
__________(填离子符号),用无水乙醚洗涤的目的是__________。
(4)称取m g产品于锥形瓶中,先将产品中的钒元素转化为 VO,消除其他干扰,再用c
mol·L-1(NH )Fe(SO ) 标准溶液滴定至终点,消耗标准溶液的体积为V mL(已知滴定反应为
4 2 4 2
VO+Fe2++2H+===VO2++Fe3++HO),则产品中钒元素的质量分数为__________(列出计
2
算式即可)。
答案 (1) 2VO+NH+8HCl=====4VOCl +N↑+6HO
2 5 2 4 2 2 2
(2)①分液漏斗 关闭旋塞a ②Ⅲ Ⅰ Ⅱ
(3)Cl- 除去晶体表面的乙醇
(4)×100%
解析 (2)②VO2+能被O 氧化,先打开旋塞a,通入一段时间CO 排尽装置中的空气,然后
2 2
再打开旋塞b,加入VOCl 溶液,持续搅拌一段时间,使反应完全。为防止空气进入,反应
2
结束后取下P,在锥形瓶口塞上无孔橡胶塞,然后在干燥器中静置后抽滤。(3)用饱和
NH HCO 溶液洗涤可除去产物表面的Cl-,用无水乙醇洗涤除去产物表面的水,用无水乙醚
4 3
(更易挥发)洗涤除去产物表面残留的乙醇。(4)由滴定反应可得关系式 V~VO~Fe2+~(NH )Fe(SO ),n(V)=cV×10-3mol,故产品中钒元素的质量分数为×100%。
4 2 4 2
6.(2023·银川一中三模)HDS催化剂广泛用于石油炼制和化学工业生产中,通常利用加碱焙
烧-水浸取法从HDS废催化剂(主要成分为MoS、NiS、VO 、Al O)中提取贵重金属钒和钼,
2 5 2 3
其工艺流程如图所示。
已知:Ⅰ.MoO、VO、Al O 均可与纯碱反应生成对应的钠盐,而NiO不行。
3 2 5 2 3
Ⅱ.高温下,NH VO 易分解产生N 和一种含氮元素的气体。
4 3 2
回答下列问题:
(1)“浸渣”的成分为______(填化学式);“滤液2”中的成分除了 NaMoO 外,还含有
2 4
______(填化学式)。
(2) 请 写 出 “ 焙 烧 ” 过 程 中 MoS 及 Al O 分 别 与 纯 碱 反 应 的 化 学 方 程 式 :
2 3
__________________,____________________________________。
(3)“沉钒”时提钒率随初始钒的浓度及氯化铵的加入量的关系如图所示,则选择的初始钒
的浓度和NH Cl的加入量分别为______、______。
4
(4)“沉钒”时生成NH VO 沉淀,则“煅烧”后生成氧化产物和还原产物的物质的量之比为
4 3
________________。
答案 (1)NiO NaVO 、NaHCO (2)2MoS+2NaCO +5O=====2NaMoO +2CO +2SO
3 3 2 3 2 2 4 2 2
Al O+NaCO=====2NaAlO +CO↑ (3)20 g·L-1 10 g·L-1 (4)2∶3
2 3 2 3 2 2
解析 (1)硫化物焙烧时生成氧化物和二氧化硫,由于NiO不能与碳酸钠反应,故“水浸”
时以“浸渣”的形式沉淀出来,而MoO 、VO 、Al O 与纯碱反应生成NaMoO 、NaVO
3 2 5 2 3 2 4 3
和 NaAlO ,通入过量 CO 生成沉淀 Al(OH) 和 NaHCO ,故“滤液 2”中的成分除了
2 2 3 3
NaMoO 外,还含有 NaVO 、NaHCO 。(4)由信息和流程及氧化还原反应原理可知,
2 4 3 3
NH VO 沉淀煅烧时分解产生VO、N 和NH ,故反应的化学方程式为6NH VO =====3VO
4 3 2 3 2 3 4 3 2 3
+2N↑+2NH ↑+9HO,氧化产物为N,还原产物为VO,故比值为2∶3。
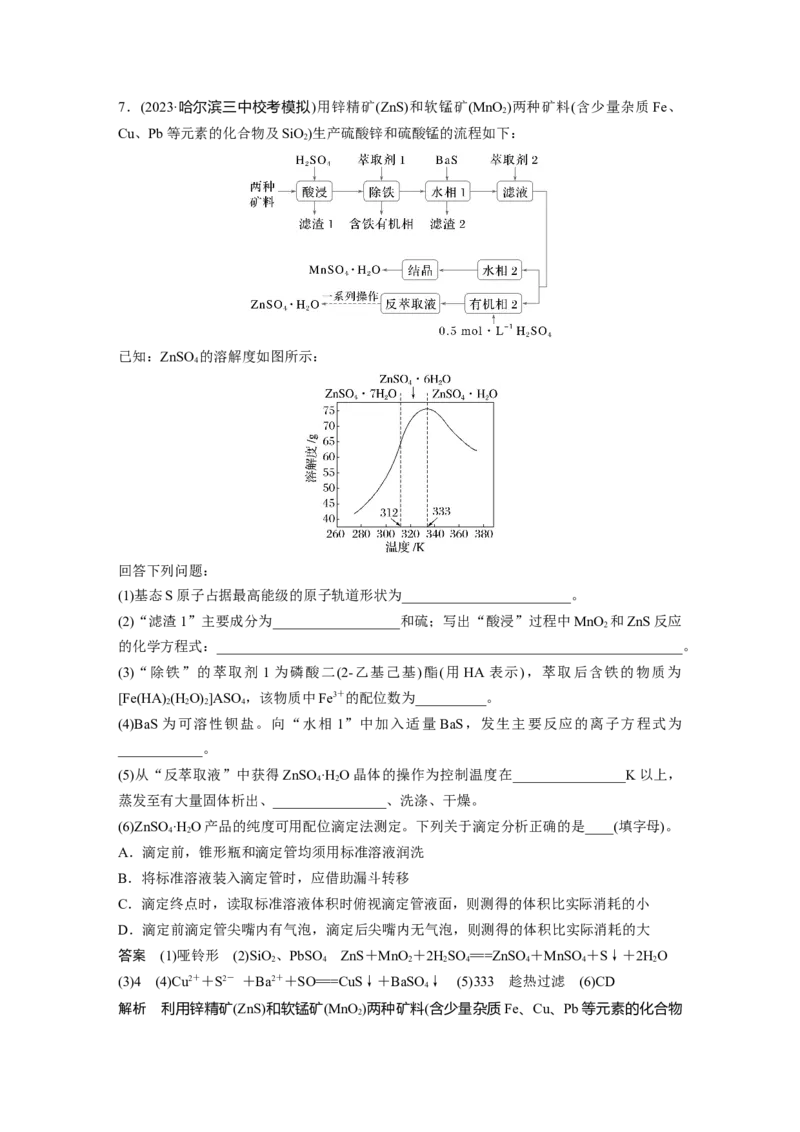
2 3 2 2 2 37.(2023·哈尔滨三中校考模拟)用锌精矿(ZnS)和软锰矿(MnO )两种矿料(含少量杂质Fe、
2
Cu、Pb等元素的化合物及SiO)生产硫酸锌和硫酸锰的流程如下:
2
已知:ZnSO 的溶解度如图所示:
4
回答下列问题:
(1)基态S原子占据最高能级的原子轨道形状为________________________。
(2)“滤渣1”主要成分为__________________和硫;写出“酸浸”过程中MnO 和ZnS反应
2
的化学方程式:__________________________________________________________________。
(3)“除铁”的萃取剂 1 为磷酸二(2-乙基己基)酯(用 HA 表示),萃取后含铁的物质为
[Fe(HA) (H O) ]ASO ,该物质中Fe3+的配位数为__________。
2 2 2 4
(4)BaS 为可溶性钡盐。向“水相 1”中加入适量 BaS,发生主要反应的离子方程式为
____________。
(5)从“反萃取液”中获得ZnSO·H O晶体的操作为控制温度在________________K以上,
4 2
蒸发至有大量固体析出、________________、洗涤、干燥。
(6)ZnSO ·H O产品的纯度可用配位滴定法测定。下列关于滴定分析正确的是____(填字母)。
4 2
A.滴定前,锥形瓶和滴定管均须用标准溶液润洗
B.将标准溶液装入滴定管时,应借助漏斗转移
C.滴定终点时,读取标准溶液体积时俯视滴定管液面,则测得的体积比实际消耗的小
D.滴定前滴定管尖嘴内有气泡,滴定后尖嘴内无气泡,则测得的体积比实际消耗的大
答案 (1)哑铃形 (2)SiO、PbSO ZnS+MnO +2HSO ===ZnSO+MnSO +S↓+2HO
2 4 2 2 4 4 4 2
(3)4 (4)Cu2++S2- +Ba2++SO===CuS↓+BaSO↓ (5)333 趁热过滤 (6)CD
4
解析 利用锌精矿(ZnS)和软锰矿(MnO )两种矿料(含少量杂质Fe、Cu、Pb等元素的化合物
2及SiO)生产硫酸锌和硫酸锰的流程中,加硫酸酸浸,锌、铁、铜、锰生成硫酸盐,硫酸铅
2
为沉淀和二氧化硅一起进入滤渣1,萃取剂1溶解铁离子,加入BaS,除去铜离子和硫酸根
离子,萃取剂2萃取硫酸锌,水相为硫酸锰,进一步得到MnSO ·H O,有机相为硫酸锌,
4 2
进一步反萃取得到ZnSO·H O。(6)滴定前,锥形瓶不须用标准溶液润洗,A错误;滴定终
4 2
点时,读取标准溶液体积时俯视滴定管液面,则测得的体积比实际消耗的小,C正确;滴定
前滴定管尖嘴内有气泡,滴定后尖嘴内无气泡,则测得的体积比实际消耗的大,D正确。