文档内容
第 66 讲 生物大分子 合成高分子
[复习目标] 1.了解糖类、核酸、氨基酸、蛋白质和有机高分子材料的组成、结构特点、主
要化学性质及应用。2.了解糖类、氨基酸和蛋白质在生命过程中的作用,了解脱氧核糖核酸、
核糖核酸的生物功能。3.掌握合成高分子的两大基本反应的特点及应用。
考点一 糖类 核酸
1.糖类
(1)糖类的概念和分类
①概念:从分子结构上看,糖类是多羟基醛、多羟基酮和它们的脱水缩合物。
②组成:碳、氢、氧三种元素。大多数糖类化合物的通式为C (H O) ,所以糖类也叫碳水化
m 2 n
合物。
③分类
(2)单糖
①a. 葡 萄 糖 : 多 羟 基 醛 CHOH(CHOH) CHO , 它 与 果 糖 [ 多 羟 基 酮
2 4
]互为同分异构体。
b.葡萄糖的性质
②戊糖——核糖、脱氧核糖
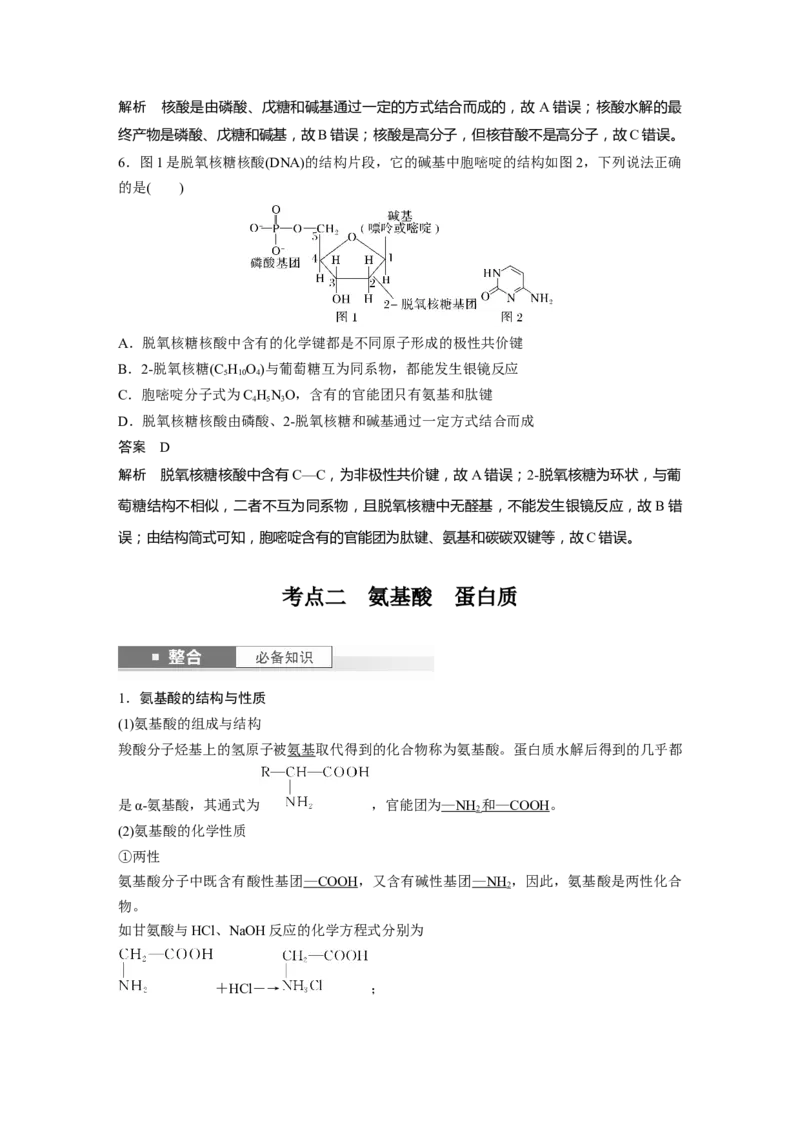
核糖和脱氧核糖是生物体的遗传物质——核酸的重要组成部分。分子式 环式结构简式
核糖 C H O
5 10 5
脱氧核糖 C H O
5 10 4
(3)二糖——蔗糖与麦芽糖
比较项目 蔗糖 麦芽糖
分子式 均为C H O
12 22 11
相同点
性质 都能发生水解反应
是否含醛基 不含 含有
不同点
水解产物 葡萄糖和果糖 葡萄糖
相互关系 互为同分异构体
(4)多糖——淀粉与纤维素
①相似点
a.都属于天然有机高分子,属于多糖,分子式都可表示为(C H O)。
6 10 5 n
b.都能发生水解反应,如淀粉水解的化学方程式为(C H O)+nHO――→nC H O。
6 10 5 n 2 6 12 6
_ 淀粉________________葡萄糖
c.都不能发生银镜反应。
②不同点
a.通式中n值不同。
b.淀粉溶液遇碘显蓝色。
2.核酸
(1)核糖核酸的形成
(2)脱氧核糖核酸的形成
(3)核酸的生物功能
核酸在生物体的生长、繁殖、遗传和变异等生命现象中起着重要的作用。1.糖类物质的分子通式都可用C (H O) 来表示( )
m 2 n
2.核酸由C、H、O、N四种元素组成( )
3.所有糖类均可以发生水解反应( )
4.医学上常用新制的Cu(OH) 检验尿液中的葡萄糖( )
2
5.核酸是生物体内具有遗传功能的生物大分子( )
6.淀粉在人体内直接水解生成葡萄糖,供人体组织的营养需要( )
7.纤维素在人体消化过程中起重要作用,纤维素可以作为人类的营养物质( )
8.淀粉、纤维素均为天然有机高分子,且二者互为同分异构体( )
答案 1.× 2.× 3.× 4.√ 5.√ 6.× 7.× 8.×
一、糖类的结构和性质
1.唐代张九龄诗句“松叶堪为酒,春来酿几多”涉及淀粉、麦芽糖、葡萄糖、乙醇等化学
物质,下列有关说法错误的是( )
A.淀粉、乙醇所含元素种类相同
B.蔗糖和麦芽糖、淀粉和纤维素都互为同分异构体
C.麦芽糖、葡萄糖都能被新制的Cu(OH) 氧化
2
D.淀粉、麦芽糖都能发生水解反应,最终生成葡萄糖
答案 B
解析 蔗糖和麦芽糖的分子式都是C H O ,互为同分异构体;淀粉和纤维素均属于多糖,
12 22 11
分子式均为(C H O),但聚合度n不同,二者不互为同分异构体,故B错误。
6 10 5 n
2.我国科学家在实验室中首次实现用二氧化碳合成淀粉,成为当今世界的一项颠覆性技术。
下列相关说法正确的是( )
A.淀粉在人体内代谢后转化成果糖
B.这种合成淀粉和天然形成的淀粉化学性质不同
C.此项技术有助于我国在未来实现“碳中和”
D.淀粉是二氧化碳分子的多聚体
答案 C
解析 淀粉可在人体内代谢后转化成葡萄糖,故 A错误;合成淀粉和天然形成的淀粉化学
性质相同,故B错误。
二、糖类的水解实验
3.下列实验结论正确的是( )
选项 实验操作 现象 结论
A 淀粉溶液中加入碘水 溶液变蓝 说明淀粉没有水解将乙醇与酸性重铬酸钾
B 橙色溶液变为绿色 乙醇具有氧化性
(K Cr O)溶液混合
2 2 7
蔗糖溶液中加入稀硫酸,水解
C 未出现银镜 水解的产物为非还原糖
后加入银氨溶液,水浴加热
将新制的Cu(OH) 与葡萄糖溶
2
D 产生砖红色沉淀(Cu O) 葡萄糖具有还原性
2
液混合加热
答案 D
解析 A项,也有可能是淀粉部分水解,错误;B项,重铬酸钾具有强氧化性,能把乙醇氧
化,橙色溶液变为绿色,说明乙醇具有还原性,错误;C项,发生银镜反应需要在碱性条件
下进行,错误;D项,实验表明葡萄糖被氧化,说明葡萄糖具有还原性,正确。
4.某同学为了检验纤维素的水解产物是否为葡萄糖,他将纤维素与 70%的硫酸共热后加入
新制的Cu(OH) 并加热煮沸,无砖红色沉淀生成,下列解释正确的是( )
2
A.纤维素水解产物中无葡萄糖
B.使用的硫酸过浓只发生了脱水反应
C.由于水解后混合液中含有HSO ,所以见不到砖红色沉淀
2 4
D.加热时间不够长,所以见不到砖红色沉淀
答案 C
解析 葡萄糖与新制的Cu(OH) 反应必须在碱性环境下,因而纤维素水解后应先加入 NaOH
2
溶液中和硫酸,再和新制的Cu(OH) 反应。
2
三、核酸的组成与生物功能
5.核酸是生命的基础物质,是病毒的“身份证”。下列关于核酸的叙述正确的是( )
A.核酸是核蛋白的非蛋白部分,也是由氨基酸残基组成的
B.核酸水解产物中含有磷酸、葡萄糖和碱基
C.核酸、核苷酸都是高分子
D.核酸有核糖核酸和脱氧核糖核酸两类,对蛋白质的合成和生物遗传起重要作用
答案 D解析 核酸是由磷酸、戊糖和碱基通过一定的方式结合而成的,故 A错误;核酸水解的最
终产物是磷酸、戊糖和碱基,故B错误;核酸是高分子,但核苷酸不是高分子,故C错误。
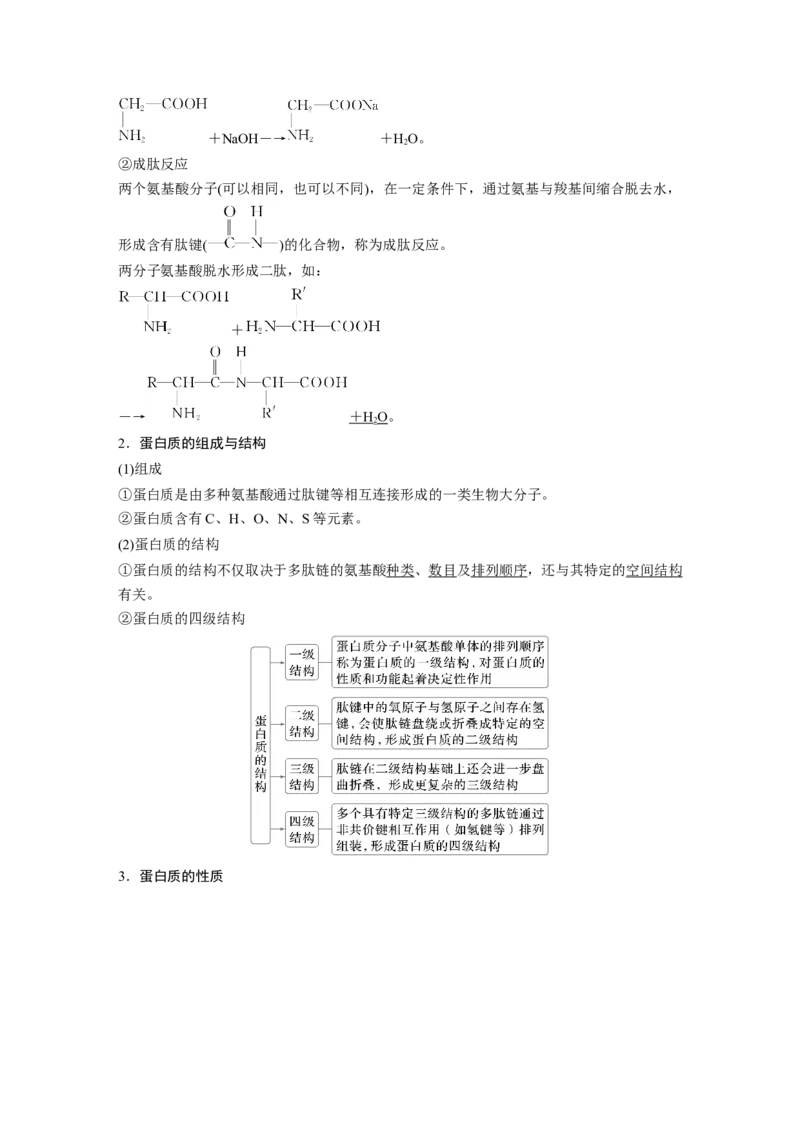
6.图1是脱氧核糖核酸(DNA)的结构片段,它的碱基中胞嘧啶的结构如图2,下列说法正确
的是( )
A.脱氧核糖核酸中含有的化学键都是不同原子形成的极性共价键
B.2-脱氧核糖(C H O)与葡萄糖互为同系物,都能发生银镜反应
5 10 4
C.胞嘧啶分子式为C HNO,含有的官能团只有氨基和肽键
4 5 3
D.脱氧核糖核酸由磷酸、2-脱氧核糖和碱基通过一定方式结合而成
答案 D
解析 脱氧核糖核酸中含有C—C,为非极性共价键,故A错误;2-脱氧核糖为环状,与葡
萄糖结构不相似,二者不互为同系物,且脱氧核糖中无醛基,不能发生银镜反应,故B错
误;由结构简式可知,胞嘧啶含有的官能团为肽键、氨基和碳碳双键等,故C错误。
考点二 氨基酸 蛋白质
1.氨基酸的结构与性质
(1)氨基酸的组成与结构
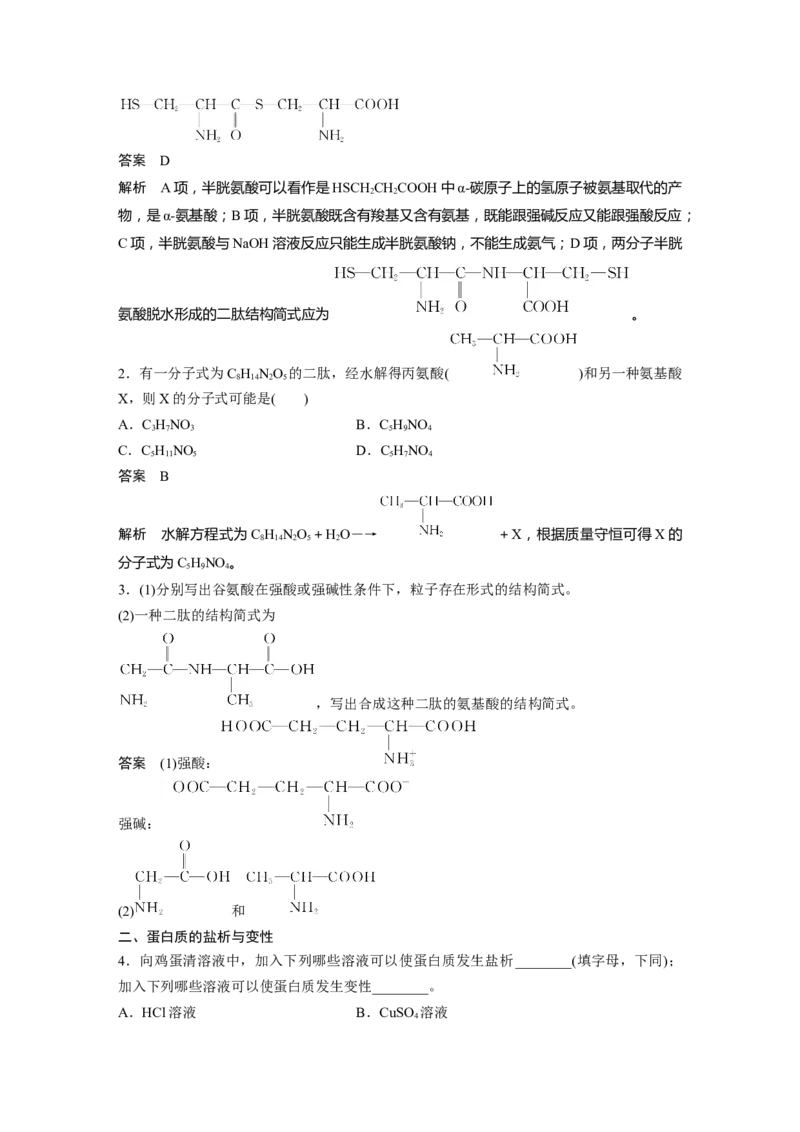
羧酸分子烃基上的氢原子被氨基取代得到的化合物称为氨基酸。蛋白质水解后得到的几乎都
是α-氨基酸,其通式为 ,官能团为 — NH 和— COOH 。
2
(2)氨基酸的化学性质
①两性
氨基酸分子中既含有酸性基团 — COOH ,又含有碱性基团 — NH ,因此,氨基酸是两性化合
2
物。
如甘氨酸与HCl、NaOH反应的化学方程式分别为
+HCl―→ ;+NaOH―→ +HO。
2
②成肽反应
两个氨基酸分子(可以相同,也可以不同),在一定条件下,通过氨基与羧基间缩合脱去水,
形成含有肽键( )的化合物,称为成肽反应。
两分子氨基酸脱水形成二肽,如:
+
―→ + H O。
2
2.蛋白质的组成与结构
(1)组成
①蛋白质是由多种氨基酸通过肽键等相互连接形成的一类生物大分子。
②蛋白质含有C、H、O、N、S等元素。
(2)蛋白质的结构
①蛋白质的结构不仅取决于多肽链的氨基酸种类、数目及排列顺序,还与其特定的空间结构
有关。
②蛋白质的四级结构
3.蛋白质的性质4.酶
(1)大部分酶是蛋白质,具有蛋白质的性质。
(2)酶是一种生物催化剂,催化作用具有以下特点:
①条件温和;
②具有高度的专一性;
③具有高效催化作用。
1.氨基酸是两性化合物,能与酸、碱反应生成盐( )
2.α-氨基丙酸与α-氨基苯丙酸混合脱水成肽,只生成2种二肽( )
3.天然氨基酸均为无色晶体,一般能溶于水,难溶于乙醇、乙醚等有机溶剂( )
4.高温或日常用的消毒剂可使病毒蛋白质变性( )
5.用浓NaSO 、CuSO 溶液或浓HNO 使蛋清发生盐析,进而分离、提纯蛋白质( )
2 4 4 3
答案 1.√ 2.× 3.√ 4.√ 5.×
一、氨基酸及成肽反应
1.科学家发现半胱氨酸能增强艾滋病病毒感染者的免疫力,对控制艾滋病病毒的蔓延有奇
效。已知半胱氨酸的结构简式为 ,则下列说法错误的是( )
A.半胱氨酸属于α-氨基酸
B.半胱氨酸既能跟强酸反应又能跟强碱反应
C.半胱氨酸不能与NaOH溶液反应放出碱性气体
D.两分子半胱氨酸脱水形成的二肽结构简式为答案 D
解析 A项,半胱氨酸可以看作是HSCH CHCOOH中α-碳原子上的氢原子被氨基取代的产
2 2
物,是α-氨基酸;B项,半胱氨酸既含有羧基又含有氨基,既能跟强碱反应又能跟强酸反应;
C项,半胱氨酸与NaOH溶液反应只能生成半胱氨酸钠,不能生成氨气;D项,两分子半胱
氨酸脱水形成的二肽结构简式应为 。
2.有一分子式为C H NO 的二肽,经水解得丙氨酸( )和另一种氨基酸
8 14 2 5
X,则X的分子式可能是( )
A.C HNO B.C HNO
3 7 3 5 9 4
C.C H NO D.C HNO
5 11 5 5 7 4
答案 B
解析 水解方程式为C H NO +HO―→ +X,根据质量守恒可得X的
8 14 2 5 2
分子式为C HNO 。
5 9 4
3.(1)分别写出谷氨酸在强酸或强碱性条件下,粒子存在形式的结构简式。
(2)一种二肽的结构简式为
,写出合成这种二肽的氨基酸的结构简式。
答案 (1)强酸:
强碱:
(2) 和
二、蛋白质的盐析与变性
4.向鸡蛋清溶液中,加入下列哪些溶液可以使蛋白质发生盐析________(填字母,下同);
加入下列哪些溶液可以使蛋白质发生变性________。
A.HCl溶液 B.CuSO 溶液
4C.(NH )SO 溶液 D.甲醛溶液
4 2 4
E.酒精溶液 F.NaOH溶液
G.NaSO 溶液 H.Pb(Ac) 溶液
2 4 2
答案 CG ABDEFH
5.请比较蛋白质的盐析和变性的区别有哪些?举例说明盐析和变性的作用。
答案 蛋白质的盐析是物理变化,是可逆的,加水可以溶解;蛋白质的变性是化学变化,是
不可逆的,加水不溶解。盐析可用于分离、提纯蛋白质,而变性可用于进行消毒、杀菌。
蛋白质的盐析与变性比较
盐析 变性
蛋白质在某些可溶性盐的浓溶液 在某些物理或化学因素的影响下,蛋白质的
概念
中因溶解度降低而析出 性质和生理功能发生改变的现象
特征 可逆 不可逆
实质 溶解度降低,物理变化 结构、性质改变,化学变化
碱金属、镁、铝等轻金属盐和铵 加热、强酸、强碱、强氧化剂、紫外线、重
条件
盐的浓溶液 金属盐、苯酚、甲醛、乙醇等
用途 分离、提纯蛋白质 杀菌、消毒、保存标本
硫酸铵或硫酸钠等盐溶液使蛋白
实例 重金属盐(例如硫酸铜)溶液能使蛋白质变性
质盐析
考点三 合成高分子
1.高分子的结构特点
(1)单体:能够进行聚合反应形成高分子的小分子化合物。
(2)链节:高分子中化学组成相同、可重复的最小结构单元。
(3)聚合度:高分子链中含有链节的数目。
2.合成高分子的两个基本反应
加聚反应 缩聚反应
由不饱和单体加成聚合生成高分 单体分子间通过缩合反应生成高分子的反
概念
子的反应 应,生成缩聚物的同时,还伴有小分子的副产物(如水、氨、卤化氢等)的生成
单体 含有两个或两个以上的反应基团(如—OH、
含有双键或三键的不饱和有机物
特点 —COOH、—NH 、—X等)
2
产物 高聚物与单体具有相同的组成, 生成高聚物和小分子,高聚物与单体有不同
特征 生成物一般为线型结构 的组成
3.高分子的分类及性质特点
其中,塑料、合成纤维、合成橡胶又被称为“三大合成材料”。
1.加聚反应单体有一种,而缩聚反应的单体应该有两种( )
2.氨基酸分子间可发生缩聚反应( )
3.缩聚反应生成小分子的化学计量数为(n-1)( )
4. 是由苯酚和甲醛发生加成反应后的产物脱水缩合而成的( )
5.天然橡胶是高聚物,不能使溴水褪色( )
6.酚醛树脂和聚氯乙烯都是热固性塑料( )
7.聚乙烯可包装食品,而聚氯乙烯塑料不可用于包装食品( )
8.橡胶的老化实质上发生的是酯化反应( )
9. 的结构中含有酯基( )
10.单体与由该单体形成的高聚物具有相同的性质( )
答案 1.× 2.√ 3.× 4.√ 5.× 6.× 7.√ 8.× 9.√ 10.×一、有机高分子材料的概述
1.下列对有机高分子的认识正确的是( )
A.有机高分子被称为聚合物或高聚物,是因为它们大部分是由高分子通过聚合反应得到的
B.有机高分子的相对分子质量很大,因而其结构很复杂
C.对于一块高分子材料来说,n是一个整数值,因而它的相对分子质量是确定的
D.高分子材料可分为天然高分子材料和合成高分子材料两大类
答案 D
解析 高分子主要是由小分子通过聚合反应制得的,故 A错误;有机高分子的相对分子质
量很大,但与结构无关,有的简单,有的复杂,故B错误;对于一块高分子材料,n是一个
整数值,由于n不确定,所以它的相对分子质量也不确定,故C错误。
2.食品保鲜膜按材质分为聚乙烯(PE)、聚氯乙烯(PVC)等种类。PE保鲜膜可直接接触食品,
PVC保鲜膜则不能直接接触食品,它对人体有潜在危害。下列有关叙述不正确的是( )
A.PE、PVC都属于链状高分子,受热易熔化
B.PE、PVC均能使溴水褪色,它们的单体都是不饱和烃
C.焚烧PVC保鲜膜会放出有毒气体,如HCl
D.废弃的PE和PVC均可回收利用以减少白色污染
答案 B
3.四氯乙烯( )是一种衣物干洗剂,聚四氟乙烯( )是家用不粘锅内
侧涂层的主要成分。下列关于四氯乙烯和聚四氟乙烯的叙述正确的是( )
A.它们都可以由乙烯发生加成反应得到
B.它们的分子中都不含氢原子
C.四氯乙烯对油脂有较好的溶解作用,聚四氟乙烯的化学性质比较活泼
D.它们都能发生加成反应,都能使酸性高锰酸钾溶液褪色
答案 B
解析 四氯乙烯可由乙炔发生取代、加成反应得到,聚四氟乙烯是由四氟乙烯发生加聚反应
得到,故A错误;二者都只含C和卤素原子,故B正确;聚四氟乙烯中不含碳碳不饱和键,
性质较稳定,不能发生加成反应,不能使酸性高锰酸钾溶液褪色,故C、D错误。
4.(2023·重庆模拟)聚乙烯(CH—CH)可用于制作食品包装袋,在一定条件下可通过乙
2 2
烯的加聚反应生成聚乙烯,下列说法正确的是( )
A.等质量的乙烯和聚乙烯完全燃烧时,聚乙烯消耗的氧气多
B.工业合成的聚乙烯高分子的聚合度是相同的C.乙烯是纯净物,常温下为气态;聚乙烯也是纯净物,常温下为固态
D.聚乙烯链节中碳元素的质量分数与其单体中碳元素的质量分数相等
答案 D
解析 乙烯是聚乙烯的单体,它们的最简式相同,都是CH ,故含C和H的质量分数分别
2
相等,则等质量的二者完全燃烧时消耗氧气的量相同,故A错误、D正确;工业上用乙烯
合成聚乙烯时,所得高分子的聚合度一般不等,故B错误。
二、聚合方程式的书写
5.按要求完成下列方程式。
(1)加聚反应
①nCH==CH—CH ――→ 。
2 3
②nCH==CH—CH==CH――→CH—CH==CH—CH 。
2 2 2 2
③nCH==CH+ ――→ 。
2 2
(2)缩聚反应
①nHOCH —CHOH + nHOOC—COOH + ( 2 n -
2 2
1)H O;
2
nHOCH —CH—COOH + ( n - 1)H O。
2 2 2
②nHN—CH COOH――→ +(n-1)H O;
2 2 2
nHNCH COOH+ ――→
2 2
+ ( 2 n - 1)H O。
2
③nHCHO+n ――→ ( n - 1)H O + 。
2
1.加聚反应的书写方法
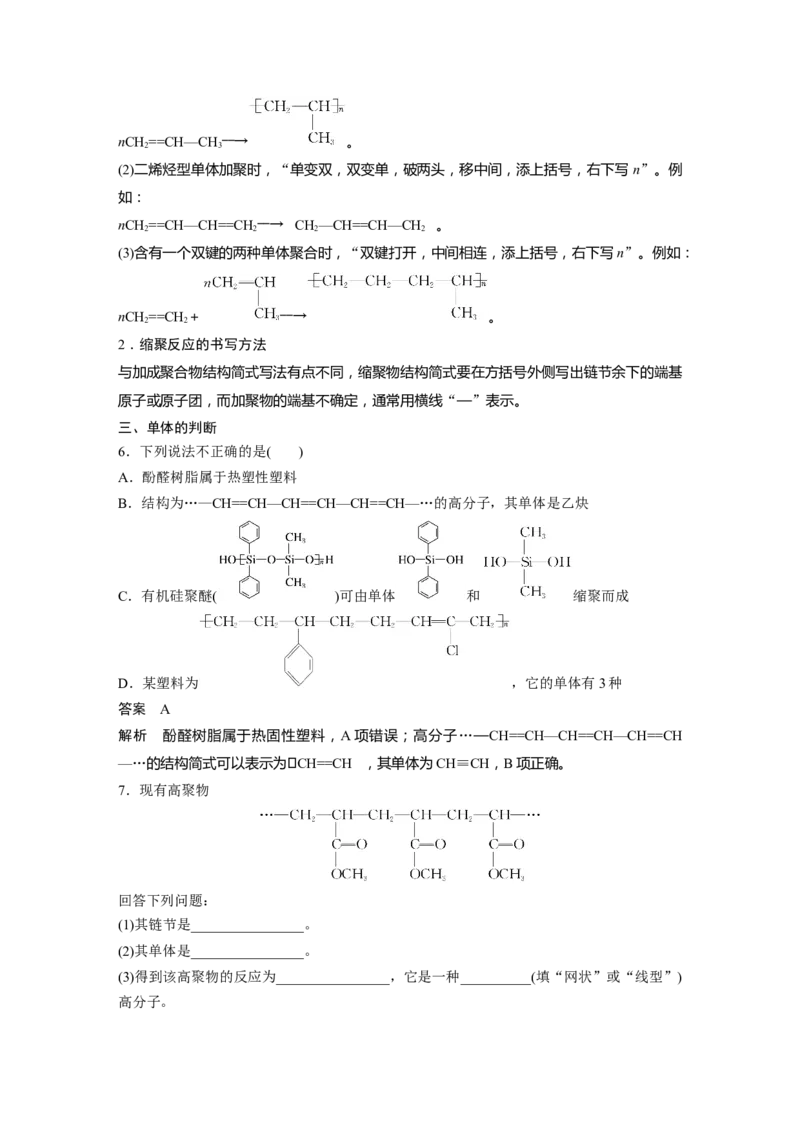
(1)单烯烃型单体加聚时,“断开双键,键分两端,添上括号,右下写n”。例如:nCH==CH—CH ――→ 。
2 3
(2)二烯烃型单体加聚时,“单变双,双变单,破两头,移中间,添上括号,右下写n”。例
如:
nCH==CH—CH==CH――→CH—CH==CH—CH 。
2 2 2 2
(3)含有一个双键的两种单体聚合时,“双键打开,中间相连,添上括号,右下写n”。例如:
nCH==CH+ ――→ 。
2 2
2.缩聚反应的书写方法
与加成聚合物结构简式写法有点不同,缩聚物结构简式要在方括号外侧写出链节余下的端基
原子或原子团,而加聚物的端基不确定,通常用横线“—”表示。
三、单体的判断
6.下列说法不正确的是( )
A.酚醛树脂属于热塑性塑料
B.结构为…—CH==CH—CH==CH—CH==CH—…的高分子,其单体是乙炔
C.有机硅聚醚( )可由单体 和 缩聚而成
D.某塑料为 ,它的单体有3种
答案 A
解析 酚醛树脂属于热固性塑料,A项错误;高分子…—CH==CH—CH==CH—CH==CH
—…的结构简式可以表示为CH==CH,其单体为CH≡CH,B项正确。
7.现有高聚物
回答下列问题:
(1)其链节是________________。
(2)其单体是________________。
(3)得到该高聚物的反应为________________,它是一种__________(填“网状”或“线型”)
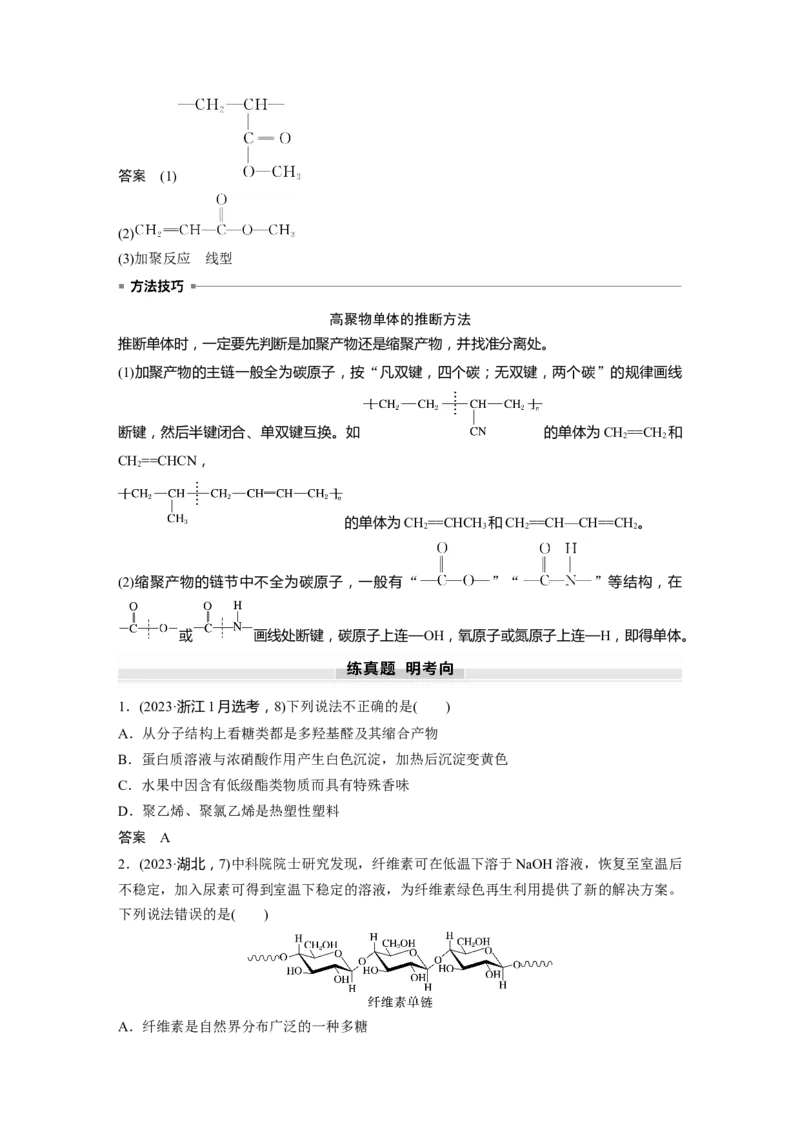
高分子。答案 (1)
(2)
(3)加聚反应 线型
高聚物单体的推断方法
推断单体时,一定要先判断是加聚产物还是缩聚产物,并找准分离处。
(1)加聚产物的主链一般全为碳原子,按“凡双键,四个碳;无双键,两个碳”的规律画线
断键,然后半键闭合、单双键互换。如 的单体为CH==CH 和
2 2
CH==CHCN,
2
的单体为CH==CHCH 和CH==CH—CH==CH。
2 3 2 2
(2)缩聚产物的链节中不全为碳原子,一般有“ ”“ ”等结构,在
或 画线处断键,碳原子上连—OH,氧原子或氮原子上连—H,即得单体。
1.(2023·浙江1月选考,8)下列说法不正确的是( )
A.从分子结构上看糖类都是多羟基醛及其缩合产物
B.蛋白质溶液与浓硝酸作用产生白色沉淀,加热后沉淀变黄色
C.水果中因含有低级酯类物质而具有特殊香味
D.聚乙烯、聚氯乙烯是热塑性塑料
答案 A
2.(2023·湖北,7)中科院院士研究发现,纤维素可在低温下溶于NaOH溶液,恢复至室温后
不稳定,加入尿素可得到室温下稳定的溶液,为纤维素绿色再生利用提供了新的解决方案。
下列说法错误的是( )
A.纤维素是自然界分布广泛的一种多糖B.纤维素难溶于水的主要原因是其链间有多个氢键
C.NaOH提供OH-破坏纤维素链之间的氢键
D.低温降低了纤维素在NaOH溶液中的溶解性
答案 D
解析 纤维素分子中含羟基,羟基之间形成氢键,导致纤维素分子难与水分子形成氢键,B
正确;氢氧化钠中的OH-主要破坏纤维素链间的氢键,促进其溶解,C正确;低温下纤维
素可溶于氢氧化钠溶液,而恢复至室温后不稳定,所以低温增强了纤维素在氢氧化钠溶液中
的溶解性,D错误。
3.(2021·河北,2)高分子材料在生产生活中应用广泛。下列说法错误的是( )
A.芦苇可用于制造黏胶纤维,其主要成分为纤维素
B.聚氯乙烯通过加聚反应制得,可用于制作不粘锅的耐热涂层
C.淀粉是相对分子质量可达几十万的天然高分子物质
D.大豆蛋白纤维是一种可降解材料
答案 B
解析 芦苇中含有天然纤维素,可用于制造黏胶纤维,故 A正确;聚氯乙烯在高温下会分
解生成有毒气体,因此不能用于制作不粘锅的耐热涂层,故B错误;淀粉为多糖,其相对
分子质量可达几十万,属于天然高分子物质,故C正确;大豆蛋白纤维的主要成分为蛋白
质,能够被微生物分解,因此大豆蛋白纤维是一种可降解材料,故D正确。
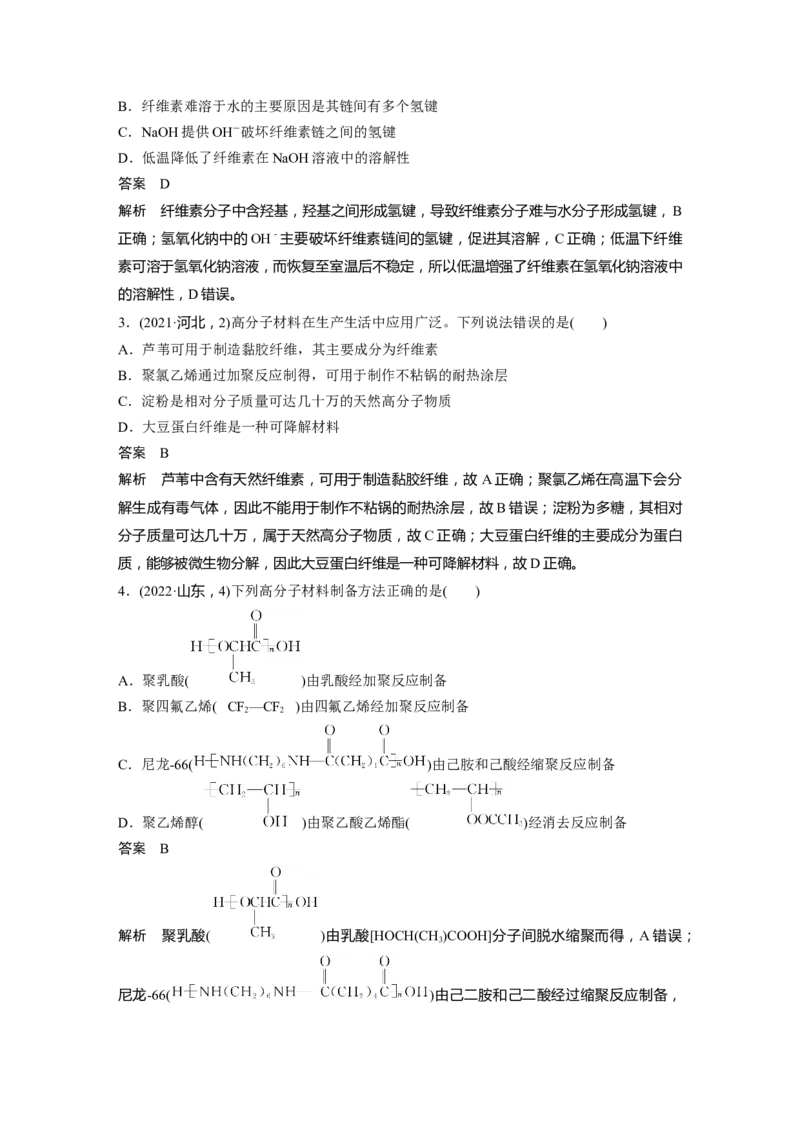
4.(2022·山东,4)下列高分子材料制备方法正确的是( )
A.聚乳酸( )由乳酸经加聚反应制备
B.聚四氟乙烯(CF—CF)由四氟乙烯经加聚反应制备
2 2
C.尼龙-66( )由己胺和己酸经缩聚反应制备
D.聚乙烯醇( )由聚乙酸乙烯酯( )经消去反应制备
答案 B
解析 聚乳酸( )由乳酸[HOCH(CH )COOH]分子间脱水缩聚而得,A错误;
3
尼龙-66( )由己二胺和己二酸经过缩聚反应制备,C错误;聚乙烯醇( )由聚乙酸乙烯酯( )经水解反应制备,D
错误。
5.(2023·北京,9)一种聚合物PHA的结构简式如图所示,下列说法不正确的是( )
A.PHA的重复单元中有两种官能团
B.PHA通过单体 缩聚合成
C.PHA在碱性条件下可发生降解
D.PHA中存在手性碳原子
答案 A
解析 PHA的重复单元中只含有酯基一种官能团,A项错误;由PHA的结构可知其为聚酯,
由单体 缩聚合成,碱性条件下可发生降解,B、C项正确;PHA的重复单元中只
连有1个甲基的碳原子为手性碳原子,D项正确。
课时精练
1.民以食为天,《黄帝内经》说:“五谷为养,五果为助,五畜为益,五菜为充”,下列
说法正确的是( )
A.“五谷”富含淀粉,淀粉是天然高分子
B.“五果”富含糖类,其中的葡萄糖、蔗糖都能发生水解反应
C.“五畜”富含油脂和蛋白质,它们的组成元素相同
D.“五菜”富含纤维素,纤维素不属于糖类
答案 A
解析 葡萄糖不能水解,B错误;油脂和蛋白质的组成元素不同,C错误;纤维素属于糖类,
D错误。
2.(2023·宁波高三下学期高考模拟)下列说法不正确的是( )
A.麦芽糖、蔗糖互为同分异构体,分子式均为C H O
12 22 11
B.硬化油可作为制造肥皂和人造奶油的原料
C.合成硝酸纤维、醋酸纤维、聚酯纤维均要用到纤维素
D.蛋白质在乙醇、重金属的盐类、紫外线等的作用下会发生变性,失去生理活性
答案 C解析 麦芽糖与蔗糖的分子式均为C H O ,但结构不同,二者互为同分异构体,故A正
12 22 11
确;硬化油即油脂与H 加成所得,不易被空气氧化变质,可作为制造肥皂和人造奶油的原
2
料,故B正确;硝酸纤维和醋酸纤维是由纤维素反应所得,但聚酯纤维一般是二元醇与二
元羧酸缩聚反应所得,故C错误;蛋白质在乙醇、重金属的盐类、紫外线等的作用下会发
生变性,变性会使蛋白质失去生理活性,故D正确。
3.下列说法不正确的是( )
A.相同条件下等质量的甲烷、汽油、氢气完全燃烧,放出的热量依次增加
B.油脂在碱性条件下水解生成的高级脂肪酸盐是肥皂的主要成分
C.蛋白质水解的最终产物是氨基酸
D.淀粉、纤维素、蛋白质都属于高分子
答案 A
解析 单位质量的H元素燃烧放出的热量大于C元素,甲烷为含氢量最高的烃,则相同条
件下,等质量的甲烷、汽油、氢气完全燃烧,氢气放出的热量最多,甲烷次之,汽油最少,
A项错误;油脂在碱性条件下的水解反应即为皂化反应,得到的高级脂肪酸盐是肥皂的主要
成分,B项正确。
4.科学佩戴口罩对防控流感病毒有重要作用。生产一次性医用口罩的主要原料为聚丙烯树
脂。下列说法错误的是( )
A.聚丙烯的结构简式为
B.由丙烯合成聚丙烯的反应类型为缩聚反应
C.聚丙烯为热塑性合成树脂
D.聚丙烯在自然环境中不容易降解
答案 B
解析 聚丙烯由丙烯(CH==CHCH )通过加聚反应制得,聚丙烯的结构简式为
2 3
,A正确、B错误;由聚丙烯的结构可知聚丙烯为线型结构,具有热塑性,
C正确;聚丙烯结构中的化学键为单键,不易被氧化、不能水解,因此聚丙烯在自然环境中
不容易降解,D正确。
5.DNA指纹法在案件侦破工作中有着重要作用,从案发现场提取DNA样品,可为案件侦
破提供证据,其中的生物学原理是( )
A.不同人体内的DNA所含的碱基种类不同
B.不同人体内的DNA所含的戊糖和磷酸不同
C.不同人体内的DNA的空间结构不同
D.不同人体内的DNA所含的脱氧核苷酸排列顺序不同答案 D
6.链状高分子 可由有机化工原料R和其他有机试剂,
通过加成、水解、氧化、缩聚反应得到,则R是( )
A.1-丁烯 B.乙烯
C.1,3-丁二烯 D.2-丁烯
答案 B
解析 合成高分子 的反应为缩聚反应,需要 HOOCCOOH、
HOCH CHOH两种原料发生酯化反应制取。乙二醇连续氧化生成乙二酸,乙二醇可由二卤
2 2
代烃水解制取;二卤代烃可由乙烯与卤素单质加成制取,则R应为乙烯。
7.下列说法不正确的是( )
A.葡萄糖、蔗糖、纤维素都是糖类物质,都可发生水解反应
B.天然植物油中不饱和脂肪酸甘油酯含量高,常温下呈液态
C.氨基酸、二肽、蛋白质均既能与强酸又能与强碱反应
D.淀粉水解液加足量碱后,再加新制氢氧化铜,加热,产生砖红色沉淀
答案 A
8.一种自修复材料的结构(图甲)和修复原理(图乙)如图所示。下列说法错误的是( )
A.该高分子材料所制容器不能用于盛放碳酸钠溶液
B.合成该高分子的两种单体均为乙酸乙酯的同系物
C.该高分子可通过加聚反应合成
D.图示高分子材料破坏及自修复过程不涉及化学键的变化
答案 B
解析 该高分子材料中含有酯基,能与碱溶液发生水解反应,则其所制容器不能用于盛放碳
酸钠溶液,故 A 正确;合成该高分子的两种单体分别为 CH==C(CH)COOCH 、
2 3 3
CH==CHCOOCH CHCHCH,乙酸乙酯只有酯基,没有碳碳双键,结构不相似,不互为同
2 2 2 2 3系物,故B错误;由图可知,自修复过程中“—COOCH CHCHCH”基团之间没有化学键
2 2 2 3
的变化,故D正确。
9.凯夫拉是一种高强度、耐腐蚀的芳纶纤维,军事上称为“装甲卫士”,但长期浸渍在强
酸或强碱中其强度有所下降。下表中是凯夫拉的两种结构:
名称 结构简式
芳纶1313
芳纶1414
下列说法不正确的是( )
A.“芳纶1313”和“芳纶1414”互为同分异构体
B.“芳纶1313”和“芳纶1414”中数字表示苯环上取代基的位置
C.凯夫拉在强酸或强碱中强度下降,可能与“ ”的水解有关
D.以 和 为原料制备“芳纶1414”的反应
为缩聚反应
答案 A
解析 “芳纶1313”和“芳纶1414”都是高分子,n值不一定相同,所以它们不互为同分
异构体,A项错误;“芳纶1313”是指苯环上1、3位置被取代,“芳纶1414”是指苯环上
1、4位置被取代,B项正确; 可发生水解反应,故芳纶纤维的强度在强酸或强碱
中 下 降 与 “ ” 的 水 解 有 关 , C 项 正 确 ; 和
反应生成 和HX,属于缩
聚反应,D项正确。
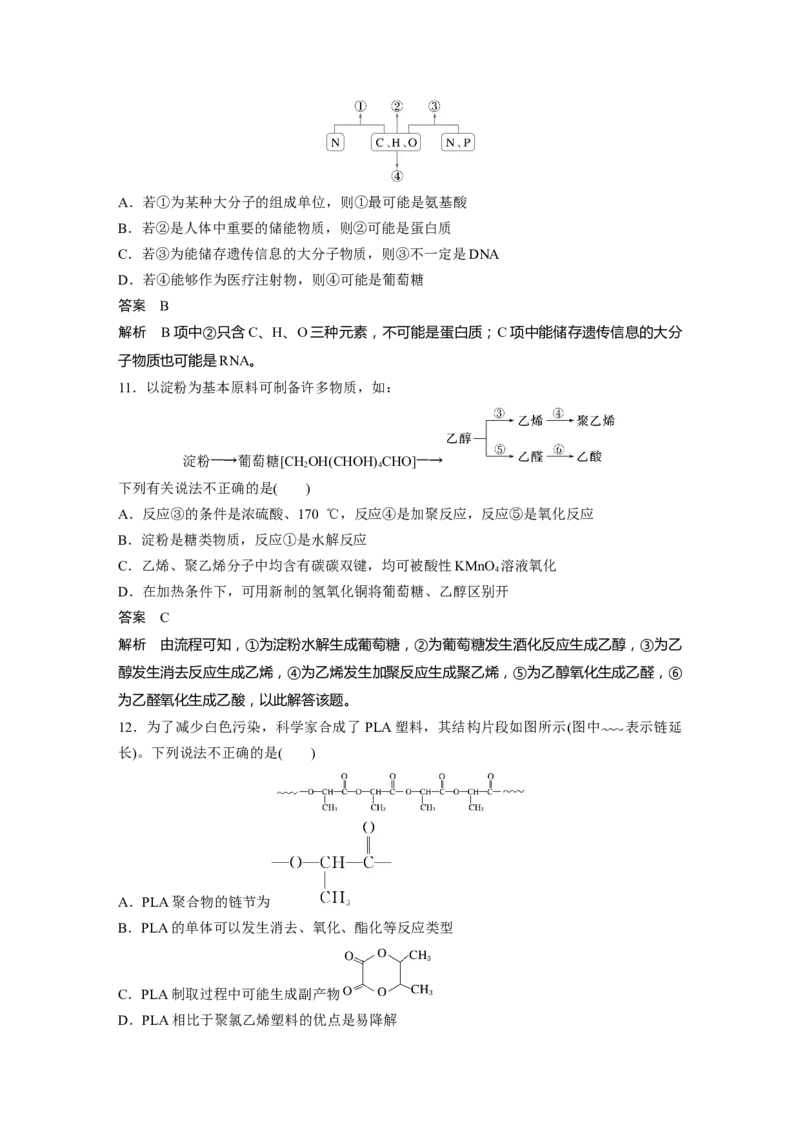
10.如图表示不同化学元素所组成的生物大分子及其水解产物,以下说法错误的是( )A.若①为某种大分子的组成单位,则①最可能是氨基酸
B.若②是人体中重要的储能物质,则②可能是蛋白质
C.若③为能储存遗传信息的大分子物质,则③不一定是DNA
D.若④能够作为医疗注射物,则④可能是葡萄糖
答案 B
解析 B项中②只含C、H、O三种元素,不可能是蛋白质;C项中能储存遗传信息的大分
子物质也可能是RNA。
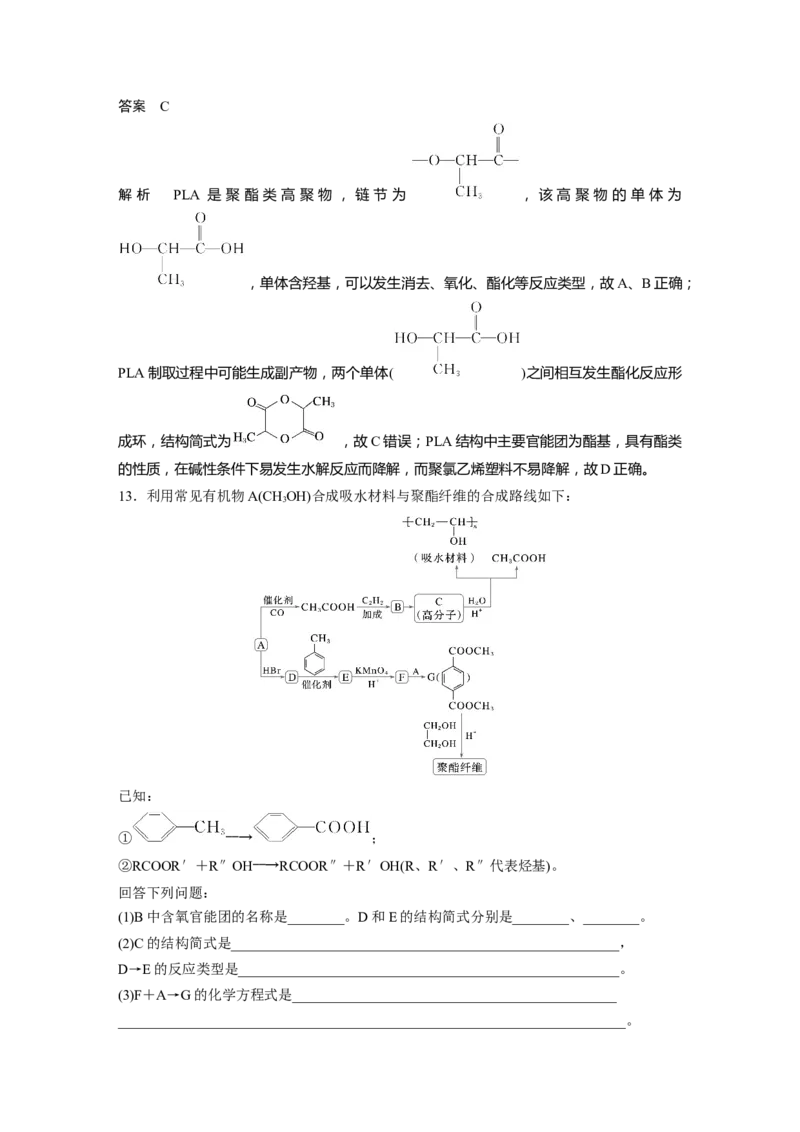
11.以淀粉为基本原料可制备许多物质,如:
淀粉――→葡萄糖[CHOH(CHOH) CHO]――→
2 4
下列有关说法不正确的是( )
A.反应③的条件是浓硫酸、170 ℃,反应④是加聚反应,反应⑤是氧化反应
B.淀粉是糖类物质,反应①是水解反应
C.乙烯、聚乙烯分子中均含有碳碳双键,均可被酸性KMnO 溶液氧化
4
D.在加热条件下,可用新制的氢氧化铜将葡萄糖、乙醇区别开
答案 C
解析 由流程可知,①为淀粉水解生成葡萄糖,②为葡萄糖发生酒化反应生成乙醇,③为乙
醇发生消去反应生成乙烯,④为乙烯发生加聚反应生成聚乙烯,⑤为乙醇氧化生成乙醛,⑥
为乙醛氧化生成乙酸,以此解答该题。
12.为了减少白色污染,科学家合成了PLA塑料,其结构片段如图所示(图中 表示链延
长)。下列说法不正确的是( )
A.PLA聚合物的链节为
B.PLA的单体可以发生消去、氧化、酯化等反应类型
C.PLA制取过程中可能生成副产物
D.PLA相比于聚氯乙烯塑料的优点是易降解答案 C
解 析 PLA 是 聚 酯 类 高 聚 物 , 链 节 为 , 该 高 聚 物 的 单 体 为
,单体含羟基,可以发生消去、氧化、酯化等反应类型,故A、B正确;
PLA制取过程中可能生成副产物,两个单体( )之间相互发生酯化反应形
成环,结构简式为 ,故C错误;PLA结构中主要官能团为酯基,具有酯类
的性质,在碱性条件下易发生水解反应而降解,而聚氯乙烯塑料不易降解,故D正确。
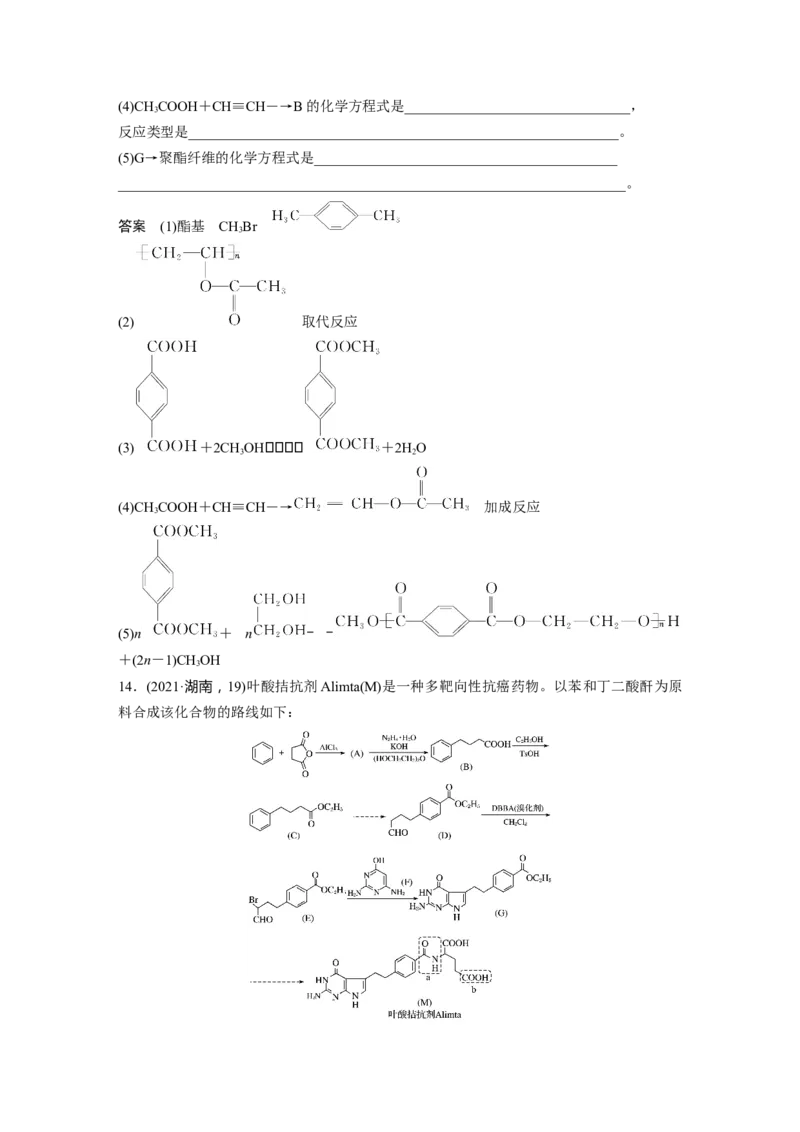
13.利用常见有机物A(CH OH)合成吸水材料与聚酯纤维的合成路线如下:
3
已知:
① ――→ ;
②RCOOR′+R″OH――→RCOOR″+R′OH(R、R′、R″代表烃基)。
回答下列问题:
(1)B中含氧官能团的名称是________。D和E的结构简式分别是________、________。
(2)C的结构简式是_______________________________________________________,
D→E的反应类型是______________________________________________________。
(3)F+A→G的化学方程式是______________________________________________
________________________________________________________________________。(4)CH COOH+CH≡CH―→B的化学方程式是________________________________,
3
反应类型是_____________________________________________________________。
(5)G→聚酯纤维的化学方程式是___________________________________________
________________________________________________________________________。
答案 (1)酯基 CHBr
3
(2) 取代反应
(3) +2CHOH +2HO
3 2
(4)CH COOH+CH≡CH―→ 加成反应
3
(5)n + n ― ― →
+(2n-1)CHOH
3
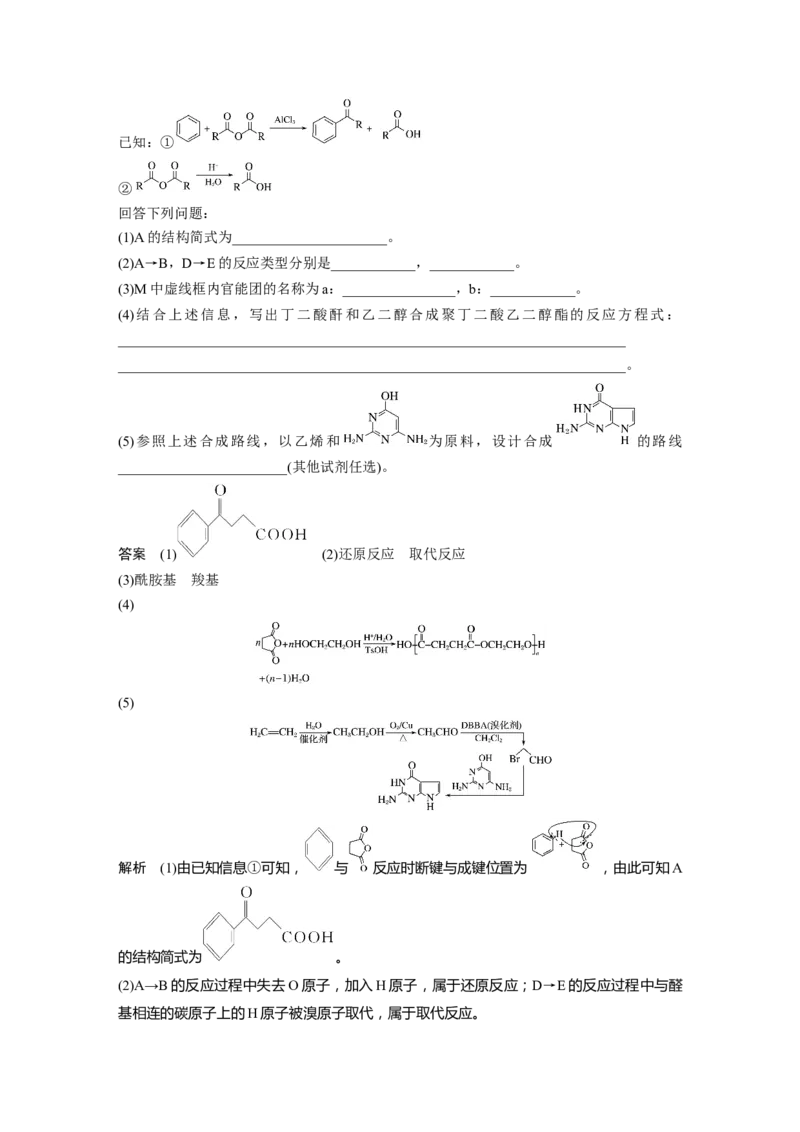
14.(2021·湖南,19)叶酸拮抗剂Alimta(M)是一种多靶向性抗癌药物。以苯和丁二酸酐为原
料合成该化合物的路线如下:已知:①
②
回答下列问题:
(1)A的结构简式为______________________。
(2)A→B,D→E的反应类型分别是____________,____________。
(3)M中虚线框内官能团的名称为a:________________,b:____________。
(4)结合上述信息,写出丁二酸酐和乙二醇合成聚丁二酸乙二醇酯的反应方程式:
________________________________________________________________________
________________________________________________________________________。
(5)参照上述合成路线,以乙烯和 为原料,设计合成 的路线
________________________(其他试剂任选)。
答案 (1) (2)还原反应 取代反应
(3)酰胺基 羧基
(4)
(5)
解析 (1)由已知信息①可知, 与 反应时断键与成键位置为 ,由此可知A
的结构简式为 。
(2)A→B的反应过程中失去O原子,加入H原子,属于还原反应;D→E的反应过程中与醛
基相连的碳原子上的H原子被溴原子取代,属于取代反应。(4) 丁 二 酸 酐 ( ) 和 乙 二 醇 (HOCHCHOH) 合 成 聚 丁 二 酸 乙 二 醇 酯 (
2 2
)的过程中,需先将 转化为丁二酸,可利用已
知信息②实现,然后利用B→C的反应类型合成聚丁二酸乙二醇酯。
(5)以乙烯和 为原料合成 的路线设计过程中,可利用E+F→G的反应类
型实现,因此需先利用乙烯合成 , 中醛基可通过羟基催化氧化而
得, 中溴原子可利用D→E的反应类型实现。