文档内容
2022~2023(一)天津市第十四中学高三年级期末考试
化学试卷
第Ⅰ卷
本卷共12题,共36分。
可能用到的相对原子质量:
1. 下列说法不正确的是
A. 硬铝密度小、强度高,具有较强的抗腐蚀能力,是制造飞机的理想材料
B. 普通玻璃以纯碱、石灰石和石英砂为原料,在玻璃窑中反应制得
C. 膳食纤维是人体七大营养素之一,在人体内水解为葡萄糖加以吸收利用
D. 和 的溶液均显碱性,可用作食用碱或工业用碱
2. 下列物质仅含共价键且水溶液呈碱性的是
A. B. C. D. 纯碱
3. 下列说法正确的是
A. 、 互 为同位素 B. 第一电离能大小:
C. 的电子式: D. 的球棍模型:
4. 关于反应 ,下列说法不正确的是
A. 是氧化剂 B. 是还原产物
C. 中的S元素被还原 D. 消耗1mol ,转移2mol电子
5. 设N 代表阿伏加德罗常量的值。下列说法正确的是
A
A. 100g46%乙醇溶液中含有的氧原子数为4N
A
B. 标准状况下,11.2L乙烷和乙烯混合物中含有的氢原子数为2.5N
A
C. 2molNO与1molO 在密闭容器中充分反应后,容器中的分子总数为2N
2 A
D. 用铜作电极电解饱和NaCl溶液,当电路上通过0.2mole-时,阴、阳两极产生的气体分
子总数为0.2N
A
6. 下列实验所涉及反应的离子方程式错误的是
A. 过氧化钠与水反应:
B. 向海带灰浸出液中滴加几滴硫酸酸化的过氧化氢溶液:C. 向硫酸铜溶液中通入
D. 用酸性高锰酸钾标准溶液滴定草酸:
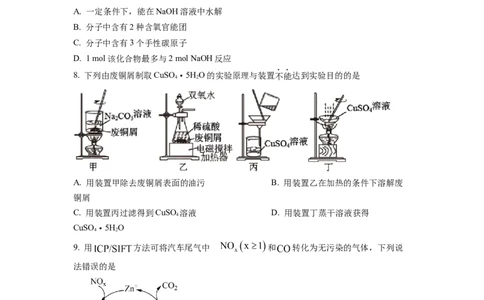
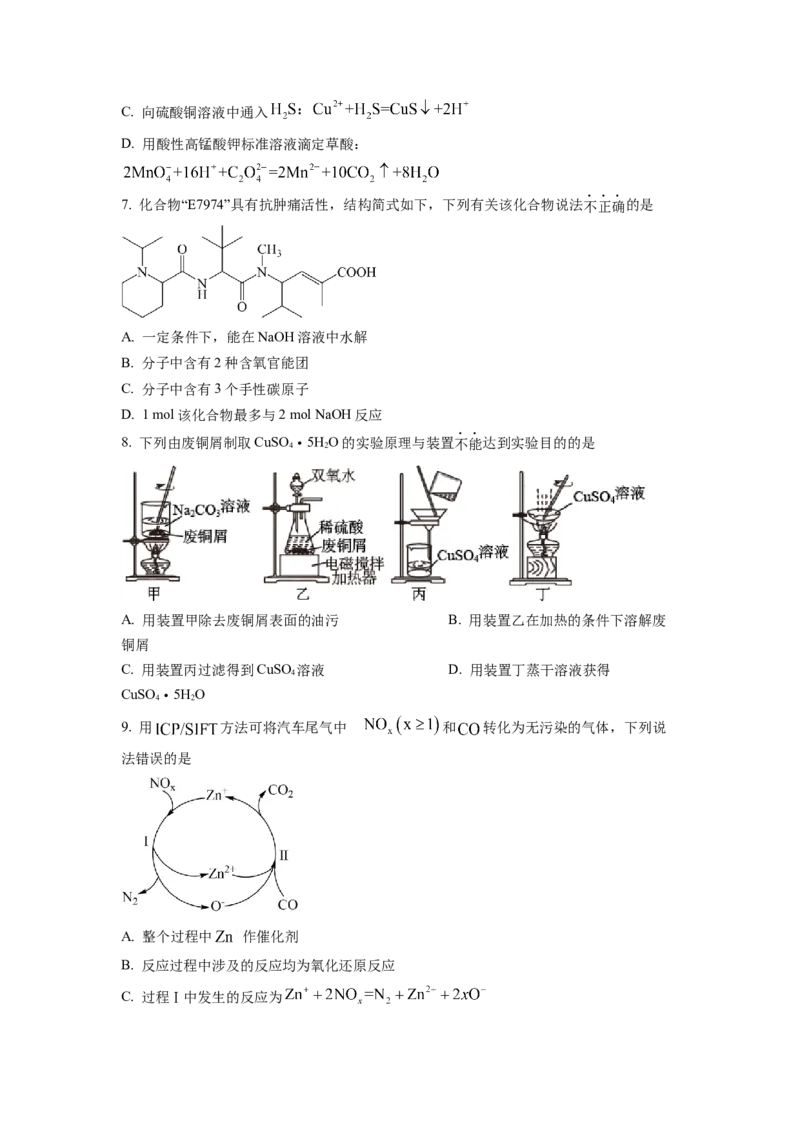
7. 化合物“E7974”具有抗肿痛活性,结构简式如下,下列有关该化合物说法不正确的是
A. 一定条件下,能在NaOH溶液中水解
B. 分子中含有2种含氧官能团
C. 分子中含有3个手性碳原子
D. 1 mol该化合物最多与2 mol NaOH反应
8. 下列由废铜屑制取CuSO ·5HO的实验原理与装置不能达到实验目的的是
4 2
A. 用装置甲除去废铜屑表面的油污 B. 用装置乙在加热的条件下溶解废
铜屑
C. 用装置丙过滤得到CuSO 溶液 D. 用装置丁蒸干溶液获得
4
CuSO ·5HO
4 2
9. 用 方法可将汽车尾气中 的和 转化为无污染的气体,下列说
法错误的是
A. 整个过程中 作催化剂
B. 反应过程中涉及的反应均为氧化还原反应
C. 过程Ⅰ中发生的反应为D. 总反应中氧化剂和还原剂的物质的量之比为
10. 下列溶液中各微粒浓度关系正确的是
A. 室温下,pH=4的0.1 mol/L的NaHC O 溶液中:c( )>c(H+)>c(H C O)>c(
2 4 2 2 4
)
B. 0.1 mol/L的CHCOONH 溶液中:c(CHCOO−)+c(CHCOOH)=c(NH •H O)+c( )
3 4 3 3 3 2
C. 同温下,两种盐溶液的浓度相同且pH(NaX)>pH(NaY),则c(X−)+c(OH−)>c(Y−)+c(OH−)
D. 向含有BaSO、BaCO 的饱和溶液中加入少量的Ba(NO ),溶液中 的值减小
4 3 3 2
(已知:K (BaSO)=1.1×10-10;K (BaCO)=2.58×10-9)
sp 4 sp 3
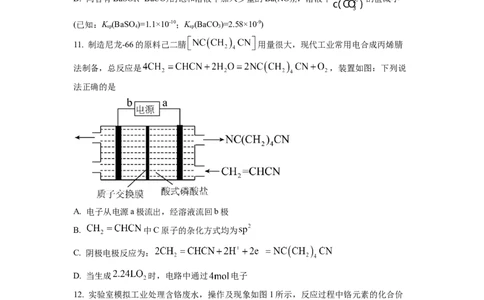
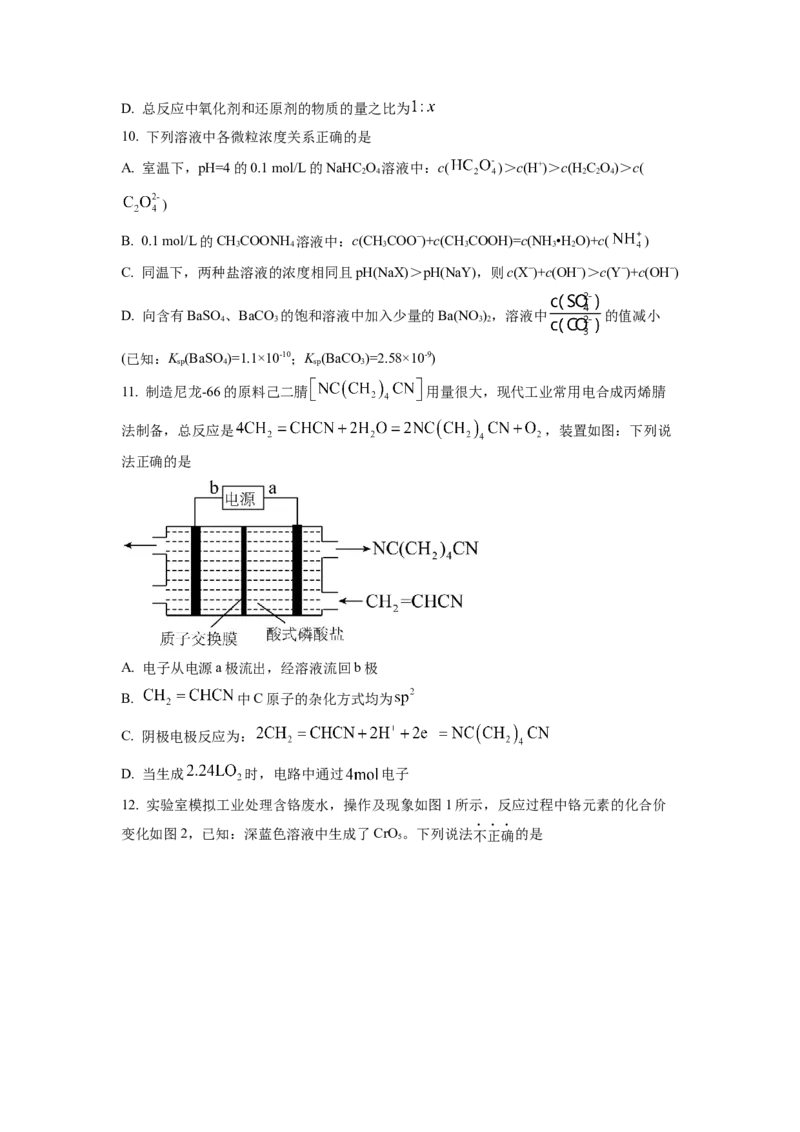
11. 制造尼龙-66的原料己二腈 用量很大,现代工业常用电合成丙烯腈
法制备,总反应是 ,装置如图:下列说
法正确的是
A. 电子从电源a极流出,经溶液流回b极
B. 中C原子的杂化方式均为
C. 阴极电极反应为:
D. 当生成 时,电路中通过 电子
12. 实验室模拟工业处理含铬废水,操作及现象如图1所示,反应过程中铬元素的化合价
变化如图2,已知:深蓝色溶液中生成了CrO。下列说法不正确的是
5A. 0-5 s过程中,发生的氧化还原反应为:
B. 实验开始至30 s溶液中发生的总反应离子方程式为:
C. 30-80 s过程中,Cr元素被氧化,可能是溶液中剩余的HO 所致
2 2
D. 80 s时,在碱性条件下,溶液中含铬微粒主要为
第Ⅱ卷
本卷共4题,共64分。
13. 请回答下列问题。
(1)钴及其化合物有重要的用途,探究其结构有重要意义。
①请写出基态钴原子的核外电子排布式_________。
②按照核外电子排布,可把元素周期表划分为5个区, 在元素周期表中属于_________
区。
(2) 是 的一种重要配合物。
①该配合物 一的种配体是 , 的空间结构呈_________形,是_________(填“极性”
或“非极性)分子。
② 的价层电子轨道表示式是_________。
③ 中含有的 键的数目为_________ (用 代表阿伏加德罗常数) 。
④设计实验证实该配合物溶于水时,离子键发生断裂,配位键没有断裂。实验如下:称取
该配合物,先加水溶解,再加足量 溶液,_________(补全实验操作),称量
沉淀质量为_________(精确到 ,相对分子质量 :250.5;
:143.5) 。
(3)第ⅤA族元素及其化合物的结构和性质如下:
① 、 、 的沸点由高到低的顺序为_________(填化学式,下同),键角由大到
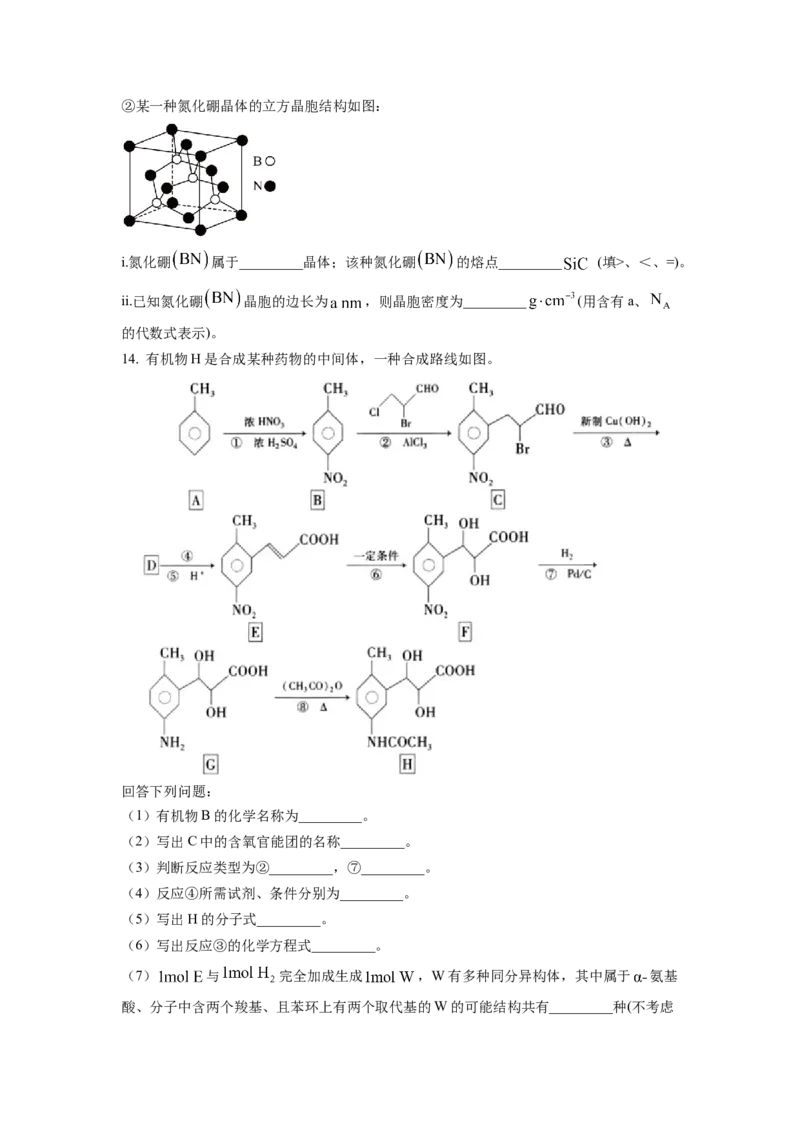
小的顺序为_________。②某一种氮化硼晶体的立方晶胞结构如图:
i.氮化硼 属于_________晶体;该种氮化硼 的熔点_________ (填>、<、=)。
ii.已知氮化硼 晶胞的边长为 ,则晶胞密度为_________ (用含有a、
的代数式表示)。
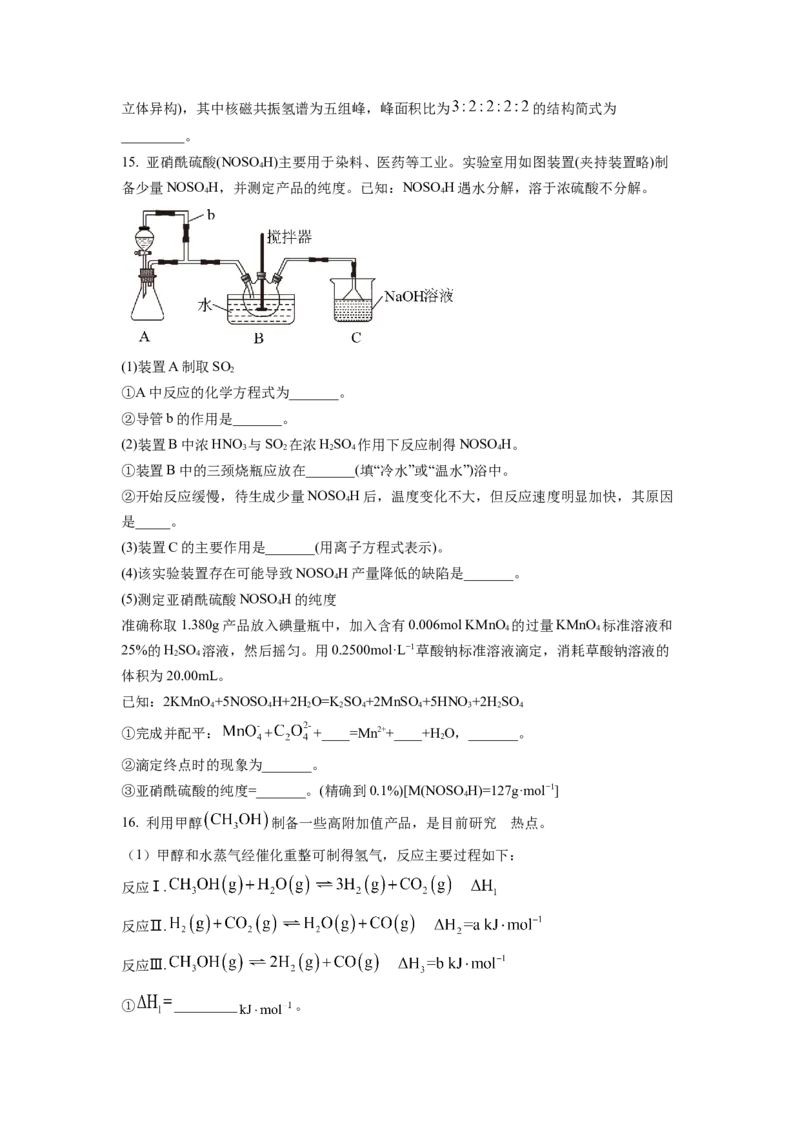
14. 有机物H是合成某种药物的中间体,一种合成路线如图。
回答下列问题:
(1)有机物B的化学名称为_________。
(2)写出C中的含氧官能团的名称_________。
(3)判断反应类型为②_________,⑦_________。
(4)反应④所需试剂、条件分别为_________。
(5)写出H的分子式_________。
(6)写出反应③的化学方程式_________。
(7) 与 完全加成生成 ,W有多种同分异构体,其中属于 氨基
酸、分子中含两个羧基、且苯环上有两个取代基的W的可能结构共有_________种(不考虑立体异构),其中核磁共振氢谱为五组峰,峰面积比为 的结构简式为
_________。
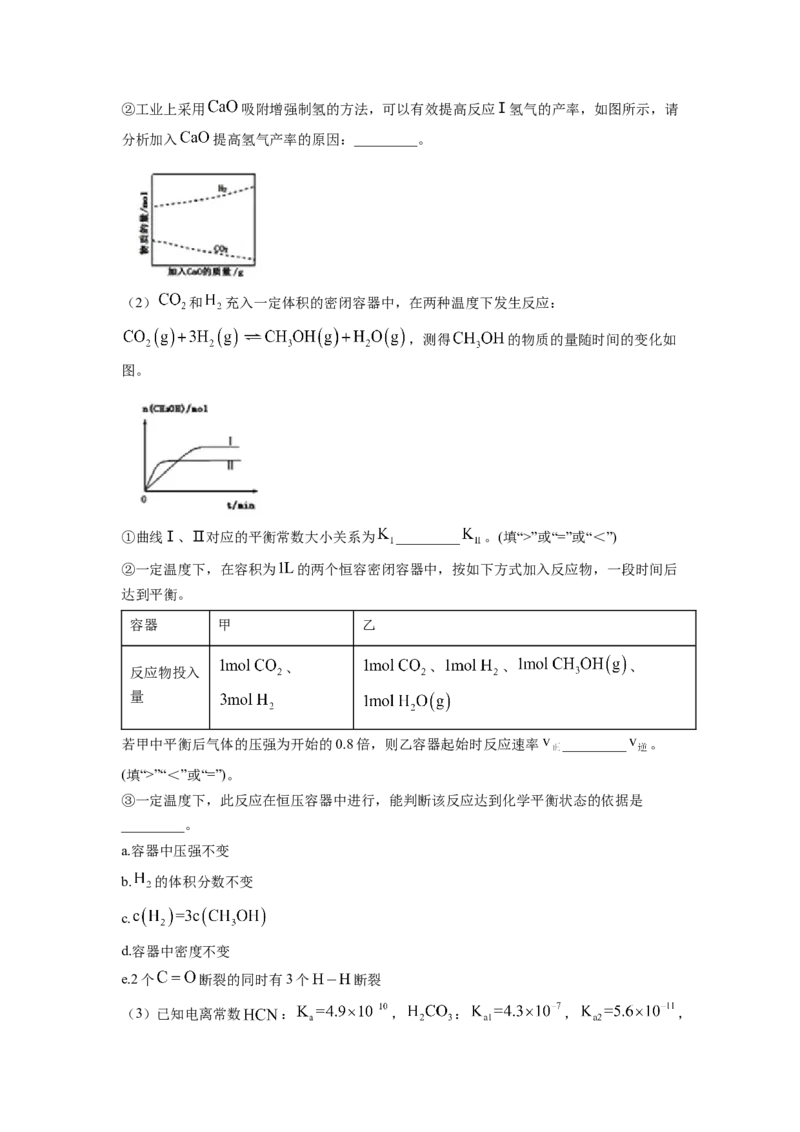
15. 亚硝酰硫酸(NOSOH)主要用于染料、医药等工业。实验室用如图装置(夹持装置略)制
4
备少量NOSOH,并测定产品的纯度。已知:NOSOH遇水分解,溶于浓硫酸不分解。
4 4
(1)装置A制取SO
2
①A中反应的化学方程式为_______。
②导管b的作用是_______。
(2)装置B中浓HNO 与SO 在浓HSO 作用下反应制得NOSOH。
3 2 2 4 4
①装置B中的三颈烧瓶应放在_______(填“冷水”或“温水”)浴中。
②开始反应缓慢,待生成少量NOSOH后,温度变化不大,但反应速度明显加快,其原因
4
是_____。
(3)装置C的主要作用是_______(用离子方程式表示)。
(4)该实验装置存在可能导致NOSOH产量降低的缺陷是_______。
4
(5)测定亚硝酰硫酸NOSOH的纯度
4
准确称取1.380g产品放入碘量瓶中,加入含有0.006mol KMnO 的过量KMnO 标准溶液和
4 4
25%的HSO 溶液,然后摇匀。用0.2500mol·L−1草酸钠标准溶液滴定,消耗草酸钠溶液的
2 4
体积为20.00mL。
已知:2KMnO +5NOSO H+2HO=KSO +2MnSO +5HNO +2H SO
4 4 2 2 4 4 3 2 4
①完成并配平: + +____=Mn2++____+H O,_______。
2
②滴定终点时的现象为_______。
③亚硝酰硫酸的纯度=_______。(精确到0.1%)[M(NOSO H)=127g·mol−1]
4
16. 利用甲醇 制备一些高附加值产品,是目前研究 热的点。
(1)甲醇和水蒸气经催化重整可制得氢气,反应主要过程如下:
反应Ⅰ.
反应Ⅱ.
反应Ⅲ.
① _________ 。②工业上采用 吸附增强制氢的方法,可以有效提高反应Ⅰ氢气的产率,如图所示,请
分析加入 提高氢气产率的原因:_________。
(2) 和 充入一定体积的密闭容器中,在两种温度下发生反应:
,测得 的物质的量随时间的变化如
图。
①曲线Ⅰ、Ⅱ对应的平衡常数大小关系为 _________ 。(填“>”或“=”或“<”)
②一定温度下,在容积为 的两个恒容密闭容器中,按如下方式加入反应物,一段时间后
达到平衡。
容器 甲 乙
反应物投入 、 、 、 、
量
若甲中平衡后气体的压强为开始的0.8倍,则乙容器起始时反应速率 _________ 。
(填“>”“<”或“=”)。
③一定温度下,此反应在恒压容器中进行,能判断该反应达到化学平衡状态的依据是
_________。
a.容器中压强不变
b. 的体积分数不变
c.
d.容器中密度不变
e.2个 断裂的同时有3个 断裂
(3)已知电离常数 : , : , ,则向 溶液中通入少量 时的离子方程式为_________。
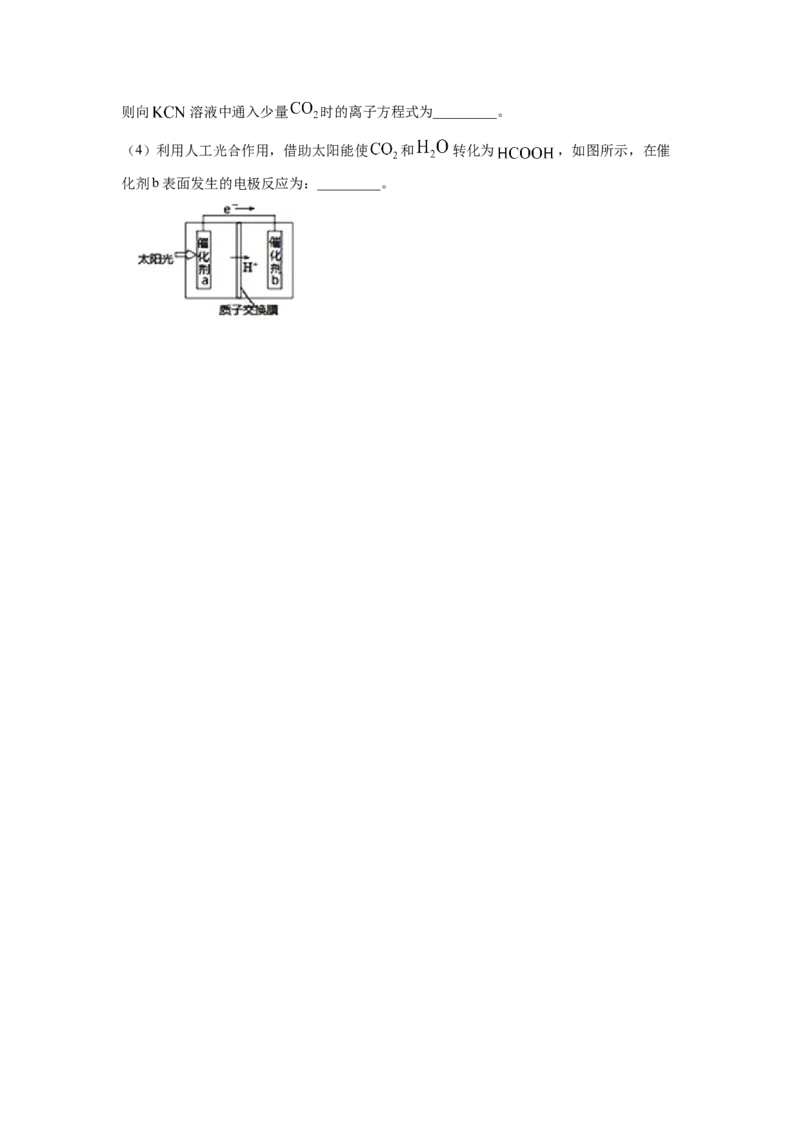
(4)利用人工光合作用,借助太阳能使 和 转化为 ,如图所示,在催
化剂b表面发生的电极反应为:_________。2022~2023(一)天津市第十四中学高三年级期末考试
化学试卷
第Ⅰ卷
本卷共12题,共36分。
可能用到的相对原子质量:
【1题答案】
【答案】C
【2题答案】
【答案】B
【3题答案】
【答案】B
【4题答案】
【答案】C
【5题答案】
【答案】A
【6题答案】
【答案】D
【7题答案】
【答案】D
【8题答案】
【答案】D
【9题答案】
【答案】C
【10题答案】
【答案】B
【11题答案】
【答案】C
【12题答案】
【答案】A
第Ⅱ卷
本卷共4题,共64分。
【13题答案】
.
【答案】(1) ① 1s22s22p63s23p63d74s2 ②. d(2) ①. 三角锥形 ②. 极性 ③. ④. 21N
A
⑤. 充分反应后过滤,将沉淀洗涤、干燥后称量 ⑥. 2.87
(3) ①. NH >AsH >PH ②. NH >PH >AsH ③. 原子 ④. > ⑤.
3 3 3 3 3 3
【14题答案】
【答案】(1)对硝基甲苯
(2)硝基、醛基 (3) ①. 取代反应 ②. 还原反应
(4)氢氧化钠醇溶液,加热
(5)C H ON
12 15 5
(6) + 2Cu(OH) +NaOH + Cu O↓ +3H O
2 2 2
(7) ①. 12 ②.
【15题答案】
【答案】 ①. NaSO +H SO (浓)=Na SO +H O+SO ↑ ②. 平衡压强,使分液漏斗中
2 3 2 4 2 4 2 2
的液体能顺利流下 ③. 冷水 ④. 生成的NOSOH作为该反应的催化剂 ⑤.
4
SO +2OH−= +H O ⑥. C装置中的水蒸气会进入B中使NOSOH分解 ⑦. 2
2 2 4
+5 +16H+=2Mn2++10CO ↑+8H O ⑧. 溶液恰好由紫红色变为无色,且半分
2 2
钟内不恢复 ⑨. 92.0%
【16题答案】
【答案】(1) ①. b—a ②. CaO消耗CO ,生成物CO 的浓度减小,平衡向正反
2 2
应方向移动,氢气的产率增大
(2) ①. > ②. < ③. bd
(3)CO+CN—+H O=HCN+HCO
2 2
(4)CO+2H++2e—=HCOOH
2