文档内容
“皖东县中联盟”2022~2023 学年第一学期高三联考
化学试题
考生注意:
1.本试卷分选择题和非选择题两部分。满分100分,考试时间 90分钟。
2.答题前,考生务必用直径 0.5毫米黑色墨水签字笔将密封线内项目填写清楚。
3.考生作答时,请将答案答在答题卡上。选择题每小题选出答案后,用 2B 铅笔
把答题卡上对应题目的答案标号涂黑;非选择题请用直径 0.5毫米黑色墨水签字
笔在答题卡上各题的答题区域内作答,超出答题区域书写的答案无效,在试题
卷、草稿纸上作答无效。
4.本卷命题范围:高考范围。
5.可能用到的相对原子质量:
H1 C12 N14 O16 Na23 S32 Cl35.5 Mn55 Cu64 Zn65
一、选择题(本题共14小题,每小题 3分,共计 42分。在每小题列出的四个选
项中,只有一项是符合题目要求的)
1.生活中处处有化学。下列叙述正确的是
A.水银温度计破损后撒一些硫粉防止汞中毒
B.2B铅笔芯的主要成分是石墨和二氧化铅
C.聚氯乙烯无毒无害,可以制作自热饭盒
D.用焰色试验的方法可以鉴别味精和食盐
点燃
2.用化学用语表示2H S3O 2SO 2H O 中的相关微粒,其中正确的是
2 2 2 2
A.SO 分子的空间构型为V形
2
B.H S的电子式为
2
C.S原子的结构示意图为
试卷第1页,共9页D.基态O原子的价电子轨道表示式为
3.设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.25℃时,pH13的BaOH 溶液中含有OH的数目为0.1N
2 A
B.标准状况下,22.4L四氯化碳中含共价键数目为4N
A
C.46g由NO 与N O 组成的混合气体中N原子数目为N
2 2 4 A
D.7.1g Cl 与足量H O充分反应后转移电子数为0.1N
2 2 A
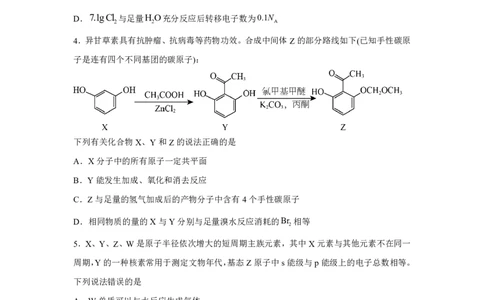
4.异甘草素具有抗肿瘤、抗病毒等药物功效。合成中间体Z的部分路线如下(已知手性碳原
子是连有四个不同基团的碳原子):
下列有关化合物X、Y和Z的说法正确的是
A.X分子中的所有原子一定共平面
B.Y能发生加成、氧化和消去反应
C.Z与足量的氢气加成后的产物分子中含有4个手性碳原子
D.相同物质的量的X与Y分别与足量溴水反应消耗的Br 相等
2
5.X、Y、Z、W是原子半径依次增大的短周期主族元素,其中X元素与其他元素不在同一
周期,Y的一种核素常用于测定文物年代,基态Z原子中s能级与p能级上的电子总数相等。
下列说法错误的是
A.W单质可以与水反应生成气体
B.Z、W所在周期内,Z、W元素第一电离能大小相邻
C.X与Y组成的化合物沸点可能比水的高
D.X、Y、Z、W的单质均可以在空气中燃烧
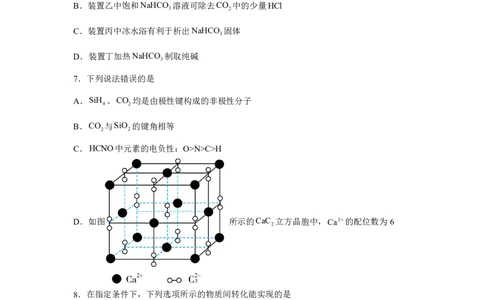
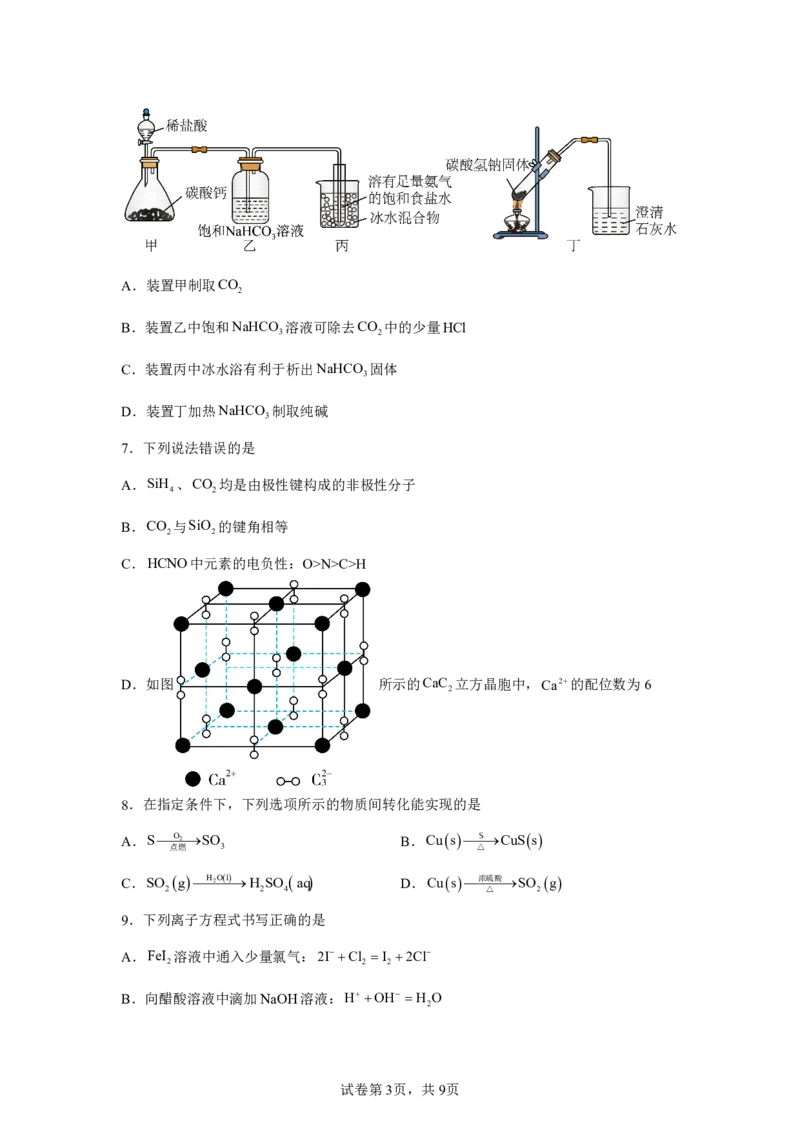
6.实验室用下列装置模拟侯氏制碱法。下列说法错误的是
试卷第2页,共9页A.装置甲制取CO
2
B.装置乙中饱和NaHCO 溶液可除去CO 中的少量HCl
3 2
C.装置丙中冰水浴有利于析出NaHCO 固体
3
D.装置丁加热NaHCO 制取纯碱
3
7.下列说法错误的是
A.SiH 、CO 均是由极性键构成的非极性分子
4 2
B.CO 与SiO 的键角相等
2 2
C.HCNO中元素的电负性:O>N>C>H
D.如图 所示的CaC 立方晶胞中,Ca2的配位数为6
2
8.在指定条件下,下列选项所示的物质间转化能实现的是
A.SO2SO B.CusSCuSs
点燃 3 △
C.SO gH2OlH SO aq D.Cus浓硫酸SO g
2 2 4 △ 2
9.下列离子方程式书写正确的是
A.FeI 溶液中通入少量氯气:2ICl I 2Cl
2 2 2
B.向醋酸溶液中滴加NaOH溶液:H OH H O
2
试卷第3页,共9页C.向Na CO 溶液中通入少量SO :CO2SO SO2CO
2 3 2 3 2 3 2
通电
D.用石墨电极电解氯化镁溶液:2ClH O Cl 2OHH
2 2 2
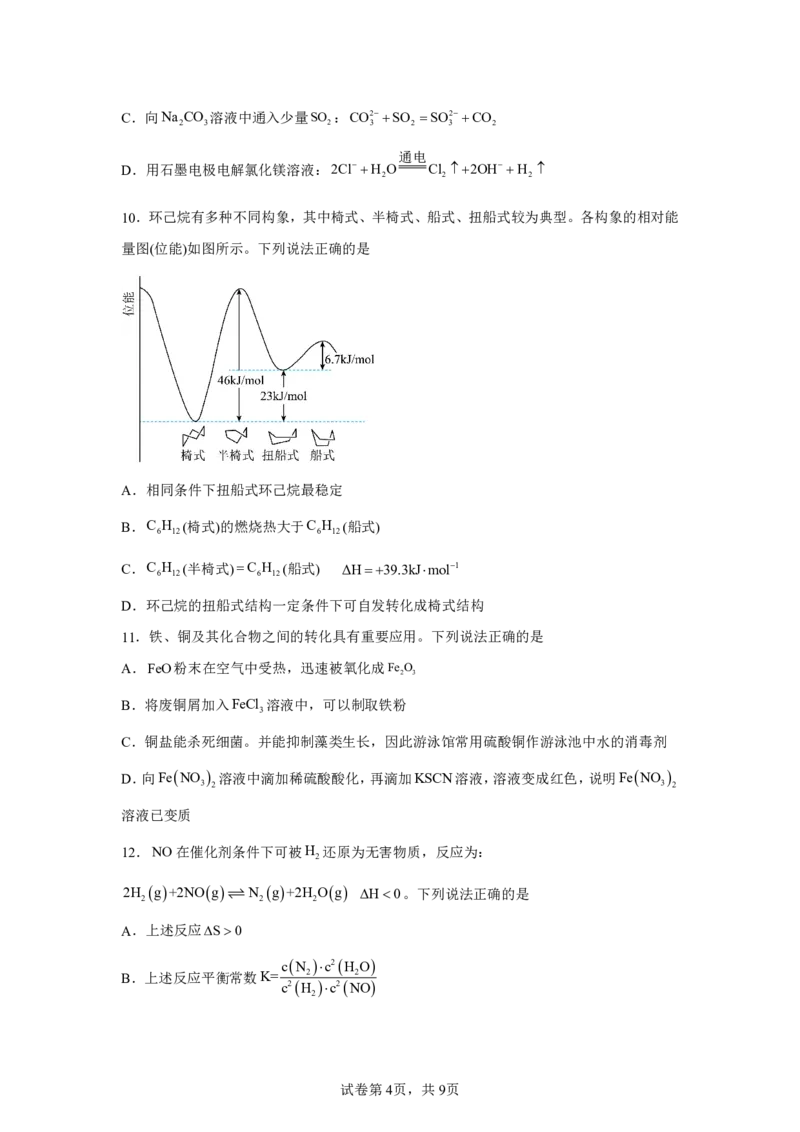
10.环己烷有多种不同构象,其中椅式、半椅式、船式、扭船式较为典型。各构象的相对能
量图(位能)如图所示。下列说法正确的是
A.相同条件下扭船式环己烷最稳定
B.C H (椅式)的燃烧热大于C H (船式)
6 12 6 12
C.C H (半椅式)C H (船式) ΔH39.3kJmol1
6 12 6 12
D.环己烷的扭船式结构一定条件下可自发转化成椅式结构
11.铁、铜及其化合物之间的转化具有重要应用。下列说法正确的是
A.FeO粉末在空气中受热,迅速被氧化成Fe O
2 3
B.将废铜屑加入FeCl 溶液中,可以制取铁粉
3
C.铜盐能杀死细菌。并能抑制藻类生长,因此游泳馆常用硫酸铜作游泳池中水的消毒剂
D.向FeNO 溶液中滴加稀硫酸酸化,再滴加KSCN溶液,溶液变成红色,说明FeNO
3 2 3 2
溶液已变质
12.NO在催化剂条件下可被H 还原为无害物质,反应为:
2
2H g+2NOg N g+2H Og H0。下列说法正确的是
2 2 2
A.上述反应S0
cN c2H O
B.上述反应平衡常数K= 2 2
c2H c2NO
2
试卷第4页,共9页C.上述反应中生成1mol N ,转移电子的数目为26.021023
2
D.上述反应中,充入水蒸气增大压强可以提高NO平衡转化率
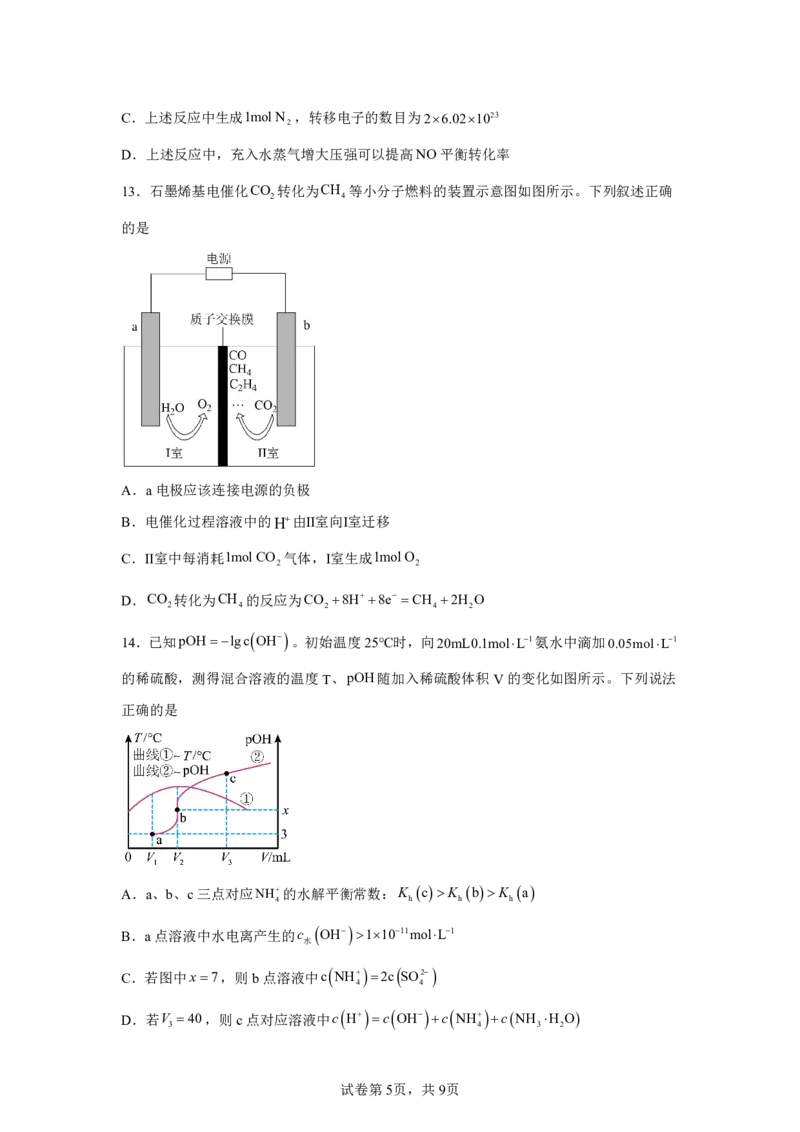
13.石墨烯基电催化CO 转化为CH 等小分子燃料的装置示意图如图所示。下列叙述正确
2 4
的是
A.a电极应该连接电源的负极
B.电催化过程溶液中的H由Ⅱ室向Ⅰ室迁移
C.Ⅱ室中每消耗1mol CO 气体,Ⅰ室生成1mol O
2 2
D.CO 转化为CH 的反应为CO 8H 8e CH 2H O
2 4 2 4 2
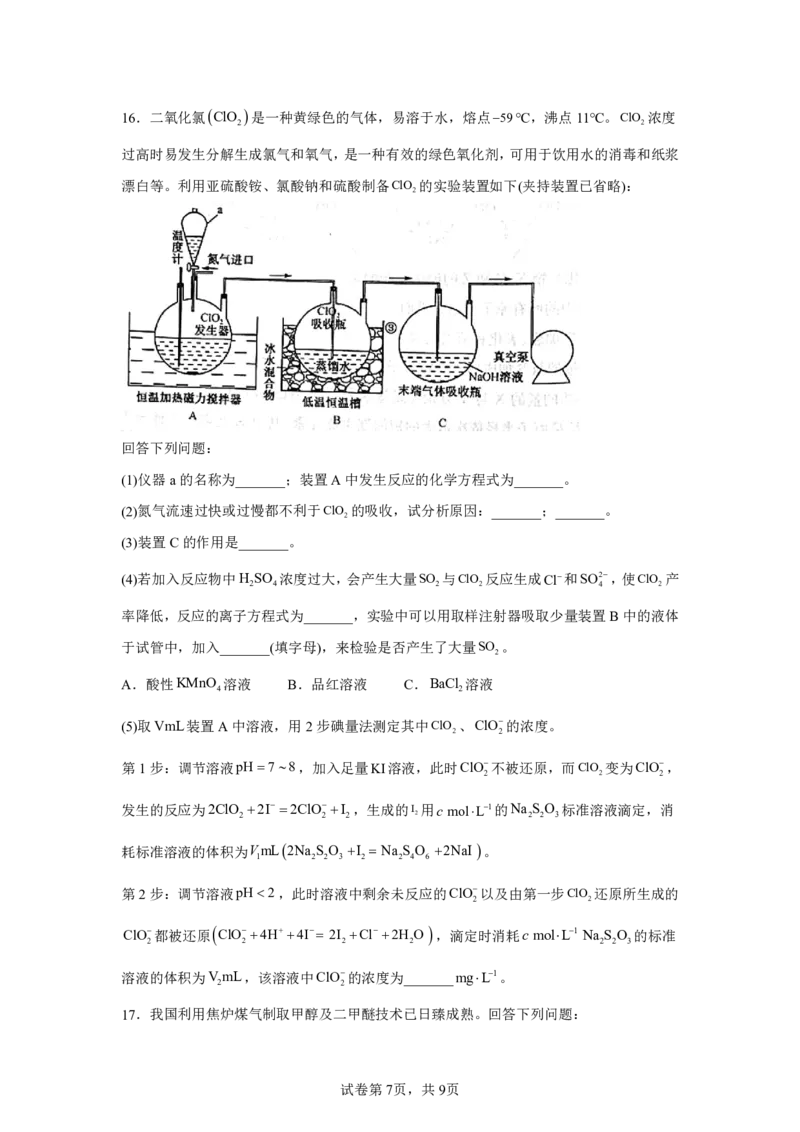
14.已知pOHlgc
OH
。初始温度25℃时,向20mL0.1molL1氨水中滴加0.05molL1
的稀硫酸,测得混合溶液的温度T、pOH随加入稀硫酸体积V的变化如图所示。下列说法
正确的是
A.a、b、c三点对应NH的水解平衡常数:K cK bK a
4 h h h
B.a点溶液中水电离产生的c OH 11011molL1
水
C.若图中x7,则b点溶液中c
NH
2c
SO2
4 4
D.若V 40,则c点对应溶液中c H c OH c NH cNH H O
3 4 3 2
试卷第5页,共9页二、非选择题(本题共4小题,共 58分)
15.利用软锰矿(主要成分是MnO ,其中还含有少量CaO、MgO、SiO 、Al O 等杂质)
2 2 2 3
制取高纯硫酸锰的工艺流程如下图所示。
已知:常温下,一些金属氢氧化物沉淀时的pH如下表:
氢氧化物 FeOH FeOH MnOH AlOH
3 2 2 3
开始沉淀pH 1.5 6.5 7.7 3.8
沉淀完全pH 3.7 9.7 9.8 5.2
常温下,一些难溶电解质的溶度积常数如下表:
难溶电解质 MnF CaF MgF
2 2 2
K 5.3103 1.51010 7.41011
sp
回答下列问题:
(1)“浸取”时,铁屑与MnO 反应生成Fe3的离子方程式为_______;“浸出液”需要鼓入一段
2
时间空气后,再进行“沉铁”的原因是_______。
(2)“沉铁、铝”时,加CaCO 控制溶液pH范围是_______;完全沉淀时,金属离子浓度为
3
1105molL1,则常温下K
sp
FeOH
3
=_______。
(3)深度除杂中加入MnF 可以除去钙离子、镁离子的原因是_______(用平衡移动原理解释,
2
已知:K>105可以认为反应几乎完全进行)。
(4)用石墨和金属Mn作电极,电解硫酸锰溶液可以制取金属锰,其中金属Mn应与电源
_______(填“正”或“负”)极相连;阳极产生标准状况下体积为4.48L气体时,理论上可以制取
_______g Mn。
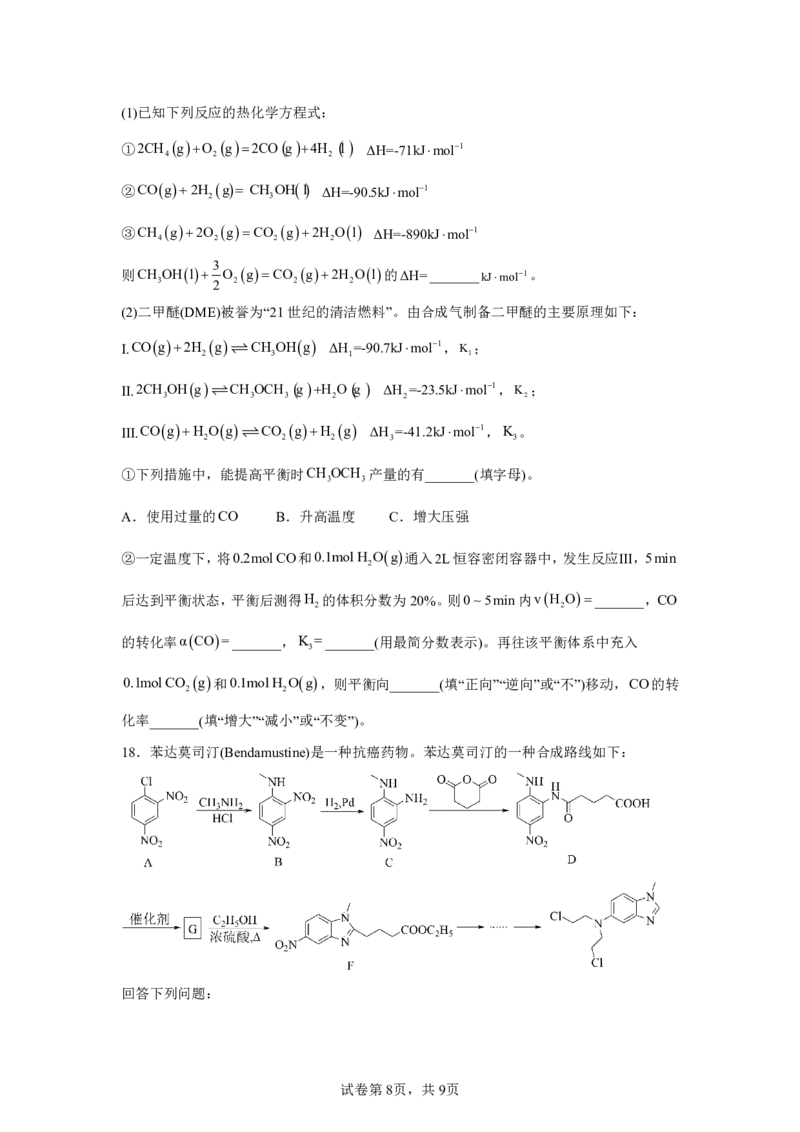
试卷第6页,共9页16.二氧化氯ClO 是一种黄绿色的气体,易溶于水,熔点59℃,沸点11℃。ClO 浓度
2 2
过高时易发生分解生成氯气和氧气,是一种有效的绿色氧化剂,可用于饮用水的消毒和纸浆
漂白等。利用亚硫酸铵、氯酸钠和硫酸制备ClO 的实验装置如下(夹持装置已省略):
2
回答下列问题:
(1)仪器a的名称为_______;装置A中发生反应的化学方程式为_______。
(2)氮气流速过快或过慢都不利于ClO 的吸收,试分析原因:_______;_______。
2
(3)装置C的作用是_______。
(4)若加入反应物中H SO 浓度过大,会产生大量SO 与ClO 反应生成Cl和SO2,使ClO 产
2 4 2 2 4 2
率降低,反应的离子方程式为_______,实验中可以用取样注射器吸取少量装置B中的液体
于试管中,加入_______(填字母),来检验是否产生了大量SO 。
2
A.酸性KMnO 溶液 B.品红溶液 C.BaCl 溶液
4 2
(5)取VmL装置A中溶液,用2步碘量法测定其中ClO 、ClO的浓度。
2 2
第1步:调节溶液pH78,加入足量KI溶液,此时ClO不被还原,而ClO 变为ClO,
2 2 2
发生的反应为2ClO 2I 2ClOI ,生成的I 用c molL1的Na S O 标准溶液滴定,消
2 2 2 2 2 2 3
耗标准溶液的体积为VmL2Na S O I Na S O 2NaI 。
1 2 2 3 2 2 4 6
第2步:调节溶液pH2,此时溶液中剩余未反应的ClO以及由第一步ClO 还原所生成的
2 2
ClO都被还原 ClO4H 4I 2I Cl2H O ,滴定时消耗c molL1 Na S O 的标准
2 2 2 2 2 2 3
溶液的体积为VmL,该溶液中ClO的浓度为_______mgL1。
2 2
17.我国利用焦炉煤气制取甲醇及二甲醚技术已日臻成熟。回答下列问题:
试卷第7页,共9页(1)已知下列反应的热化学方程式:
①2CH gO g2CO g4H l ΔH=-71kJmol1
4 2 2
②COg2H g CH OHl ΔH=-90.5kJmol1
2 3
③CH g2O gCO g2H Ol ΔH=-890kJmol1
4 2 2 2
3
则CH OHl O gCO g2H Ol的ΔH=_______kJmol1。
3 2 2 2 2
(2)二甲醚(DME)被誉为“21世纪的清洁燃料”。由合成气制备二甲醚的主要原理如下:
Ⅰ.COg2H g CH OHg ΔH =-90.7kJmol1,K ;
2 3 1 1
Ⅱ.2CH OHg CH OCH g H O g ΔH =-23.5kJmol1,K ;
3 3 3 2 2 2
Ⅲ.COgH Og CO gH g ΔH =-41.2kJmol1,K 。
2 2 2 3 3
①下列措施中,能提高平衡时CH OCH 产量的有_______(填字母)。
3 3
A.使用过量的CO B.升高温度 C.增大压强
②一定温度下,将0.2mol CO和0.1mol H Og通入2L恒容密闭容器中,发生反应Ⅲ,5min
2
后达到平衡状态,平衡后测得H 的体积分数为20%。则05min内vH O_______,CO
2 2
的转化率αCO=_______,K =_______(用最简分数表示)。再往该平衡体系中充入
3
0.1mol CO g和0.1mol H Og,则平衡向_______(填“正向”“逆向”或“不”)移动,CO的转
2 2
化率_______(填“增大”“减小”或“不变”)。
18.苯达莫司汀(Bendamustine)是一种抗癌药物。苯达莫司汀的一种合成路线如下:
回答下列问题:
试卷第8页,共9页(1)A分子中杂化方式为sp2的原子数目为_______。
(2)E的结构简式为_______。
(3)由C生成D的反应类型为_______。
(4)E中含氧官能团的名称是_______。
(5)写出由E生成F反应的化学方程式:_______。
(6)在一定条件下,1mol苯达莫司汀与足量的氢气反应,最多能消耗_______mol H ;C物质
2
的核磁共振氢谱有_______组峰。
(7)链状有机物G是 的同分异构体,并且G能发生水解反应,1mol G发生银镜
反应生成4mol Ag,符合上述条件的G的结构有_______种(不考虑立体异构)。
试卷第9页,共9页