文档内容
宣城市三校 2022-2023 学年高二上学期 8 月期初联考
化学试题
考生注意:
1.本试卷分选择题和非选择题两部分.满分100分,考试时间75分钟.
2.考生作答时,请将答案答在答题卡上.选择题每小题选出答案后,用2B铅
笔把答题卡上对应题目的答案标号涂黑;非选择题请用直径0.5毫米黑色墨水
签字笔在答题卡上各题的答题区域内作答,超出答题区域书写的答案无效,在
试题卷、草稿纸上作答无效.
3.本卷命题范围:必修第一册(20%)、必修第二册(80%).
4.可能用到的相对原子质量:H 1 C 12 O 16 C 135.5 S 32
一、选择题:本题共15小题,每小题3分,共45分.在每小题给出的四个选
项中,只有一项是符合题目要求的.
1.化学与生活密切相关,下列有关说法正确的是( )
A.液氨汽化吸收大量的热,可用作制冷剂
B.二氧化硫具有漂白性,可大量用于漂白银耳
C.单晶硅可用于制造光导纤维
D.冬奥会的火炬外壳使用了新型有机非金属材料——碳纤维复合材料
2.下列有关化学用语表示正确的是( )
A. 的电子式
B. O的结构式:
C.聚丙烯的结构简式:
D. 的电离方程式:
3.化学与人类的健康息息相关,下列说法错误的是( )
A.纤维素是人体中能量的重要来源
B.淀粉可在人体内逐步水解,最终生成葡萄糖
C.结晶牛胰岛素是蛋白质
D.油脂可以看作是高级脂肪酸与甘油反应生成的酯
4.现代食品工业中,食品添加剂的使用满足了人们对食品多样化的需求.下列有关食品添加剂的说法正确的是( )
A.亚硝酸钠可作为防腐剂和护色剂,可大量使用
B.硫酸锌、硫酸亚铁都可作为营养强化剂C.碳酸氢铵、碳酸钙都可作为膨松剂
D.谷氨酸钠是一种着色剂
5. 为阿伏加德罗常数的值,下列说法正确的是( )
A. 固体中含有的离子总数为
B.标准状况下, 中含有的分子数为
C. 与 充分反应,转移电子数为
D.常温常压下, 乙醇所含共价键为
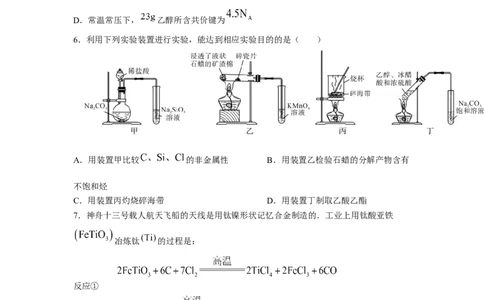
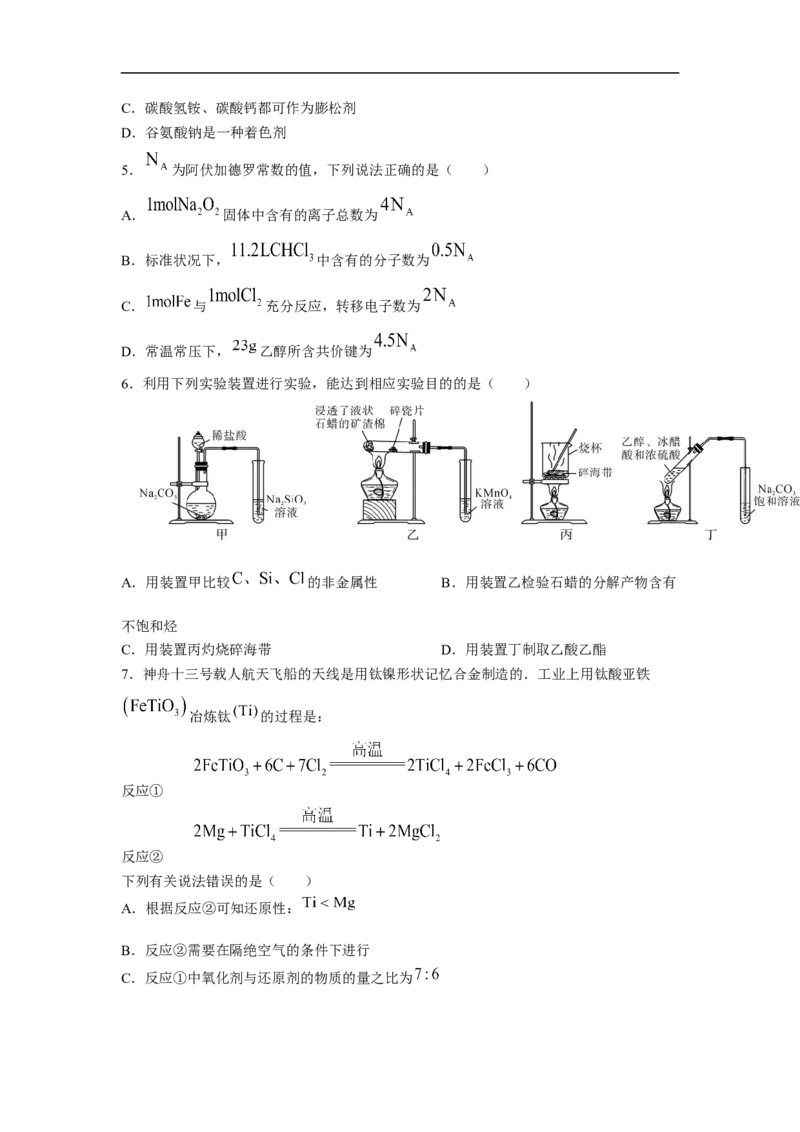
6.利用下列实验装置进行实验,能达到相应实验目的的是( )
A.用装置甲比较 的非金属性 B.用装置乙检验石蜡的分解产物含有
不饱和烃
C.用装置丙灼烧碎海带 D.用装置丁制取乙酸乙酯
7.神舟十三号载人航天飞船的天线是用钛镍形状记忆合金制造的.工业上用钛酸亚铁
冶炼钛 的过程是:
反应①
反应②
下列有关说法错误的是( )
A.根据反应②可知还原性:
B.反应②需要在隔绝空气的条件下进行
C.反应①中氧化剂与还原剂的物质的量之比为D.反应①若生成标准状况下 ,则转移 电子
8.下列指定反应的离子方程式书写正确的是( )A.过量的 通入 溶液:
B.用氢氟酸蚀刻玻璃:
C.铜片加入稀硝酸中:
D.氢氧化钠吸收二氧化氮:
9.X、Y、Z是三种短周期元素,其中X、Y位于同一主族.X原子的最外层电子数是其电
子层数的3倍.Z原子的核外电子数比Y的核外电子数多1.下列说法正确的是( )
A.离子半径由大到小的顺序:
B.由X、Y两种元素组成的化合物可能具有漂白性
C.简单氢化物的稳定性:
D.最高价氧化物对应水化物的酸性:
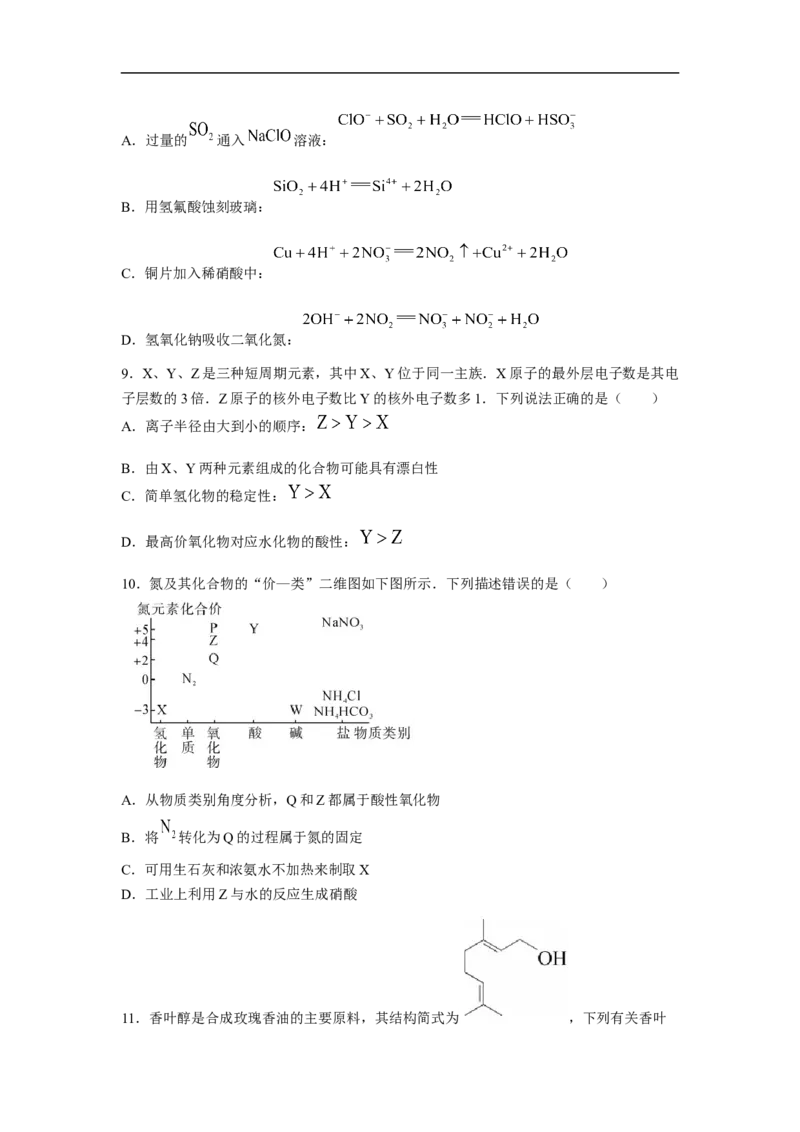
10.氮及其化合物的“价—类”二维图如下图所示.下列描述错误的是( )
A.从物质类别角度分析,Q和Z都属于酸性氧化物
B.将 转化为Q的过程属于氮的固定
C.可用生石灰和浓氨水不加热来制取X
D.工业上利用Z与水的反应生成硝酸
11.香叶醇是合成玫瑰香油的主要原料,其结构简式为 ,下列有关香叶醇的叙述正确的是( )
A.该有机物与乙醇互为同系物B.香叶醇的分子式为
C.该有机物不能使溴的四氯化碳溶液褪色
D. 该有机物最多可以与 发生加成反应
12.下列实验操作、实验现象和实验结论都正确的是( )
选项 实验操作 实验现象 实验结论
A 得到澄清溶液
向 溶液中滴加过量氨水 与 能大量共
存
B 紫色褪去
向酸性 溶液中加入 粉 中含二价铁
末
C 向乙醇中加入一块金属钠 有气泡产生 乙醇中含有水
D 向蓝色石蕊试纸上滴加新制氯水 试纸边缘呈红色,中间为白 氯水既有酸性又有还原性
色
A.A B.B C.C D.D
13.一定温度下,在容积不变的密闭容器中进行如下可逆反应:
,下列能表明该反应已达到化学平衡状态的
是( )
① ② 的体积分数不再变化
③容器内气体压强不再变化 ④ 键断裂的同时,有 键
断裂
⑤混合气体的体积不再变化
A.①②③ B.②③ C.②④⑤ D.③④⑤
14. 电池是目前电池中综合性能最好的一种电池,其原理示意图如图所示.已
知电池放电时的反应为 .下列说法正确的是( )A. 为电池的正极,发生氧化反应 B.电流由 经负载,流向 极C.正极的电极反应式为
D.将熔融的 改为 的水溶液,电池性能更好
15. 为白色固体,难溶于水和乙醇,潮湿时易被氧化,常用于媒染剂.以废铜渣
(主要成分为 ,含少量 、 等)为原料制备 的工艺流程如下:
下列说法正确的是( )
A.“碱溶”时发生的反应为
B.“过滤”时使用到的仪器有分液漏斗、玻璃棒、烧杯等
C.“酸溶”过程中,有大量的气体产生
D.“还原”反应所得的溶液中大量存在
二、非选择题:本题共4大题,共55分.
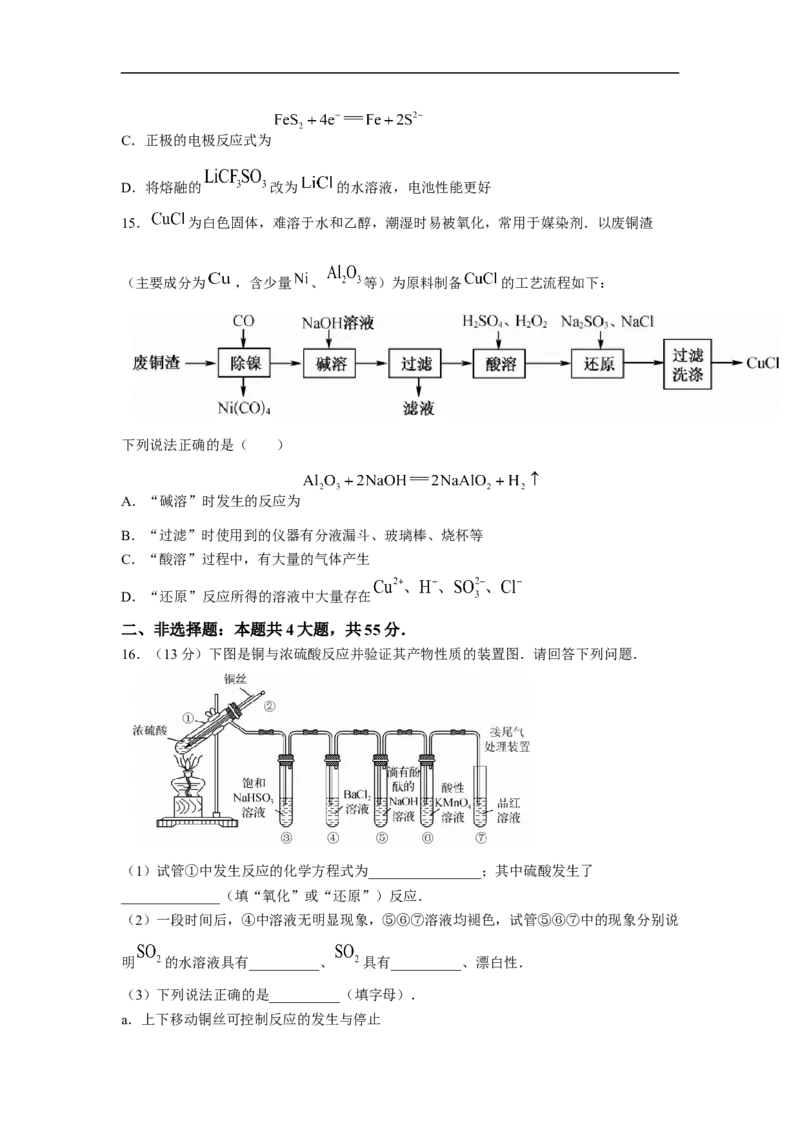
16.(13分)下图是铜与浓硫酸反应并验证其产物性质的装置图.请回答下列问题.
(1)试管①中发生反应的化学方程式为________________;其中硫酸发生了
______________(填“氧化”或“还原”)反应.
(2)一段时间后,④中溶液无明显现象,⑤⑥⑦溶液均褪色,试管⑤⑥⑦中的现象分别说
明 的水溶液具有__________、 具有__________、漂白性.
(3)下列说法正确的是__________(填字母).
a.上下移动铜丝可控制反应的发生与停止b.反应结束后,从导管向装置中鼓入空气,使气体完全被吸收,防止污染c.实验结束后,试管①中有白色固体出现,为确认白色固体为产物 ,可立刻向试
管①中加水,观察颜色
(4)充分反应后发现,铜丝与硫酸都有剩余,在此情况下,加入下列物质能使溶液中
变大的是____________(填字母).
a. b. C.
(5)反应停止后,待装置冷却,向试管④中加入氯水,产生白色沉淀,反应的离子方程式
为______________.
(6)为了测定尾气中 的含量,将尾气样品经过管道通入盛有 酸性
溶液的密闭容器中.若管道中气体流量为 ,经过 溶液恰好褪色,
假定样品中 被充分吸收,该尾气样品中 的含量为____________ .(假设尾
气中其他气体不与酸性 溶液反应)
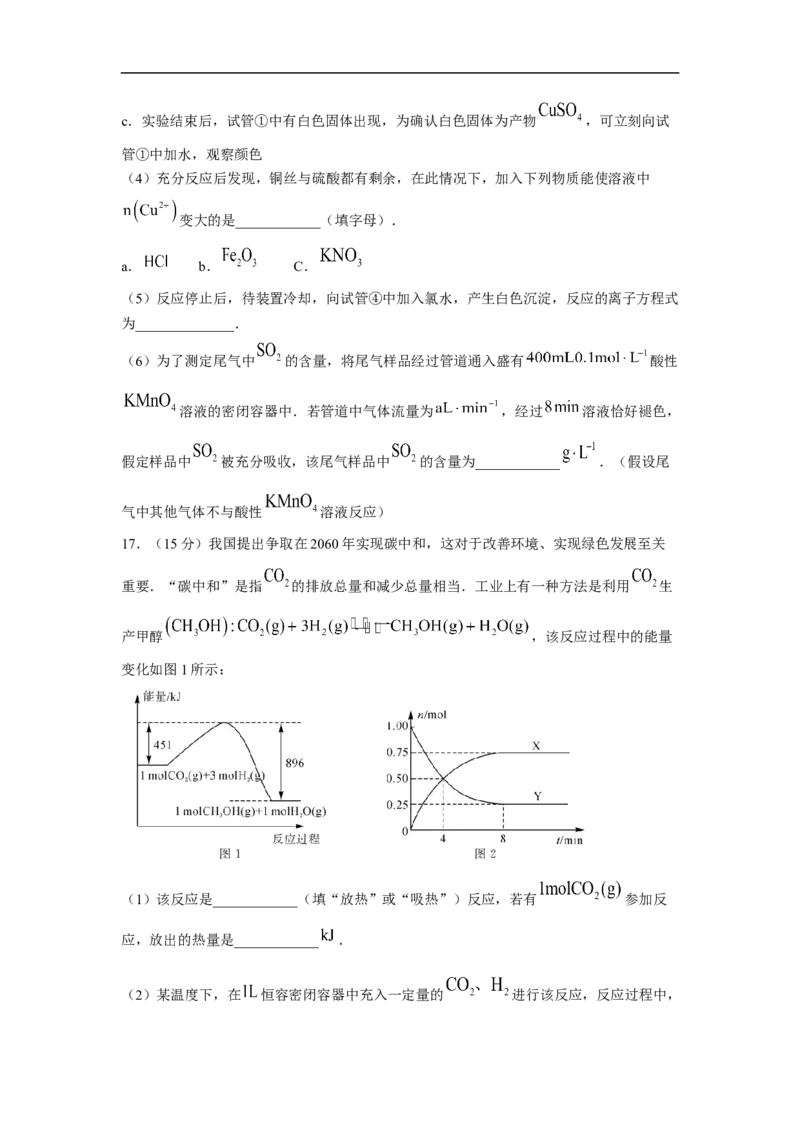
17.(15分)我国提出争取在2060年实现碳中和,这对于改善环境、实现绿色发展至关
重要.“碳中和”是指 的排放总量和减少总量相当.工业上有一种方法是利用 生
产甲醇 ,该反应过程中的能量
变化如图1所示:
(1)该反应是____________(填“放热”或“吸热”)反应,若有 参加反
应,放出的热量是____________ .
(2)某温度下,在 恒容密闭容器中充入一定量的 进行该反应,反应过程中,其中两种气体的物质的量 随时间 的变化情况如图2所示.
①Y代表的反应物的化学式为_____________.
② 时, ________ (填“>”“<”或“=”).③若要增大反应速率,可采取的措施有_____________(写一条即可).
④反应开始至 时,X的平均反应速率为__________________.
⑤若该反应分别在甲、乙、丙三个相同的密闭容器中进行,经相同时间后,测得三个容器
中的反应速率分别为甲: ,乙:
,丙: .则甲、乙、丙三个
容器中反应速率由快到慢的顺序为____________.
(3)工业上甲醇可以用做燃料电池,电池总反应为: .
则甲醇作电池的_________极(填“正”或“负”),若电池工作中有 转移,则理
论上消耗甲醇的质量是________g.
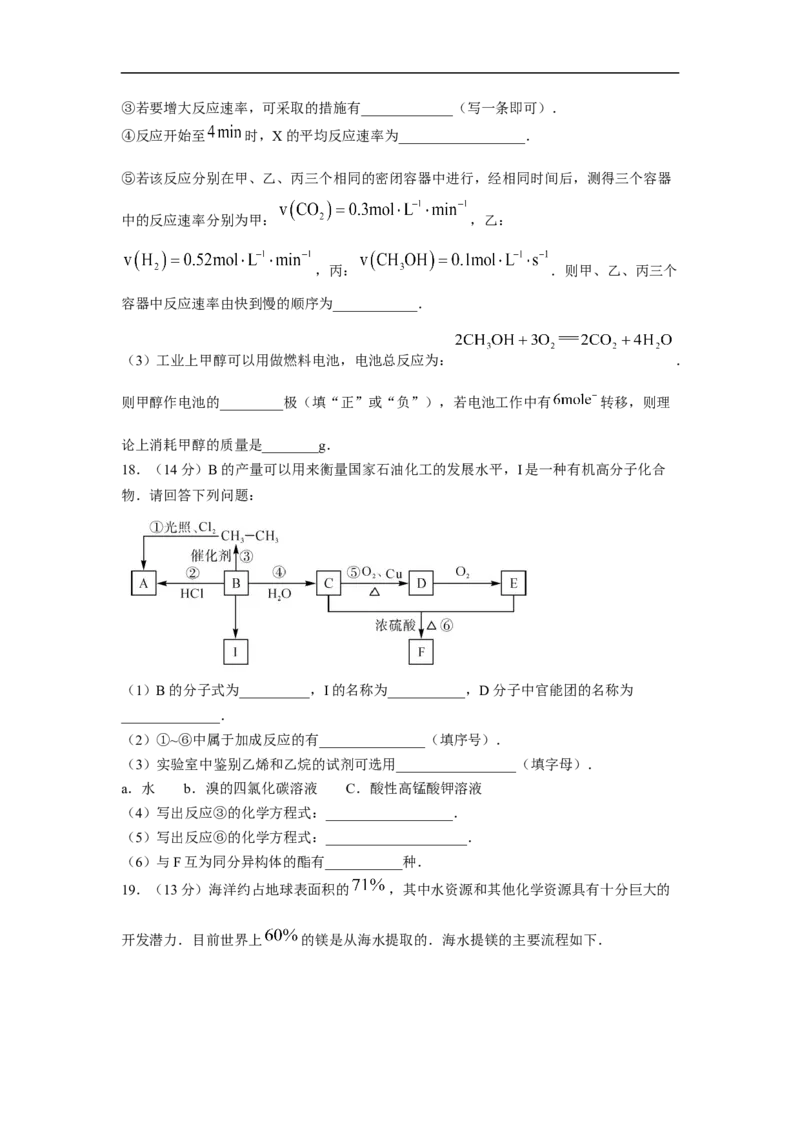
18.(14分)B的产量可以用来衡量国家石油化工的发展水平,I是一种有机高分子化合
物.请回答下列问题:
(1)B的分子式为__________,I的名称为___________,D分子中官能团的名称为
______________.
(2)①~⑥中属于加成反应的有_______________(填序号).
(3)实验室中鉴别乙烯和乙烷的试剂可选用_________________(填字母).
a.水 b.溴的四氯化碳溶液 C.酸性高锰酸钾溶液
(4)写出反应③的化学方程式:__________________.
(5)写出反应⑥的化学方程式:____________________.
(6)与F互为同分异构体的酯有___________种.
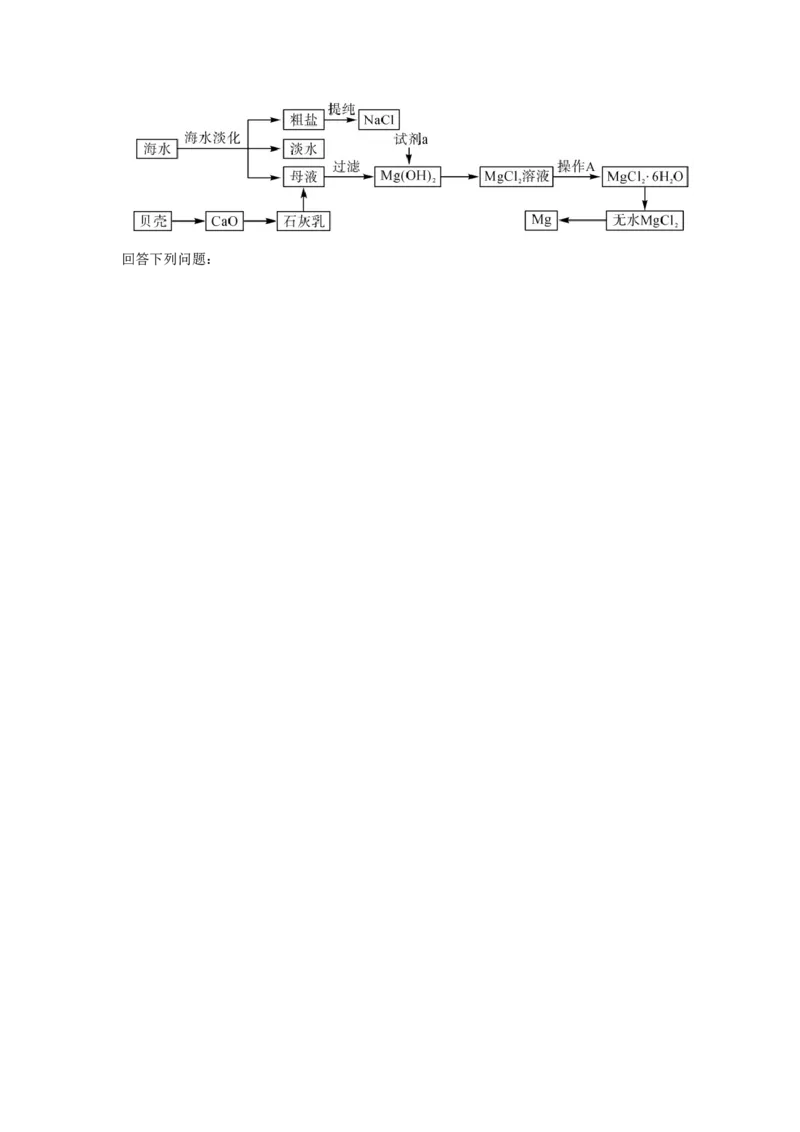
19.(13分)海洋约占地球表面积的 ,其中水资源和其他化学资源具有十分巨大的
开发潜力.目前世界上 的镁是从海水提取的.海水提镁的主要流程如下.回答下列问题:(1)海水淡化的方法主要有_____________、_____________蒸馏法.
(2)从粗盐中制得的精盐还可以作为化工原料用于生产纯碱,原理为(用化学方程式表
示)
__________________________; .
(3)工业上从母液中获取 用石灰乳而不用 溶液的原因是_____________.
(4)试剂a为_____________(填化学式),操作A为_____________.
(5)无水 在熔融状态下,通电后会生成 和 ,该反应的化学方程式是
__________________________.
(6)海水提镁的过程,先将海水中的氯化镁转变为氢氧化镁,再转变为氯化镁的原因是
__________________________.宣城市三校 2022-2023 学年高二上学期 8 月期初联考
化学参考答案
1-10 ADABC BCDBA 11-15 DBBCC
16.(1) (2分) 还原(1分)
(2)酸性(1分) 还原性(1分)
(3)ab(2分)
(4)bc(2分)
(5) (或
)(2分)
(6) (2分)
17.(1)放热(1分) 445(2分)
(2)① (2分) ②>(2分) ③升高温度(或加入反应物或合适的催化剂等)
(1分)
④ (2分)
⑤丙>甲>乙(2分)
(3)负(1分) 32(2分)
18.(1) (1分) 聚乙烯(2分) 醛基(1分)
(2)②③④(2分)
(3)bc(2分)
(4) (2分)(条件写加热、催化剂亦可)
(5) (2分)
(6)3(2分)
19.(1)电渗析法 离子交换法(各1分)(2) (2分)(3)石灰乳原料丰富,成本低(2分)
(4) (1分) 蒸发浓缩、冷却结晶、过滤(2分)
(5) (2分)
(6)海水中氯化镁的含量很大,但镁离子浓度很低,该过程可以使镁离子富集,提高镁离
子浓度(或其他合理答案,答到富集或提高 浓度都可得分)(2分)