文档内容
微专题突破3 新情境方程式的书写二
一、选择题
1.(2024·淮安市淮海中学三模)下列离子方程式与所给事实不相符的是
A.用过量的氨水吸收SO :NH ·HO+SO =NH+HSO -
2 3 2 2 3
B.用饱和食盐水制烧碱:2Cl-+2HO====2OH-+Cl↑+H↑
2 2 2
C.用TiCl 制TiO ·xHO:TiCl +(x+2)HO====TiO ·xHO↓+4HCl
4 2 2 4 2 2 2
D.用焦炭还原石英砂制粗硅:SiO+2C====Si+2CO↑
2
2.(2024·南师附中三模)宏观辨识与微观探析是化学学科核心素养之一,下列反应的离子方程式
书写错误的是
A.漂白粉溶液吸收CO 后产生白色沉淀:Ca2++CO+HO=CaCO ↓+2H+
2 2 2 3
B.氯气通入氢氧化钠溶液制“84”消毒液:Cl+2OH-=Cl-+ClO-+HO
2 2
C.过氧化钠溶于水制氧气:2NaO+2HO=4Na++4OH-+O↑
2 2 2 2
D.用氯化铁溶液蚀刻覆铜板:2Fe3++Cu=2Fe2++Cu2+
3.(江苏高考模拟组合题)室温下,下列实验探究方案能达到探究目的的是
选项 探究方案 探究目的
向0.1 mol·L-1 HO 溶液中滴加0.1 mol·L-1 KMnO 溶液,
A 2 2 4 HO 具有氧化性
2 2
观察溶液颜色变化
向2 mL NH Fe(SO ) 溶液中滴加几滴0.1 mol·L-1 KI溶液,
B 4 4 2 Fe3+是否具有氧化性
再滴加淀粉溶液,观察溶液颜色变化
向KBr、KI混合溶液中依次加入少量氯水和CCl ,振荡后静置,
C 4 氧化性:Cl>Br >I
2 2 2
观察CCl 层颜色
4
D 向Fe(NO ) 溶液中滴加淀粉,再通入HI气体,观察现象 比较Fe3+与I 氧化性的强弱
3 3 2
4.(2024·南通通州模拟)金属Na可以与液氨反应制取一种强碱性物质NaNH ;金属Mg可以在
2
高温条件下还原TiCl 制备熔点较高金属Ti,金属Ti是一种重要的航空材料,其性质稳定,常温下不与稀
4
盐酸反应;金属Al可以用来作电池的负极材料,一种Al-空气电池在碱性电解质中的总反应为 4Al+3O
2
+6HO+4OH-=4[Al(OH)]-。下列化学反应表示正确的是
2 4
A.Na与液氨反应:Na+NH =NaNH +H↑
3 2 2
B.MgCl 的水解反应:Mg2++2HO=Mg(OH)↓+2H+
2 2 2
C.Al溶于氢氧化钠溶液中:2Al+2NaOH+6HO=2Na[Al(OH)]+3H↑
2 4 2
D.该Al-空气电池的负极反应式:Al+4OH-+3e-=4[Al(OH)]-
4
二、填空题
5.(2024·江苏南京市、盐城市一模)VO-WO/TiO 催化剂可以催化NH 脱除烟气中的NO。
2 5 3 2 3
VO 的回收。回收VO 的过程可表示为:
2 5 2 5
①酸浸时,投料完成后提高原料浸出率的措施有___________________________________________。
②酸浸过程中,VO 转化成VO2+,该反应的离子方程式为
2 5
___________________________________________________________。
6.(2024·扬州市高三下学期开学考)以盐湖锂矿(主要成分为LiO••Al O •4SiO ,还含有Fe2+及
2 2 3 2微专题突破3 新情境方程式的书写二
少量有机物等)为原料制备LiCO 的方法如下:
2 3
净化:
①加碱调节滤液的pH至弱碱性,使Al3+沉淀;将再加入适量Ca(ClO) 溶液将Fe2+转化为沉淀,过
2
滤。ClO-与Fe2+反应的离子方程式为_________________________________________________________。
②调节滤液的pH,再加入适量NaCO 粉末,过滤,得LiSO 溶液。过滤所得滤渣的主要成分是
2 3 2 4
___________。
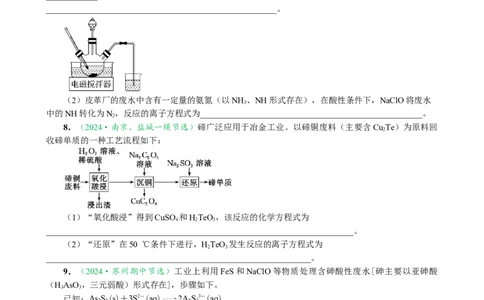
7.(2021·江苏高考17题节选)(1)以软锰矿粉(含MnO 及少量Fe、Al、Si、Ca、Mg等的氧化
2
物)为原料制备电池级MnO 。将一定量软锰矿粉与NaSO 、HSO 溶液中的一种配成悬浊液,加入到三
2 2 3 2 4
颈瓶中(如图),70 ℃下通过滴液漏斗缓慢滴加另一种溶液,充分反应,过滤。滴液漏斗中的溶液是
____________;MnO 转化为Mn2+的离子方程式为
2
______________________________________________________。
(2)皮革厂的废水中含有一定量的氨氮(以NH 、NH形式存在),在酸性条件下,NaClO将废水
3
中的NH转化为N,反应的离子方程式为____________________________________________________。
2
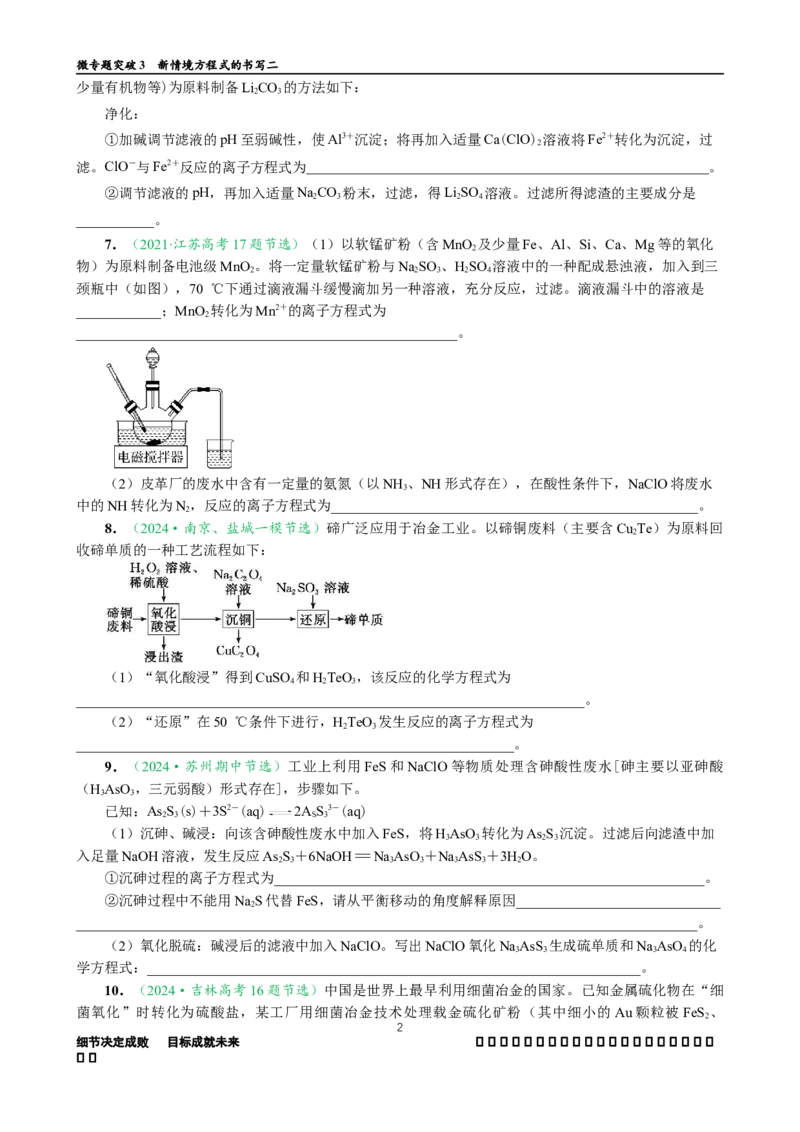
8.(2024·南京、盐城一模节选)碲广泛应用于冶金工业。以碲铜废料(主要含Cu Te)为原料回
2
收碲单质的一种工艺流程如下:
(1)“氧化酸浸”得到CuSO 和HTeO ,该反应的化学方程式为
4 2 3
________________________________________________________________________。
(2)“还原”在50 ℃条件下进行,HTeO 发生反应的离子方程式为
2 3
______________________________________________________________。
9.(2024·苏州期中节选)工业上利用FeS和NaClO等物质处理含砷酸性废水[砷主要以亚砷酸
(HAsO ,三元弱酸)形式存在],步骤如下。
3 3
已知:As S(s)+3S2-(aq) 2A S3-(aq)
2 3 S 3
(1)沉砷、碱浸:向该含砷酸性废水中加入FeS,将HAsO 转化为As S 沉淀。过滤后向滤渣中加
3 3 2 3
入足量NaOH溶液,发生反应As S+6NaOH=NaAsO +NaAsS +3HO。
2 3 3 3 3 3 2
①沉砷过程的离子方程式为_____________________________________________________________。
②沉砷过程中不能用NaS代替FeS,请从平衡移动的角度解释原因_____________________________
2
________________________________________________________________________________________。
(2)氧化脱硫:碱浸后的滤液中加入NaClO。写出NaClO氧化NaAsS 生成硫单质和NaAsO 的化
3 3 3 4
学方程式:______________________________________________________________________。
10.(2024·吉林高考16题节选)中国是世界上最早利用细菌冶金的国家。已知金属硫化物在“细
菌氧化”时转化为硫酸盐,某工厂用细菌冶金技术处理载金硫化矿粉(其中细小的Au颗粒被FeS 、
2
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
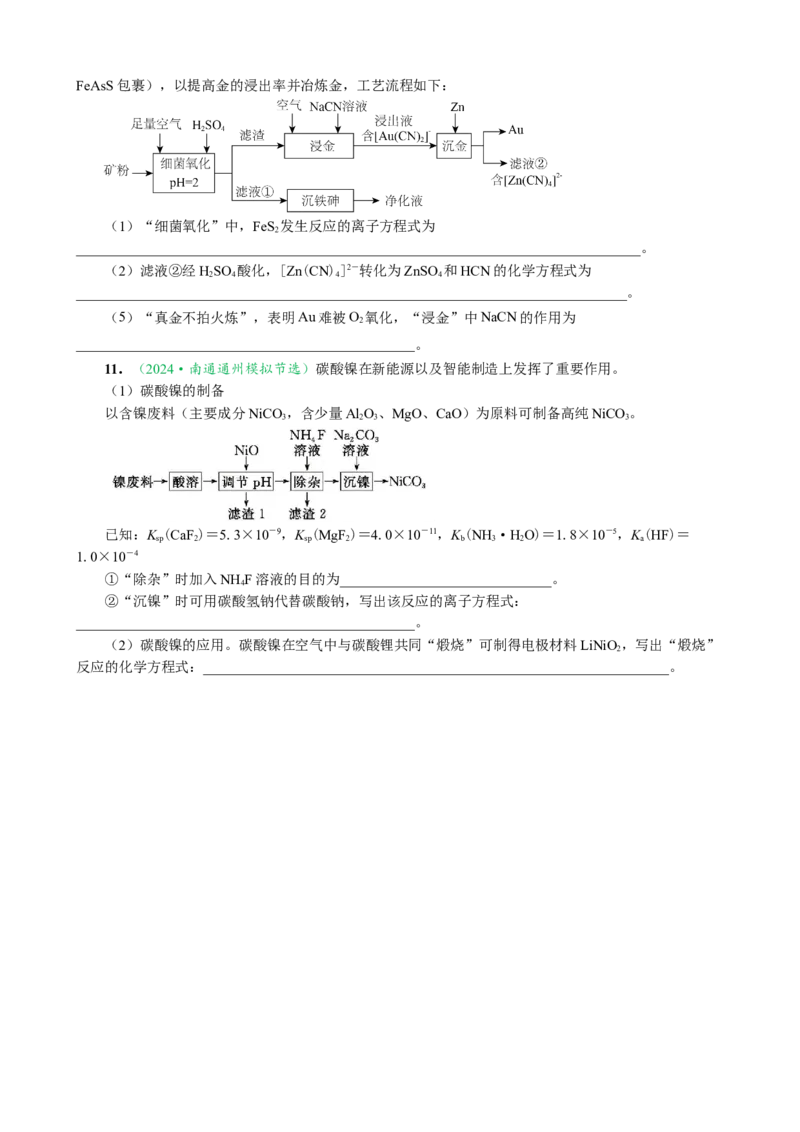
找找FeAsS包裹),以提高金的浸出率并冶炼金,工艺流程如下:
(1)“细菌氧化”中,FeS 发生反应的离子方程式为
2
________________________________________________________________________________。
(2)滤液②经HSO 酸化,[Zn(CN)]2-转化为ZnSO 和HCN的化学方程式为
2 4 4 4
______________________________________________________________________________。
(5)“真金不拍火炼”,表明Au难被O 氧化,“浸金”中NaCN的作用为
2
________________________________________________。
11.(2024·南通通州模拟节选)碳酸镍在新能源以及智能制造上发挥了重要作用。
(1)碳酸镍的制备
以含镍废料(主要成分NiCO,含少量Al O、MgO、CaO)为原料可制备高纯NiCO。
3 2 3 3
已知:K (CaF )=5.3×10-9,K (MgF )=4.0×10-11,K (NH ·HO)=1.8×10-5,K(HF)=
sp 2 sp 2 b 3 2 a
1.0×10-4
①“除杂”时加入NH F溶液的目的为______________________________。
4
②“沉镍”时可用碳酸氢钠代替碳酸钠,写出该反应的离子方程式:
________________________________________________。
(2)碳酸镍的应用。碳酸镍在空气中与碳酸锂共同“煅烧”可制得电极材料LiNiO ,写出“煅烧”
2
反应的化学方程式:__________________________________________________________________。