文档内容
押广东卷第 19 题
化学反应原理综合题
核心考点 考情统计 考向预测 备考策略
考查气相中的化学反应原
气相中的
2021·广东卷,19 理,难点在于K 的考查;
化学平衡 P 1.重视热化学、氧化还原、物
考查液相中的化学反应原
质结构、物质性质等于基础得
理,难点在于水溶液图像的
分点,确保基础分。
解读和三大守恒的应用。
2.关注K 、K 、三大守恒、图
P C
无论是哪种情况,热化学、
液相中的 2023·广东卷,19 像分析等,实现难点突破。
氧化还原、物质结构、物质
化学平衡 2022·广东卷,19
性质等都属于基础得分点。
1.(2023广东卷,19)配合物广泛存在于自然界,且在生产和生活中都发挥着重要作用。
(1)某有机物 能与 形成橙红色的配离子 ,该配离子可被 氧化成淡蓝色的配离子
。
①基态 的 电子轨道表示式为 。
②完成反应的离子方程式:
(2)某研究小组对(1)中②的反应进行了研究。
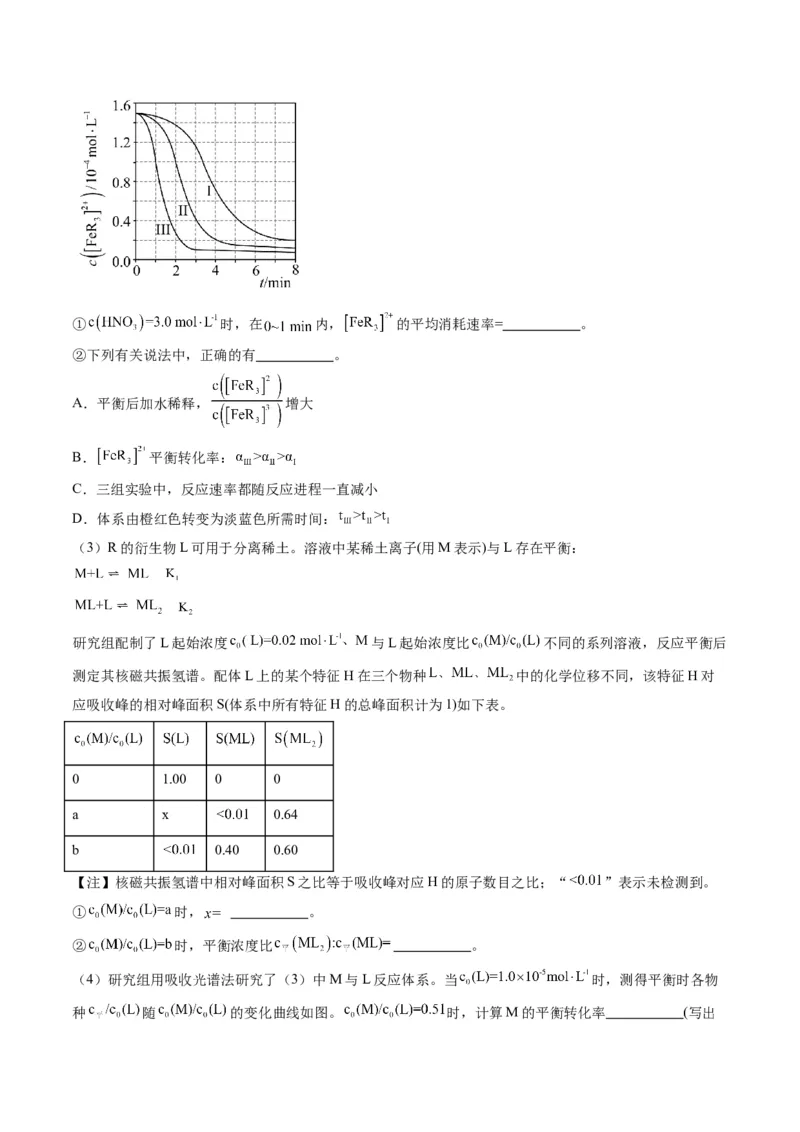
用浓度分别为 的 溶液进行了三组实验,得到 随时间t的
变化曲线如图。① 时,在 内, 的平均消耗速率= 。
②下列有关说法中,正确的有 。
A.平衡后加水稀释, 增大
B. 平衡转化率:
C.三组实验中,反应速率都随反应进程一直减小
D.体系由橙红色转变为淡蓝色所需时间:
(3)R的衍生物L可用于分离稀土。溶液中某稀土离子(用M表示)与L存在平衡:
研究组配制了L起始浓度 与L起始浓度比 不同的系列溶液,反应平衡后
测定其核磁共振氢谱。配体L上的某个特征H在三个物种 中的化学位移不同,该特征H对
应吸收峰的相对峰面积S(体系中所有特征H的总峰面积计为1)如下表。
0 1.00 0 0
a x 0.64
b 0.40 0.60
【注】核磁共振氢谱中相对峰面积S之比等于吸收峰对应H的原子数目之比;“ ”表示未检测到。
① 时, 。
② 时,平衡浓度比 。
(4)研究组用吸收光谱法研究了(3)中M与L反应体系。当 时,测得平衡时各物
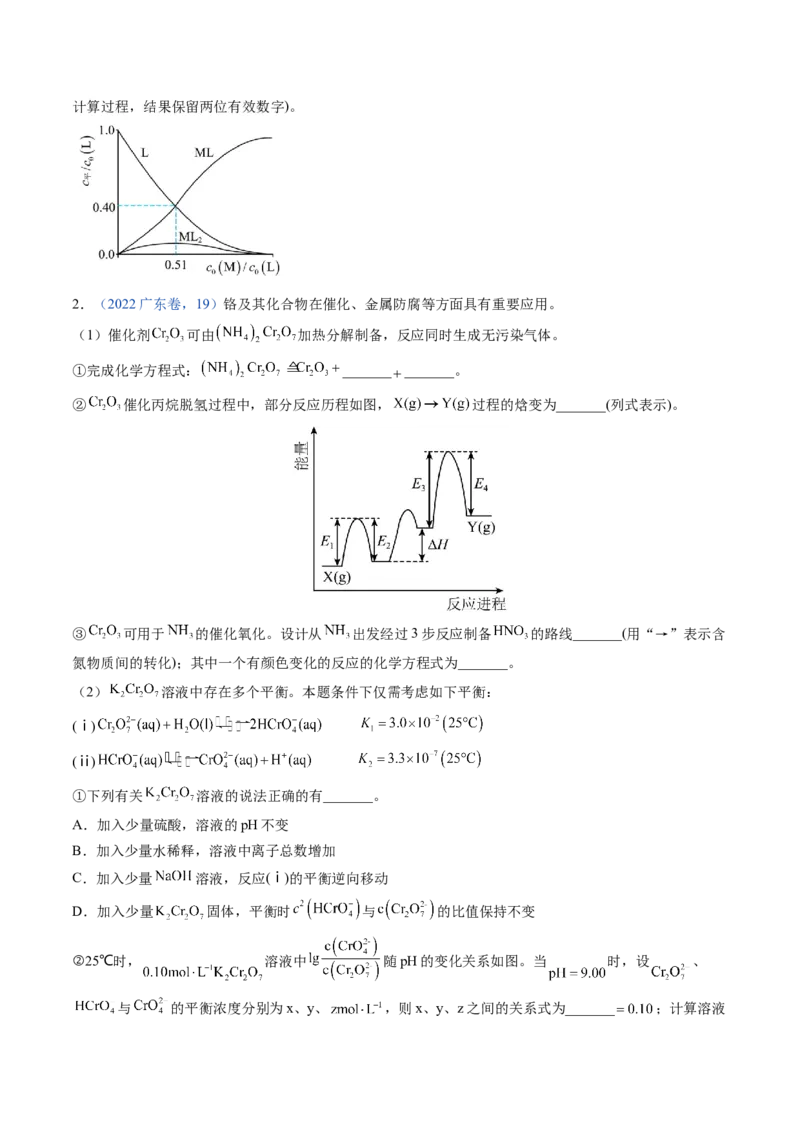
种 随 的变化曲线如图。 时,计算M的平衡转化率 (写出计算过程,结果保留两位有效数字)。
2.(2022广东卷,19)铬及其化合物在催化、金属防腐等方面具有重要应用。
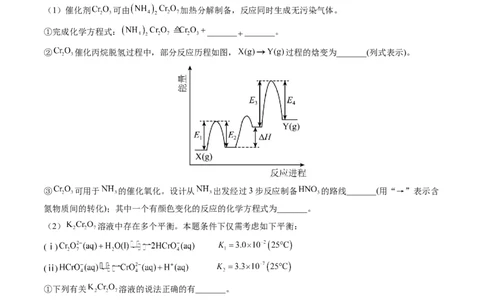
(1)催化剂 可由 加热分解制备,反应同时生成无污染气体。
①完成化学方程式: _______ _______。
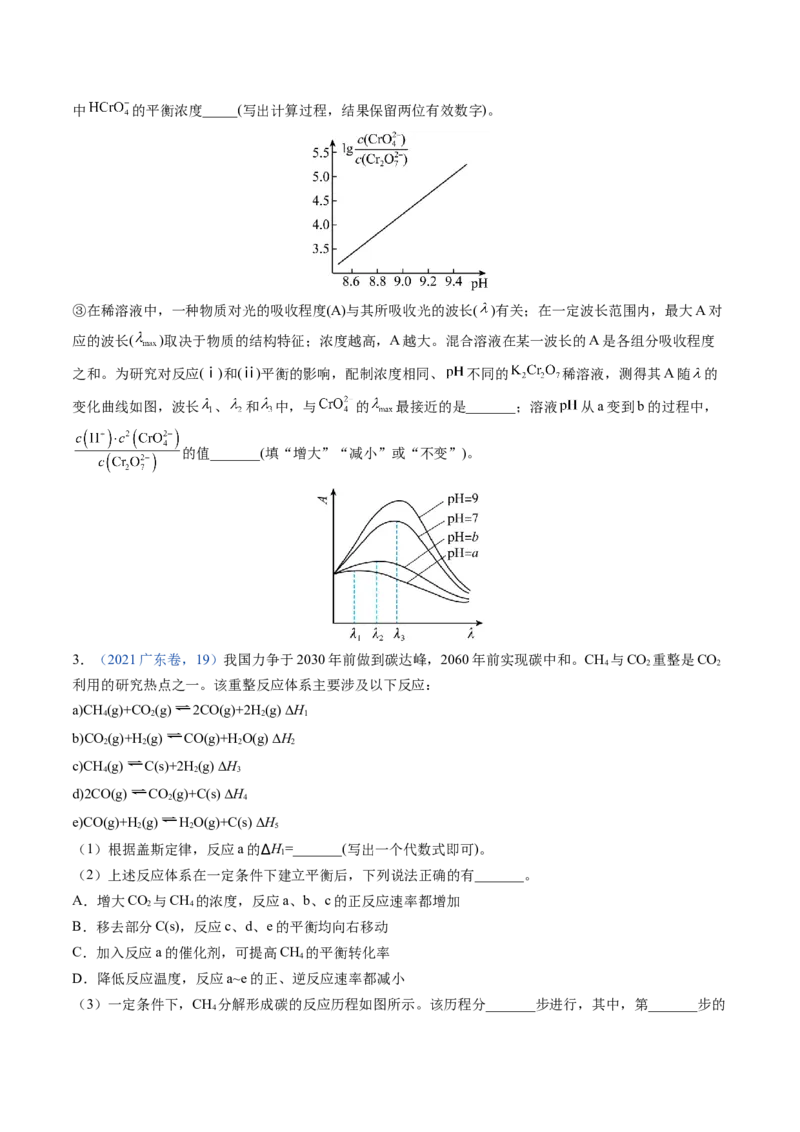
② 催化丙烷脱氢过程中,部分反应历程如图, 过程的焓变为_______(列式表示)。
③ 可用于 的催化氧化。设计从 出发经过3步反应制备 的路线_______(用“→”表示含
氮物质间的转化);其中一个有颜色变化的反应的化学方程式为_______。
(2) 溶液中存在多个平衡。本题条件下仅需考虑如下平衡:
(ⅰ)
(ⅱ)
①下列有关 溶液的说法正确的有_______。
A.加入少量硫酸,溶液的pH不变
B.加入少量水稀释,溶液中离子总数增加
C.加入少量 溶液,反应(ⅰ)的平衡逆向移动
D.加入少量 固体,平衡时 与 的比值保持不变
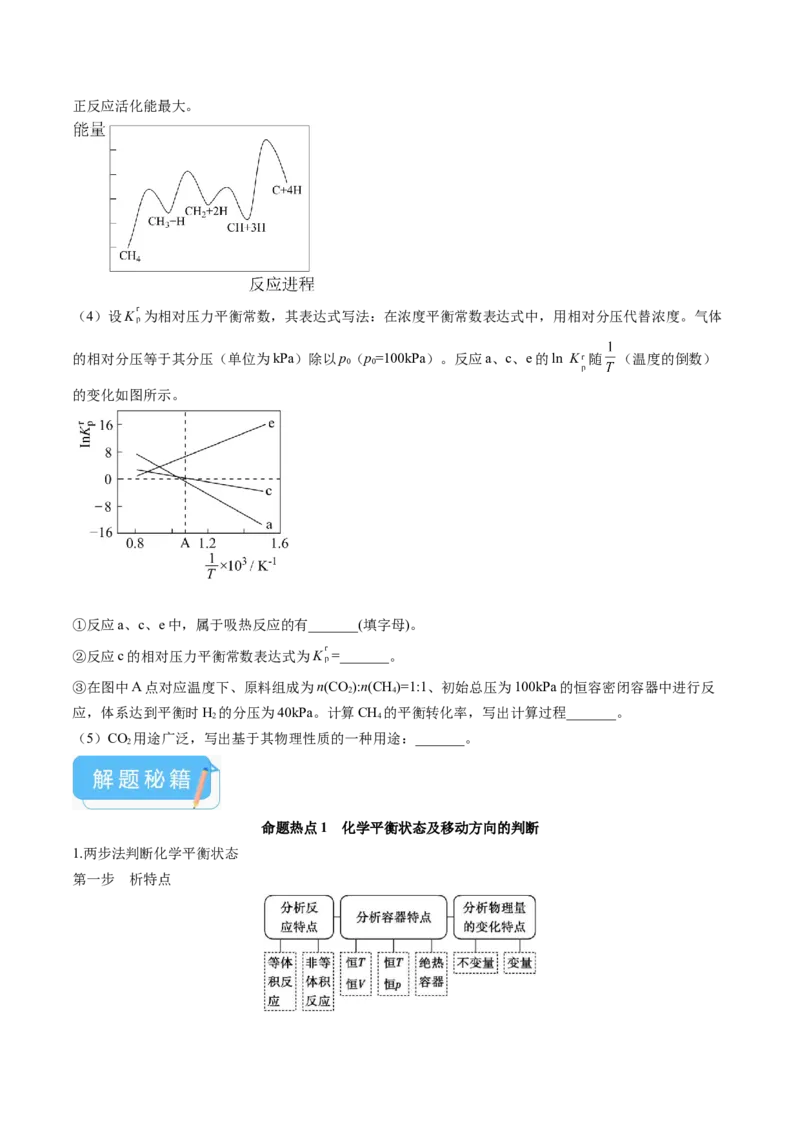
②25℃时, 溶液中 随pH的变化关系如图。当 时,设 、
与 的平衡浓度分别为x、y、 ,则x、y、z之间的关系式为_______ ;计算溶液中 的平衡浓度_____(写出计算过程,结果保留两位有效数字)。
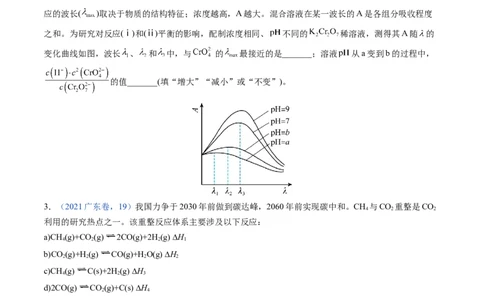
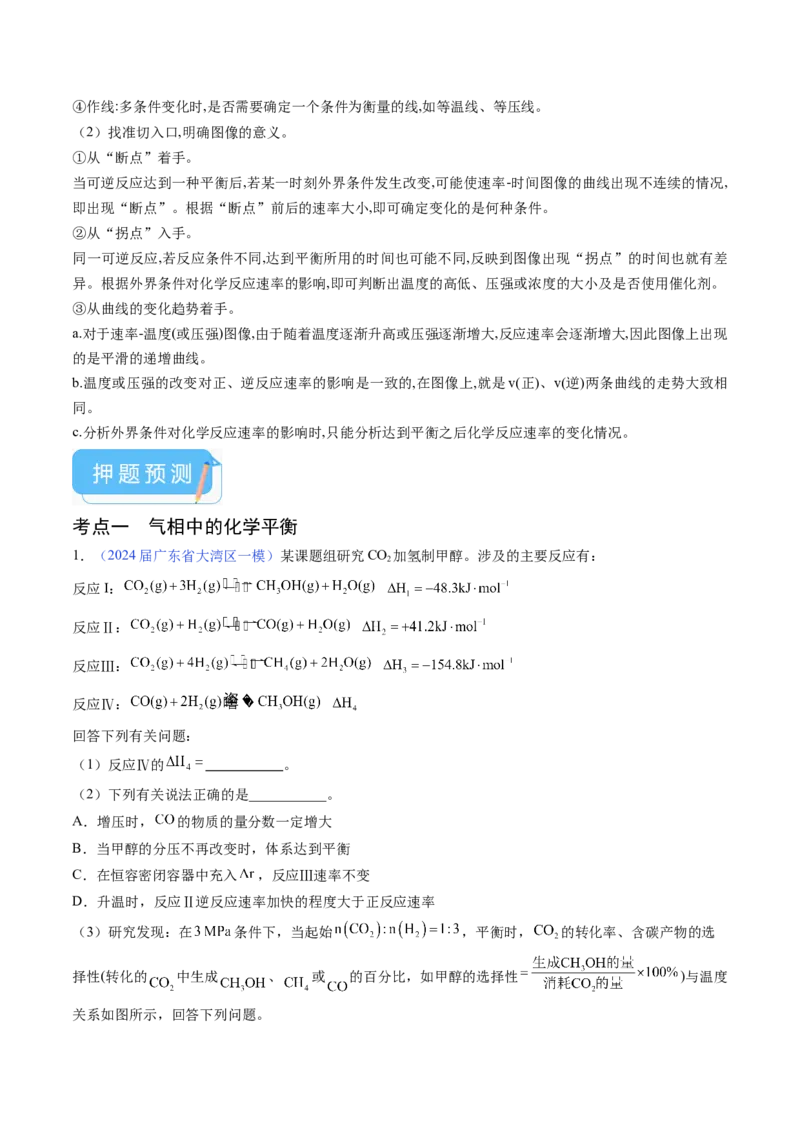
③在稀溶液中,一种物质对光的吸收程度(A)与其所吸收光的波长( )有关;在一定波长范围内,最大A对
应的波长( )取决于物质的结构特征;浓度越高,A越大。混合溶液在某一波长的A是各组分吸收程度
之和。为研究对反应(ⅰ)和(ⅱ)平衡的影响,配制浓度相同、 不同的 稀溶液,测得其A随 的
变化曲线如图,波长 、 和 中,与 的 最接近的是_______;溶液 从a变到b的过程中,
的值_______(填“增大”“减小”或“不变”)。
3.(2021广东卷,19)我国力争于2030年前做到碳达峰,2060年前实现碳中和。CH 与CO 重整是CO
4 2 2
利用的研究热点之一。该重整反应体系主要涉及以下反应:
a)CH(g)+CO (g) 2CO(g)+2H(g) ∆H
4 2 2 1
b)CO(g)+H(g) CO(g)+HO(g) ∆H
2 2 2 2
c)CH(g) C(s)+2H(g) ∆H
4 2 3
d)2CO(g) CO(g)+C(s) ∆H
2 4
e)CO(g)+H(g) HO(g)+C(s) ∆H
2 2 5
(1)根据盖斯定律,反应a的∆H=_______(写出一个代数式即可)。
1
(2)上述反应体系在一定条件下建立平衡后,下列说法正确的有_______。
A.增大CO 与CH 的浓度,反应a、b、c的正反应速率都增加
2 4
B.移去部分C(s),反应c、d、e的平衡均向右移动
C.加入反应a的催化剂,可提高CH 的平衡转化率
4
D.降低反应温度,反应a~e的正、逆反应速率都减小
(3)一定条件下,CH 分解形成碳的反应历程如图所示。该历程分_______步进行,其中,第_______步的
4正反应活化能最大。
(4)设K 为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体
的相对分压等于其分压(单位为kPa)除以p(p=100kPa)。反应a、c、e的ln K 随 (温度的倒数)
0 0
的变化如图所示。
①反应a、c、e中,属于吸热反应的有_______(填字母)。
②反应c的相对压力平衡常数表达式为K =_______。
③在图中A点对应温度下、原料组成为n(CO):n(CH)=1:1、初始总压为100kPa的恒容密闭容器中进行反
2 4
应,体系达到平衡时H 的分压为40kPa。计算CH 的平衡转化率,写出计算过程_______。
2 4
(5)CO 用途广泛,写出基于其物理性质的一种用途:_______。
2
命题热点1 化学平衡状态及移动方向的判断
1.两步法判断化学平衡状态
第一步 析特点第二步 作判断
根据参加反应的体系的特点,通过推理作出判断,如v =v ,则处于平衡状态,否则反应未达到平衡状态。
正 逆
2.化学平衡移动的判断
如果改变影响平衡的一个条件(如温度、浓度、压强等),平衡就向能使
依据勒夏特列原理判断
这种改变减弱的方向移动
依据图像中正、逆反应速率相
若v >v ,则平衡向正反应方向移动;反之向逆反应方向移动
正 逆
对大小判断
依据变化过程中速率变化的性 若平衡移动的过程中,正反应速率增大(减小),则平衡向逆(正)反应方向
质判断 移动
依据浓度商(Q)规则判断 若某温度下QK,反应向逆反应方向进行
命题热点2 速率、转化率及平衡常数的计算
1.速率、转化率及平衡常数的计算方法——三段式法
mA(g)+nB(g) pC(g)+qD(g)
起始量/(mol/L) a b 0 0
变化量/(mol/L) mx nx px qx
平衡量/(mol/L) a-mx b-nx px qx
某反应物转化的量 mx
(1)平衡转化率= ×100%,如α(A) = ×100%。
某反应物起始的量 平 a
(px)p·(qx)q
(2)平衡常数:K= 。
(a-mx)m·(b-nx)n
a-mx
(3)百分含量: (A)= ×100%。
(a-mx)+(b-nx)+px+qx
p (a-mx)+(b-nx)+px+qx
平
(4)平衡前后的压强之比(物质的量之比): = 。
p a+b
始
a·M(A)+b·M(B)
(5)平均摩尔质量:M= g/mol。
(a-mx)+(b-nx)+px+qx
某气体组分的物质的量
(6)某气体组分的体积分数= ×100%。
混合气体总的物质的量
实际产量
(7)生成物的产率:产率= ×100%。
理论产量
2.分压常数(K )与速率常数(k 、k )
p 正 逆
(1)K 的两种计算模板。
p
①平衡总压为p。
0
N(g) + 3H(g) 2NH (g)
2 2 3
n(平) a b c
a b c
p(分压) p p p
a+b+c 0 a+b+c 0 a+b+c 0c
( p ) 2
a+b+c 0
K= 。
p a b
( p )·( p ) 3
a+b+c 0 a+b+c 0
②刚性容器起始压强为p,平衡转化率为α。
0
2NO (g) NO(g)
2 2 4
p(始) p 0
0
1
Δp pα pα
0 2 0
1
p(平) p-pα pα
0 0 2 0
1
p α
K= 2 0 。
p
(p -p α)2
0 0
(2)K 与k 、k 的关系。
p 正 逆
以2NO (g) NO(g)为例:
2 2 4
v =k ·p2(NO ) ] k p(N O )
正 正 2 k ·p2(NO )=k ·p(N O) 正 = 2 4 =K 。
v =k ·p(N O ) 正 2 逆 2 4 k p2(NO ) p
逆 逆 2 4 逆 2
3.平衡常数与速率常数之间的关系
对 于 基 元 反 应 aA(g)+bB(g) cC(g)+dD(g),v =k ·ca(A)·cb(B),v =k ·cc(C)·cd(D), 平 衡 常 数 K=
正 正 逆 逆
cc(C)·cd(D) k ·v k
正 逆 正
= ,反应达到平衡时v =v ,故K= 。
ca(A)·cb(B) k ·v 正 逆 k
逆 正 逆
命题热点3 速率、平衡图像题的综合分析
1.新高考试题中速率、平衡图像题的特点
(1)图像的形式。
①直接呈现平衡体系中变量的变化:物质的量浓度-时间、组分百分含量-温度、压强-温度。
②平衡体系变量延伸出的变量的变化:分压(物质的量)-时间、转化率-原料物质的量分数、平衡常数K(ln K)-
1
温度倒数( )的图像。
T
(2)考查方式。
①分析出纵、横坐标之间的关系,判断出适宜的反应条件(温度、压强、浓度、反应物的配比等)。
②需要根据分析出的数据信息进行转化、计算得出结果。
2.化学反应速率、平衡图像的分析方法
(1)整体扫描图像,明确面、线、点的物理、化学意义。
①看面:弄清纵、横坐标的物理含义,注意把坐标的变化转变为化学量的变化。
②看线:弄清线的斜率、变化趋势及线的陡与平所代表的化学意义。
③看点:弄清曲线上点的含义,特别是一些特殊点,如与坐标轴的交点、曲线的交点、拐点、最高点与最低点
等。④作线:多条件变化时,是否需要确定一个条件为衡量的线,如等温线、等压线。
(2)找准切入口,明确图像的意义。
①从“断点”着手。
当可逆反应达到一种平衡后,若某一时刻外界条件发生改变,可能使速率-时间图像的曲线出现不连续的情况,
即出现“断点”。根据“断点”前后的速率大小,即可确定变化的是何种条件。
②从“拐点”入手。
同一可逆反应,若反应条件不同,达到平衡所用的时间也可能不同,反映到图像出现“拐点”的时间也就有差
异。根据外界条件对化学反应速率的影响,即可判断出温度的高低、压强或浓度的大小及是否使用催化剂。
③从曲线的变化趋势着手。
a.对于速率-温度(或压强)图像,由于随着温度逐渐升高或压强逐渐增大,反应速率会逐渐增大,因此图像上出现
的是平滑的递增曲线。
b.温度或压强的改变对正、逆反应速率的影响是一致的,在图像上,就是v(正)、v(逆)两条曲线的走势大致相
同。
c.分析外界条件对化学反应速率的影响时,只能分析达到平衡之后化学反应速率的变化情况。
考点一 气相中的化学平衡
1.(2024届广东省大湾区一模)某课题组研究CO 加氢制甲醇。涉及的主要反应有:
2
反应I:
反应Ⅱ:
反应Ⅲ:
反应Ⅳ:
回答下列有关问题:
(1)反应Ⅳ的 。
(2)下列有关说法正确的是___________。
A.增压时, 的物质的量分数一定增大
B.当甲醇的分压不再改变时,体系达到平衡
C.在恒容密闭容器中充入 ,反应Ⅲ速率不变
D.升温时,反应Ⅱ逆反应速率加快的程度大于正反应速率
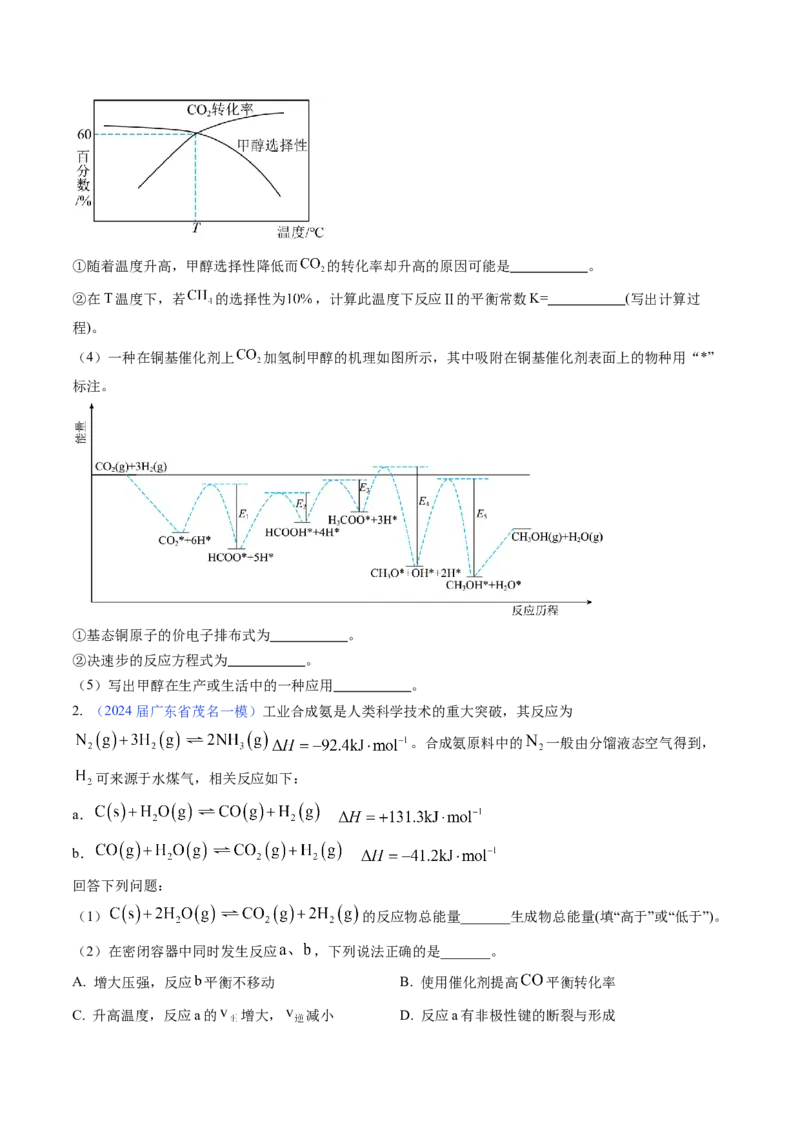
(3)研究发现:在 条件下,当起始 ,平衡时, 的转化率、含碳产物的选
择性(转化的 中生成 、 或 的百分比,如甲醇的选择性 )与温度
关系如图所示,回答下列问题。①随着温度升高,甲醇选择性降低而 的转化率却升高的原因可能是 。
②在T温度下,若 的选择性为 ,计算此温度下反应Ⅱ的平衡常数K= (写出计算过
程)。
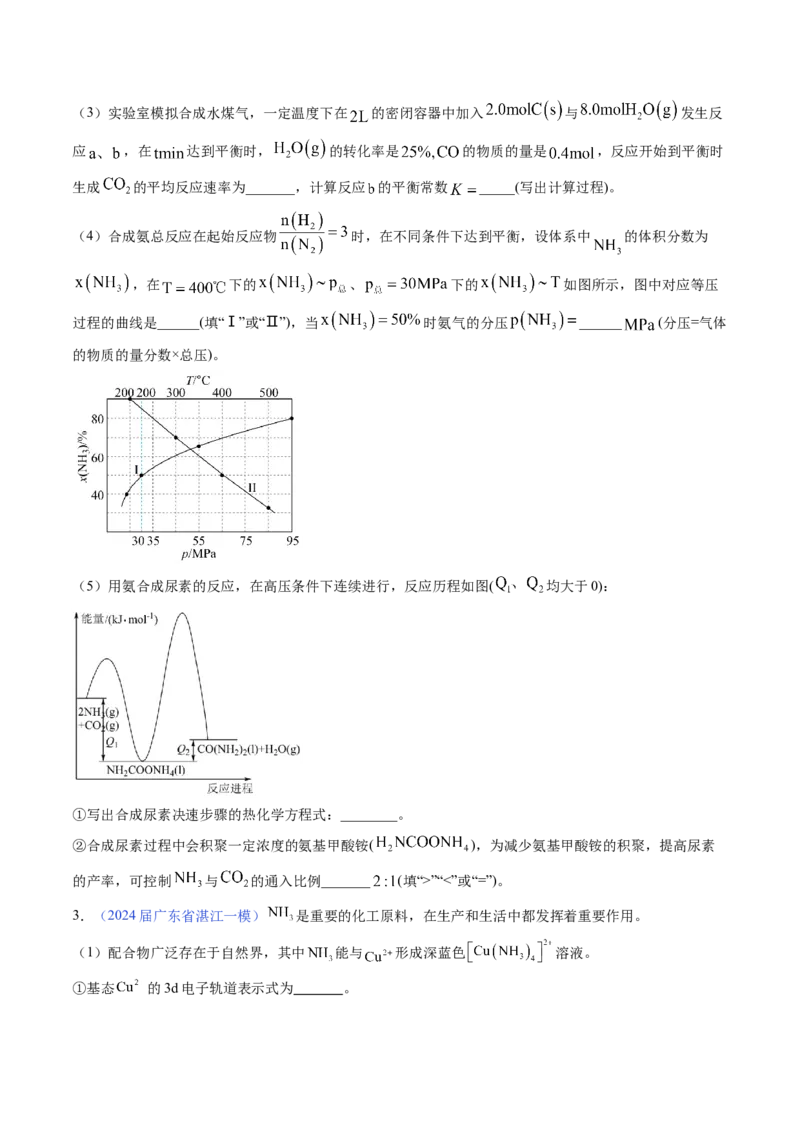
(4)一种在铜基催化剂上 加氢制甲醇的机理如图所示,其中吸附在铜基催化剂表面上的物种用“*”
标注。
①基态铜原子的价电子排布式为 。
②决速步的反应方程式为 。
(5)写出甲醇在生产或生活中的一种应用 。
2. (2024届广东省茂名一模)工业合成氨是人类科学技术的重大突破,其反应为
。合成氨原料中的 一般由分馏液态空气得到,
可来源于水煤气,相关反应如下:
a.
b.
回答下列问题:
(1) 的反应物总能量_______生成物总能量(填“高于”或“低于”)。
(2)在密闭容器中同时发生反应 ,下列说法正确的是_______。
A. 增大压强,反应 平衡不移动 B. 使用催化剂提高 平衡转化率
C. 升高温度,反应a的 增大, 减小 D. 反应a有非极性键的断裂与形成(3)实验室模拟合成水煤气,一定温度下在 的密闭容器中加入 与 发生反
应 ,在 达到平衡时, 的转化率是 的物质的量是 ,反应开始到平衡时
生成 的平均反应速率为_______,计算反应 的平衡常数 _____(写出计算过程)。
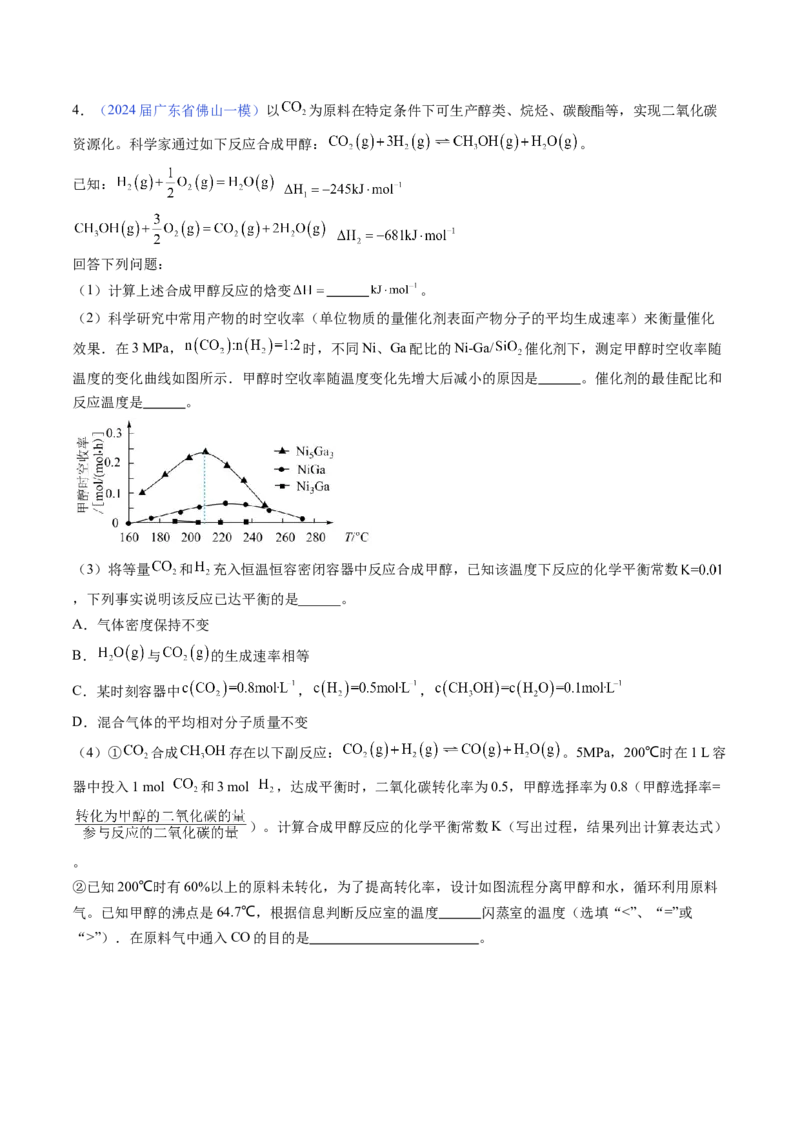
(4)合成氨总反应在起始反应物 时,在不同条件下达到平衡,设体系中 的体积分数为
,在 下的 、 下的 如图所示,图中对应等压
过程的曲线是______(填“Ⅰ”或“Ⅱ”),当 时氨气的分压 ______ (分压=气体
的物质的量分数×总压)。
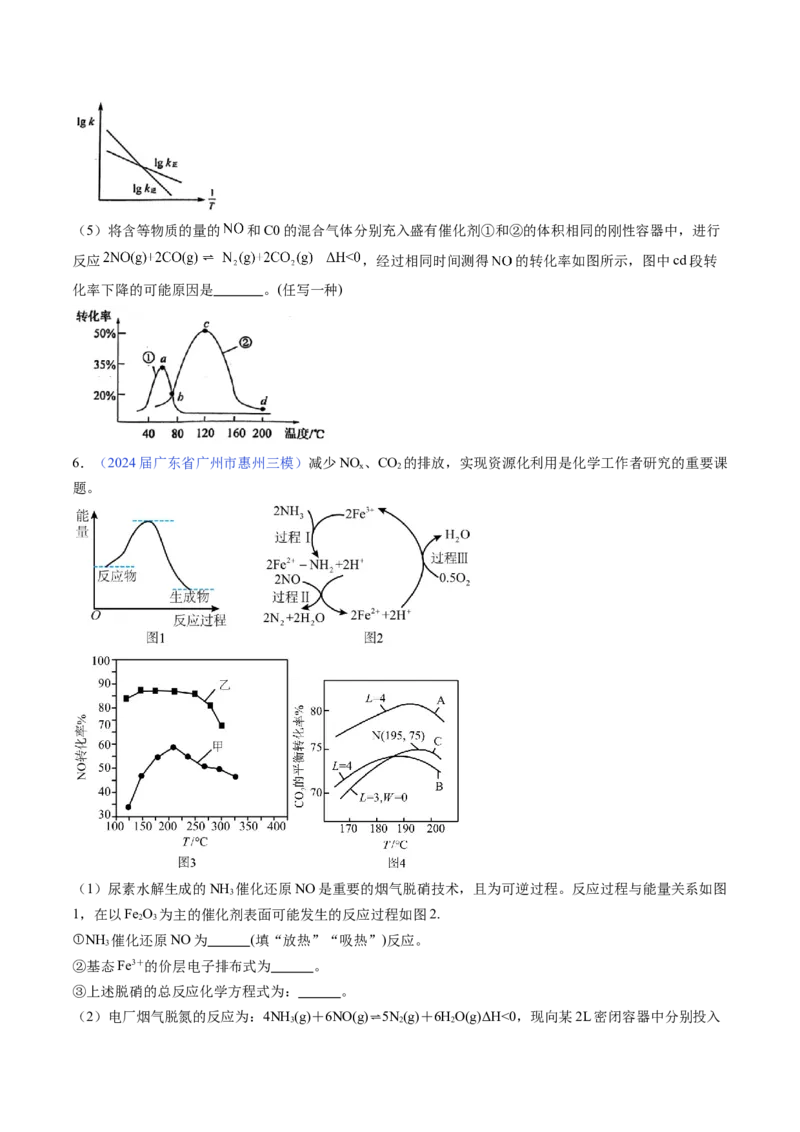
(5)用氨合成尿素的反应,在高压条件下连续进行,反应历程如图( 均大于0):
①写出合成尿素决速步骤的热化学方程式:________。
②合成尿素过程中会积聚一定浓度的氨基甲酸铵( ),为减少氨基甲酸铵的积聚,提高尿素
的产率,可控制 与 的通入比例_______ (填“>”“<”或“=”)。
3.(2024届广东省湛江一模) 是重要的化工原料,在生产和生活中都发挥着重要作用。
(1)配合物广泛存在于自然界,其中 能与 形成深蓝色 溶液。
①基态 的3d电子轨道表示式为 。② 的配位原子是 ,氨气中H—N—H的键角小于配合物中H—N—H的键角,其原因
是 。
(2)氨是制取硝酸的重要原料。氨的催化氧化过程主要有以下两个反应:
Ⅰ.
Ⅱ.
①反应 。
②不同温度下氨催化氧化的平衡常数如下( );
温度(℃) 300 500 700 900 1100
反应Ⅰ( ) 6.3×1041 1.1×1026 2.1×1019 3.8×1015 3.4×1011
反应Ⅱ( ) 7.3×1056 7.1×1034 2.6×1025 1.5×1020 6.7×1016
下列说法正确的是 。
A.如果对反应不加控制,氨和氧气反应的最终产物主要是
B.为使反应有利于向生成更多的NO方向进行,不必关注热力学问题(平衡移动问题),需要关注动力学问
题(反应速率问题)
C.在实际生产中,需采用高压氧化,以利于提高NO的产率
D.反应中需控制氨氧比、选择性催化剂的形状、气固相接触时间等
(3)已知可通过下列方法合成尿素:
第一步:
第二步:在体积为5 L的密闭容器中加入1 mol 和4 mol ,在一定条件下反应进行到10 min时,
测得 和尿素的物质的量均为0.25 mol,15 min后,测得 的物质的量为0.1 mol,如图所示。
①若用单位时间内物质的量的变化来表示固体或纯液体的反应速率,则 10 min内第一步反应中生成
(氨基甲酸铵)的平均反应速率为 。
②反应进行15分钟后,随着时间的变化,尿素和氨基甲酸铵的物质的量变化比较明显,但氨气和二氧化碳
的物质的量基本不变,其主要原因是 ,第一步反应的平衡常数 (列出算式即可)。4.(2024届广东省佛山一模)以 为原料在特定条件下可生产醇类、烷烃、碳酸酯等,实现二氧化碳
资源化。科学家通过如下反应合成甲醇: 。
已知:
回答下列问题:
(1)计算上述合成甲醇反应的焓变 。
(2)科学研究中常用产物的时空收率(单位物质的量催化剂表面产物分子的平均生成速率)来衡量催化
效果.在3 MPa, 时,不同Ni、Ga配比的Ni-Ga/ 催化剂下,测定甲醇时空收率随
温度的变化曲线如图所示.甲醇时空收率随温度变化先增大后减小的原因是 。催化剂的最佳配比和
反应温度是 。
(3)将等量 和 充入恒温恒容密闭容器中反应合成甲醇,已知该温度下反应的化学平衡常数
,下列事实说明该反应已达平衡的是______。
A.气体密度保持不变
B. 与 的生成速率相等
C.某时刻容器中 , ,
D.混合气体的平均相对分子质量不变
(4)① 合成 存在以下副反应: 。5MPa,200℃时在1 L容
器中投入1 mol 和3 mol ,达成平衡时,二氧化碳转化率为0.5,甲醇选择率为0.8(甲醇选择率=
)。计算合成甲醇反应的化学平衡常数K(写出过程,结果列出计算表达式)
。
②已知200℃时有60%以上的原料未转化,为了提高转化率,设计如图流程分离甲醇和水,循环利用原料
气。已知甲醇的沸点是64.7℃,根据信息判断反应室的温度 闪蒸室的温度(选填“<”、“=”或
“>”).在原料气中通入CO的目的是 。5.(2024届广东省广州市天河区二模)研究氮氧化物分解的反应机理,对于控制汽车尾气排放、保护环
境有重要意义。
I.直接催化分解法是消除 的主要方法,已知部分 催化分解过程如下:
①
②
③
④
(1)反应 的 。
(2)T℃,在密闭容器中尝试利用表面催化工艺分解 ,用 分别表示 、
、 和固体催化剂,则在固体催化剂表面分解 的反应过程可用下图表示。
已知: 在固体催化剂表面吸附过程自发发生,且总熵减小。画出从状态A到状态D体系能量的变化曲
线图 。
(3)T℃和恒定压强 时,在密闭容器中模拟废气中的 催化分解过程,各组分的信息如下表:
物质
N(投料)/ 19 34 6.5 25 0 0
n(平衡)/ 50 1 20 25 x y
①x= ,y= ,该温度下反应②的压强平衡常数 (分压=总压×物质的量分数)。
②若先除去废气中的 ,再在相同条件下模拟实验,发现 的平衡转化率明显降低,其原因是
。
Ⅱ.用含碳物质消除氮氧化物也是防治污染的有效方法。
(4)活性炭还原法消除氮氧化物污染的反应原理为: 。已知该反
应正、逆反应速率方程分别为 、 ,其中 、 分别为正、逆反
应速率常数,其变化曲线如下图所示,则该反应的反应热 0(填“>”或“<”)。(5)将含等物质的量的 和C0的混合气体分别充入盛有催化剂①和②的体积相同的刚性容器中,进行
反应 ,经过相同时间测得 的转化率如图所示,图中cd段转
化率下降的可能原因是 。(任写一种)
6.(2024届广东省广州市惠州三模)减少NO 、CO 的排放,实现资源化利用是化学工作者研究的重要课
x 2
题。
(1)尿素水解生成的NH 催化还原NO是重要的烟气脱硝技术,且为可逆过程。反应过程与能量关系如图
3
1,在以Fe O 为主的催化剂表面可能发生的反应过程如图2.
2 3
①NH 催化还原NO为 (填“放热”“吸热”)反应。
3
②基态Fe3+的价层电子排布式为 。
③上述脱硝的总反应化学方程式为: 。
(2)电厂烟气脱氮的反应为:4NH
3
(g)+6NO(g)⇌5N
2
(g)+6H
2
O(g)ΔH<0,现向某2L密闭容器中分别投入一定量的NH 和2.0×10-4molNO发生以上反应。其他条件相同时,在甲、乙两种催化剂的作用下,反应
3
1min时NO的转化率与温度的关系如图3.
①在催化剂甲的作用下,温度高于210℃小于300℃时,NO转化率降低的可能原因是 。
②100—300℃区间,0~1min内,使用甲催化剂时NO的最高平均速率为 。
(3)工业以NH 和CO 为原料合成尿素。液相中,合成尿素的热化学方程式为:2NH (l)+CO(l)
3 2 3 2
HO(l)+NH CONH (l) ΔH<0,在液相中,CO 的平衡转化率与温度、初始氨碳比(用L表示,L=
2 2 2 2
)、初始水碳比(用W表示,W= )关系如图4.
①曲线A、B中, (填“A”或“B”)的W较小。
②对于液相反应,常用某组分M达到平衡时的物质的量分数x(M)代替平衡浓度来计算平衡常数(记作K)。
x
195℃时,2NH (l)+CO(l) HO(l)+NH CONH (l)的K 的值为 。
3 2 2 2 2 x
7.(2024届广东省江门一模)二氧化碳加氢是对温室气体的有效转化,也是合成再生能源与化工原料的
重要途径。
(1)已知在25℃和101kPa时, 和 的燃烧热分别为 和 。由 加氢反
应制备 的反应为: ,该反应的反应热 。
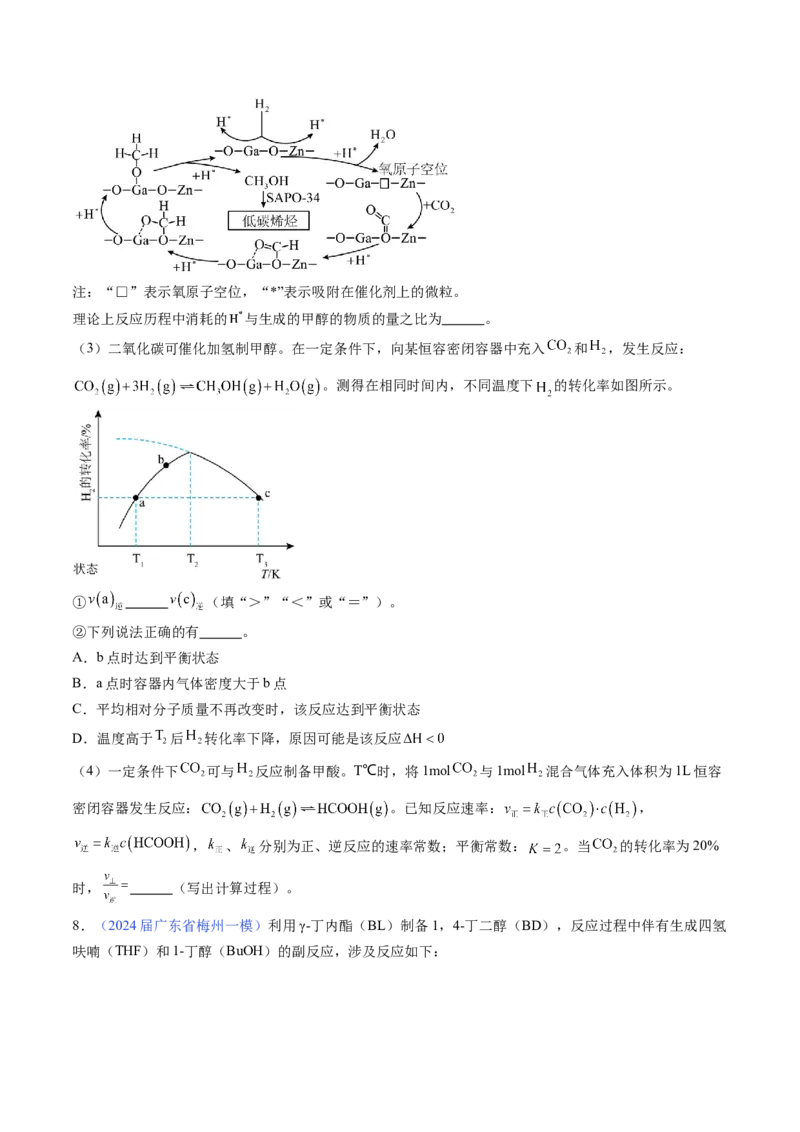
(2)① 催化加氢可以制低碳烯烃: ,该反应在恒压条件下,
反应温度、投料比 对 平衡转化率的影响如图所示,该反应为 反应(填“吸热”或
“放热”), 、 、 的相对大小为 。
② 催化加氢制低碳烯烃,反应历程如下图所示, 首先在 表面解离成2个 ,随
后参与到 的转化过程。注:“□”表示氧原子空位,“*”表示吸附在催化剂上的微粒。
理论上反应历程中消耗的 与生成的甲醇的物质的量之比为 。
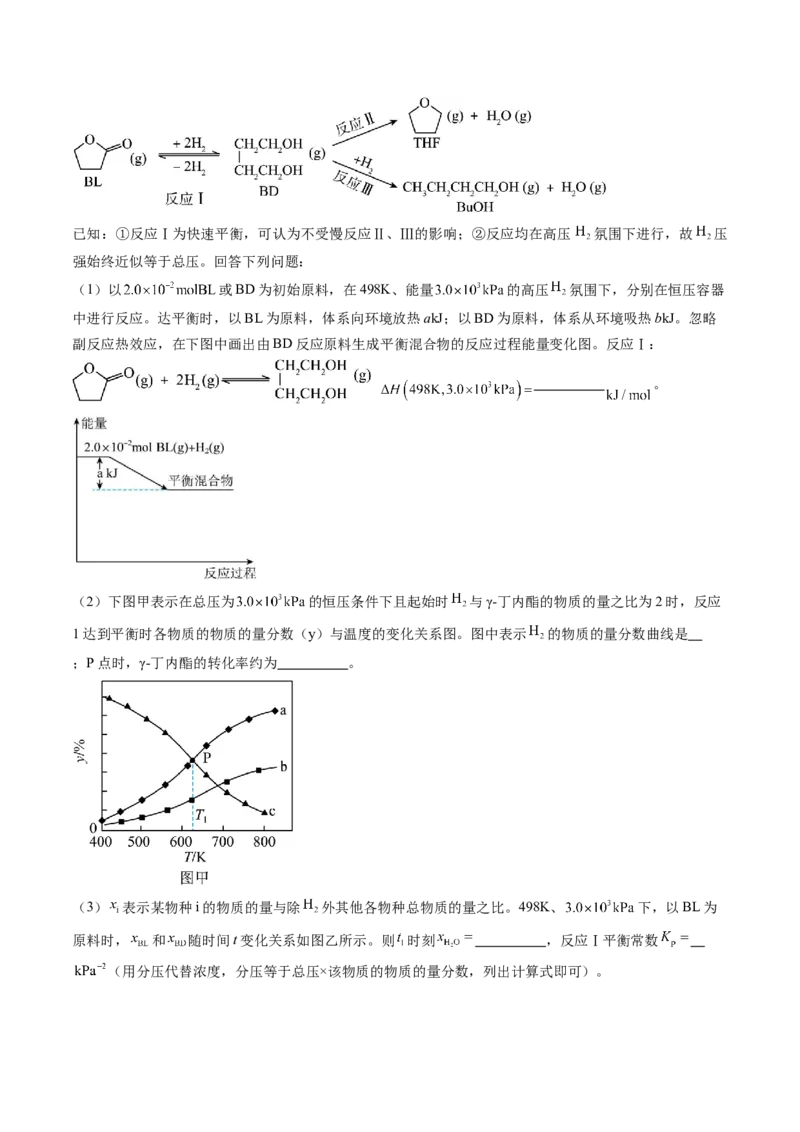
(3)二氧化碳可催化加氢制甲醇。在一定条件下,向某恒容密闭容器中充入 和 ,发生反应:
。测得在相同时间内,不同温度下 的转化率如图所示。
① (填“>”“<”或“=”)。
②下列说法正确的有 。
A.b点时达到平衡状态
B.a点时容器内气体密度大于b点
C.平均相对分子质量不再改变时,该反应达到平衡状态
D.温度高于 后 转化率下降,原因可能是该反应
(4)一定条件下 可与 反应制备甲酸。T℃时,将1mol 与1mol 混合气体充入体积为1L恒容
密闭容器发生反应: 。已知反应速率: ,
, 、 分别为正、逆反应的速率常数;平衡常数: 。当 的转化率为20%
时, (写出计算过程)。
8.(2024届广东省梅州一模)利用γ-丁内酯(BL)制备1,4-丁二醇(BD),反应过程中伴有生成四氢
呋喃(THF)和1-丁醇(BuOH)的副反应,涉及反应如下:已知:①反应Ⅰ为快速平衡,可认为不受慢反应Ⅱ、Ⅲ的影响;②反应均在高压 氛围下进行,故 压
强始终近似等于总压。回答下列问题:
(1)以 或BD为初始原料,在498K、能量 的高压 氛围下,分别在恒压容器
中进行反应。达平衡时,以BL为原料,体系向环境放热akJ;以BD为原料,体系从环境吸热bkJ。忽略
副反应热效应,在下图中画出由BD反应原料生成平衡混合物的反应过程能量变化图。反应Ⅰ:
。
(2)下图甲表示在总压为 的恒压条件下且起始时 与γ-丁内酯的物质的量之比为2时,反应
1达到平衡时各物质的物质的量分数(y)与温度的变化关系图。图中表示 的物质的量分数曲线是
;P点时,γ-丁内酯的转化率约为 。
(3) 表示某物种i的物质的量与除 外其他各物种总物质的量之比。498K、 下,以BL为
原料时, 和 随时间t变化关系如图乙所示。则 时刻 ,反应Ⅰ平衡常数
(用分压代替浓度,分压等于总压×该物质的物质的量分数,列出计算式即可)。(4)利用电解合成法也能在有机质子溶剂中实现BL→BD的转化,该转化发生在 极,电极反
应式为 。
9.(2024届广东省韶关一模)油气开采、石油化工、煤化工等行业废气普遍含有硫化氢,需要回收处理
并加以利用。回答下列问题:
(1)已知下列反应的热化学方程式;
①
②
③
则 kJ/mol,反应③能够自发的条件是 。
(2)下列叙述能说明反应③达到平衡状态的是 (填字母序号)。
A.2v (H S)=v (CS) B.恒温恒容条件下,体系压强不再变化
正 2 逆 2
C.气体的总质量不再变化 D.混合气体平均摩尔质量不再变化
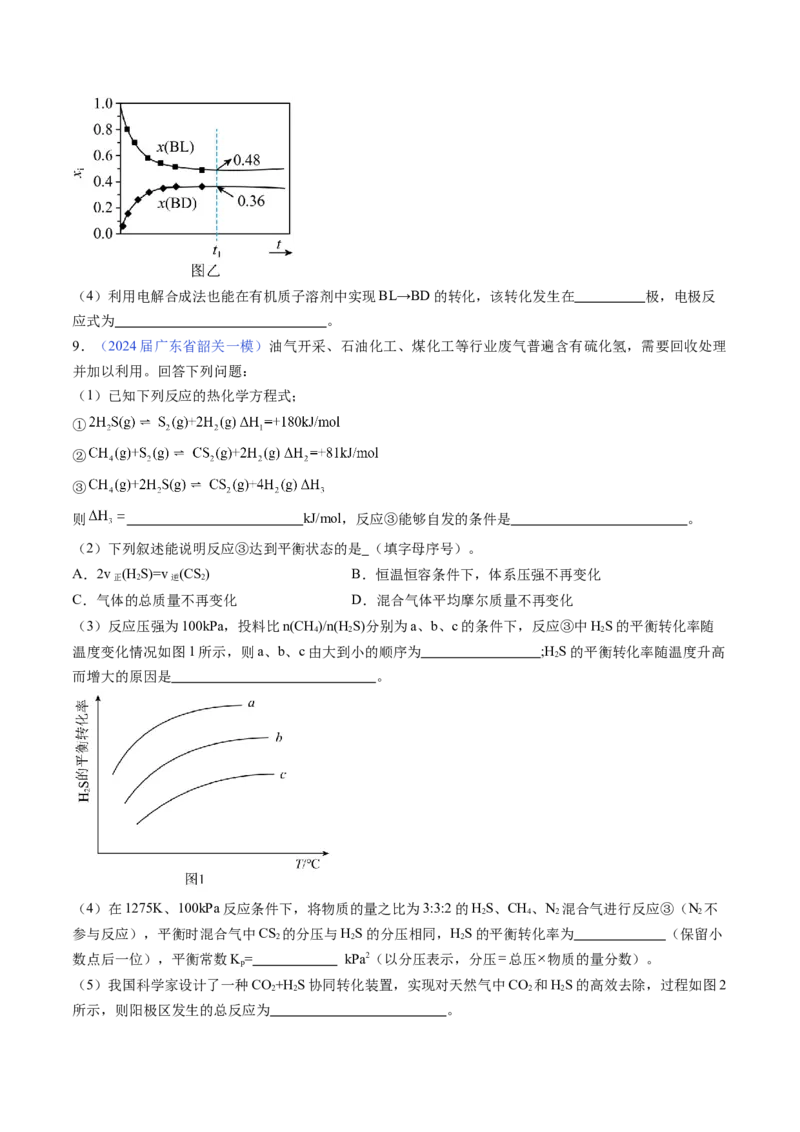
(3)反应压强为100kPa,投料比n(CH)/n(HS)分别为a、b、c的条件下,反应③中HS的平衡转化率随
4 2 2
温度变化情况如图1所示,则a、b、c由大到小的顺序为 ;H S的平衡转化率随温度升高
2
而增大的原因是 。
(4)在1275K、100kPa反应条件下,将物质的量之比为3:3:2的HS、CH、N 混合气进行反应③(N 不
2 4 2 2
参与反应),平衡时混合气中CS 的分压与HS的分压相同,HS的平衡转化率为 (保留小
2 2 2
数点后一位),平衡常数K= kPa2(以分压表示,分压 总压 物质的量分数)。
p
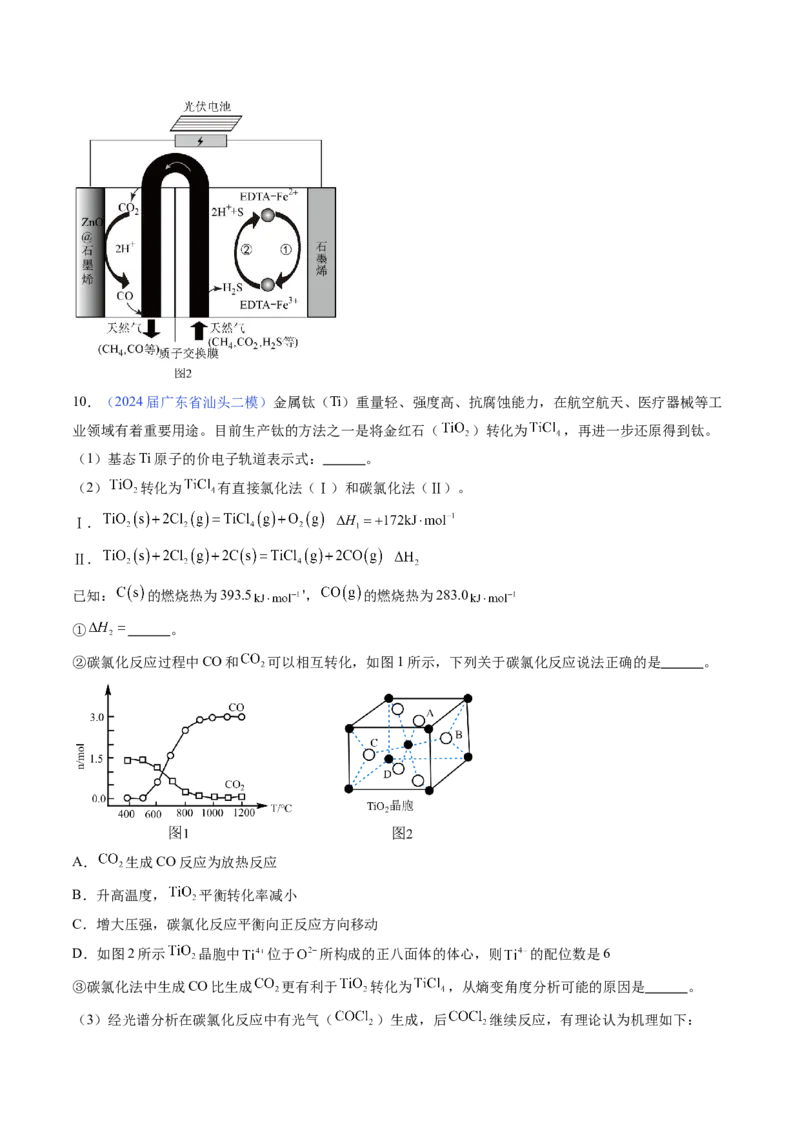
(5)我国科学家设计了一种CO+H S协同转化装置,实现对天然气中CO 和HS的高效去除,过程如图2
2 2 2 2
所示,则阳极区发生的总反应为 。10.(2024届广东省汕头二模)金属钛(Ti)重量轻、强度高、抗腐蚀能力,在航空航天、医疗器械等工
业领域有着重要用途。目前生产钛的方法之一是将金红石( )转化为 ,再进一步还原得到钛。
(1)基态Ti原子的价电子轨道表示式: 。
(2) 转化为 有直接氯化法(Ⅰ)和碳氯化法(Ⅱ)。
Ⅰ.
Ⅱ.
已知: 的燃烧热为393.5 ', 的燃烧热为283.0
① 。
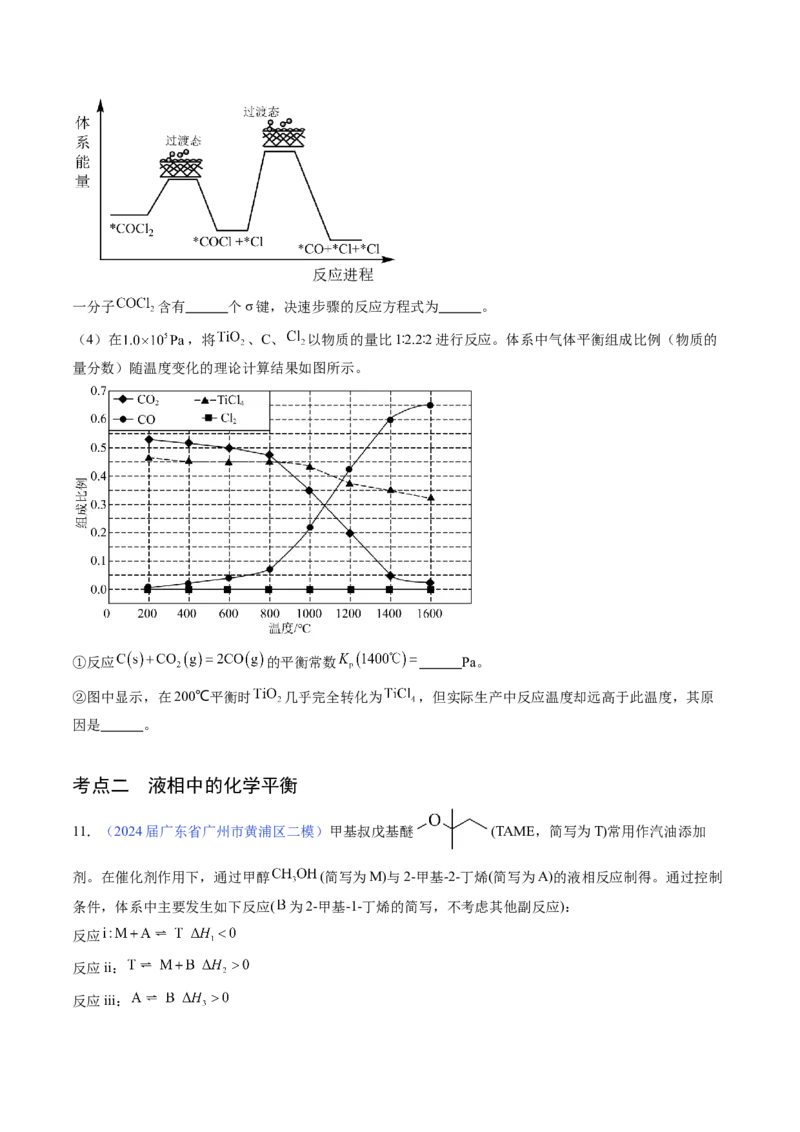
②碳氯化反应过程中CO和 可以相互转化,如图1所示,下列关于碳氯化反应说法正确的是 。
A. 生成CO反应为放热反应
B.升高温度, 平衡转化率减小
C.增大压强,碳氯化反应平衡向正反应方向移动
D.如图2所示 晶胞中 位于 所构成的正八面体的体心,则 的配位数是6
③碳氯化法中生成CO比生成 更有利于 转化为 ,从熵变角度分析可能的原因是 。
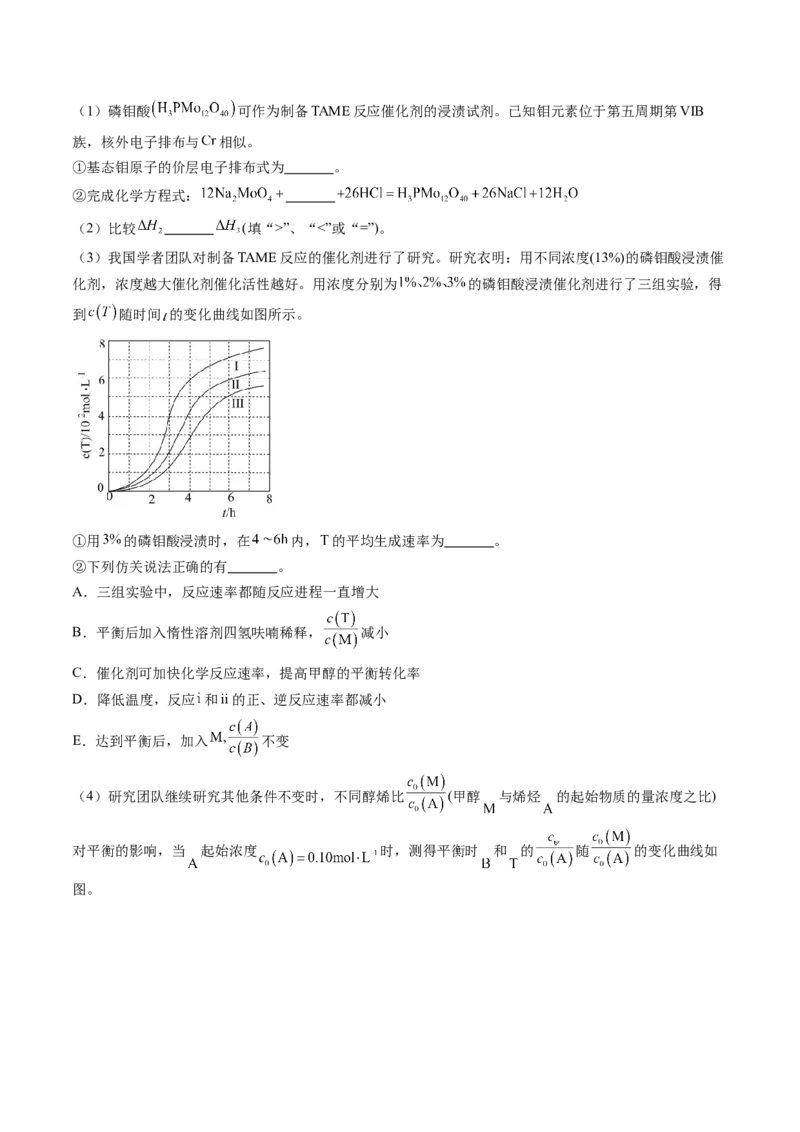
(3)经光谱分析在碳氯化反应中有光气( )生成,后 继续反应,有理论认为机理如下:一分子 含有 个σ键,决速步骤的反应方程式为 。
(4)在 ,将 、C、 以物质的量比1∶2.2∶2进行反应。体系中气体平衡组成比例(物质的
量分数)随温度变化的理论计算结果如图所示。
①反应 的平衡常数 Pa。
②图中显示,在200℃平衡时 几乎完全转化为 ,但实际生产中反应温度却远高于此温度,其原
因是 。
考点二 液相中的化学平衡
11.(2024届广东省广州市黄浦区二模)甲基叔戊基醚 (TAME,简写为T)常用作汽油添加
剂。在催化剂作用下,通过甲醇 (简写为M)与2-甲基-2-丁烯(简写为A)的液相反应制得。通过控制
条件,体系中主要发生如下反应( 为2-甲基-1-丁烯的简写,不考虑其他副反应):
反应
反应ii:
反应iii:(1)磷钼酸 可作为制备TAME反应催化剂的浸渍试剂。已知钼元素位于第五周期第VIB
族,核外电子排布与 相似。
①基态钼原子的价层电子排布式为 。
②完成化学方程式:
(2)比较 (填“>”、“<”或“=”)。
(3)我国学者团队对制备TAME反应的催化剂进行了研究。研究衣明:用不同浓度(13%)的磷钼酸浸渍催
化剂,浓度越大催化剂催化活性越好。用浓度分别为 的磷钼酸浸渍催化剂进行了三组实验,得
到 随时间 的变化曲线如图所示。
①用 的磷钼酸浸渍时,在 内, 的平均生成速率为 。
②下列仿关说法正确的有 。
A.三组实验中,反应速率都随反应进程一直增大
B.平衡后加入惰性溶剂四氢呋喃稀释, 减小
C.催化剂可加快化学反应速率,提高甲醇的平衡转化率
D.降低温度,反应 和ii的正、逆反应速率都减小
E.达到平衡后,加入 不变
(4)研究团队继续研究其他条件不变时,不同醇烯比 (甲醇 与烯烃 的起始物质的量浓度之比)
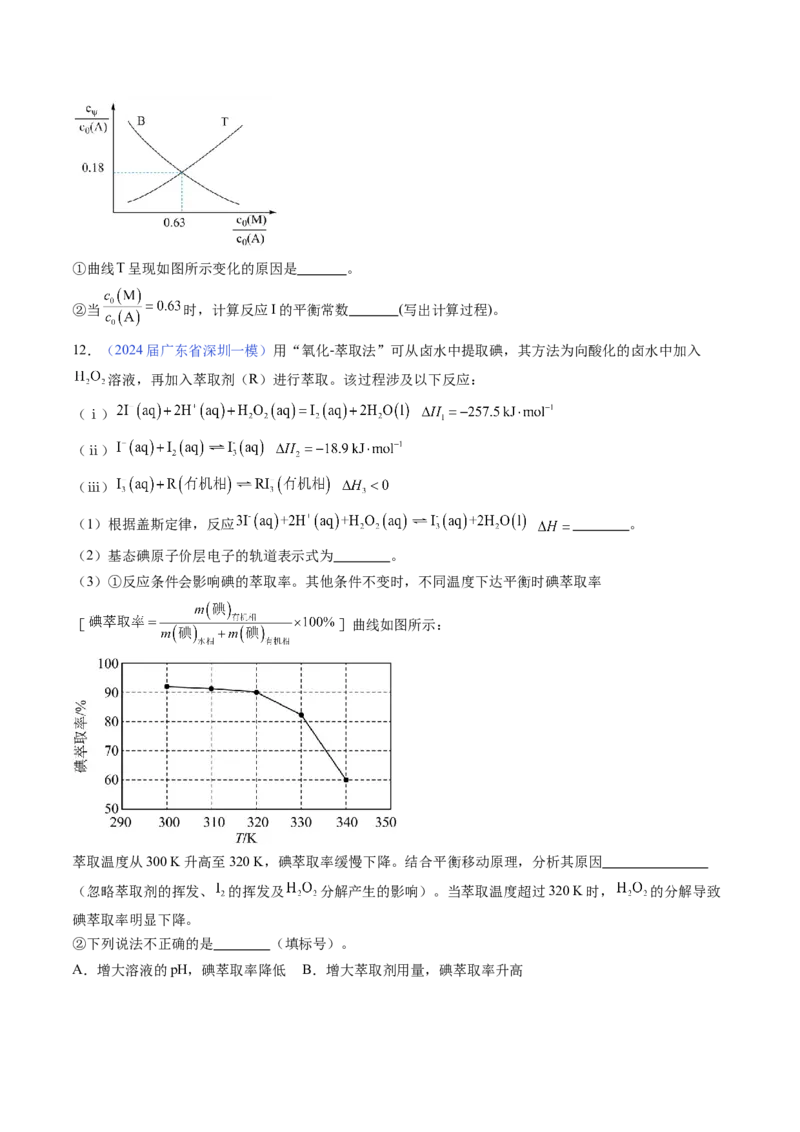
对平衡的影响,当 起始浓度 时,测得平衡时 和 的 随 的变化曲线如
图。①曲线 呈现如图所示变化的原因是 。
②当 时,计算反应I的平衡常数 (写出计算过程)。
12.(2024届广东省深圳一模)用“氧化-萃取法”可从卤水中提取碘,其方法为向酸化的卤水中加入
溶液,再加入萃取剂(R)进行萃取。该过程涉及以下反应:
(ⅰ)
(ⅱ)
(ⅲ)
(1)根据盖斯定律,反应 。
(2)基态碘原子价层电子的轨道表示式为 。
(3)①反应条件会影响碘的萃取率。其他条件不变时,不同温度下达平衡时碘萃取率
[ ]曲线如图所示:
萃取温度从300 K升高至320 K,碘萃取率缓慢下降。结合平衡移动原理,分析其原因
(忽略萃取剂的挥发、 的挥发及 分解产生的影响)。当萃取温度超过320 K时, 的分解导致
碘萃取率明显下降。
②下列说法不正确的是 (填标号)。
A.增大溶液的pH,碘萃取率降低 B.增大萃取剂用量,碘萃取率升高C.萃取体系平衡后加水稀释, 变小 D.增大 的浓度,反应(ⅰ)的速率增大
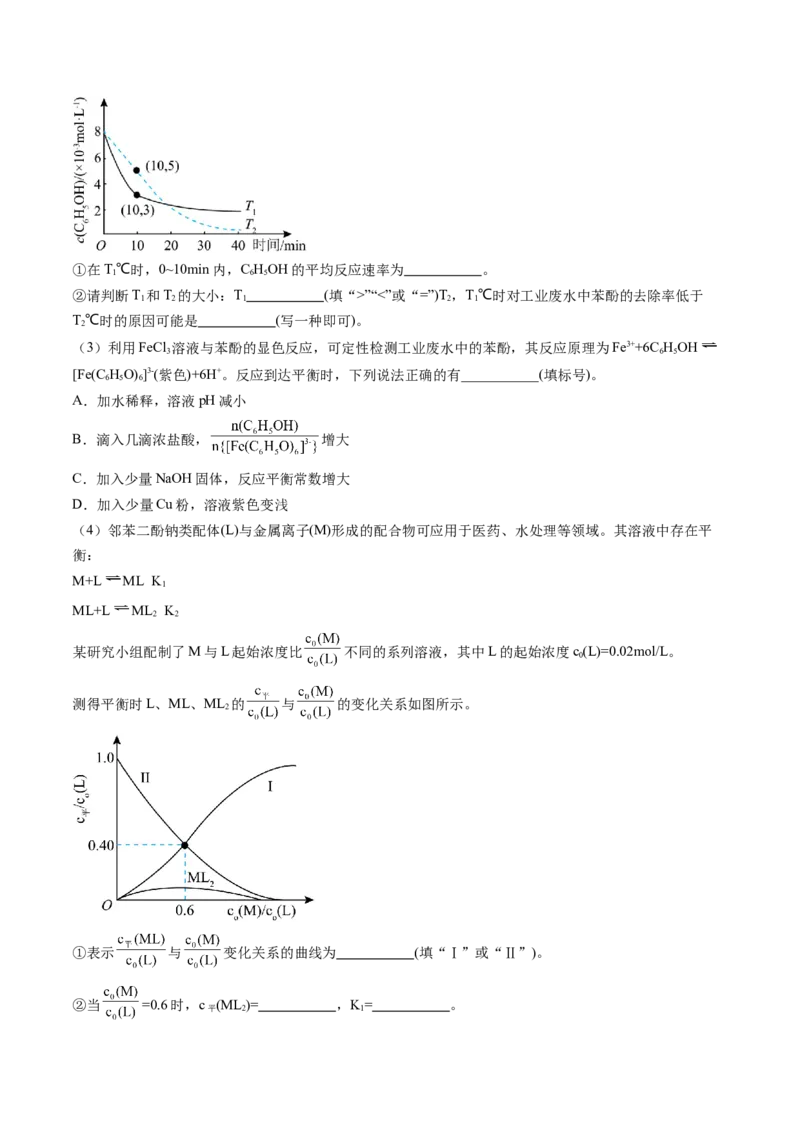
(4)未加萃取剂时,固定总碘浓度为 ,平衡时溶液中的 、 、 分布系数 与溶液中初始
关系如图所示。[总碘浓度 各组分折合为 后的浓度之和, ,
如 ]
①设平衡时 、 、 分别为 、 、 ,则 、 、 之间的关系式为
。
②计算反应 的平衡常数 (结果保留3位有效数字)。
(5)测定卤水中的 方法:取 卤水于锥形瓶中,加适量氧化剂恰好将 全部氧化为 ;加
溶液酸化后,再加入适量 溶液,密闭静置后,用 标准溶液滴定至溶液呈
微黄色,加入淀粉指示剂,继续滴定至终点;平行测定3次,平均消耗 ,则卤水中
。(已知: )
13.(2024届广东省肇庆二模)酚类化合物在医疗、环保、工业等方面有着广泛的用途。
(1)苯酚可用于外科器械消毒、皮肤杀菌与止痒,可通过磺化法制备。该工艺具体流程如下:
反应③的化学方程式为 。
(2)石油加工、造纸等企业易产生含有苯酚的工业废水,可通过O-H O 氧化法进行处理,其原理为
3 2 2
C HOH+H O+O →CO+H O(非可逆反应,反应未配平)。在T℃和T℃时,分别向含有苯酚的水样中加入
6 5 2 2 3 2 2 1 2
等量的30%H O 溶液,再以相同的流速向水样中通入O,测得水样中苯酚的含量随时间变化的曲线如图所
2 2 3
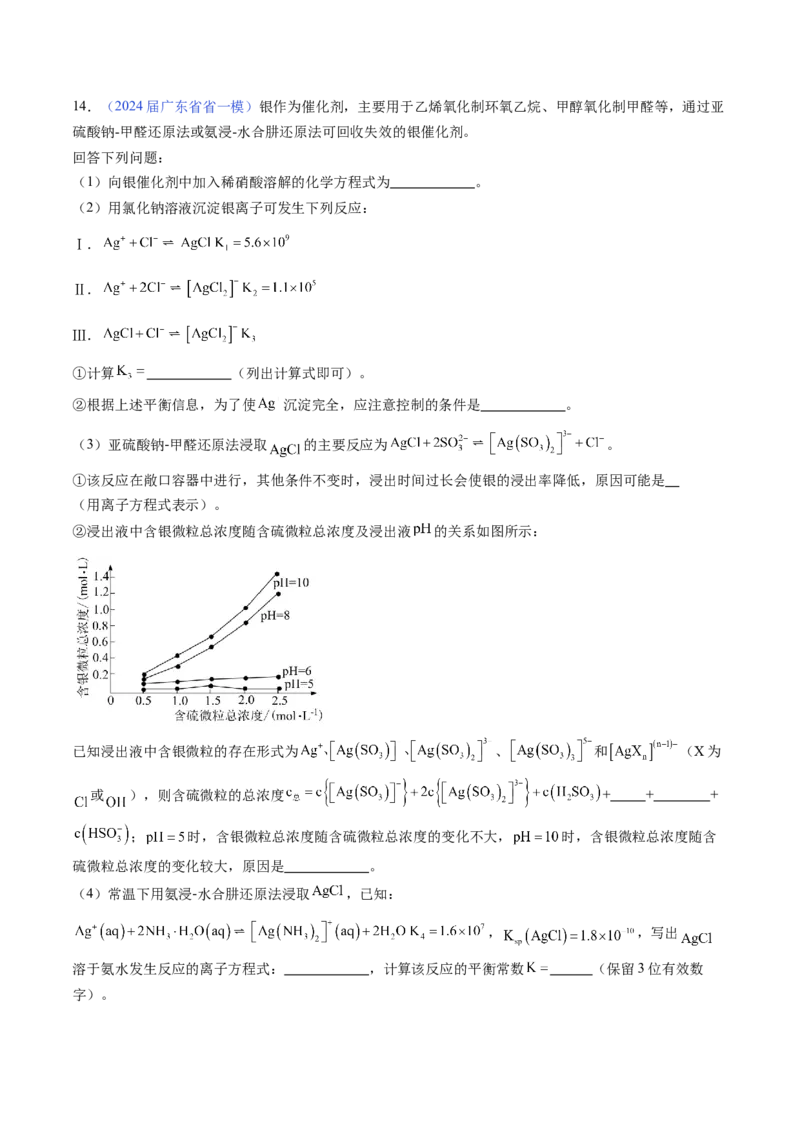
示。①在T℃时,0~10min内,C HOH的平均反应速率为 。
1 6 5
②请判断T 和T 的大小:T (填“>”“<”或“=”)T,T℃时对工业废水中苯酚的去除率低于
1 2 1 2 1
T℃时的原因可能是 (写一种即可)。
2
(3)利用FeCl 溶液与苯酚的显色反应,可定性检测工业废水中的苯酚,其反应原理为Fe3++6C HOH
3 6 5
[Fe(C HO) ]3-(紫色)+6H+。反应到达平衡时,下列说法正确的有___________(填标号)。
6 5 6
A.加水稀释,溶液pH减小
B.滴入几滴浓盐酸, 增大
C.加入少量NaOH固体,反应平衡常数增大
D.加入少量Cu粉,溶液紫色变浅
(4)邻苯二酚钠类配体(L)与金属离子(M)形成的配合物可应用于医药、水处理等领域。其溶液中存在平
衡:
M+L ML K
1
ML+L ML K
2 2
某研究小组配制了M与L起始浓度比 不同的系列溶液,其中L的起始浓度c(L)=0.02mol/L。
0
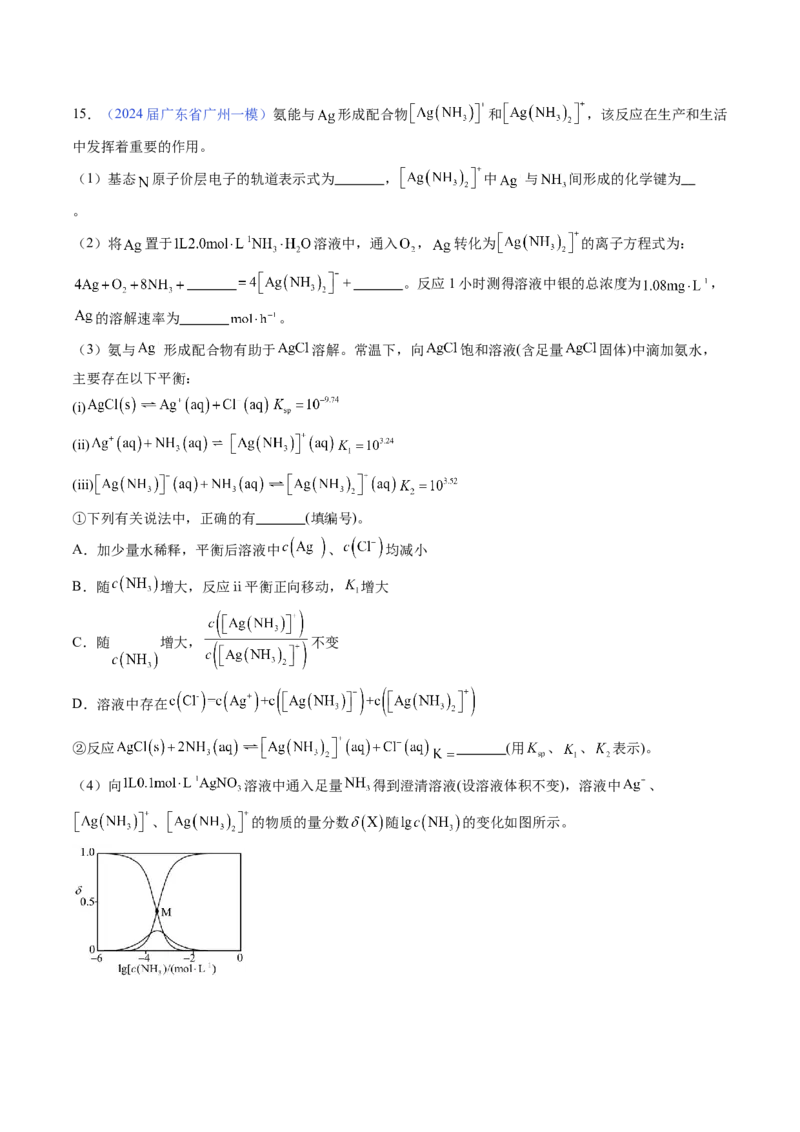
测得平衡时L、ML、ML 的 与 的变化关系如图所示。
2
①表示 与 变化关系的曲线为 (填“Ⅰ”或“Ⅱ”)。
②当 =0.6时,c (ML )= ,K= 。
平 2 114.(2024届广东省省一模)银作为催化剂,主要用于乙烯氧化制环氧乙烷、甲醇氧化制甲醛等,通过亚
硫酸钠-甲醛还原法或氨浸-水合肼还原法可回收失效的银催化剂。
回答下列问题:
(1)向银催化剂中加入稀硝酸溶解的化学方程式为 。
(2)用氯化钠溶液沉淀银离子可发生下列反应:
Ⅰ.
Ⅱ.
Ⅲ.
①计算 (列出计算式即可)。
②根据上述平衡信息,为了使 沉淀完全,应注意控制的条件是 。
(3)亚硫酸钠-甲醛还原法浸取 的主要反应为 。
①该反应在敞口容器中进行,其他条件不变时,浸出时间过长会使银的浸出率降低,原因可能是
(用离子方程式表示)。
②浸出液中含银微粒总浓度随含硫微粒总浓度及浸出液 的关系如图所示:
已知浸出液中含银微粒的存在形式为 、 和 (X为
或 ),则含硫微粒的总浓度 + + +
; 时,含银微粒总浓度随含硫微粒总浓度的变化不大, 时,含银微粒总浓度随含
硫微粒总浓度的变化较大,原因是 。
(4)常温下用氨浸-水合肼还原法浸取 ,已知:
, ,写出
溶于氨水发生反应的离子方程式: ,计算该反应的平衡常数 (保留3位有效数
字)。15.(2024届广东省广州一模)氨能与 形成配合物 和 ,该反应在生产和生活
中发挥着重要的作用。
(1)基态 原子价层电子的轨道表示式为 , 中 与 间形成的化学键为
。
(2)将 置于 溶液中,通入 , 转化为 的离子方程式为:
。反应1小时测得溶液中银的总浓度为 ,
的溶解速率为 。
(3)氨与 形成配合物有助于 溶解。常温下,向 饱和溶液(含足量 固体)中滴加氨水,
主要存在以下平衡:
(i)
(ii)
(iii)
①下列有关说法中,正确的有 (填编号)。
A.加少量水稀释,平衡后溶液中 、 均减小
B.随 增大,反应ⅱ平衡正向移动, 增大
C.随 增大, 不变
D.溶液中存在
②反应 (用 、 、 表示)。
(4)向 溶液中通入足量 得到澄清溶液(设溶液体积不变),溶液中 、
、 的物质的量分数 随 的变化如图所示。已知溶液中 , 。
① 点溶液中 。
②计算 点溶液中 的转化率 (写出计算过程,已知 )。
16.(2024届广东省江门联考)铜及其化合物在生产及生活中应用广泛。
(1)铜-铁催化剂可用于电催化还原 为 ,完成下列离子方程式: 。
+______+______
(2)铜-铁催化剂还可以催化 分解转化为燃料氢气,反应为 。往体
积为 的密闭容器中加入 分解制 。图中曲线a、b分别表示在分别表示在铜-铁催化剂I的作
用下, 时 及 时 随时间的变化;曲线 表示在铜-铁催化剂Ⅱ的作用下, 时
随时间的变化。
① (填“<”“>”或“=”)。
②在铜-铁催化剂I的作用下, 时, 内平均反应速率 。
③上述三种条件下,分解反应的平衡常数 的大小关系为
(3)工业合成氨中,常用亚铜盐的氨水溶液除去原料气中的 ,反应的离子方程式为
,该反应的 。
其他条件不变时,下列说法正确的有______(填字母)。
A. 与 的浓度相等时,反应达到平衡
B.平衡后增大 的浓度, 的转化率增大
C.平衡后加水稀释, 与 的浓度之比增大
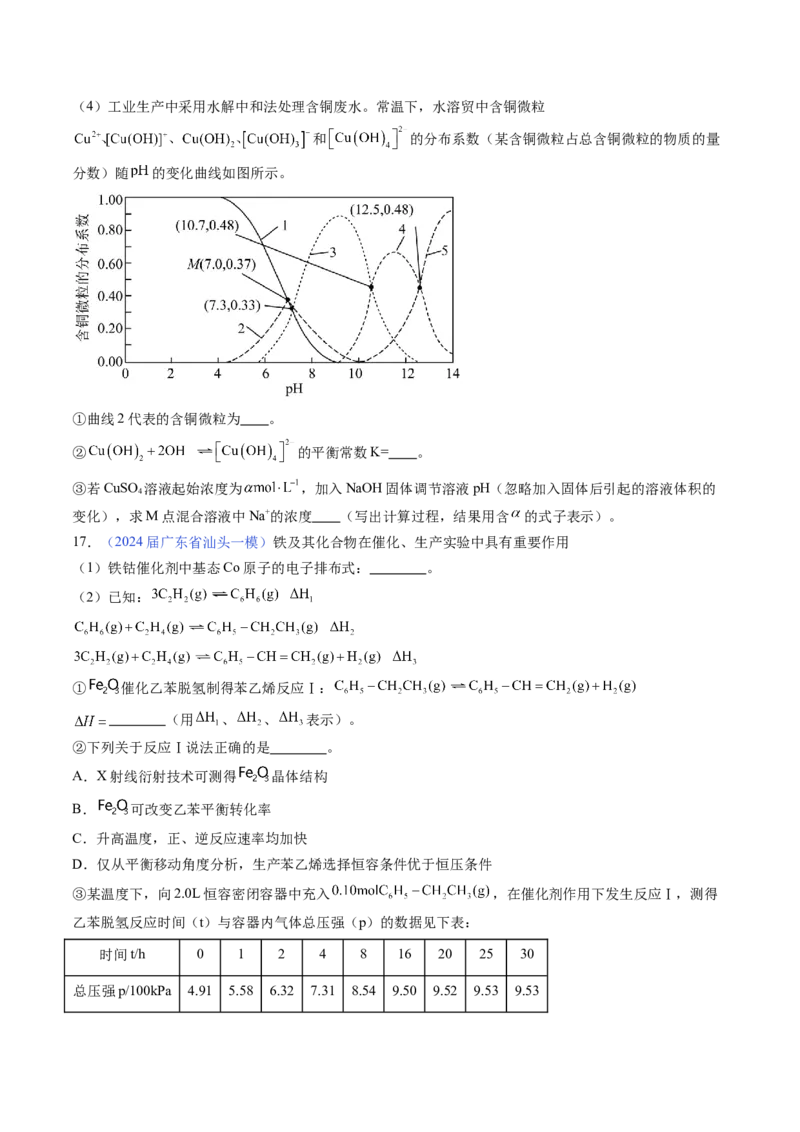
D.可采用加热 溶液的方法实现 的再生(4)工业生产中采用水解中和法处理含铜废水。常温下,水溶贸中含铜微粒
和 的分布系数(某含铜微粒占总含铜微粒的物质的量
分数)随 的变化曲线如图所示。
①曲线2代表的含铜微粒为 。
② 的平衡常数K= 。
③若CuSO 溶液起始浓度为 ,加入NaOH固体调节溶液pH(忽略加入固体后引起的溶液体积的
4
变化),求M点混合溶液中Na+的浓度 (写出计算过程,结果用含 的式子表示)。
17.(2024届广东省汕头一模)铁及其化合物在催化、生产实验中具有重要作用
(1)铁钴催化剂中基态Co原子的电子排布式: 。
(2)已知:
① 催化乙苯脱氢制得苯乙烯反应Ⅰ:
(用 、 、 表示)。
②下列关于反应Ⅰ说法正确的是 。
A.X射线衍射技术可测得 晶体结构
B. 可改变乙苯平衡转化率
C.升高温度,正、逆反应速率均加快
D.仅从平衡移动角度分析,生产苯乙烯选择恒容条件优于恒压条件
③某温度下,向2.0L恒容密闭容器中充入 ,在催化剂作用下发生反应Ⅰ,测得
乙苯脱氢反应时间(t)与容器内气体总压强(p)的数据见下表:
时间t/h 0 1 2 4 8 16 20 25 30
总压强p/100kPa 4.91 5.58 6.32 7.31 8.54 9.50 9.52 9.53 9.53用单位时间内气体分压的变化来表示反应速率,即 ,则前4h内平均反应速率
。
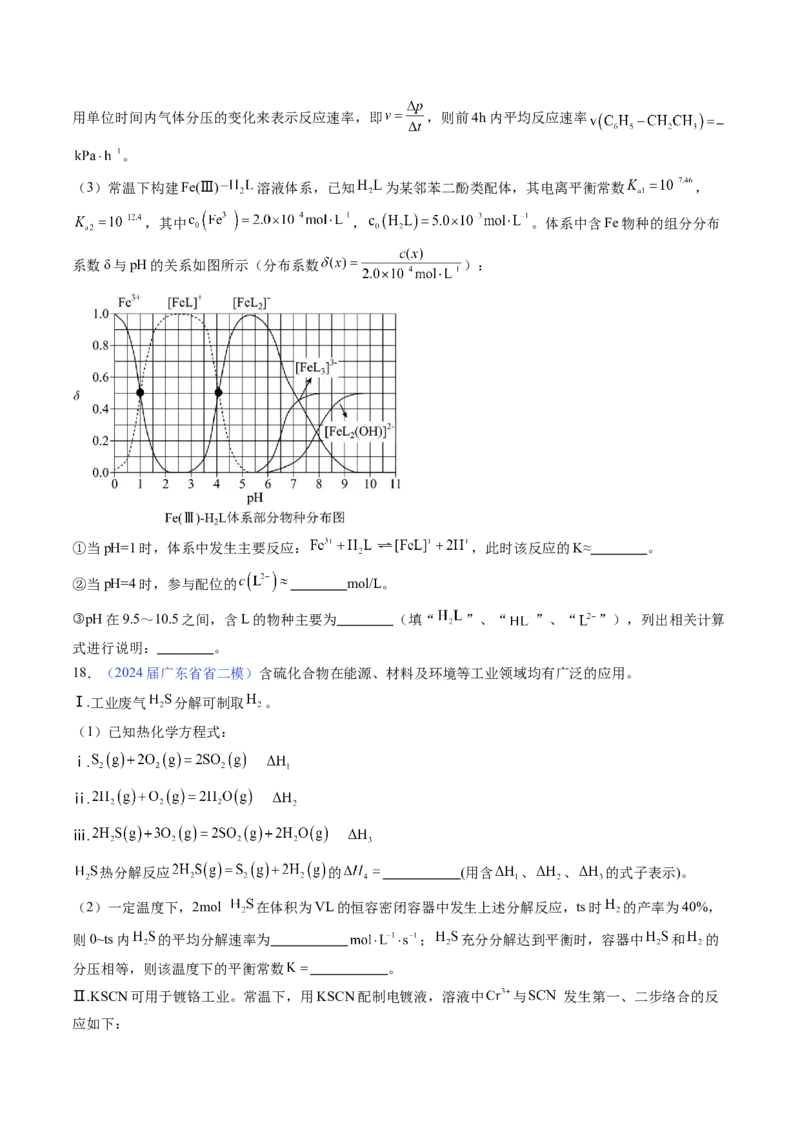
(3)常温下构建Fe(Ⅲ) 溶液体系,已知 为某邻苯二酚类配体,其电离平衡常数 ,
,其中 , 。体系中含Fe物种的组分分布
系数δ与pH的关系如图所示(分布系数 ):
①当pH=1时,体系中发生主要反应: ,此时该反应的K≈ 。
②当pH=4时,参与配位的 mol/L。
③pH在9.5~10.5之间,含L的物种主要为 (填“ ”、“ ”、“ ”),列出相关计算
式进行说明: 。
18.(2024届广东省省二模)含硫化合物在能源、材料及环境等工业领域均有广泛的应用。
Ⅰ.工业废气 分解可制取 。
(1)已知热化学方程式:
ⅰ.
ⅱ.
ⅲ.
热分解反应 的 (用含 、 、 的式子表示)。
(2)一定温度下,2mol 在体积为VL的恒容密闭容器中发生上述分解反应,ts时 的产率为40%,
则0~ts内 的平均分解速率为 ; 充分分解达到平衡时,容器中 和 的
分压相等,则该温度下的平衡常数 。
Ⅱ.KSCN可用于镀铬工业。常温下,用KSCN配制电镀液,溶液中 与 发生第一、二步络合的反
应如下:ⅳ.
ⅴ.
(3)根据以上络合反应,下列说法正确的有___________(填字母)。
A.加水稀释后,溶液中离子的总数减少
B.加入少量 固体,溶液中含铬微粒总数不变
C.反应 的平衡常数
D.溶液中 减小, 与 浓度的比值减小
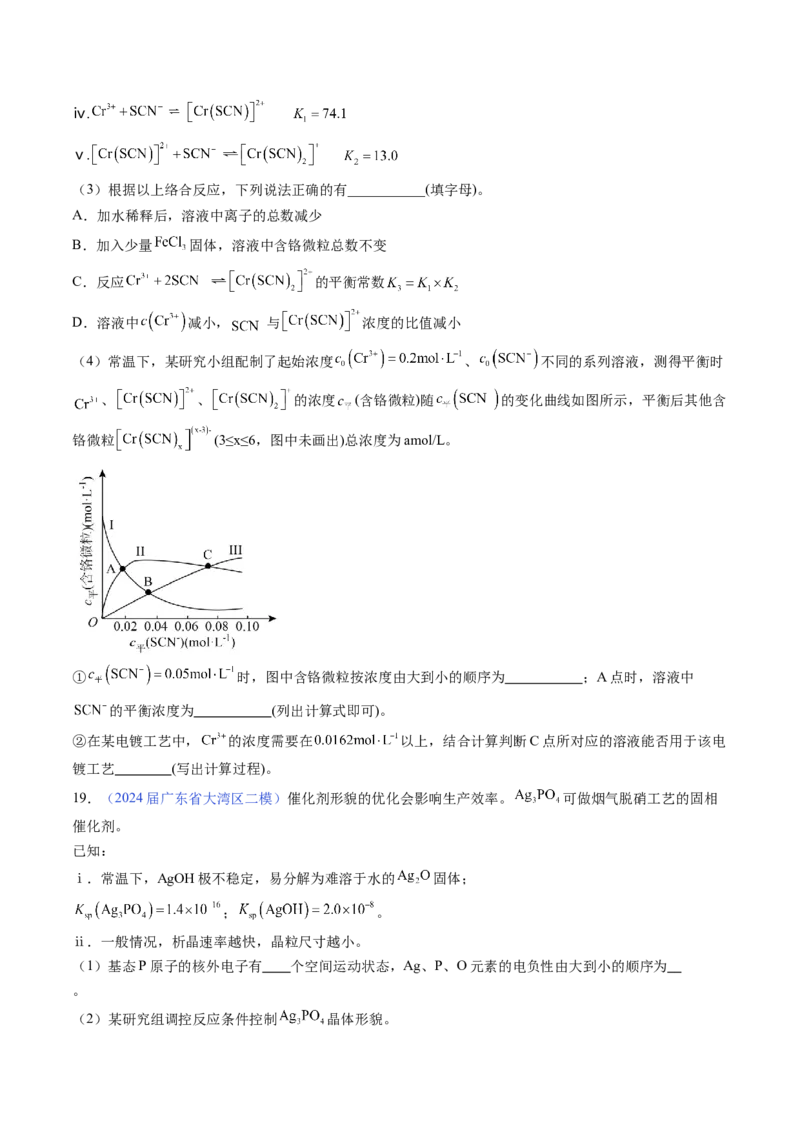
(4)常温下,某研究小组配制了起始浓度 、 不同的系列溶液,测得平衡时
、 、 的浓度 (含铬微粒)随 的变化曲线如图所示,平衡后其他含
铬微粒 (3≤x≤6,图中未画出)总浓度为amol/L。
① 时,图中含铬微粒按浓度由大到小的顺序为 ;A点时,溶液中
的平衡浓度为 (列出计算式即可)。
②在某电镀工艺中, 的浓度需要在 以上,结合计算判断C点所对应的溶液能否用于该电
镀工艺 (写出计算过程)。
19.(2024届广东省大湾区二模)催化剂形貌的优化会影响生产效率。 可做烟气脱硝工艺的固相
催化剂。
已知:
ⅰ.常温下,AgOH极不稳定,易分解为难溶于水的 固体;
; 。
ⅱ.一般情况,析晶速率越快,晶粒尺寸越小。
(1)基态P原子的核外电子有 个空间运动状态,Ag、P、O元素的电负性由大到小的顺序为
。
(2)某研究组调控反应条件控制 晶体形貌。①常温下,向银氨溶液逐滴加入 溶液制得 晶体,完善该反应的离子方程式 。
②在不同pH条件下,向 溶液中加入 溶液制得磷酸银收率如图所示。样品A的晶粒较小,
请从平衡移动与速率的角度解释原因 。
③下列有关说法正确的是
A.样品A中 杂质含量最高
B.可加入盐酸调控体系的pH制得不同样品
C.向 溶液中加入少量 溶液时,溶液中 减小
D.向 溶液中加入 溶液得到晶粒尺寸与上述样品相同
(3)研究组发现: 溶液与0.2 溶液等体积混合也能制得 。
①刚开始生成 沉淀时,溶液中的 。
②常温下溶液中含磷物种的分布系数 , 或 与pH的关系如图所示,则磷
酸的一级电离平衡常数 。
③体系中 由 第一步电离决定,可表示为 ,当生成 沉淀时,溶液中 至少为 (写出计算过程)。
20.(2024届广东省佛山二模)金属有机配合物广泛应用于各类催化反应。
Ⅰ.某铁的配合物催化1-丁烯和 加成的部分历程如图。
(1)①写出1-丁烯和 加成的化学方程式 。
②若丙→乙的活化能为 ,则甲→丙的反应热△H= (用含a的式子表达)。
(2)甲、乙的结构如图所示,Ar表示苯基。
①乙中Fe的配位数为 。
②下列说法正确的是 (填标号)。
A.甲→乙的过程中有 键的断裂和形成
B.乙→丙的速率比甲→乙慢
C.升高温度,乙的平衡浓度减小
D.选用合适的催化剂可提高1-丁烯的平衡转化率
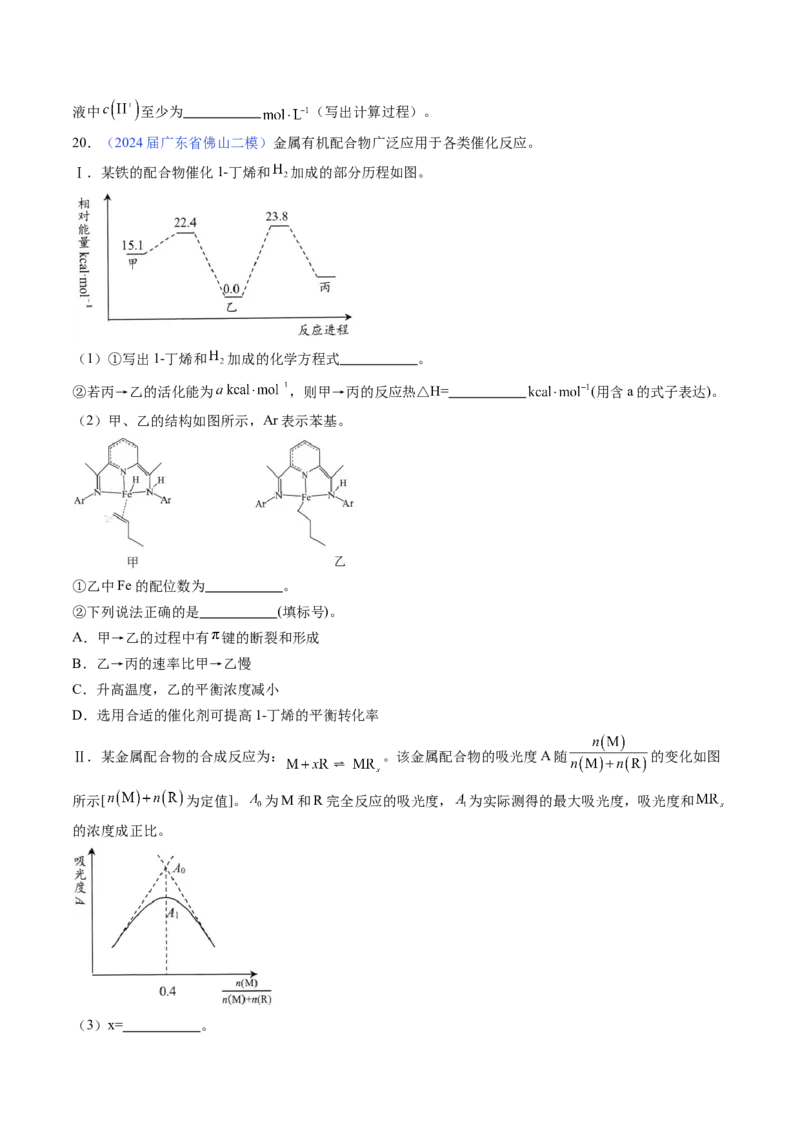
Ⅱ.某金属配合物的合成反应为: 。该金属配合物的吸光度A随 的变化如图
所示[ 为定值]。 为M和R完全反应的吸光度, 为实际测得的最大吸光度,吸光度和
的浓度成正比。
(3)x= 。(4)解离平衡 的解离度 (即 的平衡转化率)为 (用含 、 的式子表
示)。
(5)若x=1,将10mL 0.01 、5mL 0.001 M溶液、5mL 0.001 R溶液混
合,测得解离度 ,计算 的解离平衡常数 (写出计算过程)。