文档内容
易错专题 03 阿伏加德罗常数(N )
A
聚焦易错点:
►易错点一 N 常设陷阱
A
►易错点二 N 解题指导
A
典例精讲
易错点一 N 常设陷阱
A
【易错典例】
例1用N 表示阿伏加德罗常数,下列说法正确的是( )
A
①36g 18O 中所含的中子数为16N ②78g Na O 与足量水完全反应,转移电子数为1N ③标准状况下,2.24
2 A 2 2 A
L Cl 溶于水中达到饱和,可得到 HClO分子的数目是 0.1N ④在标准状况下,22.4 LHF的分子数目为
2 A
1N ⑤3.4g过氧化氢中含有的离子数为0.3N ⑥在常温常压下,0.1 mol铁与0.1 molCl 充分反应,转移的电
A A 2
子数为0.3N ⑦配制480mL2mol·L-1NaCl溶液,需要用托盘天平称量1N 氯化钠固体⑧S 和S 的混合物共
A A 2 8
6.4 g,其中所含硫原子数一定为0.2N
A
A.只有②⑧正确 B.只有②④⑦⑧正确 C.只有①②③⑤⑥正确 D.都不正确
【解题必备】
气体摩尔体积适用的对象是气体(包括混合气体)
在使用标准状况下气体摩尔体积“22.4 L·mol-1”时,要判断气体是否处于标准状况
物质的状态 在标准状况下物质的状态不是气态,而是液态或固态的有:水、溴单质、苯、SO 、乙
3
醇、四氯化碳、二硫化碳、氯仿、碳原子数大于4小于16的烃为液态(新戊烷除外)、
大于或等于16的烃为固态等
确定粒子个数要弄清楚微粒中相关粒子(质子、中子、电子)及离子、化学键之间的数
粒子个数 量关系
单原子分子:稀有气体He、Ne等;双原子分子:Cl、N、O、H 等;特殊物质:
2 2 2 2
O、P、18O、DO、NaO、 CO、甲烷、乙烯、乙炔等
3 4 2 2 2 2 2
最简式相同的物质,无论以何种质量比混合,原子个数均以最简式计算。如O 和
2
O、NO 和NO、烯烃和环烷烃等
3 2 2 4
同位素 如DO、TO、18O、14CO 等因物质的摩尔质量发生变化,导致物质的量变化
2 2 2 2
σ键和π键 有机物分子中单键为σ键,双键中含有1个σ键和1个π键,三键中含有1个σ键和2
个π键
溶液的体积 已知溶液的浓度,缺少溶液的体积,是不能计算溶质的物质的量的。
转移电子的数目 如1 mol Na O 与HO(或CO)反应、1 mol Cl 与足量的Fe反应(或NaOH溶液反应)、1
2 2 2 2 2
mol Cu与足量的稀硝酸反应等
可逆反应 可逆反应不能进行到底,如2NO NO,Cl+H O HClO+HCl等
2 2 4 2 2
水解反应 在水中某些离子能发生水解反应,离子数目发生改变。如0.1 mol FeCl 溶液中的
3Fe3+数目小于0.1N 、0.1 mol Na CO 溶液中含CO2—数小于0.1N
A 2 3 3 A
【变式突破】
1.(2023·广东惠州·一模)N 是阿伏加德罗常数的值。下列说法正确的是
A
A.22.4 L(标准状况)氮气中含有7N 个中子
A
B.1 mol重水比1 mol水多N 个质子
A
C.12 g石墨烯和12 g金刚石均含有N 个碳原子
A
D.1 L 1 mol·L−1 NaCl溶液含有28N 个电子
A
2.(2024·吉林白山·二模)N 代表阿伏加德罗常数的值。下列说法正确的是
A
A.常温常压下,124 g P 中所含P—P键数目为4N
4 A
B.100 mL 1mol·L−1FeCl 溶液中所含Fe3+的数目为0.1N
3 A
C.标准状况下,11.2 L甲烷和乙烯混合物中含氢原子数目为2N
A
D.密闭容器中,2 mol SO 和1 mol O 催化反应后分子总数为2N
2 2 A
易错点二 N 解题指导
A
【易错典例】
例2用N 表示阿伏加德罗常数的值,下列叙述中正确的是( )
A
①31g白磷中含有1.5N 个P-P
A
②1L0.1 mol/L的NaCO 溶液中含阴离子总数为0.1N 个
2 3 A
③标准状况下,22.4 L HF含N 个分子
A
④电解精炼铜时转移了N 个电子,阳极溶解32 g铜
A
⑤标准状况下,2.24 L Cl 溶于水,转移的电子数目为0.1N
2 A
⑥常温下,含0.2 mol HSO 的浓硫酸与足量铜反应,生成SO 的分子数小于0.1 N
2 4 2 A
⑦142gNa SO 和NaHPO 固体混合物中,阴、阳离子总数为3N
2 4 2 4 A
⑧N 个Fe(OH) 胶体粒子的质量为107g
A 3
A. ①③④⑧ B. ①⑥⑦ C. ③⑤⑦ D. ①⑥⑧
【解题必备】
判断一定量的物质中所含某种粒子数目的多少,是高考命题的热点之一。命题者青睐将阿伏加德罗常数与
气体摩尔体积(涉及外界条件、物质状态等)、物质结构(涉及质子数、中子数、电子数、化学键数等)、电离
与水解(涉及弱电解质的电离特点及盐类的水解特点、溶液中离子浓度)、氧化还原反应(涉及电子转移数
目)、可逆反应等结合。阿伏加德罗常数类试题具有较强的综合性,在复习备考中除了需要注意相关的解
题技巧外,还需要对相关知识有比较深入的认识,将知识准确、合理的应用。以阿伏加德罗常数为基础点
进行辐射,将相关知识总结归纳,在准确把握各量与阿伏加德罗常数之间关系的前提下,着重关注易错
点,并通过练习加强理解掌握,这样才能通过复习切实提高得分率。同时还要注意以下细微易错之处:
1.注意外界条件和物质状态:若题目给出的是物质的体积,则要注意外界条件和物质的状态,如水在标
准状况下为液态、SO 在标准状况下为固态、标准状况下碳原子数大于4的烃为液态或固态;气体的体积
3
受温度和压强的影响,应用阿伏加德罗常数时,要注意条件是否是标准状况,是否是同温同压;物质的
量、质量不受任何条件的影响,如任何条件下2 g H 的物质的量必是1 mol,所含分子数为N ,1 mol H 在
2 A 2任何条件下其质量都为2 g,所含分子数为N 。
A
2.明确物质的组成和结构:特殊物质的原子个数、电子个数,如Ne、O 等;特殊物质的摩尔质量,如
3
DO、18O 等;−些物质中的化学键数目,如SiO、CH、CO 等;最简式相同的物质中的微粒数目与物质
2 2 2 4 2
的组成有关,如NO 和NO、乙烯和丙烯等;摩尔质量相同的物质中的分子数相同,原子数不一定相同,
2 2 4
如:N、CO、C H 等;物质中所含化学键的数目与物质的结构有关,如HO、C H 中化学键的数目分
2 2 4 2 2 n 2n+2
别为3、3n+1。
3.注意氧化还原反应中的微粒:考查指定物质参加氧化还原反应时,常设置氧化还原反应中氧化剂、还
原剂、氧化产物、还原产物、被氧化、被还原、电子转移(得失)数目方面的陷阱。如NaO、NO 与HO的
2 2 2 2
反应;电解AgNO 溶液、CuSO 溶液的反应;Cl 与HO、NaOH、Fe的反应等等,分析该类题目时还要注
3 4 2 2
意反应产物以及过量计算问题。
4.弱电解质的电离或盐类的水解:考查电解质溶液中粒子数目及粒子浓度大小关系时,常涉及弱电解质
的电离平衡及盐类的水解平衡。弱电解质在水溶液中部分电离;可水解的盐溶液中,离子发生微弱水解,
电离产生的离子数量均小于理论数量。如1 L 0.1 mol·L-1的乙酸溶液和1 L 0.1 mol·L-1的乙酸钠溶液中
CHCOO-的数目不相等且都小于0.1N 。
3 A
5.一些特殊的反应:如一氧化氮和氧气不需要条件即可反应,二氧化氮和四氧化二氮之间存在相互转化,
合成氨反应属于可逆反应等。
【变式突破】
3.设 为阿伏加德罗常数的值。下列说法正确的是
A. 中含有的中子数为
B. 分子中含有的 键数目为
C.标准状况下, 气体中 数目为
D. 的 溶液中 数目为
4.设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.在25℃时,1LpH为12的Ba(OH) 溶液中含有OH-数目为0.01N
2 A
B.1.8g重水(D O)中所含质子数为N
2 A
C.足量的浓盐酸与8.7gMnO 反应,转移电子的数目为0.4N
2 A
D.32g甲醇的分子中含有C—H键的数目为4N
A
考点精练
1.(2024·安徽黄山·二模)设 为阿伏加德罗常数的值。下列说法正确的是
A.电解精炼铜时,阳极质量减少 ,电路中转移电子数可能是
B. 晶体和 晶体含有的离子数目均为
C. 与足量乙醇在一定条件下反应,生成的酯基的数目为
D. 水解能力弱于 的 溶液中 和 的总数大于2.(2024·吉林·三模)设N 为阿伏加德罗常数的值。下列叙述中正确的是
A
A.28gC H 的烃分子中含有C-C σ键的数目一定为1.6N
5 10 A
B.在标准状况下,22.4L由SO 和SO 组成的混合物中含有硫原子的数目为N
2 3 A
C.有2.00L0.5mol·L−1的稀硫酸和足量金属钠反应,消耗钠原子的数目为2N
A
D.在2CuH+2HCl==Cu+CuCl +2H↑反应中,每生成4.48L(标准状况)H ,反应转移的电子数目为
2 2 2
0.3N
A
3.(2024·贵州黔西·一模)设 为阿伏加德罗常数的值。下列叙述正确的是
A. 乙烯和丙烯的混合气体中p-p 键数目为
B. 氯化铵溶液中 和 数目之和为
C. 和 充分反应后的混合气体中原子数小于
D.25℃时, 的氨水中含有 数目为
4.(2024·广东·一模)设 为阿伏加德罗常数的值,下列说法错误的是
A.50g质量分数为64%的甲醇水溶液中含有σ键数目为5
B.一定条件下,5.6g Fe与0.1mol 充分反应,转移的电子数为0.2
C.浓硝酸热分解生成 、 共69g时,转移电子数为1.5
D.常温下,1L pH=2的稀盐酸中含有的H+数目为0.01
5.(2024·广西·二模) 为阿伏加德罗常数的值,下列叙述正确的是
A. 溶液中 数目是
B.标准状况下, 与足量 反应生成 分子数为
C.0.1mol 中 杂化的碳原子数为
D. 分子中含有 键的数目为
6.(2024·广东江门·一模)设 为阿伏加德罗常数的值。氯碱工业涉及 和 等物质,
下列说法正确的是
A. 固体所含质子的数目为
B. 与足量 溶液反应转移电子的数目为
C.标准状况下, 和 的混合气体中所含原子的数目为
D. 的氯水中,含 和 的总数为
7.(2024·福建福州·二模)工业制备硝酸的重要反应之一为: 。设 为阿伏加德罗常数的值,下列说法正确的是
A. 水中 键数目为
B. 中质子数目为
C. 氨水中,含有的 数为
D.每生成 转移电子数目为
8.(2024·四川泸州·二模)设 为阿伏加德罗常数的值。下列说法正确的是
A.1mol 含有的共价键数为
B.1L 溶液中含有 总数为
C.标准状况下,11.2L 含有的电子数大于
D.向 盐酸溶液中通氨气至中性, 的数目大于
9.(2024·广西柳州·三模) 为阿伏加德罗常数的值。下列说法正确的是
A. 中含有的质子数为
B. 的盐酸溶液中 的数目为
C. 在空气中充分燃烧生成 ,转移的电子数目为
D.8 g甲烷和15 g乙烷的混合气体中含有 共价键的数目为
10.(2024·吉林白山·二模) 是一种半导体材料,一种制备方法是 。
设 为阿伏加德罗常数的值。下列叙述正确的是
A.标准状况下, 含 键数目为
B. (金刚石)含非极性键数目为
C.每生成 时转移电子数目为
D. 溶于足量盐酸,溶液中含 数目为
11.(2024·江西九江·二模) 的结构是 ,含有3中心5电子的大 键。其制方法如下:
。 为阿伏加德罗常数的数值,下列说法正确的是
A. 所含的原子数为
B.1mol 中心原子的价层电子对数为
C.用上述方法制备1mol 转移电子数为
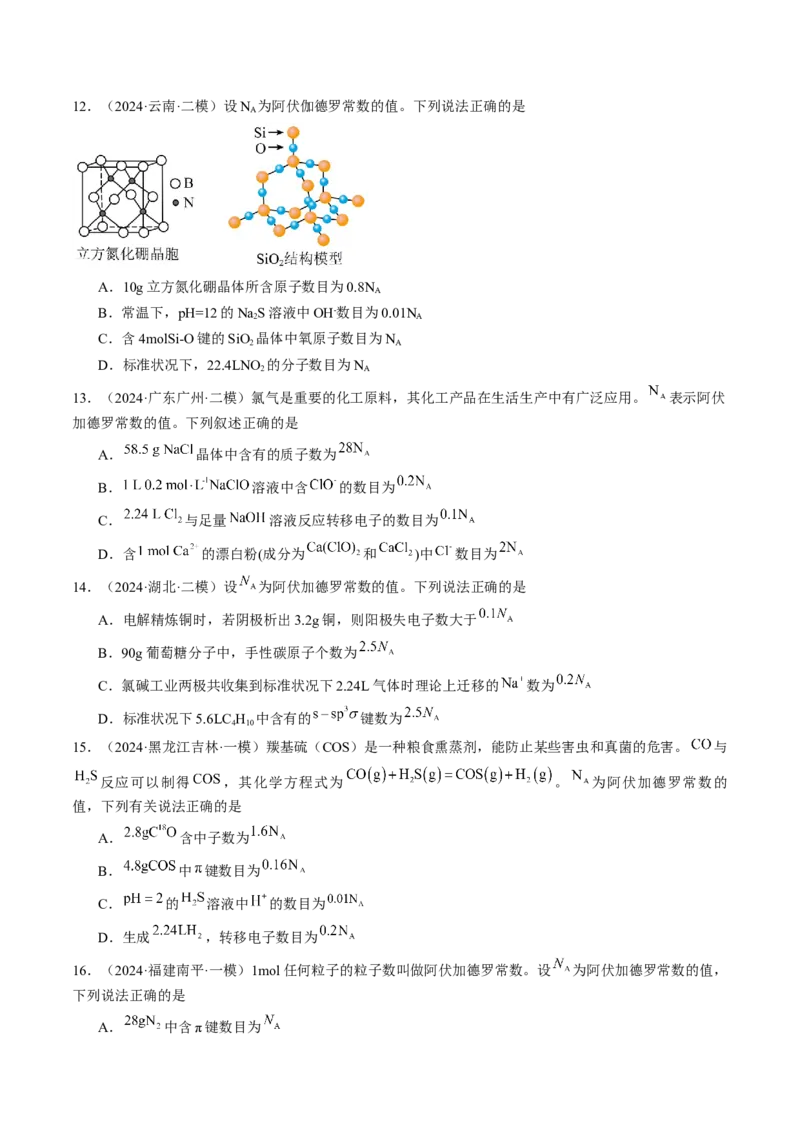
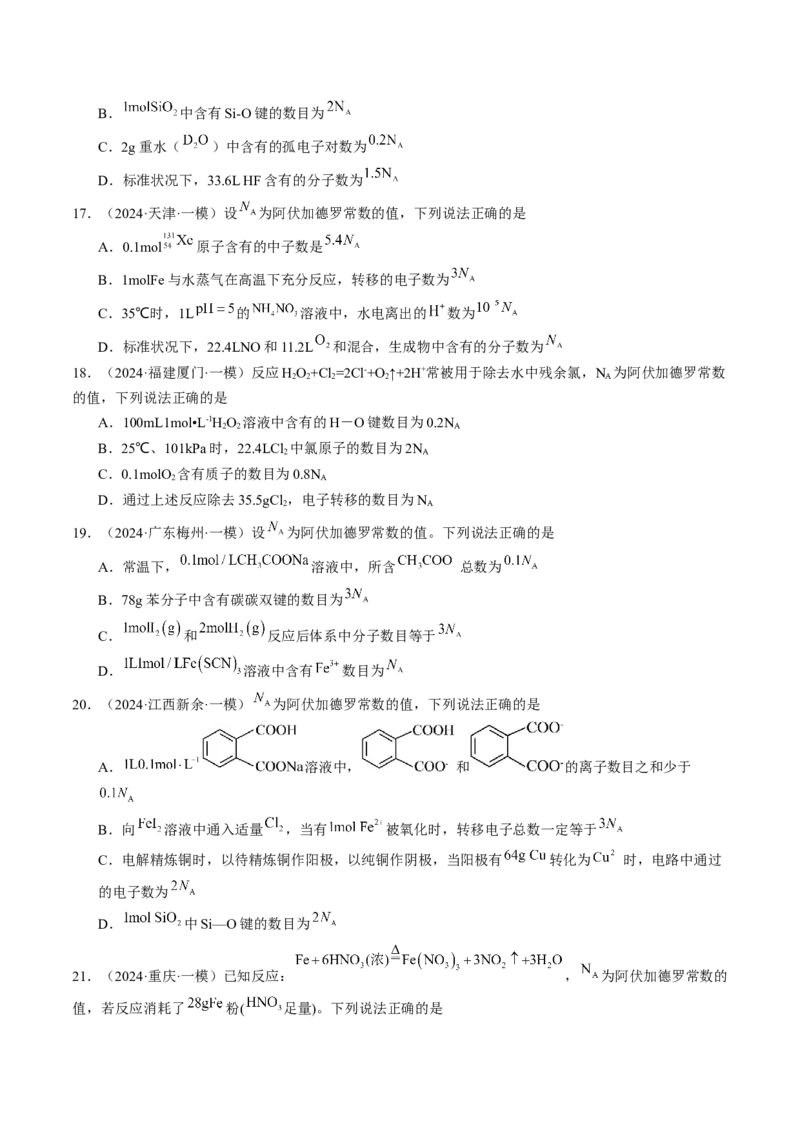
D. 溶液中所含 数目为12.(2024·云南·二模)设N 为阿伏伽德罗常数的值。下列说法正确的是
A
A.10g立方氮化硼晶体所含原子数目为0.8N
A
B.常温下,pH=12的NaS溶液中OH-数目为0.01N
2 A
C.含4molSi-O键的SiO 晶体中氧原子数目为N
2 A
D.标准状况下,22.4LNO 的分子数目为N
2 A
13.(2024·广东广州·二模)氯气是重要的化工原料,其化工产品在生活生产中有广泛应用。 表示阿伏
加德罗常数的值。下列叙述正确的是
A. 晶体中含有的质子数为
B. 溶液中含 的数目为
C. 与足量 溶液反应转移电子的数目为
D.含 的漂白粉(成分为 和 )中 数目为
14.(2024·湖北·二模)设 为阿伏加德罗常数的值。下列说法正确的是
A.电解精炼铜时,若阴极析出3.2g铜,则阳极失电子数大于
B.90g葡萄糖分子中,手性碳原子个数为
C.氯碱工业两极共收集到标准状况下2.24L气体时理论上迁移的 数为
D.标准状况下5.6LCH 中含有的 键数为
4 10
15.(2024·黑龙江吉林·一模)羰基硫(COS)是一种粮食熏蒸剂,能防止某些害虫和真菌的危害。 与
反应可以制得 ,其化学方程式为 。 为阿伏加德罗常数的
值,下列有关说法正确的是
A. 含中子数为
B. 中 键数目为
C. 的 溶液中 的数目为
D.生成 ,转移电子数目为
16.(2024·福建南平·一模)1mol任何粒子的粒子数叫做阿伏加德罗常数。设 为阿伏加德罗常数的值,
下列说法正确的是
A. 中含π键数目为B. 中含有Si-O键的数目为
C.2g重水( )中含有的孤电子对数为
D.标准状况下,33.6L HF含有的分子数为
17.(2024·天津·一模)设 为阿伏加德罗常数的值,下列说法正确的是
A.0.1mol 原子含有的中子数是
B.1molFe与水蒸气在高温下充分反应,转移的电子数为
C.35℃时,1L 的 溶液中,水电离出的 数为
D.标准状况下,22.4LNO和11.2L 和混合,生成物中含有的分子数为
18.(2024·福建厦门·一模)反应HO+Cl=2Cl-+O ↑+2H+常被用于除去水中残余氯,N 为阿伏加德罗常数
2 2 2 2 A
的值,下列说法正确的是
A.100mL1mol•L-1HO 溶液中含有的H-O键数目为0.2N
2 2 A
B.25℃、101kPa时,22.4LCl 中氯原子的数目为2N
2 A
C.0.1molO 含有质子的数目为0.8N
2 A
D.通过上述反应除去35.5gCl,电子转移的数目为N
2 A
19.(2024·广东梅州·一模)设 为阿伏加德罗常数的值。下列说法正确的是
A.常温下, 溶液中,所含 总数为
B.78g苯分子中含有碳碳双键的数目为
C. 和 反应后体系中分子数目等于
D. 溶液中含有 数目为
20.(2024·江西新余·一模) 为阿伏加德罗常数的值,下列说法正确的是
A. 溶液中, 和 的离子数目之和少于
B.向 溶液中通入适量 ,当有 被氧化时,转移电子总数一定等于
C.电解精炼铜时,以待精炼铜作阳极,以纯铜作阴极,当阳极有 转化为 时,电路中通过
的电子数为
D. 中Si—O键的数目为
21.(2024·重庆·一模)已知反应: , 为阿伏加德罗常数的
值,若反应消耗了 粉( 足量)。下列说法正确的是A.所得溶液中 数目为 B.收集到的 分子数为
C.转移的电子数为 D.生成的 含共价键数为
22.(2024·广东·一模)设 为阿伏加德罗常数的值。下列说法正确的是
A. 和 混合物中含有的离子数为
B. 与足量消石灰反应转移的电子数为
C. 的醋酸溶液中的氢离子数为
D.标准状况下, 中的氧原子数为
23.(2024·全国·模拟预测)设N 表示阿伏伽德罗常数的值。下列说法正确的是
A
A.标准状况下,11.2LC HOH中含-OH数目为0.5N
2 5 A
B.1L0.2mol•L-1NaHCO 溶液中,H+的数目为0.2N
3 A
C.等物质的量的HO、DO、TO所含中子数相等
2 2 2
D.氢氧燃料电池中,负极上1mol气体参与反应时转移电子数目为2N
A
24.(2024·湖南长沙·二模)设阿伏加德罗常数的值为 ,则下列说法正确的是
A.标准状况下,16.8L 与足量氯气在光照下反应生成 分子数目小于0.75
B.常温常压下,56g Fe和足量浓盐酸反应转移电子数为3
C.1.05mol 分别与足量 、 反应,转移的电子数目均为1.05
D.将50mL、18mol/L的浓硫酸与足量铜粉共热,产生的 分子数为0.45
25.(2024·广东江门·一模)设 为阿伏加德罗常数的值。反应 常用
于监测 含量是否达到排放标准。下列说法正确的是
A.生成2.33g 沉淀时,转移电子数目为0.04
B.标准状况下,22.4L 中硫原子的孤电子对数为2
C.25℃时, 的HCl溶液中含有 的数目为0.1
D. 晶体和 晶体混合物共1 mol,则极性键数目为2